Amibas de vida libre en playas de Tuxpan y Arrecife Ingeniero, Veracruz, México
Amibas de vida libre en playas de Tuxpan y Arrecife Ingeniero, Veracruz, México
Revista de Zoología, núm. 29, pp. 1-5, 2018
Universidad Nacional Autónoma de México
Recepción: 22 Agosto 2017
Aprobación: 08 Noviembre 2017
Resumen: Las amibas de vida libre (AVL) son organismos anfizóicos, es decir que tienen la capacidad de vivir como organismos de vida libre y también como parásitos oportunistas. Por lo cual el objetivo de este estudio fue determinar la presencia de AVL en dos localidades de Veracruz que son Tuxpan y Arrecife Ingeniero en Boca del Río, ya que la evaluación de dichas especies constituye un indicador elemental en la calidad del agua para uso recreativo. Se tomaron tres tipos de muestra que fueron: agua, biopelícula y sedimento de la zona intermareal, provenientes de colectas en la Planta Termoeléctrica “Adolfo López Mateos”, en Tuxpan y Arrecife Ingeniero (en Boca del Río) respectivamente. Se registraron in situ los parámetros fisicoquímicos de las muestras de agua: pH, salinidad (UPS), oxígeno disuelto (mg/L), temperatura, así como una prueba de indicadores biológicos de calidad de agua. Las muestras fueron procesadas en el Laboratorio de la UIICSE de la FES-Iztacala, UNAM, sembrándolas en placas con agar no nutritivo (NNE) con Enterobacter aerogenes e incubándose a 37 °C. Posterior al crecimiento de los cultivos amibianos se identificaron por morfometría utilizando las claves taxonómicas de Page. De 31 aislados se determinaron un total de 13 géneros de AVL colectados de los biotopos agua, biopelícula y sedimento. Estas especies fueron: Naegleria sp., Vahlkampfia sp., Rosculus sp., Sappinia sp., Vannella sp., Korotnevella sp., Mayorella sp., Vexillifera sp., Heteramoeba sp., Euglypha sp., Paramphitrema sp., siendo Tuxpan el lugar donde se observó una mayor riqueza específica. En ambas localidades el género dominante fue Acanthamoeba sp., género el cual se sabe que posee especies patógenas. Además, se aislaron enterobacterias del género Klebsiella y Escherichia coli. Aunque estas enterobacterias juegan un papel muy importante para las AVL, en los resultados se pudo observar que las variables fisicoquímicas tales como el oxígeno disuelto y la salinidad influyeron en la riqueza de especies de AVL en Tuxpan comparado con el Arrecife Ingeniero.
Palabras clave: Amibas de Vida Libre (AVL), anfizóicos, Acanthamoeba, termotolerantes, Veracruz .
Abstract: Free-living amoebae (AVL) are amphizoic organisms, it means, that they have the capacity to live as free-living organisms and also as opportunistic parasites. Therefore, the objective of this study was to determine the presence of AVL in two localities of Veracruz that are Tuxpan and Ingeniero Reef in Boca del Río, since the evaluation of this species constitutes an elementary indicator in the water quality for recreational use. Three kinds of samples were taken: water, biofilm and sediment of the intertidal zone, collected from the Thermoelectric Plant "Adolfo López Mateos", in Tuxpan and in Arrecife Ingeniero (in Boca del Río) respectively. The physicochemical parameters of the water samples were analyzed in situ: pH, salinity (UPS), dissolved oxygen (mg/L), temperature, as well as a bacteriological indicator of water quality test. The samples were processed in the laboratory of the UIICSE of the FES-Iztacala, UNAM, inoculating the samples in plates with non-nutritive agar (NNE) with Enterobacter aerogenes and incubated at 37 ° C. After the growth of amoebic cultures, they were identified by morphometry using Page's taxonomic keys. From 31 isolates, a total of 13 genera of AVL collected from the biotopes water, sediment and biofilms were determined. These species were: Naegleria sp., Vahlkampfia sp., Rosculus sp., Sappinia sp., Vannella sp., Korotnevella sp., Mayorella sp., Vexillifera sp., Heteramoeba sp., Euglypha sp., Paramphitrema sp. being Tuxpan. the place where a greater specific richness was observed. In both locations the dominant genus was Acanthamoeba, a genus which is known to possess pathogenic species. In addition, Enterobacteria like Klebsiella and Escherichia coli. were isolated. Although these Enterobacteria play a very important role in the feeding of the AVL in the results, it can be observed that physicochemical variables such as dissolved oxygen and salinity influenced the richness of AVL species in the Tuxpan compared to the Ingeniero Reef.
Keywords: Free-Living Amoeba (FLA), amphizoic, Acanthamoeba, thermotolerant, Veracruz.
INTRODUCCIÓN
Las amibas de vida libre (AVL) son organismos anfizóicos, debido a que tienen la capacidad de vivir como organismos de vida libre y también como parásitos oportunistas. Se les considera organismos cosmopolitas debido a que se distribuyen en toda la biosfera, principalmente en las interfaces: agua-suelo, agua-planta, agua-aire, agua-animal (Gallegos y col., 2014).
Cuando las condiciones ambientales son desfavorables, estos organismos pueden formar quistes como estrategia de supervivencia, por ejemplo, cuando hay grandes periodos de escasez de alimento o un cambio en las condiciones ambientales (Gallegos y col., 2014). Las temperaturas elevadas favorecen la proliferación de las AVL por lo que se les encuentra con frecuencia en aguas termales naturales y en aguas contaminadas térmicamente por descargas industriales (Ávila y col., 2006).
Como depredadores de bacterias, las amibas contribuyen a la estabilidad de comunidades microbianas, manteniendo el tamaño de la población que promueve la diversidad de especies de microorganismos. Además, recientes publicaciones han documentado la interacción huésped-hospedero en la que diversas bacterias son endosimbiontes naturales o parásitos obligados de las amibas, llamándose a estas “bacterias resistentes a la fagocitosis” (Gallegos y col., 2014).
.El estudio de las AVL, ha demostrado que son un grupo de protozoos de gran importancia ecológica y médica. A algunos géneros de estas amibas se les considera organismos oportunistas e invasores, capaces de producir infecciones severas en el Sistema Nervioso Central (SNC), como son la Meningoencefalitis Amibiana Primaria (MEAP), Encefalitis Amibiana Granulomatosa (EAG), Queratitis amibiana y Acantamebiosis Cutánea. Las infecciones humanas por AVL son ocasionadas principalmente por los géneros: Naegleria, Acanthamoeba, Sappinia y Balamuthia (Ávila y col., 2006). Estos géneros se caracterizan por ser termófilos, se encuentra idealmente entre los 25 a 45 °C, por lo que se localizan en climas tropicales y subtropicales, durante todo el año y en zonas geográficas templadas, proliferando durante el verano (Goñi y col., 2014).
Se han descrito diversos géneros de amibas tanto para agua dulce como marina y en algunos casos, especies ocupando ambos ambientes. Es conocido que algunos géneros desarrollan la habilidad de adaptarse a los cambios en la salinidad. Un ejemplo es el género Acanthamoeba, que se ha aislado repetidamente de agua marina contaminada (Oshima y col., 1986).
Sawyer aisló 26 especies de AVL en el Golfo de México y el Océano Pacífico, incluso se han encontrado nuevas especies de AVL en algas marinas (El Kadiri, 1992) y recientemente en Corea se descubrió una nueva AVL marina con cromatóforos fotosintéticos originados por la endosimbiosis con cianobacterias (Kim y Park, 2016). A su vez se ha demostrado que la distribución de AVL en cuerpos de agua, es similar en la superficie como en el sedimento.
El número exacto de especies de AVL conocidas para México, permanece siendo una incógnita; sin embargo, por primera vez Gallegos y colaboradores en 2014, realizaron un recuento de especies del periodo de revisión correspondiente a 171 años (1841-2012) con 144 contribuciones arrojando un total de 315 especies. Por lo cual el objetivo de este estudio fue determinar la presencia de AVL en dos localidades del estado de Veracruz ya que la evaluación de dichas especies constituye un indicador elemental en la calidad del agua para uso recreativo y desafortunadamente estos estudios se han visto limitados en México, especialmente el de amibas marinas.
ÁREA DE ESTUDIO
El municipio de Tuxpan se encuentra ubicado en la zona norte del estado de Veracruz, en las coordenadas 20°57'N y 97°24'W a una altitud de 10 msnm. Limita al norte con los municipios de Tamiahua y Naranjos, al oeste con Temapache y al sur con Tihuatlán y Poza Rica. Tiene una superficie de 966.18 Km2. Este municipio está irrigado por el río Tuxpan que desemboca en el Golfo de México formando la barrera en esta zona.
En la región existe un clima tropical, con una temperatura media anual de 24.1°C; con lluvias abundantes dado que su precipitación pluvial media anual es de 1,241mm.
MATERIALES Y MÉTODOS
Se realizó un solo muestreo en el mes de marzo del 2016; fueron siete y ocho colectas en la planta termoeléctrica “Adolfo López Mateos”, en Tuxpan y en Arrecife Ingeniero (en Boca del Río) respectivamente. Se tomaron cuatro tipos de muestra que fueron: agua, alga, biopelícula y sedimento de la zona intermareal. Las primeras dos se guardaron en frascos de vidrio dejando una cuarta parte de aire, mientras que, para las biopelículas, estas fueron seleccionadas aleatoriamente de rocas adyacentes a la zona litoral y posteriormente se guardaron en tubos de centrífuga estériles de 50 mL con agua marina.
De las muestras obtenidas se tomaron alícuotas de 30 mL en tubos de centrífuga estériles y se centrifugaron a 2500 rpm durante 10 min. Las pastillas se inocularon en cajas de Petri con medio sólido NNE (Agar no nutritivo) y en placas de ocho pozos con medio líquido Prescott-James con una monocapa de bacteria Enterobacter aerogenes inactivada por calor a 70 °C por 15 min como fuente de alimento. Las cajas con medio sólido se incubaron a 38 °C de 48 a 72 h para seleccionar a las amibas termotolerantes.
Para el aislamiento de AVL, en condiciones estériles, se vertió 1mL de solución salina estéril sobre la placa y se realizó un barrido con un asa de vidrio, concentrando la suspensión acuosa con amibas, se tomó una gota de esta suspensión, se colocó en un portaobjetos para su observación en el microscopio invertido de contraste de fases Nikon Eclipse TS100 y se realizó la identificación taxonómica observando las características morfológicas del trofozoíto y del quiste, usando de referencia las claves taxonómicas de Page (1988).
Se determinó la calidad bacteriológica del agua usando la técnica del número más probable. La cual incluye tres fases: 1) Prueba presuntiva; 2) Prueba confirmativa y 3) Prueba completa. En la prueba presuntiva, se utilizaron dos concentraciones de caldo lactosado (concentración doble y concentración sencilla). Para el caldo de concentración doble se usaron tres tubos a los cuales se les agregaron 10 mL de muestra de agua a cada uno, posteriormente se utilizaron seis tubos con caldo lactosado de concentración sencilla, a tres de estos tubos se les agrego 1 mL de muestra de agua y a los otros tres tubos restantes se les agrego 0.1 mL de la muestra. Se incubaron a 37°C por 24 horas, posteriormente se realizó la prueba confirmativa de microorganismos coliformes totales.
Para la prueba confirmativa se transfirieron las muestras positivas del caldo lactosado a medio bilis verde brillante (BVB) con ayuda de un asa de siembra y se incubó a 37°C por 24 horas. Se seleccionó un tubo de medio BVB de cada muestra de agua, se sembró en cajas de Petri con agar con Eosina y Azul de Metileno (EMB) y se incubaron a 37°C por 24 h. Después de la incubación se resembró en medio de Sulfuro Indol para Movilidad (SIM), Rojo de Metilo Voges-Proskauer (RM-VP) y Citrato de Simmons (CS), se incubó a 37°C de 24 a 48 h. Finalmente se hizo la lectura e interpretación de las pruebas.
RESULTADOS
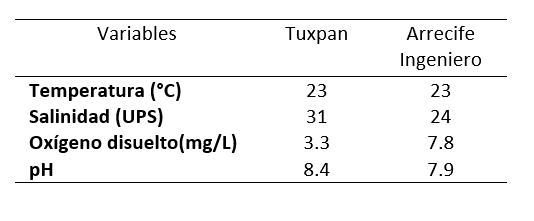
La temperatura ambiental de ambas localidades fue de 23 °C, sin embargo, en parámetros como el oxígeno disuelto y salinidad presentaron variaciones de hasta 4 y 7 unidades de diferencia, respectivamente, el pH fue ligeramente básico (Cuadro 1).
Cuadro 1
Cuadro 1
Promedio de los resultados de las variables fisicoquímicas del agua marina de Tuxpan y Arrecife Ingeniero.
De 31 aislados se determinaron un total de 13 géneros de AVL colectados de los biotopos agua, alga, sedimento y biopelículas. Estas especies fueron: Naegleria sp., Vahlkampfia sp., Rosculus sp., Sappinia sp., Vannella sp., Dactylamoeba sp., Mayorella sp., Vexillifera sp., Heteramoeba sp., Euglypha sp., Paramphitrema sp., siendo Tuxpan el lugar donde se observó una mayor riqueza específica. En ambas localidades los géneros dominantes fueron Acanthamoeba sp., seguido de Mayorella sp. para Tuxpan y Vannella sp. para la localidad de Arrecife Ingeniero (Figura 1). Por otra parte, el biotopo que presentó mayor número de AVL fueron las biopelículas, seguido del agua (Figura 2).
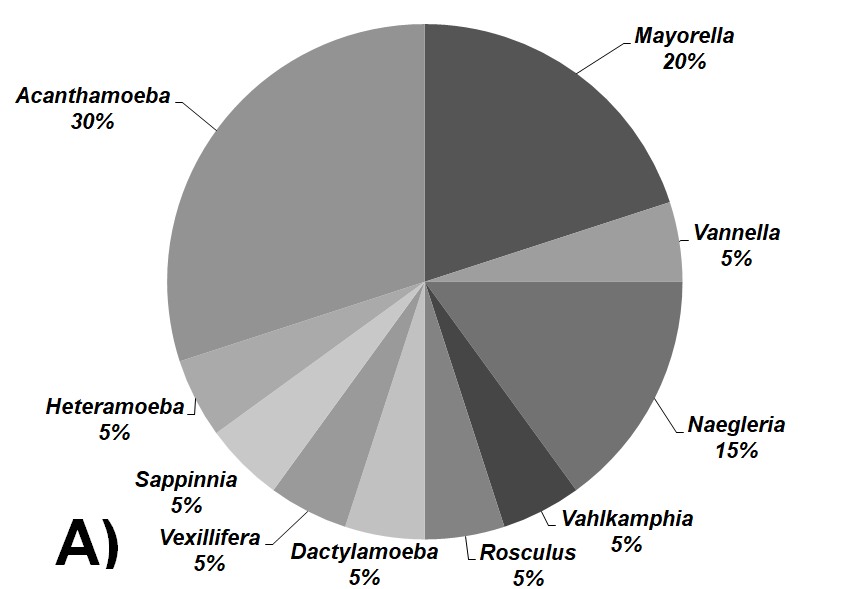
Figura 1
Figura 1
Porcentaje de géneros de AVL aisladas de las muestras colectadas en todos los biotopos (A) Tuxpan y (B) Arrecife Ingeniero.
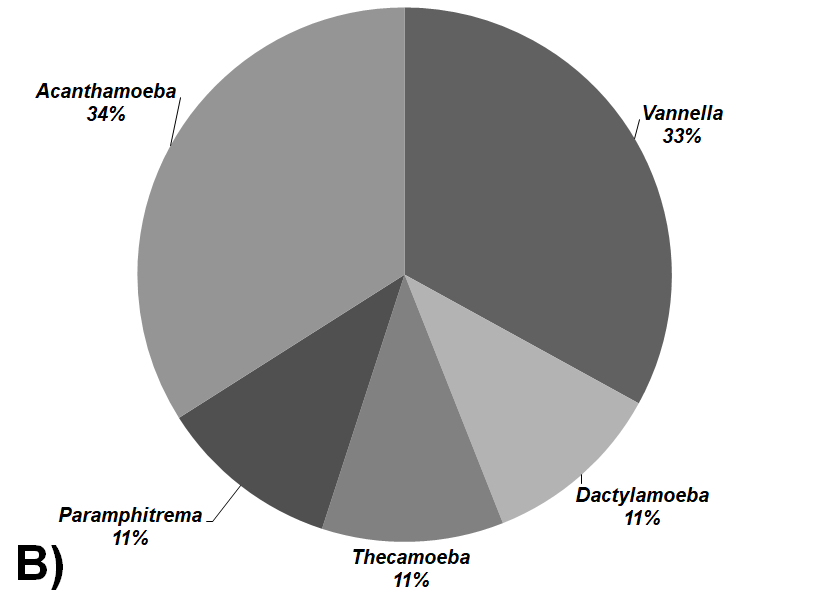
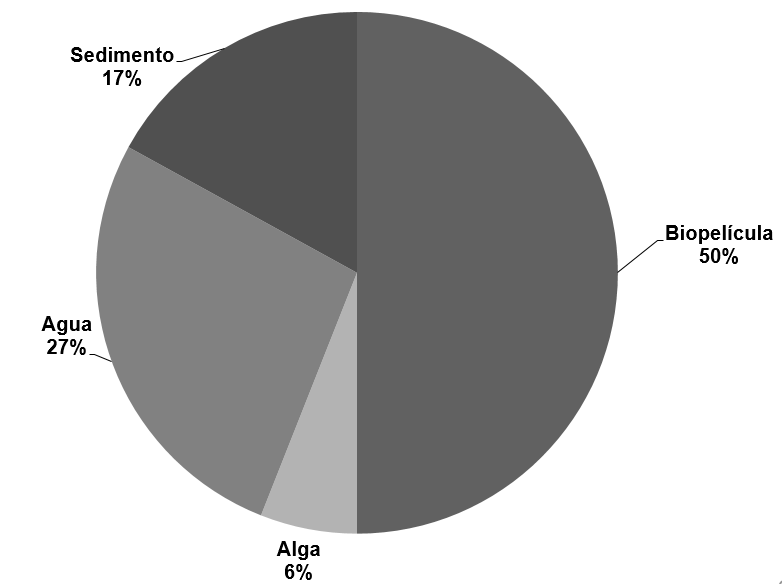
Figura 2
Figura 2
Porcentaje de géneros de AVL aislados por biotopo.
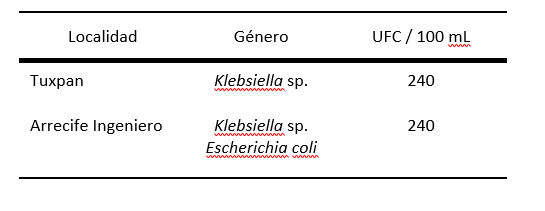
En cuanto a las bacterias aisladas e identificadas mediante las pruebas de NMP, IMVIC y Kligler, se obtuvieron un total de 240 UFC/100mL para ambas muestras. En Arrecife Ingeniero se determinaron dos géneros diferentes a diferencia de Tuxpan en el cual se determinó sólo un género (Cuadro 2).
Cuadro 2
Cuadro 2
Géneros de bacterias aisladas de en Tuxpan y en Arrecife Ingeniero.
DISCUSIÓN
Debido a que los ámbitos de temperatura, pH, salinidad y oxígeno disuelto, óptimos para el desarrollo de AVL son muy amplios (Ettinger y col., 2003), resulta difícil mostrar con claridad la relación entre la presencia amibiana y las variables fisicoquímicas del agua, sin embargo, uno de los parámetros determinantes que difiere entre ambas localidades fue el porcentaje de salinidad. La oscilación en la salinidad confiere una mayor dificultad de adaptación y proliferación de estos microorganismos afectando de manera importante los niveles de osmolaridad a nivel intracelular, provocando un mayor gasto de energía y retrasando la división celular (Oshima y col., 1985).
Una variable fisicoquímica que mostró diferencias fue la concentración de oxígeno disuelto. Bonilla y col. (2014) reportaron que una alta concentración de oxígeno disuelto puede favorecer el desarrollo de AVL, sin embargo, en Tuxpan se reportó una menor concentración de este parámetro y una mayor riqueza específica en comparación con Arrecife Ingeniero. Los altos valores de oxígeno podrían estar relacionados a la presencia de organismos fotosintéticos (algas y pasto marino).
Visvesvara y col. (2007), mencionan que existen cuatro géneros de AVL patógenas, que se caracterizan por ser termófilas: Acanthamoeba spp., Balamuthia mandrillaris, Sappinia pedata y Naegleria fowleri. Otras especies de AVL pueden sobrevivir a más de 37 °C, sin embargo, esta temperatura no es óptima para su desarrollo por lo que se les considera termo-tolerantes.
La termo-tolerancia es una condición necesaria para que se les considere potencialmente patógenas, pero se requieren pruebas de patogenicidad para confirmarlo (Rohr y col., 1998).
Por otro lado, con respecto a los biotopos muestreados, las biopelículas presentaron una mayor riqueza específica. Algunas investigaciones sugieren que las biopelículas favorecen un suministro de nutrientes a las AVL adheridas, explicando elevada presencia en este biotopo (Greub y Raoult,, 2004;Preston, 2003; Rodríguez-Zaragoza, 1994; Thomas y col., 2010).
Uno de los factores que podría favorecer el desarrollo de LAS AVL fue la presencia de organismos bacterianos, esto podría ser debido a que las AVL se alimentan principalmente de bacterias, las cuales al ser pequeñas son fáciles de fagocitar (Krusnell y Linder, 2001). A pesar de que en el arrecife Ingeniero se identificó a Escherichia coli y Klebsiella sp., las cuales son enterobacterias, se observó menor riqueza específica de AVL en este lugar, considerándose que la presencia de AVL puede estar más influenciada por las variables fisicoquímicas que por la presencia de colonias bacterianas en el ambiente.
Según Silva (2011), en México no se cuentan con valores de referencia legales para analizar la calidad de aguas costeras, excepto en el caso de los enterococos que se consideran indicadores de contaminación de origen fecal, a pesar de esto las especies de Klebsiella sp. y Escherichia coli , los cuales son bacilos productores de beta-lactamasas de espectro extendido, lo cual les confiere multiresistencia a distintos antimicrobianos, de esta forma la presencia de estos microorganismos podría ser un foco de infección para las personas que tengan contacto con estas aguas (Argüez de Paz y col., 2015)
CONCLUSIÓN
Se determinó la riqueza específica de AVL en Tuxpan y Arrecife Ingeniero, siendo Acanthamoeba el género predominante y reportándose la presencia de otras AVL con potencial patógeno como es el caso de Naegleria sp., Vahlkampfia sp. y Sappinia sp., siendo la biopelícula, el biotopo donde mayor número de amebas fueron encontradas.
Se considera que las variables fisicoquímicas: oxígeno disuelto y salinidad influyeron en la mayor presencia de especies de AVL en el arrecife Tuxpan comparado con el Arrecife Ingeniero.
El hallazgo de bacterias tales como Klebsiella sp. y Escherichia coli, así como las amibas con potencial patógeno antes mencionadas representan un riesgo para las personas que realizan actividades recreativas o de pesca en esta zona.
LITERATURA CITADA
Argüez de Paz. R.; A. Rodríguez & N. Rojas. 2015. Klebsiella sp. y Escherichia coli productoras de betalactamasas en pacientes con infección del tracto urinario. Rev. Cubana Med. Int. Emerg. 14(4): 10-14.
Ávila. I.; M. Rodríguez; D. Infante; V. Llovera; O. Álvarez & M. Briceño. 2006. Amibas de vida libre potencialmente patógenas en aguas del parque “Las Cocuizas”, Maracay, Venezuela. Rev. Cubana Med. Trop. 58 (1):19-24.
CONABIO. 2008. Ficha técnica para la evaluación de los sitios prioritarios para la conservación de los ambientes costeros y oceánicos de México (s.f.). World Wid Web. http://www. conabio.gob.mx/gap/images/1/14/55_Humedales_Costeros_y_Arrecifes_de_Tuxpan.pdf; última consulta: Febrero. 2016.
EI Kadiri. G. & L. Joyon. 1992. Pernina chaumonti, n.g., n.sp., a new marine amoeba (Rhizopoda, Heterolobosea). Morphological and ultrastructural characterization. Eur. J. Parasitology. 28: 43-50. Ettinger. M. R.; S. R. Webb; S. A. Harris; S. P. McIninch; G. C. Garman & B. L. Brown. 2003. Distribution of free-living amoebae in James river, Virginia, USA. J. Parasitol. Res. 89: 6–15.
Gallegos. E.; A. Lugo; A. Calderón; M. Sánchez & R. Mayén. 2014. Biodiversidad de protistas amébidos de vida libre en México. Rev. Mex. Biodiv. 85 (1): 10-25.
Goñi. P.; M. Fernández & E. Rubi. 2014. Identifying endosymbiont bacteria associated with free-living amoebae. Environ. Microbiol. Rep. 16 (2): 339-349.
Greub, G. & D. Raoult. 2004. Microorganisms resistant to free-living amoebae. Clin. Microbiol. Rev. 17: 413–433.
Kim. S. & M. Park. 2016. Paulinella longichromatophora sp. nov., a New marine photosynthetic testate amoeba containing a cromatophore. Protist. 167: 1-12.
Page, F.C. 1988. A new key to freshwater and Soil Gymnamoebae. Freshwater Biological Association. Cumbria, England. 122 pp.
Krusnell, W.K. & Linder, E. 2001.Bacterial Infections of free-living amoebae. Res. Microbiol. 152: 613-619.
Oshima. N.; F. Takeda; & K. Ishii. 1986. Responses of freshwater amoebae to salinity changes. Comp. Biochem. Physiol. 85 (1): 395-399.
Preston, T.M. 2003. The water–air interface: a microhabitat for amoebae. Eur. J. Protistol. 39: 385–389.
Rodriguez-Zaragoza, S. 1994. Ecology of free-living amoebae. Crit. Rev. Micrbiol. 20: 225–241.
Rohr. U.; S. Weber; R. Michel; F. Selenka & M. Wilhelm. 1998. Comparasion of free-living amoebae in hot water systems of hospitals with isolates from moist sanitary areas by identifying genera and determinig temperature tolerance. Appl. Environ. Microbiol. 64 (5):1822-1824.
Silva, N.S. 2011. Estudio Comparativo de la Calidad del Agua de Mar en las Playas de Acapulco. Tesis para obtener el título de maestría en Tecnología Avanzada del Instituto Politécnico Nacional. México. 78 p.
Thomas. V.; G. McDonnell; S. P. Denyer & J. I. Maillard. 2010. Free-living amoebae and their intracellular pathogenic microorganisms: risks for water quality. FEMS Microbiol. Rev. 34: 231–259.
Visvesvara. G. S.; H. Moura & F. Shuster. 2007. Pathogenic and oportunistic free-living amoebae: Acanthamoeba spp., Balamuthia mandrillaris, Naegleria fowleri and Sappinia diploidea. FEMS Immunol. Med. Microbiol 50: 1-26.
Ettinger. M. R.; S. R. Webb; S. A. Harris; S. P. McIninch; G. C. Garman & B. L. Brown. 2003. Distribution of free-living amoebae in James river, Virginia, USA. J. Parasitol. Res. 89: 6–15.