Revisiones
Mastitis puerperal
Puerperal mastitis
Mastite puerperal
Mastitis puerperal
Medicina U.P.B., vol. 38, núm. 2, pp. 140-146, 2019
Universidad Pontificia Bolivariana

Esta obra está bajo una Licencia Creative Commons Atribución 3.0 Internacional.
Recepción: 16 Octubre 2018
Aprobación: 27 Marzo 2019
Resumen: La mastitis puerperal es un problema de salud importante en el posparto, la incidencia varía del 2% al 33%. Se define como la inflamación de los lóbulos glandulares, siendo la infección la etiología más frecuente y el puerperio, en las primeras semanas, el periodo de mayor prevalencia. La mayoría de las mujeres experimentan algún grado de congestión mamaria, al preparar la glándula para la eyección láctea durante el amamantamiento, pero cuando la técnica es inadecuada y lleva a fisuras del pezón, se genera riesgo de colonización bacteriana de los ductos mamarios con sobreinfección e, incluso, formación de abscesos, que van a requerir manejo hospitalario, antibioticoterapia e intervenciones quirúrgicas. Es esta la causa más importante de suspensión de la lactancia y su repercusión en la alimentación y desarrollo del recién nacido. No hay uniformidad en los criterios y el diagnóstico sigue siendo fundamentalmente clínico. El microrganismo más implicado es el estafilococo, su confirmación microbiológica se hace a partir del Gram y cultivo del drenaje de abscesos o de cultivos de leche, siendo estos, pocas veces realizados, a menos que el cuadro se complique con repercusión sistémica (sepsis) o no haya respuesta a la antibioticoterapia empírica. El tratamiento fundamental es el drenaje del seno, por lo que debe mantenerse la lactancia.
Palabras clave: mastitis, mama, absceso.
Abstract: Puerperal mastitis is a major health problem in the postpartum period, whose incidence varies from 2% to 33%. It is defined as the inflammation of the glandular lobes. The infection would be the most frequent etiology, and the puerperium would be the period of highest prevalence in the first weeks. In general, most women experience some degree of breast engorgement, preparing the mammary gland for milk ejection during breastfeeding, but when the technique is inadequate and leads to nipple fissures, there is a risk of bacterial colonization of the mammary ducts with superinfection and even the formation of abscesses, which will require hospital management, antibiotic therapy and surgical interventions. This is the most important cause of breastfeeding suspension and its impact on the feeding and development of the newborn. There is no uniformity in the diagnostic criteria. It remains fundamentally clinical. The most implicated microorganism is staphylococcus. Its microbiological confirmation is made from the Gram and the culture of the drainage of abscesses, or milk cultures. These are only a few times carried out, unless the patient’s record gets complicated with systemic repercussion (sepsis) or there is no response to empirical antibiotic therapy. The fundamental treatment is sinus drainage; therefore, breastfeeding should be maintained.
Keywords: mastitis, breast, infection, abscess.
Resumo: A mastite puerperal é um problema de saúde importante no pós-parto, a incidência varia de 2% a 33%. Se define como a inflamação dos lóbulos glandulares, sendo a infecção a etiologia mais frequente e o puerpério, nas primeiras semanas, o período de maior prevalência. A maioria das mulheres experimentam algum grau de congestão mamária, ao preparar a glândula para a ejeção láctea durante a amamentação, mas quando a técnica é inadequada e leva a fissuras do mamilo, se gera risco de colonização bacteriana dos ductos mamários com sobreinfecção e, incluso, formação de abscessos, que vão a requerer manejo hospitalar, antibioticoterapia e intervenções cirúrgicas. É esta a causa mais importante de suspensão da amamentação e sua repercussão na alimentação e desenvolvimento do recém-nascido. Não há uniformidade nos critérios e o diagnóstico segue sendo fundamentalmente clínico. O microrganismo mais implicado é o estafilococo, sua confirmação microbiológica se faz a partir do Gram e cultivo da drenagem de abscessos ou de cultivos de leite, sendo estes, poucas vezes realizados, a menos que o quadro se complique com repercussão sistémica (sepse) ou não haja resposta à antibioticoterapia empírica. O tratamento fundamental é a drenagem do seio, pelo que deve manter-se a amamentação.
Palavras-chave: mastite, mama, abscesso.
INTRODUCCIÓN
La lactancia materna tiene importantes beneficios nutricionales, inmunológicos y sobre la relación madre-hijo. La Organización Mundial de la Salud (OMS) recomienda la lactancia materna exclusiva para los primeros seis meses de vida y lactancia continua, hasta los dos años1,2. El objetivo de esta revisión es resaltar que, a pesar que la mastitis puerperal es la infección más frecuente en el puerperio, no hay uniformidad en los criterios diagnósticos ni terapéuticos, a la vez, la etiopatogenia no está bien definida. También, se destaca que el diagnóstico de mastitis sigue siendo fundamentalmente clínico y solo en algunos casos está indicado el cultivo de leche y la confirmación microbiológica. Son pocos los estudios que han permitido identificar y cuantificar los agentes causales, así como estudiar la sensibilidad a los antibióticos, lo que permite evitar tratamientos inadecuados, amamantamiento doloroso o abandono de la lactancia.
Definición
La mastitis puerperal o de la lactancia es la inflamación de uno o varios lóbulos de la glándula mamaria acompañada o no de infección1,2. Se presenta más frecuentemente en el puerperio3,4,5,6,7,8, es decir, durante el periodo que sigue inmediatamente al parto y que se extiende, normalmente, de seis a ocho semanas o 40 días, tiempo necesario para que el cuerpo materno (hormonas y aparato reproductor) vuelvan a condiciones pregestacionales9.
Epidemiología
La incidencia de mastitis puerperal es del 10%, aunque el rango puede variar del 3% a 33% de mujeres lactantes10,11. Los factores de riesgo incluyen la edad y la mayor incidencia se presenta entre los 21 y 35 años12, la historia de mastitis en embarazos previos, los pezones agrietados o adoloridos, el uso de ungüentos, las prácticas incorrectas de amamantamiento y la antibioterapia periparto13,14.
Clínica
Los síntomas son dolor mamario y signos inflamatorios (calor, rubor y eritema). Puede haber cambios sistémicos que incluyen temperaturas superiores a 38.5 °C, decaimiento, dolores articulares, escalofríos, náuseas (similares a cuadros gripales)6,9,15. Se ha propuesto para el diagnóstico clínico de mastitis la presencia de, al menos, dos síntomas mamarios (dolor, enrojecimiento o bulto) y, al menos, uno general, como la fiebre o los síntomas gripales. Cuando se tienen en cuenta estas características que tienen una buena precisión diagnóstica, se evidencian prevalencias hasta del 17%3. En la Figura 1 se muestran algunos de los aspectos locales propios de la mastitis.
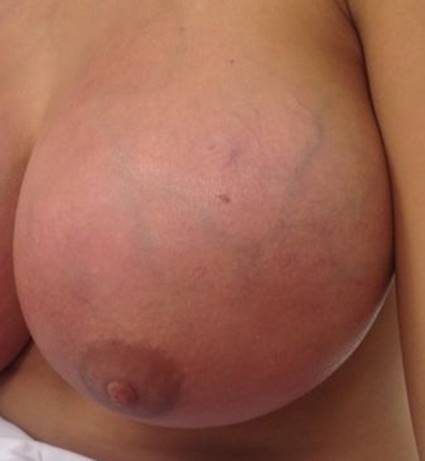
Figura 1.
Inflamación mamaria propia de la mastitis.
El 80% de los casos se asocia a fisuras en el pezón, generalmente, unilaterales8,16, aunque entre un 3% y un 12% pueden ser bilaterales1,17, estas lesiones tienen una recurrencia de entre el 4% y el 8%6. La incidencia de absceso mamario, como complicación de una mastitis aguda (Figura 2), está entre el 0.4% y el 11%3,8,17,18,19. Según su localización, se diferencian tres tipos de absceso: superficial, intramamario y retromamario, en su mayoría producidos por bacterias de tipo estafilococo (aureus, epidermidis y otras coagulasa negativas)20.
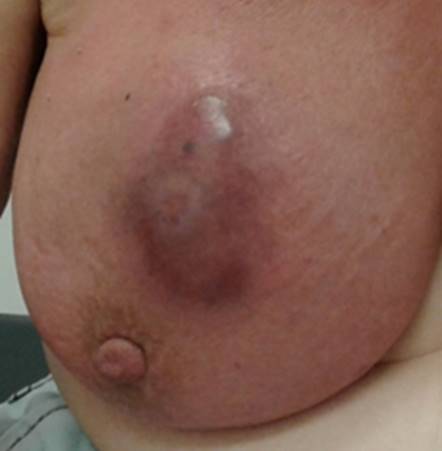
Figura 2.
Absceso mamario.
La mastitis de la lactancia se clasifica en diferentes categorías, dependiendo del curso agudo, subagudo y crónico. Una mastitis aguda dura en promedio de dos a tres semanas (aunque es objeto de discusión), mientras que la crónica dura más de tres meses, puede ser recurrente o granulomatosa21. La entidad también se clasifica según las manifestaciones, en clínica o subclínica; esta última se expresa como mastalgia sin signos inflamatorios locales ni sistémicos y puede llevar a errores diagnósticos y a un abordaje terapéutico incorrecto21.
Desde el punto de vista histológico, la mastitis se divide en: 1. Subareolar, que es una afectación de la dermis subyacente; 2. Glandular o galactoforitis supurada, que es una afectación lobulillar, con secreción purulenta; 3. Intersticial, que es una afectación del tejido conjuntivo adiposo interlobular; 4. Abscedada (5%), donde se presenta una colección purulenta con cápsula piógena; y 5. Flemonosa o edematosa, en la que el agente causal es el estreptococo22.
En el posparto, la mastalgia y sensibilidad en los pezones son quejas comunes que se dan hasta en el 73.7% de las mujeres durante las primeras dos semanas de lactancia23. La congestión mamaria, otro diagnóstico diferencial, se presenta como tensión o ingurgitación vascular y glandular difusa y bilateral, con solo una leve hiperemia, que mejora con la evacuación de leche, sin que aparezca eritema ni síntomas sistémicos24.
Fisiopatología
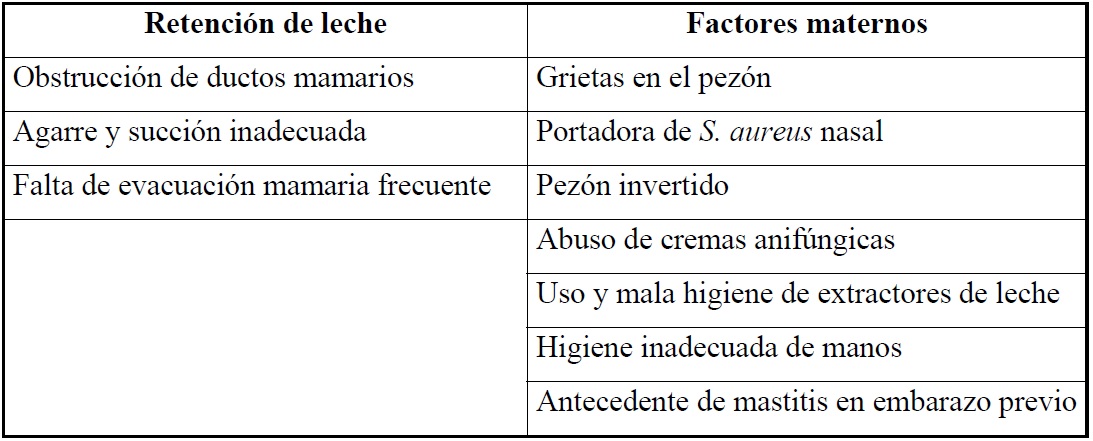
Fuera de la virulencia bacteriana, los factores predisponentes incluyen circunstancias que inhiben el adecuado drenaje de leche y llevan a su estancamiento (estasis), como conductos obstruidos, inadecuada succión25,26 y factores maternos, como fisuras del pezón, antecedente de mastitis en embarazo previo, uso de extractores de leche y de cremas anifúngicas27. Los factores de riesgo para mastitis se resumen en la Tabla 11,2,6,17.
El amamantamiento incluye el agarre y la succión, y cuando no es adecuado, constituye un factor predisponente para fisuras en el pezón. El agarre adecuado implica que la boca del bebe cubra completamente la areola, los labios sobresalgan y el pezón esté completamente en el interior de la boca, y en la succión se deben observar mejillas rellenas (no hoyitos), sonido de deglución (paso de leche), además, las mamadas deben ser lentas profundas y con pausa, el bebé suelta el pecho cuando está satisfecho y la madre no debe sentir dolor (Figura 3)28.

Figura 3.
Adecuado agarre del pezón.
Tradicionalmente, se ha considerado que la leche humana es estéril29, pero esta idea ha sido refutada por varios estudios que demuestran que contiene su propia microbiota. Los gérmenes hallados más frecuentemente son: Lactobacillus spp., Lactococcus lactis, Bifidobacterium spp. y Propioni-bacterium spp.30,31,32. Estos pueden ayudar a establecer la microbiota gastrointestinal comensal del lactante10,33,34,35,36. Se ha postulado que la alteración de la flora de este microentorno o disbiosis puede llevar al desarrollo de la mastitis, pero esto aún no se ha comprobado37,38.
El cultivo rara vez se utiliza para confirmar la infección bacteriana, porque los positivos pueden ser resultado de la colonización normal y los negativos no descartan la mastitis39,40,41. Esta técnica ha sido recomendada cuando la infección es grave, inusual o nosocomial o si no responde al tratamiento en las primeras 48 horas39. Si el cultivo está indicado, la forma adecuada de realizarlo incluye asepsia de manos y de pezón, y la expresión manual de la mama con recogida de la leche, utilizando un frasco estéril de orina. Se recomienda desechar las tres o cinco primeras gotas, recoger por lo menos un ml de leche y transportar lo más pronto posible al laboratorio42. Se siembra en medios convencionales, como agar sangre y agar chocolate. La mayoría de bacterias causantes de la infección mamaria se pueden evidenciar entre las 18-24 horas de incubación a 35-37 ◦C42.
Fisiológicamente, puede haber recuentos que indican una concentración de bacterias menor de 1000 UFC/ml1,2,11 (esto explica el reducido número de bacterias aisladas en heces de niños, con lactancia materna exclusiva17), cualquier valor por encima de esta cifra es sugestivo de infección mamaria y se relaciona con la formación biopelículas en el interior de los conductos galactóforos, que ocasionan su obstrucción43,44. Generalmente, la presencia de Staphylococcus y Streptocococcus en la concentración señalada se considera anormal17,41; estos pueden proliferar y sintetizar toxinas que ocasionan inflamación mamaria. Cuando las toxinas se absorben y alcanzan la circulación sistémica, pueden dar lugar a un cuadro semejante a la gripa. En estos casos es conveniente evaluar si hace falta suspender la lactancia del seno afectado, hasta la negativización del cultivo45,46.
El Staphylococcus aureus es responsable de la mayoría de las mastitis lactacionales (65%-90%). El Staphylococcus epidermidis es causante, principalmente, de las mastitis subagudas y subclínicas. Los Streptocococcus S. agalactie, S.viridans, S. mitis, S. salivarius y S. pneumoniae son el segundo grupo bacteriano responsable de infección47.
Paraclínicos
Los estudios de laboratorio incluyen leucograma y eritrosedimentación, y los hallazgos más habituales son leucocitosis, neutrofilia con desviación izquierda y elevación de la velocidad de sedimentación globular. Además, permiten diferenciar la mastitis de la congestión de leche no infecciosa1,6.
El principal estudio de imagen es el ultrasonido. La lobulitis se observa como un aumento difuso de la ecogenicidad y vascularización, y los abscesos se ven como una colección hipoecoica heterogénea, irregular, con vascularización periférica, pero no central48,49. El ultrasonido es útil, tanto para el drenaje percutáneo como para las tomas de muestra para cultivo50.
Tratamiento
Los casos leves y tempranos pueden manejarse, exitosamente, manteniendo la lactancia materna, con evacuaciones más frecuentes y mejorando el drenaje mamario sin que se tenga que modificar la unión madre-hijo. Si los síntomas no se resuelven después de 12 a 24 horas de manejo conservador y hay fiebre >38.5 °C, síntomas sistémicos o absceso, estará indicada la antibioticoterapia23.
Es importante continuar la lactancia, es especial del seno afectado, para que permanezca bien drenado. Si el dolor por fisuras del pezón lo impide, se puede amamantar el seno contralateral y realizar extracción manual y vaciado del afectado. Se puede hacer masaje y usar paños tibios24.
El uso de antinflamatorios no esteroideos es útil como analgésico, debido a que el dolor puede afectar negativamente el reflejo de eyección. El ibuprofeno es compatible con la lactancia, se obtienen bajos niveles en la leche y concentraciones pequeñas en el infante, del 0.1% al 0.7%51.
Durante la infección aguda se puede notar una reducción en el volumen de leche, esto puede mejorar gradualmente después de la resolución del cuadro, aunque algunas mujeres presentan producción decreciente de leche o, incluso, parada prematura de la lactancia51.
En el tratamiento de las fisuras de pezón se ha estudiado el uso del ungüento de lanolina, durante una semana, sin demostrar beneficio6. Los esteroides tópicos podrían retrasar la cicatrización. Otros tratamientos, como la glicerina, la leche materna extraída y los ungüentos combinados (antibiótico, esteroide y antimicótico) tampoco demostraron beneficio52.
El tratamiento de la congestión mamaria se ha manejado con otras opciones, por ejemplo, acupuntura, hojas de repollo, oxitocina y ultrasonido mamario, sin mejoría significativa53.
El uso de probióticos, cepas de Lactobacillus (10 log10 UFC), por un período de cuatro semanas mejoró los síntomas clínicos de la mastitis y redujo la colonización de cepas de Staphylococcus, sin embargo, se considera que el beneficio no es costo-efectivo54.
La antibioticoterapia debe ser dirigida a los microorganismos encontrados más comúnmente: Staphylococcus y Streptococcus26,11. Típicamente, se utiliza una penicilina resistente a la penicilinasa, con una duración del tratamiento de 10 a 14 días55. En la Tabla 2 se resume el tratamiento de la mastitis aguda56,57,58,59,60,61.
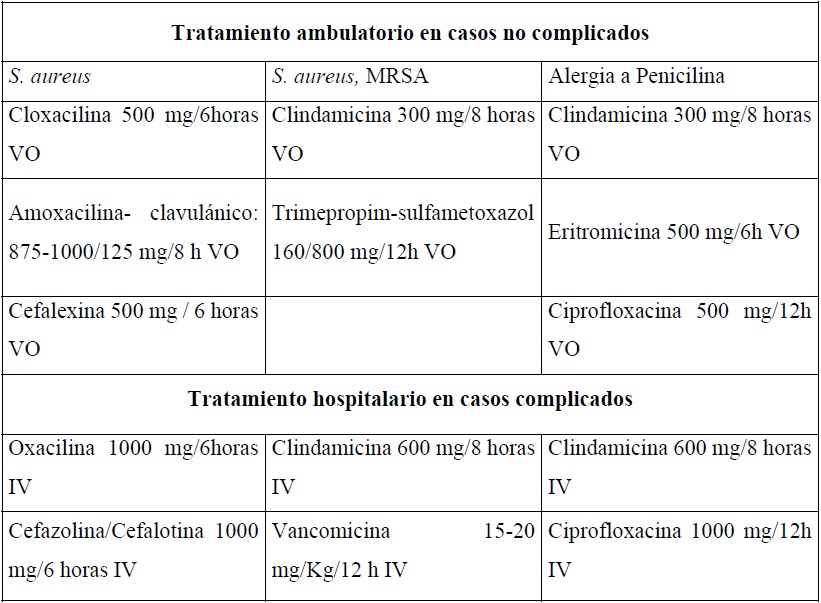
Nota S. aureus: Staphylococcus aureus; MRSA Staphylococcus aureus meticilino resistente; mg: miligramo; h: horas; VO: vía oral; IV: intravenoso; Kg: kilogramo.
Para el tratamiento de abscesos de mama hay que tener en cuenta que el agente causal más común es el Staphylococcus aureus meticilino resistente (MRSA)6,17. El tratamiento consiste en intensificar la antibioterapia y extraer el contenido purulento por aspiración con aguja o mastotomía1,6. La lactancia materna por el seno afectado puede hacerse, si no hay galactorrea purulenta2.
De manera tradicional se ha realizado mastotomía con incisión en la piel, que se deja abierta para que drene el fluido infectado. Bajo anestesia general, con incisiones arqueadas en la zona de máxima fluctuación y con desbridamiento de todos los posibles tabiques y lavados con abundante suero fisiológico61. La tasa de efectividad es del 100%, pero tiene como inconveniente cicatriz poco cosmética y necesidad de curaciones de la herida. La cicatrización por segunda intención retrasa la restitución del hasta en seis semanas1,3.
Una forma menos invasiva de tratar el absceso mamario es por aspiración con aguja percutánea, guiada por ecografía. Tiene como ventajas que no hay cicatrices y la duración de la hospitalización es menor. Por otra parte, se requiere de ecógrafo con sonda de alta frecuencia (7.5-12 MHz). Los abscesos menores de 3 cm tienen mayor tasa de éxito48,62. Se infiltra anestésico local en la piel y en la zona adyacente a la cápsula piógena, y se punciona con jeringa de 10 o 20 cc y aguja larga calibre 18-16 gauge, se toma muestra para cultivo microbiológico y se enjuaga la cavidad con solución salina, hasta que el centro se aclare48.
El seguimiento es clínico y se puede realizar un nuevo ultrasonido, si reaparece una masa indurada o si los síntomas empeoran48. La aspiración se puede repetir, pero si hay fallo, está indicada la mastotomía48,50,62. Las tasas de mejoría varían entre el 54% y el 100%48.
CONCLUSIONES
La mastitis puerperal es frecuente, pero no hay uniformidad en los criterios diagnósticos ni terapéuticos. La fisiopatología más aceptada es la que incluye la estasis de leche y la obstrucción de los conductos mamarios. El diagnóstico de la mastitis aguda es fundamentalmente clínico y la antibioticoterapia es empírica, pocas veces se realizan cultivos de leche con fines diagnósticos. La ecografía es el método diagnóstico complementario de elección, porque permite reconocer la presencia de abscesos y guiar procedimientos de drenaje percutáneo. Se recomienda continuar la lactancia, aumentar el número de tomas y mantener evacuado el seno afectado.
REFERENCIAS
1. OMS. Mastitis: causas y manejo. Ginebra: WHO/FCH/CAH; 2000. [Acceso: 26 de julio de 2016]. Disponible en:http://apps.who.int/iris/bitstream/10665/66925/1/WHO_FCH_CAH_00.13_spa.pdf.
2. Amir L. Academy of Breastfeeding Medicine Protocol Committee. ABM clinical protocol #4: mastitis. Breastfeed Med 2014;9(5):239-243.
3. Amir LH, Forster DA, Lumley J, McLachlan H. A descriptive study of mastitis in Australian breastfeeding women: Incidence and determinants. BMC Public Health. 2007;7:62.
4. Foxman B, D’Arcy H, Gillespie B, Bobo JK, Schwartz K. Lactation mastitis: Occurrence and medical management among 946 breastfeeding women in the United States. Am J Epidemiol. 2002;155(2):103-114.
5. Mediano P, Fernández L, Rodríguez JM, Marín M. Case control study of risk factors for infectious mastitis in Spanish breastfeeding women. BMC Pregnancy Childbirth. 2014;14:195.
6. Barbosa-Cesnik C, Schwartz K, Fozman B. Lactation mastitis. JAMA 2003;289(13):1609-1612.
7. Scott JA, Robertson M, Fitzpatrick J, Knight C, Mulholland S. Occurrence of lactational mastitis and medical management: A prospective cohort study in Glasgow. Int Breastfeed J. 2008;25:3-21.
8. Michie C, Lockie F, Lynn W. The challenge of mastitis. Arch Dis Child. 2003;88(9):818-821.
9. Lawrence RA, Lawrence RM. Protocolo 4: Mastitis. En: Lawrence RA, Lawrence RM, eds. Lactancia materna, una guía para la profesión médica. 6 ed. Madrid: Elsevier; 2007:1142-1146.
10. Jiménez E, Fernández L, Maldonado A, Martín R, Olivares M, Xaus J, et al. Oral administration of Lactobacillus strains isolated from breast milk as an alternative for the treatment of infectious mastitis during lactation. Appl Environ Microbiol. 2008;74(15):4650-4655.
11. Civardi E, Garofoli F, Tzialla C, Paolillo P, Bollani L, Stronati M. Microorganisms in human milk: Lights and shadows. J Matern Fetal Neonatal Med. 2013;26(Suppl 2):30-34.
12. Jonsson S, Pulkkinen MO. Mastitis today: Incidence, prevention and treatment. Ann Chir Gynaecol. 1994;Suppl 208:84-87.
13. Betzold CM. An update on the recognition and management of lactational breast inflammation. J Midwifery Womens Health. 2007;52(6):595-605.
14. Spencer JP. Management of mastitis in breastfeeding women. Am Fam Phys. 2008;78(6):727-731.
15. Delgado S, Arroyo R, Jiménez E, Marín ML, del Campo R, Fernández L, et al. Staphylococcus epidermidis strains isolated from breast milk of women suffering infectious mastitis: Potential virulence traits and resistance to antibiotics. BMC Microbiol 2009;9:82-93.
16. Jahanfar S, Ng CJ, Teng CL. Antibiotics for mastitis in breastfeeding women. Cochrane Database Syst Rev 2013;2:CD005458.
17. Contreras GA, Rodríguez JM. Mastitis: Comparative etiology and epidemiology. J Mammary Gland Biol Neoplasia. 2011;16(4):339-356.
18. Amir LH, Forster D, McLachlan H, Lumley J. Incidence of breast abscess in lactating women: Report from an Australian cohort. Br J Obstet Gynaecol. 2004;111:1378-1381.
19. Lawrence RA, Lawrence RM. Complicaciones médicas en la madre. En: Lawrence RA, Lawrence RM eds. Lactancia maternal, una guía para la profesión médica. 6 ed. Madrid: Elsevier; 2007:615-692.
20. Moazzez A, Kelso RL, Towfigh S, Sohn H, Berne TV, Mason RJ. Breast abscess bacteriologic features in the era of community- acquired methicillin-resistant Staphylococcus aureus epidemics. Arch Surg. 2007;142:881-884.
21. Fernández L, Arroyo R, Espinosa I, Marín M, Jiménez E, Rodríguez JM. Probiotics for human lactational mastitis. Benef Microb. 2014;5(2):169-183.
22. Tratado de obstetricia y ginecología SEGO. 13ª ed. Barcelona: Panamericana; 2013.
23. DNPAO. National Center for Chronic Disease Prevention and Health Promotion. Infant Feeding Practices Survey II: Results. Centers for Disease Control and Prevention. 2009. Disponible en: http://www.cdc.gov/ifps/results/ch2/table2-37.htm.
24. McClellan HL, Hepworth AR, Garbin CP, Rowan MK, Deacon J, Hartmann PE, et al. Nipple pain during breastfeeding with or without visible trauma. J Hum Lact. 2012;28:511-521.
25. Fetherston C. Risk factors for lactation mastitis. J Hum Lact. 1998;14:101-109.
26. World Health Organization. Mastitis: Causes and management. Geneva: World Health Organization; 2000.
27. Mediano P, Fernández L, Rodríguez JM, Marín M. Case-control study of risk factors for infectious mastitis in Spanish breastfeeding women. BMC Pregnancy Childbirth. 2014;14:195.
28. Victora CG, Bahl R, Barros AJD, França GVA, Horton S, Krasevec J, et al. Breastfeeding in the 21st century: Epidemiology, mechanisms, and lifelong effect. Lancet. 2016;387(10017):475-490.
29. West PA, Hewitt JH, Murphy OM. The influence of methods of collection and storage on the bacteriology of human milk. J Appl Microbiol. 1979;46(2):269-277.
30. Patel SH, Vaidya YH, Patel RJ, Pandit RJ, Joshi CG, Kunjadiya AP. Culture independent assessment of human milk microboal community in lactational mastitis. Sci Rep. 2017;7:7804.
31. Heikkila MP, Saris PE. Inhibition of Staphylococcus aureus by the commensal bacteria of human milk. J Appl Microbiol. 2003;95(3):471-478.
32. Murphy K, Curley D, O’Callaghan TF, O’Shea C-A, Dempsey EM, O’Toole PW et al. The Composition of human milk and infant faecal microbiota over the first three months of life: A pilot study. Sci Rep. 2017;7:40597.
33. Serafini AB, André MC, Rodrigues MA, Kipnis A, Carvalho CO, Campos MR, et al. Qualidade microbiológica de leite humano obtido em banco de leite. Rev Saúde Pública. 2003;37:775-779.
34. Martín R, Jiménez E, Heilig H, Fernández L, Marín ML, Zoetendal EG, et al. Isolation of bifidobacteria from breast milk and assessment of the bifidobacterial population by PCR-denaturing gradient gel electrophoresis and quantitative real-time PCR. Appl Environ Microbiol. 2009;75:965-969.
35. Martín V, Maldonado-Barragán A, Moles L, Rodríguez-Banõs M, del Campo R, Fernández L, et al. Sharing of bacterial strains between breast milk and infant feces. J Hum Lact. 2012;28:36-44.
36. Jost T, Lacroix C, Braegger CP, Rochat F, Chassard C. Vertical mother-neonate transfer of maternal gut bacteria via breastfeeding. Environ Microbio. 2014;16(9):2891-2904.
37. Latuga MS, Stuebe A, Seed PC. A review of the source and function of microbiota in breast milk. Semin Reprod Med. 2014;32:68-73.
38. Fernandez L, Langa S, Martın V, et al. The human milk microbiota: Origin and potential roles in health and disease. Pharmacol Res. 2013;69:1-10.
39. Department of Child and Adolescent Health and Development. Mastitis: Causes and management. Geneva, Switzerland: World Health Organization; 2000. http:// whqlibdoc.who.int/hq/2000/WHO_FCH_CAH_00.13. pdf. Accessed June 15, 2008.
40. Wambach KA. Lactation mastitis: A descriptive study of the experience. J Hum Lact. 2003;19(1):24-34.
41. Osterman KL, Rahm VA. Lactation mastitis: Bacterial cultivation of breast milk, symptoms, treatment, and outcome. J Hum Lact. 2000;16(4):297-302.
42. Arroyo R, Mediano P, Jiménez E, Delgado S, Fernández L, Marín M, et al. Diagnóstico etiológico de las mastitis infecciosas: propuesta de protocolo para el cultivo de muestras de leche humana. Acta Pediatr Esp. 2011;69:276-281.
43. Delgado S, Arroyo R, Jiménez E, Fernández L, Rodríguez JM. Mastitis infecciosas durante la lactancia: un problema infravalorado (I). Acta Pediatr Esp. 2009;67:77-84.
44. Jiménez E, Delgado S, Arroyo R, Fernández L, Rodríguez JM. Mastitis infecciosas durante la lactancia: un problema infravalorado (II). Acta Pediatr Esp. 2009;67:125-132.
45. Kayıran PG, Can F, Kayıran SM, Ergonul O, Gürakan B. Transmission of methicillin-sensitive Staphylococcus aureus to a preterm infant through breast milk. J Matern Fetal Neonatal Med. 2014;27(5):527-529.
46. Jawa G, Hussain Z, Da Silva O. Recurrent late-onsetgroup B Streptococcus sepsis in a preterm infant acquired by expressed breastmilk transmission: A case report. Breastfeed Med. 2013;8(1):134-136.
47. Aldea-Mansilla C, García de Viedma D, Cercenado E, Martin- Rabadán P, Marín M, Bouza E. Comparison of phenotypic with genotypic procedures for confirmation of coagulase-negative Staphylococcus catheter-related blood-stream infections. J Clin Microbiol. 2006;44:3529-3532.
48. Trop I, Dugas A, David J, El Khoury M, Boileau JF, Larouche N, et al. Breast abscesses: Evidence-based algorithms for diagnosis, management, and follow-up. Radiographics. 2011;31:1683-1699.
49. Hook GW, Ikeda DM. Treatment of breast abscesses with US-guided percutaneous needle drainage withoutind welling catheter placement. Radiology. 1999;213:579-582.
50. Ulitzsch D, Nyman MK, Carlson RA. Breast abscess in lactating women: US-guided treatment. Radiology. 2004;232:904-909.
51. Odom EC, Li R, Scanlon KS, Perrine CG, Grummer-Strawn L. Reasons for earlier than desired cessation of breastfeeding. Pediatrics. 2013;131:e726-e732.
52. Dennis CL, Jackson K, Watson J. Interventions for treating painful nipples among breastfeeding women. Cochrane Database Syst Rev. 2014;12:CD007366.
53. Mangesi L, Dowswell T. Treatments for breast engorgement during lactation. Cochrane Database Syst Rev. 2010;8:CD006946.
54. Arroyo R, Martín V, Maldonado A, Jiménez E, Fernández L, Rodríguez JM. Treatment of infectious mastitis during lactation: antibiotics versus oral administration of lactobacilli isolated from breast milk. Clin Infect Dis 2010;50:1551-1558.
55. Brockway M, Benzies K, Hayden KA. Interventions to improve breastfeeding self-efficacy and resultant breastfeeding rates: A systematic review and meta-analysis. J Hum Lact. 2017;33(3):486-499.
56. Betzold C. Results of microbial testing exploring the etiology of deep breast pain during lactation: A systematic review and meta-analysis of nonrandomized trials. J Midwifery Womens Health. 2012;57(4):353-364.
57. Betzold C. An update on the recognition and management of lactational breast inflammation. J Midwifery Womens Health. 2007;52(6):595-605.
58. Cusack L, Brennan M. Lactational mastitis and breast abscess, diagnosis and management in general practice. Aus Fam Physician. 2011;40(12):976-979.
59. Kataria K, Srivastava A, Dhar A. Management of lactational mastitis and breast abscesses: Review of current knowledge and practice. Indian J Surg. 2013;75(6):430-435.
60. Montalto M, Lui B. MRSA as a cause of postpartum breast abscess in infant and mother. J Hum Lact. 2009;25(4):448-450.
61. Barbosa-Cesnik C, Schwartz K, Foxman B. Lactation mastitis. JAMA 2003;289:1609-1612.
62. Ozseker B, Ozcan UA, Rasa K, Cizmeli OM. Treatment of breast abscesses with ultrasound-guided aspiration and irrigation in the emergency setting. Emerg Radiol. 2008;15(2):105-108.
Notas de autor
mastologia.bonilla@gmail.com
Información adicional
DECLARACIÓN DE CONFLICTO DE INTERESES: El autor declara no tener ningún conflicto de interés.