Revisiones

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 30 Agosto 2022
Aprobación: 07 Junio 2023
DOI: https://doi.org/10.18566/medupb.v43n1.a08
Resumen: El trauma es la principal causa de muerte de la población en edad productiva. El abordaje del trauma torácico cerrado todavía es un desafío para el médico de urgencias. Aunque no es una entidad frecuente, se asocia con una alta mortalidad y resultados adversos. El diagnóstico del trauma cerrado de aorta torácica (LCAT) requiere un alto índice de sospecha, dado que los signos y síntomas no son específicos de esta enfermedad (dolor torácico, dolor interescapular, disnea, disfagia, estridor, disfonía). Es importante resaltar que la ausencia de inestabilidad hemodinámica no debe descartar una lesión aórtica. Para su diagnóstico imagenológico se debe tener en cuenta que los rayos X de tórax no tienen el rendimiento adecuado, el patrón de referencia es la angiotomografía y el ecocardiograma transesofágico (ETE) constituye una opción diagnóstica. El manejo incluye líquidos endovenosos y antihipertensivos como medida transitoria, manejo quirúrgico definitivo y, en algunos casos, manejo expectante o diferido. Los pacientes inestables o con signos de ruptura inminente deben ser llevados de manera inmediata a cirugía. El manejo quirúrgico temprano ha impactado en la mortalidad. A pesar de los avances en las técnicas quirúrgicas, la técnica quirúrgica abierta documenta mayor tasa de mortalidad que el manejo endovascular, el cual tiene numerosas ventajas al ser poco invasivo. Esta es una revisión narrativa que destaca algunos aspectos clave sobre los mecanismos de lesión, diagnóstico y manejo inicial del trauma cerrado aorta torácica. Por último, se propone un algoritmo de abordaje de trauma de aorta.
Palabras clave: trauma cerrado de aorta torácica, trauma cerrado de tórax, trauma aórtico no penetrante.
Abstract: Trauma is the leading cause of death in the productive-age population. Addressing blunt chest trauma is still a challenge for the emergency physician. Although it is not a common entity, it is associated with high mortality and adverse outcomes. The diagnosis of blunt thoracic aortic trauma (LCAT) requires a high index of suspicion, given that the signs and symptoms are not specific to this disease (chest pain, interscapular pain, dyspnea, dysphagia, stridor, dysphonia). It is important to highlight that the absence of hemodynamic instability should not rule out aortic injury. For its imaging diagnosis, it must be taken into account that chest X-rays do not have adequate performance; the reference standard is angiotomography and transesophageal echocardiography (TEE) is a diagnostic option. Management includes intravenous fluids and antihypertensives as a temporary measure, definitive surgical management and, in some cases, expectant or deferred management. Unstable patients or patients with signs of imminent rupture should be taken immediately to surgery. Early surgical management has impacted mortality. Despite advances in surgical techniques, the open surgical technique documents a higher mortality rate than endovascular management, which has numerous advantages as it is minimally invasive. This is a narrative review that highlights some key aspects about the mechanisms of injury, diagnosis and initial management of blunt thoracic aortic trauma. Finally, an algorithm for addressing aortic trauma is proposed.
Keywords: blunt thoracic aortic injury, blunt chest trauma, nonpenetrating aortic injury.
Introducción
El trauma todavía es la causa más común de muerte en pacientes que se encuentran en edad productiva1. En el estudio Crash II, dentro de los datos que aporta Colombia, se reportó que cerca del 90 % de las muertes por trauma en el país son de origen violento, en mayor proporción que las atribuibles a trauma por accidentes de tránsito o trauma cerrado. En este estudio se evaluaron 1.667 pacientes de los que se recopiló información desde el 2005 hasta el 2008. En Colombia, solo el 27.2 % de los casos tenía trauma cerrado, en cambio, en el resto del mundo, la mayoría de los casos fueron por trauma cerrado y solo el 25 % por heridas penetrantes2.
Si bien el trauma cerrado de la aorta torácica no es la presentación más frecuente en casos de trauma cerrado de tórax (ocurre en menos del 1 % de los accidentes de vehículos motorizados) se asocia con una alta mortalidad3. Se estima que es responsable del 16 % de las muertes y que el 80 % de los pacientes fallece antes de llegar a una institución de salud4.
Por lo general, las lesiones de aorta torácica se generan en un 80 % de los casos por accidentes de tránsito, conductor o pasajero en el 50 % y peatones arrollados por vehículo en un 30 %. Es usual que las lesiones sean el resultado de fenómenos de fuerza de desaceleración, pinzamiento óseo, torsión y aumento de la presión hidrostática con el fenómeno descrito como martillo de agua, el sitio más afectado es el istmo aórtico, hasta en un 45 %1,3,4,5,6.
A continuación, se describen las tres teorías principales que explican la lesión cerrada de aorta torácica (LCAT)1:
1. Istmo aórtico: esta área está predispuesta a ir en vectores opuestos durante una desaceleración rápida, provoca desgarro de la íntima.
2. Resistencia a la tracción: el istmo aórtico tiene una baja resistencia, lo que lo hace más vulnerable a las lesiones.
3. Punto de compresión: pinzamiento óseo entre las estructuras óseas de la parte anterior del tóraz y la columna vertebral durante un traumatismo por desaceleración.
En el registro nacional de trauma americano del 2012, se reportaron 850 lesiones traumáticas de la aorta torácica con una prevalencia del 0.3 %. Por su parte, en el registro alemán de trauma se evidenciaron 74 casos anuales con una prevalencia del 1.28 % y una mortalidad global descrita hasta en un 64 %5,6.
Debido a su alta mortalidad, es importante la búsqueda activa de signos y síntomas sugestivos de lesión de aorta torácica desde el primer contacto del paciente con trauma en el servicio de urgencia. Esto en contexto de una cinemática de trauma específica para definir posibles riesgos y lesiones asociadas, con el fin de dar inicio al manejo de manera temprana y orientar las ayudas diagnósticas pertinentes6,7,8.
Desde el escenario prehospitalario puede obtenerse información importante para determinar los riesgos de algunas lesiones específicas. Por ejemplo, en cuanto a la cinemática de alta energía, para aumentar la sospecha de LCAT, se pueden tener en cuenta: el accidente en vehículo automotor a más de 50 km/h, accidente de vehículo automotor contra barreras artificiales, paciente que sale eyectado del vehículo, encontrar ruedas rotas, accidentes en motocicleta o aéreos, peatones arrollados por vehículo automotor, caídas de altura mayores de 3 metros, lesiones por aplastamiento o hundimiento en el vehículo, no uso de cinturón de seguridad y la pérdida de consciencia. Por ello, será de vital importancia obtener estos datos del personal de atención prehospitalaria, pues diferentes registros describen condiciones que sugieren una cinemática de alta energía involucrada hasta en el 33.8 % de los casos9,10.
El objetivo de esta revisión narrativa es realizar una evaluación de la literatura actual y proponer un algoritmo de manejo según la evidencia actual para la LCAT.
Tema central
Manifestaciones clínicas
A pesar de la descripción clínica que ofrece la literatura, menos del 50 % de los pacientes presentan síntomas específicos. En un análisis retrospectivo de los pacientes del registro Alfred de trauma, se encontró que los pacientes con LCAT presentaron dolor torácico hasta en un 44.2 %, disnea en un 32.9 % y el dolor en el dorso solo se describe para el 11.8 %11,12.
Algunos de los síntomas que pueden presentar los pacientes son: dolor torácico, dolor interescapular, disnea, disfagia, estridor y disfonía. Esta última debe aumentar la sospecha clínica de un hematoma mediastinal12.
Además del examen físico, deben describirse las condiciones en las que ingresa el paciente, por ejemplo, los signos vitales, signos de hipoperfusión clínica y hallazgos como estigmas del cinturón de seguridad, impronta de llanta en tórax, hematoma supraclavicular izquierdo o nuevo soplo cardíaco. Se debe buscar de manera activa deformidad o equimosis que sugieran fractura del esternón, escápula o clavícula, estos últimos como indicativos de una cinemática de alta energía involucrada8,9,10,11. En cuanto a la hipotensión, esta solo se documenta del 20 al 50 % de los de los casos11, se encuentra con mayor frecuencia en el contexto de politrauma y otras lesiones asociadas. Se debe resaltar que la ausencia de inestabilidad hemodinámica no debe descartar una lesión aórtica9,10,12.
Por otra parte, la alteración del estado de conciencia a menudo se toma como parámetro de perfusión, sin embargo, en este escenario es difícil diferenciar su etiología (trauma craneoencefálico vs. hipoperfusión). Se evidencia hasta en el 41 % de los casos9,10,12.
Por último, la sospecha diagnóstica dependerá de una sumatoria de variables, como: la cinemática del trauma y los síntomas y signos del paciente. Así que se requieren ayudas diagnósticas para la confirmación de la LCAT9,10.
Ayudas diagnósticas
Rayos X de tórax
Los rayos X de tórax están disponibles de forma amplia en los servicios de urgencias y pueden aportar información que aumente la sospecha de una LCAT. Aunque se debe aclarar que por sí solos no tienen el rendimiento adecuado para realizar o descartar el diagnóstico13.
Entre los hallazgos radiográficos se describen: el ensanchamiento mediastinal (≥ 8 cm), lateralización de la tráquea o esófago a la derecha, pérdida del contorno aórtico normal, pérdida de la ventana aortopulmonar, opacidad pleural apical y depresión del bronquio principal izquierdo14. Otros hallazgos, como la presencia de fracturas claviculares y vertebrales torácicas, pueden indicar un trauma con cinemática de alta energía14,15,16,17.
Se debe tener en cuenta que la imagen puede ser normal en un 7 % a 13 % de los casos. Ninguno de los hallazgos descritos es específico de la lesión y, de forma independiente, el hallazgo de ensanchamiento mediastinal tiene una sensibilidad para la detección de lesión del 33 %14,15,16,17,18.
Angiotomografía
El patrón de referencia para el diagnóstico de la lesión aórtica es la ATAC, con una sensibilidad y especificidad del 99 %. Su alta sensibilidad, la rapidez para su realización y su creciente disponibilidad la han ubicado como la imagen diagnóstica de elección15. En la ATAC se pueden encontrar signos como: hematoma mediastinal o periaórtico, alteración de la grasa para aórtica, pared aórtica de contornos irregulares, pseudocoartación, formación de aneurisma sacular con calcificación periférica, hematomas o flaps de disección y extravasación activa del medio de contraste16,17,18,19,20,21,22,23.
Los hallazgos tomográficos más frecuentes son los planos grasos mal definidos en el 39 % de los casos y la hemorragia mediastinal en el 18 %. Ciertos autores sugieren que la ausencia de este último está relacionada con la ausencia de lesiones mayores de la aorta torácica. Como signos directos de la lesión se describen las anormalidades en el contorno aórtico hasta en un 3.7 % de los casos de LCAT. Algunos autores describen que la ausencia de los anteriores hallazgos tiene un valor predictivo negativo del 100 %, por lo que es posible descartar dicha entidad16,17,18,19,20,21,22,23.
Patel et al. sugieren el uso de una lista de chequeo para el reporte radiológico de la angiotomografía de tórax, en contexto de lesión traumática de la aorta, que podría usarse por el clínico durante la revisión de la imagen. Los componentes de dicha lista se presentan a continuación17:
● Contorno de la curvatura inferior del arco aórtico.
● Desgarro o flap intimal.
● Presencia de pseudoaneurisma.
● Hematoma mediastinal.
● Hematoma periaórtico.
● Presencia de hemotórax.
● Lesiones adicionales, como fracturas (vertebrales, omóplato, primer y segundo arco costal).
Ecocardiograma transesofágico (ETE)
El ETE constituye una opción diagnóstica. Con este se puede identificar un flap de la íntima, regurgitación de la válvula aórtica, presencia de hematoma intramural o signos de ruptura libre. Si el paciente está inestable o se encuentra en medio de una intervención quirúrgica para controlar el shock hemorrágico por lesión en otro sitio anatómico, los resultados de esta pueden ayudar a guiar otros enfoques y necesidades durante reanimación1.
Clasificación de las lesiones aórticas en trauma cerrado de tórax
A partir de las imágenes diagnósticas puede clasificarse la lesión y definir un posible abordaje. En la literatura se describen dos clasificaciones para la lesión cerrada de aorta torácica, entre ellas: la clasificación de la sociedad de cirugía vascular (SVS, por sus siglas en inglés) y Harborview, como se describe en la tabla 1 con su respectiva frecuencia de presentación24,25.
Clasificación de las lesiones aórticas trauma cerrado de aorta
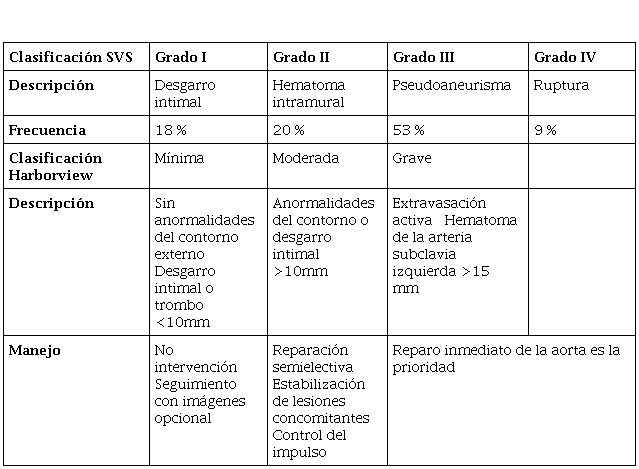
Nota adaptada por los autores(referencias: 24,25).
Factores de riesgo de ruptura temprana
Harris et al. describieron un score para predecir el riesgo de ruptura aórtica temprana, dentro de las variables están: un lactato >4 mmol/L, un diámetro de hematoma en la aorta torácica descendente >10 mm y una relación entre el diámetro del pseudoaneurisma con el diámetro de la aorta >1.4. Si se identifican >2 de los anteriores criterios, existe una sensibilidad del 100 % y especificidad del 88 % para predecir una ruptura de aquellas que no se presentan de manera inmediata con evidencia de extravasación activa del medio de contraste, se presenta entre 44 minutos y dos horas posteriores al trauma. Rabin et al. describen dentro de los factores de riesgo para ruptura: una circunferencia de pseudoaneurisma mayor o igual al 50 % de la circunferencia aórtica y un hematoma mediastinal con efecto de masa, pseudocoartación de aorta o hemotórax izquierdo25.
Manejo de la lesión aórtica en trauma cerrado de tórax
Manejo médico
Dentro del abordaje inicial es fundamental realizar un soporte vital dirigido, como propone el Advanced Trauma Life Support (ATLS) a través del ABCDE26.
En cuanto a los líquidos endovenosos, no existen recomendaciones claras en la literatura. Aun así, podría tomarse la recomendación de estudios como el Smart Trial y el PROSPERO; lo ideal son soluciones balanceadas en el paciente crítico y limitar el volumen infundido de los mismos, ya que el aumento de la presión intravascular podría llevar al aumento de la presión hidrostática y, como consecuencia, a progresión la lesión. Esto tiene bases en estudios, por ejemplo, el realizado por Bickell et al. como una estrategia de reanimación hídrica diferida27,28,29.
Respecto al uso de antihipertensivos, usados entre el 25 al 84 % de los casos, existen reportes de caso desde el año 1970 sobre su uso y ahora constituye la piedra angular en el manejo médico. Su uso es una medida transitoria hasta llevar a cabo una intervención quirúrgica o endovascular, en algunas series se asocia con una menor mortalidad o presencia de ruptura antes de la intervención23,30,31,32.
Existen diferentes recomendaciones con respecto a las metas de presión arterial en el escenario de LTAI grado II-grado IV, la ATLS recomienda mantener una presión arterial media entre 60 a 70 mmHg, con una frecuencia cardiaca menor a ≤80 latidos por minuto. No obstante, otros autores abogan por mantener una presión arterial sistólica ≤100 mmHg y una frecuencia cardiaca ≤100 latidos por minuto, con iguales recomendaciones para las cifras de tensión arterial media. Esto permitiría disminuir el estrés sobre la pared del vaso. En los casos de neurotrauma o pacientes gestantes, no se recomienda dicha estrategia por el riesgo de hipoperfusión en el sistema nervioso central o disminución en el flujo sanguíneo placentario25,26,32.
Manejo quirúrgico abierto y endovascular
En principio, el reparo quirúrgico inmediato era la regla. A pesar de esto y dado que no es usual que la lesión de aorta torácica se presente como lesión aislada (y las otras lesiones complicarían la intervención), varios estudios han mostrado seguridad en el abordaje diferido (>24 horas) en pacientes con otras lesiones asociadas32,33,34.
El tiempo óptimo para la intervención quirúrgica de la aorta aún es controversial, se ha visto que la cirugía inmediata tiene una alta morbimortalidad, entre un 20 y 40 %. En diferentes estudios se ha observado que el reparo diferido tiene mayores beneficios sobre la supervivencia, lo que se traduce en menor mortalidad en comparación con el manejo temprano abierto4.
Los pacientes inestables o con signos de ruptura inminente deben ser llevados de manera inmediata, ya sea a manejo quirúrgico abierto o a manejo endovascular. A pesar de las mejoras en las técnicas quirúrgicas abiertas, este abordaje tiene una morbimortalidad alta, incluso al realizarse de manera diferida35,36.
Rabin et al. realizaron un seguimiento de los pacientes manejados de manera conservadora, en quienes se describió una mortalidad del 31 %, secundaria a las lesiones asociadas (trauma craneoencefálico severo, trauma de abdomen y pelvis). Incluso, durante el seguimiento por un periodo promedio de 3.8 meses, el 91 % de los pacientes presentaron resolución o no evidencia en la progresión de la lesión, sin documentarse muertes relacionadas con ruptura o necesidad de manejo emergente en LCAT37.
De acuerdo con las clasificaciones ya descritas, la LCAT grado IV requiere un procedimiento emergente y está asociada con una mayor mortalidad. Las lesiones grado III se deberían reparar de manera urgente y pacientes sin signos secundarios de lesión se pueden someter a un reparo diferido después del manejo médico inicial37. Por otro lado, las lesiones grado I y grado II son las más susceptibles de manejo conservador37,38.
Manejo quirúrgico abierto
En las últimas décadas el reparo abierto ha tenido numerosas modificaciones. En los años 70 se hablaba de un manejo basado en "pinzar y suturar", una técnica que por lo general incluye la interposición de un injerto de Dacrón para hacer puente al defecto. Estas técnicas se asociaban con una mortalidad de hasta el 16 %, con reportes de paraplejia en un 19 % de los pacientes4.
Luego se emplearon técnicas que adicionan el uso de shunts heparinizados desde la aorta proximal hasta la aorta distal para llevar sangre de manera pasiva más allá del sitio de la lesión. La intención es reducir el riesgo de infarto espinal, sin embargo, esa reducción no fue significativa hasta que se adicionó un sistema de bombeo activo, "perfusión activa", que redujo la tasa de parálisis a un 2.3 %. La perfusión activa puede alcanzarse de dos maneras, una es con un bypass desde la aurícula izquierda a la arteria femoral o aorta descendente, en su defecto, que se puede realizar con una cantidad baja de heparina si se cuenta con una bomba centrífuga. La otra manera es realizando un bypass veno arterial que requiere la canulación de la arteria pulmonar y de la arteria femoral, así se inserta una cánula larga a través de la vena femoral que llegue a la aurícula derecha4,36.
Para la técnica abierta se requiere intubación orotraqueal con tubo de doble lumen y exposición de la lesión a través de una toracotomía anterolateral izquierda en el cuarto espacio intercostal, asociado a ventilación unilateral derecha para permitir el acceso a la lesión. Despues, se pinza la aorta proximal, distal al origen de la subclavia izquierda; es usual necesitar la colocación de un injerto de interposición4,36,39.
A pesar de los avances en las técnicas, la evidencia recolectada de la experiencia en centros de trauma especializados ha documentado una tasa de mortalidad de hasta el 31 % y 8.7 % de paraplejía4.
Manejo quirúrgico endovascular
El manejo endovascular fue descrito hace 50 años, primero por Parodi, extrapolado del manejo de aneurismas de aorta abdominal, con la colocación de endoprótesis a través de la arteria femoral40. Esta técnica tiene numerosas ventajas al ser poco invasiva, pues no se requiere intubación selectiva y se ahorran las comorbilidades asociadas a una toracotomía. También tiene la ventaja de requerir mínimas dosis de heparina, inclusive puede realizarse sin necesidad del anticoagulante pues no se realiza ningún bypass40.
Para esta estrategia se reporta una mortalidad intrahospitalaria entre el 6.8 % y el 7.3 % mucho menor en contraste con la técnica quirúrgica abierta, donde se han descrito diferentes factores de riesgo como la edad, sexo masculino, insuficiencia renal, compromiso de la arteria subclavia izquierda y un alto índice de gravedad de la lesión. En cuanto a sus complicaciones, la prevalencia de endofuga solo se describe entre el 0.01 %-1.2 %3,34,35.
Estos hallazgos han sido documentados en otras series, lo cual indica que el manejo endovascular parece tener una mortalidad inferior y una menor tasa de complicaciones al compararse con el manejo quirúrgico abierto40,41,42,43. Dado lo anterior, la literatura propone el manejo endovascular como la primera elección de tratamiento por encima del reparo abierto23,32,44,45,46.
Según las guías de manejo endovascular de la SVS se sugiere manejo en las primeras 24 horas. Se deben priorizar otras lesiones concomitantes o repararse de manera inmediata una vez esas lesiones extra aórticas que amenazan la vida hayan sido resueltas. De esa manera, se expone una mortalidad de 46 %47.
Si la lesión aórtica es mínima, como defectos intimales, periadvencicia, o hematomas que no se visualizan en la imagen tomográfica, se recomienda un manejo expectante en lesiones tipo I-II, dado que no se encuentra diferencia entre el manejo médico o el endovascular en desenlaces como ventilación mecánica prolongada (>48 horas), estancia hospitalaria, estancia en unidad de cuidados intensivos, mortalidad hospitalaria y mortalidad asociada a la lesión aórtica. En caso de escoger esta estrategia, debe realizarse imagen radiográfica vigilando posible progresión41,47,48.
Por otra parte, se han propuesto diferentes factores independientes asociados a mayor mortalidad, dentro de los cuales se incluyen la edad avanzada (>60 años), sexo masculino, lesión renal (creatinina >1.2 mg/dL), compromiso de la arteria subclavia izquierda y altos puntajes de ISS.49 La presencia de estos factores podría orientar la toma de decisiones desde el servicio de urgencias y conducta quirúrgica.
Las lesiones grado II (hematomas intramurales), grado III (pseudoaneurismas) o grado IV (ruptura), siempre deben ser reparadas. Con respecto a la heparinización sistémica se recomienda utilizar dosis más bajas que en una endoprótesis electiva e inclusive una pequeña parte del comité describe que puede no ser necesaria por la duración del procedimiento y el escaso riesgo trombótico que implica. Aun así, debe individualizarse cada paciente35,50,51.
Abordaje del trauma cerrado de aorta desde el servicio de urgencias (Conclusión)
La lesión traumática de la aorta representa un desafío diagnóstico debido a los síntomas de presentación altamente inespecíficos, su identificación dependerá de la sospecha clínica basada en los hallazgos iniciales. El diagnóstico temprano es crucial para el manejo guiado y la reparación definitiva.
A continuación, se presenta una propuesta de los autores para el abordaje del trauma cerrado de aorta desde el servicio de urgencias (figura 1).
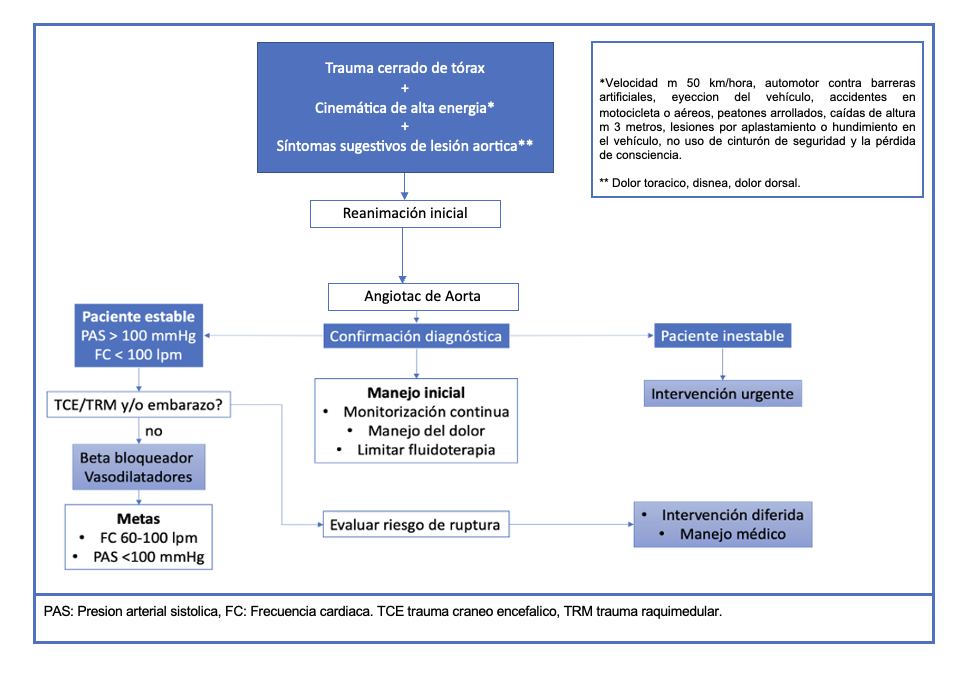
Figura 1
Propuesta de abordaje del trauma cerrado de aorta.
Referencias
1. Mouawad NJ, Paulisin J, Hofmeister S, Thomas MB. Blunt thoracic aortic injury - Concepts and management. Journal of Cardiothoracic Surgery. 2020;15(1):62.
2. Mejia J, Puentes F, Ciro J, Morales C. Hemorragia y trauma, avances del estudio CRASH2 en Colombia. Rev Colomb Cir. 2009;24:175-83.
3. Estrera AL, Miller CC, Guajardo-Salinas G, Coogan S, Charlton-Ouw K, Safi HJ, et al. Update on blunt thoracic aortic injury: Fifteen-year single-institution experience. J Thor Cardiovasc Surg. 2013;145(3):S154-S158.
4. Neschis DG, Scalea TM, Flinn WR, Griffith BP. Blunt aortic injury. 2008;359(16):1708-16.
5. Loren BF, Colonel L, Mattingly TW, Gen B, Manion WC, Jahnke EJ. Nonpenetrating traumatic injury of the aorta. 1958;17(6):1086-101.
6. Demetriades D. Blunt thoracic aortic injuries: Crossing the Rubicon. Journal of the American College of Surgeons. 2012;214(3):247–59.
7. Dahal R, Acharya Y, Tyroch AH, Mukherjee D. Blunt thoracic aortic injury and contemporary management strategy. Angiology. 2022;73(6):497-507.
8. Gombert A, Barbati ME, Storck M. Treatment of blunt thoracic aortic injury in Germany-Assessment of the TraumaRegister DGU®. Plos One. 2017;12(3):0171837.
9. Malekpour M, Dove JT, Wild JL, Orlova K. Association between timing of traumatic thoracic aortic injury repair and outcome: A national trauma databank study. J Am Coll Surg. 2018;227(4):e229.
10. Cook CC, Gleason TG. Great vessel and cardiac trauma. Surgical Clinics of North America. 2009;89(4):797-820.
11. Bade-Boon J, Mathew JK, Fitzgerald MC, Mitra B. Do patients with blunt thoracic aortic injury present to hospital with unstable vital signs? A systematic review and meta-analysis. Emergency Medicine Journal. 2018;35(4):231-237.
12. O'Conor CE. Diagnosing traumatic rupture of the thoracic aorta in the emergency department. Emerg Med J. 2004 Jul;21(4):414-9.
13. Gutiérrez A, Inaba K, Siboni S, Effron Z, Haltmeier T, Jaffray P, et al. The utility of chest X-ray as a screening tool for Blunt Thoracic Aortic Injury. Injury. 2016;47(1):32–6.
14. Parry, Moffat, Vogt C. Blunt thoracic trauma: Recent advances and outstanding questions. Curr Opin Crit Care. 2015;21(6):544-8.
15. Forman MJ, Mirvis SE, Hollander DS. Blunt thoracic aortic injuries: CT characterisation and treatment outcomes of minor injury. Eur Radiol. 2013;23(11):2988-95.
16. Bade-Boon J, Mathew JK, Fitzgerald MC, Mitra B. Traumatic aortic injury presenting to an adult major trauma centre. Trauma (United Kingdom). 2019;21(4):272-279.
17. Patel NR, Dick E, Batrick N, Jenkins M, Kashef E. Pearls and pitfalls in imaging of blunt traumatic thoracic aortic injury: A pictorial review. Br J Radiol. 2018;91(1089):20180130.
18. Fox N, Schwartz D, Salazar JH. Evaluation and management of blunt traumatic aortic injury: A practice management guideline from the Eastern Association for the Surgery of Trauma. J Tr Acute Care Surg. 2015;78(1):136-146.
19. Steenburg SD, Ravenel JG, Ikonomidis JS, Schönholz C, Reeves S. Acute traumatic aortic injury: Imaging evaluation and management. Radiology. 2008;248(3):748-762.
20. Bruckner BA, DiBardino DJ, Cumbie TC, Trinh C, Blackmon SH, Fisher RG, et al. Critical evaluation of chest computed tomography scans for blunt descending thoracic aortic injury. Annals of Thoracic Surgery. 2006;81(4):1339–46.
21. Yu L, Baumann BM, Raja AS, Mower WR, Langdorf MI, Medak AJ, et al. Blunt traumatic aortic injury in the pan-scan era. Acad Emerg Med. 2020;27(4):291-296.
22. Dyer DS, Moore EE, Ilke DN. Thoracic aortic injury: How predictive is mechanism and is chest computed tomography a reliable screening tool? A prospective study of 1,561 patients. J Trauma. 2000;48(4):673-82.
23. Akhmerov A, DuBose J, Azizzadeh A. Blunt thoracic aortic injury: Current therapies, outcomes, and challenges. Annals Vasc Dis. 2019;12(1):1-5.
24. Quiroga E, Starnes BW, Tran NT, Singh N. Implementation and results of a practical grading system for blunt thoracic aortic injury. J Vasc Surg. 2019;70:1082-1088.
25. Harris DG, Rabin J, Kufera JA. A new aortic injury score predicts early rupture more accurately than clinical assessment. J Vasc Surg. 2015;61(2):332-338.
26. ATLS - Advanced trauma life support. 10th edition: American College of Surgeons, Committee on Trauma. 2018.
27. Bickell WH, Wall MJ Jr, Pepe PE, Martin RR, Ginger VF, Allen MK, et al. Immediate versus delayed fluid resuscitation for hypotensive patients with penetrating torso injuries. N Engl J Med. 1994;331(17):1105-9.
28. Semler MW, Self WH, Wanderer JP, Ehrenfeld JM, Wang L, Byrne DW, et al. Balanced crystalloids versus saline in critically ill adults. N Engl J Med. 2018;378(9):829-839.
29. Hammond DA, Lam SW, Rech MA, Smith MN, Westrick J, Trivedi AP, et al. Balanced crystalloids versus saline in critically ill adults: A systematic review and meta-analysis. Ann Pharmacother. 2020;54(1):5-13.
30. Harris DG, Rabin J, Starnes BW, et al. Evolution of lesion-specific management of blunt thoracic aortic injury. J Vasc Surg. 2016;64(2):500-505.
31. American College of Surgeons. Committee on Trauma. Advanced Trauma Life Support: Student Course Manual. American College of Surgeons; 2012.
32. Fabian TC, Davis KA, Gavant ML, Croce MA, Melton SM, Patton JH Jr, et al. Prospective study of blunt aortic injury: Helical CT is diagnostic and antihypertensive therapy reduces rupture. Ann Surg. 1998;227(5):666-76.
33. Azizzadeh A, Charlton-Ouw KM, Chen Z, Rahbar MH, Estrera AL, Amer H, et al. An outcome analysis of endovascular versus open repair of blunt traumatic aortic injuries. J Vasc Surg. 2013;57(1):108–15.
34. Hemmila MR, Arbabi S, Rowe SA, Brandt M-M, Wang SC, Taheri PA, et al. Delayed repair for Blunt thoracic aortic injury: Is it really equivalent to early repair? Journal of Trauma: Injury, Infection, and Critical Care. 2004;56(1):13–23.
35. di Marco L, Pacini D, di Bartolomeo R. Acute traumatic thoracic aortic injury: Considerations and reflections on the endovascular aneurysm repair. AORTA. 2013;1(2):117-122.
36. Medeiros R, Tavares E, Manuel de Almeida C, Pampolha G, Da Silva A, Madrini V, et al. Blunt aortic injury: Surgical treatment of the ascending and descending aorta. Multimed Man Cardiothorac Surg. 2021;2021.
37. Rabin J, DuBose J, Sliker CW, O’Connor J, Scalea TM, Griffith BP. Parameters for successful nonoperative management of traumatic aortic injury. J Thor Cardiovasc Surg. 2014;17:143-150.
38. Sandhu HK, Leonard SD, Perlick A, Saqib NU, Miller CC, Charlton-Ouw KM, et al. Determinants and outcomes of nonoperative management for Blunt traumatic aortic injuries. J Vasc Surg. 2018;67(2):389–98.
39. Calcaterra D. Blunt traumatic aortic injury. In: Sözen S, Kanat BH, editors. Trauma and emergency surgery [Internet]. London: IntechOpen; 2021 [citado 29 de agosto de 2022]. Disponible en: https://www.intechopen.com/chapters/77555 doi: 10.5772/intechopen.98724
40. Akowuah E, Baumbach A, Wilde P, Angelini G, Bryan AJ. Emergency repair of traumatic aortic rupture: Endovascular versus conventional open repair. J Thor Cardiovasc Surg. 2007;134(4):897–901.
41. Gaffey AC, Zhang J, Saka E, Quatromoni JG, Glaser J, Kim P, et al. Natural history of nonoperative management of grade II blunt thoracic aortic injury. Ann Vasc Surg. 2020;65:124-129.
42. Watson J, Slaiby J, Garcia M, Marcaccio EJ, Chong TT. A 14-year experience with blunt thoracic aortic injury. J Vasc Surg. 2013;58:380-385.
43. Khoynezhad A, Azizzadeh A, Donayre CE, Matsumoto A, Velazquez O, White R. Results of a multicenter, prospective trial of thoracic endovascular aortic repair for Blunt thoracic aortic injury (RESCUE trial). J Vasc Surg. 2013;57(4): 899-905.e1.
44. Ho XN, Wee IJ, Syn N, Harrison M, Wilson L, Choong AM. The endovascular repair of blunt traumatic thoracic aortic injury in Asia: A systematic review and meta-analysis. Vascular. 2019;27(2):213-223.
45. Murad MH, Rizvi AZ, Malgor R, Carey J, Alkatib AA, Erwin PJ, et al. Comparative effectiveness of the treatments for thoracic aortic transaction. J Vasc Surg. 2011;53(1):193-199.e1-21.
46. Karmy-Jones R, Ferrigno L, Teso D, Long WB, Shackford S. Endovascular repair compared with operative repair of traumatic rupture of the thoracic aorta: A Nonsystematic Review and a plea for trauma-specific reporting guidelines. Journal of Trauma: Injury, Infection & Critical Care. 2011;71(4):1059–72.
47. Lee WA, Matsumura JS, Mitchell RS. Endovascular repair of traumatic thoracic aortic injury: Clinical practice guidelines of the Society for Vascular Surgery. J Vasc Surg. 2011;53(1):187-192.
48. DuBose JJ, Charlton-Ouw K, Starnes B, Saqib N, Quiroga E, Morrison J, et al. Do patients with minimal blunt thoracic aortic injury require thoracic endovascular repair? J Trauma Acute Care Surg. 2021;90(2):384-387.
49. Mohapatra A, Liang NL, Makaroun MS, Schermerhorn ML, Farber A, Eslami MH. Risk factors for mortality after endovascular repair for blunt thoracic aortic injury. J Vasc Surg. 2020;71(3):768-773.
50. DuBose JJ, Leake SS, Brenner M, Pasley J, O’Callaghan T, Luo-Owen X, et al. Contemporary Management and outcomes of Blunt Thoracic Aortic Injury. Journal of Trauma and Acute Care Surgery. 2015;78(2):360–9.
51. Dahal R, Acharya Y, Tyroch AH, Mukherjee D. Blunt thoracic aortic injury and Contemporary Management Strategy. Angiology. 2022;73(6):497–507.
Notas de autor
cindyzeta33@outlook.es
Información adicional
Conflictos de interés: Los autores declaran no tener conflictos de intereses.
