Originales

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 20 Abril 2024
Aprobación: 22 Octubre 2024
DOI: https://doi.org/10.18566/medupb.v44n1.a02
Resumen:
Objetivo: evaluar el efecto de la terapia de estimulación magnética transcraneal repetitiva (EMTr) en el tratamiento del dolor neuropático de origen oncológico y no oncológico, puesto que la EMTr es una alternativa innovadora para el manejo del dolor neuropático y es una técnica de estimulación cerebral no invasiva que induce corrientes eléctricas en el tejido nervioso de la corteza.
Métodos: la búsqueda bibliográfica se realizó en las bases de datos CENTRAL, MEDLINE, Embase, PsycINFO, SCOPUS y LILACS. Los criterios de inclusión fueron 1) población: hombres y mujeres entre 18 y 85 años, con dolor neuropático oncológico y no oncológico; 2) intervención: tratado con estimulación magnética transcraneal; 3) comparación: grupos de control inactivos e intervenciones activas paralelas; y 4) resultado: el resultado primario fue la modulación del dolor. Los resultados secundarios fueron la calidad de vida y los efectos adversos. También se evaluaron el riesgo de sesgo y la calidad de la evidencia.
Resultados: la búsqueda arrojó 1116 artículos, de los cuales 21 cumplieron los criterios PICO. 12 estudios controlados aleatorizados (ECAS) y 9 estudios observacionales. La muestra total fue de 911 pacientes, el número de sesiones varía desde una única sesión hasta 15 sesiones, con una media de 3.5 sesiones. El seguimiento se realizó entre el día 7 y los 311.8 días, con un promedio de 45 días. La reducción del dolor fue reportada en los 21 estudios.
Conclusión: la EMTr puede ser una opción terapéutica eficaz para tratar el dolor neuropático oncológico y no oncológico. Se encontró evidencia de calidad moderada para la modulación del dolor; para la calidad de vida los resultados son inciertos al momento de determinar cambios, debido a que la evidencia es muy baja. Se necesitan esfuerzos de investigación adicionales para reducir el sesgo y mejorar la calidad de los estudios.
Palabras clave: dolor neuropático, estimulación magnética transcraneal, dolor oncológico.
Abstract:
Objective: Repetitive Transcranial Magnetic Stimulation (rTMS) is a ground-breaking alternative for the treatment of neuropathic pain. rTMS is a brain stimulation technique that is noninvasive and induces electrical currents in the cortex’s nervous tissue. The aim of this study was to assess the effect of rTMS for the treatment of pain, regardless of its non-oncological or oncological origin.
Methods: We performed a search in MEDLINE, CENTRAL, Embase, PsycINFO, LILACS and SCOPUS. The inclusion criteria were 1) population: men and women between 18 and 85 years-age, with neuropathic pain (oncological and non-oncological); 2) intervention: treatment with transcranial magnetic stimulation; 3) comparison: inactive control groups and parallel active interventions; and 4) outcome: primary outcome, pain modulation. Secondary outcomes, quality of life and adverse effects. The risk of bias and quality of evidence were assessed as well.
Results: The search yielded 1116 articles, of which 21 met the PICO criteria. 12 randomized controlled trials (RCTs) and 9 observational studies. The total sample was 911 patients, the number of sessions varied from one single session to 15, with a mean of 3.5 sessions. Follow-up was performed between day 7 and 311.8 days, with a mean of 45 days. Pain reduction was reported in all 21 reports.
Conclusion: rTMS might be an effective therapeutic choice for oncological and non-oncological neuropathic pain. Evidence of moderate quality was found for pain modulation; for the quality of life the results are uncertain to determine changes, because the evidence level is very low. Additional research efforts are needed to reduce bias and improve the quality of the studies.
Keywords: neuropathic pain, transcranial magnetic stimulation, cancer pain.
Resumo:
Objetivo: avaliar o efeito da terapia de Estimulação Magnética Transcraniana Repetitiva (EMTr) no tratamento da dor neuropática de origem oncológica e não oncológica, uma vez que a EMTr é uma alternativa inovadora para o manejo da dor neuropática e é uma técnica de estimulação cerebral. invasivo que induz correntes elétricas no tecido nervoso do córtex.
Métodos: a busca bibliográfica foi realizada nasbases de dados CENTRAL, MEDLINE, Embase, PsycINFO, SCOPUS e LILACS. Os critérios de inclusão foram 1) população: homens e mulheres entre 18 e 85 anos, com dor neuropática oncológica e não oncológica; 2) intervenção: tratada com estimulação magnética transcraniana; 3) comparação: grupos de controle inativos e intervenções ativas paralelas; e 4) desfecho: o desfecho primário foi a modulação da dor. Os desfechos secundários foram qualidade de vida e efeitos adversos. O risco de viés e a qualidade da evidência também foram avaliados.
Resultados: A busca retornou 1.116 artigos, dos quais 21 atenderam aos critérios PICO. 12 estudos controlados aleatorizados (ECAS) e 9 estudos observacionais. A amostra total foi de 911 pacientes, o número de sessões varia de uma única sessão até 15 sessões, com média de 3.5 sessões. O acompanhamento foi realizado entre o dia 7 e 311.8 dias, com média de 45 dias. A redução da dor foi relatada em todos os 21 estudos.
Conclusão: A EMTr pode ser uma opção terapêutica eficaz no tratamento da dor neuropática oncológica e não oncológica. Encontramos evidências de qualidade moderada para modulação da dor; para qualidade de vida, os resultados são incertos na determinação de alterações, pois a evidência é muito baixa. Esforços adicionais de pesquisa são necessários para reduzir preconceitos e melhorar a qualidade dos estudos.
Palavras-chave: dor neuropática, estimulação magnética transcraniana, dor oncológica.
INTRODUCCIÓN
El dolor neuropático incluye cualquier tipo de disfunción o lesión primaria que afecte tanto al sistema nervioso periférico (SNP) como al central (SNC)1,2. Etiológicamente puede ocurrir por diversas causas: traumatismo, isquemia o hemorragia, inflamación, neurotoxicidad, neurodegeneración, alteración metabólica, deficiencia de vitaminas o cáncer3,4.
La prevalencia estimada de dolor neuropático en la población general está entre el 7 % y el 10 %5, entre el 11 % y el 57 % de las personas con accidente cerebrovascular6, el 53 % de las personas con trauma raquimedular7 y el 40 % de las personas con diabetes tipo 28. Esto puede variar según los criterios de diagnóstico, los métodos de evaluación y las características del paciente9.
Adicionalmente, el dolor es un problema muy común en los pacientes con cáncer10,11, más del 30 % de los pacientes experimentan dolor neuropático12; la tercera parte es causada por neuropatía inducida por la quimioterapia, con un impacto relevante en la calidad de vida de dicha población13,14.
El dolor es un síntoma complejo de innegable importancia en la práctica clínica, el cual demanda un tratamiento multidimensional15. Según la Asociación Internacional para el Estudio del Dolor (IASP, por sus siglas en inglés), el dolor neuropático (DN) es causado por una lesión o disfunción del sistema somatosensorial16. Este tipo de dolor causa hiperalgesia, alodinia y parestesia17. Por tanto, estos síntomas tan complejos afectan la dimensión física, psicológica y emocional de los pacientes, lo que les provoca depresión y ansiedad18,19,20. Actualmente, las opciones de tratamiento farmacológico incluyen medicamentos como moduladores del sistema nervioso, anticonvulsivos, antidepresivos tricíclicos y opioides, que podrían desarrollar diversos efectos secundarios. Otras alternativas de tratamiento incluyen: fisioterapia, terapia complementaria, psicoterapia, cirugía y bloqueos nerviosos2,4,21,22,23.
En este sentido, en la búsqueda de opciones terapéuticas para pacientes con dolor crónico, surge como una alternativa innovadora la terapia de estimulación magnética transcraneal repetitiva (EMTr), la cual consiste en una estimulación cerebral no invasiva, segura e indolora que induce corrientes eléctricas en el tejido nervioso de la corteza cerebral24. El efecto analgésico comienza con la estimulación de la corteza motora primaria (M1) y la producción de opioides endógenos25.
La EMTr es una técnica novedosa en el campo de la fisioterapia que constituye una opción terapéutica en rehabilitación, al promover la neuroplasticidad y la readaptación de los circuitos neuronales relacionados con las áreas de procesamiento del dolor26,27,28. Dicha técnica es recomendada por las guías de práctica clínica desarrolladas por Cruccu et al.5 y Lefaucheur et al.29. Adicionalmente, la evidencia describe su uso efectivo y seguro para diferentes condiciones patológicas, como fibromialgia, neuropatía posherpética, dolor fantasma por amputación, síndrome de dolor regional complejo, entre otros30,31,32,33. Sin embargo, existen pocos artículos relacionados con la EMTr en población oncológica34.
Adicionalmente, la evidencia sugiere que es importante analizar el efecto de la EMTr en términos de desempeño físico y mental, y del impacto sobre la calidad de vida en general, para que la efectividad del tratamiento sea evaluada no solo desde los cambios en las puntuaciones de dolor, sino también desde los resultados en la funcionalidad, las actividades de la vida diaria y la perspectiva propia del paciente35. En este sentido, Hodaj et al.36 describieron una mejora significativa en la percepción del dolor, la ansiedad-depresión y la calidad de vida; dichos resultados, evaluados desde un enfoque multidimensional, se correlacionan positivamente con la percepción de mejoría global reportada por dichos pacientes.
Finalmente, el fisioterapeuta, como parte del grupo interdisciplinario en el tratamiento del dolor neuropático, debe promover servicios de salud integrales y de alta calidad con técnicas basadas en la evidencia. Por este motivo, el objetivo de este estudio fue evaluar el efecto de la estimulación magnética transcraneal en el manejo del dolor neuropático oncológico y no oncológico.
METODOLOGÍA
La actual revisión sistemática se realizó de acuerdo con las recomendaciones publicadas por Cochrane37 y se reportó de acuerdo con los lineamientos PRISMA38. El protocolo de investigación fue registrado en PROSPERO (número de registro: CRD42021236999).
Criterios de selección
Los criterios de selección se definieron según el acrónimo PICO (es decir, población, intervención, comparación, resultados y diseño del estudio). Con base en las directrices del grupo Cochrane EPOC (Práctica y organización efectiva de la atención). Para la revisión sistemática se incluyeron los siguientes diseños de estudio: ensayos clínicos controlados aleatorizados (ECAS), ensayos clínicos controlados no aleatorizados y series de tiempo interrumpido39.
Tipo de participantes
Hombres y mujeres entre 18 y 85 años con dolor neuropático oncológico y no oncológico.
Tipo de intervención
Tratados con estimulación magnética transcraneal.
Ajustes: no limitamos el entorno ni el formato de ejecución de las intervenciones.
Tiempo: estudios que evaluaron al menos una sesión, en la que se midió el resultado de interés a través de instrumentos validados.
Comparación
Grupos de control inactivos (ej., sin intervención), así como intervenciones activas paralelas, como la estimulación nerviosa eléctrica transcutánea (TENS) y la estimulación directa transcraneal (tDCS, por sus siglas en inglés).
Medidas de resultado
Resultados primarios
Modulación del dolor medido en escalas validadas, como la escala visual análoga (EVA), la escala de descriptor verbal (EDV), la escala de calificación numérica (NRS, por sus siglas en inglés), la escala del síndrome de dolor pélvico neuropático funcional (FPPS, por sus siglas en inglés), el inventario de síntomas de dolor neuropático (NPSI, por sus siglas en inglés), el cuestionario McGill de dolor (MPQ, por sus siglas en inglés), el inventario de sensibilización central (CSI, por sus siglas en inglés), el inventario breve de dolor (BPI, por sus siglas en inglés), evaluación de Leeds autocompletada de síntomas y signos neuropáticos (S-LANCSS, por sus siglas en inglés) u otras escalas cuantitativas.
Resultados secundarios
1. Calidad de vida medida con escalas validadas, como la encuesta de salud de formato corto de 36 ítems (SF-36), la calidad de vida europea en 5 dimensiones de 5 niveles (EQ-5D-5L, por sus siglas en inglés), el impacto del dolor neuropático en la calidad de vida (NePIQoL, por sus siglas en inglés) u otras escalas cuantitativas.
2. Efectos adversos de recibir la intervención o relacionados con resultados falsos positivos de cualquier síntoma.
Criterios de exclusión
Se excluyeron todos los ensayos clínicos en los cuales la evaluación del dolor no se limitaba al dolor de tipo neuropático o no respondía a la pregunta PICO.
Métodos de búsqueda
La búsqueda se realizó entre los años 2011 – 2024, estas fechas se seleccionaron debido al creciente número de artículos que estudian el efecto de la intervención magnética transcraneal para el dolor neuropático40. No se aplicaron restricciones de idioma. Los términos de búsqueda se detallan en el Apéndice en el pdf del artículo. Se consultaron las siguientes fuentes de búsqueda en bases de datos electrónicas: Registro Cochrane Central de Ensayos Controlados (CENTRAL), MEDLINE, EMBASE, PsycINFO, SCOPUS y LILACS. Para registros de ensayos clínicos se examinó el portal de búsqueda de la plataforma internacional de Registros de ensayos clínicos de la OMS (ICTRP, por sus siglas en inglés) (http://apps.who.int/trialsearch/), el archivo de ensayos clínicos del Instituto Nacional de Salud (http://clinicaltrials.gov) y el Registro Internacional de Ensayos Controlados (http://www.owned-trials.com). Para identificar estudios adicionales, se realizó una búsqueda manual de las referencias bibliográficas de todos los estudios incluidos. Además, se realizó una búsqueda de literatura gris en OpenSIGLE (www.opengrey.eu). Cuando se requirió información adicional, se estableció contacto con los autores correspondientes (ver, Apéndice en el pdf del artículo).
Recolección y análisis de datos
Selección de estudios
Las referencias identificadas en las búsquedas bibliográficas se exportaron a Mendeley (https://www.mendeley.com) y al software para revisiones sistemáticas Rayyan (https://rayyan.qcri.org), para realizar, después, la eliminación de duplicados y evaluación de los títulos y resúmenes por los cuatro evaluadores independientes CLM, ICAB, SPBB y MGVM. El siguiente paso fue recuperar el texto completo de los estudios que cumplieron los criterios de inclusión. Las discrepancias entre revisores se resolvieron mediante discusión o con la participación de otro evaluador (SGT o DVM).
Los estudios que fueron excluidos durante el proceso de valoración del texto completo se agruparon en una lista que se denominó "Características de los estudios excluidos" y se reportaron los motivos de la exclusión en la Figura 1.

Figura 1.
Diagrama PRISMA
Extracción de datos
Para dicha función se tomó como referencia el formato de extracción de datos sugerido por Cochrane37 para recopilar información pertinente de cada estudio, incluidas las características de los participantes, las características de las intervenciones, las comparaciones, los diseños de los estudios y los resultados. Un evaluador (ICAB) extrajo los datos de los estudios incluidos y un segundo evaluador (CLM) verificó la pertinencia y precisión de la información. Cualquier desacuerdo se resolvió por consenso, consultando a un tercer investigador (SPBB).
Evaluación del riesgo de sesgo
Dos revisores independientes (SPPB y CLM), que estaban cegados a los conceptos del otro, evaluaron el riesgo de sesgo en los estudios incluidos. El riesgo de sesgo de los ECAS se evaluó sistemáticamente mediante la herramienta Cochrane de riesgo de sesgo41. Los ensayos no aleatorizados y no controlados se evaluaron con los instrumentos de evaluación de calidad para estudios antes y después sin grupo de control, del Instituto Nacional del Corazón, los Pulmones y la Sangre (NHLBI, por sus siglas en inglés)42 y la lista de verificación para estudios cuasiexperimentales (estudios experimentales no aleatorizados del Instituto Johana Brinks). Cualquier desacuerdo se resolvió mediante reuniones de consenso o consultando a un tercer revisor cuando fue necesario.
Síntesis de datos
Debido a la heterogeneidad de los estudios incluidos, decidimos proporcionar una síntesis narrativa de los hallazgos principales. No se realizó ningún metanálisis.
Calidad de la evidenciaCalidad de la evidencia
Dos revisores independientes (SPBB, CLM) utilizaron el enfoque GRADE (Grading of Recommendations, Assessment, Development, and Assessment) para evaluar la calidad de la evidencia43. El cual incluye los siguientes factores: limitaciones en el diseño y la implementación del estudio (riesgo de sesgo), inconsistencia de los resultados, evidencia indirecta, imprecisión y sesgo de publicación44. El resumen de los hallazgos se generó en el software GRADEpro45.
RESULTADOS
Hallazgos principales
La búsqueda arrojó un total de 1116 artículos (ver Figura 1), 667 de Medline, 5 de Lilacs, 270 de Cochrane, 138 de Embase, 34 de PsycINFO y 2 de literatura gris. Luego de eliminar los duplicados se leyeron 95 resúmenes para identificar el cumplimiento de los criterios de selección. Se excluyeron 65 por evaluar diferentes resultados y 9 por tipo de estudio. Un total de 21 artículos cumplieron con los criterios de búsqueda. Esos artículos se resumen en la Tabla 1.
Intervenciones y resultados de los estudios incluidos.
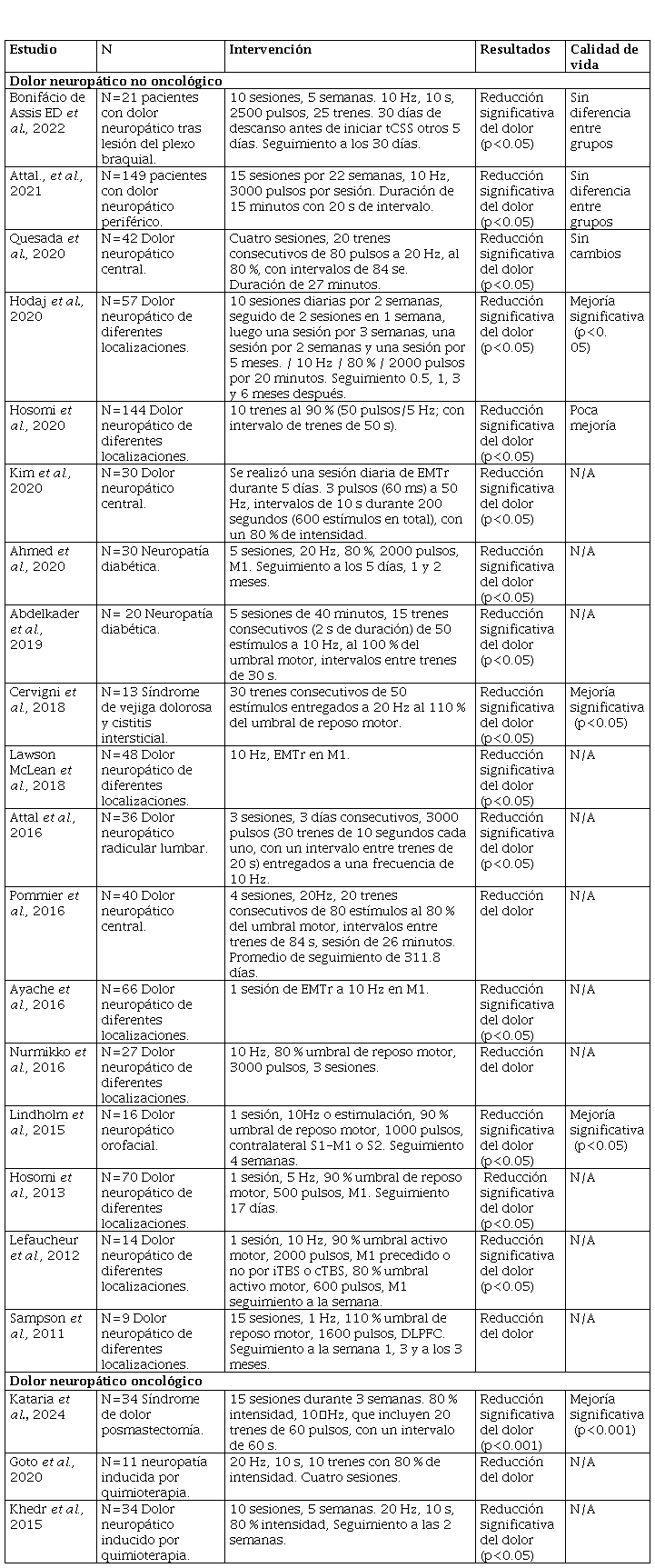
Nota EMTr: estimulación magnética transcraneal repetitiva. cTBS: estimulación continua Theta burst. iTBs: estimulación intermitente theta burst. DLPFC: corteza prefrontal dorsolateral. P<0.05 Significancia estadística.
Características de los participantes
Se incluyeron 21 artículos: 12 ECAS y 9 estudios observacionales. La muestra total de los estudios fue de 911 pacientes, siendo 428 (46.98 %) mujeres y 483 (53.01 %) hombres. La edad promedio fue de 52 años.
Intervención
Todos los estudios utilizaron EMTr en su tratamiento, el número de sesiones varió desde una única sesión hasta las 15 sesiones, con un promedio de 3,5 sesiones. El seguimiento fue variable, oscilando entre 7 y 311.8 días, con un promedio de 45 días. Se obtuvieron reducciones del dolor en los 21 estudios.
Estudios excluidos
Los principales motivos de exclusión fueron las diferentes intervenciones, la naturaleza del dolor y el tipo de estudio (ver Apéndice en el pdf del artículo).
Resultados primarios
Modulación del dolor
De los 21 artículos incluidos, 12 fueron ECAS34,46,47,48,49,50,51,52,53,54,55,56, con una población total de 623 pacientes.
Para el caso del dolor neuropático no oncológico se incluyeron 10 artículos. Bonifacio de asís et al.55 incluyeron 21 pacientes con dolor neuropático después de una lesión del plexo braquial. Los pacientes recibieron un total de 10 sesiones de EMT (5 días consecutivos con 30 días de descanso, antes de iniciar la estimulación transcraneal de corriente directa (tDCS, por sus siglas en inglés) durante otros 5 días. La escala visual análoga (EVA) se evaluó al inicio del estudio, en la quinta sesión y en el seguimiento a los 30 días. La estimulación con EMT y tDCS disminuyó significativamente las puntuaciones de intensidad del dolor en comparación con el grupo control (p = 0.016 y p = 0.047, respectivamente).
El artículo de Attal et al.54 incluyó 149 pacientes con dolor neuropático periférico. El estudio implementó 15 sesiones durante 22 semanas. Los autores incluyeron BPI (Inventario breve del dolor) y EVA para evaluar el dolor. Según sus resultados, EMTr-M1 redujo la intensidad del dolor versus el grupo simulado (95 %), esto también se evidenció en el alivio del dolor, la dimensión sensorial del dolor y la fatiga. Por otro lado, la estimulación de la corteza prefrontal dorsolateral no mostró mejoría en comparación con el grupo control.
El estudio de Quesada et al.46 incluyó a 42 adultos con dolor central, divididos en fase activa y control. Cada fase incluyó 4 sesiones y un reposo de 8 semanas entre fases. El dolor se evaluó con el porcentaje de alivio del dolor (%R) y EVA después de cada sesión de EMTr y al final de la fase. Los resultados describieron una diferencia de %R significativamente mayor (p<0.001) en la evaluación posterior a la EMTr activa: 33.81 %R (IC 95 %: [23.99-43.74]) que en la evaluación posterior a la EMTr simulada: 13.02 %R (IC 95 %: [6.64-19.76.]). Para la EVA, los autores describieron una disminución significativa en la fase activa entre el inicio y el final del tratamiento (p = 0.002, diferencia de medias del IC del 95 % [0.07-1.19]).
El estudio de Hosomi et al.51 incluyó a 144 pacientes con dolor de diferentes localizaciones. 70 pacientes para tratamiento activo y 67 pacientes para EMTr simulada. Los pacientes recibieron 5 sesiones diarias de EMTr activa o simulada. Además, los pacientes cuya EVA disminuyó un promedio de 10 mm o más, fueron sometidos a sesiones adicionales de al menos una vez a la semana durante 4 semanas. La EVA se registró antes y después de cada intervención, la disminución en la EVA media fue de 8.0 (DE:12.1) en el grupo de estimulación activa y de 9.2 (DE 13.6) en el grupo simulado, y no hubo diferencias significativas entre los grupos. Finalmente, las sesiones adicionales suministradas a los pacientes que mostraron reducción del EVA reportaron efectos significativos en la disminución del dolor en el grupo activo versus el grupo simulado (p=0.001).
Kim et al.53 incluyeron 30 pacientes que presentaron dolor neuropático central, 15 pacientes en el grupo de EMT real y 15 en el grupo simulado. Se realizó una sesión diaria de EMTr durante 5 días. Los pacientes fueron evaluados con la escala de calificación numérica (NRS), el inventario de síntomas de dolor neuropático (NPSI), evaluación de Leeds autocompletada de síntomas y signos neuropáticos (S-LANCSS). Se reportó una reducción significativa en todos los parámetros evaluados (p<0.005).
Dos artículos incluyeron adultos con neuropatía diabética47,48. Los resultados fueron evaluados con EVA en ambos estudios. Ahmed et al.48 encontraron disminuciones significativas (P<0,05) en la intensidad del dolor después de la EMT en comparación con la intervención del TENS. Abdelkader et al.47 informaron una reducción media significativa de la EVA para pacientes insulinodependientes (5.10 ± 2.6 mm; p = 0.011) y pacientes no insulinodependientes (4.0 ± 1.7 mm; p = 0.005).
En el artículo de Cervigni et al.50 se eligieron 13 pacientes con dolor neuropático causado por síndrome de vejiga dolorosa/cistitis intersticial. El primer grupo de pacientes recibió tratamiento real con EMT durante cinco días consecutivos, seguido de un período de descanso de 6 semanas, para el tratamiento simulado de EMT; el segundo grupo recibió los mismos tratamientos en orden inverso. Las escalas utilizadas para evaluar el dolor fueron EVA, el síndrome de dolor pélvico neuropático funcional (FPPS), el inventario de síntomas de dolor neuropático (NPSI), el cuestionario de McGill y el inventario de sensibilización central (CSI). En la fase de estimulación real, los pacientes obtuvieron una reducción global significativa de la EVA después del tratamiento (p = 0.001).
El artículo de Attal et al.49 incluyó una población de 36 pacientes, 24 para estimulación activa y 12 para el grupo control. El protocolo de tratamiento incluyó dos bloques separados por un intervalo de tres semanas. Cada bloque constaba de tres sesiones de EMT o tDCS (estimulación directa transcraneal) durante tres días consecutivos (V1, V2, V3). Los efectos del tratamiento se evaluaron con una escala de calificación numérica (ECN) inmediatamente antes de la estimulación en V1, en V2 y V3 y cinco días después de la última sesión. El estudio concluyó que la EMT activa fue superior a la tDCS en cuanto a la modulación del dolor (F= 14.88; p <0.001). La proporción de pacientes que respondieron con una disminución en la intensidad media del dolor de al menos el 50 % fue significativamente mayor en el grupo de EMT (30,4 %) que en el grupo de tDCS (8.6 %, p=0.040) y grupo control (8.6 %; p=0.031).
El artículo de Hosomi et al.52, incluyó a 70 pacientes con dolor neuropático de diferentes localizaciones, 34 en el grupo A y 36 en el grupo B. En cuanto al tratamiento, se aplicó una sesión de EMT diaria durante 10 días consecutivos. La intensidad del dolor se evaluó mediante EVA. En los resultados, las tasas medias de reducción de la EVA (IC del 95 %) en la EMTr real y simulada fueron del 6.51 % (3.68–9.34) frente al 2.44 % (0.98–5.62) respectivamente, lo que corresponde a un efecto significativo de la intervención (p<0.001).
En relación con los resultados obtenidos en el dolor neuropático oncológico se encuentran 2 ECAS. Kataria, et al.56 incluyeron 17 pacientes con dolor neuropático posmastectomía que recibieron 15 sesiones de EMT y 17 pacientes que pertenecieron al grupo control. Las puntuaciones de dolor se obtuvieron antes de la primera sesión de estimulación (preintervención) y después de la última sesión de estimulación (posintervención) a través de la escala análoga visual. Los autores reportaron reducción de dolor con significancia estadística (p<0.0001) en el grupo de intervención.
Y el artículo de Khedr et al.34 incluyó a 34 pacientes con diagnóstico de neuropatía inducida por quimioterapia, el tratamiento con EMT se realizó con 10 sesiones diarias. La evaluación del dolor se realizó antes y después de la primera, quinta y décima sesión y luego 15 días y 1 mes después. Los cambios en la escala descriptiva verbal (EDV) y la escala visual análoga (EVA) fueron significativos en el grupo de intervención, particularmente al final del tratamiento (p<0.001). Los autores informaron una reducción del dolor del 49.1 % con EDV y del 36.7 % con EVA al final del tratamiento y del 45.6 % con EDV y el 35.5 % con EVA a los 15 días de seguimiento.
De los 21 estudios, 9 artículos eran estudios cuasiexperimentales36,57,58,59,60,61,62,63,64, con una población total de 288 pacientes.
Para este caso 8 de los artículos incluidos estudiaron el dolor neuropático en población no oncológica. El estudio de Hodaj et al.36 incluyó a 57 pacientes con dolor de diferentes localizaciones. El tratamiento consistió en una sesión por día durante 5 días en el transcurso de 2 semanas (semanas 1 y 2), después 2 sesiones en la semana siguiente (semana 3), para un total de 12 sesiones. Se realizó una terapia de mantenimiento, que consistió en una sesión de EMTr en la semana 4 y luego sesiones bimensuales durante los siguientes 5 meses, para un total de 11 sesiones. Todas las medidas de dolor disminuyeron significativamente con el tiempo después del tratamiento (p<0.0001).
McLean et al.61 incluyeron 48 pacientes con dolor facial atípico y el tratamiento con EMTr se realizó diariamente durante un total de 9 sesiones. La intensidad del dolor se documentó según la escala visual análoga. Después de seis semanas, 28 de los 46 pacientes informaron un nivel significativo de alivio del dolor (p<0.001).
Pommier et al.59 incluyeron 40 adultos con dolor neuropático de origen central a los que se les realizaron 4 sesiones separadas entre sí por un intervalo de 3-4 semanas. La evaluación se realizó después de 4 sesiones. En los 31 pacientes que respondieron al tratamiento, el promedio de sesiones por paciente fue de 11, el seguimiento promedio fue de 311,8 días, el intervalo promedio entre sesiones fue de 28.4 días. El porcentaje promedio de alivio del dolor (% R global) en el grupo de los pacientes que respondieron fue del 41 % (rango 10-100 %). La puntuación EVA media antes de la EMT fue de 6.35 frente a 6.16 después de cuatro sesiones.
Ayache et al.54 incluyeron 66 pacientes con dolor neuropático de diferentes causas y localizaciones, a quienes se evaluó el efecto analgésico en una sola sesión. Este estudio comparó la analgesia inducida por la estimulación de la ubicación del dolor dentro del punto motor de la mano (hMHS, por sus siglas en inglés) versus la corteza motora primaria (M1). El efecto analgésico se evaluó con EVA, y se encontró que el porcentaje de reducción del dolor durante 1 semana, y para los días 2 y 3, mostró una diferencia significativa durante el procedimiento dirigido a hMHS y el M1 en comparación con el procedimiento simulado (p<0.05 y p<0.001, respectivamente).
El estudio de Nurmikko et al.63 incluyó a 27 pacientes con dolor en diferentes localizaciones. Divididos en 3 grupos: tratamiento farmacológico, EMT y grupo control. El tratamiento se diseñó aplicando 3 ciclos de 5 sesiones de EMT, 3-5 veces por semana. Los pacientes calificaron su dolor promedio cada 24 horas con el NRS, y antes y después de 5 sesiones con el inventario breve de dolor (BPI). Los resultados mostraron que la EMT proporcionó alivio del dolor y aumentó la tasa total de pacientes que respondieron al tratamiento en un 58 %.
El estudio de Lindholm et al.58, por su parte, incluyó a 16 adultos con dolor orofacial. Todos los participantes recibieron 2 tratamientos activos de EMTr y 1 tratamiento simulado. Los 3 tratamientos estuvieron separados entre sí por 4 semanas. La NRS se evaluó al inicio y después de cada sesión de EMT. El inventario breve de dolor (BPI) se evaluó al inicio del estudio, 3 a 5 días después del tratamiento y 1 mes después. La intensidad del dolor (NRS) fue más baja el tercer día después de la estimulación S2 (corteza somatosensorial secundaria) con un puntaje promedio de 3.8, en comparación con la estimulación S1/M1 con una NRS media de 5.4 (p= 0.0071) y el grupo control con un puntaje de 5.3 (p=0.0187). Estos resultados permanecen después de 1 mes. Las puntuaciones de intensidad del dolor del BPI de 3 a 5 días después de la sesión de estimulación en S2 fueron significativamente más bajas con una media de 4.5 en comparación con las puntuaciones antes de las sesiones (5.4; p=0.0127) y las puntuaciones después de la sesión con estimulación en S1/M1 (6.2; p=0.001) y las sesiones del grupo control (5.1; p=0.0491).
En el estudio de Lefaucheur et al.62 se incluyeron 14 pacientes con diferentes localizaciones del dolor. Los pacientes se sometieron a 3 sesiones de EMT separadas por cuatro semanas. El dolor se evaluó con EVA durante 1 semana, antes de la primera sesión de EMTr y después de cada sesión. La puntuación media de reducción del dolor fue del 41 % cuando se combinó con iTBS (estimulación theta-burst intermitente) y del 31 % en comparación con cTBS (estimulación theta-burst continua). Las pruebas posteriores al tratamiento mostraron una reducción de todas las puntuaciones de dolor después de cualquier tipo de EMT en comparación con el valor inicial previo a la estimulación (p<0.05).
Sampson et al.64 realizaron 15 sesiones de EMT en 9 pacientes con dolor de diferentes localizaciones (5 días a la semana, durante 3 semanas). La EVA se evaluó antes y después de todos los tratamientos con EMT y mensualmente durante 3 meses. En los resultados, tres sujetos tuvieron una disminución del 50 % en las puntuaciones de dolor al finalizar los tratamientos y 1 sujeto respondió más lentamente con una mejora del 50 % en el dolor, al final del seguimiento de 3 meses.
Solo un artículo cuasiexperimental evaluó población con cáncer. Goto et al.57 incluyeron 11 adultos con diagnóstico oncológico y neuropatía inducida por quimioterapia, a quienes se les realizaron 4 sesiones de EMT. El dolor se evaluó al inicio, antes y después de la intervención. Las puntuaciones de EVA disminuyeron en un 90 % (media 55.3; [DE] [43.0]) en la preestimulación y una media de 46.8; DE [38.6] en la posestimulación.
Resultados secundarios
Calidad de vida
En la búsqueda se encontraron 8 artículos que evaluaron la calidad de vida en sus resultados. Lo cual incluye 476 pacientes36,46,50,51,54,55,56,58.
Bonifacio et al.55 no informaron diferencias entre los grupos EMT, tDCS y simulado con respecto a las puntuaciones logradas en calidad de vida (SF-36) durante el curso del tratamiento (p > 0.05).
Attal et al.54 aplicaron el instrumento europeo de calidad de vida 5 dimensiones de 5 niveles (EQ-5D-5L, por sus siglas en inglés) para medir la calidad de vida, los resultados no difirieron entre M1-EMT, EMT en la corteza dorsolateral prefrontal (DLPFC, por sus siglas en inglés) y el grupo control, ya que todos los grupos mejoraron de manera similar después de repetidas sesiones de EMT.
En el estudio de Hosomi et al.51 se registró la calidad de vida mediante la escala EQ-5D-5L después de cada intervención, el primer y quinto día y la cuarta semana. Ninguno de los resultados fue significativamente diferente entre el grupo activo y de control.
Hodaj et al.36 utilizaron el Sf-36 para evaluar la calidad de vida. Describieron una mejora significativa en las puntuaciones de los componentes físico y mental (p<0.001).
En el estudio de Quesada et al.46 se evaluó la calidad de vida con el EQ-5D-5L, que se aplicó al inicio y al final de cada fase. En los resultados, la calidad de vida se mantuvo sin cambios, tanto en la fase activa como en la simulada.
En el artículo de Cervigni et al.50 describieron un efecto positivo significativo en la subpuntuación de la SF-36 relacionada con el dolor físico (p= 0.034) y la subpuntuación relacionada con el estado emocional (p = 0.016) para el grupo intervención.
Lindholm et al.58 incluyeron a 16 adultos con dolor orofacial, la calidad de vida se evaluó mediante la escala de impacto del dolor neuropático en la calidad de vida (NePIQoL, por sus siglas en inglés) y la SF-36 al inicio del tratamiento y 1 mes después, encontrando una reducción en puntuación total de NePIQol 1 mes después de la estimulación S2 con un valor de 79.8, en comparación con el valor inicial de 86.6 (p = 0.0031).
Solo un artículo evaluó la calidad de vida el dolor neuropático oncológico. Kataria et al.56 reportaron una eficacia superior de la terapia EMTr (sobre la terapia simulada) para mejorar calidad de vida, la cual fue evaluada mediante la escala FACT B, mejorando los componentes físico (p=0.037), emocional (p=0.033) y funcional (p=0.020).
Efectos adversos
De los 21 artículos incluidos en esta revisión sistemática, tres (15 %)34,48,61 no mencionan ninguna información respecto a los efectos adversos de EMT, tres de ellos (15 %)49,55,64 mencionan que estos efectos fueron observados y medidos, sin describir sus conclusiones. Cuatro artículos (20 %)50,52,54,63 mencionaron efectos adversos clasificados como leves, incluyendo dolor de cabeza, dolor en las extremidades, mareos y somnolencia. Finalmente, 11 artículos (52 %)36,46,47,51,53,56,57,58,59,60,62 describieron no tener efectos adversos graves en sus protocolos.
Riesgo de sesgo
12 de los 21 estudios34,46,47,48,49,50,51,52,53,54,55,56 fueron evaluados con la herramienta Cochrane de riesgo de sesgo para ensayos aleatorizados. En resumen, los estudios mostraron un riesgo bajo de sesgo de selección, pero un riesgo alto de sesgo de realización y detección, debido a la falta de cegamiento de los participantes, el personal y los evaluadores de resultados (Figura 2).
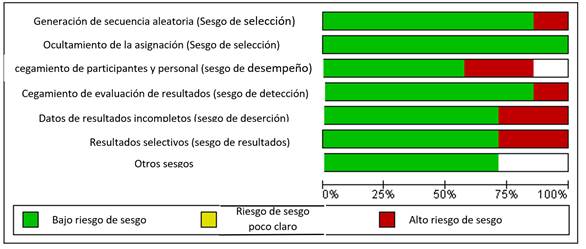
Figura 2
Gráfico Cochrane de riesgo de sesgo.
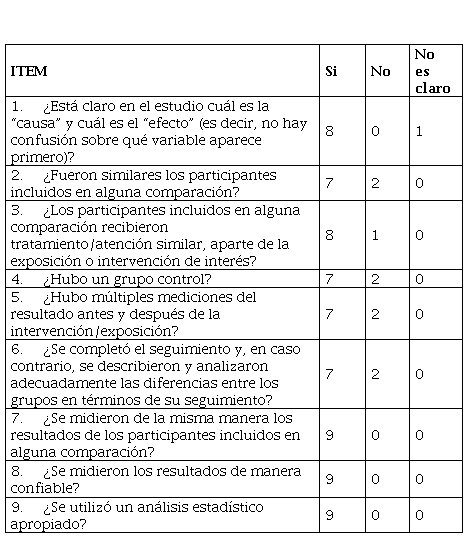
Los estudios con otras metodologías36,57,58,59,60,61,62,63,64 fueron evaluados con la lista de verificación de evaluación crítica del JBI, para estudios cuasiexperimentales de la Facultad de Ciencias Médicas y de la Salud de la Universidad de Adelaida, Australia del Sur. 7 de los 9 artículos cumplieron más del 50 % de los ítems de la lista de verificación (Tabla 2).
Lista de verificación de evaluación crítica para estudios cuasiexperimentales del JBI.
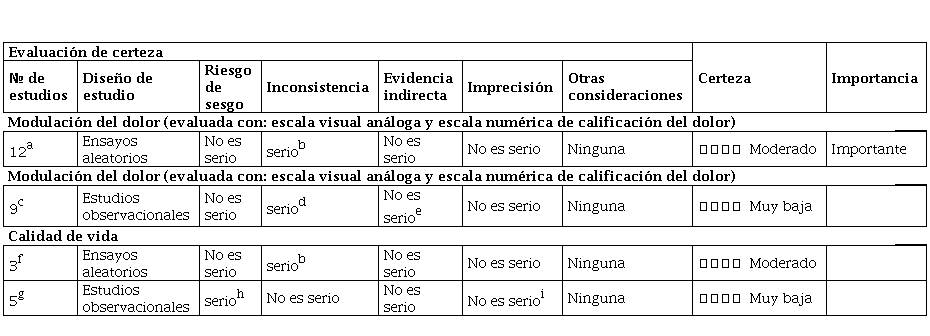
Calidad de la evidencia
Se encontró evidencia de calidad moderada sobre los efectos de las intervenciones en la modulación del dolor. Es importante resaltar que para la certeza en la calidad de la evidencia en relación a la modulación del dolor a través de la EMT se tuvieron en cuenta ambas poblaciones (oncológica y no oncológica), no obstante, solo se contó con 2 ECAS34,56 que incluyeron pacientes con cáncer, dichos artículos no contribuyen al cambio en la certeza incluidas ambas poblaciones, pero si constituyen una muestra pequeña para esta población específica.
Por otra parte, se encontró evidencia de muy baja calidad sobre el efecto en los cambios en la calidad de vida, para esto solo se contó con un artículo que incluyó población oncológica56 (Tabla 3).
Calidad de la evidencia
Explicaciones a. (Bonifácio de asis et al., 2022), (Attal et al., 2021), (Quesada et al., 2020), (Hosomi et al., 2020), (Kim et al., 2020), (Ahmed et al., 2020), (Abdelkader et al., 2019), (Cervigni et al., 2018), (Attal et al., 2016), (Hosomi et al., 2013), (Kataria et al 2024), (Khedr et al., 2015).
b. Es evidente una amplia variación en las estimaciones puntuales entre algunos estudios y una superposición mínima de los intervalos de confianza.
c. (Hodaj et al., 2020), (Lawson et al., 2018), (Pommier et al., 2016), (Ayache et al., 2016), (Nurmiko et al., 2016), (Lindholm et al., 2015), (Lefaucheur et al., 2012), (Sampson et al., 2011), (Goto et al., 2020).
d. Existe heterogeneidad entre los estudios con una amplia variación de estimaciones puntuales entre ellos.
e. Los estudios responden plenamente a la PICO.
f. (Bonifácio de asis et al., 2022), (Attal et al., 2021, (Kataria et al 2024)
g. (Quesada., et al 2020), (Hosomi., et al2020), (Hodaj., et al 2020), (Cervigni., et al 2018), (Lindholm., et al 2015)
h. El riesgo de sesgo fue evaluado mediante la herramienta de evaluación de calidad para estudios antes-después (Pre-Post) sin grupo de control del Instituto Nacional del Corazón, los Pulmones y la Sangre.
i. Tamaño de muestra pequeño y número limitado de estudios.
DISCUSIÓN
El uso de EMTr para tratar el dolor neuropático ha aumentado significativamente en los últimos años, seguido de un rápido crecimiento en estudios relacionados40,65,66,67. La presente revisión sistemática identificó 12 ensayos aleatorios y 9 estudios observacionales, de los cuales sólo 3 artículos son específicos para la población oncológica34,56,57.
El dolor es un síntoma complejo de gran importancia e impacto en el bienestar de las personas con diferentes patologías y está asociado a una alta carga económica, por ello requiere de una atención integral y prioritaria68,69. Las encuestas epidemiológicas han demostrado que muchos pacientes con dolor neuropático no reciben el tratamiento adecuado70. Esto puede deberse a una falta de precisión diagnóstica, una comprensión insuficiente de los mecanismos fisiopatológicos del dolor y opciones de tratamiento farmacológico y no farmacológico relativamente ineficaces71,72. Por tanto, aún son necesarios mejores enfoques y diversificación de opciones terapéuticas, que permitan una modulación eficaz del dolor y un impacto positivo en la calidad de vida de esta población73.
En este sentido, la EMT es un procedimiento no invasivo que ha sido ampliamente reconocido como un tratamiento eficaz para el dolor neuropático intratable de diferentes orígenes30,74. Con respecto a los efectos analgésicos de la EMTr, los 21 estudios incluidos en la revisión sistemática describieron una mejora en las tasas de dolor; sin embargo, el promedio de alivio del dolor fue muy variable entre los estudios, probablemente debido a al número diferente de sesiones, frecuencia y origen del dolor, y seguimiento de las intervenciones. Pommier et al.59 informaron que, después de tres sesiones, los pacientes tenían un 43 % de posibilidades de experimentar al menos un 40 % de alivio del dolor con una duración media de 17,8 días. Por otra parte, Khedr et al.34 describieron que no hubo efectos significativos en la escala visual análoga después de la primera sesión, pero sí aparecieron después de la quinta sesión.
Actualmente, no existe suficiente evidencia clínica para determinar el efecto a largo plazo de la terapia con EMT. De los estudios incluidos, sólo un artículo realizó seguimiento prolongado con una media de 381.6 días59. Estos autores sugirieron que los pacientes que tuvieron al menos un 40 % de alivio del dolor después de tres sesiones tienen un 89 % de posibilidades de experimentar alivio del dolor al año de seguimiento. Algunos de los artículos seleccionados para la revisión sistemática incluyeron de 2 a 4 semanas de seguimiento34,47,51,52,55,58. Sin embargo, Hodaj et al.36 informaron períodos más prolongados de alivio del dolor y descubrieron que el efecto analgésico todavía estaba presente en un seguimiento de 5 meses.
Respecto al seguimiento en la población oncológica Kehdr et al.34 describieron que el efecto de la EMT se mantuvo 2 semanas después del final de las sesiones de tratamiento, pero ya no estaba presente al mes de seguimiento. Otro artículo describió que con respecto a la extremidad objetivo, las puntuaciones de disestesia y dolor disminuyeron significativamente a los 2 meses57. Por su parte los autores Kataria et al.56 describen un impacto positivo de la terapia EMTr sobre el dolor, la calidad de vida y la sensibilidad térmica en pacientes con mastectomía, lo que abre nuevas vías para las estrategias de manejo del dolor de dicha población, aunque aún se requieren estudios que incluyan mayor población para permitir su estandarización. Es importante aclarar que los 3 estudios encontrados con población oncológica tan solo incluyeron una muestra de 79 participantes.
Algunos artículos de la revisión sistemática evaluaron la variable de la depresión, la cual ha mostrado relación con el dolor neuropático de origen oncológico y no oncológico34,36,49,50,51,52,54,58,63. Esta variable puede ser un elemento importante a evaluar en futuras investigaciones, para favorecer una evaluación integral del dolor neuropático incluyendo todas las dimensiones del paciente y promoviendo una participación activa en su tratamiento desde las medidas de resultados informadas por el paciente (PROMS, por sus siglas en inglés)75. En este sentido algunas investigaciones describen la importancia de evaluar en esta población otros factores como el funcionamiento físico y emocional, actividades de la vida diaria, calidad del sueño y la calidad de vida en general los cuales representan resultados de tratamiento relevantes a tener en cuenta76. Autores como Kataria et al.56, Cervigni et al.50 y Lindholm et al.58 reportaron mejorías significativas en el estado físico y emocional, la funcionalidad y la interferencia del dolor en las actividades de la vida diaria. De lo anterior se resaltan elementos multidimensionales que influyen en el bienestar del paciente, que van más allá de la calificación numérica del dolor.
Además de lo anterior y acorde con los resultados secundarios reportados por la actual revisión sistemática en relación con los efectos secundarios generados por la EMTr en la población oncológica y no oncológica, algunos autores reportan efectos adversos como dolor de cabeza, fatiga, trastornos del sueño y náuseas, sin reportarse ninguna complicación seria77. Lo anterior sugiere que esta técnica es una estrategia segura para el tratamiento de este tipo de dolor.
Finalmente, hay evidencia disponible sobre la efectividad de la estimulación magnética transcraneal para el dolor neuropático de origen oncológico y no oncológico; sin embargo, existen varias debilidades metodológicas debido a la inconsistencia y la heterogeneidad del diseño de los estudios, la población incluida y las medidas de resultado. Aunque el tamaño muestral de los estudios primarios es pequeño, tienen el tamaño de información óptimo (OIS, por sus siglas en inglés), lo que favorece la precisión en los resultados. Por tanto, es necesario desarrollar estudios más rigurosos que puedan informar, estandarizar y mejorar la práctica clínica con respecto a la modulación del dolor neuropático con EMTr en diferentes poblaciones.
En conclusión, de acuerdo a los resultados de los 21 estudios experimentales, incluidos 12 ensayos controlados aleatorizados y 9 artículos observacionales, la revisión sistemática actual sugiere que la estimulación magnética transcraneal puede ser una opción terapéutica eficaz y segura para tratar el dolor neuropático oncológico y no oncológico. Se encontró evidencia de calidad moderada para la modulación del dolor; mientras que para la calidad de vida los resultados son inciertos en determinar cambios, debido a que la evidencia es muy baja. Por ello, sugerimos incluir la estimulación magnética transcraneal en los protocolos de tratamiento del dolor neuropático oncológico y no oncológico. En cuanto a la calidad de la evidencia, abogamos por desarrollar estudios más amplios en los que se mida el impacto de la modulación del dolor en la calidad de vida. Además, se justifican ECAS bien estructurados que incluyan metodologías más estandarizadas e intervenciones mejor informadas, con especial énfasis en la población con cáncer.
REFERENCIAS
1. World Health Organization. WHO Normative Guidelines on Pain Management. 2007.
2. Colloca L, Ludman T, Bouhassira D, Baron R, Dickenson AH, Yarnitsky D, et al. Neuropathic pain. Nat Rev Dis Primer. 2017;3(1):1–19.
3. Correa-Illanes G. Dolor neuropático, clasificación y estrategias de manejo para médicos generales. Rev Médica Clínica Las Condes. 2014;25:189–99.
4. Liampas A, Rekatsina M, Vadalouca A, Paladini A, Varrassi G, Zis P. Non-pharmacological management of painful peripheral neuropathies: A Systematic Review. Adv Ther. 2020;37(10):4096–106.
5. Cruccu G, Truini A. A review of neuropathic pain: From guidelines to clinical practice. Pain Ther. 2017;6(Suppl 1):35–42.
6. Liampas A, Velidakis N, Georgiou T, Vadalouca A, Varrassi G, Hadjigeorgiou GM, et al. Prevalence and management challenges in central post-stroke neuropathic pain: A systematic review and meta-analysis. Adv Ther. 2020;37(7):3278–91.
7. Burke D, Fullen BM, Stokes D, Lennon O. Neuropathic pain prevalence following spinal cord injury: A systematic review and meta-analysis. Eur J Pain Lond Engl. 2017;21(1):29–44.
8. Pfannkuche A, Alhajjar A, Ming A, Walter I, Piehler C, Mertens PR. Prevalence and risk factors of diabetic peripheral neuropathy in a diabetics cohort: Register initiative “diabetes and nerves.” Endocr Metab Sci. 2020;1(1):100053.
9. Rincón-Carvajal AM, Olaya- Osorio CA, Martínez-Rojas S, Bernal L. Recomendaciones basadas en la evidencia para el manejo del dolor neuropático (revisión de la literatura). Rev Soc Esp Dolor. 2018;25(6).
10. Perruchoud C, Dupoiron D, Papi B, Calabrese A, Brogan SE. Management of cancer-related pain with intrathecal drug delivery: A systematic review and meta-analysis of clinical studies. Neuromodulation J Int Neuromodulation Soc. 2022;S1094-7159(21)06969-5.
11. Zis P, Paladini A, Piroli A, McHugh PC, Varrassi G, Hadjivassiliou M. Pain as a first manifestation of paraneoplastic neuropathies: A systematic review and meta-analysis. Pain Ther. 2017;6(2):143–51.
12. Bao H, Wu Z, Wang Q, Wang J, Zhang L, Meng L, et al. The efficacy of gabapentin combined with opioids for neuropathic cancer pain: a meta-analysis. Transl Cancer Res. 2021;10(2):637–44.
13. Desforges AD, Hebert CM, Spence AL, Reid B, Dhaibar HA, Cruz-Topete D, et al. Treatment and diagnosis of chemotherapy-induced peripheral neuropathy: An update. Biomed Pharmacother Biomedecine Pharmacother. 2022;147:112671.
14. Yoon SY, Oh J. Neuropathic cancer pain: Prevalence, pathophysiology, and management. Korean J Intern Med. 2018;33(6):1058–69.
15. Khosravi P, Castillo A, Pérez G. Manejo del dolor oncológico. An Med Interna. 2007;24(11):554–7.
16. Aydede M. Defending the IASP definition of pain. The Monist. 2017;100(4):439–64.
17. Hershman DL, Lacchetti C, Dworkin RH, Lavoie EM, Bleeker J, Cavaletti G, et al. Prevention and management of chemotherapy-induced peripheral neuropathy in survivors of adult cancers: American Society of Clinical Oncology clinical practice guideline. J Clin Oncol Off J Am Soc Clin Oncol. 2014;32(18):1941–67.
18. Girach A, Julian TH, Varrassi G, Paladini A, Vadalouka A, Zis P. Quality of life in painful peripheral neuropathies: A systematic review. Pain Res Manag. 2019;2019:2091960.
19. Aamir A, Girach A, Sarrigiannis PG, Hadjivassiliou M, Paladini A, Varrassi G, et al. Repetitive magnetic stimulation for the management of peripheral neuropathic pain: A systematic review. Adv Ther. 2020;37(3):998–1012.
20. Guerrero A, Gómez M. VIII Estudio Nacional de Dolor 2014: Prevalencia del dolor crónico en Colombia: Federación Latinoamericana de Asociaciones para el Estudio del Dolor [Internet]. 2014 [cited 2022 Jan 12]. Available from: http://fedelat.com/encuestade-dolor-2/
21. Casanova-García C, Lerma S, Pérez M, Ruano D, Santana E. Non-pharmacological treatment for neuropathic pain in children with cancer. Med Hypotheses. 2015;85(6):791–7.
22. Corrêa LA, Bittencourt JV, Mainenti MA, Mathieson S, Saragiotto BT, Telles GF, et al. Neural management plus advice to stay active on clinical measures and sciatic neurodynamic for patients with chronic sciatica: Study protocol for a controlled randomised clinical trial. PloS One. 2022;17(2):e0263152.
23. Zhang YH, Hu HY, Xiong YC, Peng C, Hu L, Kong YZ, et al. Exercise for neuropathic pain: A systematic review and expert consensus. Front Med. 2021;8:756940.
24. Yang S, Chang MC. Effect of repetitive transcranial magnetic stimulation on pain management: A systematic narrative review. Front Neurol. 2020;11:114.
25. Yu K, Niu X, He B. Neuromodulation management of chronic neuropathic pain in the central nervous system. Adv Funct Mater. 2020;30(37):1908999.
26. Bernetti A, Agostini F, de Sire A, Mangone M, Tognolo L, Di Cesare A, et al. Neuropathic pain and rehabilitation: A systematic review of international guidelines. Diagn Basel Switz. 2021;11(1):74.
27. Barros SC, Borba dos Santos R, Borba dos Santos P, Cabral ME, Monte-Silva K. Efficacy of coupling repetitive transcranial magnetic stimulation and physical therapy to reduce upper-limb spasticity in patients with stroke: A randomized controlled trial. Arch Phys Med Rehabil. 2014;95(2):222–9.
28. Dos Santos RBC, Galvão SCB, Frederico LMP, Amaral NSL, Carneiro MIS, de Moura AG, et al. Cortical and spinal excitability changes after repetitive transcranial magnetic stimulation combined to physiotherapy in stroke spastic patients. Neurol Sci Off J Ital Neurol Soc Ital Soc Clin Neurophysiol. 2019;40(6):1199–207.
29. Lefaucheur JP, Aleman A, Baeken C, Benninger DH, Brunelin J, Di Lazzaro V, et al. Evidence-based guidelines on the therapeutic use of repetitive transcranial magnetic stimulation (rTMS): An update (2014-2018). Clin Neurophysiol Off J Int Fed Clin Neurophysiol. 2020;131(2):474–528.
30. Gunduz A, Kumru H, Pascual-Leone A. Outcomes in spasticity after repetitive transcranial magnetic and transcranial direct current stimulations. Neural Regen Res. 2014;9(7):712–8.
31. Mendonca ME, Simis M, Grecco LC, Battistella LR, Baptista AF, Fregni F. Transcranial direct current stimulation combined with aerobic exercise to optimize analgesic responses in fibromyalgia: A randomized placebo-controlled clinical trial. Front Hum Neurosci. 2016;10:68.
32. Ramger BC, Bader KA, Davies SP, Stewart DA, Ledbetter LS, Simon CB, et al. Effects of non-invasive brain stimulation on clinical pain intensity and experimental pain sensitivity among individuals with central post-stroke pain: A systematic review. J Pain Res. 2019;12:3319–29.
33. Garcia-Pallero MÁ, Cardona D, Rueda-Ruzafa L, Rodriguez-Arrastia M, Roman P. Central nervous system stimulation therapies in phantom limb pain: A systematic review of clinical trials. Neural Regen Res. 2022;17(1):59–64.
34. Khedr EM, Kotb HI, Mostafa MG, Mohamad MF, Amr SA, Ahmed MA, et al. Repetitive transcranial magnetic stimulation in neuropathic pain secondary to malignancy: A randomized clinical trial. Eur J Pain Lond Engl. 2015;19(4):519–27.
35. Carneiro BD, Tavares I. Transcranial magnetic stimulation to treat neuropathic pain: A bibliometric analysis. Healthcare. 2024;12(5):555.
36. Hodaj H, Payen JF, Hodaj E, Dumolard A, Maindet C, Cracowski JL, et al. Long-term treatment of chronic orofacial, pudendal, and central neuropathic limb pain with repetitive transcranial magnetic stimulation of the motor cortex. Clin Neurophysiol. 2020;131(7):1423–32.
37. Higgins J, Thomas J, Chandler J, Cumpston M, Li T, Page M, et al. Cochrane handbook for systematic reviews of interventions version 6.2 (updated February 2021) [Internet]. Cochrane; 2021. Available from: www.training.cochrane.org/handbook
38. Urrútia G, Bonfill X. [PRISMA declaration: a proposal to improve the publication of systematic reviews and meta-analyses]. Med Clin (Barc). 2010;135(11):507–11.
39. Oslo Nor Knowl Cent Health Serv. Cochrane effective practice and organisation of care group. Eff Pract Organ Care EPOC Suggest Risk Bias Criteria EPOC Rev EPOC Resour Rev Authors. 2015. 2015.
40. Jin Y, Xing G, Li G, Wang A, Feng S, Tang Q, et al. High frequency repetitive transcranial magnetic stimulation therapy for chronic neuropathic pain: A meta-analysis. Pain Physician. 2015;18(6):E1029-1046.
41. Higgins JPT, Altman DG, Gøtzsche PC, Jüni P, Moher D, Oxman AD, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ. 2011;343:d5928.
42. National Institute of Heart, lungs and blood (NIHLBI). NIH. Estudiar herramientas de evaluación de la calidad [Internet]. Disponible en: https://www.nhlbi.nih.gov/health-topics/study-quality-assessment-tools
43. GRADE home [Internet]. [Citado el 12 de enero de 2021]. GRADE home. Disponible en: http://www.gradeworkinggroup.org/
44. Aguayo-Albasini JL, Flores-Pastor B, Soria-Aledo V. Sistema GRADE: clasificación de la calidad de la evidencia y graduación de la fuerza de la recomendación. Cir Esp. 2014;92(2):82–8.
45. Gradepro [Internet]. [Citado el 12 de enero de 2021]. Gradepro. Disponible en: https://gradepro.org/
46. Quesada C, Pommier B, Fauchon C, Bradley C, Créac’h C, Murat M, et al. New procedure of high-frequency repetitive transcranial magnetic stimulation for central neuropathic pain: a placebo-controlled randomized crossover study. Pain. 2020;161(4):718–28.
47. Abdelkader AA, El Gohary AM, Mourad HS, El Salmawy DA. Repetitive TMS in treatment of resistant diabetic neuropathic pain. Egypt J Neurol Psychiatry Neurosurg. 2019;55(1):30.
48. Ahmed GM, Maher EA, Elnassag BAEMR, Sayed HM, Kabbash SI. Effects of repetitive transcranial magnetic stimulation versus transcutaneous electrical nerve stimulation to decrease diabetic neuropathic pain. Int J Ther Rehabil. 2020;27(2):1–10.
49. Attal N, Ayache SS, Ciampi De Andrade D, Mhalla A, Baudic S, Jazat F, et al. Repetitive transcranial magnetic stimulation and transcranial direct-current stimulation in neuropathic pain due to radiculopathy: A randomized sham-controlled comparative study. Pain. 2016;157(6):1224–31.
50. Cervigni M, Onesti E, Ceccanti M, Gori MC, Tartaglia G, Campagna G, et al. Repetitive transcranial magnetic stimulation for chronic neuropathic pain in patients with bladder pain syndrome/interstitial cystitis. Neurourol Urodyn. 2018;37(8):2678–87.
51. Hosomi K, Sugiyama K, Nakamura Y, Shimokawa T, Oshino S, Goto Y, et al. A randomized controlled trial of 5 daily sessions and continuous trial of 4 weekly sessions of repetitive transcranial magnetic stimulation for neuropathic pain. Pain. 2020;161(2):351–60.
52. Hosomi K, Shimokawa T, Ikoma K, Nakamura Y, Sugiyama K, Ugawa Y, et al. Daily repetitive transcranial magnetic stimulation of primary motor cortex for neuropathic pain: a randomized, multicenter, double-blind, crossover, sham-controlled trial. Pain. 2013;154(7):1065–72.
53. Kim JK, Park HS, Bae JS, Jeong YS, Jung KJ, Lim JY. Effects of multi-session intermittent theta burst stimulation on central neuropathic pain: A randomized controlled trial. NeuroRehabilitation. 2020;46(1):127–34.
54. Attal N, Poindessous-Jazat F, De Chauvigny E, Quesada C, Mhalla A, Ayache SS, et al. Repetitive transcranial magnetic stimulation for neuropathic pain: A randomized multicentre sham-controlled trial. Brain J Neurol. 2021;144(11):3328–39.
55. Bonifácio ED, Martins WKN, de Carvalho CD, Ferreira CM, Gomes R, de Almeida ET, et al. Effects of rTMS and tDCS on neuropathic pain after brachial plexus injury: A randomized placebo-controlled pilot study. Sci Rep. 2022;12(1):1440.
56. Kataria M, Gupta N, Kumar A, Bhoriwal S, Singh A, Shekhar V, et al. Assessing the effectiveness of high frequency repetitive transcranial magnetic stimulation for post-mastectomy pain in breast cancer patients: A randomized controlled trial. Breast Cancer Tokyo Jpn. 2024;31(5):841–50.
57. Goto Y, Hosomi K, Shimokawa T, Shimizu T, Yoshino K, Kim SJ, et al. Pilot study of repetitive transcranial magnetic stimulation in patients with chemotherapy-induced peripheral neuropathy. J Clin Neurosci Off J Neurosurg Soc Australas. 2020;73:101–7.
58. Lindholm P, Lamusuo S, Taiminen T, Pesonen U, Lahti A, Virtanen A, et al. Right secondary somatosensory cortex-a promising novel target for the treatment of drug-resistant neuropathic orofacial pain with repetitive transcranial magnetic stimulation. Pain. 2015;156(7):1276–83.
59. Pommier B, Créac’h C, Beauvieux V, Nuti C, Vassal F, Peyron R. Robot-guided neuronavigated rTMS as an alternative therapy for central (neuropathic) pain: Clinical experience and long-term follow-up. Eur J Pain Lond Engl. 2016;20.
60. Ayache SS, Ahdab R, Chalah MA, Farhat WH, Mylius V, Goujon C, et al. Analgesic effects of navigated motor cortex rTMS in patients with chronic neuropathic pain. Eur J Pain Lond Engl. 2016 Oct;20(9):1413–22.
61. Lawson A, Frank S, Zafar N, Waschke A, Kalff R, Reichart R. Time course of the response to navigated repetitive transcranial magnetic stimulation at 10 Hz in chronic neuropathic pain. Neurol Res. 2018;40(7):564–72.
62. Lefaucheur JP, Ayache SS, Sorel M, Farhat WH, Zouari HG, Ciampi de Andrade D, et al. Analgesic effects of repetitive transcranial magnetic stimulation of the motor cortex in neuropathic pain: influence of theta burst stimulation priming. Eur J Pain Lond Engl. 2012;16(10):1403–13.
63. Nurmikko T, MacIver K, Bresnahan R, Hird E, Nelson A, Sacco P. Motor cortex reorganization and repetitive transcranial magnetic stimulation for pain-a methodological study. Neuromodulation J Int Neuromodulation Soc. 2016;19(7):669–78.
64. Sampson SM, Kung S, McAlpine DE, Sandroni P. The use of slow-frequency prefrontal repetitive transcranial magnetic stimulation in refractory neuropathic pain. J ECT. 2011;27(1):33–7.
65. Jiang X, Yan W, Wan R, Lin Y, Zhu X, Song G, et al. Effects of repetitive transcranial magnetic stimulation on neuropathic pain: A systematic review and meta-analysis. Neurosci Biobehav Rev. 2022;132:130–41.
66. Attia M, McCarthy D, Abdelghani M. Repetitive transcranial magnetic stimulation for treating chronic neuropathic pain: A systematic review. Curr Pain Headache Rep. 2021;25(7):48.
67. Che X, Cash RFH, Luo X, Luo H, Lu X, Xu F, et al. High-frequency rTMS over the dorsolateral prefrontal cortex on chronic and provoked pain: A systematic review and meta-analysis. Brain Stimulat. 2021;14(5):1135–46.
68. Kwon JH. Overcoming barriers in cancer pain management. J Clin Oncol Off J Am Soc Clin Oncol. 2014;32(16):1727–33.
69. Hall JA, Konstantinou K, Lewis M, Oppong R, Ogollah R, Jowett S. Systematic review of decision analytic modelling in economic evaluations of low back pain and sciatica. Appl Health Econ Health Policy. 2019;17(4):467–91.
70. Piano V. A case vignette study to assess the knowledgeof pain physicians of neuropathic cancer pain: Room for improvement. Pain Physician. 2013;6;16(6;11):E779–88.
71. Torrance N, Ferguson JA, Afolabi E, Bennett MI, Serpell MG, Dunn KM, et al. Neuropathic pain in the community: More under-treated than refractory? Pain. 2013;154(5):690–9.
72. Giménez-Campos MS, Pimenta-Fermisson-Ramos P, Díaz-Cambronero JI, Carbonell-Sanchís R, López-Briz E, Ruíz-García V. A systematic review and meta-analysis of the effectiveness and adverse events of gabapentin and pregabalin for sciatica pain. Aten Primaria. 2022;54(1):102144.
73. Lopes-Júnior LC, Rosa GS, Pessanha RM, Schuab SIP de C, Nunes KZ, Amorim MHC. Efficacy of the complementary therapies in the management of cancer pain in palliative care: A systematic review. Rev Lat Am Enfermagem. 2020;28:e3377.
74. Lefaucheur JP, André-Obadia N, Antal A, Ayache SS, Baeken C, Benninger DH, et al. Evidence-based guidelines on the therapeutic use of repetitive transcranial magnetic stimulation (rTMS). Clin Neurophysiol. 2014;125(11):2150–206.
75. Sachau J, Sendel M, Péchard M, Schnabel K, Schmieg I, Medkour T, et al. Patient reported outcome measures in chronic neuropathic pain clinical trials - a systematic literature review. J Pain. 2023;24(1):38–54.
76. Pogatzki-Zahn E, Schnabel K, Kaiser U. Patient-reported outcome measures for acute and chronic pain: Current knowledge and future directions. Curr Opin Anaesthesiol. 2019;32(5):616–22.
77. Tsai YY, Wu WT, Han DS, Mezian K, Ricci V, Özçakar L, et al. Application of repetitive transcranial magnetic stimulation in neuropathic pain: A narrative review. Life. 2023;13(2):258.
Notas de autor
catalinalopera8@gmail.com
Información adicional
CONFLICTOS DE INTERÉS: Los autores declaran no tener conflictos de intereses.
FINANCIACIÓN: El actual manuscrito fue financiado por la Fundación Universitaria Universidad María Cano.
