Artículos de investigación
Análisis del aceite esencial de muña (Minthosthachys acris Schmidt-Leb.) y evaluación de su actividad antimicótica sobre Sporothrix schenckii
Analysis of the essential oil of muña (Minthosthachys acris Schmidt-Leb.) and assay of its antimycotic activity on Sporothrix schenckii
Análisis del aceite esencial de muña (Minthosthachys acris Schmidt-Leb.) y evaluación de su actividad antimicótica sobre Sporothrix schenckii
Revista CENIC. Ciencias Químicas, vol. 50, núm. 1, pp. 022-032, 2019
Centro Nacional de Investigaciones Científicas
Recepción: 07 Mayo 2019
Aprobación: 07 Septiembre 2019
Abstract: Analysis of the essential oil from leaves of muña (Minthostachys acris Schmidt-Leb.) and the in vitro antimycotic effect on seven strains of Sporothrix schenckii were examined. The essential oil was obtained by steam distillation was analyzed by gas chromatography with flame ionization detector and gas chromatography-mass spectrometry. The oil yield was 0.21 % v/m. A total of 58 volatile compounds were identified, in which oxygenated monoterpenes were the major chemical class, being pulegone (54.4 %) and cis-mentone (11.0 %) the most abundant. Other major compound was the phenol thymol (6.3 %). Growth inhibition for mycelial and yeast phase of was evaluated by the agar diffusion method, whereas the tube dilution method was used only in mycelial phase. Essential oil concentrations ≥10% tested significantly inhibited the mycelial and yeast phase of (p<0.0001) and had larger inhibition zones than the control group. In the tube dilution, total inhibition was observed at dilutions of 2 to 50 uL. In experimental conditions, the essential oil of Minthostachys acris significant antifungal effect on in vitro.
Keywords: Minthostachys acris, muña, essential oil, composition, antimycotic activity, Sporothrix schenckii.
Resumen: Se analizó el aceite esencial de hojas de muña (Minthostachys acris Schmidt-Leb.) y se evaluó su efecto antimicótico in vitro sobre siete cepas aisladas de Sporothrix schenckii. El aceite esencial se obtuvo mediante destilación por arrastre con vapor y se analizó por cromatografía de gases con detector de llama y cromatografía de gases acoplada a espectrometría de masas. El rendimiento de aceite esencial fue de 0,21 % v/m. Un total de 58 compuestos volátiles fueron identificados, donde predominaron los monoterpenos oxigenados, siendo la pulegona (54.4 %) y cis-mentona (11.0 %) los más abundante. Otro compuesto mayoritario fue el fenol timol (6.3 %). La inhibición del crecimiento de la fase miceliar y levaduriforme del , se evaluó mediante el método de difusión en agar, mientras que por el método de dilución en tubo se evaluó solo la fase miceliar. Las concentraciones del aceite esencial ensayadas ≥10 % inhibieron significativamente la fase micelial y levaduriforme de (.<0,0001) y presentaron halos de inhibición mayores que el grupo control. En la dilución en tubo se observó inhibición total en las diluciones de 2 a 50 μL. El aceite esencial de Minthostachys acris tiene un efecto antimicótico significativo sobre el in vitro.
Palabras clave: Minthostachys acris, muña, aceite esencial, composición, actividad antimicótica, Sporothrix schenckii.
INTRODUCCIÓN
La esporotricosis es una infección subaguda o crónica causada por hongos del complejo Sporothrix schenckii, que incluyen: senso stricto, S. brasiliensis, S. globosa y S. luriei (Suzuki et al., 2016). La principal vía de transmisión de la esporotricosis es percutánea, a través de traumatismos y moretones con superficies contaminadas. Aunque tiene una distribución geográfica universal, esporotricosis predomina en el sur de África, América, Asia y Oceanía (Torres-Guerrero, 1999). Cuando el hongo penetra a través de la piel del individuo sensibilizado produce un síndrome chancriforme, caracterizado por un nódulo primario en el lugar de la implantación y nódulos secundarios satélites que evolucionan hacia gomas y se ulceran siguiendo el trayecto de los vasos linfáticos. También se presenta en forma de una placa fija localizada, verrugosa crónica sin linfangitis y es una enfermedad de fácil control terapéutico (Ramírez-Soto, 2012). En Perú, es la micosis subcutánea más frecuente, sobre todo en áreas rurales y agrícolas (Pappas et al., 2000; Bastos de Lima Barros et al., 2004; Ramírez-Soto et al., 2012).
El agente etiológico causante de esporotricosis, en la provincia de Abancay, pertenece a la especie Sporothrix schenckii, que es un hongo geófilo, dimórfico que crece en forma de levadura en tejido y en cultivo a 37 °C, pero como hongo filamentoso a 30 °C (Mackay, 2013). Las colonias de levadura son de color crema, húmedas y lisas, mientras que las colonias miceliales son inicialmente pequeñas, glabrosas y de color gris-blanco, y después de siete días son arrugadas y correosas con coloración de la superficie de gris a negro (Crothers et al., 2009).
Debido a los límites de los antifúngicos disponibles, la investigación de nuevas moléculas terapéuticas a partir de plantas naturales constituye un gran interés en todo el mundo. Muchos trabajos científicos han revelado propiedades terapéuticas de las plantas siendo utilizadas en la medicina tradicional (Jaset-Dongmo et al., 2008; Boyom et al., 2011). La familia Lamiaceae está constituida por especies que han exhibido una amplia gama de la actividad del espectro antimicrobiano (Jaset-Dongmo et al., 2008). El género Minthostachys está representado por 17 especies de arbustos aromáticos propios de los andes de América del Sur. El género tiene gran valor etnobotánico, farmacológico y comercial (Schmidt-Lebuhn, 2008). En particular, M. acris Schmidt-Leb. es un arbusto aromático, que crece silvestre en el Cusco y tiene varios usos como especia, para el tratamiento de la diarrea, cólicos, contusiones y como pesticida. M. acris es tratado frecuentemente como especie separada en las investigaciones peruanas, pero erróneamente llamado como M. glabrescens (Benth.) Epling (Schmidt-Lebuhn, 2008). No se conocen reportes en relación con la actividad antifúngica de este aceite esencial (Schmidt-Lebuhn, 2008), aunque en el aceite esencial de M. mollis (Kunth) Griseb, de similar composición, se ha demostrado actividad antifúngica (Cano et al., 2008).
El objetivo de este estudio fue determinar la composición química del aceite esencial de hojas de muña (Minthostachys acris Schmidt-Leb.) y evaluar su actividad antimicótica sobre cepas de Sporothrix schenckii aisladas de pacientes con esporotricosis.
MATERIALES Y MÉTODOS
Recolección de la muestra y aislamiento del aceite esencial
El espécimen fue recolectado en el distrito de Lamay, provincia de Calca (Cusco) a 2 941 m.s.n.m. El material fue tomado de las laderas de los cerros, zonas pedregosas, fueron cortadas con una hoz a unos 10 cm por encima de la superficie del suelo y las hojas fueron separadas. La muestra se registró en el herbario Vargas (Cuz.) de la Facultad de Biología de la UNSAAC con número 763 de identificación. El aceite esencial se aisló por destilación con arrastre por vapor de agua a partir de 10 kg de hojas frescas.
Análisis por cromatografía de gases
Se realizó en un equipo Konik 4000A (Konik, Barcelona) con detector de llama de hidrógeno (GC-FID) y con una columna de 30 m x 0,25 mm i.d. x 0,25 mm del tipo HP-5ms (Santa Clara, CA, EE.UU.). Los parámetros de operación fueron: programa de temperatura, 60 .C (2 min), 60 a 220 .C (4 .C/min) y 220 .C (5 min); gas portador hidrógeno a 1 mL/min; temperaturas del inyector y detector 240 .C. La cuantificación de los compuestos se hizo por normalización.
El aceite esencial también fue analizado por cromatografía gaseosa-espectrometría de masas en un equipo Agilent 6890N (Santa Clara, CA, EE.UU.) acoplado a un detector de masas Agilent 5975B. Se usó una columna similar al GC-FID, el mismo programa de temperatura y helio como gas portador. EIMS, con energía de 70 eV; temperatura de la fuente iónica y conexiones a 250 .C. La adquisición fue en modo scan (rango de 35 a 400 m/z). Los compuestos se identificaron por sus índices de retención lineales (IRL) y espectros de masas. Los IRL se calcularon por interpolación lineal relativa a los tiempos de retención de .-alcanos (C.–C24) y se compararon contra estándares y la literatura (Adams, 2001). Los espectros de masas se compararon con los obtenidos con estándares y reportados (NIST 05, Wiley 6, NBS 75k y Flavorlib).
Determinación de la actividad antimicótica in vitro del aceite esencial sobre Sporothrix schenckii
Se utilizaron siete cepas aisladas de pacientes clínicamente diagnosticados con esporotricosis siguiendo las recomendaciones del Instituto Nacional de Salud (MINSA & INS, 2010). Por cada paciente se realizaron los cultivos por triplicado en agar Sabouraud con cloranfenicol manteniéndoles a temperatura ambiente; de los positivos, se cultivó el hongo en agar BHI + 5 % de sangre a 37 °C durante 5 días en ambiente de CO., para la conversión a su estado de levadura. Todo el proceso se realizó en condiciones de esterilidad. Las cepas aisladas fueron certificadas por el INS.
Método de difusión en agar
Esta prueba se utilizó para evaluar la actividad antimicótica del aceite esencial frente a la fase levaduriforme y micelial de, basándose en la inhibición del crecimiento fúngico, mediante la difusión de las sustancias activas en un medio sólido, y posteriormente se evidencia por la formación de halos claros. En el caso del hongo en su fase levaduriforme se seleccionaron 4 o 5 colonias bien aisladas del cultivo en BHI y se transfirió una porción de cada colonia con un asa de siembra a un tubo de 4 a 5 mL de solución salina estéril. Se incubó el caldo entre 35 a 37 °C hasta alcanzar la turbidez del estándar McFarland (2 a 6 h). Se inoculó la suspensión de levaduras en el agar BHI, previamente preparado, cubriendo toda la placa utilizando la técnica del hisopo, se abrieron pozos en la placa con un sacabocados estéril de 11 mm de diámetro; se procedió a colocar 0,1 mL del aceite esencial al 100, 75, 50, 25, 20, 15, 10, 5, y 1 % (v/v), en los pozos previamente hechos. Se dejó reposar por un periodo de 30 minutos a temperatura ambiente y se incubaron las placas a 37 °C durante 7 días. Para el control negativo se sembró la levadura en una placa de agar BHI con etanol al 50 % y como control positivo una placa con anfotericina B (1 mg/mL). Transcurrido el tiempo de incubación, se procedió a realizar la lectura con la observación de las zonas claras de inhibición del crecimiento, mediante el registro de los diámetros en mm de estas zonas.
Para la evaluación de la actividad antimicótica del aceite esencial frente a la fase micelial de, se preparó el medio Takashio (Sabouraud modificado para producción de esporas) en tubos de ensayo, con los siguientes reactivos: dextrosa 0,6 g; Na.SO. 0,3 g; KH.PO. 0,3 g; peptona 0,3 g y agar-agar 6,0 g. Se agregaron a 300 mL de agua destilada (Gaitan, 2005). El hongo se sembró en medio Takashio a 27 °C durante 21 días hasta obtener un crecimiento homogéneo (aproximadamente 15 días). Se agregó a cada tubo de Takashio 2 mL de solución salina estéril y desprendió el hongo con el asa de nicromo. El material se trasvasó a tubos estériles con tapa de rosca y luego se agitó durante 2 min en vórtex para luego hacer un conteo de esporas en cámara de Neubauer (Gaitan, 2005). La suspensión de esporas preparada en solución salina fue de 100 esporas/μL, que es igual a 1 x 10⁵ esporas/mL (aproximadamente 10 esporas/cuadrante) y se almacenó en tubos estériles con tapa rosca, en refrigeración. De esta suspensión de esporas se sembraron placas con agar Sabouraud cubriendo todo el diámetro por el método del hisopo. Se abrieron pozos en las placas con ayuda de un sacabocados estéril de 11 mm de diámetro. Se procedió a colocar 0,1 mL del aceite esencial a 100, 75, 50, 25, 20, 15, 10, 5 y 1 % (v/v), en los pozos previamente hechos. Después de un reposo por 30 min a temperatura ambiente, se incubaron las placas a 27 °C por 14 a 21 días. Como control negativo se utilizó etanol al 50 % y como control positivo anfotericina B (1 mg/mL). Luego de transcurrir el tiempo de incubación se procedió a realizar la lectura con la observación de las zonas claras de inhibición del crecimiento.
Método de dilución en tubo
Se utilizó este método solo para la fase micelial. Esta prueba se basó en la inhibición del crecimiento fúngico, mediante la dilución del aceite esencial en tubos con agar y se evidenció por la ausencia de crecimiento en los tubos. Se prepararon diluciones usando 50, 25, 10, 5, 4, 3, 2 y 1 uL del aceite esencial tal cual, diluido en 10 mL del agar dextrosa Sabouraud fundido e inoculado con. Los tubos fueron determinados por inspección visual observando la inhibición de crecimiento de cada uno de los tubos comparado con el tubo control de crecimiento (libre de muestra). Las pruebas se realizaron por triplicado.
RESULTADOS Y DISCUSIÓN
El rendimiento de aceite esencial fue de 0,21 % v/m, valor inferior al 1 % reportado antes para esta especie (Svendsen et al., 1987). Un total de 58 compuestos volátiles fueron identificados en el aceite esencial de las hojas de muña (99,8 % del total de la composición) (Tabla 1). Como se aprecia, los monoterpenos oxigenados son la clase más abundante, donde sobresalen la pulegona y cis-mentona. Otro constituyente mayoritario fue el timol. El análisis del aceite esencial de M. acris reportó 36 compuestos, en el que los constituyentes mayoritarios fueron la pulegona (45,3 %), trans-mentona (17,8 %) y cis-mentona (6,4 %) (Svendsen et al., 1987), lo que arroja un patrón diferente a los resultados del presente trabajo. La composición química de los aceites esenciales depende de numerosos factores, entre los que pueden citarse las condiciones geobotánicas, técnicas de cultivo, edad de la planta, foto periodicidad, fecha de cosecha, entre otros (Figueiredo et al., 2008).
En el presente estudio se determinó la actividad antimicótica contra siete cepas del agente etiológico de micosis subcutánea, del aceite esencial de M. acris. Por ser este un hongo dimórfico, el ensayo se realizó tanto para la fase micelial (saprofítica) como para la levaduriforme (parasítica). El bioensayo de la fase micelial fue una adaptación de la metodología de Brancato y Golding modificada por MacRae para hongos filamentosos (Gaitán, 2005). Una vez obtenido el crecimiento óptimo de, se realizaron mediciones del diámetro de la colonia cada 3 días, durante 27 días. El hongo se desarrolló adecuadamente según la metodología; obteniéndose un crecimiento máximo de la colonia después de 18 días de incubación.
Según la Fig. 1, se puede observar que no existió actividad antimicótica con el etanol (control negativo) sobre la fase levaduriforme de , donde hubo un crecimiento óptimo del hongo; es a partir del 1 % de concentración de aceite que se observó el inicio de la actividad antimicótica mostrando un halo medio de 13,59 mm, considerándose como una actividad moderada, se incrementó esta actividad con el 5 %; a partir del 10 % la inhibición fue total, es decir, no hubo crecimiento del hongo en la placa. En cuanto a la anfotericina B (control positivo) para esta fase hubo un halo medio de inhibición de 35,43 mm, lo cual fue menor a la concentración de aceite al 10 %, ya que en el medio con anfotericina B si hubo crecimiento y en la concentración de 10 % la inhibición fue total.
En las comparaciones múltiples de Duncan (Fig. 2) se puede apreciar que no hubo actividad antimicótica con el etanol (control negativo) sobre la frase micelial de , donde el crecimiento fue óptimo, tampoco presentó actividad con 1 y 5 % de concentración de aceite; es a partir del 10 % de la concentración del aceite que empezó el inicio de la actividad antimicótica mostrando un halo medio de 24,66 mm, a partir del 25 % la inhibición fue total, es decir, no hubo crecimiento del hongo. En cuanto a la anfotericina B (control positivo) para esta fase tubo un halo medio de inhibición de 18,68 mm, lo cual podemos indicar que es menor a la concentración del aceite al 10 %. Es en ambas fases que el diámetro medio del halo inhibición de la anfotericina B fue menor al diámetro medio del halo de inhibición con el aceite a la concentración de 10 %. En ambas fases el diámetro medio del halo de inhibición de la anfotericina B fue menor al diámetro medio del halo de inhibición del aceite al 10 %. Lo cual puede indicar que el aceite a una concentración del 10 % es más efectivo que la anfotericina B, lo que podría deberse a que el aceite esencial posee varios principios activos que pueden actuar a bajas concentraciones, contrariamente a los medicamentos sintéticos que tienen un solo principio activo.
La fase levaduriforne de fue más susceptible al aceite esencial de M. acris, lo que puede deberse a la cantidad de ergosterol presente en la pared celular del hongo, lo cual es menor en una levadura que el micelio de un hongo. Es posible que los compuestos activos presentes en el aceite esencial inhiban la biosíntesis de ergosterol o de otros esteroles, lesionando la pared celular fúngica y alterando su permeabilidad; como consecuencia se produce la pérdida de elementos intracelulares esenciales. Otro posible mecanismo antifúngico es la inhibición de la síntesis de triglicéridos y fosfolípidos o la inhibición de la actividad enzimática oxidativa y peroxidativa, lo que conlleva a la acumulación de concentraciones tóxicas de peróxido de hidrogeno, que contribuyen al deterioro de los órganos subcelulares y necrosis celular (Gaitan, 2005). Sin embargo, no se puede definir el mecanismo de acción del aceite esencial ya que aún no se cuenta con el compuesto puro al que se le atribuya la actividad en forma precisa, ni con los bioensayos que lo comprueben. La razón por la cual un aceite esencial actúa a cierta concentración aún se desconoce, pero se le puede atribuir al mecanismo de acción de los compuestos presentes en el aceite esencial, como son pulegona, mentona y a la susceptibilidad de la célula fúngica ante ellos. Un aspecto que ha complicado la situación de pacientes con esporotricosis es el desarrollo de mecanismos de resistencia a los antimicóticos sintéticos por algunas especies, se explica en parte porque la mayoría de fármacos son fungistáticos y por la administración prolongada de los tratamientos en el tiempo, lo cual permite la aparición de clones resistentes. Esto apoya la búsqueda de otros antimicrobianos, como los de origen natural que actúen por ruptura de la membrana celular microbiana, en la descomposición de la fuerza motriz de los protones, agotamiento de la reserva de ATP, que puede provocar la liberación de biomoléculas esenciales. Además, pueden interferir con la replicación del ácido nucleico y transcripción, y síntesis de proteínas (Pisoschi et al., 2018).
Se reconoce que la actividad antimicótica del aceite esencial depende de sus propiedades lipofílicas o hidrofílicas. Los terpenos pueden servir como un ejemplo de agentes liposolubles, los cuales afectan la actividad de las enzimas catalizadoras a nivel de membrana, por ejemplo, ciertos componentes del aceite esencial pueden actuar como desacopladores, los cuales interfieren en la translocación de protones sobre la membrana y subsecuentemente interrumpir por la fosforilación del ADP (Kunicka-Styczynska et al., 2009). En el aceite esencial de muña, los monoterpenos se encontraron en mayor cantidad que conjuntamente al actuar con otros compuestos químicos mostraron un amplio espectro fungicida-fungistático frente a cepas de . Los analitos responsables de estas actividades podrían ser la pulegona, limoneno y mentona (Skoczen, 2006). En los estudios de las actividades farmacológicas de los aceites esenciales debe tenerse en consideración diferentes factores, los cuales pueden afectar los resultados de estos estudios (especies, factores ecológicos y condiciones ambientales). Como así también: el porcentaje de humedad del material recolectado, y los métodos de extracción han sido identificados como posibles fuentes de variación de la composición química, toxicidad y bioactividad de los aceites esenciales (Lahlou, 2004). En cuanto al mecanismo de acción del aceite esencial de muña, se fundamenta en: la destrucción de la pared del hongo y la membrana citoplasmática los cuales conllevan al rompimiento de la membrana y coagulación del citoplasma. El aceite esencial también inhibe la síntesis de DNA, RNA, proteínas y polisacáridos en los hongos, evocando cambios similares a los obtenidos a los antimicóticos de acción tópica (Gilma et al., 2012).
Se han reportado trabajos de investigación en los cuales los aceites esenciales son más efectivos que los agentes sintéticos (antimicóticos); el timol y carvacrol inhibieron el crecimiento de un gran número de microrganismos, y su eficacia contra: Phytophora capsicii, fue mayor que el de los antimicóticos de patente (Kunicka-Styczynska et al., 2009). Ocurre lo mismo en el presente estudio al usar la anfotericina B como control positivo donde la formación del halo es menor o igual a las concentraciones usadas con el aceite. En la acción antimicótica de estos componentes (metabolitos secundarios) el carácter lipofilico e hidrofílico de sus grupos funcionales son de gran importancia, debido a la polaridad que poseen, tiene propiedades antisépticas, antimicrobianas y antimicóticas; siendo esta actividad biológica de mayor a menor: fenoles, aldehídos, cetonas y alcoholes. Los esfuerzos para encontrar correlación entre la composición y bioactividad de los aceites esenciales no han sido totalmente dilucidados. Se presume que la actividad biológica de estos aceites esenciales no está determinada por la cantidad de monoterpenos, sino más por la tasa de su proporcionalidad (Lahlou, 2004). No obstante, deberá evaluarse la actividad de los componentes mayoritarios y si existen efectos sinergéticos con otros constituyentes del aceite esencial.
Por el método de dilución en tubo para la fase micelial no se observa crecimiento a los volúmenes ensayados; esto se podría deber a que el aceite está completamente puro y considerando la gran variedad de compuestos químicos presentes en los aceites esenciales, es probable que su actividad antimicótica no sea atribuible a un mecanismo especifico, sino a la acción combinada de varios de ellos sobre distintas localizaciones de la célula (Zekaria, 2007).
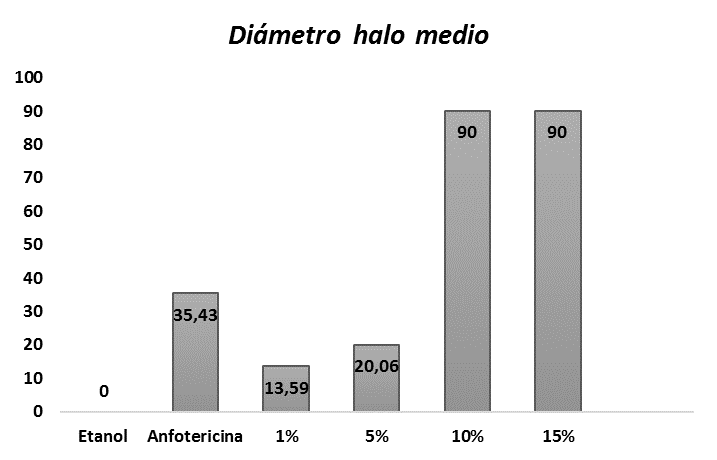
Fig. 1
Actividad antimicótica del aceite esencial Minthostachys acris Schmidt-Leb. sobre Sporothrix schenckii en su fase levaduriforme.
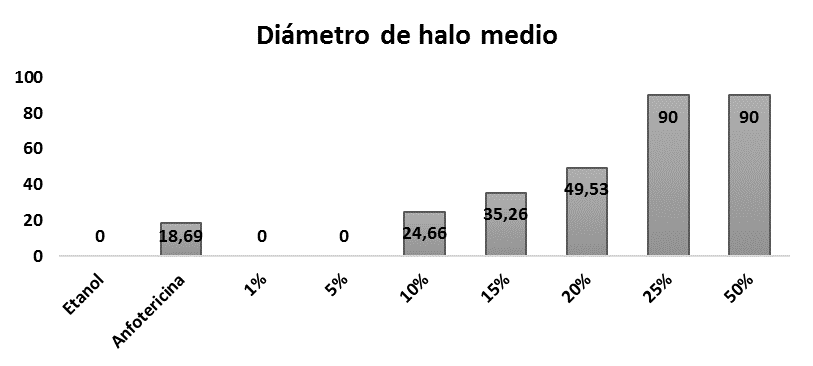
Fig. 2
Actividad antimicótica del aceite esencial de Minthostachys acris Schmidt-Leb. sobre Sporothrix schenckii en fase micelial.
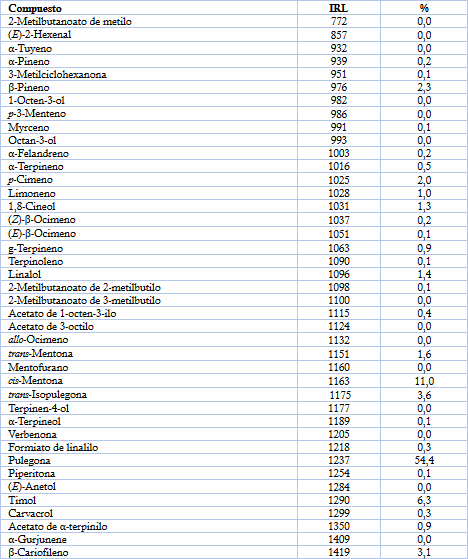
IRL: Índice de retención lineal en columna HP-5ms.

IRL: Índice de retención lineal en columna HP-5ms.
REFERENCIAS BIBLIOGRAFÍCAS
Adams, R. P. (2001). Identification of Essential Oil Components by Gas Chromatography/Quadrupole Mass Spectroscopy. Allured Publishing Co., Carol Stream, IL.
Bastos de Lima Barros, M., Oliveira Schubach, A. de, Francesconi do Valle, A. C., Gutierrez Galhardo, M. C., Conceicao Silva, F., Pacheco Schubach, T. M., & Conceicao, M. J. (2004). Cat-transmitted sporotrichosis epidemic in Rio de Janeiro, Brazil: Description of a series of cases. Clinical Infections Diseases, 38(4), 529-535.
Boyom, F. F., Ngouana, V., Kemgne, E. A. M., Zollo, P. H. A., Menut, C., Bessiere, J. M.Rosenthal, P. J. (2011). Antiplasmodial volatile extracts from Cleistopholis patens Engler & Diels and Uvariastrum pierreanum Engl. (Engl. & Diels) (Annonaceae) growing in Cameroon. Parasitology Research, 108(5), 1211-1217.
Cano, C., Bonilla, P., Roque, M., Ruiz, J. (2008). Actividad antimicótica in vitro y metabolitos del aceite esencial de las hojas de Minthostachys mollis (Muña). Revista Peruana de Medicina Experimental y Salud Publica, 25(3), 298-301.
Crothers, S. L., White, S. D., Ihrke, P. J., & Affolter, V. K. (2009). Sporotrichosis: a retrospective evaluation of 23 cases seen in northern California (1987-2007). Veterinary Dermatology, 20(4), 249-259.
Figueiredo, A. C., Barroso, J. G., Pedro, L. G., & Scheffer, J. J. C. (2008). Factors affecting secondary metabolite production in plants: volatile components and essential oils. Flavour and Fragrance Journal, 23, 213-226
Gaitán-Fernández, I. C. (2005). Actividad de doce plantas nativas guatemaltecas contra Sporothrix schenckii TT (Tesis). Universidad de San Carlos de Guatemala. Recuperado de http://biblos.usac.edu.gt/library/index.php?title=394275&lang=es
Gilman, A., & Goldman, L. S. (2012). Las Bases Farmacológicas de la Terapéutica. 6a ed. México: Interamericana. (pp. 0-2).
Jaset-Dongmo, P. M., Tatsadjieu, N. L., Tchinda-Sonwa, E., Kuate, J., Amvam-Zollo, P. H., & Menut, C. (2008). Antiradical potential and antifungal activities of essential oils of the leaves of Eucaliptus saligna and E. camaldulensis against Phaeoramularia angolensis. Afr. J. Biotechnol. 22(7), 4045-4050.
Kunicka-Styczyńska, A., Sikora, M., & Kalemba, D. (2009). Antimicrobial activity of lavender, tea tree and lemon oils in cosmetic preservative systems. J. Applied Microbiol. 107(6), 1903-1911.
Lahlou, M. (2004). Methods to study the phytochemistry and bioactivity of essential oils. Phytoth. Res. 18(6), 435-448.
MacKay, R. J. (2013). Sporotrichosis. Equine Infectious Diseases,2nd ed., Amsterdam: Elsevier Inc.
MINSA, & INS. (2010). Reglamento de Ensayos Clínicos. Recuperado de http://www.ins.gob.pe/insvirtual/images/otrpubs/pdf/Reglamentoensayosclinicos.pdf
Pappas, P. G., Tellez, I., Deep, A. E., Nolasco, D., Holgado, W., & Bustamante, B. (2000). Sporotrichosis in Peru: Description of an area of hyperendemicity. Clin. Infec. Dis., 30(1), 65-70.
Ramírez-Soto, M. C., & Loayza-Calderón M. (2012). Esporotricosis polimórfica, un problema de salud pública que debemos valorar. Galería Fotográfica, 29(2), 128-131. Recuperado de https://academic.oup.com/cid/article-lookup/doi/10.1086/313607
Ramírez-Soto M. C., Lizarraga-Trujillo J., Ticona-Sánchez E., Carrión-León, O., & Borda-López S., (2012). Perfíl clínico-epidemiológico de esporotricosis en una clínica de referencia en Abancay, Perú: 2004-2011. Rev. Per. Epidemiol. 16(2), 1-6.
Schmidt-Lebuhn, A. N. (2008). Ethnobotany, biochemistry and pharmacology of Minthostachys (Lamiaceae). J. Ethnopharmacol. 118(3), 343-353.
Skoczen, I. E. D. S. (2006). ebDB - Filling the gap for an International Ethnobotany Database. English, 11 (December).
Suzuki, R., Yikelamu, A., Tanaka, R., Igawa, K., Yokozeki, H., & Yaguchi, T. (2016). Studies in phylogeny, development of rapid identification methods, antifungal susceptibility, and growth rates of clinical strains of Sporothrix schenckii complex in Japan. Jap. J. Med. Mycol. 57(3), E 47-E 57.
Svendsen, A. B., Scheffer, J. J. C., & Looman, A. (1987) Composition of the volatile oil of Minthostachys glabrescens Epl. Flavour Fragr. J. 2, 45-46.
Torres-Guerrero, H. (1999). Ploidy study in Sporothrix schenkii. Fung. Gen. Biol. 27(1), 49–54.
Pisoschi, A. M., Pop A., Georgescu C., Turcuş V., Olah N. K., & Mathe, E. (2018). An overview of natural antimicrobials role in food. Eur. J. Med. Chem. 143, 922–935.
Zekaria, D. (2007). Los aceites esenciales, una alternativa a los antimicrobianos. Laboratorios Calier, pp. 1-6.