Artículo original
Recepción: 20 Enero 2021
Aprobación: 12 Junio 2021
RESUMEN: Las micorrizas arbusculares han sido ampliamente descritas como favorecedoras del crecimiento vegetal y realizan cambios físicos, bioquímicos y fisiológicos en las raíces que conducen a un mejor estado general de la planta y contribuyen a aliviar las situaciones de estrés de carácter abiótico y biótico. Producto de sus múltiples beneficios se ha ido incrementando paulatinamente su uso en la agricultura cubana. El sistema de recomendación de cepas de carácter generalistas del INCA se basa, fundamentalmente, en el tipo de suelo y su fertilidad asociada. Conocer cómo se integra el efecto de bioprotección de diferentes cepas con el pH puede contribuir a dilucidar si el efecto se asocia a una cepa “per se” o depende de la efectividad de las mismas. Para ello se diseñó un experimento utilizando un suelo Argissolo rojo-amarillento, ajustando las concentraciones de Ca2+ y Mg2+ a un único nivel y tres valores de pH (5,5; 6,5 y 7,2) con el objetivo de conocer si las diferencias en el pH también influyen en la bioprotección ejercida por estas cepas. Se utilizaron las cepas Rhizophagus irregularis, Glomus cubense y Rizophagus clarus recomendadas para diferentes rangos de pH y se usó como patógeno Fusarium oxysporum f. sp. phaseoli que fue inoculado en plantas de frijol de 21 días de edad. Las cepas originaron respuestas diferenciadas dependientes del pH en la intensidad de la colonización, la bioprotección ejercida y la inducción activa de peroxidasas, indicando que el efecto de bioproteccion se asoció a la efectividad que presentaba cada cepa en uno u otro pH.
Palabras clave: Fusarium oxysporum, frijol, micorrizas.
RESUMEN: Arbuscular mycorrhizae have been widely described as favoring plant growth and making physical, biochemical and physiological changes in roots that lead to a better general condition of the plant and contribute to alleviate abiotic and biotic stress situations. As a result of their multiple benefits, their use in Cuban agriculture has been gradually increasing. INCA's generalist strain recommendation system is based, fundamentally, on the soil type and its associated fertility. Knowing how the bioprotection effect of different strains is integrated with pH can contribute to elucidate whether the effect is associated with a strain "per se" or depends on the effectiveness of the strains. For this purpose, an experiment was designed using a red-yellowish Argissolo soil, adjusting the Ca2+ and Mg2+ concentrations to a single level and three pH values (5.5; 6.5 and 7.2) with the aim of finding out whether differences in pH also influence the bioprotection exerted by these strains. Rhizophagus irregularis, Glomus cubense and Rizophagus clarus strains recommended for different pH ranges were used and Fusarium oxysporum f. sp. phaseoli was inoculated on 21-day-old bean plants as pathogen. Strains originated differentiated pH-dependent responses in the intensity of colonization, bioprotection exerted and active induction of peroxidases, indicating that the bioprotection effect was associated with the effectiveness of each strain at one or another pH.
Key words: Mycorrhizae, fusarium oxysporum, bean.
INTRODUCCIÓN
Además de la nutrición de las plantas, la simbiosis micorrízica arbuscular afecta, de forma positiva, la capacidad de estas para superar los estreses biótico y abiótico, de forma tal que comúnmente mejoran la tolerancia a las condiciones ambientales desfavorables y la resistencia a los patógenos (1). El establecimiento y el mantenimiento de la asociación requieren un alto grado de coordinación entre ambos socios y un control bidireccional (planta-hongos) del intercambio justo de recursos entre simbiontes (2). De hecho, se ha propuesto una regulación precisa de los niveles hormonales como un mecanismo central en la regulación de la interacción (3).
Los hongos micorrizógenos arbusculares (HMA) no solo son microorganismos edáficos, sino que el micelio extraradical, que es la estructura más abundante y que se encarga de la absorción de los nutrientes y el agua, entre otros efectos, se encuentra en el suelo. Incluso dentro de la simbiosis es inusual porque el grueso de las estructuras se encuentra en el suelo y no dentro del hospedero; por tanto, no es de extrañar la importancia que tienen las condiciones edáficas en el funcionamiento micorrízico (4). Aunque no hay una especificidad de socio estricta en la simbiosis micorrízica arbuscular (MA), el resultado de las interacciones que se establecen depende de los socios que interactúan y las condiciones ambientales (5). En este sentido, el Instituto Nacional de Ciencias Agrícolas (INCA) ha propuesto un sistema de recomendación de cepas eficientes en términos de nutrición y ecoservicios, basado, fundamentalmente, en el tipo de suelo y su fertilidad asociada (6).
Este sistema tiene como objetivo maximizar los efectos de estos hongos, con la consecuente disminución de la aplicación de fertilizantes y un máximo de rendimiento, derivado de los ecoservicios de esta simbiosis. En el mismo se incluye el pH como determinante de la maximización de los efectos, el cual está asociado a los niveles de Ca2+ y Mg2+, de forma tal que estos también pudieran asociarse con la respuesta efectiva de las cepas.
Por otra parte, las plagas de las plantas deben ser manejadas para mantener la calidad y la abundancia de alimentos. Para ello se han utilizado diferentes enfoques con el fin de prevenir y mitigar el efecto de las plagas (7). En el marco de la agricultura actual, el uso de los HMA ha cobrado una importancia vital, no solo por su contribución al desarrollo y nutrición de las plantas, sino también por los efectos como agentes antiestrés que estos microorganismos tienen, tanto en los estreses bióticos como abióticos (8). En este sentido, el uso de HMA como agentes antiestrés contra enfermedades ha cobrado un interés cada vez más creciente. Se han propuesto diferentes mecanismos por los cuales estos hongos son capaces de inducir protección en sus hospedantes vegetales, entre los que se incluyen mejoras en la nutrición, cambios en los exudados radicales, inducción de mecanismos activos de defensa e incluso, traslocación de señales utilizando la red hifal para inducir mecanismos defensivos en las plantas de la vecindad, con el fin de que esta respuesta pueda prevenir el desarrollo y el establecimiento del patógeno (9).
Diferentes autores han hecho énfasis en el hecho de que el establecimiento y la eficiencia simbiótica de estos microorganismos están influenciados por el ambiente edáfico, específicamente por la fertilidad del suelo y su pH (6,10).
Este trabajo tuvo como objetivo dilucidar en qué medida el pH del suelo puede influenciar la eficiencia simbiótica y, por tanto, el efecto de bioprotección ejercido por tres cepas de HMA.
MATERIALES Y MÉTODOS
Material vegetal: Se empleó frijol (Phaseolus vulgaris L.) de la variedad Preto Estrela, cedida por el grupo de semillas de EMBRAPA (Empresa Brasileira de Pesquisa Agropecuária, en Portugués) Agrobiología.
Condiciones experimentales: A partir de un suelo Argissolo rojo-amarillento (11), que corresponde a un Acrisol Rhodic Santi según World Reference Base con pH-H2O de 4,94 y contenidos de Ca2+ y Mg2+ intercambiables de 0,17 y 0,05 cmolcd-1, se procedió a preparar tres condiciones de pH (5,5; 6,5 y 7,2) con CaCO3 y se ajustó a concentraciones similares de Ca2+ y Mg2+ en los tres pHs de 1,63 y 0,26 cmolcd-1 utilizando CaSO4 y MgSO4. Con el procedimiento descrito se eliminó el posible enmascaramiento que ocasionan cantidades variables de Ca2+ y Mg2+ en los diferentes tratamientos y que impide establecer el efecto del pH.
Hongos micorrízicos arbusculares (HMA): Se utilizaron las cepas de HMA Rhizophagus irregularis (Blaszk, Wubet, Renker & Buscot) Walker & Shüβler (INCAM-11, DAOM-711363) y Glomus cubense (Y. Rodr. & Dalpé) (INCAM-4, DAOM-241198), procedentes de la colección del Laboratorio de Micorrizas del INCA, San José de las Lajas, Mayabeque, que se encontraban conservadas en una solución protegida osmóticamente (12). También se usó la cepa Rizophagus clarus (Nicol. & Schenck) Walker & Shüβler (A5, CNPAB) proveniente del Biological Resource Center Johanna Döbereiner (CRB-JD) EMBRAPA Agrobiología, Seropédica, Rio de Janeiro, Brasil, conservadas en sustrato a 4 ºC cuyo título era de 75 esporas g-1 de sustrato y que se aplicó en el nicho de siembra a razón de 1 g. Esta cepa es aislada de los suelos de Brasil y, por tanto, está adaptada a las condiciones de acidez de los suelos de esta zona.
La inoculación con HMA se realizó en la siembra y en la emergencia de las plantas para Rhizophagus irregularis y Glomus cubense empleando un inóculo líquido a razón de 60 esporas mL-1 y en el nicho de siembra para Rhizophagus clarum, a razón de 1 g de inoculante sólido con un contenido de esporas de 75 esporas por g de suelo.
Se utilizaron macetas de 1 kg con una planta por maceta, a las cuales se les adicionó semanalmente solución de Hoagland ajustada a una concentración de fósforo, equivalente a un cuarto de la solución inicial (1/4 P equivale a 0,204 g L-1), para mantener un suministro de nutrientes que permitieran el correcto desarrollo del cultivo, así como alcanzar una micorrización efectiva.
Las plantas se desarrollaron en condiciones semicontroladas de temperatura (24 ºC±2 ºC), humedad relativa (80-85 %) y fotoperíodo natural (14 horas luz-10 horas oscuridad). Los experimentos se ejecutaron en condiciones de invernadero en las aéreas de EMBRAPA Agrobiología, Seropédica, Rio de Janeiro, Brasil.
Los tratamientos establecidos se pueden observar en la Tabla 1.
Tratamientos establecidos a cada valor de pH
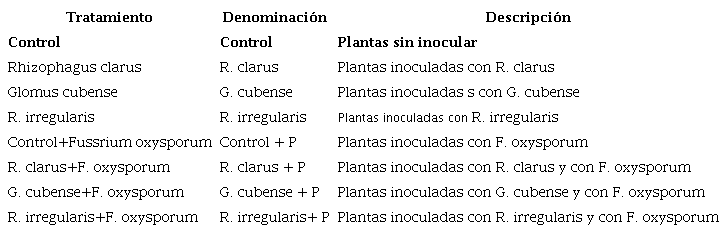
Patógeno: Se utilizó como patógeno Fusarium oxysporum f. sp. phaseoli mantenido en PDA y cedido por el laboratorio de fitopatógenos de EMBRAPA Brasilia, Brasil. El inóculo del fitopatógeno se obtuvo a partir de colonias crecidas por 15 días en placas Petri de 90x14 mm, contentivas del medio de esporulación para frijol (Agar 15 g; dextrosa 20 g; hojas de frijol 200 g y completar con agua destilada a 1000 mL pH 5,9) (11) y se realizó un inóculo mixto con las razas 149 y 151 que son las de mayor incidencia en las condiciones de Brasil. A las placas se les añadió 20 mL de agua destilada estéril y se colectó el micelio con una espátula de Drigalski. Se ajustó la concentración a 105 esporas mL-1 por conteo en cámara de Neubauer. La inoculación se realizó en plantas de 21 días de edad, aplicándose el patógeno por aspersión en la zona de la raíz a razón de 5 mL planta-1.
Se desarrolló un experimento de parcela dividida en la que cada parcela correspondió a un pH con ocho tratamientos para cada parcela, que consistieron en la inoculación simple de cada cepa de HMA y un testigo sin inocular combinados con la inoculación o no del patógeno, según Tabla 1. Se utilizaron ocho macetas por tratamiento con tres plantas cada uno. Las plantas inoculadas con Fusarium oxysporum se mantuvieron separadas de las no inoculadas. Posterior a la inoculación del patógeno, a los 21 días de emergidas las plantas, estas se mantuvieron en cámara húmeda cerradas con nylon por 48 horas. En todos los tratamientos se evaluaron diariamente los síntomas y signos de la enfermedad, contando como día cero el momento en que las plantas fueron inoculadas y hasta el día cinco que correspondió a plantas de 25 días después de la germinación. En cada momento se evaluó el porcentaje de necrosis foliar por hoja, calculándose el promedio de las mediciones en todas las hojas de cada planta. La severidad de los daños se evaluó mediante la medición del grado de marchitez en cada planta (13). Durante cada evaluación se realizó el muestreo destructivo de las plantas de una maceta para determinar la frecuencia e intensidad de la colonización micorrízica, así como la extracción de proteínas totales para evaluar actividad enzimática de peroxidasas.
Determinación de la ocupación fúngica: Se conformó una muestra de un pool de raíces correspondientes a tres plantas/tratamiento que se secaron a 70 °C y se tiñeron con tinta al 5 % en ácido acético al 2 % (14). Se evaluaron la frecuencia de colonización por el método de los interceptos (15) y la intensidad de la colonización (D.V) mediante el método descrito (16).
Extracción de enzimas y determinación de Peroxidasas: Las muestras de raíces y hojas se maceraron en nitrógeno líquido de forma independiente y se homogenizaron en proporción 1:2 (g mL-1), con solución amortiguadora de extracción (acetato de sodio, 0,1 M, pH 5,2; que contenía 5 g de polivinilpirrolidona y 0,05 g de β- mercaptoetanol, en 100 mL de solución de extracción). El homogenato se agitó en zaranda durante 45 minutos, en baño de hielo, luego se filtró a través de gasa y se centrifugó a 14 000 x G, a 4 °C durante 25 minutos, en centrífuga refrigerada. El sobrenadante se almacenó a -80 °C hasta su uso, para las determinaciones de concentración de proteínas totales y la actividad enzimática peroxidasa. La concentración de proteínas se determinó por el método descrito por Bradford (17).
Actividad peroxidasa (PRX) (Clasificación enzimática (E.C) 1.11.1.7): Se realizó según el método continúo descrito (18). La velocidad de oxidación del guayacol se determinó en espectrofotómetro (Ultrospec Plus Spectrophotometer, Pharmacia LKB), registrándose los valores de absorbancia a 470 nm. Se tomó la variación de la absorbancia, durante dos minutos a intervalos de 10 segundos. La actividad enzimática se expresó como μmoles de producto formado min-1 mL-1 de enzima.
Posteriormente se calculó la actividad específica, a partir de la relación de la actividad enzimática y la concentracion de proteínas de cada muestra.
Análisis estadístico de los datos: Se usaron técnicas paramétricas y no paramétricas en función de la variable analizada. La severidad de la enfermedad producida por el patógeno se presenta según la siguiente fórmula % de plantas sanas=100-% de marchitez detectada, para visualizar una dinámica de severidad.
RESULTADOS Y DISCUSIÓN
Una de las premisas que se establecen para que los hongos micorrízicos ejerzan su efecto es que deben estar establecidos y con suficientes estructuras fúngicas que les permitan ejercer su acción (7). En este sentido, la Figura 1 representa los niveles de intensidad de la colonización que incluyen, no solo la presencia o ausencia del hongo en la raíz como en el caso de la frecuencia o colonización, sino también la cantidad de estructuras fúngicas que se detectan como un mejor indicativo del funcionamiento de la simbiosis (15,19).
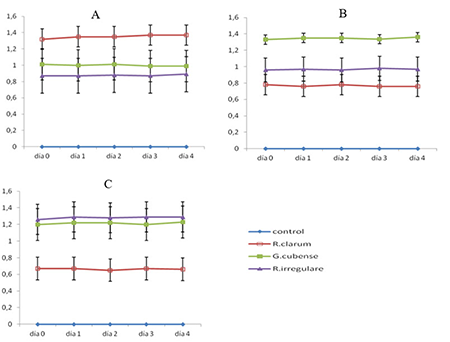
Figura 1
Intensidad de la colonización detectada para cada una de las cepas analizadas en los diferentes pH-H2O que se establecieron durante el experimento
A: pH=5,5, B: pH=6,5 y C: pH=7,2. El eje de las ordenadas representa la intensidad de la colonización medida según se describe en Materiales y Métodos y las abscisas el tiempo en días. Las barras corresponden a los intervalos de confianza para p≤0,05 %
La cepa cedida por el grupo de EMBRAPA Agrobiología presentó la mayor intensidad micorrízica en el pH más ácido, mientras que en el pH de 6,5 la mayor ocupación se encontró con la inoculación de G. cubense, seguida por la inoculación de R. irregulare y con un comportamiento inferior de la cepa R. clarus. En el pH 7,2 los comportamientos de R. irregulare y G. cubense fueron muy similares y superiores al obtenido al inocular R. clarus, Los resultados que se han alcanzado en Cuba sobre manejo de inoculantes micorrízicos, incluyen la utilización de cepas eficientes de carácter generalista, cuya condición de eficiencia es dependiente del pH del suelo o sustrato en que se vaya a desarrollar el cultivo inoculado (6). La cepa G. cubense/INCAM-4 se recomienda para utilizar en suelos cuyos pH-H2O fluctúan entre 5,8 y 7,2.; mientras que la cepa R. irregulare/INCAM-11 se recomienda para pH entre 7 y 8, con una zona de solapamiento o transición de la eficiencia de ambas cepas entre pH 7 y 7,2. Los resultados de este trabajo corroboran los criterios ya descritos por diferentes autores (6) y permiten incluir este tipo de suelo de origen brasilero, que como se observa, cambia la cepa eficiente en función del pH, con lo cual se incrementan los tipos de suelos en que se cumplen y no quedan circunscritos a los suelos cubanos. En el caso de la cepa R. clarus es una cepa aislada de suelos de Brasil, recomendada para inocular diversos cultivos en los suelos más ácidos de este país y, por tanto, que presentara la mayor efectividad en el pH ácido.
Es de señalar que trabajos de comparación de efectividad de las cepas INCAM con varias especies de gramíneas forrajeras y en diversos suelos, realizados anteriormente (20), demostraron un cambio de efectividad de las cepas por tipo de suelo y explicable por los cambios en el pH, aunque las altas correlaciones en condiciones naturales entre el pH y los contenidos de Ca y Mg en los suelos enmascararon el referido efecto.
Los HMA se adaptan a un amplio espectro de condiciones edáficas que están relacionadas con su ocurrencia, desarrollo y eficacia (21) e influyen en el funcionamiento de la simbiosis micorrízica sujeta a la interacción de varios factores edáficos (4), con especial énfasis en el pH (22). El pH es considerado una de las propiedades químicas más importantes del suelo (23), debido al efecto que ejerce, tanto sobre las características físicas, químicas y biológicas de éste, como también sobre el rendimiento de los cultivos. Esta variable puede determinar, desde el punto de vista biológico, el tipo de organismo que se desarrolle sobre un suelo, debido a su gran influencia sobre la disponibilidad de nutrientes. Al respecto, se afirma que los hongos y el grupo de bacterias actinomicetos constituyen los dos grandes grupos de microorganismos del suelo y el predominio de uno u otro grupo depende de las condiciones locales, especialmente del pH y del contenido de humedad (24). Entre estos microorganismos se encuentran los hongos micorrízicos arbusculares, los cuales viven en simbiosis mutualista con alrededor del 95 % de las especies del reino vegetal (6).
Se considera que la condición de acidez del suelo, expresada a través de su pH, se encuentra vinculada al funcionamiento de los HMA (25). Actualmente son explicables los efectos del pH sobre la disponibilidad de nutrientes, la regulación de procesos de intercambio iónico y la diversidad de microorganismos asociados a la micorrizosfera (26,27). Además se han informado otros efectos más directos sobre la germinación y la esporulación (25). No obstante, se considera que aún no está suficientemente claro cuál es el mecanismo que explica y condiciona los cambios en funcionamiento y efectividad de estas cepas con el pH del suelo.
Las Figuras 2 y 3 presentan los niveles de protección ejercidos por las diferentes cepas en los pHs usados en el experimento y la actividad específica de peroxidasas detectadas.
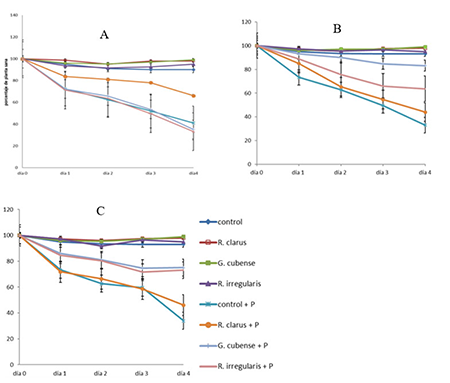
Figura 2
Porcentaje de plantas sanas encontradas en los diferentes pHs durante el enfrentamiento entre plantas micorrizadas e inoculadas o no con el patógeno
A: pH=5,5, B: pH=6,5 y C: pH=7,2. Se emplearon plantas de frijol (P. vulgaris L.) de la variedad Preto Estrela de 21 días de edad, las cepa de HMA Rhizophagus clarus (R. clarus), R. irregularis (R.irregulare) y Glomus cubense (G. cubense) y Fusarium oxysporum f. sp. Phaseoli como patógeno (P), crecido en medio de esporulación para frijol. En el eje de las ordenadas se presentan el porcentaje de plantas sanas por la formula presentada en Materiales y Métodos y en el eje de las abscisas el tiempo en días Las barras corresponden a los intervalos de confianza para p≤0,05 %
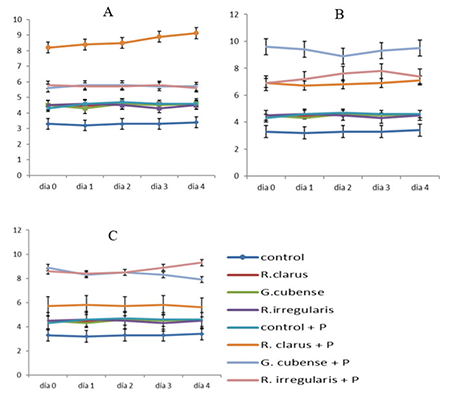
Figura 3
Dinámica de Actividad Peroxidasa en cada uno de los tratamientos analizados en los diferentes pHs en los que se estableció el experimento
A: pH= 5,5, B: pH=6,5 y C: pH=7,2. Los puntos representan la media de los tratamientos muestreados. El eje de las ordenadas representa la actividad específica calculada según Materiales y Métodos y las abcisas representan el tiempo en días. Las barras corresponden a los intervalos de confianza para p≤0,05 %
Las plantas que no fueron inoculadas con el patógeno no presentaron daños en las hojas y sin diferencias significativas entre dichos tratamientos. En los tratamientos inoculados con las cepas de F. oxysporum, si bien en todos los pH se encontraron daños en las plantas, independientemente de la inoculación de una u otra cepa de HMA, aunque en estos últimos los daños fueron mucho menores, variando el referido efecto de bioprotección alcanzado con cada cepa con el pH.
La magnitud del efecto de bioprotección que originó cada cepa de HMA en un determinado pH se asoció con el grado de intensidad fúngica que alcanzó dicha cepa en ese mismo pH (Figura 1), de forma tal que en cada pH la cepa o cepas con mayor intensidad de colonización presentaron, a la vez, el mayor efecto de bioprotección. Por tanto, los resultados indicaron que el efecto de bioprotección se asoció con el grado de efectividad o funcionamiento micorrízico que presentó cada cepa, el cual fue dependiente del pH.
Es de destacar la alta relación entre el efecto de bioprotección que presentaron las cepas INCAM4 e INCAM11 y la recomendación de cepas HMA eficientes en función del pH como criterio para su inoculación (6). Los resultados también indicaron el valor agregado que presenta la utilización de estas cepas como base para la conformación de los inoculantes, ya que no solo alcanzaron un alto funcionamiento micorrízico y los beneficios comúnmente asociados a este (20), sino también un mayor efecto de bioprotección.
El efecto de bioprotección relacionado con el funcionamiento micorrízico ha estado asociado a la inducción de mecanismos defensivos de las plantas y dentro de estos mecanismos las peroxidasas han sido una de la PR-proteínas vinculadas (7,28). En la Figura 3 se aprecia que en cualquiera de los pH en los tratamientos que no recibieron el patógeno, se encontraron niveles basales de actividad PRX que no difirieron entre sí, bien fueran inoculadas con cepas de HMA o el control.
Sin embargo, en presencia del patógeno, en todos los casos, la inducción enzimática fue superior. En el caso de las plantas micorrizadas se encontraron diferencias significativas entre las inducciones de peroxidasas ocasionadas por las cepas de HMA y dependiente este efecto del pH. En cada pH, la cepa que originó los mayores valores de la inducción de peroxidasas, fue la que ocasionó el mayor efecto de bioprotección y, al mismo tiempo, alcanzó la mayor intensidad fúngica.
Los mecanismos inducidos por los HMA para atenuar el daño oxidativo y proteger la función de la célula vegetal abarcan a una serie de mecanismos de tolerancia activados por estos hongos como mejoras en la nutrición y la toma de agua, la modulación y la expresión de genes que están relacionados con la señalización y, por tanto, la respuesta al estrés (7). El funcionamiento de estos hongos, sin embargo, está mediado por las condiciones edáficas entre las que el pH destaca como un elemento importante ya que esta propiedad química del suelo determina en muchos casos la eficiencia del endófito, el porcentaje de germinación de las esporas y el desarrollo de las micorrizas arbusculares (29,30).
La acidez del suelo limita la productividad de las plantas, inhibe la elongación de la raíz y reduce la solubilidad del fósforo (P). Es por este motivo que algunas especies de HMA pueden verse afectadas por esta condición de acidez, como la mayoría de las especies de Glomus (30). La relación que se establece entre los rangos de pH del suelo y el efecto de la colonización micorrizógena es verdaderamente complejo, dependiendo no sólo de la especie micótica, sino también del tipo de suelo, la forma en que se encuentran los nutrientes (fundamentalmente P y N y otros elementos como Cu, Zn, Mo, B, etc.) y en menor medida de la especie de planta sobre la que se desarrolla (27).
Las cepas que componen el biofertilizante EcoMic® producido en Cuba y de las cuales, dos formaron parte de este estudio, se pueden clasificar según Opik (30), como generalistas con los cultivos y específicas con el pH del suelo (6). En este sentido, la eficiencia de las cepas está maximizada en las condiciones en las que desempeña su mejor función, no solo en la toma de nutrientes y agua (20,31,32), sino también en cuanto a los mecanismos de protección que inducen en las plantas y que se demuestran aquí en la inducción de peroxidasas, que se revierte en una protección de las membranas biológicas (7,28). Esta resultó siempre mejor en la cepa que funcionó en el pH para la cual se recomienda, con lo cual deja claro que, en nuestro caso, la bioprotección es un atributo más de la efectividad de la simbiosis.
CONCLUSIÓN
La inoculación de cepas eficientes de HMA produce un significativo efecto de bioprotección que se asocia directamente con la inducción de peroxidasas y ambos son consecuencia del grado de funcionamiento micorrízico que alcanzan las diferentes cepas. Este último, depende del pH del suelo en que se desarrollan las plantas micorrizadas. Al menos con las cepas estudiadas el efecto de bioprotección no se asocia a una cepa “per se” y es otro atributo de la efectividad del funcionamiento micorrízico.
BIBLIOGRAFÍA
Rivero J, Gamir J, Aroca R, Pozo MJ, Flors V. Metabolic transition in mycorrhizal tomato roots. Frontiers in Microbiology [Internet]. 2015 [cited 05/07/2022]; doi:10.3389/fmicb.2015.00598
Lanfranco L, Bonfante P, Genre A. The Mutualistic Interaction between Plants and Arbuscular Mycorrhizal Fungi. Microbiology Spectrum. 2016;1-20. doi:10.1128/microbiolspec.FUNK-0012-2016
Pozo MJ, López-Ráez JA, Azcón-Aguilar C, García-Garrido JM. Phytohormones as integrators of environmental signals in the regulation of mycorrhizal symbioses. New Phytologist. 2015;205(4):1431-6. doi:https://doi.org/10.1111/nph.13252
Helgason T, Fitter AH. Natural selection and the evolutionary ecology of the arbuscular mycorrhizal fungi (Phylum Glomeromycota). Journal of Experimental Botany. 2009;60(9):2465-80. doi:10.1093/jxb/erp144
Smith FA, Smith SE. How harmonious are arbuscular mycorrhizal symbioses? Inconsistent concepts reflect different mindsets as well as results. The New Phytologist. 2015;205(4):1381-4.
Espinosa R, Felix F, Martinez L, Cañizares P, Yakelín R, Ortega E. Manejo, integración y beneficios del biofertilizante micorrízico EcoMic (r) en la producción agrícola [Internet]. 2020. INCA. Mayabeque, Cuba; 2020. 155 p.
Hashem A, Abd_Allah EF, Alqarawi AA, Egamberdieva D. Arbuscular Mycorrhizal Fungi and Plant Stress Tolerance. In: Egamberdieva D, Ahmad P, editors. Plant Microbiome: Stress Response [Internet]. Singapore: Springer; 2018 [cited 11/07/2022]. p. 81-103. doi:10.1007/978-981-10-5514-0_4
Lanfranco L, Fiorilli V, Gutjahr C. Partner communication and role of nutrients in the arbuscular mycorrhizal symbiosis. New Phytologist. 2018;220(4):1031-46. doi:https://doi.org/10.1111/nph.15230
Venturi V, Keel C. Signaling in the Rhizosphere. Trends in Plant Science. 2016;21(3):187-98. doi:10.1016/j.tplants.2016.01.005
Herrera-Peraza RA, Hamel C, Fernández F, Ferrer RL, Furrazola E. Soil-strain compatibility: the key to effective use of arbuscular mycorrhizal inoculants? | SpringerLink. 2011;21:183-193.
Wendland-Ferreira A. Comunicación personal EMBRAPA [Internet]. 2020 [19/07/2022]. Available from: https://www.embrapa.br/agencia-de-informacao-tecnologica/inicial
Fernández F, Dell’Amico J, Pérez Y. Inoculante micorrizógeno líquido. Oficina Cubana de la Propiedad Industrial. 2009;23479.
Pozo MJ, Cordier C, Dumas‐Gaudot E, Gianinazzi S, Barea JM, Azcón‐Aguilar C. Localized versus systemic effect of arbuscular mycorrhizal fungi on defence responses to Phytophthora infection in tomato plants. Journal of Experimental Botany. 2002;53(368):525-34. doi:10.1093/jexbot/53.368.525
Vierheilig H, Schweiger P, Brundrett M. An overview of methods for the detection and observation of arbuscular mycorrhizal fungi in roots†. Physiologia Plantarum. 2005;125(4):393-404. doi:https://doi.org/10.1111/j.1399-3054.2005.00564.x
Giovannetti M, Mosse B. An Evaluation of Techniques for Measuring Vesicular Arbuscular Mycorrhizal Infection in Roots. The New Phytologist. 1980;84(3):489-500.
Trouvelot A, Kough JL, Gianinazzi-Pearson V. Mesure du taux de mycorhization VA d’un système radiculaire. Recherche de méthode d’estimation ayant une signification fonctionnelle. In 1986 [cited 11/07/2022]. p. 217-21. Available from: http://pascal-francis.inist.fr/vibad/index.php?action=getRecordDetail&idt=8758731
Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry. 1976;72(1):248-54. doi:10.1016/0003-2697(76)90527-3
Heitefuß R, Williams PH. Oxidative enzymes. In: HEITEFUSS, R., and P. H. WILLIAMS. In: Physiological Plant Pathology [Internet]. New York: Springer Science & Business Media; 2012. p. 617-27. Available from: https://books.google.es/books?hl=es&lr=&id=hfLuCAAAQBAJ&oi=fnd&pg=PA1&dq=Oxidative+enzymes.+In:+HEITEFUSS,+R.,+and+P.+H.+WILLIAMS+(eds.).+Physiological+Plant+Pathology.+Encyclopedia+of+Plant+Pathology&ots=fu0GAetnMC&sig=pBM1iYFG95tlKKzYoQXrcb4q7UQ#v=onepage&q&f=false
Sun-Xue G, Tang M. Comparison of four routinely used methods for assessing root colonization by arbuscular mycorrhizal fungi. Botany. 2012;90:1073-83. doi:10.1139/b2012-084
Rivera R, González PJ, Hernández A, Martín G, Ruiz L, Fernández K, et al. La importancia del ambiente edáfico y del pH sobre la efectividad y la recomendación de cepas eficientes de HMA para la inoculación de los cultivos. In: VIII Congreso de la Sociedad Cubana de la Ciencia del Suelo. 2015.
Kanwal S, Bano A, Malik RN. Role of arbuscular mycorrhizal fungi in phytoremediation of heavy metals and effects on growth and biochemical activities of wheat (Triticum aestivum L.) plants in Zn contaminated soils. African Journal of Biotechnology. 2016;15(20):872-83. doi:10.4314/ajb.v15i20
Chaudhary VB, O’Dell TE, Rillig MC, Johnson NC. Multiscale patterns of arbuscular mycorrhizal fungal abundance and diversity in semiarid shrublands. Fungal Ecology. 2014;12:32-43. doi:10.1016/j.funeco.2014.06.003
Alguacil M del M, Torres MP, Montesinos-Navarro A, Roldán A. Soil Characteristics Driving Arbuscular Mycorrhizal Fungal Communities in Semiarid Mediterranean Soils. Applied and Environmental Microbiology. 2016;82(11):3348-56. doi:10.1128/AEM.03982-15
Wild A. Condiciones del suelo y desarrollo de las plantas según Russell. In: La población microbiana del suelo. Mur di-Prensa. Madrid, España: Ed. Mundi-Prensa; 1992. p. 471-94.
Igiehon NO, Babalola OO. Below-ground-above-ground Plant-microbial Interactions: Focusing on Soybean, Rhizobacteria and Mycorrhizal Fungi. The Open Microbiology Journal. 2018;12:261-79. doi:10.2174/1874285801812010261
Jamiołkowska A, Księżniak A, Gałązka A, Hetman B, Kopacki M, Skwaryło-Bednarz B. Impact of abiotic factors on development of the community of arbuscular mycorrhizal fungi in the soil: a review. International Agrophysics. 2018;32(1):133-40. doi:10.1515/intag-2016-0090
Bücking H, Kafle A. Role of Arbuscular Mycorrhizal Fungi in the Nitrogen Uptake of Plants: Current Knowledge and Research Gaps. Agronomy. 2015;5(4):587-612. doi:10.3390/agronomy5040587
Choudhary KK, Chaudhary N, Agrawal S, Agrawal M. Reactive Oxygen Species in Plants: Boon Or Bane - Revisiting the Role of ROS. In: Reactive oxygen species: generation, damage and quenching in plants during stress. In: Singh V.P. Wiley, Hoboken. NJ, USA: John Wiley & Sons; 2017.
Ouzounidou G, Skiada V, Papadopoulou KK, Stamatis N, Kavvadias V, Eleftheriadis E, et al. Effects of soil pH and arbuscular mycorrhiza (AM) inoculation on growth and chemical composition of chia (Salvia hispanica L.) leaves. Brazilian Journal of Botany. 2015;38(3):487-95. doi:10.1007/s40415-015-0166-6
Öpik M, Zobel M, Cantero JJ, Davison J, Facelli JM, Hiiesalu I, et al. Global sampling of plant roots expands the described molecular diversity of arbuscular mycorrhizal fungi. Mycorrhiza. 2013;23(5):411-30. doi:10.1007/s00572-013-0482-2
Gilbert L, Johnson D. Chapter Four - Plant-Plant Communication Through Common Mycorrhizal Networks. In: Becard G, editor. Advances in Botanical Research [Internet]. Academic Press; 2017 [cited 19/07/2022]. p. 83-97. (How Plants Communicate with their Biotic Environment; vol. 82). doi:10.1016/bs.abr.2016.09.001
Lambers H, Albornoz F, Kotula L, Laliberté E, Ranathunge K, Teste FP, et al. How belowground interactions contribute to the coexistence of mycorrhizal and non-mycorrhizal species in severely phosphorus-impoverished hyperdiverse ecosystems. Plant and Soil. 2018;424(1):11-33. doi:10.1007/s11104-017-3427-2
Notas de autor
*Autor para correspondencia: eduardo@inca.edu.cu
