Artículo original
Received: 20 January 2021
Accepted: 14 October 2021
RESUMEN: Esta investigación se desarrolló con el objetivo de evaluar la respuesta a la inoculación de hongos micorrícicos arbusculares (HMA) en diferentes líneas de trigo de primavera, en condiciones controladas. Se utilizaron semillas de cinco líneas de trigo (Triticum durum L.) de primavera (AW-774, AC Carberry, HY-162, Major y AAC Scotia), con un 98 % de germinación, que se desinfectaron antes de la siembra. Se utilizó la cepa de HMA INCAM - 4: Glomus cubense (en formulación sólida y líquida), el inoculante comercial canadiense MYKE®PRO: Rhizoglomus irregulare y un control sin inoculación. Los tratamientos se distribuyeron con un arreglo de parcelas divididas bajo un diseño completamente aleatorizado, siendo la parcela principal la inoculación del HMA y como sub-parcelas las cinco líneas de trigo de primavera. Las evaluaciones se realizaron a los 120 días después de la siembra y se determinaron variables relacionadas con el funcionamiento micorrícico (frecuencia e intensidad de la colonización), con el crecimiento y desarrollo de las plantas y el rendimiento del cultivo. Los resultados mostraron un efecto positivo de la inoculación de Glomus cubense, con ambas formulaciones (sólido y líquido). También, se observó una respuesta diferencial de las líneas de trigo de primavera a la inoculación de HMA. Las líneas Major y AW-774, mostraron incrementos significativos en las variables estudiadas, comparadas con el resto.
Palabras clave: Cereal, micorrizas, rendimiento.
ABSTRACT: With the aim to evaluate the response to arbuscular mycorrhizal fungi inoculation in different lines of spring wheat this research was developed under controlled conditions. Seeds from five spring wheat (Triticum durum L.) lines (AW-774, AC Carberry, HY-162, Major and AAC Scotia), with 98 % germination, were used and disinfected before sowing. The INCAM-4 strain: Glomus cubense (in solid and liquid formulation), the Canadian commercial inoculant MYKE®PRO (Rhizoglomus irregulare) and a control without inoculation were used. Treatments were distributed with an arrangement of divided plots under a completely randomized design, the main plot being the inoculation of AMF and the five lines of spring wheat as sub-plot. The evaluations were carried out at 120 days after sowing and variables related to mycorrhizal functioning (frequency and intensity of colonization), with the growth and development of the plants and the crop yield were determined. The results showed a positive effect of Glomus cubense inoculation in both formulations (solid and liquid). A differential response in AMF inoculation was observed among spring wheat lines. The Major and AW-774 lines showed significant increases in the variables studied compared to the rest.
Key words: Cereal, mycorrhiza, yield.
INTRODUCCIÓN
La agricultura actual requiere nuevos enfoques en materia de sostenibilidad y sustentabilidad, avalados por la investigación, la innovación y la tecnología, con vistas a garantizar la seguridad alimentaria (1). En este contexto, los hongos micorrícicos arbusculares (HMA) representan un grupo de microorganismos edáficos que establecen simbiosis con numerosas especies vegetales de interés agrícola (2).
Dentro de los principales beneficios de esta simbiosis se destacan: los efectos directos en la nutrición mineral; especialmente en la absorción de macro y micronutrientes (3, 4), la inducción de tolerancia frente a condiciones de estrés biótico (ej. patógenos) (5) y abiótico (ej. sequía y salinidad) (6, 7), su participación en los procesos de fitorremediación (8) y su contribución en la estabilidad de los agregados del suelo (9).
Especial interés muestra la simbiosis que se establece entre los HMA y los cereales (10,11), específicamente con el trigo (Triticum spp.), cultivo que representa el tercer cereal de mayor producción a escala mundial, por ser una importante fuente de proteína vegetal, cultivándose en diversas condiciones edafoclimáticas (12).
Los cultivares de trigo de primavera se diferencian de los cultivares de invierno por presentar un mayor contenido de proteína, dureza del grano y mejores propiedades fisicoquímicas de la masa, lo que favorece su proceso de molinado y le confiere a su harina una calidad superior (13). Algunos estudios han demostrado la efectividad de la simbiosis micorrízica en plantas de trigo, destacando, que una mejor nutrición en la planta incrementa su rendimiento; por lo que se plantea que los HMA pueden formar parte de las estrategias que conduzcan a una mejor seguridad alimentaria (14).
Atendiendo estos criterios, el objetivo de este estudio fue evaluar la respuesta a la inoculación de hongos micorrízicos arbusculares en diferentes lineas de trigo de primavera, en condiciones controladas.
MATERIALES Y MÉTODOS
Características generales del experimento
El experimento se condujo en condiciones controladas de invernaderos del Instituto Agrícola de Ottawa, Canadá. Los tratamientos se distribuyeron con un arreglo de parcelas divididas bajo un diseño completamente aleatorizado, siendo la parcela principal la inoculación del HMA y como sub-parcelas las cinco líneas de trigo de primavera. Se empleó una mezcla de sustrato orgánico comercial: Lambert (musgo de turba de Sphagnum canadiense con pH = 7,1) y arena lavable, en proporción 1:1 (v/v), el cual se esterilizó en autoclave a 121 ºC durante dos horas, en ciclos de tres días continuos. Se sembraron seis semillas por maceta y a los siete días de la emergencia de las plantas, se realizó un raleo y se dejaron tres plantas por cada una.
Las plantas se desarrollaron en condiciones controladas con una temperatura promedio que osciló entre los 20 - 22 °C, un 80 % de humedad relativa y fotoperiodo ajustado a 16 horas luz / 8 horas oscuridad. Se aplicó urea a razón de 5 g por maceta, la cual se fraccionó en dos momentos del ciclo del cultivo: 3 g a los 15 días posteriores a la siembra y el resto 30 días después, de acuerdo a las normas establecidas para estas líneas de trigo en invernadero (15). Se realizaron seis observaciones por tratamiento para un total de 120 macetas.
Descripción del material vegetal
El material vegetal consistió en semillas de cinco líneas de trigo (Triticum durum L.) de primavera (AW-774, AC Carberry, HY-162, Major y AAC Scotia), con un 98 % de germinación y certificadas por la oficina de registro de variedades de la Agencia de Inspección Alimentaria de Canadá (15). Las semillas se sembraron en macetas de 5 kg de capacidad (0,22 m de altura y 0,24 m de diámetro superior).
Descripción del material fúngico
Se utilizó la cepa INCAM - 4: Glomus cubense (Y. Rodr. & Dalpé) (16), en formulación sólida y líquida, procedente de la colección del Instituto Nacional de Ciencias Agrícolas (INCA) de Cuba y registrada en el Herbario Nacional Micológico de Canadá, Ottawa, con código DAOM 241198, además del inoculante comercial canadiense MYKE®PRO (Rhizoglomus irregulare) (Blaszk., Wubet, Renker & Buscot) (17).
La aplicación de la formulación sólida (FS) de G. cubense, con una concentración promedio de 20 esporas por gramo de inoculante, consistió en 1 g por maceta, mientras que en el caso del producto comercial MYKE®PRO, con una pureza de 1 propágulo por gramo de inoculante, se inocularon 20 gramos por maceta. Ambas aplicaciones se realizaron en el momento de la siembra.
Para la aplicación del inoculante en formulación líquida (FL) se empleó una bomba hidráulica de inyección dosificadora para productos solubles en agua (ECOFERTIC), a una presión de 0,15 MPa y con una entrega de 5 mL por maceta en cada riego. La bomba se ajustó al sistema de riego por goteo con mangueras como líneas distribuidoras y goteros espaciados a 30 cm, con salida para cuatro macetas. Se realizó una única aplicación de esta formulación en el momento de la siembra, a la concentración de 20 esporas por mL, en un volumen final de 150 mL del producto.
En los tratamientos inoculados con la formulación sólida (FS) de G. cubense, el producto comercial MYKE®PRO y el control, el riego se realizó de forma manual, a la frecuencia y el volumen de agua empleada en el tratamiento inoculado mediante el riego por goteo. En el caso del tratamiento inoculado con la formulación líquida, el riego se realizó mediante el sistema automatizado. En ambos casos, el riego estuvo en correspondencia con la fenología de las líneas de trigo de primavera (15).
Evaluaciones y Análisis estadístico
El experimento se extendió por 120 días después de la siembra (DDS) de las semillas y se evaluaron los siguientes indicadores:
-
Frecuencia e intensidad de colonización fúngica (%): se tomaron 250 mg de raíces secundarias, en cada muestra, las cuales se lavaron cuidadosamente, se secaron en una estufa a 70 ºC hasta masa constante, se tiñeron, clarificaron (18) y cuantificaron (19).
-
Crecimiento y desarrollo de las plantas: Se determinó la longitud de la espiga (cm), la masa fresca y seca de la parte aérea y de la raíz (g) y el volumen de la raíz (m3). La masa fresca se determinó por pesada, en balanza técnica digital (Acom JW-1, nivel de precisión 0,1 g), mientras que la masa seca se determinó luego de secar las muestras a 70 ºC en la estufa, hasta masa constante. Las raíces se lavaron con abundante agua para eliminar las partículas de suelo. Posteriormente, se colocaron en un escáner y con el programa WinRhizo-Pro para Windows se determinó el volumen de raíz.
-
Rendimiento del cultivo: Se determinó el número de espigas por planta, masa promedio de los granos (g) y rendimiento del cultivo (g por m2).
Se verificó el cumplimiento de los supuestos de normalidad y homogeneidad de varianza. El procesamiento estadístico de los datos se realizó mediante un análisis multivariado de componentes principales y conglomerados jerárquico de ligamento completo. El agrupamiento obtenido a partir de estos análisis fue verificado usando un Análisis Factorial Discriminante. Se empleó el paquete estadístico IBM SPSS versión 19.0.
RESULTADOS
El análisis de Componentes Principales permitió identificar cuáles de las variables evaluadas estaban más relacionadas con las diferencias observadas, no solo en el crecimiento y desarrollo de las líneas de trigo, sino también en la respuesta de éstas a la inoculación con HMA. Como resultado del análisis se encontraron dos componentes que demostraron una varianza acumulada de 85,51 % (Tabla 1).
Representación de los valores propios y la varianza explicada para el método de Componentes principales

En la Tabla 2 se presentan las variables que mostraron mayores coeficientes de correlación con ambas componentes.
Correlaciones entre las variables iniciales y las dos primeras componentes del análisis de componentes principales

En el caso de la componente 1, las variables de mayor incidencia fueron las relacionadas con el crecimiento de las plantas (longitud de la espiga, masa seca y fresca aérea y de la raíz y el volumen de raíz), el rendimiento del cultivo (número de espigas por planta y rendimiento) y la frecuencia de colonización; mientras que con la componente 2 se relacionó la intensidad de colonización de los HMA.
En la Figura 1 se muestra el agrupamiento de los tratamientos, tras la aplicación de ambos métodos multivariados (Componentes Principales y Conglomerado Jerárquico de Ligamento Completo).
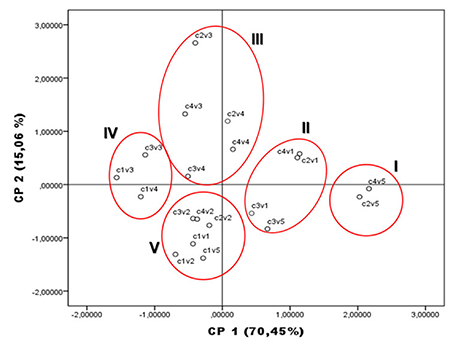
Figura 1
Distribución de los tratamientos, según el análisis de Componentes Principales y de Conglomerado Jerárquico de Ligamento Completo, en los indicadores evaluados
c1: Control; c2: Glomus cubense (líquido); c3: Rhizoglomus irregulare; c4: Glomus cubense (sólido);V1: AW-774; V2: AAC Scotia; V3: HY-162; V4: AC Carberry; V5: Major. Matriz de las componentes principales 1 y 2 (CP1 y CP2). Agrupamiento: I (c4V5, c2V5); II (c2V1, c3V1, c3V5, c4V1); III (c2V3, c2V4, c4V3, c4V4); IV (c1V3, c1V4, c3V3, c3V4); V (c1V1, c1V2, c1V5, c2V2, c3V2, c4V2)
El agrupamiento de los tratamientos fue el resultado del orden de su aparición a partir del análisis de Conglomerado Jerárquico de Ligamento Completo (Figura 2) realizado. Para la distribución de los tratamientos se tuvo en cuenta las variables de mayor correlación en la componente 1.
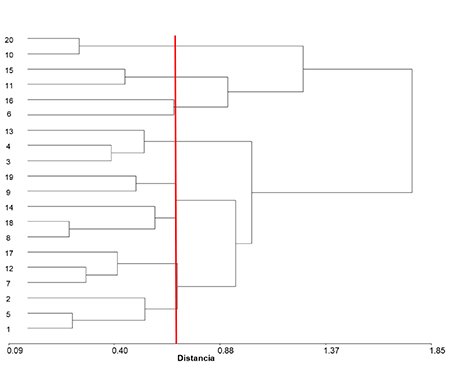
Figura 2
Agrupamiento de los tratamientos con la aplicación del método multivariado Conglomerado Jerárquico de Ligamento Completo
Línea vertical (color rojo) en el gráfico indica la distancia a la cual se estableció el agrupamiento. 1: C1V1, 2: C1V2, 3: C1V3, 4: C1V4, 5: C1V5, 6: C2V1, 7: C2V2, 8: C2V3, 9: C2V4, 10: C2V5, 11: C3V1, 12: C3V2, 13: C3V3, 14: C3V4, 15: C3V5, 16: C4V1, 17: C4V2, 18: C4V3, 19: C4V4, 20: C4V5. C1: Control; C2: Glomus cubense (líquido); C3: Rhizoglomus irregulare; C4: Glomus cubense (sólido); V1: AW-774; V2: AAC Scotia; V3: HY-162; V4: AC Carberry; V5: Major
El grupo I estuvo representado por los tratamientos inoculados por G. cubense, en ambas formulaciones, en la línea de trigo Major. Cercano a él se ubicó el grupo II, identificado por las combinaciones de G. cubense (sólido y líquido) y R. irregulare en las líneas AW-774 y Major. El grupo III estuvo conformado por los tratamientos inoculados por G. cubense (sólido y líquido) y R. irregulare en las líneas de trigo HY-162 y AC Carberry. Un poco distante se ubicó el grupo IV, con los tratamientos control y el inoculado con R. irregulare en las mismas líneas del agrupamiento anterior. Finalmente, el grupo V estuvo integrado por el tratamiento control en las líneas AW-774, AAC Scotia y Major y la inoculación de G. cubense (sólido y líquido) y R. irregulare en la línea AAC Scotia.
El análisis multivariado permitió encontrar, de forma integral, un efecto positivo de la inoculación micorrízica en las diferentes líneas de trigo de primavera, a partir de incrementos significativos en los tratamientos inoculados con relación al control absoluto, destacándose los tratamientos con G. cubense, en ambas formulaciones, en la línea Major (grupo I) con los mejores comportamientos.
Con el análisis factorial discriminante se demostró un 100 % de coincidencia entre los grupos que se formaron. En la Tabla 3 se muestran las medias de las variables evaluadas por cada grupo conformado. Se observó que los valores superiores de los indicadores evaluados se ubicaron en el grupo I, con una tendencia a la disminución en los grupos IV y III, mientras que el grupo V estuvo representado por los tratamientos con valores inferiores.
Medias de las variables por cada grupo formado a partir del análisis factorial discriminante

DISCUSIÓN
Aunque algunos estudios se refieren al carácter inespecífico de la simbiosis micorrízica por la diversidad de familias del reino vegetal, al ser susceptibles de ser colonizadas (20), cada especie vegetal, e incluso cultivares o variedades dentro de una misma especie, tienen un grado de dependencia micorrízica diferente (21).
En apoyo a esta teoría, algunos autores evaluaron la factibilidad de un sistema de cultivo autotrófico en la producción de esporas y su capacidad para reproducir el ciclo de vida del hongo en condiciones in vitro en diferentes cultivares europeos y andinos de papa (Solanum tuberosum L.) y encontraron una respuesta diferencial entre ellos, lo cual pudo estar relacionado con caracteres fisiológicos y genéticos de cada cultivar que determinaron grados de dependencia diferentes (22).
De igual manera, en otras investigaciones se evaluó el efecto de la inoculación de R. irregulare en 5 cultivares de trigo y encontraron una dependencia micorrízica diferente en cada cultivar, con porcentajes de colonización variables que se correlacionaron con el resto de los indicadores evaluados (biomasa seca, masa de los granos y contenido de fósforo en el grano) (23).
Los elementos descritos anteriormente, de conjunto con el comportamiento diferencial antes mencionado en las líneas de trigo evaluadas en este estudio, confirman que, a pesar que los HMA desarrollan asociaciones no específicas con sus plantas hospedantes, el grado de dependencia micorrízica suele variar para algunas combinaciones planta-hongo.
CONCLUSIONES
Los tratamientos inoculados con G. cubense, independientemente del tipo de formulación empleada, describieron un comportamiento superior al observado cuando se aplicó R. irregulare, en todas las variedades evaluadas. De igual forma, se observó que las líneas de trigo de primavera presentaron un grado de respuesta diferente a la inoculación, destacándose las líneas Major y AW-774 con valores superiores en cuanto al rendimiento, específicamente.
BIBLIOGRAFÍA
Okur N. A Review: Bio-Fertilizers- Power of Beneficial Microorganisms in Soils. Biomedical Journal of Scientific and Technical Research. 2018;4(4):4028-4029. DOI:10.26717/BJSTR.2018.04.001076.
Quinones-Aguilar EE, Hernández LV, López L, Rincon EG. Efectividad de hongos micorrízicos arbusculares nativos de rizósfera de Agave como promotores de crecimiento de papaya. Terra Latinoamericana. 2019;37(2):163-174. DOI: 10.28940/terra.v37i2.397.
Cavagnaro TR, Bender SF, Asghari HR, van der Heijden MGA. The Role of Arbuscular Mycorrhizas in Reducing Soil Nutrient Loss. Trends in Plant Science. 2015;20:283-290. DOI: 10.1016/j.tplants.2015.03.004 PMID: 25840500
Zhang L, Xu M, Liu Y, Zhang F, Hodge A, Feng G. Carbon and phosphorus exchange may enable cooperation between an arbuscular mycorrhizal fungus and a phosphate-solubilizing bacterium. New Phytologist. 2016;210(3):1022-1032. DOI: 10.1111/nph.13838
Lenoir I, Fontaine J, Lounès-Hadj SA. Arbuscular mycorrhizal fungal responses to abiotic stresses: A review. Phytochemistry. 2016;23:4-15. DOI: 10.1016/j.phytochem.2016.01.002
Augé RM, Toler HD, Saxton AM. Arbuscular mycorrhizal symbiosis alters stomatal conductance of host plants more under drought than under amply watered conditions: a meta-analysis. Mycorrhiza. 2015;25(1):13-24. DOI: 10.1007/s00572-014-0585-4
Sánchez-Romera B, Ruiz-Lozano JM, Zamarreño AM, García-Mina JM, Aroca R. Arbuscular mycorrhizal symbiosis and methyl jasmonate avoid the inhibition of root hydraulic conductivity caused by drought. Mycorrhiza. 2016;26(2):111-22. DOI: 10.1007/s00572-015-0650-7.
Kanwal S, Bano A, Malik RN. Role of arbuscular mycorrhizal fungi in phytoremediation of heavy metals and effects on growth and biochemical activities of wheat (Triticum aestivum L.) plants in Zn contaminated soils. African Journal of Biotechnology. 2016;15(20):872-883. DOI: 10.5897/AJB2016.15292.
Qiang-Sheng W, Srivastava AK, Ming-Qin C, Wang J. Mycorrhizal function on soil aggregate stability in root zone and root-free hyphae zone of trifoliate orange. Archives of Agronomy and Soil Science. 2015;61(6):813-825. DOI: 10.1080/03650340.2014.952226.
Bernaola L, Cange G, Way MO, Gore J, Hardke J, Stout M. Natural colonization of rice by arbuscular mycorrhizal fungi in different production areas. Rice Science. 2018;25(3):169-174. DOI: 10.1016/j.rsci.2018.02.006.
Campo S, Martín-Cardoso H, Olivé M, Pla E, Catala-Forner M, Martínez-Eixarch M, San Segundo B. Efecto de la colonización de raíces por hongos micorrízicos arbusculares sobre el crecimiento, la productividad y la resistencia a la explosión en el arroz. Arroz. 2020;13(42). DOI: 10.1186/s12284-020-00402-7.
Lehnert H, Serfling A, Friedt W, Ordon F. Genome-Wide association studies reveal genomic regions associated with the response of wheat (Triticum aestivum L.) to mycorrhizae under drought stress conditions. Frontiers in Plant Science. 2018;9:1728. DOI: 10.3389/fpls.2018.01728.
Ahmed M, Fayyaz-ul-H. Response of Spring Wheat (Triticum aestivum L.) Quality Traits and Yield to Sowing Date. PLoS ONE. 2015;10(4):e0126097. DOI:org/10.1371/journal.pone.0126097
Ercoli L, Schüßler A, Arduini I, Pellegrino E. Strong increase of durum wheat iron and zinc content by field-inoculation with arbuscular mycorrhizal fungi at different soil nitrogen availabilities. Plant and Soil. 2017:419(1):153-167. DOI:org/10.1007/s11104-017-3319-5
Agri-Food Canada. 2012. Crop profile for Spring Wheat in Canada. Catalogue No. A118-10/30-2012E. Agriculture and Agri-Food Canada (Editor), 2012; 67 p.
Rodríguez Y, Dalpé Y, Séguin S, Fernández K, Fernández F, Rivera RA. Glomus cubense sp. nov., an arbuscular mycorrhizal fungus from Cuba. Mycotaxon. 2011;118:337-347. DOI: 10.5248/118.337.
Schüßler A, Walker C. The Glomeromycota: A species list with new families and new genera. Create Space Independent Publishing Platform (Editor). 2011; 57 p.
Rodríguez Y, Arias L, Medina A, Mujica Y, Medina LR, Fernández K, Mena A. Alternativa de la técnica de tinción para determinar la colonización micorrízica. Cultivos Tropicales. 2015;36(2):18-21.
Trouvelot A, Kough J, Gianinazzi-Pearson V. Mesure du Taux de Mycorhization VA d'un Systeme Radiculaire. Recherche de Methodes d'Estimation ayantune Signification Fonctionnelle. Proceedings of the 1st European Symposium on Mycorrhizae: Physiological and Genetical Aspects of Mycorrhizae, Dijón. (Gianinazzi-Pearson, V.; Gianinazzi, S. Eds.). INRA, Paris. 1986; p. 217-222.
Bonfante P, Requena N. Dating in the dark: How roots respond to fungal signals to establish arbuscular mycorrhizal symbiosis. Current Opinion in Plant Biology. 2011;14(4):451-7. DOI: 10.1016/j.pbi.2011.03.014.
Lin G, McCormack ML, Guo D. Arbuscular mycorrhizal fungal effects on plant competition and community structure. Journal of Ecology, 2015; 103(5):1224-1232. DOI: 10.1111/1365-2745.12429.
Voets L, Dupré de Boulois H, Renard L, Strullu DG, Declerck S. Development of an autotrophic culture system for the in vitro mycorrhization of potato plantlets. FEMS Microbiology Letters. 2005;248(1):111-118. DOI: 10.1016/j.femsle.2005.05.025.
Sawers RJH, Ramírez-Flores MR, Olalde-Portugal V, Paszkowski U. The Impact of Domestication and Crop Improvement on Arbuscular Mycorrhizal Symbiosis in Cereals: Insights from Genetics and Genomics. New Phytologist. 2018;220:1135-1140. DOI: 10.1111/nph.15152 PMID: 29658105.
Author notes
*Autor para correspondencia: ymujica@inca.edu.cu
