Artículo original
Efecto de un fungicida sistémico en el establecimiento de Hongos Micorrizógenos Arbusculares en el cultivo de maíz (Zea mays L.)
Effect of a systemic fungicide on the establishment of Arbuscular Mycorrhizogenic Fungi in maize (Zea mays L.)
Efecto de un fungicida sistémico en el establecimiento de Hongos Micorrizógenos Arbusculares en el cultivo de maíz (Zea mays L.)
Cultivos Tropicales, vol. 43, no. 4, e06, 2022
Ediciones INCA
Received: 19 October 2020
Accepted: 25 May 2021
RESUMEN: Los fungicidas no solo afectan a los hongos patógenos, sino también a otros hongos, incluidos aquellos que son beneficiosos para el crecimiento de las plantas, como los hongos micorrízicos arbusculares. El objetivo del presente trabajo fue evaluar el efecto de un fungicida sistémico comercial en la colonización de hongos micorrizógenos arbusculares, inoculados en el cultivo del maíz, en condiciones semicontroladas. Para ello, se inocularon plantas de maíz con las cepas Rhizophagus irregularis INCAM 11, Glomus cubense INCAM 4 y con un conglomerado de diferentes especies de hongos micorrízicos arbusculares, en presencia o no del fungicida sistémico. A los 54 días de la inoculación se determinó la frecuencia de colonización y la densidad visual de los hongos micorrízicos empleados. Además, se determinó la longitud de la raíz y la masa fresca y seca total de las plantas de maíz. El conglomerado de diferentes especies de hongos micorrízicos arbusculares, junto al fungicida, presentó la mayor densidad visual. La presencia del fungicida incrementó la longitud radical y la masa fresca y seca total de las plantas control y las inoculadas con Glomus cubense INCAM 4. El efecto de la cepa Rhizophagus irregularis INCAM 11 en el crecimiento del maíz no se afectó con el empleo del fungicida sistémico.
Palabras clave: Longitud de la raíz, micorriza y pesticida.
ABSTRACT: Fungicides not only affect the pathogens fungi, but also to others, including those that are beneficial for plant growth, such as arbuscular mycorrhizal fungi. The aim of the present work was to evaluate the effect of a commercial systemic fungicide on the colonization of arbuscular mycorrhizal fungi, inoculated in corn crop, under semi-controlled conditions. Corn plants were inoculated with strains Rhizophagus irregularis INCAM 11, Glomus cubense INCAM 4 and with a conglomerate of different species of arbuscular mycorrhizal fungi, with and without of a systemic fungicide. Colonization frequency and visual density of mycorrhizal fungi were determined at 54 days after inoculation. In addition, the root length, total fresh weight and total dry weight of corn plants were determined. The conglomerate of different species of arbuscular mycorrhizal fungi with fungicide had the highest visual density. The presence of the fungicide increased the root length, total fresh weight and total dry weight of the control plants and those inoculated with Glomus cubense INCAM 4. The effect of strain Rhizophagus irregularis INCAM 11 on the corn growth was not affected for systemic fungicide.
Key words: Mycorrhiza, pesticide, root length.
INTRODUCCIÓN
Los hongos micorrizógenos arbusculares (HMA) (Glomeromycota) son parte integral de numerosos ecosistemas y se consideran particularmente ventajosos, debido a que se asocian a la mayoría de las plantas vasculares estudiadas (1,2). Dichos hongos son biótrofos obligados y colonizan las raíces de sus plantas hospedantes obteniendo azúcares. En cambio, las plantas hospedantes reciben los nutrientes minerales y el agua, absorbidos y transportados a través de una red fina de hifas extrarradicales extendidas, desde las raíces hasta el suelo circundante (3).
La utilización de los HMA resulta factible para cualquier sistema de producción agrícola, debido a las funciones que realizan una vez que se asocian con las plantas. Entre ellas se encuentra el incremento de la absorción de nutrientes minerales y agua, a partir de un aumento en el volumen de suelo explorado; confieren mayor resistencia de las plantas a las toxinas y al ataque de patógenos y el incremento de la translocación y solubilización de elementos esenciales (2,4). Los HMA contribuyen a disminuir los efectos adversos del estrés abiótico, como la presencia de metales pesados y la salinidad de los suelos, así como del estrés biótico, causado por numerosos patógenos (5,6).
Por otra parte, en los sistemas de cultivo actuales, se utilizan fungicidas para controlar o eliminar los fitopatógenos fúngicos. Sin embargo, estos productos también podrían afectar la sobrevivencia de microorganismos autóctonos, incluidos aquellos que son beneficiosos para el crecimiento de las plantas, como los HMA. Por lo tanto, el efecto esperado de la micorrización en el crecimiento y el desarrollo de las plantas hospedantes, puede afectarse negativamente por el uso de fungicidas, en los sistemas agrícolas (7).
Los fungicidas sistémicos son aquellos que, al ser aplicados al suelo, pueden ser absorbidos por las raíces y transferidos a otras partes de la planta. Son sustancias persistentes y su acción sobre los hongos micorrízicos puede influir negativamente en el desarrollo de sus estructuras vegetativas y reproductivas, por estar diseñados para destruir las quitinas fúngicas, así como otras proteínas y enzimas específicas producidas por estos hongos (8). Esto inhibe o retrasa la simbiosis entre estos hongos y las plantas, disminuyendo los efectos positivos que los HMA le reportan a la planta, como la absorción de fósforo (8). En Cuba no existen evidencias documentadas que muestren el efecto de fungicidas sistémicos en la simbiosis HMA-planta.
Teniendo en cuenta los aspectos anteriormente planteados el objetivo del presente estudio fue evaluar el efecto de un fungicida sistémico comercial en la colonización de HMA inoculados en el cultivo del maíz, en condiciones semicontroladas.
MATERIALES Y MÉTODOS
Los experimentos se realizaron en el Instituto Nacional de Ciencias Agrícolas (INCA). Se emplearon semillas de maíz cultivar “Raúl Hernández”, obtenido en el Departamento de Genética y Mejoramiento Vegetal del INCA. El experimento se desarrolló en macetas de 5 kg de capacidad, con un sustrato de suelo Pardo Mullido no estéril. El suelo presentó una concentración de 3-5 esporas de HMA residentes por g-1 de suelo. Algunas características químicas del sustrato empleado se muestran en la Tabla 1.

pH: Potenciometría; Materia Orgánica (MO): Walkley Black; Cationes intercambiables (Ca2+ y Mg2+): Complejometría
Se sembraron cinco semillas de maíz por maceta y se inocularon mediante la técnica de recubrimiento de la semilla (9). Se emplearon las cepas de HMA Rhizophagus irregularis (Blaszk., Wubet, Renker & Buscot) C. Walker & A. Schüßler (INCAM 11) y Glomus cubense Y. Rodr. & Dalpé (INCAM 4) (registrada en el Herbario Nacional Micológico de Canadá, Ottawa, con código DAOM 241198). Ambas cepas fúngicas pertenecen a la colección de hongos micorrízicos arbusculares del Instituto Nacional de Ciencias Agrícolas de Cuba. Además, se empleó un conglomerado de diferentes esporas de hongos residentes (RPR), aislados de la finca “La Fidelia”, perteneciente a la CCS Oscar Núñez Gil del Municipio Los Palacios. Los aislados se obtuvieron de un suelo Pardo mullido Carbonatado de Los Palacios que también forma parte del cepario del INCA (10). Los inóculos anteriormente mencionados poseían una concentración de 25 esporas g-1 de suelo fresco.
Se empleó además el fungicida sistémico comercial Previcur energy 840 sl (F), el cual está compuesto por un 16 % de ingredientes inertes y como componentes activos presenta un 53 % de propil 3- (dimetilamino) propil carbamato y un 31 % de etilhidrógeno fosfonato. El experimento se condujo utilizando un diseño completamente aleatorizado con arreglo bifactorial. Los factores estudiados fueron las cepas de HMA (factor 1) y la presencia o no del fungicida (factor 2) y se establecieron los siguientes tratamientos, cada uno con siete réplicas (Tabla 2).

A los cinco días de la emergencia de las plántulas, se realizó un raleo y se mantuvo una plántula por maceta. Las plántulas se mantuvieron en condiciones semicontroladas de cultivo por 54 días, a 30 ℃, humedad relativa del 80 % y fotoperiodo natural. A los 15 días de la emergencia de las plantas, se aplicó el fungicida sistémico comercial Previcur energy 840 sl, a razón de 10 mL por maceta que presentaba una concentración del fungicida de 10 mg L-1.
A los 54 días de establecido el experimento, se determinó la densidad visual y la frecuencia de colonización, según lo descrito previamente en la literatura (11). Se determinaron variables que caracterizan el crecimiento de las plantas como la longitud de la raíz, la masa fresca total y la masa seca total de la planta. Para determinar la longitud radical, se empleó una regla graduada y se midió desde el ápice de la raíz hasta el inicio del tallo. La masa fresca total de las plantas se determinó en una balanza técnica (Sartorius), después de lavar y secar con papel de filtro las raíces y la parte aérea. Para determinar la masa seca total, las muestras se secaron en estufa a 75 ℃, durante tres días hasta obtener peso constante.
Los datos se analizaron a partir de un Análisis de varianza de clasificación doble. En el caso en que se encontraran diferencias significativas en los factores evaluados, se realizó un desdoblamiento de la interacción, fijándose uno de los factores, cepa (factor 1) o fungicida (factor 2). Para ello, se empleó una prueba de comparación de medias. Se utilizó el programa STATISTIC versión 21 para el procesamiento estadístico de los datos y el programa Microsoft Excel 2010 para su representación.
RESULTADOS
Como puede apreciarse en la Figura 1 A y B, las variables de frecuencia de colonización y densidad visual tuvieron un comportamiento diferente con relación a los tratamientos evaluados.
No se encontraron diferencias significativas en la frecuencia de colonización entre las plantas inoculadas con y sin el fungicida y las plantas controles. Tampoco se identificaron diferencias entre las plantas que no se trataron con el fungicida y aquellas que sí. Se exceptúa, el tratamiento con RPR y aquel donde se inoculó la cepa INCAM 11, ambos en presencia del fungicida, entre los cuales sí se observaron diferencias (Figura 1A).
Al analizar la densidad visual, ocurrió una disminución significativa de sus valores, en los tratamientos inoculados con INCAM 4 e INCAM 11 en presencia del fungicida, respecto a los tratamientos con estas cepas sin fungicida (Figura 1B). Sin embargo, las plantas inoculadas con RPR en presencia del fungicida, alcanzaron los mayores valores de densidad visual, con relación al resto de los tratamientos.
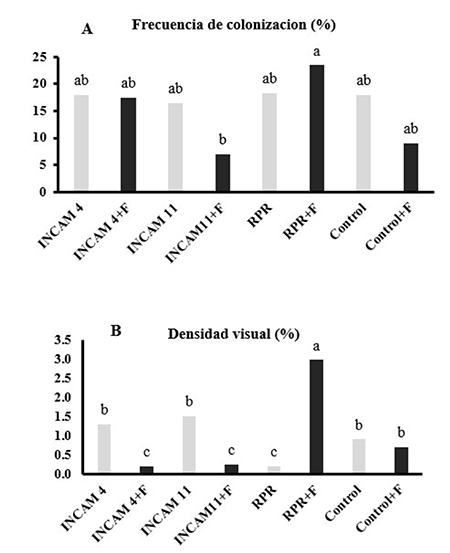
Figura 1
Valores de funcionamiento micorrízico evaluado a través de la frecuencia de colonización (A) y la densidad visual (B) en raíces de plantas de maíz, a los 54 días de inoculadas
INCAM 11, Rhizophagus irregularis; INCAM 4, Glomus cubense; RPR, conglomerado de hongos residentes, Pinar del Río; F, FungicidaMedias con letras iguales en cada barra no difieren significativamente para p≤0,05
Por otra parte, cuando se analizó el efecto de la inoculación y el empleo del fungicida se pudo apreciar que, en la mayor parte de los tratamientos, el empleo del fungicida, tanto en las plantas control como en las inoculadas, incrementó la longitud radical, la masa fresca y seca de las plantas de maíz (Figura 2 y 3 A, B).
Sin embargo, entre las plantas inoculadas con la cepa INCAM 11 no se observaron diferencias significativas en ninguna de las variables que se midieron, relacionadas con el crecimiento de las plantas de maíz. Tampoco se observaron diferencias significativas entre los dos grupos de plantas inoculadas con RPR en la masa fresca de las plantas.
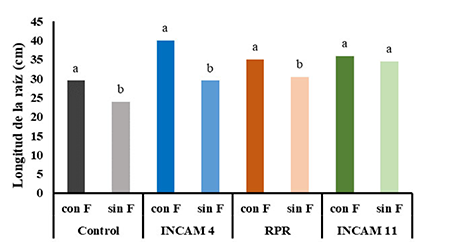
Figura 2
Longitud de la raíz de plantas de maíz inoculadas con cepas de hongos micorrízicos arbusculares con y sin la aplicación de fungicida, a los 54 días de inoculadas
Rhizophagus irregularis (INCAM 11), Glomus cubense (INCAM 4), conglomerado de hongos residentes, Pinar del Río (RPR), Fungicida (F)Letras iguales, para la misma cepa y control, no difieren para p≤0,05
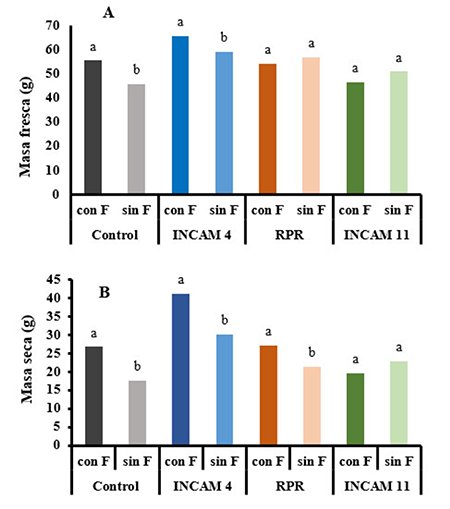
Figura 3
Masa fresca (A) y masa seca total (B), de plantas de maíz inoculadas con cepas de hongos micorrízicos arbusculares con y sin la aplicación de fungicida, a los 54 días de inoculadas
Rhizophagus irregularis (INCAM 11), Glomus cubense (INCAM 4), conglomerado de hongos residentes, Pinar del Río (RPR) Fungicida (F)Letras iguales para la misma cepa y control no difieren significativamente para p≤0,05
DISCUSIÓN
Se ha informado que el funcionamiento micorrízico y su acción sobre las plantas pueden afectarse por la aplicación de fungicidas, según las condiciones edáficas (6). Tales efectos dependen del ingrediente químico activo de estos productos y de la especie de hongo micorrizógeno (12). El incremento de la longitud de la raíz y masa fresca y seca de las plantas de maíz que se trataron con el fungicida, pueden atribuirse indirectamente a algunos factores. Entre ellos se encuentran el efecto del fungicida en la reducción de los exudados de la raíz y como un agente estresor de la planta huésped. Ambos eventos, favorecen el funcionamiento de la simbiosis micorrízica, con el consiguiente efecto en el crecimiento (13,14).
La diversidad de especies de HMA, presentes en el inoculante de Pinar del Río (RPR), puede ser un factor que explique los elevados valores de densidad visual y de número de esporas, al ser tratadas con el fungicida. En este sentido, se ha demostrado que una mayor diversidad de HMA tiene mayor tolerancia el estrés impuesto por los fungicidas, debido a que algunas especies son más resistentes a ciertos fungicidas que otras (15,16).
Se considera, que la densidad visual refleja con mayor claridad la ocupación del micelio y de hecho, la propia eficiencia simbiótica debido a que expresa la cantidad porcentual de estructuras fúngicas y de intercambio entre los simbiontes. Esto incluye los niveles de colonización y las estructuras de intercambio que se observan durante la evaluación (17). De esta manera, se puede deducir, que las especies presentes en el conglomerado RPR fueran las más eficientes en las condiciones en que se desempeñó el trabajo experimental, al presentar los mayores niveles de densidad visual.
Lo anteriormente planteado, se corresponde con estudios previos, los cuales informaron que la formación de vesículas de HMA en las raíces es significativamente mayor cuando se aplicaron fungicidas como Captan y Tebuconazol, en semillas de maíz (18). La aplicación del fungicida Metalaxilo incrementó la colonización de HMA de plantas de maíz y pueden estimular también el desarrollo del micelio fúngico, en plantas de Ananas comosus (piña) (14,18). Esto puede ocurrir por varias razones, primero una acción directa del fungicida sobre el HMA desencadenando una respuesta positiva, al estimular la producción de arbúsculos (estructura de intercambio del HMA) y también lo constituye la presencia de moléculas xenobióticas en la planta que pudiera inducir algún estrés que aprovecha oportunamente el HMA para expresar mayor colonización y densidad visual.
Otros autores plantean que el dominio de una especie de HMA en un ambiente específico se puede atribuir a diversos factores ambientales. Entre ellos se encuentran las propiedades fisicoquímicas del suelo, la morfología de la planta, la compatibilidad entre planta hospedante y especies de HMA y también la aplicación de los fungicidas (17). Por lo tanto, el empleo del fungicida sistémico, pudiera explicar los bajos valores de densidad visual encontrados en las plantas inoculadas con la cepa INCAM 4 y el fungicida. Estos hallazgos coinciden con algunos estudios, donde se corrobora que los fungicidas sistémicos pueden tener un efecto supresor sobre la actividad de los HMA e incluso en la fisiología de la interacción planta - HMA y en la absorción de nutrientes y agua (17,18).
Un estudio similar al anterior, se realizó con la aplicación del fungicida Benomyl, el cual provocó un efecto negativo sobre algunos HMA, específicamente sobre el crecimiento del micelio extrarradical, teniendo un efecto directo sobre la longitud del tubo germinativo (19). Del mismo modo, los fungicidas Bavistin y Mancozeb tuvieron un efecto negativo en la colonización de las raíces micorrizadas y el número de esporas (20).
El Bencimidazol, otro fungicida también muy empleado, ha demostrado ser perjudicial para las micorrizas y para la comunidad microbiológica del suelo (20). En algunos casos, su uso causa una reducción en el crecimiento de las plantas y la absorción de fósforo (14).
Los fungicidas Fenhexamida, Dicamba, Benomilo entre otros, probados en los estudios realizados por Lekberg y col. (14), redujeron significativamente la densidad y longitud del micelio extrarradical de la cepa de HMA Funneliformis mosseae. De igual modo su viabilidad y la capacidad de explorar la superficie de las membranas de las plantas se vieron negativamente afectadas especialmente por el Fenhexamida.
CONCLUSIONES
-
El fungicida sistémico Previcur energy 84 sl provocó un incremento en el crecimiento de las plantas de maíz.
-
Un caso interesante fue el efecto del fungicida en el funcionamiento micorrízico y en la promoción del crecimiento de las plantas de maíz que se inocularon con el conglomerado de especies residentes de HMA que se emplearon (PRP).
-
La adaptación de estas especies fúngicas a las condiciones edafoclimáticas establecidas y el efecto del fungicida al incremento de la densidad visual actuaron de manera sinérgica para favorecer el crecimiento de las plantas de maíz en las condiciones experimentales que se estudiaron.
BIBLIOGRAFÍA
Berruti A, Lumini E, Balestrini R, Bianciotto V. Arbuscular Mycorrhizal Fungi as Natural Biofertilizers: Let’s Benefit from Past Successes. Frontiers in Microbiology [Internet]. 2016 [cited 12/12/2022];6. doi:10.3389/fmicb.2015.01559
Giovannetti M, Avio L, Sbrana C. Functional Significance of Anastomosis in Arbuscular Mycorrhizal Networks. In: Horton TR, editor. Mycorrhizal Networks [Internet]. Dordrecht: Springer Netherlands; 2015 [cited 12/12/2022]. p. 41-67. doi:10.1007/978-94-017-7395-9_2
Bonfante P, Genre A. Mechanisms underlying beneficial plant-fungus interactions in mycorrhizal symbiosis. Nature Communications. 2010;1(1):1-11. doi:10.1038/ncomms1046
Smith SE, Smith FA. Roles of Arbuscular Mycorrhizas in Plant Nutrition and Growth: New Paradigms from Cellular to Ecosystem Scales. Annual Review of Plant Biology. 2011;62(1):227-50. doi:10.1146/annurev-arplant-042110-103846
Williams A, Manoharan L, Rosenstock NP, Olsson PA, Hedlund K. Long-term agricultural fertilization alters arbuscular mycorrhizal fungal community composition and barley (Hordeum vulgare) mycorrhizal carbon and phosphorus exchange. New Phytologist. 2017;213(2):874-85. doi:https://doi.org/10.1111/nph.14196
Lenoir I, Fontaine J, Lounès-Hadj Sahraoui A. Arbuscular mycorrhizal fungal responses to abiotic stresses: A review. Phytochemistry. 2016;123:4-15. doi:10.1016/j.phytochem.2016.01.002
Rivera-Becerril F, van Tuinen D, Chatagnier O, Rouard N, Béguet J, Kuszala C, et al. Impact of a pesticide cocktail (fenhexamid, folpel, deltamethrin) on the abundance of Glomeromycota in two agricultural soils. Science of The Total Environment. 2017;577:84-93. doi:10.1016/j.scitotenv.2016.10.098
Battini F, Cristani C, Giovannetti M, Agnolucci M. Multifunctionality and diversity of culturable bacterial communities strictly associated with spores of the plant beneficial symbiont Rhizophagus intraradices. Microbiological Research. 2016;183:68-79. doi:10.1016/j.micres.2015.11.012
Fernández F, Rivera R, Noval B. Metodología de recubrimiento de semillas con inoculo micorrizógeno. Patente Cubana. 1999;(22641).
Hernández JA, Pérez JJM, Bosch ID, Castro SN. Clasificación de los suelos de Cuba 2015. Mayabeque, Cuba: Ediciones INCA. 2015;93:91.
Trouvelot A, Kough JL, Gianinazzi-Pearson V. Mesure du taux de mycorhization VA d’un système radiculaire. Recherche de méthode d’estimation ayant une signification fonctionnelle. In 1986 [cited 12/12/2022]. p. 217-21. Available from: http://pascal-francis.inist.fr/vibad/index.php?action=getRecordDetail&idt=8758731
Helander M, Saloniemi I, Omacini M, Druille M, Salminen J-P, Saikkonen K. Glyphosate decreases mycorrhizal colonization and affects plant-soil feedback. Science of The Total Environment. 2018;642:285-91. doi:10.1016/j.scitotenv.2018.05.377
Espinosa R, Felix F, Martinez L, Cañizares P, Yakelín R, Ortega E. Manejo, integración y beneficios del biofertilizante micorrízico EcoMic (r) en la producción agrícola [Internet]. 2020.
Lekberg Y, Wagner V, Rummel A, McLeod M, Ramsey PW. Strong indirect herbicide effects on mycorrhizal associations through plant community shifts and secondary invasions. Ecological Applications. 2017;27(8):2359-68. doi:https://doi.org/10.1002/eap.1613
Cameron JC, Lehman RM, Sexton P, Osborne SL, Taheri WI. Fungicidal Seed Coatings Exert Minor Effects on Arbuscular Mycorrhizal Fungi and Plant Nutrient Content. Agronomy Journal. 2017;109(3):1005-12. doi:https://doi.org/10.2134/agronj2016.10.0597
Brígido C, van Tuinen D, Brito I, Alho L, Goss MJ, Carvalho M. Management of the biological diversity of AM fungi by combination of host plant succession and integrity of extraradical mycelium. Soil Biology and Biochemistry. 2017;112:237-47. doi:10.1016/j.soilbio.2017.05.018
Schlaeppi K, Bender SF, Mascher F, Russo G, Patrignani A, Camenzind T, et al. High-resolution community profiling of arbuscular mycorrhizal fungi. New Phytologist. 2016;212(3):780-91. doi:https://doi.org/10.1111/nph.14070
Hage-Ahmed K, Rosner K, Steinkellner S. Arbuscular mycorrhizal fungi and their response to pesticides. Pest Management Science. 2019;75(3):583-90. doi:https://doi.org/10.1002/ps.5220
Kjøller R, Rosendahl S. Effects of fungicides on arbuscular mycorrhizal fungi: differential responses in alkaline phosphatase activity of external and internal hyphae. Biology and Fertility of Soils. 2000;31(5):361-5. doi:10.1007/s003749900180
O’Connor P, Manjarrez M, Smith SE. The fate and efficacy of benomyl applied to field soils to suppress activity of arbuscular mycorrhizal fungi. Canadian journal of microbiology. 2009;55(7):901-4.
Author notes
*Autor para correspondencia: marocha@inca.edu.cu
