Artículo original
Received: 11 May 2021
Accepted: 28 January 2022
RESUMEN: Durante el sistema de cosecha en verde de la caña de azúcar, se produce una gran cantidad de residuo agrícola de cosecha que puede dejarse como cobertura sobre el suelo, retirarse del campo o incorporarse en el perfil, según las características agroecológicas de cada área. Es importante descomponer rápidamente la cobertura con residuo en zonas donde resulta perjudicial para la producción del cañaveral. Una de las alternativas para acelerar la descomposición natural del residuo es la utilización de hongos lignocelulolíticos. El objetivo de este trabajo fue aislar cepas fúngicas autóctonas, a partir de la conservación del residuo agrícola de cosecha (RAC) de la caña de azúcar, seleccionar y caracterizar en forma cultural, morfológica y molecular aquellas que presenten mayor potencial para acelerar la descomposición del residuo de la cosecha en verde del cañaveral. A partir de fragmentos de residuo recién cosechado, se aislaron cinco cepas fúngicas autóctonas. Se evaluó la actividad celulolítica y ligninolítica in vitro, utilizando carboximetilcelulosa y guaiacol, como sustratos, respectivamente. La cepa HR5E3 fue la única capaz de descomponer la celulosa y la lignina. Esta cepa, se caracterizó en forma cultural, morfológica y molecular como Trichocladium pyriforme y produjo enzimas del grupo de la lignina peroxidasa, polifenol oxidasas y lacasas. En bioensayos de fermentación en sustrato sólido, dicha cepa aceleró la descomposición del residuo mediante crecimiento diáuxico con glucosa. Trichocladium pyriforme, cepa HR5E3 podría utilizarse como un bioinoculante capaz de degradar la lignocelulosa, y evitar los efectos perjudiciales que la cobertura inalterada del residuo agrícola podría tener sobre el desarrollo del cañaveral.
Palabras clave: Biodegradación, fermentación, enzimas, lignocelulosa.
ABSTRACT: During the green harvesting system of sugarcane, a large amount of agricultural harvest residue is produced that can be left as mulch on the soil, removed from the field or incorporated into the profile, depending on the agroecological characteristics of each area. It is important to rapidly decompose the cover crop residue in areas where it is detrimental to sugarcane production. One of the alternatives to accelerate the natural decomposition of the residue is the use of lignocellulolytic fungi. The objective of this work was to isolate autochthonous fungal strains from sugarcane ARH, select and characterize culturally, morphologically and molecularly those with the greatest potential to accelerate the decomposition of the green harvest residue of the sugarcane field. Five autochthonous fungal strains were isolated from fragments of freshly harvested residue. Cellulolytic and ligninolytic activity was evaluated in vitro, using carboxymethylcellulose and guaiacol as substrates, respectively. Strain HR5E3 was the only strain able to decompose cellulose and lignin. This strain was culturally, morphologically and molecularly characterized as Trichocladium pyriforme and produced enzymes of the lignin peroxidase group, polyphenol oxidases and laccases. In solid substrate fermentation bioassays, this strain accelerated the decomposition of the residue by di-auxic growth with glucose. Trichocladium pyriforme HR5E3 could be used as a bioinoculant capable of degrading lignocellulose, and avoid the detrimental effects that the unaltered cover of the agricultural residue could have on the development of sugarcane.
Key words: Biodegradation, fermentation, lignocellulolytic enzymes.
INTRODUCCIÓN
La caña de azúcar es uno de los cultivos de mayor importancia regional en el noroeste argentino; concentrándose su producción en la provincia de Tucumán, con una superficie cultivable de 276.880 ha, para la zafra 2020 (1). En búsqueda de mejoras en las estrategias productivas, en Tucumán, se ha implementado la cosecha del cañaveral sin quema, conocida como cosecha en verde. Este cambio de sistema impulsó el estudio del manejo de los cañaverales mediante la conservación del residuo agrícola de cosecha (RAC) como cobertura. En este nuevo esquema productivo permanece sobre la superficie del suelo una importante cantidad de residuo (hojas y despuntes) que, para las condiciones de Tucumán, ha sido estimada entre 7 y 16 t ha-1 de materia seca (2). Distintos estudios han demostrado que el RAC sobre la superficie del suelo aporta materia orgánica y mejora su estabilidad estructural, favorece la conservación de humedad, disminuye la evaporación y mejora la infiltración del agua, reduce la erosión, permite el reciclado de nutrientes y disminuye la infestación por malezas (2,3). Sin embargo, la mineralización del RAC de la caña de azúcar es un proceso lento, ya que se trata de un residuo con alta relación C N-1 (2), lo cual representa una dificultad en las áreas con exceso de humedad por problemas de drenaje y presencia de una capa freática cercana a la superficie. En estas regiones, mantener el RAC como cobertura afecta, negativamente, el crecimiento del cañaveral (4); por tal motivo, lograr su rápida descomposición representa una ventaja productiva. La utilización de microorganismos descomponedores es una alternativa para acelerar la descomposición natural de los residuos agrícolas y reducir así sus posibles efectos negativos (5-7). Los hongos, son los organismos predominantes del suelo responsables de la degradación de la lignocelulosa presente en los residuos vegetales (8,9), debido a la presencia de distintos sistemas hidrolíticos enzimáticos constituidos por celulasas y hemicelulasas, y un sistema ligninolítico extracelular oxidativo formado por enzimas como lacasas, fenol oxidasas, lignina peroxidasas y manganeso peroxidasas (6,10,11). Con base en estas consideraciones, el objetivo de este trabajo fue aislar cepas fúngicas autóctonas, a partir del RAC de la caña de azúcar, seleccionar y caracterizar en forma cultural, morfológica y molecular aquellas que presenten mayor potencial en la descomposición del residuo de la cosecha en verde del cañaveral.
MATERIALES Y MÉTODOS
Aislamiento de cepas fúngicas a partir del RAC
Se colectó RAC de la variedad LCP 85-384 de cañaverales ubicados en el Departamento de Simoca, provincia de Tucumán, Argentina. Esta línea comercial es la más cultivada, con 76 % del área cañera de la provincia (12). El RAC se colectó en julio de 2018, inmediatamente después de la cosecha, las muestras se trasladaron en bolsas plásticas cerradas al laboratorio de Microbiología de la Estación Experimental Agroindustrial Obispo Colombres (EEAOC) y se conservaron a temperatura ambiente (25 ºC). Para su procesamiento, el residuo se cortó en fragmentos de ≈ 2 cm de longitud, los cuales se lavaron tres veces con agua destilada estéril, se desinfestaron con etanol al 70% (v v-1) por 1 min y luego con NaClO 3 % (v v-1) durante 3 min. Se realizaron cinco lavados sucesivos con agua destilada estéril para eliminar restos del desinfestante. Los trozos se secaron con papel absorbente estéril y se colocaron en placas de Petri que contenían el medio de cultivo agar papa glucosado (APG, Britania). Las placas se incubaron de 7 a 10 d a 35 °C. Una vez desarrollados, los hongos se purificaron mediante repiques sucesivos en el medio de cultivo extracto de malta agar (EMA) (maltosa 12,75 g L-1; dextrosa 2,75 g L-1; glicerol 2,35 g L-1; peptona bacteriológica 0,78 g L-1) y se evaluaron las actividades enzimáticas asociadas a la descomposición del residuo.
Determinación de actividades enzimáticas
La actividad ligninolítica se evaluó mediante dos técnicas: 1) se utilizó el medio de cultivo EMA con guaiacol 1 mM (Sigma Aldrich, USA) al 0,01 % (p v-1). Las placas se inocularon a partir de un cultivo sólido de las cepas fúngicas en EMA, y se incubaron por 7 d a 35 °C. La actividad ligninolítica se evaluó por la aparición de un halo de crecimiento color marrón oscuro (13); 2) se utilizó el medio de cultivo agar lignina alcalina que incluyó guaiacol 1 mM al 0,01 % (p v-1). Las placas se inocularon a partir de un cultivo sólido de las cepas fúngicas en EMA y se incubaron en las mismas condiciones que en la técnica 1. La aparición de una pigmentación color marrón oscuro; indica la oxidación del guaiacol en presencia de las enzimas manganeso y lignina peroxidasas (13). La actividad celulolítica se evaluó en el medio de cultivo mínimo salino (MMS) con carboximetilcelulosa (CMC), como única fuente de carbono (6,14).
Las placas con CMC se inocularon a partir de un cultivo sólido de las cepas fúngicas crecidas en EMA y se incubaron durante 7 d a 35 °C. Posteriormente, las placas se tiñeron con una solución de Rojo Congo (RC) 0,1 % (p v-1), durante 15 min y se lavaron tres veces con NaCl 1 M. La actividad celulolítica se determinó por la aparición de halos claros alrededor de las colonias. La técnica consistió en la capacidad del colorante RC de adherirse a la CMC, de esta forma la placa de Petri adquiere un color rojo. Cuando la CMC se degrada por el complejo enzimático de la celulasa, el área hidrolizada adquiere un color amarillo claro que indica que el colorante no pudo adherirse al polímero que se ha degradado como consecuencia de la actividad celulolítica del hongo (14). La cepa fúngica que presentó actividades ligninolíticas y celulolíticas positivas, se caracterizó en forma cultural, morfológica y molecular.
Caracterización de la cepa fúngica seleccionada
La caracterización cultural y morfológica se realizó a la cepa HR5E3, crecida en medio EMA, mediante observaciones macroscópicas y microscópicas (microscopio óptico Nikon, modelo E200). Para la caracterización molecular, el hongo se repicó en placas de Petri, con el medio de cultivo sólido EMA. Previo a la inoculación, se colocó un disco de papel celofán estéril sobre las placas, a fin de facilitar la posterior extracción del micelio. Las placas se incubaron en estufa por 10 d a 35 °C. Se realizó la extracción de ADN, con la técnica del fenol-cloroformo (15) y se llevó a cabo un análisis electroforético en gel de agarosa al 1 % (p v-1). La PCR se efectuó con los cebadores ITS1/ITS4 que están diseñados en estas mismas regiones internas, y amplifican un fragmento de 600 pb del gen ADNr, 16S. Los amplicones se verificaron por electroforesis en gel de agarosa al 1 % (p v-1) y se envió secuenciar al Laboratorio de Secuenciación del Instituto Nacional de Tecnología Agropecuaria (INTA) Castelar, Buenos Aires, Argentina. Las secuencias obtenidas se analizaron con el programa BLAST (Basic Local Alignment Search Tool) del NCBI (2020).
Perfil de producción de enzimas ligninolíticas
La producción de enzimas ligninolíticas se evaluó en el medio basal ligninasa (MBL) sólido (KH2PO4 1 g L-1; extracto de levadura 0,01 g L-1; C4H12N2O6 0,5 g L-1; CuSO4.5H2O 0,001 g L-1; MgSO4.7H2O 0,5 g L-1; Fe2(SO4)3 0,001 g L-1; CaCl2.2H2O 0,01 g L-1; MnSO4.H2O 0,001 g L-1), suplementado con sustratos específicos, según la enzima a evaluar. Como control se utilizó la cepa Pycnoporus sp. P6 con actividad ligninolítica (16). El medio sólido MBL se inoculó con discos miceliares de 0,5 cm de diámetro, obtenidos a partir de la periferia de una colonia del hongo que se desarrolló en el medio EMA durante 7 d a 35 ºC.
Las actividades enzimáticas evaluadas fueron las siguientes: 1) Lignina peroxidasa (LiP). El medio MBL se suplementó con una solución del colorante Azure B a una concentración final de 0,01 % (v v-1). La producción de LiP se evidencia según la aparición de un halo de decoloración alrededor de la colonia fúngica (17); 2) Polifenoloxidasas (POx). El medio MBL se suplementó con una solución de ácido tánico 0,5 % (p v-1). La formación de un halo color marrón alrededor de la colonia fúngica indica reacción positiva (17); 3) Lacasa (Lac). Para su evaluación se llevaron a cabo dos metodologías. Se suplementó el medio MBL con el sustrato ABTS [ácido 2,2-azino-bis (3-etilbenzotiazolina-6- sulfónico)], a una concentración final de 0,1 % (p v-1). La aparición de halos de color verde oscuro indica actividad Lac (17). Por otro lado, se crecieron cepas fúngicas en el medio MBL sin adición de sustratos. Luego de incubar las placas durante 10 d a 35 ºC, se realizaron perforaciones con un sacabocado estéril en la zona periférica de crecimiento miceliar, en las cuales se agregaron diferentes sustratos, a fin de confirmar la actividad Lac. En una de las perforaciones se agregó solución de siringaldazina (3,5-dimetoxi-4-hidroxibenzaldehidazina) 0,5 mM, disuelta en dimetilsulfóxido (DMSO), en presencia y ausencia de buffer fosfato 50 mM, pH 6. La formación de un producto quinónico de color rosa indica reacción positiva (17). En otra de las perforaciones se agregó ABTS 0,1 % (p v-1), y en otra 0,8 g L-1 de 2,6- dimetoxifenol (DMP). En este último caso, la actividad Lac se demostró por la aparición de halos de color naranja, debido a la oxidación del sustrato (18).
Bioensayo de descomposición del RAC
La descomposición del RAC se evaluó mediante un ensayo de fermentación en sustrato sólido, realizado bajo condiciones controladas (25 °C y 90 % de humedad relativa). Como soporte, se usó RAC de la variedad LCP 85-384, colectado inmediatamente después de la cosecha (julio, 2019) y esterilizado en autoclave (20 min, 121 °C). En bandejas plásticas de 500 mL, se colocaron 4 g de residuo seco esterilizado y se evaluaron los siguientes tratamientos: 1) RAC inoculado con tres fragmentos de 0,5 cm2 del medio agarizado que contenía micelio del hongo; 2) RAC inoculado con tres fragmentos de 0,5 cm2 del medio agarizado que incluía micelio del hongo y 850 μL de glucosa 8 % (p v-1) esterilizada por filtración; 3) RAC inoculado con 5 mL de una suspensión de 109 conidios mL-1; 4) RAC inoculado con 5 mL de una suspensión de 109 conidios mL-1 y 850 μL de glucosa 8 % (p v-1) esterilizada por filtración y 5) RAC sin inocular y humedecido con 850 μL de agua destilada estéril como control. Los tratamientos se distribuyeron en un diseño experimental completamente aleatorizado con tres repeticiones por tratamiento y cinco individuos por repetición. Al inicio del ensayo (t0) y a los 65 días postinoculación (t65), se determinó el contenido de lignina con la técnica lignina detergente ácida (LDA) (19). Los datos se analizaron mediante análisis de varianza (ANOVA) y la Prueba LSD Fisher con el programa InfoStat (Software Estadístico, 2010) para Windows.
RESULTADOS Y DISCUSIÓN
La utilización de cepas fúngicas autóctonas, adaptadas a las condiciones agroecológicas de los cañaverales de la región, y con capacidad para descomponer el RAC, constituye una de las alternativas promisorias a fin de acelerar la descomposición del residuo y evitar los efectos perjudiciales que genera la acumulación de biomasa sobre la superficie del suelo. A partir de RAC recién cosechado de la variedad LCP 85-384, se aislaron cinco cepas fúngicas con características culturales y morfológicas distintas. De estas, dos no presentaron actividad celulolítica ni ligninolítica, tres manifestaron actividad celulolítica cuando se incubaron en presencia de CMC y una de ellas tuvo ambas actividades (Tabla 1). Esta cepa (HR5E3) se seleccionó por su actividad ligninolítica y celulolítica para su caracterización molecular.
Actividades celulolíticas y ligninolíticas en las cepas fúngicas aisladas a partir del RAC de la caña de azúcar
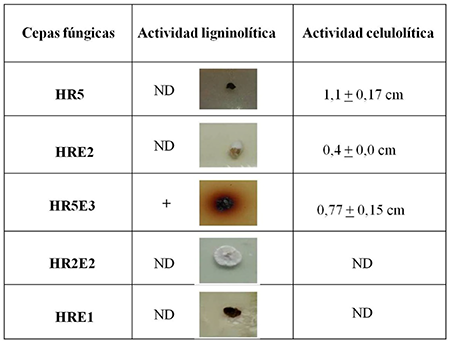
Las siglas ND indican actividad enzimática no detectada
Los resultados de la caracterización cultural y morfológica de la cepa HR5E3 se presentan en la Figura 1: la colonia, circular, desarrolló bordes irregulares con relieve, de textura aterciopelada y coloración negra grisácea, debido a la abundante producción de clamidosporas (Figura 1a) (20); las hifas, septadas, presentaron hinchazones redondeados y próximos a las septas (Figura 1b). El tamaño promedio de los conidios fue de 8-10 × 4-5 μm, con forma piriforme o “de pera” (Figura 1b)
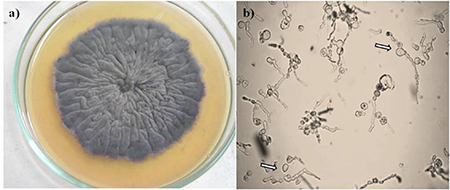
Figura 1
Morfología de Trichocladium pyriforme, cepa HR5E3. a) Apariencia de la colonia de frente, con bordes circulares y coloración grisácea; b) Aspecto microscópico de hifas y conidios
La secuenciación confirmó que la cepa fúngica seleccionada HR5E3 corresponde a la especie Trichocladium pyriforme (20), con 98,75 % de identidad. Las características morfológicas y culturales de T. pyriforme, reportadas por Dixon (20), coincidieron con las observadas en estas determinaciones. La presencia de esta especie se reportó, previamente, como parte de la comunidad fúngica asociada a hojas de caña de azúcar en descomposición (21), a pesar de las variaciones que existen en las poblaciones microbianas asociadas a los tejidos del cultivo en mención (22).
El crecimiento y la producción de enzimas ligninolíticas extracelulares por T. pyriforme, cepa HR5E3, se evaluó utilizando diversos medios de cultivo sólidos que contienen sustratos o indicadores que permiten la visualización directa de la producción de enzimas (Tabla 2).
Actividades enzimáticas ligninolíticas de Trichocladium pyriforme cepa HR5E3 en el medio sólido MBL

El número de cruces indica la intensidad de reacción positiva [débil (+) a muy fuerte (+++)]; (C) sin restricciones de crecimiento; (LiP) Lignina peroxidasa; (Lac) Lacasa; (POx) Polifenoloxidasa; (ABTS) [ácido 2,2-azino-bis (3-etilbenzotiazolina-6- sulfónico)]
Los resultados demostraron que la cepa fúngica seleccionada produjo enzimas ligninolíticas extracelulares del grupo de las LiP, Lac y POx, que están implicadas en la descomposición de la lignina (18). Sin embargo, el potencial de producción para las tres enzimas ligninolíticas evaluadas fue menor que el de la cepa control. En este trabajo, se utilizó el medio MBL suplementado con ácido tánico para detectar la producción de oxidasas extracelulares (16), pese a que solo algunos hongos son capaces de crecer en presencia de este compuesto, debido a su elevada toxicidad (23). En este sentido, T. pyriforme cepa HR5E3 no solo fue capaz de desarrollarse en presencia de ácido tánico al 0,5 % (p v-1), sino que además presentó moderada actividad POx, por lo que sería interesante estudiar el posible uso de este microorganismo, no solo para acelerar la descomposición del RAC de caña de azúcar, sino también en procesos de biorremediación de suelos contaminados con este grupo de compuestos fenólicos (24).
Debido a que Lac tiene capacidad para oxidar de manera diferencial distintos sustratos, según su potencial redox (16), se evaluó la actividad de esta enzima de la cepa en estudio en el medio MBL, suplementado con diferentes sustratos. Se demostró que las enzimas Lac extracelulares producidas por T. pyriforme HR5E3 tienen afinidad y actividad para sustratos como el ABTS y el DMP, mientras que no fueron capaces de oxidar a la siringaldazina (Tabla 3). Las diferencias observadas entre los sustratos utilizados podrían atribuirse a que presentan grupos químicos en distintas posiciones, lo que genera diferentes afinidades de las Lacs para cada compuesto (11).
Actividad Lac de Trichocladium pyriforme cepa HR5E3 en presencia de distintos sustratos

El número de cruces indica la intensidad de reacción positiva [débil (+) a muy fuerte (+++)]; (Lac) Lacasa; (POx) Polifenoloxidasa; (ABTS) [ácido 2,2-azino-bis (3-etilbenzotiazolina-6- sulfónico)]
La capacidad de T. pyriforme cepa HR5E3 de descomponer el RAC se evaluó en bioensayos de fermentación en sustrato sólido, bajo condiciones controladas. Al inicio del ensayo (t0), el contenido de lignina del RAC, previo a la inoculación, fue del 16,74 % (p p-1). Según se observa en la Tabla 4, a los 65 d postinoculación (t65), el contenido de lignina del RAC de los tratamientos 2, 3 y 4 se redujo significativamente, mientras que en el tratamiento 1, cuando la inoculación del RAC se realizó solo con el micelio del hongo, no se observaron diferencias. Como era de esperar, el contenido de lignina del RAC sin inocular (tratamiento 5) se mantuvo constante hasta el final del ensayo.
Porcentaje de lignina del RAC, en los diferentes tratamientos evaluados

(t0) tiempo inicial; (t65) 65 dias postinoculación. Letras distintas, por fila, indican diferencias significativas (Prueba LSD, Fisher) con p≤ 0,05
La inoculación con conidios sobre el RAC redujo 27,95 % el contenido de lignina, respecto al valor inicial, probablemente debido al aumento de la superficie de contacto entre el hongo y el residuo. En los dos tratamientos suplementados con glucosa 8 % (p v-1), el contenido final de lignina del RAC fue menor respecto al control y menor respecto al mismo tratamiento sin el agregado de glucosa (Tabla 4). La disminución del contenido de lignina, cuando la fermentación se realizó inoculando el RAC con un fragmento de micelio agarizado suplementado con glucosa, fue de 33,99 %, en relación con el contenido de lignina inicial; en tanto que, cuando se realizó por inoculación con conidios y se suplementó con glucosa, se alcanzó la mayor reducción en el contenido de lignina con un valor de 52,33 % (Tabla 4). Esto indicaría que la descomposición fúngica de la lignina por la cepa HR5E3 (T. pyriforme) se realiza con una cinética de crecimiento diáuxico, al estar presentes dos fuentes de carbono (C) distintas. Se reportó que un factor crítico para descomponer el residuo de cosecha de la caña de azúcar, utilizando cepas fúngicas, es agregar una fuente de C fácilmente asimilable para que los hongos inicien el desarrollo de su biomasa (25). Según lo observado en este trabajo, y en relación con lo reportado por Chu y Barnes (26), en una primera etapa, el hongo crece a expensas de la glucosa y, una vez agotada esta fuente de C, continúa su crecimiento degradando la lignina.
La capacidad de diversas especies de Trichocladium para descomponer residuos lignocelulolíticos se reportó por Durrant (27) y por Pavarina y Durrant (28), quienes observaron que, al cultivar estos hongos sobre bagazo de caña de azúcar y aserrín, se promovió la degradación del material lignocelulósico. Algunas especies del género en mención producen endo y exoglucanasas, xilanasas y β glucosidasas, capaces de descomponer la celulosa en condiciones aeróbicas, microaerofílicas y anaeróbicas. Esta capacidad, aunada a la producción de Lacs, tanto en condiciones aeróbicas como microaerofílicas, le otorga a este grupo de hongos gran versatilidad para digerir los polisacáridos estructurales de la pared celular de las plantas, independientemente del nivel de oxígeno que se encuentre en el ambiente, confiriéndole una ventaja competitiva en los ambientes naturales frente a otros microorganismos descomponedores (27).
Si se profundizan los estudios sobre las bases moleculares asociadas a la producción de estas enzimas biotecnológicas relevantes, la cepa T. pyriforme HR5E3, podría utilizarse a gran escala para favorecer la rápida liberación de azúcares fermentables a partir del RAC, para su posterior transformación en alcohol u otros compuestos. De esta forma, se lograría el aprovechamiento de un residuo de cosecha que se produce en grandes cantidades, convirtiéndolo en materia prima para la obtención de compuestos de interés, y lograr su revalorización.
CONCLUSIONES
-
La cepa HR5E3, identificada como Trichocladium pyriforme y aislada a partir del RAC de cañaverales de la variedad LCP 85-384 en Tucumán (Argentina), presentó actividad celulolítica y ligninolítica in vitro, y aceleró la descomposición del RAC en ensayos de fermentación en sustrato sólido, por crecimiento diáuxico, en presencia de glucosa.
-
La cepa seleccionada podría utilizarse como un potencial bioinoculante, a fin de acelerar la descomposición del RAC que permanece como cobertura sobre la superficie del suelo, luego de la cosecha en verde de la caña de azúcar. Esto contribuiría a evitar los efectos perjudiciales que, en algunas zonas, el mantenimiento de la cobertura inalterada de RAC podría tener sobre el crecimiento y el desarrollo del cañaveral.
AGRADECIMIENTOS
-
Los autores del trabajo agradecen al Dr. Pablo Ahmed por su colaboración y asesoramiento durante los ensayos de determinaciones enzimáticas.
BIBLIOGRAFÍA
Fandos C, Scandaliaris P, Carreras- Baldrés J, Soria F, Giardina J. Área cosechable y producción de caña de azúcar y azúcar para la zafra 2020 en Tucumán. 2020;190:3-5.
Digonzelli PA, Romero ER, Alonso L, Ullivarri F, Quinteros R, Scandaliaris J, et al. Assessing a sustainable sugarcane production system in Tucumán, Argentina. Part 1: Dynamics of sugarcane harvest residue (trash) decomposition. Revista industrial y agrícola de Tucumán. 2011;88(1):1-12.
Carvalho JLN, Nogueirol RC, Menandro LMS, Bordonal R de O, Borges CD, Cantarella H, et al. Agronomic and environmental implications of sugarcane straw removal: a major review. GCB Bioenergy. 2017;9(7):1181-95. doi:https://doi.org/10.1111/gcbb.12410
Cherubin MR, Oliveira DM da S, Feigl BJ, Pimentel LG, Lisboa IP, Gmach MR, et al. Crop residue harvest for bioenergy production and its implications on soil functioning and plant growth: A review. Scientia Agricola. 2018;75(3):255-72.
Marzi M, Shahbazi K, Kharazi N, Rezaei M. The Influence of Organic Amendment Source on Carbon and Nitrogen Mineralization in Different Soils. Journal of Soil Science and Plant Nutrition. 2020;20(1):177-91. doi:10.1007/s42729-019-00116-w
Maza M, Pajot HF, Amoroso MJ, Yasem MG. In-vitro degradation of Czapek and molasses amended post-harvest sugarcane residue by lignocellulolytic fungal strains. International Biodeterioration & Biodegradation. 2015;104:118-22. doi:10.1016/j.ibiod.2015.05.021
Maza M, Medina M, Plasencia AM, Amoroso MJ, Yasem MG. Fungal inoculation effect on post-harvest sugarcane residue decomposition under field conditions. Revista agronómica del noroeste argentino. 2018;38(2):65-73.
Chukwuma OB, Rafatullah M, Tajarudin HA, Ismail N. Lignocellulolytic Enzymes in Biotechnological and Industrial Processes: A Review. Sustainability. 2020;12(18):7282. doi:10.3390/su12187282
Ferreira JA, Mahboubi A, Lennartsson PR, Taherzadeh MJ. Waste biorefineries using filamentous ascomycetes fungi: Present status and future prospects. Bioresource Technology. 2016;215:334-45. doi:10.1016/j.biortech.2016.03.018
Kantharaj P, Boobalan B, Sooriamuthu S, Mani R. Lignocellulose degrading enzymes from fungi and their industrial applications. Int. J. Curr. Res. Rev. 2017;9(21):1-12.
Nguyen KA, Wikee S, Lumyong S. Brief review: lignocellulolytic enzymes from polypores for efficient utilization of biomass. Mycosphere. 2018;9(6):1073-88.
Ostengo S, Espinosa MA, Díaz JV, Chavanne ER, Costilla DD, Cuenya MI. Relevamiento de la distribución de variedades y de otras tecnologías aplicadas en el cultivo de caña de azúcar en la provincia de Tucumán: campaña 2016/2017. Gac. Agroindustrial EEAOC. 2018;81:14.
Sehgal J, Asha BM, Vardhan A, Siddalingeshwara KG. An Approach on Screening, Production and Characterization of Laccase from Fusarium. Journal of Current Pharma Research. 2020;10(2):3673-9.
Cruz-Hernández M. Avances de Investigación en Inocuidad de alimentos. In: Evaluación de hongos filamentosos para la producción de enzimas celulolíticas [Internet]. 2019. Available from: https://www.researchgate.net/publication/344359381_Evaluacion_de_hongos_filamentosos_para_la_produccion_de_enzimas_celuloliticas
Gaillard C, Strauss F. Ethanol precipitation of DNA with linear polyacrylamide as carrier. Nucleic Acids Research. 1990;18(2):378.
Ahmed PM, Pajot HF, de Figueroa LIC, Gusils CH. Sustainable bioremediation of sugarcane vinasse using autochthonous macrofungi. Journal of Environmental Chemical Engineering. 2018;6(4):5177-85. doi:10.1016/j.jece.2018.08.007
Pointing SB. Qualitative methods for the determination of lignocellulolytic enzyme production by tropical fungi. Fungal diversity. 1999;2:17-33.
Fonseca MI, Zapata PD, Villalba LL, Fariña JI. Characterization of the oxidative enzyme potential in wild white rot fungi from the subtropical forest of Misiones (Argentina). Acta biològica colombiana. 2015;20(1):47-56.
Goering HK, Soest PJV. Forage Fiber Analyses (apparatus, Reagents, Procedures, and Some Applications). Vol. 379. U.S. Agricultural Research Service; 1970. 24 p.
Dixon M. Trichocladium pyriformis sp. nov. Transactions of the British Mycological Society. 1968;51(1):160-4.
de Souza RSC, Okura VK, Armanhi JSL, Jorrín B, Lozano N, Da Silva MJ, et al. Unlocking the bacterial and fungal communities assemblages of sugarcane microbiome. Scientific Reports. 2016;6(1):1-15.
Miura T, Niswati A, Swibawa IG, Haryani S, Gunito H, Shimano S, et al. Diversity of Fungi on Decomposing Leaf Litter in a Sugarcane Plantation and Their Response to Tillage Practice and Bagasse Mulching: Implications for Management Effects on Litter Decomposition. Microbial Ecology. 2015;70(3):646-58. doi:10.1007/s00248-015-0620-9
Spennati F, Ricotti A, Mori G, Siracusa G, Becarelli S, Gregorio SD, et al. The role of cosubstrate and mixing on fungal biofilm efficiency in the removal of tannins. Environmental Technology. 2020;41(26):3515-23. doi:10.1080/09593330.2019.1615128
Sen SK, Raut S, Bandyopadhyay P, Raut S. Fungal decolouration and degradation of azo dyes: A review. Fungal Biology Reviews. 2016;30(3):112-33. doi:10.1016/j.fbr.2016.06.003
Beary TP, Boopathy R, Templet P. Accelerated decomposition of sugarcane crop residue using a fungal-bacterial consortium. International Biodeterioration & Biodegradation. 2002;50(1):41-6. doi:10.1016/S0964-8305(02)00056-2
Chu D, Barnes DJ. The lag-phase during diauxic growth is a trade-off between fast adaptation and high growth rate. Scientific Reports. 2016;6(1):1-15. doi:10.1038/srep25191
Durrant LR. Biodegradation of lignocellulosic materials by soil fungi isolated under anaerobic conditions. International Biodeterioration & Biodegradation. 1996;37(3):189-95. doi:10.1016/S0964-8305(96)00022-4
Pavarina EC, Durrant LR. Growth of lignocellulosic-fermenting fungi on different substrates under low oxygenation conditions. Applied Biochemistry and Biotechnology. 2002;98(1):663-77. doi:10.1385/ABAB:98-100:1-9:663
Author notes
*Autor para correspondencia: ltortora@eeaoc.org.ar
Conflict of interest declaration
