Revisión Bibliográfica
El suelo vivo: un poco de lo que ocurre en este entorno. Un énfasis en los fitopatógenos
The living soil: a bit of what happens in this environment. An emphasis on phytopathogens
El suelo vivo: un poco de lo que ocurre en este entorno. Un énfasis en los fitopatógenos
Cultivos Tropicales, vol. 45, no. 1, e06, 2024
Ediciones INCA
Received: 26 July 2022
Accepted: 21 November 2022
RESUMEN: El suelo es un ecosistema con una reserva de carbono que sustenta la diversidad biológica. En esta revisión, presentamos cuán significativa es la simbiosis entre la raíz de la planta y los macro y microorganismos del suelo, así como los beneficios que genera para lograr un equilibrio ecológico y mantener bajas poblaciones de fitopatógenos en la producción de alimentos. Por ejemplo, las lombrices de tierra, colémbolos, cochinillas y ácaros oribátidos influyen, en gran medida, en el funcionamiento del sistema del suelo, ya que construyen y mantienen la estructura del suelo y participan activamente en el ciclo de nutrientes, a través de procesos de mineralización y humificación, además de consumir fitopatógenos. Por otro lado, microorganismos como los hongos micorrízicos, que se benefician al absorber los nutrientes de la planta, la ayudan a absorber los minerales del suelo y brindan protección a las raíces frente a los fitopatógenos. Los hongos micorrízicos inducen cambios en la planta y luego la planta responde produciendo exudados de las raíces que reducen o repelen a los patógenos. Otro ejemplo es el hongo Trichoderma, conocido como agente de biocontrol para la producción de metabolitos secundarios con actividad antimicrobiana contra fitopatógenos. Los agentes de control biológico y sus metabolitos secundarios son enfoques potenciales que se utilizan actualmente para reducir o reemplazar los agroquímicos. Finalmente, el manejo integrado de cultivos promueve la competencia y el equilibrio esenciales para mantener la salud del suelo y asegurar la producción de alimentos.
Palabras clave: Anélidos, hongos, simbiosis, Trichoderma.
ABSTRACT: Soil is an ecosystem with a carbon pool that suports biological diversity. In this review, it is presented how significant is the symbiosis between the plant root and the macro and microorganisms of the soil, as well as the benefits it generates to achieve an ecological balance and maintain low populations of plant pathogens in food production. For instance, earthworms, collembola, mealybugs and oribatid mites greatly influence the functioning of the soil system, as they build and maintain soil structure and actively participate in nutrient cycling through mineralization and humification processes, in addition to consuming pathogens. On the other hand, microorganisms such as mycorrhizal fungi, which benefit by absorbing the nutrients of the plant and help it absorb minerals from the soil, provide protection to roots against phytopathogens. Mycorrhizal fungi induce changes in the plant and then the plant responds by producing exudates from the roots that reduce or repel plant pathogens. Another example is the Trichoderma fungus, known as a biocontrol agent for producing secondary metabolites with antimicrobial activity against plant pathogens. Biological control agents and their secondary metabolites are potential approaches currently being used to reduce or replace agrochemicals. Finally, integrated crop management promotes competition and balance essential to maintaining soil health and ensuring food production.
Key words: Earthworms, fungi, simbiosis, Trichoderma.
INTRODUCCIÓN
Alimentar a la población mundial es un tema prioritario, por ello la Agenda 2030 para el Desarrollo Sostenible de Naciones Unidas incluye dentro de sus 17 Objetivos de Desarrollo Sostenible, el objetivo hambre cero (1). Lograr esto es un desafío, ya que las plantas están expuestas a muchas condiciones del suelo que podrían afectar el crecimiento y la producción. Por ejemplo, las plagas y enfermedades son de los mayores desafíos que enfrentan los productores de cultivos cada año. Además, las enfermedades emergentes constituyen uno de los mayores riesgos por la devastación que provocan en la producción agrícola (2-5).
Es conocido que la aplicación excesiva de agroquímicos tiene un efecto inmediato sobre lo que se desea lograr durante la producción agrícola (6); sin embargo, esto se logra con consecuencias ambientales y daños a la salud de los trabajadores agrícolas y de los consumidores. Tecnologías sostenibles deben utilizarse para producir los alimentos que demanda la población, sin afectar los recursos naturales.
El suelo, por albergar una gran biodiversidad, se considera la base para la producción de alimentos saludables. La diversidad microbiana tiene varias funciones, una de las cuales es la solubilidad de los minerales, haciéndolos disponibles para las plantas. Por ejemplo, las bacterias solubilizadoras de fosfato contribuyen hasta el 50% de la solubilización del elemento (7). Algunos organismos, como los hongos micorrízicos, llevan los elementos a las raíces a través de sus hifas (8), incluso las endomicorrizas los depositan en el espacio interarbuscular (dentro de la planta).
Esta actividad microbiana promueve un suelo fértil y el equilibro de organismos y microorganismos. Un ejemplo es la lombriz de tierra, la cual mejora la estructura del suelo al tiempo que reduce las poblaciones de fitopatógenos (Figura 1). También, el hongo Trichoderma tiene un amplio espectro de acción que le permite reducir una gran cantidad de patógenos de plantas.
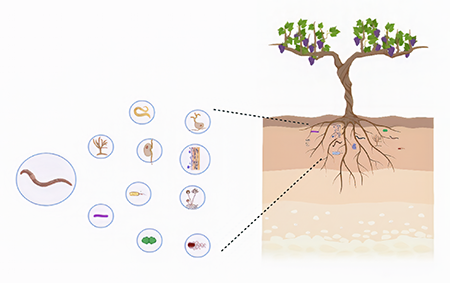
Figura 1
Lombrices de tierra y otros microorganismos miembros del ecosistema del suelo en equilibrio, cada uno con una tarea específica
DESARROLLO
Organismos del suelo
Las lombrices de tierra, por su capacidad para cavar galerías y producir perfiles demográficos y relaciones con la microflora del suelo, son un componente clave en el ciclo de nutrientes en los suelos. Su actividad física y los efectos químicos resultantes promueven ciclos cortos y rápidos de nutrientes y carbohidratos asimilables (9).
Por otra parte, en la agricultura la adición de vermicomposta es una práctica común. La vermicomposta tiene un papel fundamental para promover la vida en el suelo, mejorando la textura y promoviendo niveles satisfactorios de macro y micronutrientes (10). Contiene muchos compuestos ricos en microorganismos beneficiosos y hormonas de crecimiento que funcionan como agentes biofertilizantes y de control biológico contra plagas y patógenos de las plantas (11).
Además, durante el vermicompostaje, la lombriz roja de California (Eisenia foetida) ingiere materia orgánica que progresivamente se descompone y fragmenta. Esta materia está formada por microorganismos que incluyen una gran cantidad de hongos. Las sustancias mucosas producidas por las lombrices de tierra tienen una fuerte actividad antimicrobiana y antifúngica (12). A través de sus secreciones cutáneas y proteína antimicrobiana, controlan los microorganismos (13), reduciendo así las poblaciones de fitopatógenos del suelo.
La superficie de la cutícula de la lombriz de tierra contiene péptidos antimicrobianos que la protegen del ambiente. Descarga péptidos como la lisozima a través de su cutícula, lo que produce una actividad antimicrobiana. Además, se ha demostrado que la pared corporal y la secreción intestinal reducen las poblaciones de Fusarium oxysporum (12).
Las lombrices de tierra se alimentan de suelos que contienen materiales orgánicos, microorganismos vivos e insectos. Una vez ingerido el alimento, se modifica en el cuerpo de la lombriz de tierra para facilitar su absorción. Al entrar por la boca, el material es tragado por la faringe que es una bomba de fuerza (Figura 2). Después de eso, los músculos se contraen y mueven la comida hacia el esófago. Luego, ésta va al buche (que se contrae más que la molleja) donde se almacena y se mueve hacia la molleja. Este es un músculo fuerte que tritura el material en partes muy pequeñas, donde la secreción de enzimas participa en la descomposición de los productos. El material finamente triturado pasa por el proceso de digestión en el intestino. Aquí se agregan más enzimas para promover la descomposición en moléculas simples (14). Las enzimas que participan son la proteasa, lipasa, amilasa, liquenasa, celulasa y quitinasa (15). Este proceso consigue parcialmente la eliminación de fitopatógenos.
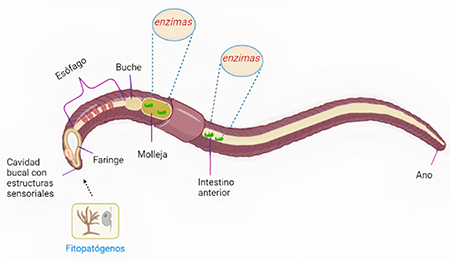
Figura 2
Órganos del cuerpo de la lombriz de tierra, donde ocurre la descomposición de la materia orgánica ingerida, por actividad enzimática
Lombrices de tierra como Eisenia foetida controlan nematodos como Pratylechus sp en tomate (16), Meloidogyne javanica en pepino (17) y Meloidogyne hapla en tomate (18).
Otros investigadores encontraron que la lombriz de tierra, Lumbricus terrestres, se alimentaba de esclerocios de Sclerotinia sclerotiorum cuando estaban hidratados (19). L. terrestris consumió en promedio el 61% de los esclerocios que se hidrataron durante 13 semanas. Además, el humus de lombriz y los hongos micorrízicos arbsculares mejoran la calidad de los frutos (20).
Microorganismos, interacciones y microambientes del suelo
La estructura biológica del suelo está formada por una gran cantidad de bacterias, actinomicetos y hongos (21). Todos ellos están asociados a materia orgánica y materiales microbianos poliméricos como enzimas y polisacáridos extracelulares que ellos mismos producen. Los microorganismos se encuentran en tejidos densos de arcilla o materia orgánica humificada, en depósitos de mucigel, en microporos o en raíces de plantas ricas en carbohidratos. En estos sitios, los microorganismos sobreviven temporalmente a condiciones adversas.
En esta revisión abordamos dos tipos de microorganismos que benefician a las plantas y que, generalmente, se encuentran de forma natural en suelos en simbiosis con plantas, y que pueden usarse para enriquecer suelos, como los hongos micorrízicos y Trichoderma spp.
Una vez que los micros y macroelementos son solubilizados por las bacterias, se transfieren a través de la hifa del hongo micorrízico a la raíz, previamente colonizada por las micorrizas. Las enzimas transportadoras de fosfato del hongo y de la planta están involucradas en este proceso (8).
Los hongos micorrízicos confieren protección a las plantas contra los fitopatógenos (22, 23). En la rizosfera, los microorganismos compiten por el espacio y los nutrientes. Además, las micorrizas también estimulan los mecanismos de defensa bioquímicos de las plantas (22).
Las interacciones entre las micorrizas y las plantas se autorregulan, de hecho, cuando los nutrientes minerales están disponibles en el suelo, la colonización de las micorrizas se reduce (24).
Aparentemente, todas las poblaciones microbianas del suelo se autorregulan, incluso la planta regula a los microorganismos en su rizosfera. Así, al añadir microorganismos al suelo, pueden estar activos durante meses o un año y desaparecer pasado ese tiempo. Algunos autores encontraron que al incorporar el hongo ectomicorrízico Pisolithus tinctorius, protegía a las plántulas de Pinus sylvestris del ataque de Fusarium moniliforme y Rhizoctonia solani; esta protección duró un año (25).
Es muy interesante conocer la simbiosis en profundidad. La interacción comienza a través de señales y, dependiendo de los requerimientos de la planta y otros factores aún desconocidos, los microorganismos del suelo se regulan.
Los hongos endomicorrízicos también protegen las raíces contra los patógenos. Por ejemplo, una mezcla de hongos micorrízicos arbusculares (HMA) compuesta por Glomus aggregatum, Gigaspora margarita y Glomus intraradices suprimió la pudrición de la raíz por Fusarium solani en Phaseolus vulgaris, en condiciones de invernadero (26).
Incluso, los hongos endomicorrízicos pueden controlar nematodos como Meloidogyne incognita (27) y Meloidogyne javanica (28).
La reducción en la penetración de M. incognita en plantas endomicorrizadas puede deberse al hecho de que los HMA inducen cambios en la planta y, en respuesta, las raíces producen exudados, lo que sugiere que los exudados afectan la motilidad de los nematodos en el suelo. Otras posibilidades son la producción de compuestos nematicidas, aumento de la lignificación de las raíces, cambios en la composición de la pared celular y activación de los mecanismos de defensa de las plantas.
Se ha demostrado la acumulación de compuestos fenólicos, como fitoalexinas y flavonoides e isoflavonoides en raíces micorrízicas en presencia del nematodo. Los HMA también pueden aumentar la actividad de las enzimas de defensa como la peroxidasa, polifenoloxidasa, superóxido dismutasa, quitinasa y β 1,3 glucanasa (27). En general, los HMA presentes de forma natural en el suelo pueden ser benéficos para la agricultura sostenible, ya que mantienen la producción al reducir a los patógenos.
Por otra parte, Trichoderma es un hongo benéfico que ha demostrado eficacia en el control de patógenos de las raíces (29), incluidos los nematodos (30), debido a su capacidad para secretar compuestos volátiles y no volátiles, y metabolitos secundarios. Su mecanismo directo incluye competencia, micoparasitismo, antibiosis e inducción de mecanismos de resistencia de las plantas, así también mecanismos indirectos, como la inactivación de las enzimas producidas por el patógeno (31-33).
Entre los metabolitos secundarios se encuentran los terpenos, pironas, gliotoxinas, gliovirinas y peptaibols (34). Los metabolitos antifúngicos producidos por Trichoderma son epipolythiodioxopiperazines, peptaibols, pironas, butenólidos, piridonas, azafilonas, koningininas, esteroides, antraquinonas, lactonas, tricotecenos y otros (35, 36).
La expresión de genes relacionados con metabolitos secundarios en Trichoderma spp. depende de factores como la señalización del pH, las proteínas del complejo de terciopelo y las señales de comunicación con otros microorganismos (37).
Estos metabolitos exhiben bioactividad contra fitopatógenos como Macrophomina phaseolina, Pythium spp., Sclerotium rolfsii, Rhizoctonia solani, Fusarium oxysporum, Verticillium dahliae, Botrytis cinerea, Ascochyta citrullina, Phytophthora parasitica, P. cinnamomi, Leptosphaeria maculans, Clavibacter spp., Gaeumannomyces graminis, Colletotrichum gloeosporioides, y otros (34, 35, 38-40).
Plantas, microorganismos y carbono
Las plantas toman dióxido de carbono de la atmósfera y exudan algo de carbono en forma de sustancia azucarada a través de sus raíces. Esta secreción alimenta a los microorganismos del suelo. Cuando las plantas mueren, los microorganismos descomponen el carbono y lo utilizan para su metabolismo. Esta descomposición microbiana libera dióxido de carbono, por lo que el suelo almacena más carbono cuando está lleno de vida microbiana (41, 42).
Los hongos micorrízicos producen sustancias mucilaginosas (8) como la glomalina. Esta es una glicoproteína recalcitrante muy estable, con una vida media de hasta 42 años, y constituye el componente más grande de la materia orgánica del suelo (43), también, promueve la agregación del suelo. Los hongos micorrízicos transfieren más carbono al suelo que otros microorganismos (44) (Figura 3).
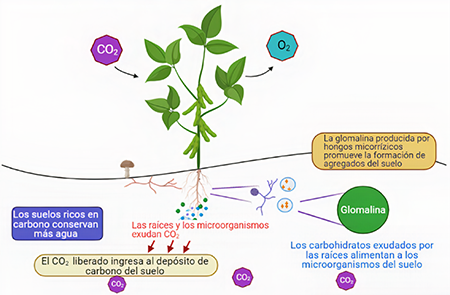
Figura 3
Esquema del dioxido de carbono (CO2) desde que ingresa al dosel del árbol hasta su filtración en el suelo, y la actividad de los microorganismos
Parte del carbono permanece en el suelo, desde días hasta algunos años. Los microorganismos pueden digerir este carbono, emitiendo así dióxido de carbono. Así es como el carbono puede permanecer durante años o décadas en un sitio (45). Una actividad agrícola importante es la aplicación de composta al suelo. La composta alberga microorganismos y puede retener carbono durante siglos. La labranza mínima hace que el carbono del suelo no esté expuesto al oxígeno y los agregados del suelo permanezcan intactos, protegiendo su carbono (45-47).
El secuestro de carbono del suelo es una forma natural de eliminar el dióxido de carbono de la atmósfera, y esto se puede lograr con prácticas agrícolas sostenibles. Estas prácticas mejorarán la capacidad de los suelos para almacenar carbono y ayudarán a minimizar los efectos del calentamiento global.
CONCLUSIONES
-
Esta revisión presenta cómo las plantas extraen CO2 del aire, sintetizan carbohidratos, que exudan de las raíces, para alimentar, atraer o repeler microorganismos. Adicionalmente, se destaca la importante actividad de los organismos y microorganismos del suelo para el beneficio de las plantas, con énfasis en lombrices de tierra, hongos micorrízicos y Trichoderma, debido a que pueden reducir las poblaciones de patógenos vegetales. Todos ellos, dentro de su especialidad, logran mediante la competencia por el espacio, o con mecanismos físicos y químicos, reducir los fitopatógenos del suelo.
-
Las lombrices de tierra, los hongos micorrízicos y Trichoderma presentes de forma natural en el suelo, pueden ser muy benéficos para la agricultura sostenible, manteniendo la producción y el equilibrio biológico en los suelos. Concluimos que el manejo integrado de cultivos promueve la competencia y el equilibrio, esenciales para mantener la salud del suelo y asegurar la producción de alimentos. Finalmente, el conocimiento de la diversidad de la biota edáfica en los agroecosistemas permite la implementación de estrategias de uso del suelo.
AGRADECIMIENTOS
Los autores agradecen a los Programas de Postgrado del Consejo Nacional de Ciencia y Tecnología (Conacyt), de la Facultad de Ciencias Agrotecnológicas de la Universidad Autónoma de Chihuahua, México.
BIBLIOGRAFÍA
ONU. Objetivos del Desarrollo Sostenible de la Agenda 2030 ONU. 2021 [citado 20/07/2021]. Disponible en: https://www.un.org/sustainabledevelopment/
Avila-Quezada G, Silva-Rojas HV, Sánchez-Chávez E, Leyva-Mir G, Martínez-Bolaños L, Guerrero-Prieto V, et al. Seguridad alimentaria: la continua lucha contra las enfermedades de los cultivos. Tecnociencia Chihuahua. 2016;10(3):133-142.
Cintora-Martínez EA, Leyva-Mir SG, Ayala-Escobar V, Avila-Quezada G, Camacho-Tapia M, Tovar-Pedraza JM. Pomegranate fruit rot caused by Pilidiella granati in Mexico. Australasian Plant Disease Notes. 2017;12(1):4.
García-González T, Sáenz-Hidalgo HK, Silva-Rojas HV, Morales-Nieto C, Vancheva T, Koebnik R, et al. Enterobacter cloacae, an emerging plant-pathogenic bacterium affecting chili pepper seedlings. The Plant Pathology Journal. 2018;34(1):1-10.
Avila-Quezada GD, Esquivel JF, Silva-Rojas HV, Leyva-Mir G, García-Avila C, Noriega-Orozco L, et al. Emerging plant diseases under a changing climate scenario: Threats to our global food supply. Emirates Journal of Food and Agriculture. 2018;30(6):443-450.
Sánchez-Chávez E, Silva-Rojas HV, Leyva-Mir G, Villareal-Guerrero F, Jiménez-Castro J, Molina-Gayoso E, et al. An effective strategy to reduce the incidence of Phytophthora root and crown rot in bell pepper. Interciencia. 2017;42(4):229-235.
Galvez ZYA, Burbano VEM. Solubilización de fosfatos: una función microbiana importante en el desarrollo vegetal. NOVA Publicación en Ciencias Biomédicas. 2015;12(21):67-79.
Madrid-Delgado G, Orozco-Miranda M, Cruz-Osorio M, Hernández-Rodríguez A, Rodríguez-Heredia R, Roa-Huerta M, et al. Pathways of phosphorus absorption and early signaling between the mycorrhizal fungi and plants. Phyton International Jornal of Experimental Botany. 2021;90(5):1321-1338.
Le Bayon RC, Bullinger-Weber G, Schomburg A, Turberg P, Schlaepfer R, Guenat C. (2017). Earthworms as ecosystem engineers: A review. Earthworms: Types, Roles and Research. NOVA Science Publishers, New York, 129-178.
Sánchez-Rosales R, Hernández-Rodríguez A, Ojeda-Barrios D, Robles-Hernández L, González-Franco A, Parra-Quezada R. Comparison of three systems of decomposition of agricultural residues for the production of organic fertilizers. Chilean Journal of Agricultural Research. 2017;77(3):287-292.
Sulaiman ISC, Mohamad A. The use of vermiwash and vermicompost extract in plant disease and pest control. In: Natural Remedies for Pest, Disease and Weed Control. Academic Press; 2020. p. 187-201.
Andleeb S, Ejaz M, Awan UA, Ali S, Kiyani A, Shafique I, et al. In vitro screening of mucus and solvent extracts of Eisenia foetida against human bacterial and fungal pathogens. Pakistan Journal of Pharmaceutical Sciences. 2016;29(3):969-977.
Prakash M, Gunasekaran G. Antibacterial activity of the indigenous earthworms Lampito mauritii (Kinberg) and Perionyx excavatus (Perrier). The Journal of Alternative and Complementary Medicine. 2011;17:167-170.
Jouni F. Synergistic interaction earthworm-microbiota: a role in the tolerance and detoxification of pesticides?. Agricultural sciences. Université d’Avignon. 2018. English. ffNNT: 2018AVIG0699ff. [citado 20/07/2021]. Disponible en: https://tel.archives-ouvertes.fr/tel-02074579/document
Edwards CA, Fletcher KE. Interactions between earthworms and microorganisms in organic-matter breakdown. Agriculture, Ecosystems & Environment. 1988;24(1-3):235-247.
Nath G, Singh K. Combination of vermicomposts and biopesticides against nematode (Pratylenchus sp.) and their effect on growth and yield of tomato (Lycopersicon esculentum). IIOAB Journal. 2011;2:27-35.
Rostami M, Olia M, Arabi M. Evaluation of the effects of earthworm Eisenia fetida-based products on the pathogenicity of root-knot nematode (Meloidogyne javanica) infecting cucumber. International Journal of Recycling of Organic Waste in Agriculture. 2014;3(2):58.
Edwards CA, Arancon NQ, Emerson E, Pulliam R. Suppressing plant parasitic nematodes and arthropod pests with vermicompost teas. Biocycle. 2007;48(12):38-39.
Euteneuer P, Wagentristl H, Steinkellner S, Scheibreithner C, Zaller JG. Earthworms affect decomposition of soil-borne plant pathogen Sclerotinia sclerotiorum in a cover crop field experiment. Applied Soil Ecology. 2019;138:88-93.
Charles NJ, Martín Alonso NJ. Uso y manejo de hongos micorrízicos arbusculares (HMA) y humus de lombriz en tomate (Solanum lycopersicum L.), bajo sistema protegido. Cultivos Tropicales. 2015;36(1):55-64.
González-Escobedo R, Muñoz-Castellanos LN, Muñoz-Ramirez ZY, Guigón López C, Avila-Quezada GD. Microbial community analysis of rhizosphere of healthy and wilted pepper (Capsicum annuum L.) in an organic farming system. Microbial Ecology. 2021; Por asignar
Zhang H, Franken P. Comparison of systemic and local interactions between the arbuscular mycorrhizal fungus Funneliformis mosseae and the root pathogen Aphanomyces euteiches in Medicago truncatula. Mycorrhiza. 2014;24:419-430.
Song Y, Chen D, Lu K, Sun Z, Zeng R. Enhanced tomato disease resistance primed by arbuscular mycorrhizal fungus. Frontiers in Plant Science. 2015;6:786.
Azcón R, Ambrosano E, Charest C. Nutrient acquisition in mycorrhizal lettuce plants under different phosphorus and nitrogen concentration. Plant Science. 2003;165(5):1137-1145.
Chakravarty P, Unestam T. Differential influence of ectomycorrhizae on plant growth and disease resistance in Pinus sylvestris seedlings. Journal of Phytopathology. 1987;120(2):104-120.
Eke P, Adamou S, Fokom R, Nya VD, Fokou PVT, Wakam LN, et al. Arbuscular mycorrhizal fungi alter antifungal potential of lemongrass essential oil against Fusarium solani, causing root rot in common bean (Phaseolus vulgaris L.). Heliyon. 2020;6(12):e05737.
da Silva Campos MA. Bioprotection by arbuscular mycorrhizal fungi in plants infected with Meloidogyne nematodes: A sustainable alternative. Crop Protection. 2020;135:105203.
Sharma M, Saini I, Kaushik P, Al Dawsari MM, Al Balawi T, Alam P. Mycorrhizal fungi and Pseudomonas fluorescens application reduces root-knot nematode (Meloidogyne javanica) infestation in eggplant. Saudi Journal of Biological Sciences. 2021;28(7): 3685-3691.
Stummer BE, Zhang Q, Zhang X, Warren RA, Harvey PR. Quantification of Trichoderma afroharzianum, Trichoderma harzianum and Trichoderma gamsii inoculants in soil, the wheat rhizosphere and in planta suppression of the crown rot pathogen Fusarium pseudograminearum. Journal of Applied Microbiology. 2020;129(4):971-990.
TariqJaveed M, Farooq T, Al-Hazmi AS, Hussain MD, Rehman AU. Role of Trichoderma as a biocontrol agent (BCA) of phytoparasitic nematodes and plant growth inducer. Journal of Invertebrate Pathology. 2021;107626.
Pozo-Serrano J, Cruz ERDL, Teresa-Cardoso M, Rodríguez-Pérez A, García-Pupo J, Pérez-Tejeda Y, et al. Efectividad antagónica In vitro de Trichoderma sp., frente a Stemphylium lycopersici. Cultivos Tropicales. 2019;40(3).
Köhl J, Kolnaar R, Ravensberg WJ. Mode of action of microbial biological control agents against plant diseases: relevance beyond efficacy. Frontiers in Plant Science. 2019;10:845.
Vinale F, Sivasithamparam K, Ghisalberti EL, Woo SL, Nigro M, Marra R. Trichoderma secondary metabolites active on plants and fungal pathogens. The Open Mycology Journal. 2014;8(1):127-139.
Vinale F, Ghisalberti EL, Sivasithamparam K, Marral R, Ritieni A, Ferracane R, Woo S, Lorito M. Factors affecting the production of Trichoderma harzianum secondary metabolites during the interaction with different plant pathogens. Letters in Applied Microbiology. 2009;48(6):705-711.
Khan RAA, Najeeb S, Hussain S, Xie B, Li Y. Bioactive secondary metabolites from Trichoderma spp. against phytopathogenic fungi. Microorganisms. 2020;8(6), 817.
Sonkar P, Chandra R, Singh R, Kumar S. Study on management of Fusarium oxysporum through different mode of action of Trichoderma spp. International Journal of Current Trends Science and Technology. 2018;8:20192-20200.
Macheleidt J, Mattern DJ, Fischer J, Netzker T, Weber J, Schroeckh V, et al. Regulation and role of fungal secondary metabolites. Annual Review of Genetics. 2016;50:371-392.
Shyamli S, Prem D, Rs T, Atar S. Production and antifungal activity of secondary metabolites of Trichoderma virens. Pesticide Research Journal. 2005;17(2):26-29.
Shi M, Chen L, Wang XW, Zhang T, Zhao PB, Song XY, Sun CY, Chen XL, Zhou BC, Zhang YZ. Antimicrobial peptaibols from Trichoderma pseudokoningii induce programmed cell death in plant fungal pathogens. Microbiology. 2012;158:166-175.
Sha S, Liu L, Pan S, Wang WM. Isolation and purification of antifungal components from Trichoderma harzianum ferment broth by high-speed counter-current chromatography. Chinese Journal of Biological Control. 2013;29(1):83-88.
Marler TE, Krishnapillai MV. Vertical strata and stem carbon dioxide efflux in Cycas trees. Plants. 2020;9(2):230.
Chikov VI, Akhtyamova GA, Khamidullina LA. Ecological significance of the interaction of photosynthesis light and dark processes. American Journal of Plant Sciences. 2021;12(04):624.
Ferrero Holtz EW, Gonzalez MG, Giuffré L, Ciarlo E. Glomalins and their relationship with soil carbon. International Journal of Applied Science and Technology. 2016;6(2):69-73.
Kaiser C, Kilburn MR, Clode PL, Fuchslueger L, Koranda M, Cliff JB, et al. Exploring the transfer of recent plant photosynthates to soil microbes: mycorrhizal pathway vs direct root exudation. New Phytologist. 2015;205(4):1537-1551.
Kittredge J. Soil Carbon Restoration: Can Biology do the Job?. NE Organic farming association, Massachusetts Chapter, 16. 2015. [citado 20/07/2021]. Disponible en: https://www.unifiedfieldcorporation.com/wp-content/uploads/2015/11/2015_White_Paper_web.pdf
Olivas‑Tarango AL, Tarango‑Rivero SH, Ávila‑Quezada GD. Pecan production improvement by zinc under drip irrigation in calcareous soils. Terra Latinoamericana, 2021;39:1-12.
Tarango-Rivero SH, Ávila-Quezada GD, Jacobo-Cuellar JL, Ramírez-Valdespino CA, Orrantia-Borunda E, Rodríguez-Heredia R, Olivas-Tarango AL. Chelated zinc and beneficial microorganisms: A sustainable fertilization option for pecan production. Revista Chapingo. Serie horticultura, 2022;28(3):145-159.
Author notes
*Autor para correspondencia: gdavila@uach.mx; gavilaq@gmail.com
Conflict of interest declaration
