INVESTIGACIÓN ORIGINAL
Medicamentos para el sistema nervioso con riesgo fetal: su uso antes y durante el embarazo en un seguro social argentino
Use of nervous system medications with fetal risk before and during pregnancy in an Argentine social security system
Medicamentos para el sistema nervioso con riesgo fetal: su uso antes y durante el embarazo en un seguro social argentino
Revista Colombiana de Obstetricia y Ginecología, vol. 76, no. 2, 4347, 2025
Federación Colombiana de Obstetricia y Ginecología; Revista Colombiana de Obstetricia y Ginecología
Received: 11 November 2024
Accepted: 18 June 2025
RESUMEN
Objetivo: describir la dispensación de fármacos para el sistema nervioso antes y durante el embarazo, según la categoría de riesgo fetal del medicamento.
Materiales y métodos: estudio descriptivo de utilización de medicamentos para el sistema nervioso en una cohorte histórica (2020-2023) de mujeres embarazadas, en un seguro de salud de Argentina. Los fármacos dispensados fueron categorizados en un grupo de riesgo fetal alto, y otro de no alto o desconocido, de acuerdo con la clasificación de agencias reguladoras seleccionadas. Se midió la prevalencia de uso antes y durante la gestación, así como la incidencia acumulada de retiro y de inicio durante el embarazo.
Resultados: de las 6.369 embarazadas incluidas, el 4,7 % recibió algún fármaco del grupo evaluado en el periodo previo y 18,8 % durante el embarazo. Este aumento se debió principalmente al paracetamol, que ascendió de 1,5 a 13,4 % durante el embarazo. Por el contrario, descendió el uso de ansiolíticos (1,6 a 0,7 %), antidepresivos (0,8 a 0,4 %) y antiepilépticos (0,7 a 0,4 %). La prevalencia de uso de medicamentos de alto riesgo descendió de 1,5 a 1 % durante el embarazo, con una incidencia acumulada de retiro de 81,3 % y de inicio del 0,7 %.
Conclusiones: la dispensación de medicamentos para el sistema nervioso con alto riesgo fetal fue baja en la cohorte estudiada. Es importante identificar el riesgo fetal de cada medicamento a fin de optimizar la selección del tratamiento para los trastornos del sistema nervioso en las mujeres gestantes. Se requieren estudios prospectivos que validen los patrones de utilización de medicamentos en la región y los desenlaces fetales y neonatales.
Palabras clave: Embarazo+ fármacos del sistema nervioso central+ utilización de medicamentos+ riesgo+ ginecología+ obstetricia+ Argentina.
ABSTRACT
Objective: To describe the dispensing of nervous system medications before and during pregnancy, according to the fetal risk category of the drug.
Material and methods: Descriptive drug utilization study of nervous system medications in a historical cohort (2020-2023) of pregnant women enrolled in a health insurance program in Argentina. Dispensed drugs were categorized into two groups: high fetal risk and non-high or unknown risk, based on the classification of selected regulatory agencies. The prevalence of use before and during pregnancy was measured, along with the cumulative incidence of drug discontinuation and initiation during pregnancy.
Results: Among the 6,369 pregnant women included, 4.7% received at least one drug from the evaluated group in the pre-pregnancy period, and 18.8% during pregnancy. This increase was mainly due to paracetamol, which rose from 1.5% to 13.4% during pregnancy. In contrast, the use of anxiolytics (1.6% to 0.7%), antidepressants (0.8% to 0.4%), and antiepileptics (0.7% to 0.4%) decreased. The prevalence of use of high-risk medications declined from 1.5% to 1% during pregnancy, with a cumulative discontinuation incidence of 81.3% and initiation incidence of 0.7%.
Conclusions: The dispensing of nervous system medications with high fetal risk was low in the studied cohort. Identifying the fetal risk associated with each drug is essential to optimize treatment selection for nervous system disorders in pregnant women. Prospective studies are needed to validate medication utilization patterns in the region and their associated fetal and neonatal outcomes.
Keywords: Pregnancy, central nervous system agents, drug utilization, risk, obstetrics, gynecology, Argentina.
INTRODUCCIÓN
El uso de medicamentos durante el embarazo implica cierto riesgo de daño fetal, especialmente durante las etapas críticas del desarrollo 1. Si bien algunos medicamentos tienen un potencial teratogénico bien establecido, como la talidomida, retinoides orales, fenitoína, entre otros 1, el riesgo de desarrollar malformaciones congénitas depende de la exposición sistémica de la madre y el feto, que está condicionada por la dosis, la duración, la vía de administración y el trimestre de gestación 2. Las primeras dos semanas del embarazo se conocen como el periodo "todo o nada", donde una exposición dañina puede resultar en la pérdida del embrión o no tener efecto alguno 2. Durante el primer trimestre hay un rápido desarrollo de los principales sistemas orgánicos, por lo que resulta especialmente vulnerable; la talidomida, por ejemplo, es teratogénica en una estrecha ventana temporal entre los días 20 y 36 desde la fertilización 3. Durante el segundo y tercer trimestre la teratogénesis es menos frecuente, pero los fármacos pueden alterar el crecimiento y la función de órganos y tejidos normalmente formados, como las tetraciclinas, que afectan el desarrollo de los huesos y dientes fetales 4, o los opioides o antidepresivos en el tercer trimestre, que pueden favorecer un cuadro de abstinencia o síndrome de mala adaptación neonatal 2.
Durante la gestación no es posible suspender todos los medicamentos ya que hay patologías como hipertensión arterial, diabetes, migraña severa, algunos trastornos psiquiátricos y la epilepsia que requieren la continuidad del tratamiento farmacológico 5-7. Algunos de los medicamentos utilizados para estas enfermedades pueden ser teratógenos, entre estos el valproato, un antiepiléptico 8; el carbonato de litio, esencial para el trastorno bipolar 9; algunos antipsicóticos 10 y las benzodicepinas para la ansiedad 11. Por otra parte, existen condiciones obstétricas, como la preeclampsia severa, que requieren el uso de antihipertensivos para prevenir complicaciones 5.
Para evaluar el uso de fármacos durante el embarazo, los enfoques metodológicos empleados son las encuestas y el análisis secundario de bases de datos administrativas 12. Las bases de datos de dispensaciones se consideran más sensibles para detectar la exposición a fármacos durante el embarazo que las encuestas a la madre o los registros de la historia clínica 13-15. No obstante, existe discrepancia en la asignación del riesgo fetal de los fármacos entre las diferentes fuentes disponibles. Comparando los sistemas australiano, estadounidense y sueco, se encontró que solo el 26 % de 236 medicamentos analizados fueron clasificados por las tres agencias en la misma categoría de riesgo 16.
Investigaciones previas internacionales 17 y en nuestro país 18 han documentado que el uso de medicamentos durante el embarazo es la norma, no la excepción, incluyendo aquellos de alto riesgo fetal. Además, dada la alta frecuencia de embarazos no planificados 19, resulta inevitable cierta exposición durante las semanas iniciales de la gestación. Aunque en Latinoamérica existen estudios sobre el uso de medicamentos en el embarazo, es poco lo que se ha publicado respecto al uso de fármacos para el sistema nervioso, ya sea los que se toman previamente y al inicio de la gestación o de novo durante esta 20-23. Así el objetivo de este estudio es describir la dispensación de fármacos para el sistema nervioso en las mujeres embarazadas antes y durante el periodo de gestación, con énfasis en las categorías consideradas de alto riesgo fetal, mediante el análisis de su dispensación en un seguro de salud.
MATERIALES Y MÉTODOS
Diseño y población. Se realizó un estudio descriptivo de utilización de medicamentos en una cohorte histórica que incluyó mujeres de 15 a 50 años de edad, que hubieran iniciado un embarazo entre el 1° febrero de 2021 y el 30 de septiembre de 2022, beneficiarias del Instituto de Obra Social de las Fuerzas Armadas y de Seguridad (IOSFA). Se excluyeron aquellas mujeres que en los nueve meses previos al inicio del embarazo hubieran cursado otro embarazo o no estuvieran aún afiliadas a IOSFA, con el fin de describir el uso de fármacos tanto durante la gestación como en el periodo previo a esta. Se utilizó un muestreo consecutivo de todas las mujeres que cumplieron los criterios de inclusión. Dado el registro histórico de IOSFA de 3.700 embarazos anuales, se esperaba tener alrededor de 6.200 registros de mujeres gestantes en los 20 meses del periodo de estudio.
El IOSFA es un seguro de salud obligatorio para los integrantes de las fuerzas armadas y de seguridad nacionales y sus familias. Cuenta con más de 550.000 afiliados de todas las edades distribuidos a lo largo del país. Para la atención del embarazo, la afiliada ingresa al Plan Materno Infantil (PMI), a través de la presentación de la certificación del diagnóstico de embarazo, considerando como fecha de inicio de la gestación la de 30 días previos al alta en el plan.
Procedimiento. Para este estudio se combinaron tres fuentes de información: 1) la base de datos de mujeres cubiertas por el PMI y el registro de embarazo en el periodo de estudio; 2) la base de datos general, para incorporar información de fecha de nacimiento de las embarazadas y datos de comorbilidades; y 3) la base de dispensaciones, desde los 270 días previos y durante todo el embarazo. Esta base de datos administrativa registra las dispensaciones de medicamentos con prescripción médica. Incluye la fecha de dispensación, marca comercial, composición del medicamento y unidades dispensadas. No se incluyen los medicamentos administrados en internación ni los de venta libre.
Se escogieron las participantes que cumplieron con los criterios de selección mencionados. Las comorbilidades se identificaron a través de los planes de cobertura específicos por enfermedad, como plan para diabetes, epilepsia, etc. De la base de datos de dispensación se tomaron de forma independiente las recibidas antes o durante la gestación. Se seleccionaron las dispensaciones de los medicamentos que actúan sobre el sistema nervioso, agrupados en la categoría “N” de la clasificación Anatómico-Terapéutico-Química (ATC - Anatomical Therapeutic Chemical Classification) de la Organización Mundial de la Salud (OMS) 24. El capítulo incluye anestésicos (N01), analgésicos (N02), antiepilépticos (N03), anti-Parkinson (N04), psicolépticos (N05) -que abarcan antipsicóticos (N05A), ansiolíticos (N05B) e hipnóticos y sedantes (N05C)-, psicoanalépticos (N06) -que incluyen antidepresivos (N06A) y psicoestimulantes (N06B)- y otros fármacos misceláneos. Aunque el clonazepam se ubica como antiepiléptico en la clasificación ATC, se agrupó con los ansiolíticos (N05B) 25-27. Para asignar el riesgo fetal de cada fármaco se utilizaron las categorías descritas por las agencias reguladoras australiana (TGA - Therapeutic Goods Administration) 28, estadounidense (FDA - Food and Drug Administration 29 y argentina (ANMAT - Administración Nacional de Medicamentos, Alimentos y Tecnología Médica) 30. Los fármacos se agruparon en dos categorías, los de riesgo alto fueron aquellos con posibilidad comprobada de daño fetal y los restantes, denominados de riesgo no alto o desconocido (NA/D), incluyeron los de riesgo bajo y aquellos de riesgo no especificado. Las categorías de riesgo y el algoritmo utilizado para su aplicación secuencial se muestran en la figura 1. En las combinaciones de dosis fijas, la categoría se estableció por el ingrediente farmacéutico activo (IFA) con categorización de embarazo más restrictiva 28.
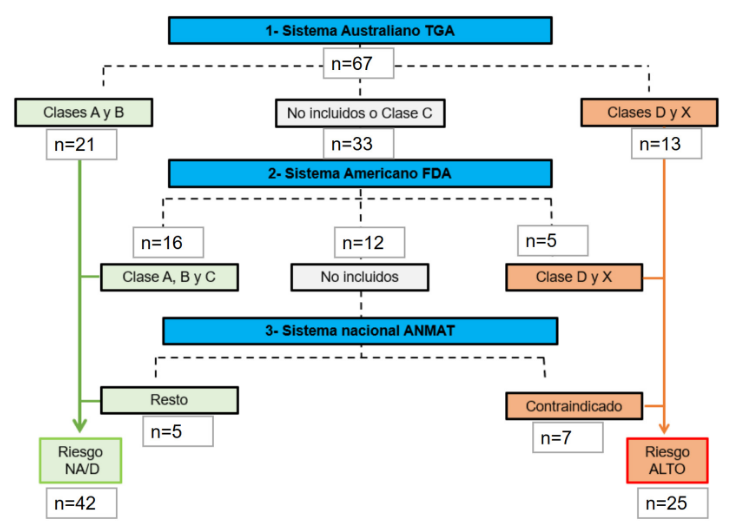
Figura 1.
Algoritmo utilizado para la clasificación de los fármacos de acuerdo con su riesgo de uso durante el embarazo. TGA: Therapeutic Goods Administration; FDA: Food Drug Administration; ANMAT: Administración Nacional de Medicamentos, Alimentos y Tecnología Médica. Riesgo NA/D: riesgo no elevado o desconocido.
Fuente: Autores
Se asumió a priori que las bases de datos de la Obra Social tienen validez, la cual se aceptó como satisfactoria, aunque no fue evaluada en forma independiente. Por otra parte, se consideró que, aunque la provisión del fármaco no equivale a su consumo efectivo, a los fines de este estudio se denominó “usuarias” a las receptoras de las dispensaciones. Dado que el embarazo resulta en una cobertura del 100 % de los gastos en medicamentos, se consideró que el riesgo de sesgos en la información sobre dispensaciones de medicamentos que requieren prescripción médica era bajo.
Variables medidas: se registraron la edad y las comorbilidades de las participantes; dispensación de medicamentos durante el embarazo, por semestre y la del período de 270 días previos al inicio de este; nivel de riesgo fetal (alto o NA/D). Se definió la prevalencia de uso de un fármaco o clase durante el embarazo o en el periodo previo como el cociente entre la cantidad de mujeres que recibieron al menos una dispensación de ese fármaco (o clase) en la etapa respectiva y el total de mujeres estudiadas (31). Se definió como nuevo uso durante el embarazo la dispensación de un fármaco (o clase) durante el mismo, que no se hubiera recibido en los nueve meses previos. La incidencia acumulada de nuevo uso en el embarazo se calculó como el cociente entre los casos de nuevo uso y el total de mujeres sin dispensaciones del fármaco (o clase) en los nueve meses previos al embarazo. Se definió como retiro en el embarazo la situación en la cual no se recibió, durante el mismo, ninguna dispensación de un fármaco (o clase) que se hubiera recibido en los nueve meses previos. La incidencia acumulada de retiro en el embarazo se calculó como el cociente entre las gestantes con retiro y el total de mujeres con dispensación del fármaco (o clase) dentro de los nueve meses previos al embarazo. Se definió como continuidad de uso en el embarazo de un fármaco (o clase) la situación en la que se dispensó un mismo fármaco (o clase) en ambos periodos.
Análisis estadístico. Se utilizaron el programa Excel y el paquete estadístico “R” versión 4.2.2 para Windows. Los datos cualitativos se describen como porcentajes y los cuantitativos como promedios con su desviación estándar (DE). Se presentan las características de la población estudiada, la dispensación de fármacos antes y durante el embarazo, y su agrupación según riesgo fetal. Para la elaboración del informe se utilizó la lista de verificación Record-PE, una adaptación de la guía Record a la farmacoepidemiología (32).
Aspectos éticos. El protocolo fue evaluado y aprobado por la Comisión de Bioética de la Fundación de la Federación Médica de la Provincia de Buenos Aires (Femeba). Los datos fueron anonimizados, agregando un código arbitrario que permitió identificar los consumos de una misma persona. Como la base de datos resultante impedía identificar a pacientes y prescriptores, se eximió al estudio del consentimiento informado de las participantes.
RESULTADOS
A partir de la base de datos del PMI, se seleccionaron las 6.399 embarazadas que cumplían el criterio de edad y cuyo embarazo se inició y finalizó dentro del periodo de estudio. Se excluyeron 30 (0,5 %) mujeres que habían estado embarazadas en los 270 días previos al inicio del embarazo índice, quedando 6.369 participantes como población de estudio (figura 2).
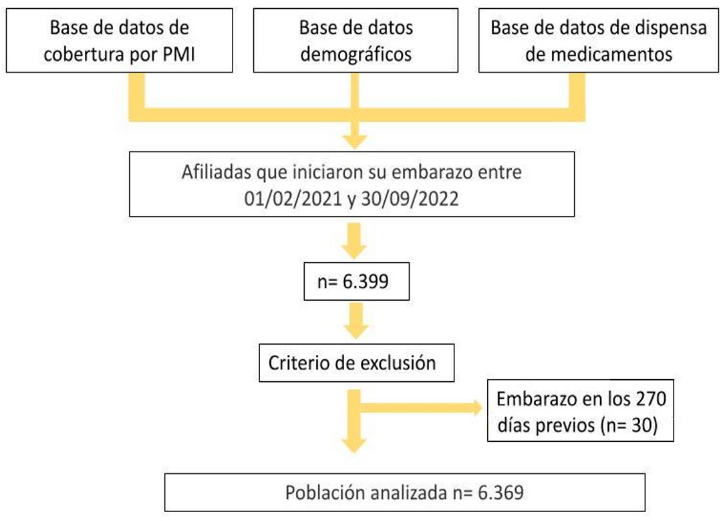
Figura 2.
Diagrama de flujo de la población seleccionada para el estudio.
Fuente: Autores.PMI: Plan materno infantil.
La edad promedio fue de 29 (DE ± 5,5) años. Un total de 494 (7,8 %) embarazadas registraba al menos una comorbilidad, destacando entre ellas la diabetes (n = 215; 3,4 %) y otros trastornos endocrinos (n = 234; 3,7 %). Solo 14 (0,2 %) mujeres estaban inscritas en programas específicos para enfermedades psiquiátricas y neurológicas (tabla 1).
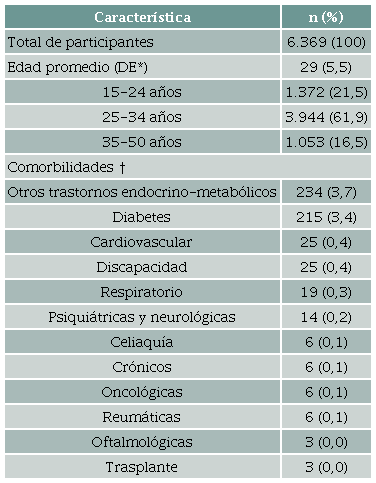
* Desvío estándar † Identificadas con los nombres asignados a los programas de cobertura específicos. Fuente: Autores.
Durante los 18 meses de seguimiento se registró un total de 45.519 dispensaciones, lo que representó un promedio de 7,1 (DE ± 7,6) por participante, con 22,2 % en la etapa previa al embarazo y 77,8 % durante este. Hubo 2.968 dispensaciones de fármacos del grupo N (6,5 % del total). La prevalencia de uso fue de 4,7 % (n = 298) en el periodo previo al embarazo y 18,8 % (n = 1196) durante el mismo (tabla 2). Las participantes recibieron dispensaciones de 67 fármacos diferentes, de los cuales 25 se categorizaron como de riesgo alto, y los 42 restantes como de riesgo NA/D ( figura 1).
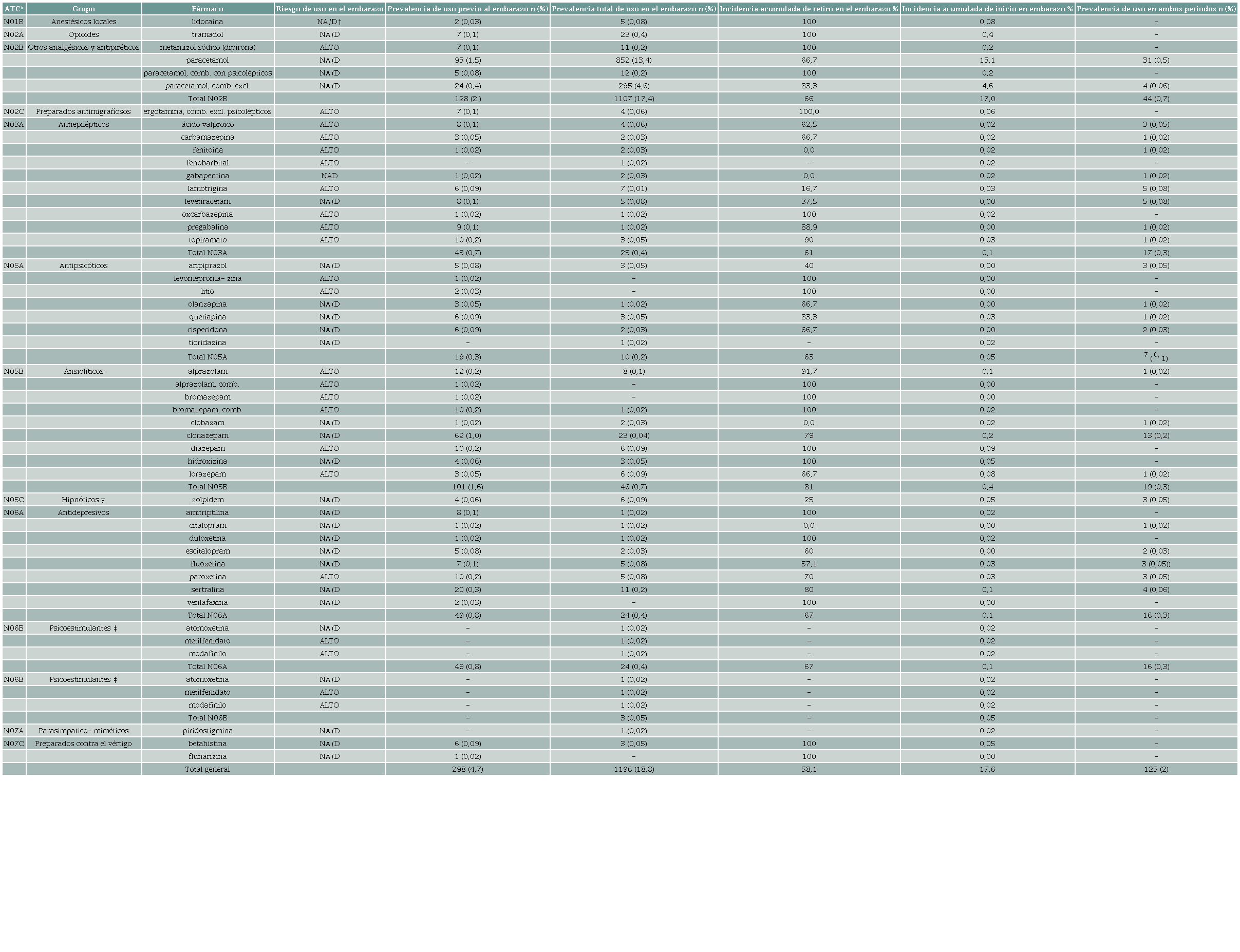
* ATC: clasificación AnatómicoTerapéutica-Química de la OMS. † NA/D: riesgo en el embarazo no elevado o desconocido. ‡ El nombre completo es “Psicoestimulantes, agentes usados para el trastorno de déficit de atención e hiperactividad, y nootrópicos”. Fuente: Autores.
Medicamentos dispensados antes del embarazo. En el periodo previo al embarazo, la mayor prevalencia de uso correspondió al grupo de antipiréticos y analgésicos no opioides (n = 128; 2,0 %), seguido por ansiolíticos (n = 101; 1,6 %), antidepresivos (n = 49; 0,8 %), antiepilépticos (n = 42; 0,7 %) y antipsicóticos (n = 19; 0,3 %) (tabla 2). Los fármacos con mayor prevalencia de uso en esta etapa fueron paracetamol solo (n = 93; 1,5 %) o en combinaciones (n = 29; 0,5 %), clonazepam (n = 62; 1 %), sertralina (n = 20; 0,3 %) y alprazolam (n = 12; 0,2 %). Entre los antiepilépticos se destacan el topiramato (n = 10; 0,2 %), pregabalina (n = 9; 0,1 %), ácido valproico (n = 8; 0,1 %) y levetiracetam (n = 8; 0,1 %). La incidencia acumulada de retiro para el conjunto de los fármacos del grupo N fue del 58,1 %, con 81 % para ansiolíticos, seguido por antidepresivos (67 %), analgésicos no opioides (66 %), antipsicóticos (63 %) y antiepilépticos (61 %). Solo 125 (2 %) embarazadas tuvieron continuidad en la dispensación de un mismo fármaco en ambos periodos (tabla 2).
Medicamentos dispensados durante el embarazo. Durante el embarazo, la prevalencia de uso de antipiréticos y analgésicos no opioides subió al 17,4 % (n=1107), mientras que se redujo la de antiepilépticos (n = 25; 0,4 %), ansiolíticos (n = 46; 0,7 %), antidepresivos (n = 24; 0,4 %) y antipsicóticos (n = 10; 0,2 %) (tabla 2). El fármaco del grupo N más dispensado durante el embarazo fue el paracetamol solo (n = 852; 13,4 %) y en combinaciones (n = 307; 4,8 %), seguido por clonazepam (n = 23; 0,4 %), tramadol (n = 23; 0,4 %), sertralina (n = 11; 0,2 %) y dipirona (n = 11; 0,2 %).
Dispensación de fármacos según el nivel de riesgo fetal. La prevalencia de uso de medicamentos de riesgo alto durante el periodo previo al embarazo fue de 1,5 % (n = 96) de las participantes y disminuyó durante el mismo a 1 % (n = 61). La incidencia acumulada de nuevo uso de medicamentos de riesgo alto en el embarazo fue del 0,7 %. Los medicamentos de alto riesgo dispensados fueron la dipirona (analgésico) en 11 mujeres (0,2 %), le siguieron el ácido valproico en 8 y la lamotrigina (antiepilépticos) en 6, el clonazepan (ansiolítico) en 23 y la paroxetina (antidepresivo) en 5 (tabla 2). Se identificó el uso de medicamentos con potencial daño comprobado como los derivados de ergotamina o los estimulantes metilfenidato y modafinilo. No se observó un desplazamiento de la dispensación hacia los fármacos antiepilépticos de riesgo NA/D durante el embarazo. Todos los antipsicóticos de alto riesgo fueron suspendidos en la gestación (tabla 2). La prevalencia de uso de los medicamentos con riesgo NA/D se incrementó en la gestación y a mayor edad gestacional, con un aumento gradual de la prevalencia de uso de los fármacos de riesgo NA/D con el valor estable de los de ALTO riesgo y de los ansiolíticos en el tercer trimestre de embarazo (tabla 3).
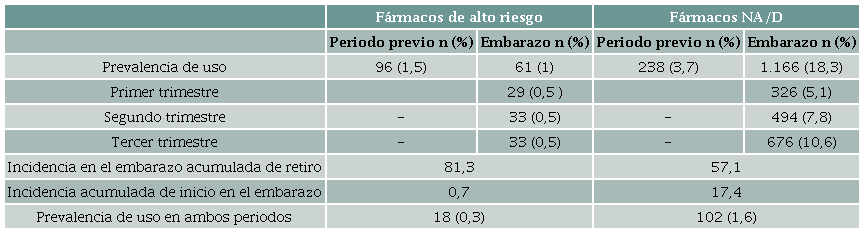
* NA/D: riesgo en el embarazo no elevado o desconocido. Fuente: Autores.
DISCUSIÓN
En este estudio de las dispensaciones de fármacos para el sistema nervioso a una cohorte de embarazadas se encontró una prevalencia de uso del 18,8 % para el total de medicamentos del grupo, y del 1 % para los fármacos considerados de alto riesgo durante el embarazo. Si bien más del 80 % de las dispensaciones de los medicamentos de alto riesgo en la etapa previa a la gestación se suspendieron con el embarazo, hubo un 0,7 % de las mujeres que iniciaron su uso durante el mismo, incluyendo antiepilépticos, antimigrañosos, psicoestimulantes, algunas benzodiazepinas y la dipirona.
La elevada prevalencia de uso de medicamentos durante el embarazo está liderada por los analgésicos no opioides, en particular paracetamol y sus combinaciones, tal como se describe en muchos otros estudios 15,18,33-37.
La prevalencia de uso de antiepilépticos previa al embarazo fue similar a la del 0,6 % de epilepsia estimada en Argentina 38. Durante el embarazo su uso descendió a valores similares a los de otras series 15,36. La prevalencia de uso de los antipsicóticos fue similar a la de otras series 15,36; la prevalencia de uso de antidepresivos mostró valores similares a los observados en informes de Japón 36, Suecia 15 y Argentina 18, sustancialmente inferiores al 4,2 % registrado en Nueva Zelanda 34. En cuanto al uso de sedantes e hipnóticos, nuestros hallazgos están en el rango del 0,5 al 1,3 % que informa la literatura 15,34,36. Nuestros hallazgos del aumento gradual de la prevalencia de uso de los fármacos NA/D durante el embarazo difiere de los de otras series, donde el uso de medicamentos del grupo N desciende a partir del primer trimestre 15,33.
Como fortalezas del estudio se tiene que este se fundamenta en una cohorte de base poblacional definida por su cobertura de salud y distribuida en todo el país, a partir de datos de dispensaciones 13,14. Además, a diferencia de otros estudios que comparan el uso de medicamentos individuales antes y durante el embarazo 1,33,34,36, este trabajo proporciona una medida de resumen de la exposición de las embarazadas a fármacos de alto riesgo fetal.
Una limitación inevitable de los estudios de dispensaciones es que no necesariamente reflejan el consumo real de los medicamentos entregados. Además, como los datos no incluyen los medicamentos de venta libre ni los usados en internación, esta información puede subestimar la exposición fetal a los fármacos. Es importante tener en cuenta que las clasificaciones del riesgo fetal de los medicamentos ubican entre un tercio y la mitad en la categoría C, incluir o no estas IFA (ingrediente farmacéutico activo) entre las de “riesgo alto” modifica sustancialmente la estimación del uso inapropiado en el embarazo. Este trabajo optó por un criterio conservador, utilizado en otros estudios 17, donde solo las categorías D y X se incluyeron en “alto riesgo”. En consecuencia, la dispensación de medicamentos de alto riesgo encontrada es solo el piso del fenómeno real, ya que la inclusión de un fármaco en nuestra categoría NA/D no garantiza su inocuidad para el feto.
CONCLUSIÓN
La dispensación de medicamentos para el sistema nervioso con alto riesgo fetal fue baja en la cohorte estudiada. Es importante identificar el riesgo fetal de cada medicamento a fin de optimizar la selección del tratamiento para los trastornos del sistema nervioso en las mujeres gestantes. Se requieren estudios prospectivos que validen los patrones de utilización de medicamentos en la región y los desenlaces fetales y neonatales.
REFERENCIAS
Gilbert-Barness E. Teratogenic Causes of Malformations. Ann Clin Lab Sci 2010;40:99-114.
Kennedy D, Batagol R. Drug safety in pregnancy. Aust Prescr. 2025;48:5-9. https://doi.org/10.18773/austprescr.2025.008.
Vargesson N. Thalidomide-induced teratogenesis: history and mechanisms. Birth Defects Res Part C Embryo Today Rev. 2015;105:140-56. https://doi.org/10.1002/bdrc.21096.
van den Anker J. Use of tetracyclines during the different stages of pregnancy. JAMA Netw Open. 2024;7:e2447322. https://doi.org/10.1001/jamanetworkopen.2024.47322.
Múnera A, Muñoz E, Ibarra J. Hipertensión arterial y embarazo. Rev Colomb Cardiol. 2021;28:3-13. https://doi.org/10.24875/rccar.m21000002.
Nurain M, Marmuji L, Mastura I, Michael F, Barakatun M, Yusof M, et al. Management of diabetes in pregnancy in primary care. J Acad Fam Physicians Mala 2019;14:55-9.
Vallejos Á, Rueda L, Santa,C. Uso de psicofármacos durante la gestación: necesidad vs seguridad. Rev Médica Risaralda. 2024;30:137-53. https://doi.org/10.22517/25395203.25400.
Pack A, Oskoui M, Williams S, Donley D, French J, Gerard E, et al. Teratogenesis perinatal, and neurodevelopmental outcomes after in utero exposure to antiseizure medication. Neurology. 2024;102:e209279. https://doi.org/10.1212/WNL.0000000000209279.
Betcher H, Montiel C, Clark C. Use of antipsychotic drugs during pregnancy. Curr Treat Options Psychiatry. 2019;6:17-31. https://doi.org/10.1007/s40501-019-0165-5.
Bruno C, Cesta C, Hjellvik V, Ulrichsen S, Bj0rk M, Esen B, et al. Antipsychotic use during pregnancy and risk of specific neurodevelopmental disorders and learning difficulties in children: A multinational cohort study. eClinicalMedicine. 2024;70:102531. https://doi.org/10.1016/j.eclinm.2024.102531.
Bellantuono C, Tofani S, Di Sciascio G, Santone G. Benzodiazepine exposure in pregnancy and risk of major malformations: A critical overview. Gen Hosp Psychiatry. 2013;35:3-8. https://doi.org/10.1016/j.genhosppsych.2012.09.003.
Nordeng H. Drug utilization in pregnant women. In: Elseviers M, Wettermark B, Almarsdóttir A, editors. Drug Util Res. John Wiley & Sons; 2016. p. 240-7. https://doi.org/10.1002/9781118949740.ch23.
Espnes M, Bjørge T, Engeland A. Comparison of recorded medication use in the Medical Birth Registry of Norway with prescribed medicines registered in the Norwegian Prescription Database. Pharmacoepidemiol Drug Saf. 2011;20:243-8. https://doi.org/10.1002/pds.2085.
Olesen C, Søndergaard C, Thrane N, Lauge Nielsen G, de Jong-van den Berg L, Olsen J, et al. Do pregnant women report use of dispensed medications? Epidemiology. 2001;12:497. https://doi.org/10.1097/00001648-200109000-00006
Stephansson O, Granath F, Svensson T, Haglund B, Ekbom A, Kieler H. Drug use during pregnancy in Sweden - Assessed by the prescribed drug register and the medical birth register. Clin Epidemiol. 2011;3:43-50. https://doi.org/10.2147/CLEP.S16305.
Addis A, Sharabi S, Bonati M. Risk classification systems for drug use during pregnancy: Are they a reliable source of information? Drug Saf. 2000;23:245-53. https://doi.org/10.2165/00002018-200023030-00006.
Daw J, Hanley G, Greyson D, Morgan S. Prescription drug use during pregnancy in developed countries: A systematic review. Pharmacoepidemiol Drug Saf 2011;20:895-902. https://doi.org/10.1002/pds.2184.
Marín G, Cañas M, Homar C, Aimetta C, Orchuela J. Uso de fármacos durante el período de gestación en embarazadas de Buenos Aires, Argentina. Rev Salud Pública. 2010;12:722-31. https://doi.org/10.1590/S0124-00642010000500003.
Bearak J, Popinchalk A, Beavin C, Ganatra B, Moller A, Tungalp O, et al. Country-specific estimates of unintended pregnancy and abortion incidence: A global comparative analysis of levels in 2015-2019. BMJ Glob Health. 2022;7:e007151. https://doi.org/10.1136/bmjgh-2021-007151.
Batista B, Correia J, Pacheco J, Oliveira V de, Gusmao W, Silva M, et al. Perfil de medicamentos utilizados por gestantes em bairro de extrema pobreza em Maceió: um estudo farmacoepidemiológico. Braz J Health Rev. 2023;6:18218-43. https://doi.org/10.34119/bjhrv6n4-327.
Gomes K, Moron A, Silva R, Siqueira A. Prevalence of use of medicines during pregnancy and its relationship to maternal factors. Rev Saude Publica 1999;33:246-54. https://doi.org/10.1590/s0034-89101999000300005.
Lutz B, Miranda V, Silveira M, Dal Pizzol T da S, Mengue S, da Silveira M, et al. Medication use among pregnant women from the 2015 pelotas (Brazil). Birth cohort study. Int J Environ Res Public Health. 2020;17:989. https://doi.org/10.3390/ijerph17030989.
Mendes G da R, Bortolini V de S, Menezes A, Colpo A, Barreto C da S, Cruz C da R, et al. Perfil farmacoepidemiológico de gestantes assistidas em uma unidade especializada de saúde na cidade de Bagé/RS. Braz J Dev. 2021;7:225182-22202. https://doi.org/10.34117/bjdv7n3-094.
WHO Collaborating Centre for Drug Statistics Methodology. ATC classification index with DDDs, 2019. Oslo, Norway; 2018.
Quaglia N, Paciaroni J, Elías M, Leiva M. Consumo de benzodiacepinas en una comuna de la región metropolitana de Rosario, provincia de Santa Fe, Argentina. Aten Primaria. 2009;41:520-1. https://doi.org/10.1016/j.aprim.2008.12.008.
Speranza N, Domínguez V, Pagano E, Artagaveytia P, Olmos I, Toledo M, et al. Consumo de benzodiazepinas en la población uruguaya. Rev Médica Urug. 2015;31:112-9.
Zorzanelli R, Giordani F, Guaraldo L, Matos G de, Brito A de, Oliveira M de, et al. Consumption of the benzodiazepine clonazepam (Rivotril®) in Rio de Janeiro State, Brazil, 2009-2013: An ecological study. Cienc Saude Coletiva. 2019;24:3129-40. https://doi.org/10.1590/1413-81232018248.23232017.
Therapeutic Goods Administration (TGA). Prescribing medicines in pregnancy database [Internet]. 2022. Disponible en: https://www.tga.gov.au/products/medicines/find-information-about-medicine/prescribing-medicines-pregnancy-database
Food and Drug Administration. Content and format of labeling for human prescription drug and biological products. Requirements for pregnancy and lactation labeling. Fed Regist [Internet]. 2008. Disponible en: https://www.federalregister.gov/documents/2008/05/29/E8-11806/content-and-format-of-labeling-for-human-prescription-drug-and-biological-products-requirements-for
Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). Vademecum Nacional de Medicamentos [Internet]. n.d. Disponible en: https://servicios.pami.org.ar/vademecum/views/consultaPublica/presentacion.zul
Hallas J, Støvring H. Templates for analysis of individual-level prescription data. Basic Clin Pharmacol Toxicol. 2006;98:260-5. https://doi.org/10.1111/j.1742-7843.2006.pto_257.x.
Langan S, Schmidt S, Wing K, Ehrenstein V, Nicholls S, Filion K, et al. The reporting of studies conducted using observational routinely collected health data statement for pharmacoepidemiology (RECORD-PE). BMJ. 2018;363:k3532. https://doi.org/10.1136/bmj.k3532.
Bérard A, Abbas-Chorfa F, Kassai B, Vial T, Nguyen K, Sheehy O, et al. The french pregnancy cohort: Medication use during pregnancy in the french population. PLOS ONE. 2019;14:e0219095. https://doi.org/10.1371/journal.pone.0219095.
Donald S, Sharples K, Barson D, Horsburgh S, Parkin L. Patterns of prescription medicine dispensing before and during pregnancy in New Zealand, 2005-2015. PLoS ONE. 2020;15:e0234153. https://doi.org/10.1371/journal.pone.0234153.
Lupattelli A, Spigset O, Twigg M, Zagorodnikova K, Mardby A, Moretti M, et al. Medication use in pregnancy: A cross-sectional, multinational web-based study. BMJ Open. 2014;4:e004365. https://doi.org/10.1136/bmjopen-2013-004365.
Nishigori H, Obara T, Nishigori T, Metoki H, Ishikuro M, Mizuno S, et al. Drug use before and during pregnancy in Japan: The Japan Environment and Children’s Study. Pharm Basel Switz. 2017;5:21. https://doi.org/10.3390/pharmacy5020021.
Sewberath V, Shankar A, Hindori A, Wickliffe J, Lichtveld M, Mans D. Prevalence and safety of prescription medicine use during pregnancy in the Republic of Suriname in the year 2017: A pharmacoepidemiological analysis. Adv Pharmacoepidemiol Drug Saf. 2021;10:249.
Melcon M, Kochen S, Vergara R. Prevalence and clinical features of epilepsy in Argentina: A community-based study. Neuroepidemiology. 2006;28:8-15. https://doi.org/10.1159/000097850.
FINANCIACIÓN
Cómo citar este artículo:
CONTRIBUCIÓN DE LOS AUTORES
Author notes
*Correspondencia: Hospital Elina de la Serna, Calle 8 n.° 483 (CP 1900), La Plata, Buenos Aires (Argentina). anahi.alvarez.rotondo@gmail.com
Conflict of interest declaration
