Reportes de caso
Cambios radiográficos después de radiocirugía/radioterapia estereotáctica corporal en cáncer de pulmón estadio I: reporte de caso
Radiographic Changes after Radiosurgery / Stereotactic Body Radiotherapy in Stage I Lung Cancer: Case Report
Cambios radiográficos después de radiocirugía/radioterapia estereotáctica corporal en cáncer de pulmón estadio I: reporte de caso
Universitas Médica, vol. 57, núm. 4, pp. 508-516, 2016
Pontificia Universidad Javeriana

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 03/03/2016
Revisado: 03/05/2016
Aprobación: 20/06/2016
Resumen: En la última década, la radioterapia estereotáctica corporal se ha implementado como tratamiento a pacientes con cáncer de pulmón estadio I, quienes son considerados inoperables o quienes rechazan el procedimiento quirúrgico. El artículo presenta el caso de uno de los primeros pacientes tratados con esta tecnología en un centro oncológico: un hombre de 72 años de edad con cáncer de pulmón estadio I, quien rechazó el manejo quirúrgico y se le realizó el tratamiento con radiocirugía, y con dos años de seguimiento, presentó cambios radiográficos, que inicialmente se interpretaron como progresión de la enfermedad. Además, se revisa la literatura relacionada con la interpretación de imágenes de seguimiento después del tratamiento.
Palabras clave: radioterapia, carcinoma de pulmón de células no pequeñas, consolidación, pulmonar, fibrosis pulmonar.
Abstract: Stereotactic radiotherapy body has been implemented in the last decade as a treatment for patients with stage I lung cancer, who are considered inoperable or who reject the surgical procedure. For one of the first patients treated with this technology in our Cancer Center presented; 72 year old man with lung cancer stage I reject the surgical management and underwent radiosurgery treatment and for 2 years follow-up, presented radiographic changes, which were initially interpreted as disease progression. Additionally, a review of the literature related to image interpretation follow-up after treatment is done.
Keywords: radiotherapy, lung carcinoma non-small cell lung consolidation, pulmonary fibrosis.
Introducción
En el mundo, el cáncer de pulmón de células no pequeñas es la primera causa de muerte, pues al año ocasiona 1,3 millones de muertes [1]. De acuerdo con las cifras de Globocan 2014, en Latinoamérica causa cerca de 56.000 muertes anualmente, de las cuales más del 90 % se presentan durante el primer año del diagnóstico. La mayor incidencia se registra en personas mayores de 55 años de edad para los dos géneros [2,3].
El tratamiento estándar del cáncer de pulmón de células no pequeñas en estadio I es quirúrgico (lobectomía), con tasas de supervivencia a cinco años del 60-70 % [4,5]. La radioterapia es una alternativa al tratamiento estándar en pacientes que no son candidatos quirúrgicos, por sus comorbilidades o porque rechazan la cirugía. Por desgracia, las tasas de supervivencia a cinco años son de entre el 10 % y el 30 %, con dosis de aproximadamente 60-66 Gy en fraccionamiento de 1,8 a 2 Gy. Las tasas de control local son en extremo pobres, con recaídas entre un 55 % y un 70 % [6].
En los últimos quince años, con los avances tecnológicos ha aparecido una nueva modalidad de suministrar la radiación: la radioterapia estereotáctica corporal, definida como una técnica de radioterapia emergente que proporciona una alta dosis radiación en un número limitado de fracciones (de una a cinco), con alta precisión en el volumen tumoral, con mínima dosis al tejido normal adyacente. Se ha difundido como una terapia alternativa con ventajas sobre la cirugía, como no ser una técnica invasiva, tener alta precisión, ofrecer un tiempo corto de tratamiento, ser un procedimiento ambulatorio, poder utilizarla a pesar de comorbilidades clínicas severas [7].
Se revisaron las principales características radiográficas como respuesta a radiocirugía con seguimiento imagenológico por tomografía axial computarizada (TAC). En este artículo se reporta un caso de un hombre de 72 años de edad con cáncer de pulmón estadio I, tratado con radiocirugía y quien obtuvo una adecuada respuesta clínica y tolerancia al tratamiento. No tuvo recaída imagenológica ni clínica en el seguimiento a dos años luego de haber finalizado el tratamiento.
Reporte del caso
Paciente de 72 años de edad quien consultó el servicio de radioterapia oncológica con un diagnóstico de cáncer de pulmón T1aN0M0, el 20 de noviembre del 2013, sin confirmación histológica.
16-10-2013. TAC de tórax: hipertensión pulmonar precapilar con prominencia de la arteria pulmonar de 36 mm, enfisema centrolobulillar y paraseptal en segmentos apicales. Lóbulo medio con imagen nodular espiculada de 16 × 15 mm, con densidad de tejidos blandos en el segmento LSD, compatible con carcinoma.
20-09-2013. Espirometría: FVC: 1,36; FEV1: 0,93 al 37 %; FEV1/FVC: 50 %.
25-10-2013. Ecocardiograma transtorácico: dentro de límites normales; baciloscopia seriada negativa; resonancia magnética nuclear cerebral, TAC de abdomen y gammagrafía ósea: negativa para lesiones metastásicas.
El caso de la paciente se llevó a junta de tórax con los servicios de oncología clínica, radioterapia, neumología, dolor y cuidado paliativo y cirugía de tórax, que determinó como primera opción el manejo con lobectomía. El paciente y la familia rechazaron este tipo de manejo quirúrgico y la biopsia de la lesión. Por esta razón se planteó como alternativa de manejo la radioterapia estereotáctica hipofraccionada.
El paciente fue simulado en un TAC y posicionado en Blue Bag Vaccum, con inmovilización diafragmática. El caso se calculó con una intensidad modulada, 10 campos, con energía de 6 MV y 50 puntos de control por campo en el sistema de planeación MÓNACO® 5.01 con el algoritmo de MonteCarlo Photon, grilla de 0,2 cm y desviación estándar de 1.
El tratamiento se realizó en un acelerador lineal Elekta Axesse a partir del 20 de diciembre 2013 con imágenes XVI (rayos X volumétricos). Previo a cada sesión, se realizaron correcciones traslacionales y rotacionales. La dosis total suministrada fue de 45 Gy en 3 fracciones, cada una de 15 Gy por día (figura 1 y tabla 1).
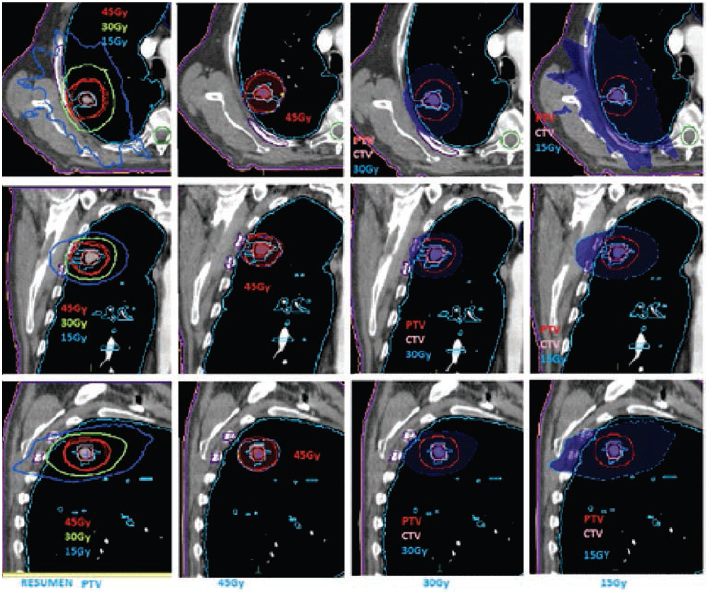
Figura 1
Hallazgos dosimétricos PTV: volumen blanco de planeación
En cortes tomográficos axiales, coronal y sagitales: observamos el adecuado cubrimiento de la dosis prescrita (isodosis color rojo) y el rápido arrastre de la dosis por fuera del PTV
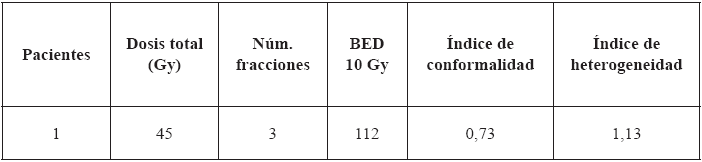
BED: dosis biológica efectiva.
En estudios de seguimiento el paciente presenta: 26/04/2014 TAC de tórax (a los 4 meses): el nódulo del lóbulo superior derecho progresa a una masa con cavitación central con paredes gruesas e irregulares, esto es, una masa espiculada de 43 mm × 40 mm × 43 mm. Se visualizaron incontables nódulos de aspecto disperso en ambos campos pulmonares con diámetros menores de 5 mm, enfisema pulmonar de predomino en lóbulos superiores y bronquiectasias bibasales. Se reportó como progresión tumoral por parte del servicio de radiología.
El caso del paciente se presentó de nuevo en una junta de tórax, que definió observación por probables cambios secundarios a la radiación. Se tomaron otros TAC cada 4 meses (figura 2).
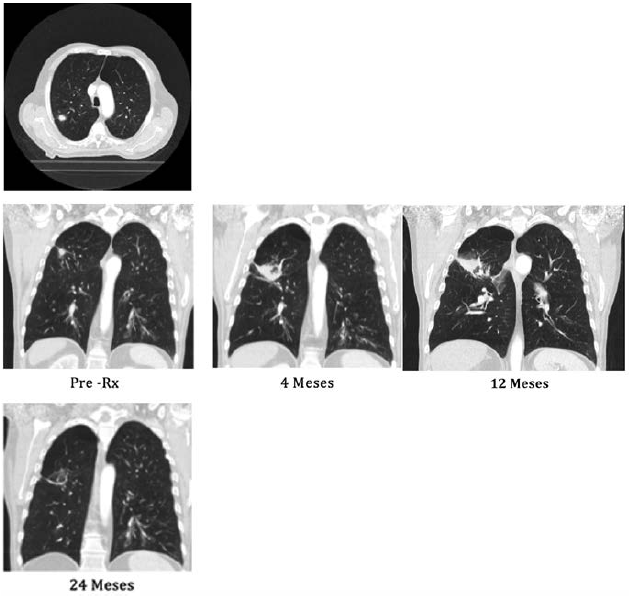
Figura 2
TAC de pretratamiento y posterior a radioterapia corporal estereotáctica en el paciente.
Antes del tratamiento: nódulo espiculado en el lóbulo superior derecho. A los 4-12 meses se evidencia una consolidación difusa y opacidad en vidrio esmerilado. A los 24 meses: respuesta completa al tratamiento y muestra un patrón cicatrizal con opacidad lineal
Discusión
En cáncer de pulmón de célula no pequeña estadio I, la cirugía es el tratamiento estándar; pero en aquellos pacientes considerados inoperables o quienes no aceptan el procedimiento quirúrgico, la radioterapia estereotáctica corporal se ha difundido como una alternativa. Los avances en la planificación de la radioterapia, como la radioterapia conformacional en 3D, la radioterapia de intensidad modulada con control de movimiento y la radioterapia guiada por imágenes, durante la última década, han llevado a aplicar esta técnica a diferentes localizaciones tumorales [8]. La radioterapia estereotáctica corporal puede lograr un control local y baja toxicidad en pacientes con cáncer pulmonar de célula no pequeña estadio I [9]. Hasta ahora, los resultados de los estudios descriptivos son prometedores, con protocolos de dosis entre 23 y 70 Gy, entregados entre 1 y 10 fracciones a tumores pulmonares estadio I. Así, se obtuvieron como resultados: tasas de control local del 60-100 % y tasas de supervivencia global del 12 al 74 %, a los 2-3 años de seguimiento [10,11].
El Colegio Americano de Tórax, en las guías para nódulos pulmonares solitarios mayores de 8 mm en TAC de tórax, pueden ser evaluados con tomografía por emisión de positrones. La probabilidad de malignidad también está determinada por la edad, la exposición a humo de tabaco y el tamaño de la lesión. Estas lesiones, con alta probabilidad pretest, deben ser llevadas a biopsia; sin embargo, en algunas instituciones el tratamiento con radioterapia estereotáctica corporal se lleva a cabo sin el diagnóstico histológico de la lesión. Esta aproximación la validó un estudio danés, que mostró que la combinación de historia clínica, examen físico y hallazgos imagenológicos radiográficos se correlaciona con el carcinoma de pulmón en más del 98 % de los casos. Nuestro paciente cumplía con todos los criterios mencionados y con el rechazo a la realización de la biopsia [12].
La toxicidad puede ocurrir hasta en el 8 % de los pacientes a quienes se le practica radioterapia estereotáctica corporal, y cuando se presenta, generalmente es grado 1 y 2 de toxicidad. El grado 1 incluye anorexia, fiebre, escalofríos, tos, eritema de la piel y malestar general, que ocurre típicamente dentro de unas pocas horas del tratamiento. Los síntomas del grado 2 incluyen tos (que requiere supresores), dolor pleural y dermatitis [13].
Sin embargo, un estudio publicado por Timmerman y colaboradores [14] con setenta pacientes con cáncer de pulmón de células no pequeñas estadio I reportó toxicidad severa grado 5 en seis pacientes que fallecieron secundaria a esta, los cuales tenían en común tumores de ubicación central. En nuestro caso, el paciente presentó toxicidad aguda grado I.
Respecto a los cambios radiográficos evidenciados en el TAC posterior a radioterapia estereotáctica corporal, la neumonitis por radiación asintomática clínicamente presenta una incidencia del 60 % al 100 % [15,16], y está dividida en cinco categorías: 1) consolidación difusa, 2) consolidación irregular y opacidad en vidrio esmerilado, 3) opacidad en vidrio esmerilado difusa, 4) opacidad en vidrio esmerilado irregular y 5) no hay evidencia de aumento de la densidad [17].
También se puede presentar fibrosis por radiación seis meses después de la radioterapia estereotáctica corporal y se clasifica en: 1) patrón convencional (consolidación, pérdida de volumen y bronquiectasias, que es menos extensa que la fibrosis por radiación convencional), 2) consolidación focal limitada alrededor del tumor y 3) patrón cicatrizal con opacidad lineal en la región del tumor asociado con la pérdida de volumen [17]. En nuestro caso, el paciente presentó, a los cuatro meses de seguimiento, hallazgos compatibles con neumonitis por radiación categoría 2; pero en los posteriores controles imagenológicos hubo resolución de estos hallazgos con presencia de patrón cicatrizal con opacidad lineal en la región del tumor asociado, con mínima pérdida de volumen.
Hoopes y cols. [18], de la Universidad de Indiana, reportaron una serie de casos de catorce pacientes que se sometieron a control imagenológico antes de la radioterapia estereotáctica corporal y después de esta con tomografía por emisión de positrones con fluordeoxiglucosa, previo a esta radioterapia y a las 2, 26 y 52 semanas después de ser llevada a cabo. Así se midió la mediana máxima de captación estándar (SUVmáx.). Trece pacientes mostraron control local, cuatro de los cuales presentaron un aumento inicial de la SUVmáx. en dos semanas, con posterior normalización a los doce meses de tratamiento. Solamente un paciente fracasó en el control local, el cual tuvo una disminución inicial en la SUVmáx. seguido por un aumento constante de la SUVmáx. en los seguimientos posteriores. Los estudios sugieren, entonces, que en el periodo posterior a radiocirugía la SUVmáx. puede permanecer elevada durante un periodo prolongado después de la radioterapia y que es probablemente debido a una respuesta inflamatoria [19].
Los estudios que evalúan el papel de la tomografía por emisión de positrones después de la radioterapia estereotáctica corporal son preliminares. Los resultados sugieren que el uso de 11 C-metionina no ofrece ventaja alguna sobre la fluordeoxiglucosa o el TAC [20], razón por la cual el control y el seguimiento imagenológico de nuestros pacientes se realiza por TAC.
Conclusiones
La radiocirugía, o también llamada radioterapia estereotáctica corporal, es una opción atractiva de tratamiento en pacientes con cáncer de pulmón de célula no pequeña estadio I, dada su buena respuesta con tasas de control local que van desde el 80 % al 95 % y a su baja toxicidad.
Basados en la interpretación imagenológica por TAC, cambios que en el seguimiento inicial pueden interpretarse como progresión tumoral, realmente son característicos de neumonitis posteriores a radiación con resolución a través del tiempo. En el caso de nuestro paciente, la radiocirugía fue una excelente opción de manejo con un adecuado control de la enfermedad y buena calidad de vida.
Referencias
1. Crabtree TD, Denlinger CE, Meyers BF, El Naqa I, Zoole J, Krupnick AS, et al. Stereotactic body radiation therapy versus surgical resection for stage I nonsmall cell lung cancer. J Thorac Cardiovasc Surg. 2010;140:377-86.
2. Timmerman R, Paulus R, Galvin J, Michalski J, Straube W, Bradley J, et al. Stereotactic body radiation therapy for inoperable early stage lung cancer. JAMA. 2010;303:1070-6.
3. Timmerman R, McGarry R, Yiannoutsos C, Papiez L, Tudor K, DeLuca J, et al. Excessive toxicity when treating central tumors in a phase II study of stereotactic body radiation therapy for medically inoperable early-stage lung cancer. J Clin Oncol. 2006;24:4833-9.
4. Rowe BP, Boffa DJ, Wilson LD, Kim AW, Detterbeck FC, Decker RH. Stereotactic body radiotherapy for central lung tumors. J Thorac Oncol. 2012;7:1394-9.
5. Mountain CF. A new international staging system for lung cancer. Chest. 1986;89:225S-33S.
6. Coy P, Kennelly GM. The role of curative radiotherapy in the treatment of lung cancer. Cancer. 1980;45:698-702.
7. Chang BK, Timmerman RD. Stereotactic body radiation therapy: a comprehensive review. Am J Clin Oncol. 2007;30(6):637-44.
8. Joanne ND, Clinton M, Sanjeev S. Stereotactic body radiotherapy for centrally located early-stage non-small cell lung cancer or lung metastases from the RSSearch® patient registry. Radiation Oncol. 2015;10:113.
9. DeRose F, Cozzi L, Navarria P, Ascolese AM, Clerici E, Infante E, et al. Clinical outcome of stereotactic ablative body radiotherapy for lung metastatic lesions in non-small cell lung cancer oligometastatic patients. Clin Oncol. 2016;28(1):13-20. doi: 10.1016/j.clon.2015.08.011
10. Ligang X, Yong Y, Spring K. Survey of stereotactic body radiation oncology for early staged non-small cell lung cancer in china. Int J Med Phys Clin Eng Radiat Oncolo. 2014;3(1):56-9. doi: 10.4236/ijmpcero.2014.31009
11. Yu JB, Soulos PR, Cramer LD, Decker RH, Kim AW, Gross CP. Comparative effectiveness of surgery and radiosurgery for stage i non-small cell lung cancer. Cancer. 2015 Jul;121(14):2341-9. doi: 10.1002/cncr.29359
12. Verstegen NE, Lagerwaard FJ, Haasbeek CJ, et al. Outcomes of stereotactic ablative radiotherapy following a clinical diagnosis of stage I NSCLC: Comparison with a contemporaneus cohort with pathologically proven disease. Radiother Oncol. 2011;101: 250-4.
13. Nanda RH, Liu Y, Gillespie TW, Mikell JL, Ramalingam SS, Fernandez FG, et al. Stereotactic body radiation therapy versus no treatment for early stage non-small cell lung cancer in medically inoperable elderly patients: A National Cancer Data Base Analysis. Cancer. 2015;121(23):4222-30.
14. Timmerman R, Papiez L, McGarry R, et al. Extracranial stereotactic radioablation: Results of a phase I study in medically inoperable stage I non - small cell lung cancer. Chest. 2003;124:1946-55.
15. Franks P, Jain MP. Stereotactic ablative body radiotherapy for lung cancer. Clin Oncol. 2015;27:280–9.
16. Pennathur A, Luketich JD, Heron DE, Schuchert MJ, Bianco V, Clump D, Burton S. Stereotactic radiosurgery/stereotactic body radiotherapy for recurrent lung neoplasm: An analysis of outcomes in 100 patients. Ann Thorac Surg. 2015;100(6):2019-24.
17. Kelley DL, Benninghoff JS. Medically inoperable peripheral lung cancer treated with stereotactic body radiation therapy. Radiat Oncol. 2015;10:120.
18. Fukumoto S, Shirato H, Shimzu S et al. Small-volume image-guided radiotherapy using hypofractionated, coplanar, and noncoplanar multiple fields for patients with inoperable Stage I nonsmall cell lung carcinomas. Cancer. 2002;95:1546-53.
19. Timmerman R, Papiez L, McGarry R, et al. Extracranial stereotactic radioablation: results of a phase I study in medically inoperable stage I non - small cell lung cancer. Chest. 2003;124:1946-55.
20. Hoopes DJ, Fletcher J, Tann M, et al. A prospective trial of serial FDG-PET in patients with medically inoperable stage I non-small cell lung cancer treated with hypofractionated stereotactic body radiotherapy (SBRT). ASTRO. 2006;66:825-6.
Notas de autor
rsanchez3004@yahoo.com
Información adicional
Cómo citar: Sánchez
Forero RA, Bruges Maya R, Pérez Moreno DP, Marín
Jiménez A. Cambios radiográficos después de
radiocirugía/radioterapia estereotáctica corporal en
cáncer de pulmón estadio I: reporte de caso. Univ Med. 2016;57(4):508-16. doi: http://doi.org/10.11144/Javeriana.umed57-4.crdr
Financiación: Recursos propios de los autores.
Conflictos de interés: Ninguno declarado.