Resumen: Se han descrito numerosas alteraciones del sueño inducidas por la epilepsia nocturna. La gabapentina (GBP), es utilizada como adyuvante o como tratamiento monoterapéutico, ya que induce una mejoría significativa en pacientes con convulsiones focales parciales o secundariamente generalizadas. En modelos animales experimentales de epilepsia, la GBP protege contra las convulsiones generadas con pentilentetrazol (PTZ). El objetivo de este trabajo fue investigar la eficacia de la GBP para proteger contra alteraciones motoras y del sueño provocadas por crisis convulsivas inducidas por PTZ. Se realizaron tres registros poligráficos a cuatro grupos de ratas Wistar macho. A cada grupo se les administró PTZ para inducir crisis convulsivas; 30 minutos antes de la administración de PTZ se aplicaron dosis de GB, un grupo recibió 15 mg/kg, otro grupo recibió 30 mg/kg y un tercer grupo recibió 60 mg/kg. Después de la administración de PTZ, se observaron las manifestaciones electrofisiológicas y conductuales que caracterizan a las crisis convulsivas. Además, los estados de vigilancia se alteraron significativamente, incrementándose la cantidad de vigilia, mientras que el sueño se inhibió durante un período de tiempo. La administración de dosis crecientes de GBP, tendió a inhibir la presencia de conductas motoras anormales, facilitando la presencia de sueño.
Palabras clave: epilepsia, vigilia, sueño, gabapentina, conducta animal, acción farmacológica.
Abstract: Numerous sleep disturbances induced by nocturnal epilepsy have been described. Gabapentin (GBP) is used as an adjuvant or as a monotherapeutic treatment, as it induces significant improvement in patients with partial or secondarily generalized focal seizures. In experimental animal models of epilepsy, GBP protects against seizures generated with pentylenetrazol (PTZ). The objective of this work was to investigate the efficacy of GBP to protect against motor and sleep disturbances caused by seizures induced by PTZ. Three polygraphic recordings were performed on four groups of male Wistar rats. Each group was given PTZ to induce seizures, 30 minutes before PTZ administration doses of GB were applied, one group received 15 mg/kg, another group received 30 mg/kg and a third group received 60 mg/kg. After administration of PTZ, electrophysiological and behavioral manifestations that characterize seizures were observed. In addition, vigilance states were significantly altered, increasing the amount of wakefulness, while sleep was inhibited for a period of time. The administration of increased doses of GBP tended to inhibit the presence of abnormal motor behaviors, facilitating the presence of sleep.
Keywords: epilepsy, wakefulness, sleep, gabapentin, animal behavior, pharmacologic effects.
Artículos
Trastornos de sueño y conductuales provocados por la epilepsia: Efecto protector de la Gabapentina
Sleep and behavioral disturbances induced by epilepsy: Protective effect of Gabapentin

Recepción: 08 Octubre 2020
Aprobación: 30 Mayo 2022
La epilepsia es una enfermedad neurológica que se considera un problema de salud importante y cuyo control continúa siendo un reto en la actualidad (Thijs, Surges, O´Brien, & Sander, 2019).
Por otra parte, el sueño es un estado reversible de inconsciencia, durante el cual el umbral sensorial permanece elevado, disminuyendo la capacidad de respuesta a estímulos medio-ambientales, dependiendo de la especie del reino animal, se presenta un estado de reposo en horas específicas del día, en un sitio y postura específica, con cambios de temperatura, tono muscular y movimientos oculares (Deboer, 2015).
Tanto en el humano como en otras especies de mamíferos, el sueño está integrado esencialmente por dos estados: Sueño de ondas lentas o sueño sin movimientos oculares rápidos (NMOR) y sueño de movimientos oculares rápidos (MOR) (Ayala-Guerrero et al., 2010; Kryger et al., 2017).
Se ha descrito desde hace tiempo que existe una relación funcional estrecha entre el sueño y la epilepsia (Malow, 2007), ya que tanto la presencia del sueño, particularmente el sueño NMOR, como la falta de sueño en general, tienen un efecto excitador sobre la génesis y la propagación de las crisis convulsivas (Foldvary-Schaefer, & Grigg-Damberger, 2006; Halász, 2013).
Cualquier tipo de alteración que presente el sueño, afecta la salud y la calidad de vida de los pacientes. En el caso de la epilepsia, se ha descrito que modifica la estructura del sueño e incrementa la latencia de inicio del sueño. Asimismo, reduce su eficiencia y su cantidad (Barreto et al., 2002; Manni, & Terzaghi, 2010). Además, tanto la epilepsia nocturna como la farmacoterapia antiepiléptica influyen en la presencia de síntomas diurnos como somnolencia excesiva y trastornos cognitivos.
Debido a que la excitabilidad del cerebro varía dependiendo de la fase de sueño, algunos tipos de epilepsia pueden originarse en un momento determinado del ciclo sueño-vigilia (Carreño, & Fernández, 2016; Malow et al., 1997; Minecan et al., 2002). Sin embargo, los mecanismos neurofisiológicos implicados en estos cambios de excitabilidad siguen siendo poco conocidos.
Un método para estudiar el efecto de la epilepsia sobre el sueño, está relacionado con el uso de modelos animales experimentales (Ayala-Guerrero et al., 2002; Ayala-Guerrero, & Mexicano, 2017). En este contexto, el pentilentetrazol (PTZ) se ha utilizado como agente inductor de convulsiones generalizadas (Klioueva et al., 2001), las cuales son similares a las de los humanos con epilepsia (Nehlig et al., 2006). Por lo cual el modelo de PTZ, se ha usado para analizar el efecto de las convulsiones generalizadas sobre la estructura del sueño y probar la eficacia de fármacos antiepilépticos (Akula et al., 2009)
El análisis del comportamiento mostrado durante las convulsiones, contribuye a establecer el nivel de gravedad alcanzado por la epilepsia. En este contexto, Racine (1972) describió un método que ha sido utilizado por diferentes grupos de investigación, sobre la base de la detección de diferentes comportamientos repetitivos, relacionados con la intensidad de la actividad convulsiva.
En relación con fármacos antiepilépticos, la Gabapentina (GBP) es un agonista del ácido γ-aminobutírico (GABA) que no tiene afinidad por el complejo receptor GABAA y pasa fácilmente a través de la barrera hematoencefálica. Aunque, no se ha identificado el mecanismo de acción preciso de la GBP en humanos (Sills, 2006), su uso clínico como fármaco único o adyuvante, induce mejoría en pacientes con crisis parciales focales secundariamente generalizadas (Czuczwar, & Patsalos, 2001; Larsen Burns et al., 2019). El mecanismo de acción de la GBP está asociado a su unión a una proteína auxiliar en la subunidad α2-δ de los canales de calcio dependientes de voltaje. Esta unión provoca la reducción del influjo de calcio en los terminales presinápticos, impidiendo la liberación de glutamato, noradrenalina y sustancia P, lo que explica su efecto antiepiléptico (Targas et al., 2014). En algunos modelos experimentales de epilepsia, se ha reportado que la GBP protege contra las crisis convulsivas inducidas por PTZ (Ayala-Guerrero et al., 2019; Dalby, & Nielsen, 1997).
Se tienen indicios de que la GBP mejora el sueño en pacientes con insomnio primario (Lo et al., 2010). Por lo cual, este fármaco antiepiléptico, pudiera ser efectivo para el tratamiento de diferentes tipos de insomnio (Robinson, & Malow, 2013; Schweitzer, & Feren, 2017). Además, la GBP incrementa el sueño NMOR (Foldvary‐Schaefer et al., 2002). En estudios futuros analizaremos el efecto sobre el sueño de la administración de únicamente GBP, para corroborar en nuestro modelo experimental lo descrito superficialmente en humanos. La evidencia de estos estudios nos lleva a plantear la hipótesis que la administración de GBP ejerce un efecto protector sobre las alteraciones en el sueño inducidas por las crisis convulsivas provocadas por el PTZ.
En consideración a las propiedades de la GBP descritas anteriormente, el objetivo de este trabajo fue investigar su eficacia para proteger contra las alteraciones del comportamiento y del sueño provocadas por las crisis convulsivas.
Se utilizaron 32 ratas Wistar macho adultas de 90-120 días de edad, con un peso de 250 a 350 g, estabuladas en el bioterio de la facultad de psicología de la Universidad Nacional Autónoma de México (UNAM). No se consideró la utilización de hembras debido a que su ciclo estral modifica las cantidades de sueño NMOR y MOR (Swift et al., 2020).
Polígrafo marca Grass modelo 7, cámara web Logitech modelo C170. Además, pentobarbital sódico marca PiSA agropecuaria, convutin (Gabapentina) marca APOTEX y pentilentetrazol marca SIGMA-ALDRICH.
Bajo anestesia general (pentobarbital sódico; 50 mg/kg ip), se colocó un par de electrodos de acero inoxidable en el área anterior (2 mm anterior a bregma 2,5 mm lateral a la línea media) y otro par en el área posterior (5 mm posterior a bregma 2,5 mm lateral a la línea media) del cerebro, para monitorear la actividad eléctrica cerebral bajo diferentes condiciones experimentales. Además, se registró el electro-oculograma (EOG) mediante dos electrodos de acero inoxidable, colocados en el canto externo e interno del ojo derecho. El electromiograma (EMG) se obtuvo por medio de dos filamentos de acero inoxidable insertados en los músculos de la nuca.
Los electrodos se soldaron a un conector, el cual era fijado en el cráneo con cemento acrílico. Los animales conectados a los cables de registro, se colocaban por separado en cajas transparentes de plexiglás, para observar y valorar su comportamiento a lo largo de los períodos experimentales y relacionarlo con los registros electrofisiológicos.
Los animales fueron separados en 4 grupos diferentes de 8 individuos cada uno y tenían acceso libre a alimentos y agua, manteniéndose a una temperatura ambiental de 23 ± 2 ° C, bajo un ciclo de luz-oscuridad de 12 h (de 07 a 19 h y de 19 a 07 h). En los cuatro grupos se administró PTZ de forma subcutánea (50 mg/kg). En tres grupos, 30 minutos antes de la administración de PTZ se aplicaron dosis de GB de forma intraperitoneal, un grupo de dosis baja (DB) recibió 15 mg/kg, un grupo de dosis media (DM) recibió 30 mg/kg, y un grupo de dosis alta (DA) recibió 60 mg/kg. Mientras que un grupo solamente recibió una dosis de PTZ.
Día 1, de línea base, en el cual los animales recibieron solo la aplicación de solución salina.
Día 2, de tratamiento, en el cual se administraron PTZ y GBP en los grupos respectivos.
Día 3, de postratamiento, no se administraron sustancias.
Durante estos tres días se realizaron los registros electrofisiológicos y conductuales durante 9 horas continuas (10 a 19 h), a una velocidad del papel de 3 mm/s, obteniéndose muestras a otras velocidades con el objeto de confirmar la calidad de los registros. Además, se hicieron videograbaciones del comportamiento.
Para analizar los niveles de intensidad de la actividad convulsiva alcanzada por los animales, se usó la escala de Racine que considera desde movimientos de masticación y mioclonías faciales, hasta contracciones tónicas y clónicas generalizadas (Racine, 1972) (Tabla 1).
Los registros electrofisiológicos obtenidos se analizaron visualmente para identificar los estados de vigilancia (vigilia, sueño NMOR y MOR) y se cuantificó el tiempo total empleado por los animales en cada uno de los estados durante las 9 horas de registro. Tanto los registros electrofisiológicos como las videograbaciones del comportamiento fueron calificados de forma independiente por dos experimentadores con bastante experiencia ya que han venido participando en análisis similares, en caso de desacuerdo se recurría a una tercera opinión.

Por medio de la prueba de Shapiro-Wilk se determinó que no todas las variables tenían una distribución normal por lo cual se llevaron a cabo análisis no paramétricos. Se realizó análisis de tipo intra-grupal mediante la prueba de Friedman, con la cual se comparó el tiempo empleado por los animales en cada estado de vigilancia bajo las condiciones experimentales mencionadas anteriormente. También, se realizó un análisis de tipo inter-grupal de cada estado de vigilancia y conductas convulsivas mediante la prueba de Kruskal-Wallis. El valor de significancia se estableció con un valor p <.05.
Todos los animales fueron tratados de acuerdo con las regulaciones especificadas por el Comité de Bioética y la Norma Mexicana para el cuidado de la producción y el uso de animales de laboratorio (NOM-062-Z00-1999).
Los animales presentaron tres estados diferentes de vigilancia con características electrofisiológicas y conductuales determinadas: durante la vigilia, la actividad cerebral estuvo constituida por ondas rápidas de baja amplitud y se presentaron potenciales musculares relacionados con movimientos del animal; mientras que durante el sueño NMOR la actividad cerebral fue lenta y de gran amplitud. Al presentarse el sueño MOR, la actividad cerebral fue semejante a la de la vigilia y se presentaron potenciales relacionados con sacudidas musculares (Figura 1).
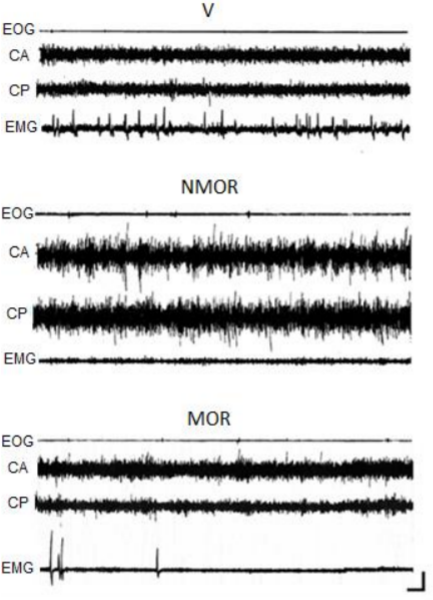
En el primer día no se evaluó la escala de Racine, ya que no se indujo actividad convulsiva. En el tercer día pocos animales presentaron alteraciones conductuales, independientemente del grupo al que pertenecieran, por lo cual el análisis estadístico se realizó considerando las conductas del segundo día correspondiente a la administración de las sustancias.
De manera general, la administración de PTZ, indujo convulsiones tónico-clónicas generalizadas en todos los animales, independientemente del grupo. Las convulsiones se caracterizaron por una fase tónica con extensión de las extremidades posteriores y una fase clónica con mioclono de las extremidades anteriores y posteriores. Las alteraciones motoras inducidas por la administración de PTZ se instalaron progresivamente. Estas consistían en la inclinación de la cabeza, movimientos masticatorios y contracciones mioclónicas de la cara y de las extremidades.
Con la prueba Kruskal-Wallis se encontraron diferencias significativas entre los cuatro grupos en las conductas evaluadas con la escala de Racine (p=.013; Chi-cuadrado=10.8; grados de libertad=3). El grupo que recibió solamente PTZ, fue el que tuvo mayor número de estados asociados a conductas convulsivas, mientras que la administración de GBP redujo la cantidad e intensidad de las alteraciones conductuales de acuerdo a la dosis administrada (Figura 2). Los animales que recibieron dosis media y alta de GBP ya no alcanzaron el nivel máximo de la escala de Racine. De acuerdo a estos datos, la cantidad total de alteraciones conductuales inducidas por la epilepsia, se reducía a medida que la dosis de GBP administrada aumentaba, Asimismo, se reducía la intensidad de la respuesta conductual.
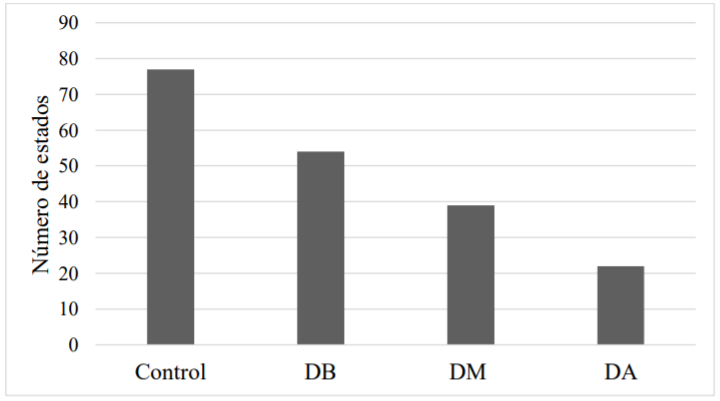
En el grupo que recibió únicamente PTZ, la administración de este fármaco (Día 2) provocó que la cantidad de vigilia se incrementara de manera significativa y que disminuyeran tanto la cantidad de sueño NMOR como la de MOR (Tabla 2). El efecto del PTZ sobre la reducción del sueño NMOR y MOR fue inmediato, precediendo la aparición de actividad convulsiva. La duración de este efecto inhibidor sobre del sueño permaneció durante todo el registro. Al día siguiente (Día 3), se observó una recuperación, ya que los valores de estos 3 estados de vigilancia fueron similares a los del día 1 de línea base (Tabla 2).
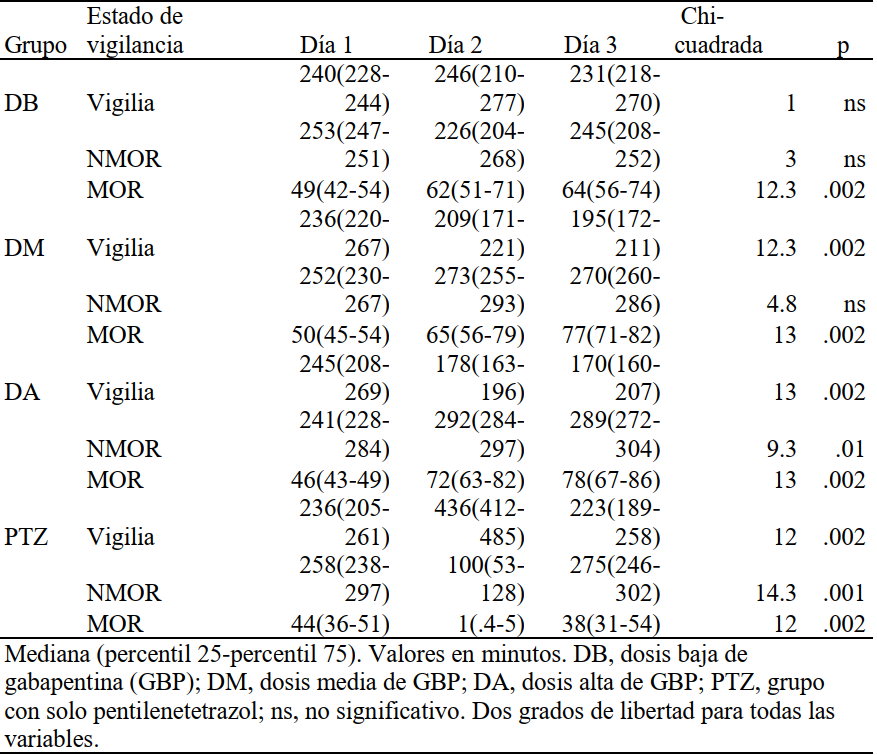
De manera general, las alteraciones del sueño producidas por la administración de PTZ disminuyeron por el efecto de la GBP. La mejoría del sueño dependía de la dosis administrada de este fármaco anticonvulsivo. En el grupo de DB, con dosis de GBP de 15 mg/kg, los valores de vigilia y sueño NMOR no tuvieron diferencias significativas entre los tres días de registro. En contraste, la cantidad de sueño MOR aumentó significativamente el día de la administración (Día 2) de la GBP, manteniéndose por encima de los niveles de la línea base durante el tercer día de registro (Tabla 2).
En el grupo de DM, aunque aumentó ligeramente la cantidad de sueño NMOR, no presentó diferencias significativas en los tres días. En contraste, en comparación con el día 1 de registro, la cantidad de vigilia disminuyó y la del sueño MOR se incrementó de forma significativa. En el tercer día, la cantidad de vigilia alcanzó niveles mínimos y mientras que la del sueño MOR mostró niveles máximos (Tabla 2). En el grupo de DA en los tres estados de vigilancia se encontraron diferencias significativas entre los tres días de registro. En el segundo día, los animales del grupo DA mostraron incremento significativo tanto del sueño NMOR como del MOR, mientras que disminuía la cantidad de vigilia. Estos niveles de los tres estados de vigilancia permanecieron en el tercer día, es decir, se manifestaba todavía el efecto de la GBP (Tabla 2).
Con la prueba de Kruskal-Wallis se tuvieron tres grados de libertad para todas las variables. En el día 1, no se encontraron diferencias significativas relacionadas con la duración de los estados de vigilancia entre los grupos de animales en la vigilia (p=.927; chi-cuadrado=.5), sueño NMOR (p=.638; chi-cuadrado=2) y sueño MOR (p=.329; chi-cuadrado=3.4). En el día 2, se encontraron diferencias significativas entre los grupos en vigilia (p<.001; chi-cuadrado=24), sueño NMOR (p<.001; chi-cuadrado=23) y sueño MOR (p<.001; chi-cuadrado=19). En este segundo día, la cantidad de vigilia fue mayor en el grupo que recibió solamente PTZ, el cual desarrolló de manera intensa la actividad convulsiva, mientras que la cantidad de sueño NMOR y MOR fue menor en este grupo comparado con los que recibieron GBP.
Finalmente, en el día 3, se tuvieron diferencias significativas en vigilia (p=.003; chi-cuadrado=14) y sueño MOR (p<.001; chi-cuadrado=20), mientras que en el sueño NMOR no hubo diferencia entre los grupos (p=.13; chi-cuadrado=11). En este día, el grupo que recibió solamente PTZ tuvo los valores menores de sueño MOR, mientras que el grupo con mayor cantidad de vigilia fue el de DB.
En esta investigación, se corroboró la utilidad del modelo animal de epilepsia generalizada, ya que los animales presentaron la gama de manifestaciones electrofisiológicas y de comportamiento descritas anteriormente por diversos autores (Avila-Luna et al., 2019; Racine, 1972; Sayyah et al., 2005; Wang, & Quin, 2010). Los automatismos motores inducidos por el PTZ se manifestaron casi inmediatamente, incrementándose progresivamente de intensidad hasta dar origen a convulsiones generalizadas. Estas alteraciones del comportamiento motor, acompañadas por actividad electroencefalográfica anormal se relacionan con alteraciones bioquímicas e histológicas semejantes a las de pacientes con epilepsia (Huang et al., 2001; Sajadian et al., 2015).
En base a diversos hallazgos experimentales, se ha sugerido que las neuronas del núcleo Pontis caudalis participan en la generación y mantenimiento de las crisis convulsivas (Faingold, 1987; Merrill et al., 2005; Raisinghani, & Faingold, 2005). En las terminaciones sinápticas de este núcleo, el PTZ se une al sitio de unión de la picrotoxina del complejo receptor GABA, alterando la actividad del canal de cloruro acoplado al sitio GABA / Benzodiacepina (Manjarrez et al., 2001) bloqueando la inhibición postsináptica mediada por el GABA (Corda et al., 1990). Por lo anterior, se considera que las convulsiones provocadas por el PTZ no están mediadas directamente por los receptores de las benzodiacepinas, sino que dependen de otros mecanismos (MacDonald, & Barker, 1977; Huang et al., 2001).
La administración de PTZ redujo significativamente la cantidad de sueño NMOR y MOR. La inhibición de ambos tipos de sueño se mantuvo durante un periodo de tiempo relativamente largo. No obstante, durante el tercer día de registro, la cantidad de sueño regresó a los niveles basales, hallazgos que concuerdan que los reportados previamente (Mexicano et al., 2005).
El insomnio provocado por la epilepsia inducida por PTZ, pudiera estar relacionado con la activación de los núcleos de la formación reticular (Franco-Pérez et al., 2015; Hantraye et al., 1987; Korpi et al., 2002) que forman parte del sistema que mantiene despiertos a los organismos, consecuentemente al ser estimulados químicamente, inducen un incremento significativo de la vigilia. El PTZ reduce la conductancia de los canales de cloruro lo que facilita la hiperexcitación neuronal que provocaría diferentes niveles de activación motora y la instalación del insomnio (Hansen et al., 2004; Pellmar, & Wilson, 1977). Sin embargo, el mecanismo por el cual esta droga provoca su acción, aún no se conoce con precisión.
En este estudio, se puso en evidencia una relación entre la dosis de GBP y la reducción de la gravedad de las alteraciones de la conducta motora y del sueño. Estos hallazgos sugieren un efecto inhibitorio ejercido por la GBP sobre la actividad epiléptica inducida por PTZ, además de favorecer los mecanismos inductores y de mantenimiento del sueño. Este efecto, puede deberse al incremento en GABA extracelular y su relación con la activación de canales de cloruro que inducen inhibición postsináptica por hiperpolarización. También, con el bloqueo en el transporte de Ca ++ al interior neuronal, lo que contribuye a una reducción de la excitabilidad neuronal (Offord, & Isom, 2016; Rose, & Kam, 2002; Sills, 2006). La inhibición de la epilepsia por la administración de GBP podría deberse a su acción sobre el núcleo Pontis oralis, lo que facilitaría los mecanismos desencadenantes del sueño en concordancia con lo descrito por otros autores (Cope et al., 2009; Santín, 2013; Valdizán et al., 1999).
Los resultados obtenidos en este trabajo experimental, pudieran ser un hallazgo importante para las terapias del sueño en pacientes que padecen epilepsia nocturna. En este contexto, resultados alentadores se han obtenido de un estudio de caso (Ayala-Guerrero, 2011), donde el paciente epiléptico después de la ingestión de GBP mostró una mejoría significativa ya que la eficiencia del sueño se incrementó de 40.76% a 86.50%, concomitantemente la fragmentación del sueño se redujo de 44 a 15 despertares durante toda la noche del registro. Además, la cantidad de fases de sueño MOR aumentó de 1 a 5 y el porcentaje de esta fase en relación con el tiempo total de sueño se incrementó de 6.41% a 27.50%. En conclusión, la GBP reduce significativamente la intensidad de las crisis epilépticas y favorece la inducción y mantenimiento del sueño. En estudios futuros analizaremos el efecto sobre el sueño de la administración de únicamente GBP para corroborar en nuestro modelo experimental sus propiedades hipnóticas.
Existe abundante literatura acerca de los efectos cognitivos y conductuales que originan las alteraciones del sueño (Kryger et al., 2017), por el cual, sería recomendable la utilización de fármacos que además de inhibir las crisis convulsivas inhiban o reduzcan dichas alteraciones.
Correspondence about this article should be addressed Fructuoso Ayala Guerrero: fayala@unam.mx



