Artículos Originales
Implante valvular aórtico percutáneo por vía transfemoral y apical. Impacto y consideraciones generales de ambos abordajes
Transapical and Transfemoral Aortic Valve Implantation. Impact and General Considerations of both Approaches
Implante valvular aórtico percutáneo por vía transfemoral y apical. Impacto y consideraciones generales de ambos abordajes
Revista Argentina de Cardiología, vol. 86, núm. 3, pp. 180-185, 2018
Sociedad Argentina de Cardiología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 17 Septiembre 2017
Aprobación: 28 Enero 2018
Resumen:
Introducción: El implante valvular aórtico percutáneo (TAVI) ha surgido como una alternativa terapéutica en pacientes con estenosis aórtica grave sintomática inoperables o de elevado riesgo quirúrgico. El acceso transapical surge como alternativa para aquellos pacientes con contraindicación de implante valvular aórtico percutáneo transfemoral.
Objetivo: Valorar la factibilidad y la reproducibilidad del implante valvular aórtico percutáneo transapical en nuestro centro y comparar la evolución a corto y mediano plazo con los pacientes sometidos a implante valvular aórtico percutáneo transfeoral.
Material y métodos: Se evaluó una cohorte retrospectiva de 80 pacientes tratados con implante valvular aórtico percutáneo transapical (n = 24) y transfemoral (n = 56) en nuestro centro. Se compararon las complicaciones relacionadas con el procedimiento según las definiciones VARC-2, y se analizó la mortalidad a corto y mediano plazo entre ambos grupos.
Resultados: Los pacientes del grupo transapical eran más añosos (83,6 ± 5 versus 80,0 ± 8,3; p = 0,04); presentaron mayor prevalencia de coronariopatía (el 75% versus el 44%; p = 0,04) y mayor prevalencia de vasculopatía periférica (el 37% versus el 16%; p = 0,01). El grupo transapical tuvo menor exposición a rayos X, (tiempo de fluoroscopia de 14,9 minutos ± 5,8 versus 22,9 minutos ± 8,7; p = 0,001); y una mayor tendencia a requerir diálisis luego del procedimiento (el 12,5% versus 1,8%, p = 0,13). El grupo transapical permaneció más tiempo internado (13,6 ± 23 días versus 7,2 ± 6,9 días, p = 0,05). La mortalidad a 30 días fue mayor en el grupo transapical (el 20,8% versus el 5,4%; p = 0,03) y al año (el 25% versus el 8,9%; p = 0,04).
Conclusiones: En nuestra experiencia, el implante valvular aórtico percutáneo transapical es factible y puede ser realizado como un procedimiento reproducible para pacientes no aptos para el implante valvular aórtico percutáneo transfemoral. El acceso transapical se asoció con mayor mortalidad durante el seguimiento, particularmente en el período posoperatorio a 30 días, lo que coincide con varios reportes publicados.
Palabras clave: Estenosis de la Válvula Aórtica, Reemplazo de la Válvula Aórtica Transcatéter, Procedimientos Endovasculares.
Abstract:
Background: Transcatheter aortic valve implantation (TAVI) has emerged as a therapeutic option in inoperable or high surgical risk patients with severe symptomatic aortic stenosis. The transapical approach is an alternative access for patients with contraindications for the transfemoral access.
Objective: The aim of this study was to evaluate the feasibility and reproducibility of transapical TAVI and compare the short and mid-term outcome with that of transfemoral TAVI.
Methods: A cohort of 80 patients undergoing transapical (n=24) and transfemoral (n=56) TAVI was retrospectively evaluated. Procedure-related complications as defined by VARC-2 criteria, and short-term and mid-term mortality were analyzed and compared in both groups.
Results: Patients in the transapical group were older (83.6 ± 5 vs. 80.0 ± 8.3; p = 0.04) and had greater prevalence of coronary artery disease (75 vs. 44%; p = 0.04) and peripheral vascular disease (37% vs. 16%; p = 0.01). Patients in the transapical group had lower fluoroscopy time (14.9 minutes ± 5.8 vs. 22.9 minutes ± 8.7; p = 0.001) and presented a non-significant trend toward greater requirement of dialysis after the procedure (12.5% vs. 1.8%, p = 0.13). Hospital stay was longer in the transapical group (13.6 ± 23 days vs. 7-2 ± 6.9 days, p = 0.05). Mortality at 30 days and one year was greater in the transapical group (20.8% vs. 5.4%; p = 0.03 and 25% vs. 8.9%; p = 0.04), respectively.
Conclusions: In our experience, transapical TAVI is a feasible and reproducible procedure for patients with severe symptomatic aortic stenosis unsuitable for transfemoral approach. Transapical access was associated with increased risk of mortality at 30 days, in agreement with several publications.
Keywords: Aortic Valve Stenosis, Transcatheter Aortic Valve Replacement, Endovascular Procedures.
INTRODUCCIÓN
El implante valvular aórtico percutáneo (TAVI) ha demostrado resultados similares en la mortalidad comparado al reemplazo valvular quirúrgico en pacientes inoperables (1) o de elevado riesgo quirúrgico. (2) El TAVI por acceso transfemoral (TAVI-TF) es preferido por sobre el acceso transapical (TAVI-TA) y otros accesos por ser menos invasivo y tener la posibilidad de realizar el procedimiento con anestesia local. (3) En contrapartida, los pacientes sometidos a TAVI-TF podrían tener mayor riesgo de accidente cerebrovascular y complicaciones vasculares secundarias a la fricción del sistema de entrega con el eje ilio-femoral, aorta ascendente y el arco aórtico. (4) Existe una población de pacientes no aptos para el acceso TF por el simple hecho de presentar arterias periféricas pequeñas o con enfermedad vascular periférica significativa, lo que imposibilita el acceso de introductores grandes y sistemas de entrega valvulares. El acceso TA ha sido aceptado como vía alternativa en pacientes con inadecuado acceso periférico. Los resultados positivos reportados en pacientes sometidos a TAVI-TA han sido inferiores en comparación con el acceso TF, y es difícil de determinar si la causa es el acceso, junto con sus complicaciones particulares, o las condiciones clínicas preexistentes de la población en estudio. (5, 6, 7) El objetivo de este estudio es valorar la factibilidad y reproducibilidad del TAVI-TA y comparar la evolución clínica a corto y mediano plazo de ambas poblaciones (TAVI-TA y TAVI-TF) en términos de mortalidad y complicaciones vinculadas con el procedimiento acorde con las definiciones VARC-2 (Valve Academic Research Consortium).(8)
MATERIAL Y MÉTODOS
Revisamos retrospectivamente los registros de 89 pacientes con estenosis aórtica grave sintomática tratados con TAVI en el Hospital Italiano de Buenos Aires, Argentina, entre marzo del 2009 y abril del 2016 inclusive. Se seleccionaron aquellos pacientes sometidos a TAVI-TA (n = 24) y TAVI-TF (n = 56) y se excluyeron pacientes con otros abordajes, como transaórtico, transilíaco o transubclavio (n = 9). Las bioprótesis valvulares utilizadas para el abordaje TA fueron Acurate TA® (Symetis), mientras que las utilizadas para el abordaje TF fueron CoreValve® (Medtronic), Accurate Neo® (Symetis) y Lotus® (Boston Scientific) según criterio del grupo tratante (Figura 1).
Las características basales de la población, los registros ecocardiográficos y angiotomográficos, y las variables vinculadas con el procedimiento y evolución clínica a corto (30 días) y largo plazo (1 año) fueron relevadas gracias al registro de la historia clínica electrónica de cada paciente. Las complicaciones fueron registradas acorde con los criterios VARC-2. (8)
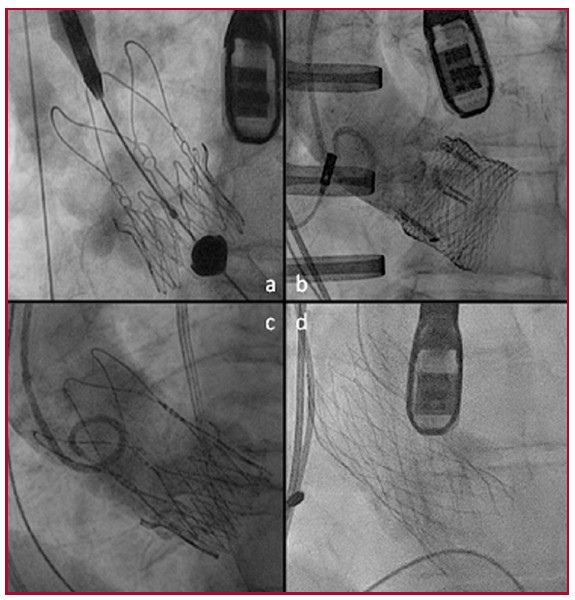
Fig. 1
Fig. 1. Bioprótesis valvulares utilizadas. (a) Acurate-TA®, (b) Lotus®, (c) Acurate Neo®, (d) CoreValve®.
Todos los pacientes seleccionados para TAVI fueron evaluados previamente y descartados para cirugía por un equipo multidisciplinario (Heart Team), que consta de un grupo de cardiólogos clínicos, cardiólogos intervencionistas, especialistas en diagnóstico por imágenes cardiovasculares, cirujanos cardiovasculares y gerontólogos, según recomendaciones. (9) Para la evaluación funcional del anciano, se aplicaron diversos scores (escala AVD, prueba de reloj, minimental, índice de Edmonton, prueba de marcha) de funcionalidad y fragilidad. El análisis de la anatomía coronaria se realizó por medio de una cinecoronariografía. Se realizó un ecocardiograma Doppler transtorácico o transesofágico según el paciente, de acuerdo con las recomendaciones sugeridas por las guías ecocardiográficas para intervenciones percutáneas en valvulopatías. (10) El análisis de los accesos vasculares sobre la anatomía aorto-ilíaca (diámetro luminal mínimo, gravedad de la calcificación y tortuosidad) por medio de angiotomografía multicorte de 64 o 320 pistas o angiografía. Todos los pacientes firmaron un consentimiento informado aprobado por el comité de ética de acuerdo con los lineamientos de la JCI (Joint Comission International).
Todos los procedimientos fueron realizados bajo anestesia general, y el acceso (TA o TF) fue abordado quirúrgicamente por el servicio de cirugía cardiovascular. A su vez, se realizó un ecocardiograma transesofágico durante cada procedimiento, salvo contraindicaciones, casos en los que se optó por ecocardiografía transtorácica.
Las variables categóricas fueron expresadas como frecuencias y porcentaje, mientras que las variables continuas como media y desviación estándar. La comparación de variables categóricas se efectuó con la prueba de Chi cuadrado o exacta de Fisher, según correspondiera. La comparación de variables continuas se efectuó con la prueba de Mann Whitney. Las curvas de sobrevida fueron estimadas con el método de Kaplan-Meier. Se compararon las curvas de sobrevida por medio de la prueba de log rank. Se empleó el software estadístico SPSS 23.0.
Consideraciones éticas
El estudio fue aprobado por el comité de ética del Hospital Italiano de Buenos Aires.
RESULTADOS
En comparación con el grupo TF; los pacientes del grupo TA fueron más añosos (83,6 ± 5 versus 80,0 ± 8.3; p = 0,04); presentaron mayor prevalencia de enfermedad coronaria (el 75% versus el 44%; p = 0,04) y mayor prevalencia de enfermedad vascular periférica (el 37% versus el 16%; p = 0,01). No hubo diferencias significativas entre el riesgo de mortalidad, tanto según el EuroSCORE II (6,2 ± 4,0 versus 6,6 ± 5,1; p = 0,73) como en el STS Score (6,1 ± 2,7 versus 6,0 ± 4,0; p = 0,87). El resto de las características basales se muestran en la Tabla 1.
Los datos del procedimiento evidencian que el grupo TA tuvo menor exposición a rayos X, con tiempos de fluoroscopia significativamente menores en comparación con el grupo TF (14,9 minutos ± 5,8 versus 22,9 minutos ± 8,7; p = 0,001). A su vez, no hubo diferencias entre ambos grupos en cuanto a la necesidad de realizar intervenciones posprocedimiento, como posdilatación con balón (grupo TA el 37% versus grupo TF el 34%; p = 0,64).
Las complicaciones vinculadas al procedimiento figuran en la Tabla 2. No hubo diferencias en el grupo TA en comparación al grupo TF en cuanto a la tasa de sangrado mayor (el 8,3% versus el 7,1%, p = 0,06); accidente cerebrovascular (el 8,3% versus el 3,5%, p = 0,53); y requerimiento de implante de marcapasos definitivo en el posprocedimiento (el 12,5% versus el 12,5%, p = 0,7). Hubo una mayor tendencia en el porcentaje de pacientes del grupo TA (el 12,5%) a requerir diálisis luego del procedimiento en comparación con el grupo TF (el 1,8%), aunque sin diferencia estadística significativa (p = 0,13), infarto dentro de las 72 h (el 8,3% versus 0%, p = 0,07) y taponamiento cardíaco (el 4,1% versus el 1,8%, p = 0,06). Los pacientes del grupo TA tuvieron una menor tendencia a permanecer con reflujo periprotésico moderado y grave en comparación con el grupo TF, sin diferencias estadísticamente significativas (el 16% versus el 28%, p = 0,30). En cuanto a la estadía hospitalaria, los pacientes del grupo TA permanecieron mayor cantidad de días en comparación a aquellos del grupo TF (13,6 ± 23 días versus 7,2 ± 6,9 días, p = 0,05).
La mortalidad global a 30 días fue del 10%, mientras que la mortalidad global al año fue del 13,7%. El grupo de pacientes sometido a abordaje TA presentó mayor mortalidad a 30 días (el 20,8% versus el 5,4%; p = 0,03) y al año (el 25% versus el 8,9%; p = 0,04) en comparación con la población sometida a abordaje TF. No hubo diferencias en cuanto a la mortalidad cardiovascular en ambos grupos (grupo TA: el 12,5% versus grupo TF: el 8,9%; p = 0,61).
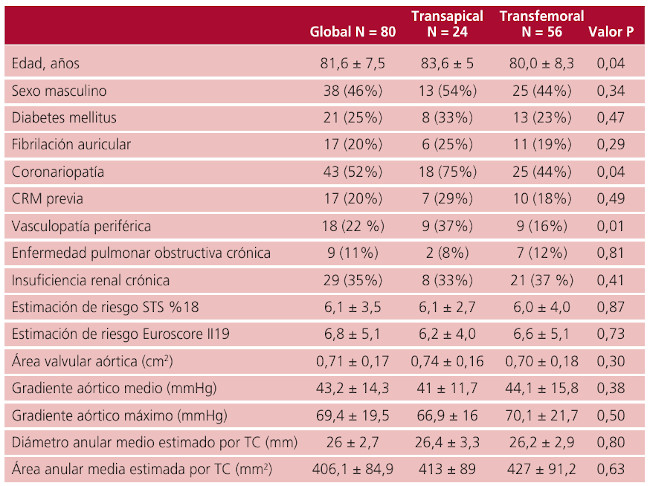
CRM: Cirugía de revascularización miocárdica; TC: Tomografía computarizada.
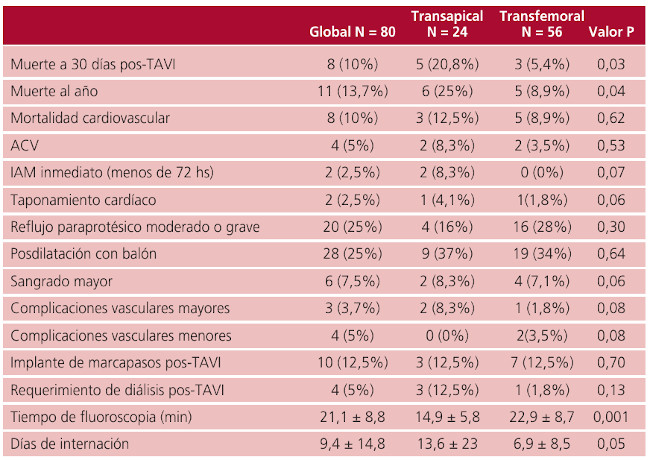
Sobre un total de 5 muertes a 30 días en el grupo TA, 3 se debieron a infecciones intrahospitalarias, de los cuales 1 falleció en el día 11 luego del TAVI-TA, debido a una neumonía intrahospitalaria, y el otrofalleció por neumonía intrahospitalaria en el día 29 posprocedimiento. De las causas no infecciosas, uno de los pacientes fue dado de alta a la semana y falleció a los 20 días cuando reingresó al hospital con un cuadro de shock cardiogénico secundario a un taponamiento cardíaco. Este paciente se encontraba anticoagulado con acenocumarol por una fibrilación auricular crónica y antiagregado con clopidogrel. El otro paciente fue sometido a un TAVI-TA más cirugía de revascularización miocárdica (CRM) con 1 puente mamario interno izquierdo a descendente anterior por minitoracotomía. El TAVI fue realizado con éxito, pero la CRM se frustró, debido a imposibilidad técnica de confeccionar el puente. El paciente sufrió un infarto agudo de miocardio (IAM) periprocedimiento y sangrado mayor que evolucionó con insuficiencia renal aguda y requerimiento de diálisis, y falleció al décimo día por falla multiorgánica. El último paciente tuvo un TAVI-TA no exitoso, debido al mal-posicionamiento de la prótesis por debajo del anillo valvular aórtico y, consecuentemente, evolucionó con insuficiencia cardíaca secundaria a reflujo paravalvular grave, el cual requirió un reemplazo valvular aórtico quirúrgico de urgencia. Falleció al tercer día por shock cardiogénico refractario.
Del grupo TF, hubo 3 muertes a 30 días. Dos pacientes fallecieron por causas relacionadas con sangrado mayores intraprocedimiento. El otro paciente falleció al tercer día pos-TAVI, debido a taquicardia ventricular en contexto de insuficiencia cardíaca (presentaba deterioro moderado de la función sistólica del ventrículo izquierdo antes del procedimiento).
La sobrevida media al año global fue de 10,5 meses ± 0,4; IC 9,7-11,3. El grupo TA tuvo una sobrevida menor (9,0 ± 1,1, IC 7,1-11,0), mientras que el grupo TF tuvo una sobrevida mayor (11,2 ± 0,3, IC 10,5-11,9). La Figura 2 muestra las curvas de sobrevida al año estimadas por Kaplan-Meier, que evidencian una diferencia significativa entre ambas (log-rank, p = 0,04).
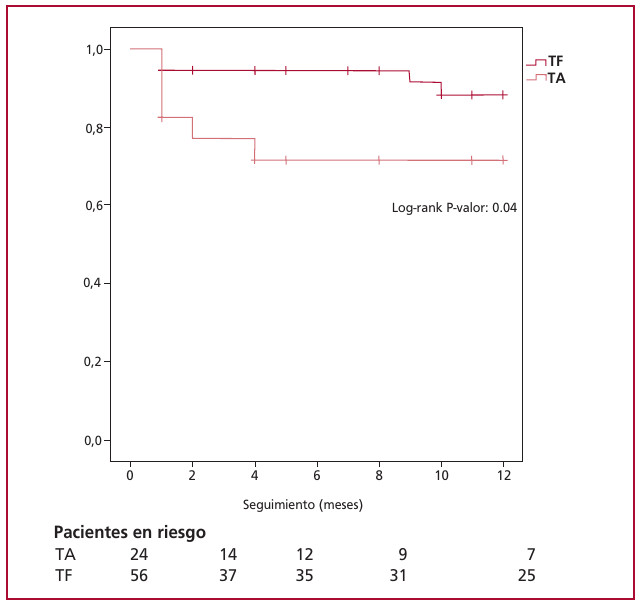
Fig. 2.
Fig. 2. Curva de sobrevida entre TAVI-TA y TAVI-TF.
DISCUSIÓN
El presente registro representa nuestra experiencia temprana en una cohorte de un centro único con pacientes de un hospital comunitario de la ciudad de Buenos Aires, Argentina tratados con TAVI-TA. Podemos rescatar algunas conclusiones relacionadas con el acceso TA en pacientes considerados para TAVI que tengan contraindicación del acceso TF. En principio y fundamentalmente, en nuestro centro el TAVI-TA, es factible y puede ser consistentemente realizado como un procedimiento reproducible, teniendo en cuenta que contamos con un 96% de éxito de los implantes realizados (salvo el paciente en que se realizó reemplazo valvular aórtico quirúrgico, debido a un implante bajo de la prótesis descripto previamente), y también habiendo realizado 24 casos desde septiembre del 2012, cuatro (4) por encima de los 20 casos necesarios para ser considerado un centro con experiencia.
En segundo lugar, el TAVI-TA se asoció con mayor riesgo de muerte durante el seguimiento comparado con el acceso TF, particularmente en el período posoperatorio a 30 días, lo que coincide con varios reportes publicados (11, 12), y en el seguimiento al año, esta diferencia se mantuvo lineal (Figura 2). Esto indicaría que el riesgo de muerte comparativo se nivela cuando supera los 30 días. La diferencia en cuanto a mortalidad a 30 días puede ser atribuida a un sesgo de selección de las poblaciones. A pesar de contar con una población con características basales similares (establecidas por el EuroSCORE II y el STS en cuanto al riesgo previo al procedimiento), la población era algo más añosa, más frágil y presentaba mayor enfermedad vascular periférica y enfermedad coronaria establecida, por lo que el grupo poblacional en cuestión podría considerarse más “enfermo”. Por otro lado, el acceso transapical en pacientes ancianos y frágiles no siempre es tolerado. Un estudio ecocardiográfico comparó la mejoría de la fracción de eyección del ventrículo izquierdo luego de TAVI-TA y TAVI transaórticos en pacientes descartados para acceso TF. (12) El estudio mostró que el acceso TA se asoció con una franca reducción en la mejoría de la fracción de eyección a los 6 y 12 meses al compararlos con el grupo transaórtico.(13) Otro grupo observaron trastornos de la motilidad regional en el ápice en un 28% de los pacientes que se realizaron TAVI-TA. (14) Aunque alrededor de un 50% de los pacientes recuperaban función ventricular, aún así se asociaron a peor fracción de eyección.
El ápex en el abordaje TA ha sido sujeto de estudio por diversos métodos de imágenes. Un estudio reciente valoró por medio de resonancia nuclear magnética cardíaca (RM) pacientes sometidos a abordaje TA versus no-TA junto con biomarcadores de necrosis miocárdica la localización y extensión del daño miocárdico por medio de RM previa y a los 30 días pos-TAVI. El grupo TA no solo presentó mayores niveles de lesión miocárdica, sino que, a su vez, presentó en la zona apical nuevo realce tardío de gadolinio con una mediana de extensión del 5% del tejido. (15)
Sumado a lo dicho, varios reportes de TAVI-TA se asociaron con mayor insuficiencia renal aguda, a pesar de utilizar menor cantidad de contraste durante el procedimiento. (12) Esto se puede correlacionar con una mayor respuesta sistémica inflamatoria y, por ende, mayor daño tisular al mayor trauma quirúrgico que genera el abordaje transapical.
Debemos considerar, a pesar de lo establecido previamente, que también existen factores relacionados con la curva de aprendizaje de la técnica TAVI-TA que pueden influir en los resultados observados. Nuestro centro comenzó con el programa TAVI en marzo del 2009 realizando únicamente abordaje transfemoral. El abordaje transapical comenzó en el año 2012 y, hasta el momento, conforman el 27% del total de los procedimientos. Esto indicaría una curva de aprendizaje disímil entre el TAVI-TA y el TAVI-TF no solamente por la menor cantidad de casos, sino también porque el programa TA comenzó 3 años después. La curva de aprendizaje en el TAVI-TA fue evaluada en un centro pionero en los abordajes TA comparando los resultados clínicos entre los primeros 150 pacientes tratados (experiencia inicial) y los últimos 149 (experiencia reciente). (16) Esto evidenció que la cantidad de contraste utilizado y la necesidad de posdilatación con balón fueron significativamente menores en el grupo de experiencia reciente. A su vez, la mortalidad a 30 días disminuyó del 11% al 6% y, al año, la mortalidad mejoró del 30,7% al 21,7% (p = 0,047). (16) Esto significa que la experiencia del centro es un factor determinante en los resultados clínicos a corto y mediano plazo cuando se considera un abordaje TA. Consideramos que, debido al número de casos de TAVI-TA, nuestra experiencia en este abordaje es inicial.
Nuestro estudio posee ciertas limitaciones. Por un lado, nuestros datos deben ser interpretados con cautela, debido a que no es un estudio aleatorizado, sino una cohorte retrospectiva, por lo que se puede esperar un sesgo de selección. A su vez, nuestros datos fueron obtenidos de la experiencia de un único centro en la Argentina. Consideramos que el número de pacientes es relativamente bajo para un análisis comparativo, teniendo en cuenta que los reportes publicados de centros únicos con alto volumen de TAVI poseen mayor cantidad de pacientes (11, 17) y, por lo tanto, generalizar los resultados podría resultar inapropiado. De todas formas, a nuestro entender, es el primer registro comparativo de TAVI-TA versus TAVI-TF en la Argentina. Otra limitación está relacionada con los tipos de dispositivos utilizados. Actualmente existen prótesis valvulares percutáneas de nueva generación que utilizan introductores de menor diámetro que los utilizados en nuestro centro en su momento. De todas formas, consideramos que estos avances tecnológicos mejorarán la factibilidad y seguridad del TAVI, particularmente en acceso TF.
En conclusión, el abordaje TA en nuestro centro es factible y reproducible para pacientes sintomáticos con estenosis aórtica grave que fueron descartados para reemplazo valvular quirúrgico y no son aptos para un abordaje transfemoral. Por otro lado, la sobrevida al año fue menor en el grupo TA, probablemente, debido a que el abordaje TA es más agresivo y las características poblacionales diferían en algunos aspectos, sumado a que nos encontramos en una fase de temprana de experiencia en el abordaje.
Declaración de conflicto de intereses
La Dra. Carla R. Agatiello es proctor de Symetis. Los demás autores declaran que no poseen conflictos de intereses. (Véanse formularios de conflicto de intereses de los autores en la web / Material suplementario).
BIBLIOGRAFÍA
1. Leon MB, Smith CR, Mack M, Miller DC, Moses JW, Svensson LG, et al, Investigators PT. Transcatheter aortic-valve implantation for aortic stenosis in patients who cannot undergo surgery. N Engl J Med 2010;363:1597-607. http://doi.org/dvzg9k
2. Smith CR, Leon MB, Mack MJ, Miller DC, Moses JW, Svensson LG, et al, Investigators PT. Transcatheter versus surgical aortic-valve replacement in high-risk patients. N Engl J Med 2011;364:2187-98. http://doi.org/dvzg9k
3. Aguirre J, Waskowski R, Poddar K, Kapadia S, Krishnaswamy A, McCullough R, et al. Transcatheter aortic valve replacement: experience with the transapical approach, alternate access sites, and concomitant cardiac repairs. J Thorac Cardiovasc Surg. 2014;148:1417-22. http://doi.org/f6j8gq
4. Bleiziffer S, Ruge H, Mazzitelli D, Hutter A, Opitz A, Bauernschmitt R, et al. Survival after transapical and transfemoral aortic valve implantation: Talking about two different patient populations. J Thorac Cardiovasc Surg 2009;138:1073-80. http://doi.org/cft895
5. van der Boon RM, Marcheix B, Tchetche D, Chieffo A, Van Mieghem NM, Dumonteil N, et al. Transapical versus transfemoral aortic valve implantation: A multicenter collaborative study. Ann Thorac Surg 2014;97:22-8. http://doi.org/f5nvsz
6. Lefevre T, Kappetein AP, Wolner E, Nataf P, Thomas M, Schachinger V, et al, Group PEI. One year follow-up of the multi-centre european partner transcatheter heart valve study. Eur Heart J 2011;32:148-57. http://doi.org/dgdkxc
7. Gilard M, Eltchaninoff H, Iung B, Donzeau-Gouge P, Chevreul K, Fajadet J; FRANCE 2 Investigators, et al. Registry of transcatheter aortic-valve implantation in high-risk patients. N Engl J Med 2012;366:1705-15. http://doi.org/j4z
8. Kappetein AP, Head SJ, Genereux P, Piazza N, van Mieghem NM, Blackstone EH, et al. Updated standardized endpoint definitions for transcatheter aortic valve implantation: The valve academic research consortium-2 consensus document. Eur Heart J 2012;33:2403-18. http://doi.org/f4bz42
9. Vahanian A, Alfieri O, Al-Attar N, Antunes M, Bax J, Cormier B, et al, European Association of Cardio-Thoracic S, European Society of C, European Association of Percutaneous Cardiovascular I. Transcatheter valve implantation for patients with aortic stenosis: A position statement from the european association of cardio-thoracic surgery (eacts) and the european society of cardiology (esc), in collaboration with the european association of percutaneous cardiovascular interventions (eapci). Eur Heart J 2008;29:1463-70. http://doi.org/d32ccg
10. Zamorano JL, Badano LP, Bruce C, Chan KL, Goncalves A, Hahn RT, et al. Eae/ase recommendations for the use of echocardiography in new transcatheter interventions for valvular heart disease. Eur Heart J 2011;32:2189-214. http://doi.org/d32ccg
11. Koifman E, Magalhaes M, Kiramijyan S, Escarcega RO, Didier R, Torguson R, et al. Impact of transfemoral versus transapical access on mortality among patients with severe aortic stenosis undergoing transcatheter aortic valve replacement. Cardiovasc Revasc Med 2016;17:318-21. http://doi.org/cqdk
12. Biancari F, Rosato S, D’Errigo P, Ranucci M, Onorati F, Barbanti M, et al. Immediate and intermediate outcome after transapical versus transfemoral transcatheter aortic valve replacement. Am J Cardiol 2016;117:245-51. http://doi.org/f8m9sc
13. Ribeiro HB, Dahou A, Urena M, Carrasco JL, Mohammadi S, Doyle D, et al. Myocardial injury after transaortic versus transapical transcatheter aortic valve replacement. Ann Thorac Surg 2015;99:2001-9. http://doi.org/f7h62t
14. Barbash IM, Dvir D, Ben-Dor I, Corso PJ, Goldstein SA, Wang Z, et al. Impact of transapical aortic valve replacement on apical wall motion. J Am Soc Echocardiogr 2013;26:255-60. http://doi.org/cqdm
15. Ribeiro HB, Larose E, de la Paz Ricapito M, Le Ven F, Nombela-Franco L, Urena M, et al. Myocardial injury following transcatheter aortic valve implantation: Insights from delayed-enhancement cardiovascular magnetic resonance. EuroIntervention 2015;11:205-13. http://doi.org/f7m7ng
16. Kempfert J, Rastan A, Holzhey D, Linke A, Schuler G, van Linden A, et al. Transapical aortic valve implantation: Analysis of risk factors and learning experience in 299 patients. Circulation 2011;124:S124-9. http://doi.org/b9bgp6
17. D’Onofrio A, Facchin M, Besola L, Manzan E, Tessari C, Bizzotto E, et al. Intermediate clinical and hemodynamic outcomes after transcatheter aortic valve implantation. Ann Thorac Surg 2016;101:881-8; Discussion 888.
18. Shahian DM, Jacobs JP, Edwards FH, Brennan JM, Dokholyan RS, Prager RL, et al. The society of thoracic surgeons national database. Heart. 2013;99:1494-501. http://doi.org/f5fg83
19. Nashef SA, Roques F, Sharples LD, Nilsson J, Smith C, Goldstone AR, et al. EuroSCORE II. Eur J Cardiothorac Surg 2012;41:734-44. http://doi.org/pvr
Abreviaturas
IAM: Infarto agudo de miocardio
CRM: Cirugía de revascularización miocárdica
RM: Resonancia magnética nuclear
TAVI: Implante valvular aórtico percutáneo
TAVI-TA: TAVI por acceso transapical
TAVI-TF: TAVI por acceso transfemoral
Notas de autor
carla.agatiello@hospitalitaliano.org.ar Tte. Gral. Juan Domingo Perón 4190, C.A.B.A. Código Postal: C1199ABB - Tél: (5411) 4959-0200 - Fax: interno 8663/9796