Artículo original
Miectomía septal ampliada en la miocardiopatía hipertrófica obstructiva, resultados clínicos y evolución ecocardiográfica a mediano plazo
Extended Septal Myectomy in Obstructive Hypertrophic Cardiomyopathy: Mid-term Clinical and Echocardiographic Outcomes
Miectomía septal ampliada en la miocardiopatía hipertrófica obstructiva, resultados clínicos y evolución ecocardiográfica a mediano plazo
Revista Argentina de Cardiología, vol. 86, núm. 2, pp. 96-102, 2018
Sociedad Argentina de Cardiología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 02 Noviembre 2017
Aprobación: 27 Diciembre 2017
Resumen:
Introducción: La miectomía septal ampliada constituye el tratamiento de elección para pacientes con miocardiopatía hipertrófica obstructiva sintomática, refractarios al tratamiento farmacológico.
Objetivos: Evaluar los resultados posoperatorios, el cambio en los síntomas y la evolución ecocardiográfica de una población sometida a miectomía septal ampliada por miocardiopatía hipertrófica obstructiva sintomática.
Material y métodos: Desde noviembre de 2011 a octubre de 2017, se intervino un total de 28 pacientes. Se analizaron la evolución posoperatoria, clínica y ecocardiográfica al alta y al seguimiento.
Resultados: Edad promedio 53,3 ± 13,4 años. La mortalidad perioperatoria (< 30 días) fue del 0%. Un paciente falleció a los 90 días (3,5%). No se produjeron comunicaciones interventriculares, daño de la válvula aórtica ni se reemplazó la válvula mitral en ningún paciente. El 91% de ellos se encontraban con disnea en CF III-IV en el preoperatorio, los restantes tenían angina o síncope. En el seguimiento, el 92,8% estaban asintomáticos, 1 paciente en CF III y otro en CF II. El gradiente preoperatorio basal promedio fue de 53,5 mmHg y con valsalva 86,4 mmHg; los gradientes basal y con valsalva posoperatorios fueron 9,4 mmHg y 13,5 mmHg (p < 0,01). Al seguimiento, los gradientes en reposo y con valsalva fueron aún más bajos, 8,3 mmHg y 10,7 mmHg, respectivamente (p: NS). Nueve pacientes (32%) presentaban insuficiencia mitral moderada a grave previa por movimiento anterior sistólico o patología intrínseca mitral. Se detectó solo un paciente con insuficiencia mitral moderada asintomática en el seguimiento (3,5%). La mediana de seguimiento fue de 400 días, Pc 25-75 de 695 días (mínimo de 30 días y el máximo de 1868 días).
Conclusión: Con la miectomía septal ampliada se obtiene una mejoría hemodinámica y clínica de los pacientes sintomáticos, con bajo número de complicaciones posoperatorias. Esto tiene como resultado una mejor calidad de vida.
Palabras clave: Cardiomiopatía Hipertrófica, Tabiques Cardíacos/cirugía, Tabiques Cardíacos/diagnóstico por imágenes, Procedimientos Quirúrgicos Cardíacos/métodos.
Abstract:
Background: Extended septal myectomy is the treatment of choice for patients with symptomatic obstructive hypertrophic cardiomyopathy, refractory to pharmacological treatment.
Objectives: The aim of this study was to evaluate postoperative results, symptom changes and echocardiographic outcome in a population undergoing extended septal myectomy for symptomatic obstructive hypertrophic cardiomyopathy.
Methods: A total of 28 patients were operated on from November 2011 to October 2017. Postoperative, clinical and echocardiographic outcomes were analyzed at discharge and during follow-up.
Results: Mean age was 53.3±13.4 years. Perioperative mortality (<30 days) was 0%. One patient died 90 days after the procedure (3.5%). No septal defect, aortic valve injury or mitral valve replacement occurred in any patient. Ninety-one percent of patients were in FC III-IV, and the rest had angina or syncope. During follow-up, 92.8% were asymptomatic, one patient was in FC III and another in FC II. Preoperative basal average gradient was 53.5 mmHg and with Valsalva maneuver 86.4 mmHg, and postoperative basal and with Valsalva gradient was 9.4 mmHg and 13.5 mmHg, respectively (p <0.01). During follow-up, gradients at rest and with Valsalva were even lower: 8.3 mmHg and 10.7 mmHg, respectively (p: NS). Nine patients (32%) presented prior moderate to severe mitral regurgitation due to mitral valve systolic anterior motion or intrinsic disease. Only one patients had evidence of asymptomatic moderate mitral regurgitation at follow-up (3.5%). Median follow-up was 400 days (25-75 IQR: 695 days; minimum: 30 days and maximum: 1,868 days).
Conclusion: Extended septal myectomy improves hemodynamic and clinical outcome in symptomatic patients, with a low number of postoperative complications, resulting in better quality of life.
Keywords: Cardiomyopathy, Hypertrophic, Heart Septum/surgery, Heart Septum/diagnostic imaging, Cardiac Surgical Procedures/methods.
INTRODUCCIÓN
La miocardiopatía hipertrófica obstructiva (MCHO), se define por la presencia de un aumento del espesor de la pared del ventrículo izquierdo que no se puede explicar únicamente por condiciones de carga anormales. (1,2,3,4) Es la cardiopatía genética más frecuente, y la principal causa de muerte súbita en los jóvenes (5,6), siendo su prevalencia de 1 cada 500 personas en la población general.
Han pasado casi 60 años desde la primera descripción de miocardiopatía hipertrófica por Brock en 1957, basado en parámetros hemodinámicos invasivos y por Teare en 1958 en autopsias. (7,8,9) Actualmente sabemos que la obstrucción del tracto de salida del ventrículo izquierdo (TSVI) está presente en aproximadamente 70% de los pacientes con miocardiopatía hipertrófica en reposo o provocada. (10) Dicha obstrucción puede generar síntomas por diferentes mecanismos: limitar el gasto cardiaco y producir síntomas de esfuerzo como disnea o pre síncope, generar un aumento de la presión de fin de diástole en el ventrículo izquierdo induciendo isquemia, puede afectar la relajación ventricular y el llenado diastólico y finalmente, la insuficiencia mitral (IM) por movimiento anterior sistólico (MAS) asociada a la obstrucción, puede determinar aumento de la presión de la aurícula izquierda, disnea y fibrilación auricular (FA). (11,12)
El objetivo primario del tratamiento es la mejoría de los síntomas particularmente los determinados por la obstrucción dinámica del TSVI. El primer escalón de tratamiento es el farmacológico, pero alrededor de 25% de los pacientes continúan sintomáticos. En estos casos, la miectomía quirúrgica constituye el tratamiento de elección. (13) La indicación habitual de miectomía incluye los pacientes con obstrucción severa del TSVI con gradientes en reposo o mayores a 30 mmHg. (14) Sin embargo, actualmente se han extendido las indicaciones incluyendo pacientes sintomáticos con bajos gradientes en reposo y obstrucción latente. (15)
En nuestro país, el tratamiento quirúrgico se encuentra limitado a escasos centros, y se desconocen los resultados del mismo, por lo cual el objetivo del presente trabajo es evaluar la evolución clínica y ecocardiográfica de una población sometida a miectomía septal ampliada (MSA) por MCHO sintomática, refractaria al tratamiento médico óptimo.
MATERIAL Y MÉTODOS
De los 550 pacientes con miocardiopatía hipertrófica en seguimiento de la institución, se identificaron aquellos sometidos a tratamiento invasivo mediante MSA. Desde noviembre de 2011 a octubre de 2017, se operaron un total de 28 pacientes con MCHO, todos refractarios a tratamiento farmacológico óptimo.
La estrategia del tratamiento y la evaluación clínica y ecocardiográfica estuvo a cargo de miembros del Centro de Miocardiopatías, constituido por cardiólogos clínicos, intervencionistas, electrofisiólogos, cirujanos, expertos en insuficiencia cardíaca y en imágenes de nuestra Institución.
Se analizaron la evolución postoperatoria, clínica y ecocardiográfica al alta y al seguimiento a mediano plazo. La mediana de seguimiento fue de 400 días, Pc 25-75 de 695 días (mínimo de 30 días y el máximo de 1868 días).
El diagnóstico y evaluación ecocardiográfica se basó en la evidencia en el ecocardiograma, de un ventrículo izquierdo con aumento de los espesores (espesor > 15 mm), no dilatado, sin otra causa cardíaca o sistémica que pudiese producir una hipertrofia similar. Se consideró el espesor máximo de la pared medido en fin de diástole. Se utilizó Doppler continuo para estimar el gradiente pico en el TSVI y se definió como obstrucción a la presencia de gradiente ≥ a 30 mmHg, en reposo, con maniobras o ejercicio.
Procedimiento quirúrgico
Luego de la inducción a anestesia general, se realizó ecocardiograma transesofágico (ETE) para evaluar la morfología de la válvula mitral y la presencia de patología primaria de la misma, así como para proyectar la extensión de la miectomía. Se midió el máximo espesor septal en varias vistas, la distancia máxima desde la válvula aórtica al punto de máxima hipertrofia, la localización del punto de MAS y la extensión hacia los segmentos medio ventricular y apical de la hipertrofia.
Luego de iniciada la circulación extracorpórea (CEC), se realizó una aortotomía exponiéndose el septum basal. Se efectuaron dos incisiones paralelas por debajo del nadir de la valva coronaria derecha, a 8-10 mm de la misma, extendiéndola hasta la base de los músculos papilares. Se completó la resección hacia apical y se continuó hacia la izquierda, hasta la valva anterior de la válvula mitral y hacia la derecha hasta la comisura póstero medial.
Se exploró el aparato valvular mitral y seccionaron trabéculas, cuerdas tendinosas anormales y músculos papilares anómalos que pudieran provocar o favorecer la obstrucción. En caso de valva anterior mitral muy redundante, se procedió a la plicatura de la misma con puntos separados en su cuerpo.
En los pacientes con FA paroxística o permanente, se realizó además ablación bipolar de las venas pulmonares y extracción de la orejuela izquierda (Maze); así como en los pacientes con coronariopatía se realizó revascularización coronaria concomitante.
El ETE se repitió una vez finalizado el procedimiento a la salida de CEC, para evaluar los gradientes residuales, en reposo y con maniobras de provocación. Se evaluó además el MAS, la IM residual y la presencia de posibles complicaciones como insuficiencia aortica o comunicación interventricular (CIV). En caso de que aún hubiera gradientes elevados o MAS, se procedió al reingreso en CEC para ampliar la miectomía o efectuar la plicatura de la valva anterior mitral.
Análisis estadístico
Las características de los pacientes se expresaron en media ± desviación estándar, mediana y rango intercuartil (RIC) o prevalencia (en porcentaje), según correspondiera. Las diferencias entre grupos se analizaron con la prueba de la t de Student para muestras independientes o con la prueba en U de Mann-Whitney para variables continuas y la prueba de chi cuadrado para variables categóricas. Se consideró estadísticamente significativo un valor de p < 0,05.
Se utilizó el software estadístico IBM® SPSS® Statistics (versión 21).
Consideraciones éticas
Los pacientes firmaron un consentimiento informado para la participación del estudio que se llevó a cabo en cumplimiento con la ley nacional de protección de datos personales 25.326.
El estudio fue conducido de acuerdo a las normas éticas nacionales (ley CABA 3301) y Ley nacional de investigación clínica en seres humanos, declaración de Helsinki y contó con la aprobación del comité de Investigación y Ética de nuestra Institución.
RESULTADOS
Las características basales de la población se muestran en la Tabla 1. La edad promedio fue de 53,3 ± 13,4 años; 15 de los p fueron varones (54%). Dos p (7,1%) tenían ablación septal con alcohol previa. El tiempo promedio desde el diagnóstico a la cirugía fue de 8,13 años.
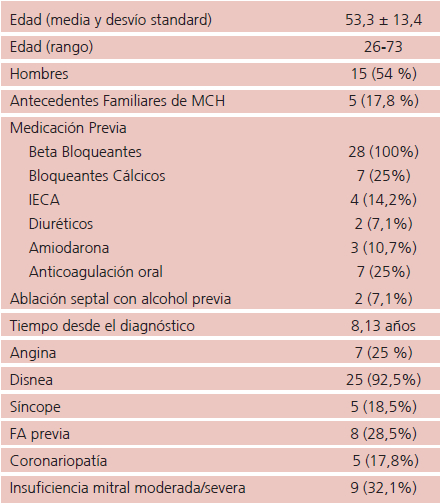
MCH: miocardiopatía hipertrófica. IECA: inhibidores de la enzima convertidora. FA: Fibrilación Auricular.
Los síntomas predominantes fueron angina en 25,9%, disnea en el 92,5% y síncope en 18,5%, habiendo pacientes con más de un síntoma. El 100% estaba tratado con betabloqueantes en dosis máximas toleradas y 7 pacientes recibían bloqueantes cálcicos concomitantemente. Ocho pacientes tenían FA preoperatoria (29,6%), en siete de ellos (26,9%) se realizó Maze.
Nueve pacientes (32%) tenían IM moderada o severa previa, en dos de ellos por patología intrínseca de la válvula mitral (prolapso, indentación) y en los restantes se debía a MAS secundario a valva anterior redundante, cuerdas anómalas o implante anterior de los músculos papilares. En los primeros pacientes se efectuó plástica mitral con corrección de la patología valvular mediante auriculotomía izquierda y en los restantes se efectuó plicatura de la valva anterior mitral en su cuerpo o borde libre, sección de cuerdas anómalas o punto de Alfieri a través de la aortotomía. Cinco pacientes tenían enfermedad coronaria (17,8%), realizándose la revascularización coronaria en todos ellos.
Dos pacientes tenían cardiodesfibrilador implantable (CDI) como prevención primaria colocados durante su seguimiento previo. La mortalidad perioperatoria (< 30 días) fue de 0%. Un paciente que tuvo ACV perioperatorio falleció a los 90 días luego de multiples complicaciones en un centro de rehabilitación, sin lograr externarlo desde la cirugia (3,5%).
Las complicaciones además del ACV citado, incluyeron un ACV isquémico con afasia de expresión, con restitución ad integrum a los 30 días de operado.
Cuatro pacientes (14,2%) requirieron marcapasos definitivo debido a bloqueo auriculoventricular completo en el postoperatorio (PO) inmediato y uno de ellos al seguimiento, por sincopes a repetición. Dos pacientes (7,1%) recibieron un CDI como prevención primaria en el PO y uno al seguimiento, sin evidencia de arritmias ventriculares o choques apropiados. Dichos pacientes tenían antecedentes de muerte súbita en la familia.
Dos pacientes presentaron FA postoperatoria (7,1%). La misma ocurrió en uno de los que recibieron ablación quirúrgica y en otro revirtió con CVE en el día 5 PO. En Holter de 12 derivaciones de control al seguimiento, solo la paciente con FA previa y postoperatoria continua fibrilada. Ningún otro paciente con Maze presenta FA en el seguimiento. (Tabla 2)
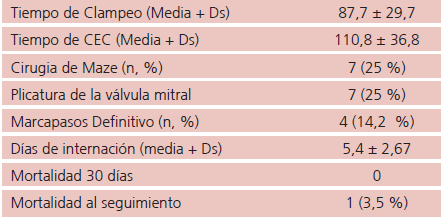
CEC: Circulación extracorpórea
No ocurrieron CIV, daño de la válvula aórtica ni se reemplazó la válvula mitral en ningún paciente.
Más de noventa por ciento de los pacientes se encontraban con disnea en CF III-IV en el preoperatorio. En el seguimiento promedio de 572 días, 92,8% se encontraban asintomáticos, (1 paciente en CF III y otro en CF II. (Figura 1).
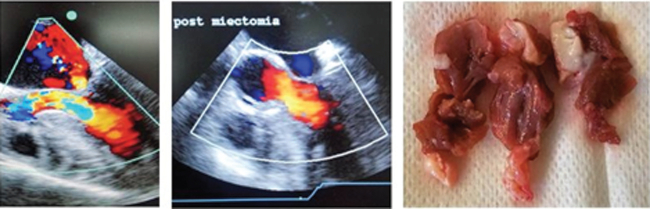
Fig. 1
ETE pre y post miectomía (A y B). Miectomía septal ampliada, pieza quirúrgica (C)
El seguimiento a mediano plazo comprendió 43.96 pacientes/año (rango 1-56 meses, media de 17 meses)
ECOCARDIOGRAMA: gradientes
El gradiente preoperatorio basal promedio fue de 53,5 mmHg (rango 16-104 mmHg) y provocado de 86,4 mmHg (rango 44-186 mmHg). Vale aclarar que solo un paciente presentó gradiente con maniobras menor a 50 mmHg, pero era portador además de insuficiencia mitral moderada severa secundaria a MAS en esfuerzo y FA paroxística recurrente con descompensación. Los gradientes basal y provocado PO fuero 9,4 mmHg y 13,5 mmHg (p < 0,01). Al seguimiento, los gradientes en reposo y provocados fueron aún más bajos, de 8,3 mmHg y 10,7 mmHg respectivamente. (p: NS) (Figura 2 A y B) (Tabla 3)
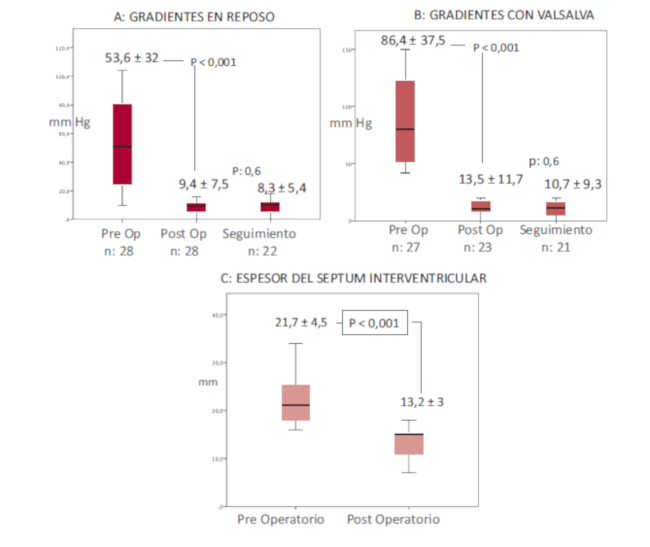
Fig. 2
Evolución de los gradientes y espesor septal
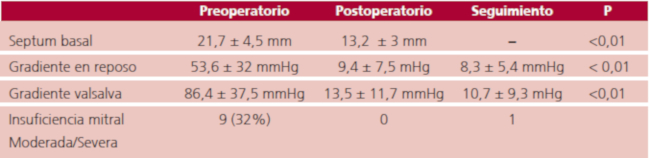
Espesor Septal e Insuficiencia mitral
Las mediciones del septum variaron entre 16 y 34 mm (media 21,9 ± 4,5 mm) en el preoperatorio. En el PO las mismas fueron de 13,2 ± 3 mm en promedio (p < 0,001). (Figura 2 C).
Los estudios con Doppler color mostraron IM moderada a severa en 32% de los pacientes en el preoperatorio. Se detectó IM moderada asintomática en un paciente al seguimiento (3,5%), sin insuficiencia severa en ninguno de ellos. Tampoco se observó insuficiencia aortica moderada o severa en el seguimiento.
DISCUSIÓN
Los consensos y las guías señalan que la miectomía septal es el tratamiento de elección para pacientes con MCHO sintomática, refractarios al tratamiento médico. (2-4) La disminución o eliminación de los gradientes del TSVI se obtienen no solo por el aumento del tamaño del mismo por la MSA, sino también por la interrupción de los eventos fisiopatológicos que causan los gradientes del tracto de salida. El principal de estos eventos es el MAS. Generalmente la eliminación de los gradientes del TSVI por la MSA, resulta en la corrección de la IM causada por el MAS; cualquier insuficiencia residual secundaria a ruptura cordal, prolapso o dilatación anular puede ser corregida por la reparación valvular y anuloplastia.
Este reporte de la experiencia inicial, forma parte de un grupo de pacientes (aproximadamente un 5% del total) que se encuentra en seguimiento por el Centro de Miocardiopatías de la Institución integrado por distintos especialistas, que luego de discutir cada caso en particular, fueron enviados a cirugía. De los 28 pacientes operados desde 2011, cuando comenzamos a desarrollar el programa de cirugía para la MCHO, 19 se operaron en los últimos 3 años.
El hecho de elegir el tratamiento quirúrgico se basó en que se trataba de pacientes sin comorbilidades importantes. Cabe destacar que nuestro centro también cuenta con la posibilidad de tratamiento mediante alcoholización, que en general se reserva para pacientes más añosos, con comorbilidades o que rechazan la cirugía. La presencia concomitante de anomalías de la válvula mitral o de su aparato subvalvular y de fibrilación auricular, también constituyó indicación de cirugía por sobre la alcoholización.
La miectomía original de Morrow, ha sido reemplazada por una resección ampliada del septum interventricular, que ha mejorado los resultados quirúrgicos y que es utilizada por los grupos quirúrgicos con más experiencia y mejores resultados con esta técnica.
La MSA con corrección mitral cuando fue necesario se asoció con mejoría significativa del cuadro clínico y hemodinámico de esta serie inicial de pacientes, tanto en el PO inmediato como al seguimiento a mediano plazo. Los gradientes del TSVI en reposo y con maniobra de valsalva, se redujeron de manera significativa en el PO inmediato y continúan bajos al seguimiento.
La clase funcional mejoró de manera significativa y se mantuvo esta mejoría al seguimiento. Estos datos coinciden con los de los centros de mayor experiencia del mundo. (16,17)
Las complicaciones más comúnmente descriptas con la miectomía son la CIV y la insuficiencia aortica. La CIV iatrogénica ocurre en menos del 1% de los pacientes y es más frecuente cuando el septum no supera los 16 mm de espesor (13). La lesión de la válvula aórtica o mitral es muy poco frecuente cuando la cirugía es realizada por un cirujano experto. (13) En nuestros pacientes, no tuvimos CIV ni insuficiencia aórtica en el PO ni al seguimiento.
La necesidad de marcapasos definitivo por bloqueo AV completo, es otra de las complicaciones habituales. Las cifras reportadas en la literatura rondan el 2% de los pacientes y es más frecuente en aquellos con bloqueo completo de rama derecha previo y en pacientes con alcoholización previa, en que la frecuencia puede llegar al 20%. (18,19) En nuestra serie la colocación de marcapasos definitivo por bloqueo AV fue de 14%. De estos cuatro pacientes uno presentó alcoholización previa con bloqueo de rama derecha residual, otro tenía antecedente de bloqueo AV de alto grado y en otro de ellos se realizó Maze derecho e izquierdo. Pensamos que esta cifra tiene relación con el antecedente de ablación con alcohol y bloqueo de rama derecha previos y con la realización de Maze completo, derecha e izquierda, con el bloqueo AV secundario al mismo. En un metaanálisis reciente, el Maze completo presentó OR de 2.6 (95% CI: 1.09-6.20, p = 0.031) para la necesidad de marcapasos definitivo. (20) Luego de estos primeros casos, limitamos el Maze a las venas pulmonares y a la aurícula izquierda, llevando a que de los últimos 15 pacientes, solo 1 requirió MCP definitivo.
La mortalidad perioperatoria reportada en diferentes series varía entre el 0,5 y 1%. (21,22,23,24) Incluso centros sin experiencia previa en esta cirugía obtienen resultados alentadores. (25,26) En nuestra experiencia, un paciente falleció en el día 90 PO debido a múltiples complicaciones secundarias a ACV perioperatorio.
En relación al ACV perioperatorio, dos pacientes presentaron esta complicación. Ambos pacientes requirieron más de un ingreso en CEC para corregir la patología con el consiguiente re clampeo aórtico, que aumenta el riesgo de esta complicación. En la paciente con ACV que la llevó al óbito, se produjo un desgarro de la aorta ascendente, con hipotensión sostenida. Entendemos que el bajo número de pacientes magnifica la tasa de este evento expresada en términos porcentuales, teniendo en cuenta que las publicaciones internacionales reportan cifras de alrededor de 1% (23)
Con respecto a la válvula mitral, cuando la misma es excesivamente redundante se ha descripto la plicatura del cuerpo o borde libre, técnica que fue realizada en 25% de nuestros pacientes. Esta técnica elimina la presencia de MAS residual favorecida por un implante anterior de los músculos papilares y porque la valva anterior mitral es redundante y contacta con el septum a pesar de la correcta miectomía. (12,27) Además, existe un grupo de pacientes en los que el septum no es severamente hipertrófico, pero en los cuales el tamaño de la valva anterior, el implante anormal de cuerdas tendinosas y músculos papilares bífidos, están asociados con obstrucción del TSVI. (28,29)
En esta experiencia inicial, hemos tratado a 4 pacientes con septum ligeramente hipertrófico (≤ 17 mm) pero con válvula mitral muy redundante, realizando la miectomía septal, plicatura valvar y sección de cuerdas de 2° orden, con buenos resultados en cuanto a reducción de gradientes e IM y con mejoría clínica.
La FA que está descripta en hasta 25% de los pacientes con MCHO y que es 4 veces más común que en la población general (30), fue tratada mediante ablación bipolar realizada durante el mismo acto operatorio. El éxito de este procedimiento fue elevado y más importante aún, 85,7% de los pacientes (6 de 7) mantienen el ritmo sinusal al seguimiento, algo que tiene importancia en la presencia de posibles complicaciones asociadas a la fibrilación auricular. (16, 31,32,33) Este resultado debe ser tomado con cautela teniendo en cuenta el número de pacientes del estudio.
Al seguimiento, los resultados clínicos, ecocardiográficos y hemodinámicos, demuestran que la mejoría inicial en la sintomatología y reducción de los gradientes, se mantiene. Se ha demostrado que la disminución de los gradientes y la mejoría clínica con cirugía, cambian la evolución de la enfermedad y mejoran la sobrevida de los pacientes en muchos artículos publicados. De esta forma, la mortalidad de pacientes con esta patología, se equipara con la mortalidad de la población general a largo plazo. (22,34)
Las guías de tratamiento de esta patología refieren que el tratamiento quirúrgico se debería realizar en centros con experiencia y cirujanos entrenados en esta técnica. Sin embargo, como toda técnica quirúrgica, luego de una curva de aprendizaje lógica y de bajo riesgo de morbimortalidad, el mismo puede aplicarse en centros nuevos, con bajo número inicial de pacientes, pero para esto es muy importante la discusión de los mismos en un grupo multidisciplinario y evaluar en él, el mejor tratamiento para cada caso en particular. (25,26)
Limitaciones
La principal limitación del estudio es que los resultados analizados corresponden a una cohorte de pacientes seleccionados tratados con MSA, con seguimiento a mediano plazo.
Conclusión
Esta experiencia inicial demuestra que cuando los pacientes son seguidos y seleccionados para el mejor tratamiento disponible por un grupo multidisciplinario especializado, se pueden obtener resultados alentadores con la MSA. Estos se traducen en mejoría hemodinámica y clínica de los pacientes a corto plazo y al seguimiento, resultando en mejor calidad de vida de los mismos.
BIBLIOGRAFIA
1. Maron BJ, McKenna WJ, Danielson GK, Kappenberger LJ, Kuhn HJ, Seidman CE, et al; Task Force on Clinical Expert Consensus Documents. American College of Cardiology; Committee for Practice Guidelines. European Society of Cardiology. American College of Cardiology/European Society of Cardiology clinical expert consensus document on hypertrophic cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. J Am Coll Cardiol 2003;42:1687-713. http://doi.org/fmthmx
2. Casabé JH, Acunzo R, Fernández A, Gabay J, Galizio N, Hita A, y cols. Consenso Argentino de Miocardiopatía Hipertrófica. Rev Argent Cardiol 2009;77:151-66.
3. Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, et al; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Association for Thoracic Surgery; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Failure Society of America; Heart Rhythm Society; Society for Cardiovascular Angiography and Interventions; Society of Thoracic Surgeons. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: executive summary: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2011;124:2761-96. http://doi.org/d88rsk
4. Task Force Members, Elliott PM, Anastasakis A, Borger MA, Borggrefe M, Cecchi F, Charron P, et al. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy: the Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). Eur Heart J 2014;35:2733-79. http://doi.org/4xx
5. Maron BJ, Gardin JM, Flack JM, Gidding SS, Kurosaki TT, Bild DE. Prevalence of hypertrophic cardiomyopathy in a general population of young adults. Echocardiographic analysis of 4111 subjects in the CARDIA Study. Coronary Artery Risk Development in (Young) Adults. Circulation 1995;92:785-9. http://doi.org/rzf
6. SEC Working Group for the 2014 ESC Guidelines on Diagnosis and Management of Hypertrophic Cardiomyopathy; Expert Reviewers for the ESC 2014 Guidelines on the Diagnosis and Management of Hypertrophic Cardiomyopathy; SEC Clinical Practice Guidelines Committee.Comments on the 2014 ESC Guidelines on the Diagnosis and Management of Hypertrophic Cardiomyopathy. A Critical View From the Perspective of Spanish Cardiology. Rev Esp Cardiol (Engl Ed) 2015;68:4-9. http://doi.org/f2xz6g
7. Functional obstruction of the left ventricle (acquired aortic subvalvar stenosis). Brock RC. Guys Hosp Rep 1957;106:221.
8. Teare D. Asymmetrical hypertrophy of the heart in young adults. Br Heart J 1958;20:1-8. http://doi.org/b38bqc
9. Maron BJ, Maron MS, Wigle ED, Braunwald E. The 50-year history, controversy, and clinical implications of left ventricular outflow tract obstruction in hypertrophic cardiomyopathy from idiopathic hypertrophic subaortic stenosis to hypertrophic. J Am Coll Cardiol 2009;54:191-200. http://doi.org/d4h9qh
10. Maron MS, Olivotto I, Zenovich AG, Link MS, Pandian NG, Kuvin JT, et al. Hypertrophic cardiomyopathy is predominantly a disease of left ventricular outflow tract obstruction. Circulation 2006;114:2232-9. http://doi.org/fn446h
11. Wigle ED, Sasson Z, Henderson MA, Ruddy TD, Fulop J, Rakowski H, et al. Hypertrophic cardiomyopathy. The importance of the site and the extent of hypertrophy. A review. Prog Cardiovasc Dis 1985;28:1-83. http://doi.org/ft7ch2
12. Sherrid MV, Balaram S, Kim B, Axel L, Swistel DG. The Mitral Valve in Obstructive Hypertrophic Cardiomyopathy: A Test in Context. J Am Coll Cardiol 2016;67:1846-58. http://doi.org/f8gxqp
13. Ommen SR. Hypertrophic Cardiomyopathy. Curr Probl Cardiol 2011;36:409-53. http://doi.org/cz46qf
14. Maron BJ, Dearani JA, Ommen SR, Maron MS, Schaff HV, Gersh BJ, et al. The case for surgery in obstructive hypertrophic cardiomyopathy. J Am Coll Cardiol 2004;44:2044-53. http://doi.org/bzpjgn
15. Schaff HV, Dearani JA, Ommen SR, et al. Expanding the indications for septal myectomy in patients with hypertrophic cardiomyopathy: Results of operation in patients with latent obstruction. J Thorac Cardiovasc Surg 143:303-309
16. Desai MY, Bhonsale A, Smedira NG, Naji P, Thamilarasan M, Lytle BW, et al. Predictors of long-term outcomes in symptomatic hypertrophic obstructive cardiomyopathy patients undergoing surgical relief of left ventricular outflow tract obstruction. Circulation 2013;128:209-16http://doi.org/bzpjgn.
17. Schaff HV, Said SM. Transaortic Extended Septal Myectomy for Hypertrophic Cardiomyopathy. Operative Techn Thorac Cardiovascr Surg 2012;17:238–50 http://doi.org/cnr7
18. ElBardissi AW, Dearani JA, Nishimura RA, Ommen SR, Stulak JM, Schaff HV. Septal myectomy after previous septal artery ablation in hypertrophiccardiomyopathy. Mayo Clin Proc 2007;82:1516-22. http://doi.org/cnrx
19. Quintana E, Sabate-Rotes A, Maleszewski JJ, Ommen SR, Nishimura RA, Dearani JA, et al. Septal myectomy after failed alcohol ablation: Does previous percutaneous intervention compromise outcomes of myectomy? J Thorac Cardiovasc Surg 2015;150:159-67. e1. http://doi.org/f7jcg6
20. Zheng S, Zhang H, Li Y, Han J, Jia Y, Meng X. Comparison of Left Atrial and Biatrial Maze Procedure in the Treatment of Atrial Fibrillation: A Meta-Analysis of Clinical Studies. Thorac Cardiovasc Surg. 2016;64:661-71. http://doi.org/cnrz
21. Minakata K, Dearani JA, Nishimura RA, Maron BJ, Danielson GK. Extended septal myectomy for hypertrophic obstructive cardiomyopathy with anomalous mitral papillary muscles or chordae. J Thorac Cardiovasc Surg 2004;127:481-9. http://doi.org/d3hxmf
22. Ommen SR, Maron BJ, Olivotto I, Maron MS, Cecchi F, Betocchi S, et al. Long-term effects of surgical septal myectomy on survival in patients with obstructive hypertrophic cardiomyopathy. J Am Coll Cardiol. 2005;46:470-6. http://doi.org/czx3gw
23. Smedira NG, Lytle BW, Lever HM, Rajeswaran J, Krishnaswamy G, Kaple RK, et al. Current effectiveness and risks of isolated septal myectomy for hypertrophic obstructive cardiomyopathy. Ann Thorac Surg 2008;85:127-33. http://doi.org/btzqhz
24. Maron BJ, Dearani JA, Ommen SR, Maron MS, Schaff HV, Nishimura RA, et al. Low Operative Mortality Achieved With Surgical Septal Myectomy: Role of Dedicated Hypertrophic Cardiomyopathy Centers in the Management of Dynamic Subaortic Obstruction. J Am Coll Cardiol 2015;66:1307-8. http://doi.org/f3hx27
25. Rastegar H, Boll G, Rowin EJ, Dolan N, Carroll C, Udelson JE, et al. Results of surgical septal myectomy for obstructive hypertrophic cardiomyopathy: the Tufts experience. Ann Cardiothorac Surg 2017;6:353-63. http://doi.org/cnr4
26. Iacovoni A, Spirito P, Simon C, Iascone M, Di Dedda G, De Filippo P, et al.A contemporary European experience with surgical septal myectomy in hypertrophic cardiomyopathy. Eur Heart J 2012;33:2080–7. http://doi.org/f37sqm
27. Balaram SK, Sherrid MV, Derose JJ Jr, Hillel Z, Winson G, Swistel DG. Beyond Extended Myectomy for Hypertrophic Cardiomyopathy: The Resection-Plication-Release (RPR) Repair. Ann Thorac Surg 2005;80:217–23. http://doi.org/dmgp69
28. Ferrazzi P, Spirito P, Iacovoni A, Calabrese A, Migliorati K, Simon C, et al. Transaortic Chordal Cutting Mitral Valve Repair for Obstructive Hypertrophic Cardiomyopathy With Mild Septal Hypertrophy. J Am Coll Cardiol 2015;66:1687-96. http://doi.org/f3jhhv
29. Patel P, Dhillon A, Popovic ZB, Smedira NG, Rizzo J, Thamilarasan M. Left Ventricular Outflow Tract Obstruction in Hypertrophic Cardiomyopathy Patients Without Severe Septal Hypertrophy: Implications of Mitral Valve and Papillary Muscle Abnormalities Assessed Using Cardiac Magnetic Resonance and Echocardiography. Circ Cardiovasc Imaging 2015;8:e003132. http://doi.org/cnr5
30. Maron BJ, Ommen SR, Semsarian C, Spirito P, Olivotto I, Maron MS. Hypertrophic Cardiomyopathy Present and Future, With Translation Into Contemporary Cardiovascular Medicine. J Am Coll Cardiol 2014; 64:83–99. http://doi.org/f2sthj
31. Costabel JP, Ametrano MC, Vrancic M, Cura F, Talavera ML, Acosta A, Diez M, Sciancalepore A, Kuschnir P, Avegliano G. Evolución a largo plazo de pacientes con miocardiopatía hipertrófica. Rev Argent Cardiol 2016; 84:222-7.
32. Quintana E, Cox JL Surgical management of atrial fibrillation at the time of septal myectomy. Ann Cardiothorac Surg 2017; 6:386-93. http://doi.org/gbx273
33. Lapenna E, Pozzoli A, De Bonis M, La Canna G, Nisi T, Nascimbene S. Mid-term outcomes of concomitant surgical ablation of atrial fibrillation in patients undergoing cardiac surgery for hypertrophic cardiomyopathy. Eur J Cardio-Thorac Surg 2017;1–7. http://doi.org/cnr6
34. Desai MY, Smedira NG, Bhonsale A, Thamilarasan M, Lytle BW, Lever HM. Symptom assessment and exercise impairment in surgical decision making in hypertrophic obstructive cardiomyopathy: Relationship to outcomes. J Thorac Cardiovasc Surg 2015;150:928-35. http://doi.org/f7s9h8
Notas de autor
Juan M. Vrancic - Blanco Encalada 1543 - (1428) Ciudad Autónoma de Buenos Aires, Argentina