Artículos Originales
La alteración de sistemas natriuréticos renales se asocia con el desarrollo de hipertensión arterial y precede en el tiempo a la aparición de daño renal en un modelo de síndrome metabólico
Alteration of Renal Natriuretic Systems Is Associated with the Development of Hypertension and Precedes the Presence of Renal Damage in a Model of Metabolic Syndrome
La alteración de sistemas natriuréticos renales se asocia con el desarrollo de hipertensión arterial y precede en el tiempo a la aparición de daño renal en un modelo de síndrome metabólico
Revista Argentina de Cardiología, vol. 86, núm. 1, pp. 6-13, 2018
Sociedad Argentina de Cardiología

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 25 Octubre 2017
Aprobación: 29 Noviembre 2017
Resumen:
Objetivos: El objetivo del trabajo consistió en determinar la existencia de alteraciones en los sistemas natriuréticos del péptido natriurético atrial y dopamina renal en un modelo de síndrome metabólico por sobrecarga de fructosa y asociarlas con cambios en la presión arterial sistólica, función renal, estado de la Na+, K+-ATPasa y microalbuminuria.
Material y Métodos: Ratas macho Sprague-Dawley fueron divididas en grupos control (C) y fructosa (F) con agua o solución de F (10%P/V) para beber durante 4, 8 y 12 semanas. En orina, se midió L-dopa y dopamina, sodio, creatinina y albúmina; y en plasma péptido natriurético atrial, insulina, sodio y creatinina. La presión arterial sistólica fue medida por método indirecto. Se midió la actividad y expresión de la Na+, K+-ATPasa así como la expresión de los receptores de péptidos natriuréticos A y C renales.
Resultados: La sobrecarga de fructosa se asoció con el aumento de la insulinemia y la presión arterial sistólica, y con la disminución en la excreción urinaria de sodio desde la semana 4. La excreción urinaria de L-dopa se incrementó y la de dopamina disminuyó (cociente L-dopa/dopamina incrementado) por sobrecarga de fructosa desde la semana 4 y el péptido natriurético atrial plasmático se redujo en las semanas 8 y 12. Estos cambios fueron acompañados por un incremento de la actividad y expresión de la Na+, K+-ATPasa, disminución del receptor de péptidos natriuréticos A y aumento del C. La microalbuminuria se observó en la semana 12 de sobrecarga de fructosa.
Conclusiones: Las alteraciones del péptido natriurético atrial y de la dopamina renal se asociaron con el desarrollo de hipertensión arterial y precedieron a la aparición de microalbuminuria, por lo que se pudo establecer una asociación temporal entre la alteración de ambos sistemas y el desarrollo de daño renal.
Palabras clave: Dopamina, Péptido natriurético atrial, Riñón, Fructosa, Hipertensión, Microalbuminuria.
Abstract:
Objective: The aim of this study was to determine the presence of alterations in the natriuretic systems of atrial natriuretic peptide and renal dopamine in a model of metabolic syndrome induced by fructose overload and to associate them with changes in systolic blood pressure, renal function, Na+/K+-ATPase status and microalbuminuria.
Methods: Male Sprague-Dawley rats were divided into control (C) and fructose (F) groups receiving drinking water or a fructose solution (10% W/V), respectively, for 4, 8 and 12 weeks. L-dopa and dopamine, sodium, creatinine and albumin were measured in urine and ANP, insulin, sodium and creatinine in plasma. Systolic blood pressure was measured by indirect method and the renal activity and expression of Na+/K+-ATPase as well as the renal expression of A- and C-type natriuretic peptide receptors were assessed.
Results: Fructose overload was associated with a significant increase in insulinemia and systolic blood pressure levels and a decrease in urinary sodium excretion since week 4. A significant increase in L-dopa excretion and a decrease in dopamine excretion (increased urinary L-dopa/dopamine ratio) due to fructose overload were observed since week 4 with a decrease in plasma atrial natriuretic peptide at weeks 8 and 12. These changes were accompanied by increased activity and expression of Na+/ K+-ATPase, decreased A-type natriuretic peptide receptor and increased C-type natriuretic peptide receptor expression. Microalbuminuria was observed at week 12 of fructose overload.
Conclusions: Altered atrial natriuretic peptide and renal dopamine were associated with the development of hypertension and preceded in time the presence of microalbuminuria, thus establishing a temporal association between the alteration of both systems and the development of renal damage.
Keywords: Dopamine, Atrial Natriuretic Peptide, Kidney, Fructose, Hypertension, Microalbuminuria.
INTRODUCCIÓN
La hipertensión arterial es la patología crónica de mayor prevalencia e incidencia a nivel mundial y constituye uno de los factores de riesgo cardiovascular que forman parte de la definición de síndrome metabólico. (1, 2) Se ha demostrado que las alteraciones en la excreción renal de sodio poseen vital importancia en la patogénesis de la hipertensión arterial. (3) La dopamina renal y el péptido natriurético atrial (ANP) son dos sistemas natriuréticos capaces de modificar el manejo renal del sodio regulando diversos transportadores de este ion en las células tubulares. (3, 4) De estas células, las proximales son capaces de sintetizar dopamina a partir de la captación y posterior decarboxilación del precursor L-dopa por acción de la enzima dopa descarboxilasa. (5) En condiciones basales, más de 50% de la excreción renal de sodio está regulada por la activación de receptores D1 mediada por dopamina. (6) Por su parte, el ANP ejerce su acción natriurética al activar el receptor de péptidos natriuréticos tipo A (NPRA) en los riñones. (7) El ANP también puede unirse al receptor de péptidos natriuréticos tipo C (NPRC), el cual es considerado un receptor de aclaramiento que medía la degradación de este péptido. (8) Durante la última década, numerosos estudios han sugerido la posible existencia de una interacción entre los péptidos natriuréticos y el sistema dopaminérgico renal. (9, 10). En este sentido, se ha descripto que la dopamina renal y el ANP pueden lograr sus efectos natriuréticos a través de una vía común que implica la desactivación reversible de la Na+, K+-ATPasa renal, enzima cuya alteración está íntimamente relacionada con la retención salina. (11, 12)
Por otro lado, se estima que cerca del 30-50% de los pacientes hipertensos poseen insulino-resistencia. (1, 13) Diversos estudios han establecido una asociación entre la insulino-resistencia y alteraciones en el sistema dopaminérgico renal en la génesis de la hipertensión arterial. (14) Se ha demostrado en ratas con insulino-resistencia por sobrecarga de fructosa (SF), la existencia de una menor excreción urinaria de dopamina, que se correlaciona en forma inversamente proporcional a los niveles de presión arterial. (15) De la misma manera, diversos estudios han confirmado una correlación entre bajos niveles de ANP y altos niveles de glucosa e insulina, así como de colesterol y triglicéridos plasmáticos. (16, 17) Sin embargo, existe poca evidencia acerca de la interacción entre la dopamina renal y el ANP en la fisiopatología de la hipertensión arterial inducida por dieta elevada en fructosa. Asimismo, el riñón es uno de los órganos blanco de la hipertensión arterial, y actualmente la microalbuminuria es un indicador precoz de nefropatía y predictor de cardiopatía isquémica en la hipertensión esencial. (18) En este contexto, se ha demostrado la existencia de una asociación entre síndrome metabólico, insulino-resistencia y daño renal. (19, 20)
El objetivo de este trabajo fue determinar si las alteraciones en los sistemas natriuréticos del ANP y la dopamina renal en ratas con insulino-resistencia por dieta elevada en fructosa se asocian a cambios en la presión arterial sistólica y función tubular renal, al aumento de actividad o expresión de la Na+, K+-ATPasa renal y a la aparición de microalbuminuria como marcador de daño estructural renal.
MATERIALES Y MÉTODOS
Animales de experimentación
Se utilizaron ratas Sprague-Dawley machos de 150 a 180 g, con ciclos de 12 h de luz/oscuridad, a 22 ºC y alimentadas con dieta balanceada para roedores.
Consideraciones éticas
Todos los experimentos se llevaron a cabo respetando las normas de ética de las reglamentaciones internacionales y de acuerdo con los principios de cuidado de animales de experimentación (protocolo aprobado por CICUAL con Res CD 2100-15; EXP-UBA:0035638/15). Las ratas fueron asignadas al azar a 2 grupos al comienzo del estudio: un grupo control (C) con agua de bebida corriente ad libitum y un grupo fructosa (F) con fructosa (al 10% P/V) en el agua de bebida ad libitum por 4, 8 y 12 semanas (n = 8 ratas por grupo y período).
Determinación de los niveles de presión arterial sistólica
Los animales fueron entrenados tres veces por semana en el procedimiento de medición de presión arterial. La presión arterial sistólica (PAS) se determinó antes de comenzar el estudio y al finalizar cada período experimental a través del método indirecto pletismográfico mediante esfigmomanómetro en la cola de la rata, usando un manguito inflable y un micrófono conectado a un amplificador Grass D. C. (modelo 7DAC, Grass Instruments Co.) acoplado a un polígrafo (modelo 79D, Grass Instruments Co.).
Recolección y procesamiento de muestras de orina y sangre
Al finalizar cada período experimental, mediante la utilización de jaulas metabólicas, se recolectaron muestras de orina de 24 h para determinar la diuresis de 24 h y la excreción urinaria de sodio, creatinina, albúmina y de L-dopa y dopamina. Antes del sacrificio y bajo anestesia intraperitoneal con ketamina (80 mg/kg) y xilazina (12 mg/kg) se recolectaron muestras de sangre del plexo retroocular y se centrifugaron a 2700 rpm durante 20 minutos a 4 °C. Las concentraciones plasmáticas y urinarias de sodio, creatinina y albúmina se determinaron en un autoanalizador automatizado (analizador automatizado Spectrum CCX, Abbott diagnostico) por método espectrofotométrico. Los niveles plasmáticos de insulina se determinaron por ELISA (Millipore Corporation). Los niveles plasmáticos de ANP se determinaron por ELISA (R&D Systems), luego de la extracción por cromatografía en fase reversa con cartuchos de Sep-Pak C18, según la metodología de purificación de Sarda y cols. (21)
Determinación de la concentración de L-dopa y dopamina
La determinación de la concentración urinaria de L-dopa y dopamina se llevó a cabo estabilizándolas con ácido acético 1 M (pH 6,10), recuperándolas en alúmina y separándolas mediante cromatografía líquida de alta resolución (HPLC) en fase reversa utilizando columnas de 4,6 mm x 25 cm (Beckman Instruments). Las catecolaminas se detectaron amperométricamente con electrodo Bioanalytical Systems 0.65 V en relación con electrodos Ag/Ag.
Cálculo de parámetros de función renal
Los valores de sodio y creatinina plasmáticos y urinarios se utilizaron para calcular los parámetros de evaluación de funcionalidad renal. La tasa de filtrado glomerular se estimó mediante el aclaramiento de creatinina. Para el estudio de la función tubular, se calculó la excreción urinaria de sodio.
Recolección y procesamiento de tejido renal
Inmediatamente luego del sacrificio, se procedió a extirpar ambos riñones de cada animal, que luego fueron decapsulados. Se obtuvieron cortes de ambos riñones que se almacenaron a –80 ºC para los estudios de western blot y actividad específica de la Na+, K+-ATPasa.
Análisis de expresión proteica por western blot
El análisis semicuantitativo de expresión proteica se llevó a cabo mediante la técnica de western blot, como fue descripto anteriormente. (22) Se determinó la expresión renal de la enzima Na+, K+-ATPasa utilizando el anticuerpo anti-Na+K+-ATPasa (Amersham, dilución 1:8000); así como la expresión renal de NPRA, utilizando el anticuerpo antiNPRA (Santa Cruz Biotechnology, dilución 1:7500); y la expresión de NPRC, utilizando el anticuerpo anti-NPRC (Santa Cruz Biotechnology, dilución 1:400). Para las reacciones secundarias y terciarias, se utilizó el anticuerpo biotinilado IgG anti-conejo (GE Healthcare Life Sciences, dilución 1:2000) y estreptavidina conjugada con peroxidasa de rabanito (GE Healthcare Life Sciences, dilución de 1:2000), respectivamente. Las muestras fueron reveladas por quimioluminiscencia usando el reactivo ECL (Amersham Pharmacia Biotech). La densidad de las bandas se cuantificó mediante el software Image J (RSB). Se utilizó el anticuerpo anti-GAPDH como estándar interno de control de carga (Santa Cruz Biotechnology, dilución 1:1500).
Análisis de actividad específica de Na+, K+-ATPasa
Muestras de 50 mg de corteza renal fueron homogeneizadas (1:10 peso/volumen) en una solución que contenía 25 mM imidazol/1 mM EDTA/0,25 M sacarosa y centrifugadas a 4700 g a 4 °C por 15 minutos. La actividad de ATPasa fue medida por determinación colorimétrica del ortofosfato liberado y se utilizó ouabaina para inhibir específicamente la actividad Na+, K+-ATPasa de acuerdo con el método de Fiske-Subarrow, como describimos previamente. (22)
Análisis estadístico
Los datos se procesaron con el programa GraphPad Prism, versión 2.0. La distribución gaussiana se evaluó por el método Kolmogorov y Smirnov y, para comparar entre los grupos, se utilizó el ANOVA seguido de la prueba de Newman-Keuls o Tukey, según corresponda. Los resultados se expresaron como la media ± SEM. Los resultados con p < 0,05 se consideraron estadísticamente significativos.
RESULTADOS
Parámetros metabólicos, hemodinámicos y de función renal
Los valores de insulina plasmática se incrementaron significativamente por la dieta elevada en fructosa con respecto a las ratas controles desde la semana 4 de tratamiento, lo que indica la existencia de hiperinsulinemia (Tabla 1). Los valores de PAS se incrementaron significativamente en las ratas con dieta elevada en fructosa con respecto a las ratas controles desde la semana 4 de tratamiento (Tabla 1). En los riñones, la sobrecarga de fructosa en la dieta se asoció a un aumento significativo de la diuresis, así como a una reducción en la excreción urinaria de sodio desde la semana 4 de tratamiento en comparación a sus respectivos controles (Tabla 1). El aclaramiento de creatinina no se modificó significativamente por el tratamiento con fructosa en ningún período experimental. La presencia de microalbuminuria como marcador de daño renal se observó en la semana 12 de tratamiento con fructosa (Tabla 1).
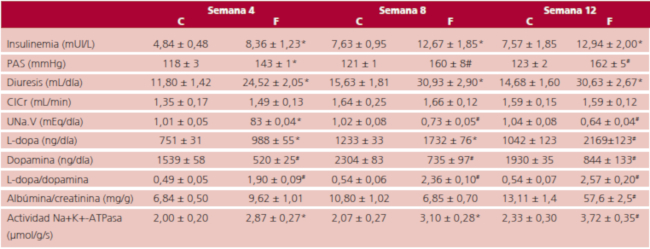
La fructosa se administró en el agua de bebida ad libitum (10% p/v). Los valores se indican como promedio ± ESM (n = 8 animales por grupo). C: Control; F: Fructosa; PAS: Presión arterial sistólica; ClCr: Aclaramiento de creatinina, UNa.V: Excreción urinaria de sodio. *p < 0,05 vs. C; #p < 0,01 vs. C.
Sistema dopaminérgico renal
Se observó una reducción significativa en la excreción urinaria de dopamina junto con un aumento en la excreción de L-dopa en las ratas con dieta elevada en fructosa con respecto a los grupos controles desde la semana 4 de tratamiento. Estos cambios originaron un incremento significativo en el cociente L-dopa/dopamina urinario desde la misma semana (Tabla 1). Los valores de PAS y del cociente L-dopa/dopamina urinario se correlacionaron positivamente durante el período de 12 semanas de estudio (R2 = 0,7816, p = 0,002).
Actividad específica y expresión de la Na+, K+-ATPasa renal
La actividad específica de la Na+, K+-ATPasa renal se incrementó significativamente desde la semana 4 de tratamiento con fructosa con respecto a las ratas controles (Tabla 1). El aumento de actividad fue acompañado por un aumento en la expresión proteica por western blot (Figura 1).
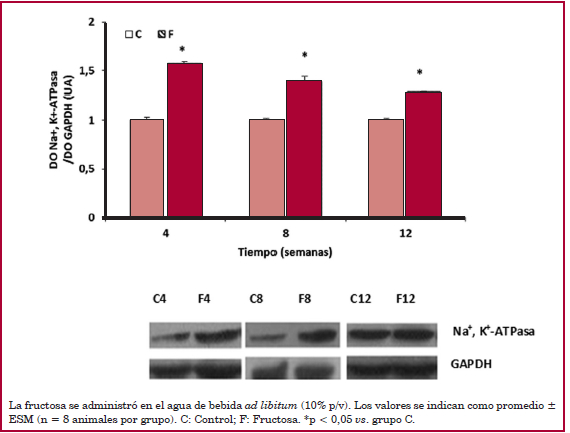
Fig. 1
Expresión proteica de la enzima Na+, K+-ATPasa renal en ratas controles y con dieta elevada en fructosa a las 4, 8 y 12 semanas de tratamiento.
Sistema del ANP
Se observó una disminución significativa de la concentración de ANP plasmático en las ratas con dieta elevada en fructosa en las semanas 8 y 12 de tratamiento (Figura 2). En los riñones, se encontró una disminución en la expresión de NPRA desde la semana 8 (Figura 3) junto con un aumento de expresión de NPRC desde la semana 4 de tratamiento (Figura 4).
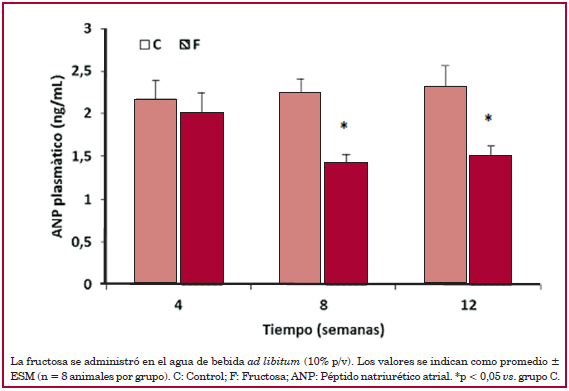
Fig. 2
Niveles de ANP plasmático en ratas controles y con dieta elevada en fructosa a las 4, 8 y 12 semanas de tratamiento.
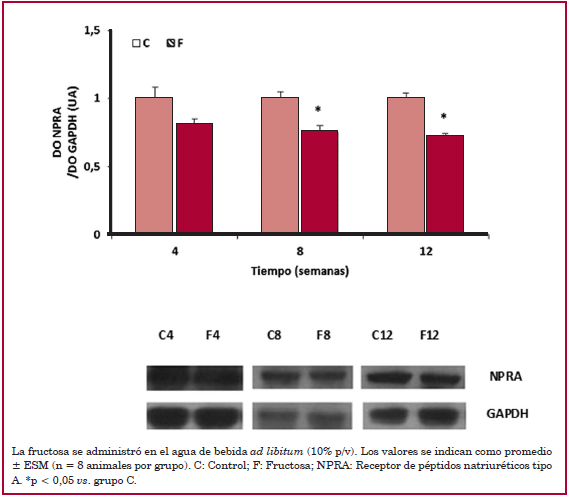
Fig. 3
Expresión proteica de NPRA en los riñones de ratas controles y con dieta elevada en fructosa a las 4, 8 y 12 semanas de tratamiento.
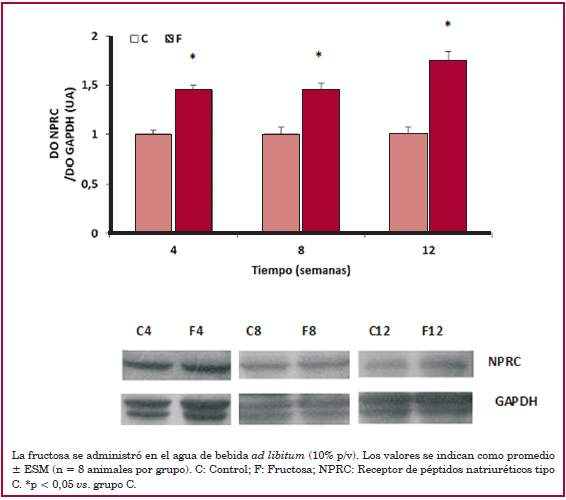
Fig. 4
Expresión proteica de NPRC en los riñones de ratas controles y con dieta elevada en fructosa a las 4, 8 y 12 semanas de tratamiento.
DISCUSIÓN
El síndrome metabólico es una entidad que comprende un conjunto de desórdenes o anormalidades metabólicas considerados factores de riesgo para desarrollar diabetes y enfermedad cardiovascular. (1) Se ha demostrado que las ratas alimentadas con dieta alta en fructosa exhiben un gran número de características del síndrome metabólico, tales como insulino-resistencia, hiperinsulinemia e hipertensión arterial. (23) En nuestros experimentos, las ratas con dieta elevada en fructosa presentaron hiperinsulinemia, lo que indica la existencia de un estado de insulino-resistencia. El incremento de la PAS fue detectado a partir de cuarta semana de tratamiento con fructosa y alcanzó los valores tensionales más altos a las 8 y 12 semanas, con niveles cercanos a los 160 mmHg. Los niveles de PAS se asociaron con una disminución de la excreción urinaria de sodio a partir de la misma semana, hechos que reflejan el estado de retención salina en este modelo experimental. Aunque todavía no se conoce el mecanismo preciso por el cual se desarrolla la hipertensión arterial en estados de insulino-resistencia, algunos estudios sugieren que la hiperinsulinemia podría causar retención de sodio y un aumento de la actividad simpática, factores claves en el desarrollo de esta patología. (24) Otros autores sugieren que el aumento de la reabsorción renal de sodio inducido por insulina está potenciado en la insulino-resistencia. La insulina estimula todos los transportadores de sodio ubicados en los túbulos proximales, entre ellos la bomba Na+, K+-ATPasa, el intercambiador Na+/H+ tipo 3 (NHE3), y el cotransportador basolateral electrogénico Na+/ HCO3– (NBCe1). (24) En nuestro modelo, se observó un incremento en la actividad específica de la enzima Na+, K+-ATPasa desde la semana 4 de tratamiento, acompañado por un incremento en su expresión proteica por western blot. Estos datos son apoyados por otros estudios, en donde se ha demostrado que la enzima Na+, K+-ATPasa es estimulada en estados de insulino-resistencia y exposición crónica de las células renales a insulina plasmática aumentada, lo que conduce a una mayor reabsorción de sodio y agua, y, por lo tanto, mayor retención hidrosalina. (25)
La dieta elevada en fructosa se asoció con alteraciones en los sistemas natriuréticos de la dopamina renal y el ANP. En cuanto al sistema dopaminérgico renal, se observó un progresivo aumento del cociente L-dopa/dopamina urinario a partir de la cuarta semana de tratamiento, a expensas de un incremento en la excreción urinaria de L-dopa y una reducción en la excreción de dopamina. Estos cambios indicarían la existencia de una reducción en la captación tubular de L-dopa, un déficit de conversión de L-dopa en dopamina en las células tubulares o una alteración en la liberación tubular de la amina. En este sentido, se ha demostrado que la insulina estimula el proceso de captación tubular de L-dopa y que dicho efecto se encuentra abolido en modelos de ratas con resistencia a la insulina por sobrecarga de fructosa. (26) En otro modelo de hiperinsulinemia inducida por obesidad, la presencia de resistencia a la insulina junto con un aumento del tono simpático se asoció con una menor actividad dopaminérgica renal. (27) El incremento en el cociente L-dopa/dopamina urinario mostró una correlación positiva con el incremento de la PAS, por lo que se constituye como un buen parámetro que acompaña al incremento de los niveles de presión arterial en este modelo. Por su parte, la concentración plasmática de ANP se redujo significativamente en las ratas con sobrecarga de fructosa a partir de la semana 8, acompañado por una disminución de la expresión del receptor NPRA. Estos resultados son consistentes con la bibliografía, en donde se ha comprobado la existencia de una asociación entre bajos niveles de ANP, reducción en la expresión de NPRA y estados de insulino-resistencia. (16, 17, 28) Una posible explicación de la reducción de la concentración plasmática de ANP consistiría en un aumento de su degradación a cargo de los receptores NPRC. En nuestro estudio, la expresión de NPRC se encontró incrementada en los riñones. Se ha descripto en modelos de obesidad e insulino-resistencia, la existencia de un incremento en los niveles de NPRC en el tejido adiposo que serían responsables de la reducción de los niveles plasmáticos de péptidos natriuréticos en estos estados. (28) Asimismo, la alteración de ambos sistemas natriuréticos precedió en el tiempo a la aparición de microalbuminuria como marcador de daño estructural renal en la semana 12, por lo que puede postularse que la alteración de dichos sistemas estaría asociada con la aparición de daño en este órgano. Con respecto a esto, se ha descripto que la dopamina renal regula el estado inflamatorio y oxidativo a través de sus receptores D2, con aumento de marcadores proinflamatorios y de estrés oxidativo en modelos con deficiencia en estos receptores. (29) Adicionalmente, se ha demostrado que el ANP posee efectos antioxidantes en ratas al atenuar los niveles de especies reactivas del oxígeno en un modelo de daño renal por isquemia-reperfusión. (30)
Nuestro equipo de trabajo ha demostrado que el ANP estimula la captación de dopamina por las células tubulares del riñón, a través de la estimulación de los receptores NPRA y la activación de proteinquinasa G (PKG). (11, 12, 22) Asimismo, se ha demostrado que el ANP incrementa la síntesis de dopamina renal al estimular la actividad de la dopa decarboxilasa. (31) En este modelo de insulino-resistencia, y como resultado de los bajos niveles de ANP plasmático, sería esperable una reducción tanto de la síntesis como de la captación de dopamina por parte de las células tubulares como consecuencia de la reducción en la expresión de los receptores NPRA en los riñones. Estos efectos explicarían la disminución en la excreción urinaria de dopamina y, por lo tanto, el incremento en el valor del cociente L-dopa/dopamina observado en nuestros experimentos.
Los resultados del siguiente trabajo permiten aportar nuevas evidencias de la interacción entre los sistemas del ANP y la dopamina renal, por lo que puede establecerse una asociación entre la reducción en la excreción urinaria de dopamina observada en este modelo de sobrecarga de fructosa en la dieta y una depresión en el sistema del ANP. Asimismo, puede postularse que la afectación de ambos sistemas estaría asociada con el desarrollo de daño renal, teniendo en cuenta que esta precedió en el tiempo a la aparición de daño estructural renal evidenciado por la microalbuminuria en la semana 12 de tratamiento con fructosa.
BIBLIOGRAFÍA
1. DeFronzo RA, Ferrannini E. Insulin resistance -a multifactorial syndrome responsible for NIDDM, obesity, hypertension, dyslipidemia, and atherosclerotic cardiovascular disease. Diabetes Care 1991;14:173-94. http://doi.org/cw3z8h
2. Guzmán NJ. Epidemiology and management of hypertension in the Hispanic population: a review of the available literature. Am J Cardiovasc Drugs 2012;12:165-78.
3. Aperia A. Intrarenal dopamine: a key signal in the interactive regulation of sodium metabolism. Annu Rev Physiol 2000;62:621-47. http://doi.org/f3xz7s
4. Beltowski J, Gorny D, Marciniak A. The mechanism of Na+, K+-ATPase inhibition by atrial natriuretic factor in rat renal medulla. J Physiol Pharmacol 1998; 49:271-83.
5. Carey RM. Theodore Cooper Lecture: Renal DA system: paracrine regulator of sodium homeostasis and blood pressure. Hipertension 2001;38:297. http://doi.org/c9qpt2
6. Armando I, Villar VA, Jose PA. Dopamine and renal function and blood pressure regulation. Compr Physiol 2011; 1:1075-117. http:// doi.org/d3hjj4
7. Anand-Srivastava MB, Trachte GJ. Atrial natriuretic factor receptors and signal transduction mechanisms. Pharmacol Rev 1993;45:455-97.
8. Anand-Srivastava MB. Natriuretic peptide receptor-C signaling and regulation. Peptides 2005;26:1044-59. http://doi.org/fvthmk
9. Marin-Grez M, Briggs JP, Schubert G, Schnermann J. Dopamine receptor antagonists inhibit the natriuretic response to atrial natriuretic factor (ANF). Life Sci 1985; 36:2171-6. http://doi.org/c437bq
10. Petterson A, Hedner J, Hedner T. The diuretic effect of atrial natriuretic peptide (ANP) is dependent on dopaminergic activation. Acta Physiol Scand 1986; 126:619-21. http://doi.org/dndxs9
11. Fernández BE; Correa AH; Choi MR. Atrial natriuretic factor stimulates renal dopamine uptake mediated by natriuretic peptidetype A receptor. Regul Pept 2005; 124:137-44. http://doi.org/ftb9pm
12. Correa AH, Choi MR, Gironacci M, Valera MS, Fernández BE. Signaling pathways involved in atrial natriuretic factor and dopamine regulation of renal Na+, K+ -ATPase activity. Regul Pept 2007;138:26-31. http://doi.org/bpck37
13. De Fronzo RA: Insulin resistance, hyperinsulinemia and coronary artery disease. J Cardiovasc Pharmacol 1992;20:S1-S16. http://doi. org/fbjzvw
14. Trivedi M, Marwaha A, Lokhandwala M. Rosiglitazone restores G-protein coupling, recruitment, and function of renal dopamine D1A receptor in obese Zucker rats. Hypertension 2004;43:376-82. http://doi.org/fbnnqs
15. Hasegawa K, Yoshida H, Ura N, Murakami H, Hagiwara M, Shimamoto K. The role of renal natriuretic and depressor systems in insulin-resistant hypertensive rats. Hypertens Res 2004;27:501-8. http://doi.org/cbqn6h
16. Miyashita K, Itoh H, Tsujimoto H, Tamura N, Fukunaga Y, Sone M, et al. Natriuretic peptides/cGMP/cGMP-dependent protein kinase cascades promote muscle mitochondrial biogenesis and prevent obesity. Diabetes 2009;58:2880-92. http://doi.org/fqncmz
17. Olsen MH, Wachtell K, Tuxen C, Fossum E, Bang LE, Hall C, et al. Opposite effects of losartan and atenolol on natriuretic peptides in patients with hypertension and left ventricular hypertrophy: a LIFE substudy. J Hypertens 2005;23:1083-90. http://doi.org/fvw3sv
18. Gerstein HC, Mann JF, Yi Q, Zinman B, Dinneen SF, Hoogwerf B, et al. Albuminuria and risk of cardiovascular events, death and hearth failure in diabetic and nondiabetic individuals. JAMA 2001;286:421-6. http://doi.org/crwp49
19. Gluba A, Mikhailidis DP, Lip GY, Hannam S, Rysz J, Banach M. Metabolic syndrome and renal disease. Int J Cardiol 2013;164:141-50. http://doi.org/f4phvp
20. Locatelli F, Pozzoni P, Del Vecchio L. Renal Manifestations in the Metabolic Syndrome. J Am Soc Nephrol 2006;17:S81-5. http:// doi.org/fhvffm
21. Sarda IR, Wigle DA, Flynn TG, Pang SC. Radioimmunoassay for rat B-type natriuretic peptide (BNP-45). J Immunoassay 1993;14:167-82. http://doi.org/d7hsdd
22. Kouyoumdzian NM, Rukavina Mikusic NL, Kravetz MC, Lee BM, Carranza A, Del Mauro JS, et al. Atrial Natriuretic Peptide Stimulates Dopamine Tubular Transport by Organic Cation Transporters: A Novel Mechanism to Enhance Renal Sodium Excretion. PLoS One 2016; 11:e0157487. http://doi.org/gbqcbp
23. Wong SK, Chin KY, Suhaimi FH, Fairus A, Ima-Nirwana S. Animal models of metabolic syndrome: a review. Nutr Metab (Lond) 2016;13:65. http://doi.org/cncp
24. Horita S, Seki G, Yamada H, Suzuki M, Koike K, Fujita T. Insulin resistance, obesity, hypertension, and renal sodium transport. Int J Hypertens 2011;2011:391762. http://doi.org/cwcsks
25. Iannello S, Milazzo P, Belfiore F. Animal and human tissue Na,K-ATPase in normal and insulin-resistant states: regulation, behaviour and interpretative hypothesis on NEFA effects. Obes Rev 2007;8:231-51. http://doi.org/brg3mf
26. Carranza A, Mendez CF, Barontini M, Nowicki S. Insulin enhances L-dopa renal proximal tubule uptake: a regulatory mechanism impaired in insulin resistance. Pflugers Arch 2004;448:85-92. http://doi.org/fqmsww
27. Moreira-Rodrigues M, Quelhas-Santos J, Roncon-Albuquerque R, Serrão P, Leite-Moreira A, Sampaio-Maia B, Pestana M. Blunted renal dopaminergic system in a mouse model of dietinduced obesity. Exp Biol Med (Maywood) 2012;237:949-55. http://doi.org/f39hwp
28. Wang TJ, Larson MG, Levy D, et al. Impact of obesity on plasma natriuretic peptide levels. Circulation 2004;109:594‐600. http://doi.org/bbqmdj
29. Armando I, Wang X, Villar VA, Jones JE, Asico LD. Hypertension 2007;49:672-8.
30. Koga H, Hagiwara S, Kusaka J, Matsumoto S, Nishida T, Yokoi I, et al. Human atrial natriuretic peptide attenuates renal ischemia-reperfusion injury. J Surgical Res 2012; 173:348-53. http://doi.org/bh54w8
31. Choi MR, Rukavina Mikusic NL, Kouyoumdzian NM, Kravetz MC, Fernández BE. Atrial natriuretic peptide and renal dopaminergic system: a positive friendly relationship? Biomed Res Int 2014;2014:710781. http://doi.org/dckpsn
Abreviaturas
ANP: Péptido natriurético atrial
NPRA: Receptor de péptidos natriuréticos tipo A
C: Grupo control
NPRC: Receptor de péptidos natriuréticos tipo C
ClCr: Aclaramiento de creatinina
PAS: Presión arterial sistólica
F: Grupo con sobrecarga de fructosa
PKG: Proteinquinasa G
HPLC: Cromatografía líquida de alta resolución
SF: Sobrecarga de fructosa
NBCe1: Cotransportador Na+/HCO3– tipo 1
UNa.V: Excreción urinaria de sodio.
NHE3: intercambiador Na+/H+ tipo 3
Notas de autor
Natalia Lucía Rukavina Mikusic - Instituto de Investigaciones Cardiológicas (ININCA), Universidad de Buenos Aires, CONICET - Marcelo T. de Alvear 2270 - C1122AAJ CABA, Buenos Aires, Argentina - Tel: (54 11) 4508-3880