PÁGINA DEL EDITOR
El costo-efectividad del implante transcatéter de la válvula aórtica en Argentina
Cost-Effectiveness of the transcatheter aortic valve implantation in Argentina
El costo-efectividad del implante transcatéter de la válvula aórtica en Argentina
Revista argentina de cardiología, vol. 88, núm. 1, pp. 76-79, 2020
Sociedad Argentina de Cardiología
En noviembre de 2019 la Comisión Nacional de Evaluación de Tecnologías de Salud (CONETEC) publicó las recomendaciones para el uso del implante transcatéter de la válvula aórtica (TAVI) en Argentina. En sus conclusiones apoya la incorporación del TAVI solo para los pacientes inoperables, y lo desaconseja para el resto de los grupos de riesgo, basadas en la falta de beneficios en puntos críticos (mortalidad), la escasa evidencia en cuanto a la durabilidad, el potencial alto impacto económicodesfavorabley el impacto negativo en la equidad y,probablemente,en la salud pública.1 El documento incluye un detallado análisis bibliográfico de los resultados clínicos internacionales y del costo-efectividad de la implementación del TAVI en Argentina.
Es probable que este análisis de un organismo gubernamental induzca a los financiadores de salud a restringir la indicación y la cobertura de un TAVI, aprovechando estos argumentos oficiales. De todas formas, en un sistemacapitalista estable y libre como el de Argentina, los médicos, los pacientes o las instituciones pueden tomar decisiones independientes que contradigan estas recomendaciones estatales.
La evaluación de las nuevas tecnologías mediante el análisis de costo-efectividad permite identificar el valor relativo de las intervenciones sobre la base de mediciones de su costo neto y sus efectos sobre la salud. Para ello compara el costo y los resultados de dos o más procedimientos y determina su relación de costo-eficiencia en el clásico cuadrante de Black 2 (Figura 1). En el caso de Argentina el TAVI se ubicaría en el cuadrante superior izquierdo (Figura 1).
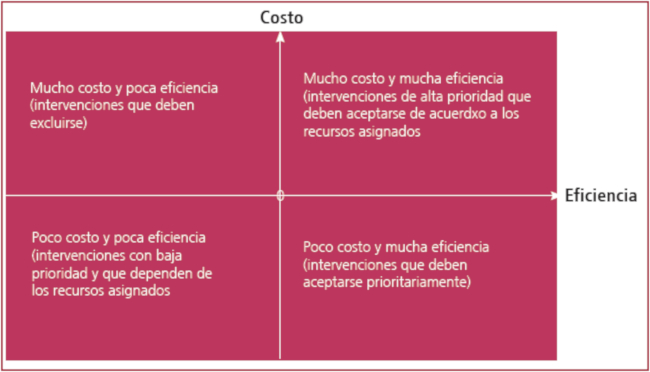
Fig. 1
Cuadrante de Black para determinar le relación de costo-eficiencia de nuevas tecnologías
El implante transcatéter de la válvula aórtica en Argentina se encuentra en el cuadrante superior izquierdo, según el análisis de laComisión Nacional de Evaluación de Tecnologías de Salud.
Las recomendaciones señalan además, que por el momento en Latinoamérica, únicamente Chile acepta la cobertura del TAVI en pacientes inoperables por cirugía convencional, mientras que el resto de los países no informan acerca de su cobertura, o no lo recomiendan, como en el caso de Brasil.
Al igual que el National Institute for Health and Care Excellence (NICE) del Reino Unido, el Medicare y el Medicaid en EE. UU. aceptan la cobertura del TAVI en pacientes inoperables o de riesgo alto, mientras que solo el Anthem Health Insurance lo recomienda en riesgos intermedio y bajo. Australia y Francia no aconsejan el uso de TAVI por el momento. De todas formas, debe mencionarse que muchas de estas recomendaciones no tienen actualizaciones recientes. En la Tabla 1 se resume en forma detallada las sugerencias de la CONETEC para el uso de TAVI en Argentina.

CONETEC: Comisión Nacional de Evaluación de Tecnologías de Salud. TAVI: Implante transcatéter de la válvula aórtica. IRA: Insuficiencia renal aguda. VI: Ventrículo izquierdo.
En rigor, el documento de la CONETEC incluye los estudios publicados hasta julio de 2019, mientras que a partir de esa fecha aparecieron algunos metaanálisis más, sobre todo para pacientes de bajo riesgo. 3,4,5,6,7 De todas formas, esta nueva evidencia no parece cambiar los resultados previos. También tras la fecha de realización de esas recomendaciones se publicó un metaanálisis sobre la ocurrencia de mismatch moderado o grave al año del uso del TAVI, con una incidencia de 36,3%. Los autores concluyeron que el mismatch grave se asoció a un mayor riesgo de mortalidad al año (OR 1,11,95%; CI 1,04-1,18, p = 0,001). 8 Otro registro reciente -de 4.336 procedimientos- comunicó un riesgo de endocarditis posTAVI de 1,4% dentro del primer año, y de 0,8% para los años siguientes; incidencia similar a la que ocurre con la cirugía. 9
Otros tres análisis de costo-efectividad aparecieron en el últimoperíodo mencionado y no fueron incluidos en las recomendaciones. En Japón se demostró que el TAVI fue costo-efectivo en los pacientes inoperables y de alto riesgo 10, en Australia lo fue en pacientes de riesgo intermedio 11, mientras que en Dinamarca fue en pacientes de bajo riesgo. 12 Con respecto a la durabilidad del TAVI, Orvin et al. 13 comunicaron recientemente un deterioro estructural de la prótesis a 5 años, de 12,3%, y Rheude et al. 14 un deterioro al año de 10,3%.
Finalmente, otros estudios posteriores podrían aportar nueva evidencia a estas recomendaciones, como son los resultados de las prótesis balón expandibles o autoexpandibles 15,16,17, o la declaración sobre TAVI de la Sociedad Cardiovascular Canadiense. 18
El sistema normativo sanitario argentino ha tenido una escasa regulación en la incorporación de nuevas tecnologías. La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) evalúa y aprueba la eficacia y la seguridad de los nuevos tratamientos, pero no tiene injerencia en su adopción por parte del sistema de salud. De esta manera, el ingreso de nuevas tecnologías queda librado a la presión de la industria, de los financiadores y de los grupos médicos interesados. Asimismo, existe implícitamente un sistema de incentivos para los médicos, en el cual la industria puja por la adopción de las innovaciones, mientras que los financiadores tienden a limitarla por una razón de costos. 19.
En este contexto la CONETEC fue creada en marzo de 2018 para evaluar el impacto sobre la salud de la población de los nuevos medicamentos, los dispositivos médicos, las técnicas y procedimientos clínicos y quirúrgicos. Si bien muchas sociedades científicas locales estudian y elaboran muy seriamente consensos y guías de recomendaciones que incluyen estas nuevas tecnologías, es común que quienes las redactan se apoyen más en los beneficios directos que tendría una innovación sobre el tratamiento o de la prevención de la enfermedad, que en su costo-efectividad; situación que empeora si se considera que habitualmente las tecnologías más eficientes suelen ser a la vez, más costosas.
En esta puja entre las ventajas de los avances tecnológicos y la necesidad de contener los costos se plantean ciertos escenarios de negociación. Por un lado, uno de los factores más importantes que influye la adopción de innovaciones por parte de los médicos es la política de reembolso. La aceptación de los financiadores de pagar por una nueva práctica acelera la difusión y la adopción de la tecnología, y viceversa. 20 Por otro lado, la implementación de un sistema de no reembolso de ganancias por usar nuevas tecnologías durante un período de evaluación inicial, podría desanimar la diseminación temprana de la innovación hasta que se determine su efectividad real; pero, a la vez, podría reducir el interés por el desarrollo de nuevos avances médicos. 21
También existen consideraciones éticas para destacar con respecto a la incorporación de innovaciones. Algunos investigadores han señalado que aunque el pago a los médicos representa solo el 20% del gasto en salud, son ellos quienes realizan el 80% de las prácticas solicitadas. 22 Sin duda, el hecho de ser decisor y autorreferente para realizar la nueva práctica, o ser el dueño del equipamiento médico, añade una complicada dimensión ética al problema. 23,24
Un aspecto adicional en la adopción de nuevas tecnologías es la participación de los pacientes en la evaluación de los beneficios. Con buena intención la CONETEC está incorporando también la opinión de los pacientes en sus decisiones. Si bien esta es una situación deseable, se debe considerar cómo se forma la opinión de los pacientes sobre las innovaciones. En primer lugar, el “boca en boca” puede ser un mecanismo de rápida aceptación de nuevos procedimientos, como fue el caso de la colecistectomía laparoscópica, en la que la popularidad no fue el resultado del discurso científico tradicional. 25 Además, otro fenómeno de influencia es la publicidad de los productos nuevos directamente en el usuario, hecho que promueve la demanda del paciente al médico para aplicar la innovación. Por último, un aspecto social que subyace bajo la adopción de innovaciones costosas es que, necesariamente, estas solo podrían ser accesibles a los grupos de pacientes con mayores recursos económicos, lo que a su vez aumentaría la inequidad en el acceso y la atención de salud, en detrimento de los grupos más marginados.
Comparado con gran parte del mundo desarrollado, mucho del inadecuado costo-efectividad del TAVI en Argentina se debe al alto precio de venta del dispositivo, situación que tal vez podría paliarse con una razonable exención de gravámenes impositivos locales.
Las recomendaciones de la CONETEC sobre el uso del TAVI en Argentina tienen carácter temporal y dinámico, y podrían cambiar ante la aparición de nueva evidencia o de otros modelos de financiación de los implantes. Pero por el momento, la CONETEC ha hecho el primer relevamiento técnico serio del costo-efectividad del TAVI en Argentina. Esperemos su resonancia en los otros actores.
BIBLIOGRAFÍA
Comisión Nacional de Evaluación de Tecnologías de Salud - CONETEC. Implante Transcatéter de válvula aórtica en la estenosis aórtica severa. Informe de Evaluación de Tecnologías Sanitarias N° 07, Buenos Aires, Argentina. Noviembre 2019. Disponible en: http://www.argentina.gob.ar/salud/conetec
Black WC. The cost-effectiveness plane: a graphic representation of cost-effectiveness. Med Des Making 1990;10:212-5.https://doi.org/10.1177/0272989X9001000308
Vipparthy SC, Ravi V, Avula S, Kambhatla S, Mahmood M, Kabour A, et al. Meta-Analysis of Transcatheter Aortic Valve Implantation Versus Surgical Aortic Valve Replacement in Patients With Low Surgical Risk. Am J Cardiol 2019 Nov 8. pii: S0002-9149(19)31222-6. https://doi.org/10.1016/j.amjcard.2019.10.036
Rawasia WF, Usman MS, Mujeeb FA, Zafar M, Khan SU, Alkhouli M. Transcatheter versus surgical aortic valve replacement in low surgical risk patients: A meta-analysis of randomized-controlled trials and propensity-matched studies. CardiovascRevasc Med 2019 Oct 24. pii: S1553-8389(19)30641-4. https://doi.org/10.1016/j.carrev.2019.09.016
Witberg G, Landes U, Lador A, Yahav D, Kornowski R. Meta-Analysis of Transcatheter Aortic Valve Implantation Versus Surgical Aortic Valve Replacement in patients at Low Surgical Risk. EuroIntervention 2019 Oct 1. pii: EIJ-D-19-00663. https://doi.org/10.4244/EIJ-D-19-00663
Siontis GCM, Overtchouk P, Cahill TJ, Modine T, Prendergast B, Praz F, et al. Transcatheter aortic valve implantation vs. surgical aortic valve replacement for treatment of symptomatic severe aortic stenosis: an updated meta-analysis. Eur Heart J 2019;40:3143-53. https://doi.org/10.1093/eurheartj/ehz275
Takagi H, Hari Y, Nakashima K, Kuno T, Ando T; ALICE (All-Literature Investigation of Cardiovascular Evidence) Group. A meta-analysis of ≥ 5-year mortality after transcatheter versus surgical aortic valve replacement. J CardiovascSurg (Torino) 2019 Oct 25. https://doi.org/10.23736/S0021-9509.19.11030-0
Sá MPBO, Cavalcanti LRP, Sarargiotto FAS, Perazzo ÁM, Rayol SDC, Diniz RGS, et al. Impact of Prosthesis-Patient Mismatch on 1-Year Outcomes after Transcatheter Aortic Valve Implantation: Meta-analysis of 71,106 Patients. Braz J CardiovascSurg 2019;34: 318-26. https://doi.org/10.21470/1678-9741-2019-0073
Bjursten H, Rasmussen M, Nozohoor S, Götberg M, Olaison L, Rück A, et al. Infective endocarditis after transcatheter aortic valve implantation: a nationwide study. EurHeart J 2019;40:3263-9. https://doi.org/10.1093/eurheartj/ehz588
Inoue S, Nakao K, Hanyu M, Hayashida K, Shibahara H, Kobayashi M, et al. Cost-Effectiveness of Transcatheter Aortic Valve Implantation Using a Balloon-Expandable Valve in Japan: Experience From the Japanese Pilot Health Technology Assessment. Value Health Reg Issues 2019;21:82-90. https://doi.org/10.1016/j.vhri.2019.07.013
Zhou J, Liew D, Duffy SJ, Walton A, Htun N, Stub D. Cost-effectiveness of transcatheter aortic valve implantation compared to surgical aortic valve replacement in the intermediate surgical risk population. Int J Cardiol 2019;294:17-22. https://doi.org/10.1016/j.ijcard.2019.06.057
Geisler BP, Jørgensen TH, Thyregod HGH, Pietzsch JB, Søndergaard L. Cost-Effectiveness of Transcatheter versus Surgical Aortic Valve Replacement in Patients at Lower Surgical Risk: Results from the NOTION Trial. EuroIntervention 2019 Aug 20. pii: EIJ-D-18-00847. http://doi.org/10.4244/EIJ-D-18-00847
Orvin K, Zekry SB, Morelli O, Barabash IM, Segev A, Danenberg H, et al. Long-Term Functional and Structural Durability of Bioprosthetic Valves Placed in the Aortic Valve Position via Percutaneous Rout in Israel. Am J Cardiol 2019;124:1748-56. https://doi.org/10.1016/j.amjcard.2019.08.043
Rheude T, Pellegrini C, Cassese S, Wiebe J, Wagner S, Trenkwalder T, et al. Hemodynamic structural valve deterioration following transcatheter aortic valve implantation with latest-generation balloon-expandable valves. EuroIntervention 2019 Sep 10. pii: EIJ-D-19-00710.
Van Belle E, Vincent F, Labreuche J, Auffret V, Debry N, Lefevre T, et al. Balloon-Expandable versus Self-Expanding Transcatheter Aortic Valve Replacement: A Propensity-Matched Comparison from The France-TAVI Registry. Circulation 2019 Nov 16. https://doi.org/10.1161/CIRCULATIONAHA.119.043785
He C, Xiao L, Liu J. Safety and efficacy of self-expandable Evolut R vs. balloon-expandable Sapien 3 valves for transcatheter aortic valve implantation: A systematic review and meta-analysis. ExpTher Med 2019;18:3893-904. https://doi.org/10.3892/etm.2019.8000
Acconcia MC, Caretta Q, Monzo L, Tanzilli G, SiliScavalli A, Sergi D, et al. Effectiveness of the new generation transcatheter aortic valve in the real life studies. Review and meta-analysis. Eur Rev Med PharmacolSci 2019;23:8018-27. https://doi.org/10.26355/eurrev_201909_19018
Asgar AW, Ouzounian M, Adams C, Afilalo J, Fremes S, Lauck S, et al. 2019 Canadian Cardiovascular Society Position Statement for Transcatheter Aortic Valve Implantation. Can J Cardiol 2019;35:1437-48. https://doi.org/10.1016/j.cjca.2019.08.011
Borracci RA, Giorgi MA, Giorgi G, Darú V, Manente D, Tajer CD, et al. Diffusion and adoption of health care innovations in cardiology, in Argentina. Rev Med Chile 2013;141:49-57.https://doi.org/10.4067/S0034-98872013000100007
Gelijns AC, Fendrick AM. The dynamics of innovation in minimally invasive therapy. Health Policy 1993;23:153-66.https://doi.org/10.1016/0168-8510(93)90013-F
James AE. The diffusion of medical technology: Free enterprise and regulatory models in USA. J Med Ethics 1991;17:150-5.https://doi.org/10.1136/jme.17.3.150
Eisenberg JM, Schwartz JS, McCaslin FC, Kaufman R, Glick H, Kroch E. Substituting diagnostic services: New tests only partly replace older ones. JAMA 1989;262:1196-200. https://doi.org/10.1001/jama.1989.03430090058033
Highes DR, Sunshine JH, Bhargavan M, Forman H. Physician self-referral for imaging and the cost of chro¬nic care for Medicare beneficiaries. Med Care 2011;49:857-64. https://doi.org/10.1097/MLR.0b013e31821b35ee
Reschovsky J, Cassil A, Pham HH. Physician ownership of medical equipment. Data Bull (Cent Stud Health Syst Change) 2010;36:1-2.
Gelijns AC, Fendrick AM. The dynamics of innovation in minimally invasive therapy. HealthPolicy 1993;23:153-66.https://doi.org/10.1016/0168-8510(93)90013-F
Declaración de intereses
