ARTÍCULO DE OPINIÓN
INTRODUCCIÓN
La sola observación del corazón “in situ” en el mediastino nos revela su situación helicoidal en el espacio. Esta realidad deriva consecuentemente en conferir una nomenclatura adecuada a las cámaras cardíacas con relación a la ubicación que ostentan en su orientación tridimensional.
Clásicamente las cámaras fueron designadas como aurículas derecha e izquierda y ventrículos derecho e izquierdo. Estas referencias espaciales no sitúan en su real ubicación a dichas cámaras ni tampoco vuelven comprensible la disposición de la estructura helicoidal del corazón para cumplir con sus funciones de torsión (eyección) y detorsión (succión). 1) (2) (3) (4) (5
Ubicación anatómica espacial. Al observar el corazón en su posición natural en el mediastino (Figura 1) fácilmente evidenciamos que la aurícula derecha corresponde a esta situación topográfica espacial. El resto de las cámaras son erróneas en su nomenclatura con relación a la disposición tridimensional que ostentan. El ventrículo derecho es ántero-derecho, casi no deja espacio en esta ubicación al ventrículo denominado izquierdo, el cual al ser desplazado por el ventrículo antero-derecho en su rotación levógira lo lleva a una ubicación apenas izquierda, pero fundamentalmente posterior en casi todo su volumen, debiendo ser llamado en consecuencia ventrículo póstero-izquierdo. Por su parte la aurícula izquierda se halla aún más rotada hacia atrás, al punto que se ubica por detrás de la aorta ascendente, separada de esta por el llamado seno transverso de Theile y apenas emerge el extremo de su orejuela en una posición izquierda (Figura 1). Por lo tanto, debería ser mencionada como aurícula posterior. Esta situación explica claramente la rotación levógira del corazón en su conformación helicoidal.
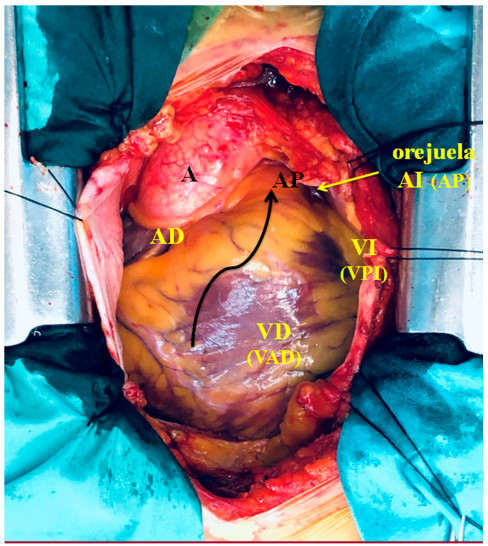
Fig. 1
Imagen de corazón humano “in situ” en un paciente previo a una cardiocirugía. Entre paréntesis la nomenclatura propuesta. Referencias. A: aorta; AP: arteria pulmonar, AD: aurícula derecha; AI (AP): aurícula izquierda (aurícula posterior); VI (VPI): ventrículo izquierdo (ventrículo póstero-izquierdo); VD (VAD): ventrículo derecho (ventrículo ántero-derecho). La flecha negra indica el sentido de la torsión helicoidal levógira del circuito venoso alrededor del arterial.
De esta manera se debe conferir una nomenclatura coherente a las cámaras cardíacas de acuerdo con la disposición tridimensional analizada. Las mismas requieren ser denominadas desde su ubicación espacial: aurícula derecha, ventrículo ántero-derecho, ventrículo póstero-izquierdo y aurícula posterior.
Esta hélice anátomo-funcional se halla constituida, en sus cámaras ventriculares, 6 por dos bandeletas denominadas descendente y ascendente. La primera incluye los segmentos derecho, izquierdo y descendente; mientras que la segunda queda conformada por el segmento restante, el ascendente (Figura 2). De este modo la estructura muscular miocárdica describe dos vueltas en espiral con inserción de sus extremos inicial y terminal en un núcleo cuya estructura es ósea, condroide o tendinosa, de acuerdo con los diferentes especímenes animales y humanos estudiados en nuestras investigaciones. Al mismo lo hemos denominado fulcro cardíaco (Figura 2). 7 Esta inserción es el único sitio perceptible de donde se originan y terminan las fibras miocárdicas.
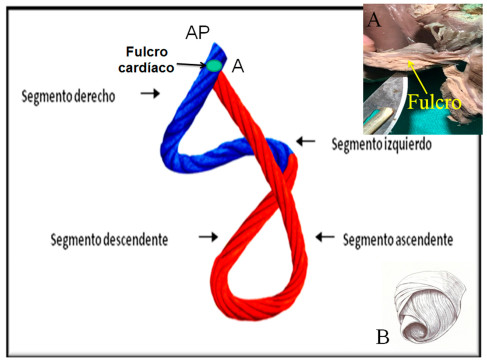
Fig. 2
Ubicación del fulcro cardíaco en el miocardio continuo (modelo de la cuerda). FC: Fulcro cardíaco; AP: Arteria pulmonar; A: Aorta. Referencias. A: Fulcro cardíaco resecado (corazón humano). B: se muestra la disposición tridimensional del miocardio continuo.
Este sitio de inserción, que hemos denominado fulcro cardíaco, se encuentra en las proximidades de la válvula tricúspide (derecha), de la aorta (superior) y del cordón pulmo-tricuspídeo (anterior). Para poder hallarlo es necesario desplazar hacia la izquierda del observador la arteria pulmonar y el segmento derecho, desnudando a la raíz de la aorta. Este gesto descubre al fulcro ubicado como un elemento complementario entre la aorta y el miocardio, equidistante de ambos trígonos, por debajo del nacimiento de la arteria coronaria derecha y desprendido de la continuidad aórtica.
Este análisis no solo es semántico, sino que evidencia la rotación del tubo primitivo en la conformación del asa cardíaca. En la observación de la Figura 1 vemos como el trayecto venoso del sistema circulatorio se halla enroscado sobre el trayecto arterial. A tal fin, la arteria pulmonar participa de esta rotación abrazando a la aorta. Se sitúa hacia la izquierda y en ubicación anterior a la aorta, y acompaña a la traslación levógira del ventrículo derecho hacia el mismo lado, al punto que éste deja de ser estrictamente derecho, para ser fundamentalmente anterior. La aorta se comporta en carácter de eje sobre la rotación espacial de las cámaras cardíacas para transformarlo en un corazón helicoidal.
Filogenia
El aparato circulatorio de los gusanos (anélidos, nemertinos) está constituido por un sistema cerrado provisto de dos lechos capilares (pulmonar y sistémico) y dos semicírculos, denominados arterial y venoso. En este sistema de circulación único la sangre se impulsa en forma peristáltica (expresión y succión) ya que carece del impulso de un corazón (Figura 3 A).
En la evolución hacia los peces se observa la aparición, en el semicírculo venoso, de un corazón primitivo constituido por tres dilataciones denominadas seno venoso, aurícula y ventrículo, ubicadas en forma consecutiva. Si bien el circuito continúa siendo único se produce la aparición de una cámara impulsora (ventrículo) con posibilidad de incrementar las presiones intravasculares (Figura 3 B). En el desarrollo biológico siguiente, constituido por anfibios y reptiles, se producen modificaciones mucho más prominentes. En ese momento evolutivo se distinguen dos circuitos, el sistémico y el respiratorio, mientras que el corazón presenta dos aurículas y un ventrículo, éste último generado por un incipiente bucle en el circuito arterial. 8) (9
La torsión del tubo circulatorio sobre sí mismo, en un segmento del semicírculo arterial (circuito sistémico), constituye un paso trascendental en el desarrollo evolutivo de las especies (Figura 3 C). Tras este bucle se van a conformar las cámaras ventriculares futuras, morfología que se comprende bien al desplegar la continuidad muscular que ostenta el miocardio. 4
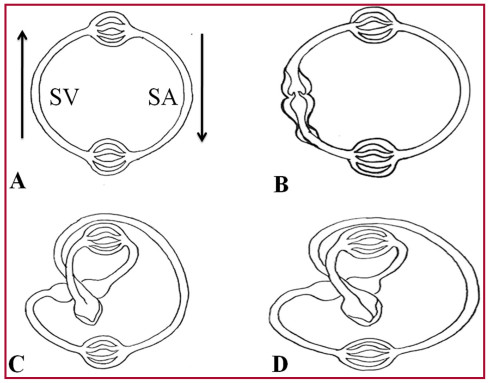
Fig. 3
Filogenia del sistema circulatorio. SV: segmento venoso; SA: segmento arterial. Las flechas señalan el sentido de la circulación. A: gusanos. B: peces. Se puede observar las tres dilataciones del segmento venoso (seno venoso, aurícula y ventrículo). C: anfibios y reptiles. Se inicia, en el segmento arterial, el bucle que dará origen a ambos ventrículos y que se completa definitivamente en D: aves y mamíferos.
El desarrollo del aparato circulatorio en las aves y los mamíferos permite distinguir dos aurículas y dos ventrículos. En el semicírculo arterial se completa el bucle iniciado en los anfibios y reptiles, con conformación de una estructura miocárdica helicoidal. En ese segmento, en el bucle instaurado en el tubo arterial primitivo, el efecto producido por una hendidura longitudinal da lugar a canales que constituirán los dos ventrículos (Figura 3 D). En los orígenes de la arteria pulmonar y de la aorta de los mamíferos se hallan evidencias que se han relacionado con esa hendidura evolutiva producida en el tramo arterial.10 Las mismas corresponderían al espacio entre los trígonos en la parte posterior de la aorta, donde encaja la valva posterior de la mitral, mientras que en la pulmonar estaría representado por la división del segmento paraendocárdico (perteneciente al segmento derecho, inicio del miocardio) en dos bandas: pulmonar y del tabique. Ambas evidencias guardan la forma de una V invertida, denunciando el inicio de la hendidura que llevó a la constitución del miocardio continuo. 9
Este proceso consigue proveer de dos cámaras para impulsar la sangre a la salida del bucle hacia el lecho sistémico, con una energía suficiente y alta velocidad (en el humano alcanza 200 cm/s) a través del ventrículo izquierdo; y a la arteria pulmonar por medio del ventrículo derecho con el desarrollo de presiones del 20% de las sistémicas. Este ardid evolutivo permitió el desarrollo de una cámara capaz de impulsar el flujo intravascular en el segmento del circuito arterial a una velocidad suficiente para que el fluido mantenga su circulación a lo largo de todo el organismo. De esta manera, los ventrículos provienen en los mamíferos del incipiente enroscamiento del segmento arterial correspondiente al circuito arterial de los anfibios y reptiles.
Si retrocedemos hacia el estadio primario en la evolución del sistema circulatorio se aprecian los hitos filogenéticos de las distintas especies. Las aurículas pertenecen al segmento venoso y los ventrículos al arterial. Una incurvación subsiguiente más pronunciada del segmento arterial permite poner en contacto a las aurículas con los ventrículos respectivos. De esta manera, la disposición en un plano horizontal de ambas aurículas (cámaras originadas en el semicírculo venoso) se adosa al plano del componente ventricular (semicírculo arterial).
En la recapitulación que la ontogenia hace de la filogenia 11 puede observarse en el embrión humano la flexión del tubo cardíaco, que primeramente se lateraliza y luego se tuerce en espiral, rememorando el proceso evolutivo (Figura 4). De esta manera el asa bulboventricular se incurva hacia la derecha y adelante. Este movimiento es posible por la desaparición del mesocardio dorsal que deja al corazón totalmente péndulo en el tórax, pero sujeto a un punto de fijación que hemos denominado fulcro cardiaco. 7 Esto implica, como en todo músculo, el punto de soporte de la palanca muscular, lo cual le permitirá ejercer las funciones de torsión y detorsión del ciclo cardíaco.
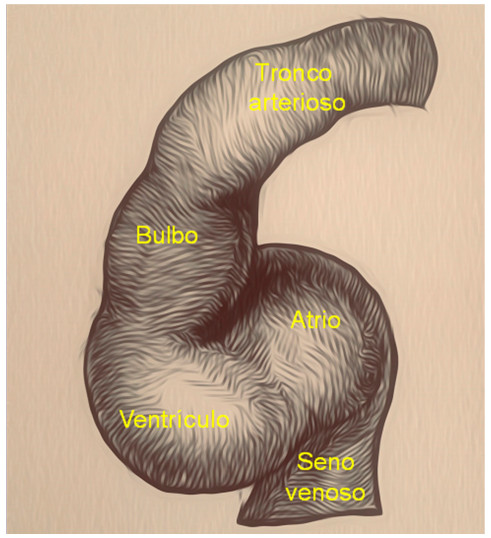
Fig. 4
Flexión del tubo cardíaco en el embrión humano
CONCLUSIONES
El concepto de trayecto circulatorio lineal imposibilitó la comprensión fidedigna de la unidad anatómica helicoidal. Si bien esta estructura secuencial conforma las cámaras cardíacas por donde la sangre circula, la acción dinámica la determina el miocardio helicoidal. 12 Se ha hecho históricamente, del trayecto sanguíneo por las cámaras auriculares y ventriculares, una interpretación que no guarda correlación entre estructura y función. La acción de torsión miocárdica permite generar una velocidad y consecuente presión intraventricular con menor gasto energético y mayor efectividad en el trabajo. Una propulsión lineal por un tubo circulatorio no tendría este efecto. En última instancia la dinámica miocárdica es el motor de la circulación, debiéndose además considerar las potenciales consecuencias de las fuerzas biomecánicas generadas por el movimiento helicoidal del flujo intracardiaco en la modulación de la morfogénesis cardíaca durante el periodo embrionario. 1314
Esta situación, avalada por la anatomía investigada y en estricta correlación con la función cardíaca, establece una organización helicoidal miocárdica muy distinta al concepto de unidad aurículo-ventricular que imposibilitó un correcto conocimiento de la fisiología cardíaca. La disposición horizontal de las aurículas (cámaras de dependencia del semicírculo venoso) se adosó al componente muscular ventricular (cámaras de dependencia del semicírculo arterial) en donde se generan la succión y el impulso eyectivo que producen el movimiento del flujo sanguíneo, de acuerdo con las fases del ciclo cardíaco.
BIBLIOGRAFÍA
Trainini JC, Elencwajg B, López-Cabanillas N, Herreros J, Lago N, Lowenstein J, y cols. Activación electrofisiológica y tiempos de propagación en la banda muscular ventricular. Primer estudio mundial en seres humanos. Rev Argent Cardiol 2016;84:475-8.
Mora Llabata V, Roldán Torresa I, Saurí Ortiza A, Fernández Galera R, Monteagudo Viana M, Romero Dorta E, y cols. Correspondence of myocardial strain with Torrent-Guasp’ s theory. Contributions of new echocardiographic parameters. Rev Argent Cardiol 2016;84:541-9.
Mora V, Roldán I, Romero E, Saurí A, Romero D, Perez-Gozabo J, Ugalde N, et al. Myocardial contraction during the diastolic isovolumetric period: analysis of longitudinal strain by means of speckle tracking echocardiography. J Cardiovasc Dev Dis 2018;5:41. https://doi.org/10.3390/jcdd5030041
Trainini J, Beraudo M, Wernicke M, Carreras Costa F, Trainini A, Mora Llabata V, et al. Evidence that the myocardium is a continuous helical muscle with one insertion. REC: CardioClinics 2022;57:194-202 https://doi.org/10.1016/j.rccl.2022.01.006
Torrent Guasp F, Buckberg G, Carmine C, Cox J, Coghlan H, Gharib M. The structure and function of the helical heart and its buttress wrapping. I. The normal macroscopic structure of the heart. Semin Thorac Cardiovasc Surg 2001;13:301-19. https://doi.org/10.1053/stcs.2001.29953
Kocica MJ, Corno AF, Carreras-Costa F, Ballester-Rodes M, Moghbel MC, Cueva CN, et al. The helical ventricular myocardial band: global, three-dimensional, functional architecture of the ventricular myocardium. Eur J Cardiothorac Surg 2006; 29:Suppl-I:S21-40. https://doi.org/10.1016/j.ejcts.2006.03.011
Trainini JC, Lowenstein J, Beraudo M, Wernicke M, Trainini A, Llabata MV, Carreras CF. Myocardial torsion and cardiac fulcrum (Torsion myocardique et pivot cardiaque). Morphologie. 2021;105:15-23. https://doi.org/10.1016/j.morpho.2020.06.010.
Torrent Guasp F. Estructura y función del corazón. Rev Esp Cardiol 1998;51:91-102. https://doi.org/10.1016/S0300-8932(98)74718-9
Trainini JC, Beraudo M, Wernicke M, Trainini A. Haber Lowenstein D, Bastarrica M, Martino DC, Lowenstein J. The myocardial support.. Rev Argent Cardiol 2021;89:217-23. https://doi.org/10.7775/ rac.v89.i3.20407
Torrent Guasp F. La estructuración macroscópica del miocardio ventricular. Rev Esp Cardiol 1980;33:265-87.
Trainini JC, Aventín GE, Auricchio R. Evolución y ventrículo derecho. Rev Argent Card 1991;59:86-9.
Nasiraei-Moghaddam A, Gharib M. Evidence for the existence of a functional helical myocardial band. Am J Physiol Heart Circ Physiol 2009;296:H127-31. https://doi.org/10.1152/ajpheart.00581.2008
Zhaoqiang W, Yichen D, Sandro S, Mehrdad R, Peng F, Tzung K.H. A Hybrid of Light-field and Light-sheet Imaging to Decouple Myocardial Biomechanics from Intracardiac Flow Dynamics. bioRxiv 2020;09.08.288480. https://doi.org/10.1101/2020.09.08.288480
Lorén C, Dahl C, Do L, Almaas V, Geiran O, Mörner, et al. Low molecular mass myocardial hyaluronan in human hypertrophic cardiomyopathy. Cells 2019;8:97. https://doi.org/10.3390/cells8020097
Notas de autor
Dirección para separatas: Jorge Carlos Trainini - E-mail: jctrainini@hotmail.com
Declaración de intereses
(Véanse formularios de conflicto de intereses de los autores en la web/Material suplementario).
