ARTÍCULO ORIGINAL
Modificaciones en la función ventricular izquierda y el electrocardiograma en ratones debidas a isquemia y reperfusión cerebral
Cerebral Ischemia and Reperfusion-Induced Changes in Left Ventricular Function and Electrocardiogram in Mice
Modificaciones en la función ventricular izquierda y el electrocardiograma en ratones debidas a isquemia y reperfusión cerebral
Revista argentina de cardiología, vol. 92, núm. 3, pp. 209-215, 2024
Sociedad Argentina de Cardiología
Recepción: 09 Febrero 2024
Aprobación: 15 Abril 2024
RESUMEN
Introducción: El accidente cerebrovascular (ACV) puede generar perturbaciones funcionales y eléctricas del corazón. Las características y mecanismos subyacentes no están completamente elucidados.
Objetivo: Evaluar si la isquemia (I) y reperfusión (R) cerebral agudas ocasionan disfunción cardíaca y alteraciones electrocardiográficas en un modelo experimental en ratones.
Material y Métodos: Ratones macho sometidos a isquemia y reperfusión cerebral (I/R) fueron evaluados mediante electrocardiografía (ECG) y ecocardiografía. Se analizó la frecuencia cardíaca, el intervalo QT corregido (QTc) y el intervalo entre el pico de la onda T - fin de la onda T (Tp-Te), la fracción de eyección ventricular izquierda (FEVI), la fracción de acortamiento (FA) y el tiempo de relajación isovolumétrica (TRIV). Se cuantificó el tamaño del infarto cerebral (TI), y el déficit neurológico se evaluó con la escala de Longa (EL).
Resultados: Encontramos una disminución estadísticamente significativa de la FEVI a las 24 horas de R (I/R: 66,5 ± 1,5% vs. sham: 74,3 ± 0,9%; p=0,002) y la FA (I/R: 42,9 ± 1,7% vs. sham: 52,3 ± 1,7%; p=0,004). Se observó una prolongación del QTc durante la I/R (basal: 125,1 ± 4,3 ms; 60 min I: 143,8 ± 5,2 ms; 24 horas R: 170,3 ± 5,8 ms; p=0,002), sin una prolongación del Tp-Te en la I (basal: 25,9 ± 1,3 ms vs. 60 min I: 23,8 ± 1,4 ms; p=0,999) pero sí en la R (24 horas R: 32,0 ± 2,3 ms; p=0,049. El tamaño del infarto cerebral fue de 34,9 ± 2,5% y la supervivencia del grupo I/R fue del 43,3%.
Conclusión: La isquemia cerebral aguda induce una disfunción ventricular izquierda leve y trastornos en la repolarización ventricular que se intensifican en las primeras 24 horas de reperfusión.
Palabras clave: Isquemia cerebral+ disfunción ventricular+ electrocardiograma+ arritmias.
ABSTRACT
Background: Stroke may produce functional and electrical heart disturbances. The underlying characteristics and mechanisms have not been fully elucidated.
Objectives: To evaluate whether acute cerebral ischemia (I) and reperfusion (R) may cause cardiac dysfunction and electrocardiographic alterations in an experimental mice model.
Methods: Male mice that underwent cerebral ischemia and reperfusion (I/R) were evaluated by electrocardiography (ECG) and echocardiography. Heart rate, corrected QT (QTc) interval, T-wave peak to T-wave end (Tp-Te) interval, left ventricular ejection fraction (LVEF), shortening fraction (SF) and isovolumetric relaxation time (IVRT) were analyzed. Cerebral infarct size was calculated, and neurological deficit was assessed with the Longa scale.
Results: Twenty-four hours after R, a statistically significant decrease in LVEF (I/R: 66.5±1.5% vs. sham: 74.3±0.9%; p=0.002) and in SF (I/R: 42.9±1.7% vs sham: 52.3±1.7%; p=0.004) was observed. QTc interval prolongation was observed during I/R (baseline: 125.1±4.3 ms; 60 min after I: 143.8±5.2 ms; 24 h after R: 170.3±5.8 ms; p=0.002). Tp-Te interval was not prolonged during I (baseline: 25.9±1.3 ms vs. 60 min after I: 23.8±1.4 ms; p=0.999) but it was prolonged during R (24 h after R: 32.0±2.3 ms; p=0.049). Cerebral infarct size was 34.9±2.5% and survival in the I/R group was 43.3%.
Conclusion: Acute cerebral ischemia induces mild left ventricular dysfunction and disturbances in ventricular repolarization which intensify within the first 24 hours after reperfusion.
Key words: Cerebral ischemia, Ventricular dysfunction, Electrocardiogram, arrhythmias.
INTRODUCCIÓN
La enfermedad cerebrovascular se encuentra entre las cuatro principales causas de mortalidad a nivel mundial, y afecta tanto a países de ingresos altos como bajos. (1) Datos recientes indican que en Argentina ocupa el segundo lugar como causa de muerte y el primer puesto en discapacidad. Entre los factores que agravan el pronóstico de estos pacientes se encuentran diversas complicaciones cardíacas agrupadas bajo el término de síndrome neurocardiogénico. Más de 1,5 millones de personas fallecen anualmente debido a las consecuencias de este síndrome, que incluyen síndromes coronarios, arritmias, síndrome de Takotsubo e insuficiencia cardíaca. (2,3)
Diversos estudios, tanto básicos como clínicos, han demostrado algunos mecanismos fisiopatológicos presentes en el deterioro del eje cerebro-corazón. Uno de los más relevantes es el desequilibrio en el sistema nervioso autónomo a favor de una exagerada descarga simpática y un deterioro parasimpático. (4,5) Aunque no es excluyente, investigaciones en humanos y diversas especies animales asocian el compromiso isquémico de la ínsula con la disautonomía. (4,6) Coincidentemente, se desencadena un estado proinflamatorio tanto a nivel local como sistémico, con aumento de citoquinas y migración de leucocitos que, ante la persistencia del estímulo, puede inducir cambios fibróticos en el miocardio. (7) Más recientemente se ha demostrado el papel de la liberación de microvesículas gliales con capacidad de transportar ARNm que llevan mensajes transcripcionales a distancia, e inducen lesiones miocárdicas. (8)
Aunque la disfunción miocárdica y los cambios eléctricos, como la fibrilación auricular, alteraciones en la conducción auriculoventricular y prolongaciones en el intervalo QT, han sido bien documentados, (4,9) su relación y evolución temporal en las etapas agudas no han sido suficientemente estudiadas. Por lo tanto, el objetivo de este trabajo fue investigar el compromiso funcional y eléctrico cardíaco durante la isquemia (I) y reperfusión (R) del hemisferio cerebral derecho en un modelo de ratones macho.
MATERIAL Y MÉTODOS
Modelo de isquemia cerebral.
Los experimentos fueron llevados a cabo siguiendo las directrices de la "Guía para el cuidado y uso de animales de laboratorio" de la Academia Nacional de Ciencias de los Estados Unidos de Norteamérica, actualizada por la American Physiological Society (10), y en conformidad con las normativas del Comité Institucional para el Cuidado y Uso de Animales de Laboratorio (CICUAL) de la Facultad de Medicina de la Universidad de Buenos Aires (Resolución CD 4081/04). El presente proyecto cuenta con la aprobación por el CICUAL (RESCD-2023-913-E-UBA-DCT#FMED).
Se utilizaron 18 ratones macho de la cepa FVB, con edades comprendidas entre 8 y 12 semanas, a los cuales se indujo I y R cerebral mediante la técnica descrita por Koizumi. (11) Para ello, se anestesiaron con una solución de ketamina-xilazina (100 mg / 10 mg) a una dosis de 4,4 µL/gr por vía intraperitoneal (IP). Después de la disección cervical, se introdujo un filamento intraluminal en la arteria carótida común, avanzando por la carótida interna, con el objetivo de obstruir el flujo de la arteria cerebral media durante 60 minutos. Para llevar a cabo la reperfusión, se retiró el filamento. Los resultados de este grupo de ratones con I/R se compararon con un grupo de ratones SHAM, o cirugía sin isquemia cerebral. Para ello, se utilizaron 5 ratones, a los que se les realizó la misma intervención quirúrgica que a los ratones del grupo I/R, con la excepción que no se ingresó el filamento intraluminal y, por ende, no se les realizó la oclusión de la arteria cerebral. La temperatura corporal se mantuvo constante a 36,5 ± 0,5ºC durante todo el procedimiento mediante una termocupla insertada por vía rectal y el uso de una lámpara de calor.
Tras la reperfusión, los animales fueron recuperados de la anestesia en una cámara con control de temperatura y, finalmente en el bioterio, fueron monitoreados durante 24 horas. Se administraron analgésicos (tramadol, 5µL/g por vía subcutánea) y antibióticos (cefazolina, 5µL/g por vía intramuscular) como parte del cuidado postoperatorio.
Evaluación neurológica y registros de mortalidad.
A las 4 y 24 horas post reperfusión, se realizaron evaluaciones de los déficits neurológicos utilizando la escala de Longa. (12) En esta escala, a la ausencia de déficit neurológico se asignan 0 puntos; a la incapacidad de flexionar los miembros contralaterales 1 punto; a los movimientos circulares hacia el lado de la lesión, 2 puntos; a los movimientos de tipo barreling o sobre el eje longitudinal se asignan 3 puntos, y al estado de coma o la falta de respuesta a estímulos externos, 4 puntos.
Se llevaron a cabo registros de sobrevida y se representaron gráficamente mediante curvas de Kaplan-Meier para analizar la evolución temporal de los ratones en función de los déficits neurológicos evaluados.
Registro electrocardiográfico.
Para la obtención de los registros electrocardiográficos, se emplearon electrodos subcutáneos (ADinstruments®) junto con el software LabChart 8®. Se realizaron registros a lo largo de los 60 minutos de I, los primeros 10 minutos de R y, finalmente, al término de este periodo. Se llevaron a cabo mediciones de la frecuencia cardíaca (FC), el intervalo QT, el intervalo QT corregido por la FC (mediante la fórmula de Bazett) y el intervalo entre el pico y el final de la onda T (Tp-Te). Para el análisis estadístico, se utilizaron los resultados basales (previo al inicio de la isquemia), a los 60 minutos de I y 24 horas de R.
Ecocardiografía.
Los estudios ecocardiográficos se llevaron a cabo en ratones bajo anestesia con 290mg/kg de una solución al 2,5% de 2,2,2 tribromoetanol (AVERTIN, Sigma Aldrich®), vía IP. (13) Se empleó un ecógrafo Acuson® Sequoia C512, equipado con un transductor de ultrasonido lineal de 14 MHz. Se realizaron registros a las 24 horas de reperfusión, durante los cuales se calcularon la fracción de eyección ventricular izquierda (FEVI), la fracción de acortamiento (FA) y el tiempo de relajación isovolumétrica (TRIV).
Evaluación del infarto cerebral.
Para visualizar el área de infarto cerebral a las 24 horas de reperfusión, los ratones fueron sacrificados mediante una sobredosis de ketamina y xilazina, (14) se extrajo el cerebro y se congeló para la obtención de secciones coronales de 2 mm de espesor. Estas secciones fueron incubadas en una solución de 2,3,5-trifeniltetrazolio (TTC) al 1% durante 20 minutos a 37ºC. El tejido cerebral no infartado se coloreó de rojo, mientras que el área infartada se presentó en blanco. Para documentar el área de infarto cerebral, se tomaron imágenes utilizando un escáner HP® y posteriormente se cuantificó el área utilizando el software ImageJ®. Utilizando la fórmula de Swanson [(hemisferio contralateral - hemisferio ipsilateral / hemisferio contralateral) x 100], se obtuvo el valor del área de infarto, corregido por edema. (15)
Análisis estadístico
Se llevaron a cabo representaciones gráficas de todos los valores mediante el software GraphPad Prism 9®. Los resultados se expresaron como la media ± error estándar. Se aplicaron pruebas estadísticas, incluyendo el análisis de varianza (ANOVA) unidireccional, seguido de la prueba t de Student para la comparación entre dos grupos. Además, se empleó el Log-rank test para analizar las curvas de Kaplan-Meier. Se consideró una diferencia significativa cuando con valor de p a 2 colas <0,05.
RESULTADOS
Tamaño del infarto cerebral, compromiso neurológico y sobrevida.
El tamaño del infarto cerebral, tras 60 minutos de I y 24 horas de R, fue de 34,9 ± 2,5% (Figura 1A y 1B). El área de infarto afecta los territorios irrigados por la arteria cerebral media, incluyendo la corteza cerebral y sustancia blanca de los lóbulos frontal, parietal y temporal, así como los núcleos caudado y putamen (Figura 1A).
El 67,9% de los ratones alcanzó un puntaje de 2 en la escala de Longa, y el 28,6% obtuvo un puntaje de 3. Solo el 3,6% obtuvo un puntaje de 0, mientras que no tuvimos casos de puntaje 1 ni 4. A las 24 horas, la sobrevida de los ratones con un puntaje 0 fue del 100%, con un puntaje de 2 fue del 77,8%, mientras que solo el 37,5% con un puntaje de 3 sobrevivió.
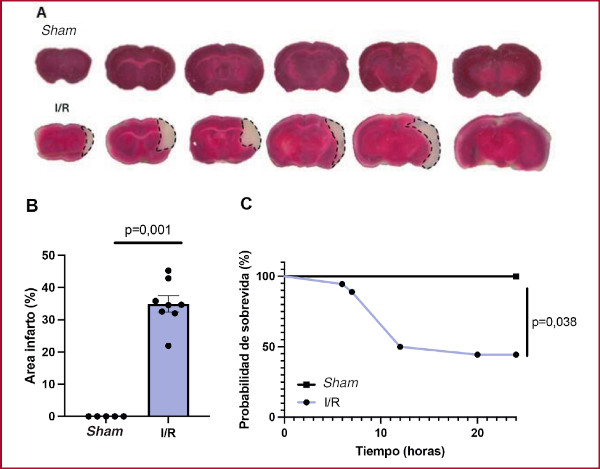
Fig. 1
A. Se presentan secciones coronales del cerebro teñidas con TTC correspondientes al grupo sham y al grupo con isquemia y reperfusión (I/R). Se evidencia el área de infarto (indicada por una línea punteada) en el territorio de la arteria cerebral media, afectando tanto la corteza como el caudo-putamen. B. Cuantificación del área de infarto. Sham n=5; I/R n=8. C. Representación de la curva de Kaplan-Meier para la sobrevida. Se observa que la tasa de supervivencia a las 24 horas fue en promedio del 43% para el conjunto de los ratones I/R. I/R: isquemia/reperfusión.
Función ventricular.
A las 24 horas de la reperfusión, se evidenció una disminución estadísticamente significativa en la FEVI en los ratones sometidos a I/R en comparación con el grupo sham (I/R: 66,5 ± 1,5% vs. sham: 74,3 ± 0,9%; p=0,002), así como en la fracción de acortamiento (FA) (I/R: 42,9 ± 1,7% vs. sham: 52,3 ± 1,7%; p=0,004). (Figura 2) Contrariamente, no se registraron cambios estadísticamente significativos en el TRIV entre ambos grupos (I/R: 20,1 ± 0,7 ms vs. sham: 19,4 ± 0,4 ms; p=0,450). (Figura 2)
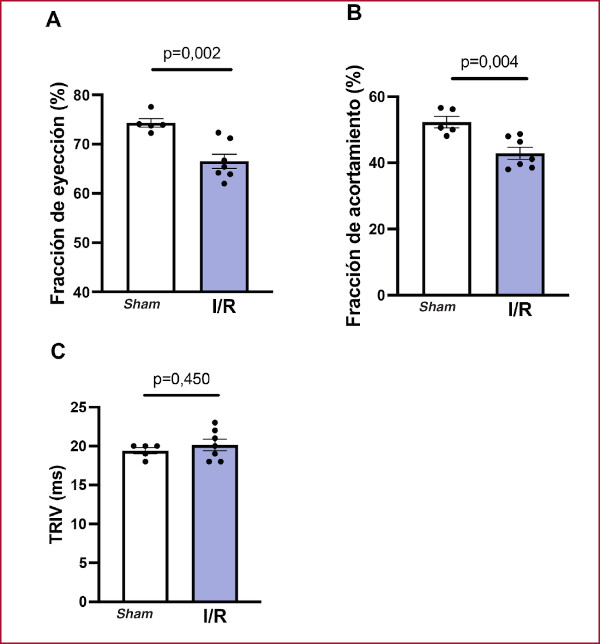
Fig. 2
Variables ecocardiográficas calculadas a las 24 horas de reperfusión cerebral. Los animales sometidos a isquemia/reperfusión (I/R) experimentaron una disminución estadísticamente significativa en la fracción de eyección (A) y la fracción de acortamiento (B), sin alteraciones en el tiempo de relajación isovolumétrica (TRIV) (C). Sham n=5; I/R n=7.
Cambios electrocardiográficos.
Durante la isquemia cerebral, se observó un aumento progresivo de la FC (basal: 252 ± 10 lpm, 60 min I: 317 lpm ± 24 lpm; p=0,182) y una prolongación gradual del intervalo QTc (basal: 125,1 ± 4,3 ms, 60 min I: 143,8 ± 5,2 ms; p=0,008) (Figura 3). A las 24 horas de reperfusión, se evidenció una prolongación aún más significativa del intervalo QTc (170,3 ± 5,8 ms; p=0,002) (Figura 3B), así como un incremento notable en la FC (384 ± 30 ms; p=0,034 vs. basal).
Por otro lado, el intervalo Tp-Te no se prolongó durante la isquemia (basal: 25,9 ± 1,3 ms, 60 min I: 23,8 ± 1,4 ms; p=0,999), pero sí lo hizo en la reperfusión (32,0 ± 2,3 ms; p=0,049 vs 60 min I; p=0,068 vs. basal). (Figura 3C).
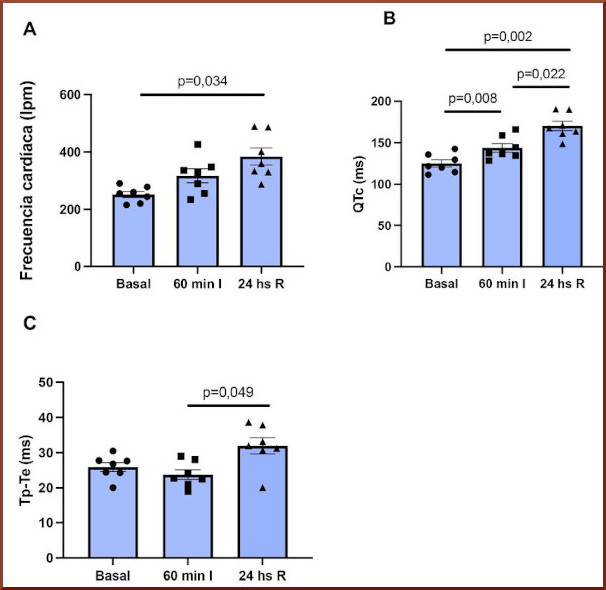
Fig.3. Cambios
electrocardiográficos evaluados en condiciones basales antes de la isquemia, al final de la misma y al final de la reperfusión. A. A las 24 horas de reperfusión, se evidencia un aumento en la frecuencia cardíaca en comparación con el estado basal y los 60 minutos de isquemia. B. Se observa una prolongación del intervalo QTc (Bazzet) a los 60 minutos de isquemia y a las 24 horas de reperfusión cerebral. C. No se registran diferencias en el intervalo Tp-Te en la isquemia, pero sí al final de la reperfusión. Isq: isquemia; RP: reperfusión; Tp-Te: pico de la onda T - final de la onda T. n=7.
DISCUSIÓN
Nuestros hallazgos evidencian que, en este modelo experimental, se produce un deterioro de la función ventricular izquierda y cambios eléctricos cardíacos en etapas tempranas tras la reperfusión cerebral. Además, destacamos que los cambios electrocardiográficos observados durante la isquemia cerebral pueden intensificarse durante la reperfusión. Aunque no fue el objetivo de este trabajo realizar un análisis comparativo con el compromiso de otras regiones del sistema nervioso central, la afectación cardíaca se manifiesta como consecuencia de una lesión cerebral que compromete un extenso territorio irrigado por la arteria cerebral media, una de las más afectadas en el accidente cerebrovascular isquémico. (16) Las lesiones corticales frontales derechas se reflejan en el tipo de compromiso funcional motor de los ratones, y la extensión de la lesión provoca diferentes grados de disfuncionalidad que se correlacionan con la mortalidad.
También observamos un compromiso de la corteza insular, lo cual podría tener implicaciones fisiopatológicas en este estudio. Trabajos previos han demostrado que el daño insular produce lesiones cardíacas como consecuencia del desequilibrio autonómico. (17,18,19) Se ha documentado el papel fisiológico de esta área cortical en la regulación diferencial del sistema nervioso parasimpático, más asociado al hemisferio izquierdo, y la regulación simpática, asociada al hemisferio derecho. (20) La mayor asociación del lado de la lesión de la ínsula con el daño cardíaco no está del todo claro; mientras algunos estudios asocian un mayor compromiso con las lesiones derechas, (14) otros lo hacen con las contralaterales. (21) Aunque aún no hemos evaluado de manera directa ni indirecta la posible asociación entre el compromiso cardíaco y la descarga catecolaminérgica, es plausible que los incrementos observados en la FC en nuestros experimentos reflejen un aumento en la actividad simpática, posiblemente atribuible al daño en la ínsula derecha. Esta hipótesis encuentra respaldo en investigaciones previas llevadas a cabo en diversas especies, las cuales han evidenciado un aumento en la actividad simpática durante la isquemia de la ínsula derecha. (19,20,21,22,23) Además, estudios sobre hemorragias cerebrales han demostrado un incremento de noradrenalina, sin alteraciones en los niveles de adrenalina ni cortisol plasmático. Los autores atribuyen este fenómeno a una respuesta no mediada por las glándulas suprarrenales. (24) La posibilidad de una descarga directa de catecolaminas en las terminales simpáticas del corazón también fue sugerida en estudios realizados en ratas, donde se observó un mayor daño en la base de los atrios, área de mayor densidad de nervios cardiacos. (4)
Resulta interesante destacar que observamos una prolongación del QTc durante la isquemia cerebral, que se tornó aún mayor durante la reperfusión, pero no observamos una prolongación del intervalo Tp-Te en la isquemia, y recién se modificó en la reperfusión. Este hallazgo indica el inicio temprano de cambios eléctricos sugestivos de trastornos en la repolarización ventricular, que se profundizan dentro de las primeras 24 horas de la reperfusión. La prolongación del QT ha sido bien documentada en otras patologías neurológicas, como la hemorragia subaracnoidea (25) o la epilepsia, (26), y en ambos casos se ha asociado con la aparición de arritmias ventriculares graves y muerte súbita de los pacientes. (27) También se han observado estos trastornos eléctricos en modelos experimentales, posterior a la estimulación eléctrica selectiva de la corteza insular, pero no de zonas aledañas. (19) Aunque no hemos evaluado específicamente la presencia de arritmias, es posible que estas puedan ser parcialmente responsables de la mortalidad observada en los ratones de nuestro estudio. Se sabe que la prolongación de ambos intervalos es un índice de mayor arritmogenicidad, (26) que la prolongación aislada del intervalo QTc. Es posible que estas alteraciones eléctricas estén asociadas a una activación simpática intensa. Esto nos motiva a continuar estudiando los trastornos en la repolarización en otros grupos experimentales.
Otro posible mecanismo asociado al compromiso cardíaco en la isquemia cerebral es la respuesta inflamatoria local y sistémica. La inflamación desempeña un papel fundamental en la patogénesis y progresión de diversas patologías cardiovasculares. (28,29) El aumento de citoquinas proinflamatorias, como la interleuquina 6 (IL-6), interleuquina 1 (IL-1) y el factor de necrosis tumoral alfa (TNF-α), se vincula tanto al daño funcional miocárdico como a alteraciones en los potenciales eléctricos, predisponiendo a la aparición de arritmias. (28) El incremento en la expresión de estas citoquinas puede llevar al reclutamiento de macrófagos y fibroblastos, generando un entorno local inflamatorio con daño funcional agudo y compromiso fibrótico a largo plazo. (30) Diversos estudios experimentales y clínicos han evidenciado el aumento de citoquinas a nivel local y sistémico, así como la movilización de leucocitos posterior a la isquemia cerebral. (7,14) Además, se reconoce la asociación dinámica y bilateral entre el aumento de la respuesta simpática y el incremento de la inflamación. (31) Por lo tanto, es probable que ambos posibles mecanismos estén implicados en la fisiopatología del daño cardiaco en nuestro modelo.
CONCLUSIÓN
En nuestro modelo experimental, la isquemia aguda con reperfusión cerebral en el hemisferio derecho, afectando la corteza insular, induce alteraciones funcionales y en la repolarización ventricular que podrían ser responsables del incremento en la tasa de mortalidad observada.
Bibliografía
World health statistics 2023: monitoring health for the SDGs, Sustainable Development Goals. Geneva: World Health Organization; 2023.
Sposato LA, Hilz MJ, Aspberg S, Murthy SB, Bahit MC, Hsieh CY, et al. World Stroke Organization Brain & Heart Task Force. Post-Stroke Cardiovascular Complications and Neurogenic Cardiac Injury: JACC State-of-the-Art Review. J Am Coll Cardiol. 2020;76:2768-85.https://doi.org/10.1016/j.jacc.2020.10.009.
Gelpi R, Buchholz B. Neurocardiología. Aspectos fisiopatológicos e implicanciones clínicas. 1a ed. Barcelona: Elsevier; 2018.
Balint B, Jaremek V, Thorburn V, Murthy SB, Bahit MC, Hsieh CY, et al. Left atrial microvascular endothelial dysfunction, myocardial inflammation and fibrosis after selective insular cortex ischemic stroke. Int J Cardiol. 2019;292:148-55. https://doi.org/10.1016/j.ijcard.2019.06.004.
Orgah JO, Yu J, Zhao T, Wang L, Yang M, Zhang Y, et al. Danhong Injection Reversed Cardiac Abnormality in Brain-Heart Syndrome via Local and Remote ß-Adrenergic Receptor Signaling. Front Pharmacol. 2018;9:692. https://doi.org/10.3389/fphar.2018.00692.
Jimenez-Ruiz A, Racosta JM, Kimpinski K, Hilz MJ, Sposato LA. Cardiovascular autonomic dysfunction after stroke. Neurol Sci. 2021;42:1751-8. https://doi.org/10.1007/s10072-021-05128-y.
Monsour M, Borlongan CV. The central role of peripheral inflammation in ischemic stroke. J Cereb Blood Flow Metab. 2023;43:622-41. https://doi.org/10.1177/0271678X221149509.
Siracusa C, Sabatino J, Leo I, Eyileten C, Postula M, De Rosa S. Circular RNAs in Ischemic Stroke: Biological Role and Experimental Models. Biomolecules. 2023;13:214. https://doi.org/10.3390/biom13020214.
Fridman S, Jimenez-Ruiz A, Vargas-Gonzalez JC, Sposato LA. Differences between Atrial Fibrillation Detected before and after Stroke and TIA: A Systematic Review and Meta-Analysis. Cerebrovasc Dis. 2022;51:152-7. https://doi.org/10.1159/000520101.
National Research Council. 2011. Guide for the Care and Use of Laboratory Animals: Eighth Edition. Washington, DC: The National Academies Press. https://doi.org/10.17226/12910.
Engel O, Kolodziej S, Dirnagl U, Prinz V. Modeling Stroke in Mice - Middle Cerebral Artery Occlusion with the Filament Model. J. Vis.Exp. 2011;6:2423. https://doi.org/10.3791/2423.
Longa EZ, Weinstein PR, Carlson S, Cummins R. Reversible middle cerebral artery occlusion without craniectomy in rats. Stroke. 1989;20:84-91. https://doi.org/10.1161/01.str.20.1.84.
Gelpi RJ, Gao S, Zhai P, Yan L, Hong C, Danridge LM, et al. Genetic inhibition of calcineurin induces diastolic dysfunction in mice with chronic pressure overload. Am J Physiol Heart Circ Physiol 2009;297:H1814-9. https://doi.org/10.1152/ajpheart.00449.2009.
Vornholz L, Nienhaus F, Gliem M, Alter C, Henning C, Lang A, et al. Acute Heart Failure After Reperfused Ischemic Stroke: Association With Systemic and Cardiac Inflammatory Responses. Front Physiol. 2021;12:78276. https://doi.org/10.3389/fphys.2021.782760.
Nouraee C, Fisher M, Di Napoli M, Salazar P, Farr TD, Jafarli A, Divani AA. A Brief Review of Edema-Adjusted Infarct Volume Measurement Techniques for Rodent Focal Cerebral Ischemia Models with Practical Recommendations. J Vasc Interv Neurol. 2019;10:38-45.
Dorrance AM, Fink G. Effects of Stroke on the Autonomic Nervous System. Compr Physiol. 2015;5:1241-63. https://doi.org/10.1002/cphy.c140016.
Winder K, Villegas Millar C, Siedler G, Knott M, Dörfler A, Engel A, et al. Acute right insular ischaemic lesions and poststroke left ventricular dysfunction. Stroke & Vascular Neurology. 2023;8:301-6. https://doi.org/10.1136/svn-2022-001724.
Micieli G, Cavallini A. The autonomic nervous system and ischemic stroke: a reciprocal interdependence. Clin Auton Res. 2008;18:308-17. https://doi.org/10.1007/s10286-008-0495-7.
Oppenheimer S. The insular cortex and the pathophysiology of stroke-induced cardiac changes. Can J Neurol Sci. 1992;19:208-11.
Krause T, Werner K, Fiebach JB, Villringer K, Piper SK, Haeusler KG, et al. Stroke in right dorsal anterior insular cortex Is related to myocardial injury. Ann Neurol. 2017;81:502-11. https://doi.org/10.1002/ana.24906.
Min J, Farooq MU, Greenberg E, Aloka F, Bhatt A, Kassab M, et al. Cardiac dysfunction after left permanent cerebral focal ischemia: the brain and heart connection. Stroke. 2009;40:2560-3. https://doi.org/10.1161/STROKEAHA.108.536086.
Bieber M, Werner RA, Tanai E, Hofmann U, Higuchi T, Schuh K, et al. Stroke-induced Chronic Systolic Dysfunction Driven by Sympathetic Overactivity. ANN NEUROL 2017;82:729-743. https://doi.org/10.1002/ana.25073.
Cechetto DF, Wilson JX, Smith KE, Wolski D, Silver MD, Hachinski VC. Autonomic and myocardial changes in middle cerebral artery occlusion: stroke models in the rat. Brain Res. 1989;502:296-305. https://doi.org/10.1016/0006-8993(89)90625-2.
Myers M, Norris JW, Hachinski VC. Plasma norepinephrine stroke. Stroke 1981; 12:200-4.
Andreoli A, di Pasquale G, Pinelli G, Grazi P, Tognetti F, Testa C. Subarachnoid hemorrhage: frequency and severity of cardiac arrhythmias. A survey of 70 cases studied in the acute phase. Stroke. 1987;18:558-64. https://doi.org/10.1161/01.str.18.3.558.
Fialho GL, Verrier RL, D'Avila A, Melo HM, Wolf P, Walz R, Lin K. Dual assessment of abnormal cardiac electrical dispersion and diastolic dysfunction for early detection of the epileptic heart condition. J Electrocardiol. 202;78:69-75. https://doi.org/10.1016/j.jelectrocard.2023.02.001.
Dinshaw L, Münch J, Dickow J, Lezius S, Willems S, Hoffmann BA, et al. The T-peak-to-T-end interval: a novel ECG marker for ventricular arrhythmia and appropriate ICD therapy in patients with hypertrophic cardiomyopathy. Clin Res Cardiol. 2018;107:130-7. https://doi.org/10.1007/s00392-017-1164-4.
Kouvas N, Kontogiannis C, Georgiopoulos G, Spartalis M, Tsilimigras DI, Spartalis E, Kapelouzou A, Kosmopoulos M, Chatzidou S. The complex crosstalk between inflammatory cytokines and ventricular arrhythmias. Cytokine. 2018;111:171-7. https://doi.org/10.1016/j.cyto.2018.08.007.
Henein MY, Vancheri S, Longo G, Vancheri F. The Role of Inflammation in Cardiovascular Disease. Int J Mol Sci. 2022;23:12906. https://doi.org/10.3390/ijms232112906.
Maruyama K, Imanaka-Yoshida K. The Pathogenesis of Cardiac Fibrosis: A Review of Recent Progress. Int J Mol Sci. 2022;23:2617. https://doi.org/10.3390/ijms23052617.
Elenkov IJ, Wilder RL, Chrousos GP, Vizi ES. The sympathetic nerve--an integrative interface between two supersystems: the brain and the immune system. Pharmacol Rev. 2000;52:595-638.
Notas
Notas de autor
Dirección para correspondencia: Bruno Buchholz Instituto de Fisiopatología Cardiovascular, Departamento de Patología, Facultad de Medicina, Universidad de Buenos Aires, Buenos Aires, Argentina. J. E. Uriburu 950 - 2do piso. C1114AAD, Buenos Aires, Argentina. E-mail: buchholz.bruno@gmail.com
Declaración de intereses
