ARTÍCULO DE REVISIÓN
Dolicoarteriopatías carotídeas: un enfoque global
Carotid Dolichoarteriopathies: A Comprehensive Overview
Dolicoarteriopatías carotídeas: un enfoque global
Revista argentina de cardiología, vol. 92, núm. 3, pp. 239-246, 2024
Sociedad Argentina de Cardiología
Recepción: 27 Marzo 2024
Aprobación: 25 Abril 2024
RESUMEN: Las dolicoarteriopatías carotídeas (DAC) son un grupo de anomalías morfológicas, con alteración de la geometría y torsión de los vasos carotídeos. Descriptas por primera vez en 1925, las DAC fueron clasificadas en tres tipos, según el grado de torsión: tortuosidad (ángulo mayor de 90°), enrollamiento o coiling (forma de S o looping), y acodamiento o kinking (ángulo menor de 90º). La fisiopatología de las DAC es controvertida, pero se han propuesto mecanismos congénitos, genéticos, enfermedades del tejido conectivo, adquiridos, relacionados con, pero no dependientes de, factores de riesgo cardiovascular, y alteraciones de la columna cervical. Las DAC han sido asociadas a diferentes eventos cardio y cerebrovasculares, secundarios a alteraciones hemodinámicas, tromboembolismo e insuficiencia e isquemia cerebrovascular. Pero la evidencia es limitada y, para algunos autores, son más una curiosidad que una condición clínica grave. Otros trabajos sustentan el valor clínico del diagnóstico y seguimiento de las DAC, y su reconocimiento no solo por internistas, cardiólogos y neurólogos, sino también por cirujanos y otorrinolaringólogos. Varios autores propusieron diversas estrategias terapéuticas, incluyendo procedimientos quirúrgicos para corregirlas. Sin embargo, las indicaciones y métodos de tratamiento son controvertidos, y son necesarios más estudios aleatorizados, multicéntricos y prospectivos para determinar cómo proceder. Hasta entonces, técnicas de imagen son la base para el diagnóstico etiológico de eventos adversos cerebrovasculares cuando se descartan todas las otras causas, y el control clínico cercano y seguimiento de los pacientes continúan siendo estrategias clave para la prevención de eventos secundarios.
Palabras clave: Dolicoarteriopatías, Tortuosidad, Arterias carótidas, Anomalías de los vasos, Enfermedad cerebrovascular, Factores de riesgo cardiovascular.
ABSTRACT: Carotid dolichoarteriopathies (CDA) represent a group of morphological abnormalities, with changes in the geometry and tortuosity of the carotid arteries. They were described in 1925 for the first time and were classified in three types according to the angle of torsion, in tortuosity (angle > 90°), coiling (S-shaped curve or loop) and kinking (angle < 90°). The pathophysiology of CDA is controversial and includes congenital mechanisms, genetic factors, connective tissue diseases, acquired mechanisms which can be associated with but not dependent on cardiovascular risk factors, and anomalies of the cervical spine. CDA have been associated with different cardiovascular and cerebrovascular events secondary to hemodynamic abnormalities, thromboembolism and cerebrovascular insufficiency and ischemia. However, the evidence is limited and for some authors they are more of a curiosity than a real predictor of ischemic events. Other studies support the clinical value of the diagnosis and follow-up of CDA and their understanding not only by internists, cardiologists and neurologists, but also by surgeons and otolaryngologists. Several authors proposed different therapeutic strategies to correct CDA, including surgical procedures. However, the indications and management approaches are controversial, and further randomized, multicenter, prospective studies are required to determine the most appropriate course of action. Until then, imaging techniques remain the basis for the etiologic diagnosis of cerebrovascular adverse events when all other causes have been excluded, and close clinical monitoring and follow-up of patients remain key strategies for the prevention of secondary events.
Key words: Dolichoarteriopathies, Tortuosity, Carotid Arteries, Vessel Abnormalities, Cerebrovascular Disease, Cardiovascular Risk Factors.
INTRODUCCIÓN
La aterosclerosis es la causa más frecuente de enfermedad de las arterias carótidas extracraneales y una de las principales causas de enfermedad cerebrovascular (ECV), y muerte. (1, 2) Constituye la etiología predominante de ECV en Occidente. (3) Empero, existen otras causas no ateroscleróticas, como fibrodisplasia, enfermedad de Takayasu y disección aórtica, entre otras, que se relacionan con ECV. (1, 4) Dentro de este grupo se incluyen las dolicoarteriopatías (del griego δόλιχος, dólichos, “anormalmente largo”), que han sido depositarias de la atención de los especialistas en los últimos tiempos. Las dolicoarteriopatías carotídeas (DAC), se han asociado a un amplio espectro de ECV, como el ictus y el accidente isquémico transitorio (AIT). (5) Sin embargo, su significado clínico real resulta poco claro. (1) En el presente trabajo, revisamos los principales aspectos de las DAC, centrándonos en su fisiopatología, diagnóstico, pronóstico y tratamiento.
MÉTODOS
Se efectuó una revisión no sistemática, seleccionando los trabajos más significativos vinculados con este tópico. Se utilizaron los buscadores PubMed, Scielo y Scholar Google, empleando las siguientes palabras: dolichoartheriopathies, carotid dolichoartheriopathies, arterial tortuosity, dolichoectasia, y sus equivalentes en español.
RESULTADOS
Definición, clasificación y epidemiología
Las DAC constituyen una anomalía anatómica consistente en un cambio de disposición geométrica que provoca enrollamiento, acodamiento y tortuosidad de los vasos carotídeos en su trayecto. (1, 5) Algunos autores las incluyen dentro del grupo de las dolicoectasias (elongación, tortuosidad y/o dilatación de los vasos). (6) Las DAC fueron descritas por primera vez por Kelly en 1925 (7), y clasificadas por Weibel y Fields (8) (Figura 1), en tres grupos:
-
Tipo I o Tortuosidad (Tortuosity): Cualquier elongación u ondulación en S o C del curso de la arteria carótida, con una angulación mayor de 90°.
-
Tipo II o Enrollamiento (Coiling): Alargamiento o redundancia de la arteria carótida interna, dando una curva en S exagerada, o en una configuración circular, adquiriendo morfología en asa (una angulación de 360° de la arteria sobre su eje transverso).
-
Tipo III o Acodamiento (Kinking): Angulación de uno o más segmentos de la arteria, con ángulo menor de 90°.

FIGURA 1.
Esquema de la clasificación de las dolicoarteriopatías carotídeas, uniendo las de Weibel-Fields y Metz. La ilustración de la clasificación de Weibel-Fields se modificó de la referencia #41. La ilustración de clasificación de Metz se modificó de la referencia #5.
Metz y cols. subclasificaron los acodamientos en función de la severidad de la angulación: Grupo I (ángulo agudo medido entre los dos segmentos que forman la torsión de una amplitud entre 90° y 60°, Figura 2, Panel A), Grupo II (entre 60° y 30°, Figura 2, Panel B), y Grupo III (menor de 30°, Figura 2, Panel C). (9)
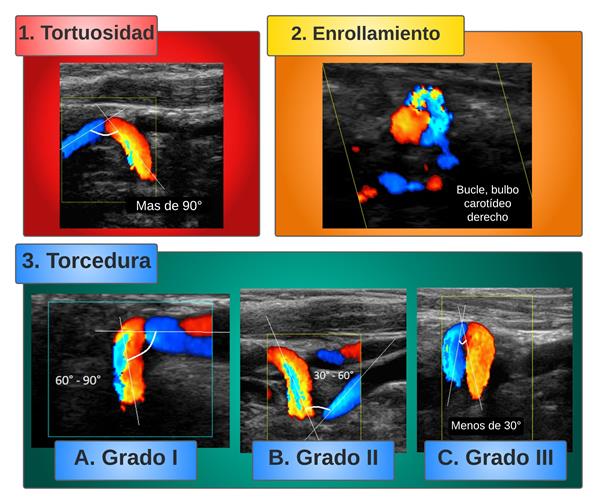
FIGURA 2.
Imágenes de diferentes tipos de dolicoarteriopatías carotídeas obtenidas con ecocardiografía Doppler color. El ángulo entre cada parte de la arteria se dibuja con líneas blancas y se describe en la imagen correspondiente.
Las DAC son una entidad frecuente, con una prevalencia del 10 - 45%. (10) Beigelman y cols. (1), y Ghilardi y cols., (11) diagnosticaron DAC en 13,3 - 31 % de los casos, mientras que en estudios de pacientes hospitalizados, la prevalencia osciló entre el 13,5 y el 58 %. (6) Las DAC son más prevalentes en mujeres y pacientes añosos, especialmente mayores de 60 años, y pueden ser tanto uni como bilaterales, afectando las arterias carótida común (ACC), interna (ACI) y externa (ACE), pero más frecuentemente la ACI, especialmente del lado izquierdo. (12, 13) Las tortuosidades y los acodamientos son más frecuentes que los enrollamientos. (1, 12)
Fisiopatología
Varios mecanismos han sido implicados en el desarrollo de DAC, aunque aún existe controversia. Una cuestión clave es si es un fenómeno congénito o adquirido, y si tiene alguna relación con la aterosclerosis u otros factores de riesgo cardiovascular. Algunos estudios arrojan luz al respecto.
A. Mecanismo embriológico
La vasculatura cerebral comienza a desarrollarse tempranamente en el embrión, durante la tercera semana de vida intrauterina, mediante la formación de los arcos aórticos (AA). (13,14) Hay seis pares de AA que conectan la aorta ventral (AV) con la aorta dorsal (AD). (14, 15) Cada AA surge del bulbo arterioso, y discurre dentro de su arco faríngeo correspondiente para terminar en la AD. (14) Los arcos primero y segundo se desintegran, y sus raíces nacientes de la AV y AD persisten como ACI y ACE incipientes. La ACI se integra con el tercer AA bilateralmente, mientras que la raíz aórtica ventral, entre el tercer y cuarto arco, persiste como ACC. (15) Existe una variabilidad considerable en el curso y la posición de las ACC y las bifurcaciones carotídeas. La elongación de las ACC y ACI conduce a tortuosidad y acodamientos. (16) La posición de la bifurcación carotídea refleja el grado de migración embriológica de la ACE, y es variable. (16) Huber y cols. situaron la bifurcación carotídea a nivel de C4 - C5 en el 48% de 658 casos, y de C3 - C4 en el 34%. (17) Hay casos descritos de bifurcación desde T3 hasta C2. (18) En niños, se observó de C2 a C3 en un 40%, y de C3 a C4 en un 40%. (19) Carney y cols. encontraron tortuosidades en 5 de 20 fetos entre los 5 meses y a término. (20) Harrison y cols. sugirieron que el desarrollo de las arterias carótidas y del sistema esquelético puede ser asincrónico, generando alteraciones y tortuosidad en el trayecto de la arteria. (21) Beigelman y cols. estudiaron una población de 885 personas (4,5 horas postnatales - 90 años), y los dividieron en un grupo control con 245 personas (niños y adolescentes hasta 15 años), y otro de 640 individuos (16 - 90 años), en los que se había solicitado eco Doppler color de vasos de cuello por sospecha clínica de aterosclerosis. La incidencia de enrollamientos y acodamientos fue similar en ambos grupos. La presencia de placas ateromatosas en la tortuosidad solo se observó en 3 pacientes del segundo grupo. Los autores encontraron una falta de asociación con otros factores de riesgo cardiovascular, y de la localización de las placas carotídeas con las DAC. (1)
B. Trastornos genéticos y moleculares
Voevoda y cols. estudiaron 61 familias cuyos niños habían sido diagnosticados previamente con DAC de la ACI mediante ecografía Doppler dúplex color. El grupo estuvo compuesto por 100 individuos con esta alteración. El grupo control (n = 245) se formó a partir de un banco de ADN basado en un enfoque poblacional. Encontraron una asociación entre el polimorfismo A80807T del gen del factor transcripcional Sp4 con las DAC. (22) Zaidi y cols. reportaron el caso de una familia kurda consanguínea cuyo niño presentaba elongación y tortuosidad severa de la aorta, carótidas y otras arterias, incluyendo otras alteraciones (piel floja, hiperlaxitud articular, hernias y rasgos faciales que se asemejan al síndrome de Ehler-Danlos [SED[). Encontraron homocigosidad del locus 20q13 en el niño afectado. (23) Arslan y cols. observaron un nivel significativamente mayor de metaloproteinasa de matriz (MMP) tipo 2 en pacientes con DAC en comparación con el grupo control. La expresión de MMP-12 fue mayor en aquellos con placas ateromatosas que en aquellos sin aterosclerosis. (24)
C. Enfermedades del tejido conectivo (ETC)
Foiadelli y cols. reportaron el caso de 7 niños con SED de entre 3 a 13 años, con DAC y manifestaciones clínicas variables. (25) Welby y cols. estudiaron 286 pacientes divididos en grupos control y con ETC. La presencia de DAC fue del 44% en el segundo grupo, y del 16% en los controles (p < 0,001). Los enrollamientos fueron más prevalentes. Se vio DAC en el 88 % de los casos con síndrome de Marfan, 63% para el síndrome de Loeys-Dietz, 42% para la neurofibromatosis tipo 1, y 19% para el SED, tanto del tipo vascular como no vascular. (26)
D. Asociación con otras enfermedades congénitas
Según Paltseva y cols., las DAC tienen niveles de elastina más altos, pero con fragmentación de fibras, mayor expresión de MMP-9, y una menor expresión de actina de músculo liso. (27) Ballotta y cols. analizaron 78 arterias carótidas con DAC y encontraron patrones típicos y atípicos de displasia fibromuscular (DFM). (28) Sethi y cols. encontraron una prevalencia significativamente mayor de DAC con curva en forma de S en pacientes con DFM. (29)
Ballota y cols. estudiaron a 43 pacientes con aneurisma de aorta abdominal (AAA) asintomáticos y DAC, y encontraron cambios displásicos degenerativos en la túnica media en todas las muestras carotídeas. En algunos casos, se superpusieron con lesiones ateroscleróticas de la íntima. Las características histológicas del AAA clásico (adelgazamiento de la túnica media subyacente a la placa aterosclerótica), se observaron en casi todas las muestras de la pared aórtica, sugiriendo una base común de alteraciones del tejido conectivo subyacente a ambas patologías. (30)
E. Mecanismos adquiridos
Harrison y cols. sostienen que las DAC podrían deberse a cifosis o lordosis que desviarían el eje carotídeo. (21) Para Etheredge y cols., la inflamación de los tejidos pericarotídeos haría que estas se retraigan y desvíen su camino, desarrollando tortuosidades. (31)
Ghilardi y cols., y Del Corso y cols., describen una gran prevalencia de hipertensión arterial (HTA) y aterosclerosis en pacientes con DAC. (11, 32) Sin embargo, ambos estudios carecen de un grupo de participantes normales, y abordan únicamente una población seleccionada por patología vascular, en los que se espera un predominio de dichos factores de riesgo cardiovascular. Para Khasiyev y cols., debido a que las DAC también muestran dilatación, la remodelación externa compensatoria en respuesta a la aterosclerosis puede desempeñar un papel en este fenotipo. (6) La dilatación de la carótida también puede reflejar una debilidad del tejido conectivo de índole no aterosclerótica. Pancera y cols. encontraron una asociación estadísticamente significativa entre acodamiento e HTA, y también entre la presencia de HTA y mayor grado de flexión del acodamiento. (33) Oliviero y cols. estudiaron la prevalencia de DAC en pacientes con HTA y diabetes. La prevalencia de DAC fue mayor en el grupo HTA que en el de diabetes y control, y también se asoció con el tiempo que los pacientes fueron hipertensos. (34) Las fuerzas excéntricas relacionadas con la HTA, y posiblemente el envejecimiento de la arteria, acompañado del desarrollo de rigidez, puede desempeñar un papel en la dilatación de la ACI y, por lo tanto, en el desarrollo de las DAC. (6)
Wang y cols. estudiaron la relación entre el índice de masa corporal (IMC) y las DAC. Analizaron un total de 513 pacientes, todos ellos sin ETC, empleando el índice de tortuosidad (IT), expresado en porcentaje, calculado como una relación entre la longitud real de la ACI (LR) y la longitud medida desde la bifurcación carotídea hasta la base del cráneo, llamada longitud del cordón (LC):
IT = [(LR/LC) - 1[*100
El sexo masculino y el IMC se correlacionaron significativamente con el IT. Por cada punto del IMC aumentó 1,59 veces el riesgo de desarrollar DAC. (35) Dilba y cols. utilizaron el mismo índice en una población de la cohorte Plaque At RISK. Concluyeron que la edad, la obesidad y la hipercolesterolemia se asocian con mayor IT. Además, encontraron mayor prevalencia y severidad de DAC en la ACI izquierda. La elevación del IMC y las DAC puede deberse a la presión abdominal alta. El aumento de la presión abdominal puede empujar hacia arriba el diafragma, y con él, todo el mediastino. Esto elevaría las arterias carótidas que, al estar rodeadas de tejido conectivo laxo, pueden deslizarse y desarrollar tortuosidad. Debido a que la arteria braquiocefálica “absorbe” parte de la fuerza de elevación, la ACI derecha desarrolla una tortuosidad menos grave que la izquierda. Así, la exposición repetida y prolongada a periodos de alto y bajo flujo deriva en estrés que afecta el remodelado arterial, provocando tortuosidad. (36)
Derubertis y cols. observaron mayor prevalencia de DAC en pacientes previamente sometidos a radioterapia. La radiación puede devenir en retracción y alteración del tejido conectivo, produciendo tortuosidad de la arteria. (37) Saba y cols. estudiaron una población de 124 pacientes con disección de ACI diagnosticada mediante tomografía computarizada (TC) o resonancia magnética (RM). Observaron una asociación estadísticamente significativa entre la disección y el acodamiento y enrollamiento . (38) Barbour y cols. encontraron una asociación significativa entre disección arterial espontánea y tortuosidad de la ACI, especialmente si la torsión es bilateral. (39) Algunos autores plantean que las alteraciones hemodinámicas pueden producir ruptura y daño endotelial. La inflamación desencadenada puede alterar la estructura del vaso, y los agentes inflamatorios derivar en disección arterial. (6)
Diagnóstico
Las DAC se pueden diagnosticar mediante un amplio espectro de técnicas de imagen. El estándar de oro parece ser la ultrasonografía. (1, 2, 6) El flujo sanguíneo turbulento dentro de los vasos tortuosos se puede estudiar con exploración Doppler. (40) Di Pino y cols. estudiaron la prevalencia de DAC en ACI empleando eco Doppler color en 2856 sujetos (0-96 años), y demostraron picos de prevalencia en los extremos etarios (<21 años y >60 años). Se detectaron DAC en el 9,9% de los participantes. Este estudio fue uno de los primeros en utilizar ultrasonografía en una gran cohorte. (41) Uchino y cols. comunicaron un caso de DAC diagnosticado por angiografía por tomografía computarizada (TC) y tomografía computarizada por emisión de fotón único (SPECT). Ambas permitieron estudiar con mayor definición la morfología de la tortuosidad de la ACI y las alteraciones secundarias de la perfusión. (42) En otros trabajos, la TC permitió evaluar anomalías finas, como microaneurismas, y las reconstrucciones 3D de la TC impresionan ser más eficaces a la hora de clasificar las variaciones morfológicas de la ACI y detectar estas anomalías. (43, 44, 45) Balevi y cols. encontraron una prevalencia de DAC del 40,3%. en la población general mediante angioresonancia (angio-RM) con contraste. (12) Tomiya y cols. realizaron angio-RM en 13 pacientes, obteniendo imágenes nítidas de DAC. (46) Yu y cols. opinan que la RM es una buena opción para el diagnóstico de las DAC. La angiografía por sustracción digital (ASD), estándar de oro para el diagnóstico de enfermedades de los vasos cervicales e intracraneales, podría proporcionar datos hemodinámicos de las DAC y estudiar su morfología, pero no puede determinar los cambios patológicos a nivel de la pared de la ACI. (40) Funcionaría como un complemento en el estudio de las DAC más que una técnica de imagen útil para el diagnóstico. Para llegar a un diagnóstico correcto, todas estas técnicas son válidas y no excluyentes, y deberían elegirse en orden de mayor complejidad e invasividad.
Implicancia clínica
La implicancia clínica de las DAC es controvertida. Hay evidencia limitada para apoyar la asociación entre DAC y ECV. (6) Yin y cols. observaron una mayor incidencia de lesiones de sustancia blanca en aquellos pacientes con DAC en comparación con controles. La gravedad de estas lesiones se relacionó directamente con el número de acodamientos. (47) Otros autores sostienen que la enfermedad isquémica es más frecuente en personas con DAC y otros factores de riesgo cardiovascular. Pancera y cols. encontraron una asociación significativa entre acodamientos y AIT. La HTA y las DAC podrían ser factores de riesgo aditivos en la fisiopatología de los AIT. (33) Oliviero y cols. demostraron que la presencia de acodamiento carotídeo en sujetos hipertensos no puede considerarse un factor de riesgo adicional para eventos isquémicos. (48) Pero, como afirman Pancera y cols., la adición de factores de riesgo a la presencia de DAC puede aumentar el riesgo de eventos vasculares. (33) Iwai-Takano y cols. observaron una asociación entre las DAC y el envejecimiento, la HTA y el género, pero no con dislipidemias, diabetes o tabaquismo. (49)
Quienes apoyan el peligro de las DAC sostienen que las curvas en la ACI, además de estrechar la arteria y generar daño endotelial, pueden producir turbulencias en el flujo sanguíneo que devendrían en un estado protrombótico. Para otros, como Balevi y cols., las DAC son más una curiosidad que un verdadero predictor de eventos isquémicos. (12) Valvano y cols. abogan por la ausencia de asociación entre DAC y ECV. (50) Las DAC pueden causar hipoperfusión cerebral, llevando a encefalopatía, vértigo, diplopía, AIT e infarto. (40) La prevalencia de síntomas cerebrovasculares en pacientes con DAC varía entre el 15 y el 23%. (51) El enrollamiento no se considera un factor de riesgo para eventos isquémicos debido a su débil asociación con los síntomas, a diferencia de los acodamientos, que impresionan ser más sintomáticos debido a la hipotensión transitoria durante el sueño o al movimiento repentino y extremo de la cabeza y el cuello. (40) Otras alteraciones observadas son la discapacidad visual como la amaurosis fugax, uveítis, retinitis y distrofia macular. (52) En casos graves, las DAC pueden producir efecto de masa, dando lugar a disfagia, disnea, estrechamiento de la vía aérea superior y apnea obstructiva, y, más raramente, acúfenos pulsátiles y espasmo mesolingual. (40, 53, 54)
Sobre la relación entre las DAC y la aterosclerosis, en el Northern Manhattan Study (NOMAS), Khasiyev y cols. estudiaron la relación entre DAC y biomarcadores de aterosclerosis en 558 participantes. Las DAC se correlacionaron con la presión arterial diastólica y el gran diámetro de la raíz aórtica, pero no con otras medidas de aterosclerosis. Determinar el riesgo de eventos vasculares asociados a este fenotipo no aterosclerótico puede ayudar a una mejor estratificación del riesgo para las personas con DAC. (55)
Beigelman y cols. estudiaron la génesis de las complicaciones neurológicas relacionadas con las DAC. Sesenta pacientes con DAC sin aterosclerosis fueron sometidos a pruebas de rotación cefálica y estudiados mediante Doppler color de las ACI y oftálmicas, y se evaluó en estas últimas su comportamiento hemodinámico. Los resultados sugirieron que las DAC no son causa de alteraciones o síntomas neurológicos, ya que no se registraron eventos durante el estudio, y se constató reducción significativa de las velocidades en la arteria oftálmica en solo 3 de 60 casos. (56)
Wang y cols. analizaron las variaciones de presión provocadas por las DAC en 12 pacientes mediante ASD. Midieron el ángulo de acodamiento mediante angiografía rotacional y calcularon la presión arterial en los sitios proximal, intra-acodamiento y distal de la ACI empleando un microcatéter. Estos resultados se compararon con dos simulaciones: una numérica, con un modelo geométrico de ACI tortuosa construido con un software; y otra de flujo in vitro, utilizando un tubo de silicona sometido a diferentes grados de torsión, a través del cual fluía agua impulsada por una bomba peristáltica. La simulación del software mostró una caída lineal de la presión del flujo con disminuciones en el ángulo de torsión. La mínima caída de presión fue en el ángulo de torsión de 180º, y la máxima en 30º. Pero ocurrió una inversión entre 30º y 20º: el aumento del grado de acodamiento condujo a una caída menor de la presión. Lo mismo ocurrió con la simulación in vitro: cuando el caudal era constante, la caída de presión disminuyó al aumentar el ángulo de torsión, pero se incrementó al aumentar el mismo de 20º a 30º. Sin embargo, estos hallazgos no se correspondieron con las observaciones clínicas: las pruebas realizadas en pacientes mostraron un aumento notable de la caída de presión cuando el ángulo de torsión era inferior a 30º, el acodamiento marcado indujo una disminución promedio del 15,5 % en la presión arterial. En la medición clínica no se observó el desarrollo de la inversión de caídas de presión con ángulos superiores a 20º - 30º. Esto se atribuyó a una excesiva elongación y estenosis de la ACI en casos de torsiones graves. Y aunque la caída de presión cambió gradualmente en las simulaciones, disminuyó rápidamente en las mediciones clínicas cuando el ángulo era menor de 45º, pero fue más gradual con ángulos más altos. Este comportamiento podría ser causado por las características del fluido (la sangre es un fluido no newtoniano), y las paredes elásticas de la ACI. Ambos factores crearían un “rango protector” que puede contribuir al mecanismo de autorregulación del flujo sanguíneo. (57) Dicho trabajo fue uno de los primeros estudios en evaluar estos aspectos de las DAC comparando observaciones clínicas y artificiales, con mediciones directas de las presiones de la ACI. Estos hallazgos evidencian que las alteraciones de la presión arterial y el flujo sanguíneo pueden ser las responsables de la interrupción de la perfusión cerebral, de isquemia consecuente y, por lo tanto, eventos cerebrovasculares.
Algunos autores observaron una relación entre DAC y aneurismas en el contexto de las ETC. (26) El valor predictivo positivo de la combinación de aneurisma de aorta y DAC asociada a ETC fue del 95,4%, con una especificidad del 98,6%. Un mayor IT de las arterias aorta y vertebral se comportó como predictor independiente de disección arterial en pacientes con síndrome de Marfan. Así, las DAC permiten sospechar la presencia de aneurismas de gran importancia clínica en pacientes con ETC. (6, 26, 40)
Las DAC se han relacionado con mayor morbimortalidad en los procedimientos quirúrgicos de cabeza y cuello. Ya en los trabajos de Weibel y Fields (8) y Metz (9) se conocía este riesgo. Nayak y cols. remarcan la importancia de estudiar la morfología de los vasos carotídeos antes de realizar procedimientos quirúrgicos en la zona faríngea, ya que pueden complicarse con lesión de los vasos, sangrado y, en casos graves, muerte por hemorragia masiva. (58) Por ello, resulta perentorio su estudio exhaustivo previo a la realización de cualquier procedimiento en la zona cervical.
Tratamiento
A pesar de la controversia sobre la implicancia clínica de las DAC, se han elaborado algunas indicaciones terapéuticas para actuar sobre ellas en función del grado de compromiso hemodinámico de la tortuosidad, entre otros parámetros. Gavrilenko y cols. (59) propusieron tratar las DAC en las siguientes condiciones:
- 1. Estenosis de la ACI del 60% o más, con placas ateroscleróticas y cualquier grado de insuficiencia cerebrovascular; o,
- 2. Estenosis de la ACI inferior al 60 % con placas ateroscleróticas, grado moderado a grave de insuficiencia cerebrovascular, en combinación con tortuosidad, flujo sanguíneo lineal de 100 cm/seg o más, y flujo sanguíneo turbulento.
Grego y cols. (60) propusieron casos específicos en los que se justifica el tratamiento, tales como:
-
AIT (síntomas hemisféricos);
-
Pacientes asintomáticos con ángulo de acodamiento menor de 30°, con oclusión carotídea contralateral;
-
Pacientes con síntomas no hemisféricos, tras descartar otras posibles causas neurológicas o no neurológicas mediante resultados positivos de los siguientes estudios: 1) ecografía Doppler de vasos de cuello con aumento de velocidades, 2) TC y angio-RM cerebral con lesiones isquémicas en hemisferio ipsilateral, y 3) inversión del flujo circulatorio en la arteria cerebral anterior y su reducción en la arteria cerebral media, en relación con maniobras de rotación y flexoextensión cefálica.
Otros autores propusieron iniciar tratamiento en casos de cociente ACI/carótida común mayor de 2, o velocidad del flujo sanguíneo mayor de 180 cm/seg (61,62). Pero la indicación real de tratamiento de las DAC sigue siendo controvertida. La mayoría concuerdan en intervenir los casos de DAC sintomáticas descartando cualquier otra causa.
Se han propuesto técnicas invasivas para corregir las DAC, con resultados exitosos (fijación de la ACI al músculo digástrico, anastomosis término-terminal, reimplantación término-lateral, endarterectomía carotídea con parche, bypass y angioplastia carotídea, y colocación de stent). (40) Sin embargo, a pesar del éxito de estas técnicas, el tratamiento adecuado sigue siendo controvertido. Son necesarios más estudios para determinar la efectividad real del abordaje quirúrgico de las DAC.
CONCLUSIÓN
Las DAC son una entidad común, con etiología multifactorial y evidencia limitada, pero no despreciable, de compromiso cerebrovascular. Son necesarios más estudios que establezcan la utilidad de las estrategias terapéuticas para mejorar su pronóstico. Un control estricto y un seguimiento más cercano de los pacientes, con una valoración global del riesgo tromboembólico, son medidas prudentes para prevenir futuros eventos.
BIBLIOGRAFÍA
Beigelman R, Izaguirre AM, Robles M, Grana DR, Ambrosio G, Milei J. Are kinking and coiling of carotid artery congenital or acquired? Angiology. 2010;61:107-12. doi: 10.1177/0003319709336417
Beigelman RL, Izaguirre AM, Azzato F, Milei J. Carotid Artery - Pathology, Plaque Structure - Relationship between Histological Assessment, Color Doppler Ultrasonography and Magnetic Resonance Imaging - Dolichoarteriopathies - Barorreceptors. In: Rezzani R, editor. Carotid Artery Disease - From Bench to Bedside and Beyond [Internet[. London: IntechOpen; 2014. doi: 10.5772/57157
The global burden of disease: 2004 update. World Health Organization (WHO) Press; 2008. http://www.nhlbi.nih.gov/health/health-topics/topics/catd/[Online[
Goldman L, Shafer A. Goldman-Cecil: internal medicine, 25° edition, Ed. Elsevier, 2016.
Dilba K, van Dam-Nolen DHK, Crombag GAJC, van der Kolk AG, Koudstaal PJ, Nederkoorn PJ, et al. Dolichoarteriopathies of the extracranial internal carotid artery: The Plaque At RISK study. Eur J Neurol 2021;28:3133-8. doi: 10.1111/ene.14982
Khasiyev F, Gutierrez J. Cervical Carotid Artery Dolichoectasia as a Marker of Increased Vascular Risk. J Neuroimaging. 2021;31:251-60. doi: 10.1111/jon.12815
Kelly AB. Tortuosity of the internal carotid in relation to the pharynx. J Laring 1925;40:15-20. doi: 10.1177%2F003591572401700607
Weibel J, Fields WS. Tortuosity, coiling and kinking of the internal carotid artery.Etiology and radiographic anatomy. Neurology.1965;15:7-18. doi: 10.1212/wnl.15.1.7
Metz H, Murray-Leslie RM, Bannister RG, Bull JW, Marshall J. Kinking of the internal carotid artery. Lancet. 1961;1:424-6. doi: 10.1016/s0140-6736(61)90004-6
Verlato F, Camporese G, Rocco S, Salmistraro G, Signorini GP. Carotid kinks relationship to atherosclerosis and cerebral ischemia. J Vasc Surg. 2000;32:293-8. doi: 10.1067/mva.2000.106953
Ghilardi G, De Monti M, Longhi F, Trimarchi S, Bortolani E. Prevalenza del kinking carotideo in unapopolazioneresidente. Risultatiparzialidelprogramma OPI (ObiettivoPrevenzione Ictus) [Prevalence of carotid kinking in a resident population. Partial results of the OPI (Objective Prevention of Ictus)[. Minerva Cardioangiol. 1993;41:129-32.
Balevi M. Dolicho-Arteriopathies (Kinking, Coiling, Tortuosity) of the Carotid Arteries: A Study by Magnetic Resonance Angiography. Int J Neck Head Surg, 2020;11:50-4. doi: 10.5005/jp-journals-10001-1405
Valvano A, Bosso G, Apuzzi V, Mercurio V, Di Simone V, Panicara V, et al. Long-term follow-up in high risk hypertensive patients with carotid dolicoarteriopathies. Int Angiol. 2020;39:24-8. doi: 10.23736/S0392-9590.19.04229-9
Bertulli L, Robert T. Embryological development of the human cranio-facial arterial system: a pictorial review. Surg Radiol Anat. 2021;43:961-73. doi: 10.1007/s00276-021-02684-y
Carlson BM. Basic Embryology by Patten. 5th edition, Mexico.McGraw - Hill, 1990.
Dungan DH, Heiserman JE. The carotid artery: embryology, normal anatomy, and physiology. Neuroimaging Clin N Am. 1996;6:789-99.
Huber P: Cerebral Angiography, ed 2. New York, Thieme Medical Publishers, 1982
Vitek JJ, Reaves P. Thoracic bifurcation of the common carotid artery. Neuroradiology. 1973;5:133-9. doi: 10.1007/BF00341527
Lie TA: Congenital Anomalies of the Carotid Arteries: An Angiographic Study and a Review of the Literature. Amsterdam, Excerpta Medica, 1968.
Cairney J. Tortuosity of the Cervical Segment of the Internal Carotid Artery. J Anat 1924;59:87-96.
Harrison J, Dávalos P. Cerebral ischemia. Arch Surg 1962; 84:109-12.
Voevoda MI, Kulikov IV, Maksimov VN, Smirnova IuV. [Association of Sp4 gene polymorphism with pathological tortuosity of internal carotid arteries[. Kardiologiia. 2009;49:46-9.
Zaidi SH, Peltekova V, Meyer S, Lindinger A, Paterson AD, Tsui LC, et al. A family exhibiting arterial tortuosity syndrome displays homozygosity for markers in the arterial tortuosity locus at chromosome 20q13. Clin Genet 2005;67:183-8. doi: 10.1111/j.1399-0004.2004.00391.x.
Arslan Y, Arslan IB, Pekçevik Y, Sener U, Köse S, Zorlu Y. Matrix Metalloproteinase Levels in Cervical and Intracranial Carotid Dolichoarteriopathies. J Stroke Cerebrovasc Dis 2016;25:2153-8. doi: 10.1016/j.jstrokecerebrovasdis.2016.05.028
Foiadelli T, Ippolito R, Corbetta R, Simoncelli AM, Amariti R, Licari A, et al. Clinical variability in children with dolichoarteriopathies of the internal carotid artery. Childs Nerv Syst 2020;36:621-8. doi: 10.1007/s00381-019-04395-7.
Welby JP, Kim ST, Carr CM, Lehman VT, Rydberg CH, Wald JT, et al. Carotid Artery Tortuosity Is Associated with Connective Tissue Diseases. AJNR Am J Neuroradiol 2019;40:1738-43. doi: 10.3174/ajnr.A6218
Paltseva EM, Oskolkova SA, Polyakova VO, Krylova YS, Ivanova AG, Abramyan AV, et al. [The structure of the internal carotid artery wall in pathological tortuosity[. Arkh Patol 2015;77:3-8. Russian. https://doi.og/10.17116/patol20157753-8
Ballotta E, Thiene G, Baracchini C, Ermani M, Militello C, Da Giau G, et al. Surgical vs medical treatment for isolated internal carotid artery elongation with coiling or kinking in symptomatic patients: a prospective randomized clinical study. J Vasc Surg 2005;42:838-46; discussion 846. doi: 10.1016/j.jvs.2005.07.034
Sethi SS, Lau JF, Godbold J, Gustavson S, Olin JW. The S curve: a novel morphological finding in the internal carotid artery in patients with fibromuscular dysplasia. Vasc Med 2014;19:356-62. doi: 10.1177/1358863X14547122
Ballotta E, Da Giau G, Bottio T. Elongation of the internal carotid artery and abdominal aortic aneurysm: is there a relationship? J Cardiovasc Surg (Torino). 1999;40:21-6
Etheredge SN, Effeney DJ, Ehrenfeld WK. Symptomatic extrinsic compression of the cervical carotid artery. Arch Neurol 1984;41:672-3. doi: 10.1001/archneur.1984.04210080084020
Del Corso L, Moruzzo D, Conte B, Agelli M, Romanelli AM, Pastine F, et al. Tortuosity, kinking, and coiling of the carotid artery: expression of atherosclerosis or aging? Angiology 1998;49:361-71. doi: 10.1177/000331979804900505
Pancera P, Ribul M, Presciuttini B, Lechi A. Prevalence of carotid artery kinking in 590 consecutive subjects evaluated by Echocolordoppler. Is there a correlation with arterial hypertension? J Intern Med 2000;248:7-12. doi: 10.1046/j.1365-2796.2000.00611.x
Oliviero U, Cocozza M, Picano T, Policino S, Russo N, Fazzio S, et al. Prevalence of carotid kinking and coiling in a population at risk.Vasc Surg 1997;31:43-9. doi: 10.1177/153857449703100106
Wang HF, Wang DM, Wang JJ, Wang LJ, Lu J, Qi P, et al. Extracranial Internal Carotid Artery Tortuosity and Body Mass Index. Front Neurol. 2017;8:508. doi: 10.3389/fneur.2017.00508
Dilba K, van Dam-Nolen DHK, Crombag GAJC, van der Kolk AG, Koudstaal PJ, Nederkoorn PJ, et al. Dolichoarteriopathies of the extracranial internal carotid artery: The Plaque At RISK study. Eur J Neurol 2021;28:3133-8. doi: 10.1111/ene.14982
Derubertis BG, Hynecek RL, Kent KC, Faries PL. Carotid tortuosity in patients with prior cervical radiation: increased technical challenge during carotid stenting. Vasc Endovascular Surg. 2011;45:619-26. doi: 10.1177/1538574411408745
Saba L, Argiolas GM, Sumer S, Siotto P, Raz E, Sanfilippo R, et al. Association between internal carotid artery dissection and arterial tortuosity. Neuroradiology 2015;57:149-53. doi: 10.1007/s00234-014-1436-x.
Barbour PJ, Castaldo JE, Rae-Grant AD, Gee W, Reed JF 3rd, Jenny D, et al. Internal carotid artery redundancy is significantly associated with dissection. Stroke. 1994;25:1201-6. doi: 10.1161/01.str.25.6.1201.
Yu J, Qu L, Xu B, Wang S, Li C, Xu X, et al. Current Understanding of Dolichoarteriopathies of the Internal Carotid Artery: A Review. Int J Med Sci. 2017;14:772-84. doi: 10.7150/ijms.19229
Di Pino L, Franchina AG, Costa S, Gangi S, Strano F, Ragusa M, et al. Prevalence and morphological changes of carotid kinking and coiling in growth: an echo-color Doppler study of 2856 subjects between aged 0 to 96 years. Int J Cardiovasc Imaging. 2021;37:479-84. doi: 10.1007/s10554-020-02014-0
Uchino A, Kohyama S. Long segment dolichoectasia of the right internal carotid artery diagnosed by CT angiography. Radiol Case Rep. 2019;14:1084-7. doi: 10.1016/j.radcr.2019.06.013
Mamedov FR, Arutiunov NV, Usachev DIu, Lukshin VA, Beliaev AIu, Mel'nikova-Pitskhelauri TV, et al. [Neuroradiological diagnostics of atherosclerotic lesions and kinking of the carotid arteries in determination of indications to surgical treatment[. Zh Vopr Neirokhir Im N N Burdenko. 2011;75:3-10.
Nagata T, Masumoto K, Hayashi Y, Watanabe Y, Kato Y, Katou F. Three-dimensional computed tomographic analysis of variations of the carotid artery. J Craniomaxillofac Surg. 2016;44:734-42. doi: 10.1016/j.jcms.2016.02.011
KazakovIu I, Ivanova OV, Pospelova AM, Vardak A. [Diagnostic peculiarities, surgical policy, and efficacy of reconstructive operations in pathological tortuosity of internal carotid arteries[. Angiol Sosud Khir. 2015;21:153-7.
Tomiya Y, Chiba S, Moriyama H, Kikuchi Y, Ohta M. [Eighteen cases of tortuosity of the internal carotid--usefulness of MR-angiography in diagnosis[. Nihon Jibiinkoka Gakkai Kaiho. 1995;98:1367-72. Japanese. doi: 10.3950/jibiinkoka.98.1367
Yin L, Li Q, Zhang L, Qian W, Liu X. Correlation between cervical artery kinking and white matter lesions. Clin Neurol Neurosurg. 2017;157:51-4. doi: 10.1016/j.clineuro.2017.04.003
Oliviero U, Scherillo G, Casaburi C, Di Martino M, Di Gianni A, Serpico R, et al. Prospective evaluation of hypertensive patients with carotid kinking and coiling: an ultrasonographic 7-year study. Angiology 2003;54:169-75. Doi: 10.1177/000331970305400205
Iwai-Takano M, Watanabe T, Ohira T. Common carotid artery kinking is a predictor of cardiovascular events: A long-term follow-up study using carotid ultrasonography. Echocardiography 2019;36:2227-33. doi: 10.1111/echo.14536
Valvano A, Bosso G, Apuzzi V, Mercurio V, Di Simone V, Panicara V, et al. Long-term follow-up in high risk hypertensive patients with carotid dolicoarteriopathies. Int Angiol. 2020;39:24-8. doi: 10.23736/S0392-9590.19.04229-9
Metz H, Murray-Leslie RM, Bannister RG, Bull JW, Marshall J. Kinking of the internal carotid artery. Lancet. 1961;1:424-6. doi: 10.1016/s0140-6736(61)90004-6
Gavrilenko AV, Kuklin AV, Kisileva TN, Abramian AV, Omarzhanova II. [Immediate and remote results of surgical treatment of patients presenting with pathological tortuosity of internal carotid arteries and accompanying ocular ischaemic syndrome[. Angiol Sosud Khir. 2013;19:114-9
Sismanis A, Girevendoulis A. Pulsatile tinnitus associated with internal carotid artery morphologic abnormalities. Otol Neurotol. 2008;29:1032-6. doi: 10.1097/MAO.0b013e3181865913
Møller AR. Vascular compression of cranial nerves: II: pathophysiology. Neurol Res. 1999;21:439-43.
Khasiyev F, Rundek T, Di Tullio MR, Wright CB, Sacco RL, Elkind MSV, et al. Systemic Arterial Correlates of Cervical Carotid Artery Tortuosity : The Northern Manhattan Study. Clin Neuroradiol. 2022;32:435-43. doi: 10.1007/s00062-021-01044-y
Beigelman R, Izaguirre A, Robles M, Grana D, Ambrosio G, Milei J. Kinking of carotid arteries is not a mechanism of cerebral ischemia: a functional evaluation by Doppler echography. Int Angiol. 2011;30:342-8
Wang L, Zhao F, Wang D, Hu S, Liu J, Zhou Z, et al. Pressure Drop in Tortuosity/Kinking of the Internal Carotid Artery: Simulation and Clinical Investigation. Biomed Res Int. 2016;2016:2428970. doi: 10.1155/2016/2428970
Nayak SB, Shetty SD. Surgical and embryological perspective of a big loop of internal carotid artery extending laterally beyond internal jugular vein. Surg Radiol Anat. 2021;43:413-16. doi: 10.1007/s00276-020-02619-z
Gavrilenko AV, Kuklin AV, Khripkov AS, Abramian AV. Otsenka éffektivnosti rekonstruktivnykh operatsii na sonnykh arteriiakh v sochetanii stenoza i patologicheskoi izvitosti [Assessment of efficacy of reconstructive operations on carotid arteries in combination of stenosis and pathological tortuosity[. Angiol Sosud Khir. 2014;20:116-22. Russian.
Grego F, Lepidi S, Cognolato D, Frigatti P, Morelli I, Deriu GP. Rationale of the surgical treatment of carotid kinking. J Cardiovasc Surg (Torino). 2003;44:79-85.
Illuminati G, Ricco JB, Caliò FG, D'Urso A, Ceccanei G, Vietri F. Results in a consecutive series of 83 surgical corrections of symptomatic stenotic kinking of the internal carotid artery. Surgery. 2008;143:134-9. doi: 10.1016/j.surg.2007.07.029
Kazakov IuI, Ivanova OV, Pospelova AM, Vardak A. [Diagnostic peculiarities, surgical policy, and efficacy of reconstructive operations in pathological tortuosity of internal carotid arteries[. Angiol Sosud Khir. 2015;21:153-7. Russian.
Notas
Notas de autor
Dirección para correspondencia: Dr. José Milei, Instituto de Investigaciones Cardiológicas Prof. Dr. Alberto C. Taquini, Facultad de Medicina, Universidad de Buenos Aires - CONICET, Buenos Aires, Argentina. josemilei@gmail.com
Declaración de intereses
