CARTA AL EDITOR
Fisiopatogenia de las ondas T acuminadas en la isquemia aguda. Las ondas T altas y acuminadas en infartos transmurales son el último baluarte de defensa en la tormenta isquémica.
Pathophysiology of Hyperacute T Waves in Acute Ischemia. High-peaked hyperacute T waves in transmural myocardial infarction are the last bastion in ischemic storm
Fisiopatogenia de las ondas T acuminadas en la isquemia aguda. Las ondas T altas y acuminadas en infartos transmurales son el último baluarte de defensa en la tormenta isquémica.
Revista argentina de cardiología, vol. 92, núm. 3, pp. 254-256, 2024
Sociedad Argentina de Cardiología
Agradecimiento a mi amigo y maestro académico Marcelo V Elizari por la ayuda en la redacción y crítica de este trabajo. Dedicado a nuestro inolvidable maestro Mauricio B Rosenbaum (QEPD), todo empezó con él.
Al editor:
La primera manifestación de la isquemia aguda es la aparición de ondas T altas y acuminadas, cuyo mecanismo ha sido atribuido a un aumento brusco de potasio (K+) en las capas epicárdicas. Se ha postulado que este fenómeno implica una protección en el desarrollo de necrosis de esta región del miocardio, provocada por la isquemia. (1)
La relación entre el voltaje de la onda T y el K+ extracelular es conocida desde hace varias décadas. La hiperkalemia de entre 5,5 y 6,5 meq/L genera ondas T altas y acuminadas en las derivaciones precordiales. En experimentos se ha demostrado que el bloqueo de los canales de K+ o el knockout de los genes que codifican dichos canales no permite la aparición de las ondas T altas y acuminadas en la isquemia miocárdica. (2,3) El ingreso de K+ eleva y acorta las ondas T en el epicardio, y menos en el endocardio. (4) Cabe destacar que estas ondas T se presentan en las isquemias súbitas, segmentarias, transmurales y subendocárdicas regionales (Figuras 1 y 2). (5) En la fase obstructiva de los infartos anteroseptales, muy bien protegidos por una profusa circulación colateral, el electrocardiograma registra únicamente una onda T alta y acuminada. (6) En un estudio experimental se logró reproducir cambios similares a los observados en la clínica mediante la oclusión con balón de la arteria descendente anterior en el corazón canino. La oclusión de la arteria durante 2 minutos generó un patrón típico de isquemia anteroseptal con elevación del segmento ST de 9 mm y una onda T alta y acuminada de 15 mm (Figura 3). Este experimento demuestra el efecto del aumento de los niveles de K+ (dependiente del adenosín-trifosfato, ATP) en el epicardio por acción del diazóxido. (7)
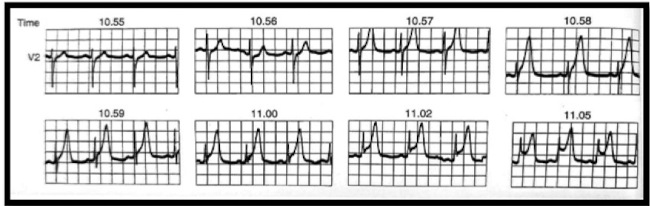
Fig. 1
Se observa la evolución electrocardiográfica de una obstrucción súbita total de la arteria descendente anterior. Nótese la evolución de onda T alta y acuminada desde 10:55 hasta 10:58 (onda de 13 mm) como primera manifestación protectora del epicardio (adenosina- K+ ATP dependiente) con elevación del segmento ST. La onda T alta y acuminada se debe a la entrada brusca de K+ al epicardio. El segmento ST está relacionado con el calcio, que actúa como buffer, a un pH muy disminuido, en el centro de la isquemia.
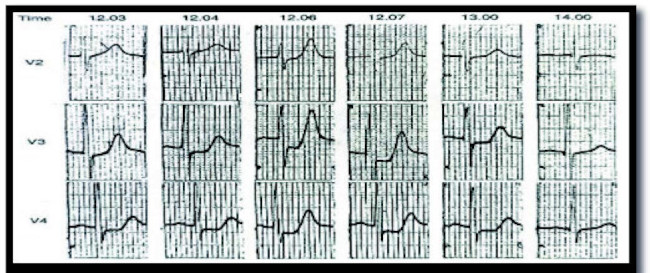
Fig. 2
La evolución electrocardiográfica de una obstrucción súbita subtotal de la arteria descendente anterior, expresado con ondas T altas y acuminadas, y segmento ST deprimido, que sugiere una isquemia subendocárdica aguda. Nótese la evolución de las ondas T altas y acuminadas de 15mm. A pesar de que la isquemia es subendocárdica, la adenosina - K+ ATP dependiente protegen el epicardio. (5) Nótese que a las 2 horas de comenzado la isquemia, aparece una onda Q mínima subendocárdica.
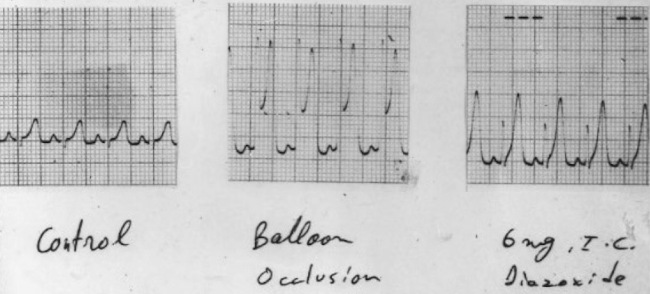
Fig. 3
Experimento en perro. A la izquierda registro en reposo. En el centro introducción de catéter balón y obstrucción súbita de la arteria coronaria descendente anterior durante 2 minutos. Se observa la típica onda T alta y acuminada de 15 mm de voltaje. A la derecha inyección intracoronaria de 5mg de diazóxido. Se registra una onda T similar a la onda T isquémica. El diazóxido estimula la secreción de adenosina, y esta aumenta la concentración de K+ en el epicardio.
Los procesos biológicos que disminuyen los efectos de la tormenta isquémica.
Las mitocondrias son organismos independientes de las células que poseen membranas y exhiben un ADN similar al de las bacterias. (8) Su principal función es aportar energía a las células. Con ácidos grasos, glucosa y oxígeno, y mediante un complejo sistema enzimático, producen adenosín-trifosfato. (9) Por fisión se desprende un catión de fósforo que produce calor y energía. De este modo, las mitocondrias de todas las células que funcionan normalmente generan energía. (10) El mecanismo es similar al de la energía atómica de las usinas de uranio que, por su fisión producen calor y energía. Después del calcio, el fósforo es el elemento más difundido en los organismos, y en la evolución ha sido utilizado como la principal fuente de energía. (11) En consecuencia, se puede postular y es de suponer, que esta fuente de energía es la más efectiva y de bajo costo energético. El miocito, que es una célula que requiere mucha energía, posee una gran cantidad de mitocondrias. En el esfuerzo las mitocondrias se reproducen, como la fisión bacteriana, en millares, en los miocitos para proveer la energía requerida. (12) Después de esta fisión se forma el adenosín- difosfato (ADP) que, aparentemente, no tiene ninguna función biológica. Una parte de él vuelve a la mitocondria para formar adenosín-trifosfato, y otra parte pierde fosfatos. En las isquemias agudas, por falta de oxígeno, se pierde otro fosfato y forma adenosín-monofosfato (AMP). (13) Este tiene una importante función biológica al introducir calcio a través de sus canales en el retículo sarcoplásmico (reservorio de calcio en el miocito).
Siguiendo la degradación del fósforo, se libera adenosina. Esta última tiene una función de gran importancia en la protección miocárdica en la tormenta isquémica. (14) La adenosina 1 bloquea los efectos de la adrenalina en el nódulo sinusal y así evita la taquicardia sinusal, factor negativo en la isquemia aguda. (15) Un aumento de la demanda energética en las taquicardias es un factor de alto riego frente a la reducción brusca del flujo coronario. Gracias a la adenosina 1, el ritmo sinusal en la isquemia aguda es de alrededor de 55 a 70 latidos por minuto, a pesar de la ansiedad y sufrimiento del paciente. En pacientes con infarto agudo, sin atención médica durante las primeras 72 horas se puede observar taquicardia sinusal, por lo general relacionada a agotamiento de la adenosina. La adenosina 2 se encuentra en el ventrículo izquierdo y tiene una función protectora de crítica importancia en el epicardio, dado que aumenta en él la concentración de K+. (16) El K+ que invade el epicardio se manifiesta con ondas T altas (más de 15 mm) y acuminadas en las derivaciones epicárdicas anteriores en los infartos anteroseptales y en algunos infartos posteroinferiores. Esta onda T isquémica es la expresión de un acortamiento de la fase 2 del potencial de acción en el epicardio, durante la cual el calcio ingresa en el miocito. La disminución de la entrada del calcio reduce la contracción del epicardio y disminuye, por lo tanto, el consumo de oxígeno (precondicionamiento). (16)
La definición de infarto transmural anteroseptal expresa la necrosis de 2/3 de la pared (17,18,19). El tercio epicárdico está protegido por el aumento de K+ dado por la adenosina 2. En casos de infartos anteroseptales que sufren una ruptura cardíaca, se observan ondas T de alrededor de menos de 5mm, y un reducido gradiente ST-T, situación que permite especular que el epicardio no está protegido por el mecanismo de aumento de la adenosina 2 y el K+. (20) La adenosina A2A tiene también un efecto sobre el cerebro, contrario al café, lo cual sugiere que el paciente con infarto agudo evita movimientos para disminuir la demanda cardíaca de energía, otro efecto protector para el infarto de miocardio en la etapa obstructiva. (21)
En el comienzo de este siglo se han publicado numerosos estudios sobre la función y disfunción de las mitocondrias, especialmente en insuficiencia cardiaca y en la hipertrofia. (22)
Pero no hemos encontrado en la literatura médica referencias sobre la importancia que tienen las mitocondrias y la cascada biológica desde el ATP, el aumento de la adenosina y la entrada de K+ ATP dependiente como protector del epicardio anteroseptal. En el caso de la ruptura cardíaca en el contexto del infarto agudo, nosotros especulamos que tal vez es una manifestación de disfunción mitocondrial. En la Figura 3 mostramos en un experimento en perro el efecto de la inyección de diazóxido intracoronario, que estimula la producción de adenosina, que a su vez induce la entrada de K+ ATP dependiente al epicardio. La onda T obtenida en el experimento es muy similar a la onda T en la obstrucción de la arteria descendente anterior (ambas miden 15mm).
BIBLIOGRAFÍA
Hears DJ. Activation of ATP sensitive potassium channels. A novel pharmacological approach to myocardial protection. Cardiovasc Res 1995;30;1-7.
Lukas A, Antzelevitch C. Differences in the electrophysiological response of canine ventricular epicardium and endocardium to ischemia. Role of the transient outward current. Circulation 1993;88:2903-15. https://doi.org/10.1161/01.cir.88.6.2903. PMID: 8252704.
Li RA, Leppo M, Miki T, Seino S, Marbán E. Molecular basis of electrocardiographic ST-segment elevation. Circ Res 2000;87:837-9. https://doi.org/10.1161/01.res.87.10.837.
Furukawa T, Kimura S, Furukawa N, Bassett AL, Myerburg RJ. Role of cardiac ATP-regulated potassium channels in differential responses of endocardial and epicardial cells to ischemia. Circ Res 1991;68:1693-702. https://doi.org/10.1161/01.res.68.6.1693.
Sclarovsky S, Rechavia E, Strasberg B, Sagie A, Bassevich R, Kusniec J, et al. Unstable angina: ST segment depression with positive versus negative T wave deflections--clinical course, ECG evolution, and angiographic correlation. Am Heart J 1988;116:933-41. https://doi.org/10.1016/0002-8703(88)90143-3.
Sagie A, Sclarovsky S, Strasberg B, Kracoff O, Rechavia E, Bassevich R, et al. Acute anterior wall myocardial infarction presenting with positive T waves and without ST segment shift. Electrocardiographic features and angiographic correlation. Chest 1989;95:1211-5. https://doi.org/10.1378/chest.95.6.1211.
Fedorov VV, Glukhov AV, Ambrosi CM, Kostecki G, Chang R, Janks D, et al. Effects of KATP channel openers diazoxide and pinacidil in coronary-perfused atria and ventricles from failing and non-failing human hearts. J Mol Cell Cardiol 2011;51:215-25. https://doi.org/10.1016/j.yjmcc.2011.04.016.
Boguszewska K, Szewczuk M, Kazmierczak-Baranska J, Karwowski BT. The Similarities between Human Mitochondria and Bacteria in the Context of Structure, Genome, and Base Excision Repair System. Molecules 2020;25:2857. https://doi.org/10.3390/molecules25122857.
Bertram R, Gram Pedersen M, Luciani DS, Sherman A. A #simplified model for mitochondrial ATP production. J Theor Biol 2006;243:575-86. https://doi.org/10.1016/j.jtbi.2006.07.019.
Bird RP, Eskin NAM. The emerging role of phosphorus in human health. Adv Food Nutr Res 2021;96:27-88. https://doi.org/10.1016/bs.afnr.2021.02.001.
Mishra P, Chan DC. Metabolic regulation of mitochondrial dynamics. J Cell Biol 2016;212:379-87. https://doi.org/10.1083/jcb.201511036.
Mubagwa K, Flameng W. Adenosine, adenosine receptors and myocardial protection: an updated overview. Cardiovasc Res 2001;52:25-39. https://doi.org/10.1016/s0008-6363(01)00358-3.
Watanabe A, Besch J. Cyclic adenosine monophosphate modulation of calcium influx channels. Circ Res 1974;35;216-22.
Crimm A, Severance HW Jr, Coffey K, McKinnis R, Wagner GS, Califf RM. Prognostic significance of isolated sinus tachycardia during first three days of acute myocardial infarction. Am J Med. 1984;76:983-8. https://doi.org/10.1016/0002-9343(84)90846-5.
Tseng CJ, Ho WY, Lin HC, Tung CS, Kuan CJ. Modulatory effects of endogenous adenosine on epinephrine secretion from the adrenal medulla of the rat. Hypertension 1994;24:714-8. https://doi.org/10.1161/01.hyp.24.6.714.
Murry CE, Jennings RB, Reimer KA. Preconditioning with ischemia: a delay of lethal cell injury in ischemic myocardium. Circulation. 1986;74:1124-36. https://doi.org/10.1161/01.cir.74.5.1124.
O'Rourke B. Myocardial K(ATP) channels in preconditioning. Circ Res. 2000;87:845-55. https://doi.org/10.1161/01.res.87.10.845.
Liu Y, Sato T, O'Rourke B, Marban E. Mitochondrial ATP-dependent potassium channels: novel effectors of cardioprotection? Circulation. 1998;97:2463-9. https://doi.org/10.1161/01.cir.97.24.2463.
Sclarovsky S. The electrocardiogram of acute ischemic syndrome. Martin Dunitz 1999 London chapter 2 fig 2.22. The electrocardiograms from 6 patients with evolving acute anteroseptal MI, with ventricular rupture.
Lazarus M, Shen HY, Cherasse Y, Qu WM, Huang ZL, Bass CE, et al. Arousal effect of caffeine depends on adenosine A2A receptors in the shell of the nucleus accumbens. J Neurosci. 2011;31:10067-75. https://doi.org/10.1523/JNEUROSCI.6730-10.2011.
Zhou B, Tian R. Mitochondrial dysfunction in pathophysiology of heart failure. J Clin Invest. 2018;128:3716-26. https://doi.org/10.1172/JCI120849.
Zhou B, Tian R. Mitochondrial dysfunction in pathophysiology of heart failure. J Clin Invest. 2018;128:3716-26. https://doi.org/10.1172/JCI120849.
Notas
Notas de autor
Dirección para correspondencia: Samuel Sclarovsky. E-mail: samuel_s@netvision.net.il
Declaración de intereses