CARTA CIENTÍFICA
Trasplante cardíaco de emergencia en paciente con miocardiopatía arritmogénica y tormenta eléctrica
Emergency Cardiac Transplantation in Patient with Arrhythmogenic Cardiomyopathy and Electrical Storm
La miocardiopatía arritmogénica (MA) es una enfermedad genética del músculo cardíaco caracterizada por progresiva sustitución de células musculares por tejido fibroso y adiposo, que afecta frecuentemente al ventrículo derecho (VD) con compromiso variable del ventrículo izquierdo (VI), y provoca disfunción ventricular y predisposición a arritmias potencialmente fatales y muerte súbita. Se asocia a herencia autosómica dominante con penetrancia variable, y compromete a genes codificadores de los desmosomas. Representan un desafío tanto su diagnóstico como el manejo clínico. 1
Se presenta un paciente de sexo masculino de 27 años, con antecedente en 2018 de extrasístoles ventriculares (EV) frecuentes, electrocardiograma con ondas T negativas en DIII, aVF, V2-V6, constatadas en estudio prequirúrgico. Fue evaluado mediante un ECG Holter que evidenció 17 183 EV en el día, bigeminias y tripletas; un ecocardiograma que mostró deterioro moderado de la función sistólica del VI, fracción de eyección del VI 40 %, hipoquinesia global, dilatación y disfunción marcada del VD; y resonancia magnética cardíaca con realce tardío subepicárdico inferior, de pared libre y tracto de salida del VD, deterioro moderado del VI y disincronía interventricular, compatible con miocardiopatía arritmogénica con compromiso biventricular. Ante dichos hallazgos se colocó un cardiodesfibrilador implantable (CDI) como prevención primaria de muerte súbita. Luego presentó una internación en otra institución por choque efectivo del CDI, con evidencia de múltiples episodios de taquicardia ventricular (TV), por lo que realizó tratamiento con betabloqueantes y antiarrítmicos, sotalol a máximas dosis y amiodarona, que debió ser suspendida por hipertiroidismo.
Consultó a nuestra institución por palpitaciones seguidas de choque del CDI en dos oportunidades. Al ingreso estaba lúcido, clínicamente estable, bien perfundido, sin signos de congestión, buena entrada de aire sin ruidos agregados, con saturación de oxígeno 98 % al aire ambiente, y sin alteraciones en laboratorio. Repitió
palpitaciones y se constató TV sostenida por monitoreo. (Figura 1) Ante arritmia ventricular demostrada y dos choques de CDI en las últimas 24 horas, se diagnosticó tormenta eléctrica e inició protocolo con lidocaína y sulfato de magnesio con reversión a ritmo sinusal.
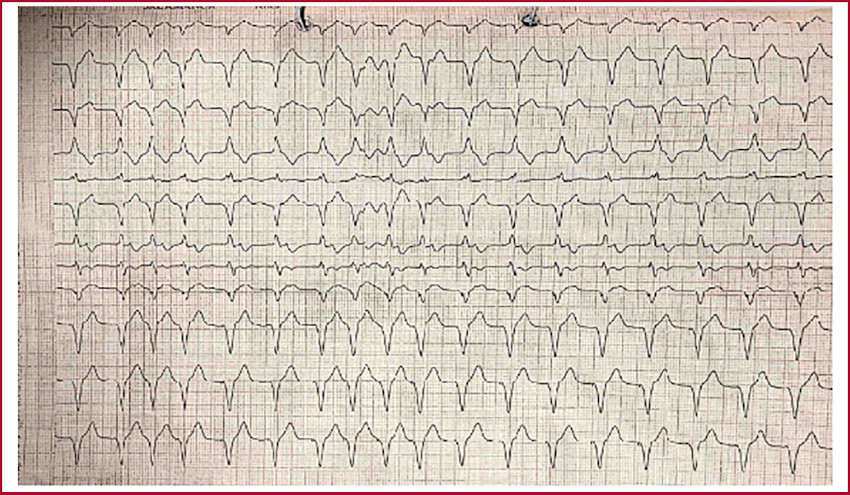
Se realizó la lectura del dispositivo y se constataron múltiples episodios de TV sostenida con cardioversión eléctrica efectiva en dos oportunidades y terapias antitaquicardia en reiteradas ocasiones.
Por considerarse un posible gatillo isquémico, se efectuó angiotomografía cardíaca que descartó enfermedad coronaria. En conjunto con Electrofisiología, se evaluó la posibilidad de ablación por radiofrecuencia mediante resonancia magnética cardíaca, que constató dilatación del VD con volúmenes marcadamente incrementados, función sistólica con deterioro grave, fibrosis transmural de toda la pared libre con adelgazamiento de la misma.
Ante el severo adelgazamiento, se desestimó la ablación por el riesgo elevado de ruptura ventricular y taponamiento cardíaco.
Evolucionó con múltiples episodios de tormenta eléctrica con reinicio de protocolo de lidocaína. Debido al cuadro refractario, se decidió la intubación orotraqueal, soporte respiratorio mecánico y sedación profunda para disminuir el estímulo adrenérgico. Presentó un episodio de fibrilación ventricular con reanimación cardiopulmonar y desfibrilación cardíaca externa con retorno a circulación espontánea, luego del cual presentó síndrome de bajo volumen minuto por lo que requirió el inicio de soporte inotrópico con milrinona y levosimendán.
Ante su evolución tórpida se realizó evaluación para trasplante cardíaco y posterior ingreso en lista de espera en situación de Emergencia B. Se inició mexiletina, con lo que resolvió en gran parte la densidad arrítmica y se logró la extubación. Se realizó trasplante cardíaco ortotópico bicavo, sin complicaciones postoperatorias inmediatas. Se envió el corazón nativo a estudio anatomo-patológico, que constató extensa sustitución adiposa y desorganización de haces musculares con focos de necrosis miocitaria, con diagnóstico definitivo de MA con afectación biventricular (Figura 2).
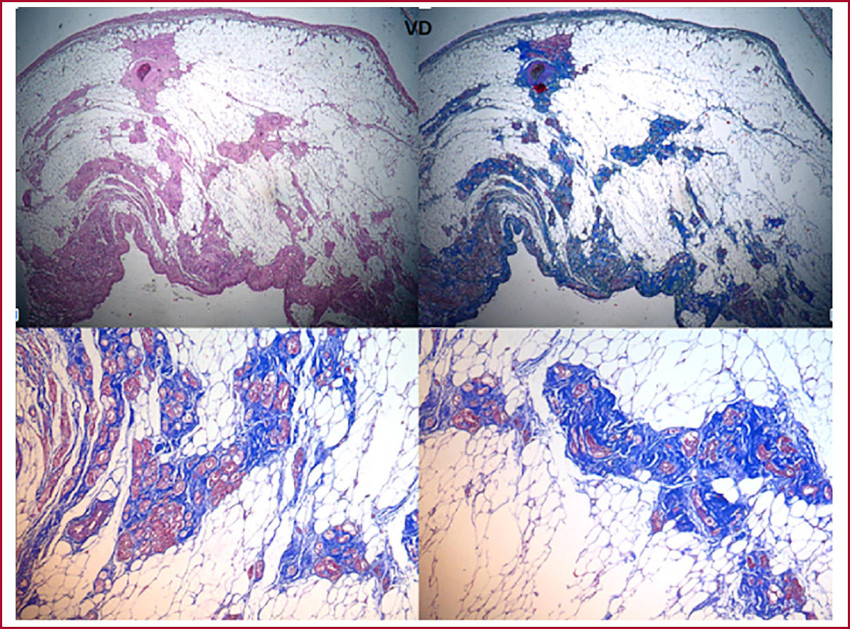
Se realizó biopsia endomiocárdica previo a su egreso. Presentaba rechazo celular grado 2R sin evidencias de rechazo mediado por anticuerpos, por lo cual recibió corticoides a altas dosis con resolución clínica e histopatológica del mismo. Posteriormente, completó su internación sin otras intercurrencias.
La MA es una enfermedad cardiaca hereditaria rara, potencialmente mortal, que requiere atención clínica y un enfoque terapéutico integral. El diagnóstico actual está basado en los criterios Task Force 2010, consistentes en alteraciones estructurales en estudios imagenológicos e histopatológicos, alteraciones de la conducción y repolarización en el electrocardiograma, la presencia de taquicardia ventricular con morfología de bloqueo completo de rama izquierda en electrocardiograma o Holter y la historia familiar, especialmente aquellos de primer grado con estudio genético confirmatorio. 1
Se define tormenta eléctrica a tres o más episodios de arritmia ventricular sostenida, terapia antitaquicardia o choque de CDI en 24 horas; predispone a descompensación por insuficiencia cardíaca y aumento de la mortalidad. Se sugiere un manejo inicial con betabloqueantes, de preferencia no selectivos, combinados con amiodarona. De mantenerse refractaria al tratamiento, se debe considerar la sedación profunda e intubación con asistencia respiratoria mecánica para disminuir el estrés psicológico y el tono simpático proarritmogénico. La ablación con catéter se asocia a reducción de la arritmia y recurrencia de tormenta en pacientes aptos para el procedimiento. 2
Acorde al registro de Johns Hopkins de 2012, con 1000 pacientes con MA, solo 18 recibieron trasplante cardíaco entre 1995 y 2009; se presentaron a edad joven y con compromiso de VI, consiguiéndose supervivencias al año postrasplante de 94 %. En 13 de estos, el motivo del trasplante fue insuficiencia cardíaca sintomática, y solo en 5 arritmia ventricular refractaria. 3
Según el registro Nordic de trasplante cardíaco en pacientes con MA, publicado en 2017, se realizaron 31 trasplantes entre 1988 y 2014. Comparados con un grupo control con MA no trasplantados, el único factor de riesgo independiente predictor de trasplante fue la aparición del primer síntoma antes de los 35 años. El 90 % se trasplantaron por insuficiencia cardiaca, frente al 10 % por TV, con supervivencia posttrasplante de 91 % a 5 años. 4
Las guías actuales de trasplante cardíaco no proveen recomendaciones específicas para la MA debido a su baja frecuencia, y solo una pequeña proporción de esta población necesita ser considerada para el mismo;5 sin embargo, existen recomendaciones de inclusión de pacientes con arritmias ventriculares refractarias. 6

