CARTA AL EDITOR
Apuntes sobre el electrocardiograma en la infancia y la adolescencia
Notes on the Electrocardiogram in Childhood and Adolescence
Apuntes sobre el electrocardiograma en la infancia y la adolescencia
Revista argentina de cardiología, vol. 92, no. 4, pp. 316-319, 2024
Sociedad Argentina de Cardiología
Las hipertrofias fisiológicas en la infancia
Al nacer el mamífero se cierra el ductus arterioso y se reduce la resistencia vascular pulmonar. La predominancia del ventrículo derecho persiste un tiempo limitado. (Figura 1) La predominancia del ventrículo izquierdo aparece en las ratas a las 2 semanas, en los cerdos a las 6 semanas (1) y en el humano a las 12 semanas. (Figura 1) Es asombroso observar a los pequeños terneros y potrillos en las praderas, que a las 4 horas de nacer, pueden correr a 40 - 60 Km/h. Para esto deben tener un ventrículo izquierdo perfectamente adaptado para subsistir. La evolución prepara el ventrículo izquierdo durante el embarazo para soportar intensos esfuerzos a las pocas horas del nacimiento.
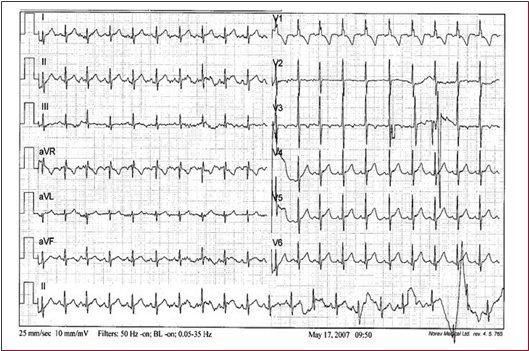
Fig. 1
Bebé de 3 meses, todavía con predominancia del ventrículo derecho. Ver onda R en V1
El recién nacido tiene una frecuencia cardíaca de 190 a 200 lpm y se mantiene una frecuencia alta durante la infancia, entre 80 y 120 lpm. (2) Esta frecuencia cardíaca está determinada por las catecolaminas. La adrenalina es segregada por 2 fuentes, una endocrina (la glándula suprarrenal) y otra paracrina (las fibras simpáticas cardíacas terminales). En los miocitos hay receptores alfa y beta. El estímulo exagerado de los beta receptores es muy perjudicial para el miocito. (3) Para evitar este efecto existe un betabloqueante biológico, la arrestina. (4) Pero el efecto sobre los receptores alfa (en la membrana del miocito hay 3 tipos de receptores alfa) estimula la formación de sarcómeros. (5) Los sarcómeros se van agregando en forma longitudinal. (5,6) El efecto de la adrenalina sobre el receptor alfa genera el crecimiento de los sarcómeros y el alargamiento del miocito, que determina el voltaje del QRS.
Pero hay otro sistema electromecánico que estimula las hipertrofias fisiológicas. En el endocardio del ventrículo izquierdo hay receptores de tensión, cuya distribución en el subendocardio no es homogénea. (7) Es posible especular que la morfología de electrocardiograma del niño varía, dependiendo de la concentración de receptores de tensión en el endocardio. Mayor concentración de receptores de tensión, más el estímulo de los receptores alfa, inducirán las hipertrofias fisiológicas.
El electrocardiograma del niño en un 30 % de los casos es normal (Figura 2). En la niñez existe en el 70% de los casos una hipertrofia fisiológica que acompaña el crecimiento corporal. El ECG puede registrar 4 diferentes fenotipos de hipertrofia: 1) apical (Figura 3), que se expresa con ondas R dominantes en V4 y V5; 2) anteroseptal (Figura 4), que se expresa con ondas R dominantes en V2 (tercio superior del septo), V2 y V3 (tercio superior y medio), y V2 a V4 (tercio superior, medio e inferior del septo); 3) posteroseptal (Figura 5), que se expresa con ondas S profundas en V2, V3 y V4; y 4) lateral, que se expresa con ondas R altas en DI y S profundas en AVR y V1. En los roedores se han identificado receptores de tensión endocárdicos distribuidos en forma no homogénea en el septum y en ápex lateral. (8) Se podría sospechar que la distribución no homogénea de receptores de tensión es factor de importancia universal en el funcionamiento cardíaco en la infancia de los mamíferos.
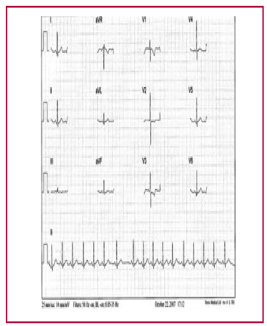
Fig. 2
Niño de 6 años sin hipertrofia fisiológica excéntrica, proba blemente hipertrofia fisiológica concéntrica.
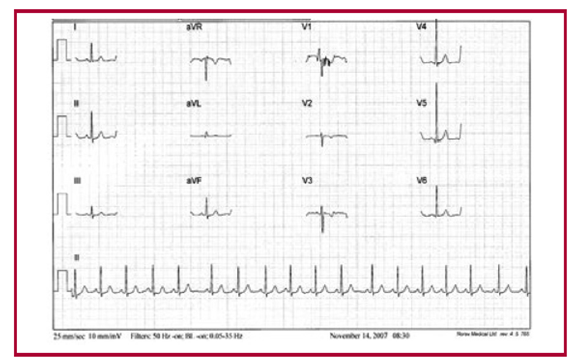
Fig. 3
Niño de 9 años con hipertrofia excéntrica apical con ondas R altas en V4 y V5
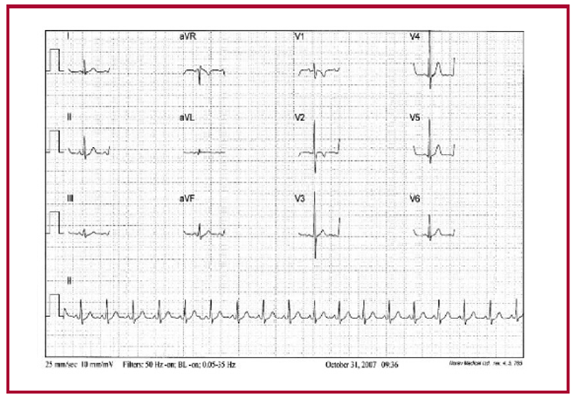
Fig. 4
Niño de 9 años con hipertrofia fisiológica excéntrica ante roseptal, con ondas R altas en V2, V3 y V4
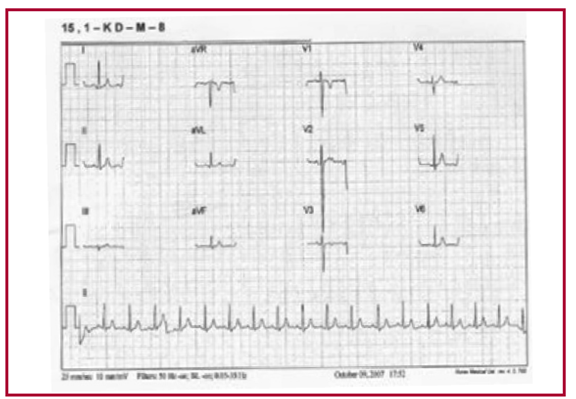
Fig. 5
Niño de 5 años con hipertrofia excéntrica posteroseptal, con onda S en V2 de 40 mm.
El ECG con trazado normal podría ser debido a hipertrofia concéntrica, a que los receptores de tensión están distribuidos en forma homogénea o una mutación en la cascada hipertrófica. (9) Es importante señalar que en adultos con sobrecarga sistólica también un 30 % no presenta hipertrofias excéntricas (experiencia personal). La actividad eléctrica/mecánica induce una reacción retroalimentada. La actividad eléctrica estimula la línea Z y la proteína titina para aumentar la tensión en el complejo actina miosina. (10)
El programa fetal genético existe en la vida embrionaria, que tiene un entorno ligeramente hipoxémico. (11) En este contexto las mitocondrias usan la glucosa para generar energía. Pero con el nacimiento las mitocondrias comienzan a usar los ácidos grasos oxigenados como combustible energético. El programa fetal se mantiene escondido, inactivo; pero en casos de hipertrofias fisiológicas o patológicas se reactiva. Este programa previene la progresión de las hipertrofias hacia la dilatación y la insuficiencia cardíaca. Nosotros especulamos que en las hipertrofias fisiológicas cardíacas en los niños podría existir un programa fetal genético como protección del miocardio. Es interesante la observación de que las hipertrofias fisiológicas de los niños ya no se observan en la adolescencia.
Las hormonas sexuales determinan la morfología de la repolarización del electrocardiograma en la adolescencia
Los estrógenos controlan la corriente de salida transitoria rectificada rápida del canal de potasio (12), que forma la rama descendente de la onda T, lenta y alargada comparada con esta rama en el sexo masculino, y también la corriente del canal de potasio rectificada lenta, (13) que forma la punta de la onda T, muy baja o negativa comparada con la onda T alta y acuminada masculina.
Estas hormonas controlan también la entrada de calcio en la fase 2 del potencial de acción, expresándose con un segmento ST alargado. (14)
Los andrógenos tienen un efecto estimulante sobre los canales de potasio (15) y de calcio, que se expresa con la punta de la onda T alta y acuminada, una rama descendente corta y rápida, y el segmento ST corto y elevado. (15) El efecto de la testosterona sobre el canal del calcio influye en el segmento ST, que es corto y elevado generalmente en V2 y V3. (16) (Ver figuras 6 y 7)
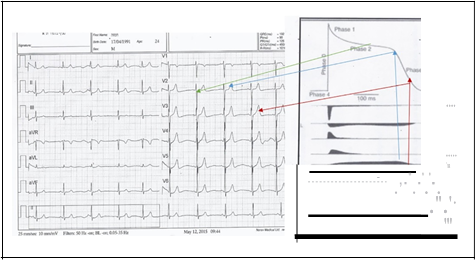
Fig. 6
ECG de varón de 22 años.
La flecha roja señala la corriente del canal de potasio rectificada rápida, que actúa en la fase 3 del potencial de acción (PA) que y forma la rama descendente corta y rápida de la onda T. La flecha azul señala la corriente del canal de potasio rectificada lenta que actúa en la unión de las fases 2 y 3 del PA y forma la onda T alta y acuminada. La flecha verde señala la corriente del canal del calcio que actúa en la fase 2 del PA y condiciona el ST corto y elevado en el ECG.
De Nerbonne JM, Kass RS. Molecular physiology of cardiac repolarization. Physiol Rev. 2005;85:1205-53. Modificado por Sclarovsky S

Fig. 7
ECG de mujer de 16 años.
La flecha roja señala la relación entre la corriente rectificada rápida del canal de potasio y la fase 3 del potencial de acción (PA), que condiciona la rama descendente, lenta y atenuada de la onda T (con respecto a la onda T masculina).
La flecha azul señala la relación de la corriente rectificada lenta del canal de potasio con la unión de las fases 2 y 3 del PA, que forma la punta de la onda T atenuada.
La flecha verde señala la relación entre la corriente de calcio, la fase 2 del PA, y el segmento ST largo y atenuado.
De Nerbonne JM, Kass RS. Molecular physiology of cardiac repolarization. Physiol Rev. 2005;85:1205-53. Modificado por Sclarovsky SBIBLOGRAFÍA
Ahuja P, Sdek P, MacLellan WR. Cardiac myocyte cell cycle control in development, disease, and regeneration. Physiol Rev 2007;87:521-44. https://doi.org/10.1152/physrev.00032.2006 .
Cysarz D, Linhard M, Edelhäuser F, Längler A, Van Leeuwen P, Henze G, et al. Symbolic patterns of heart rate dynamics reflect cardiac autonomic changes during childhood and adolescence. Auton Neurosci 2013;178:37-43. https://doi.org/10.1016/j.autneu.2013.02.003 .
Hu A, Jiao X, Gao E, Koch WJ, Sharifi-Azad S, Grunwald Z, Ma XL, Sun JZ. Chronic beta-adrenergic receptor stimulation induces cardiac apoptosis and aggravates myocardial ischemia/reperfusion injury by provoking inducible nitric-oxide synthase-mediated nitrative stress. J Pharmacol Exp Ther 2006;318:469-75. https://doi.org/10.1124/jpet.106.102160 .
Lohse MJ, Benovic JL, Codina J, Caron MG, Lefkowitz RJ. beta-Arrestin: a protein that regulates beta-adrenergic receptor function. Science 1990;248:1547-50. https://doi.org/10.1126/science.2163110 .
Cotecchia S, Del Vescovo CD, Colella M, Caso S, Diviani D. The alpha1-adrenergic receptors in cardiac hypertrophy: signaling mechanisms and functional implications. Cell Signal 2015;27:1984-93. https://doi.org/10.1016/j.cellsig.2015.06.009 .
Piascik MT, Perez DM. Alpha1-adrenergic receptors: new insights and directions. J Pharmacol Exp Ther 2001;298:403-10.
Kelly D, Mackenzie L, Hunter P, Smaill B, Saint DA. Gene expression of stretch-activated channels and mechanoelectric feedback in the heart. Clin Exp Pharmacol Physiol 2006;33:642-8. https://doi.org/10.1111/j.1440-1681.2006.04392.x .
Stones R, Gilbert SH, Benoist D, White E. Inhomogeneity in the response to mechanical stimulation: cardiac muscle function and gene expression. Prog Biophys Mol Biol 2008;97:268-81. https://doi.org/10.1016/j.pbiomolbio.2008.02.010 .
Esposito G, Rapacciuolo A, Naga Prasad SV, Takaoka H, Thomas SA, Koch WJ , et al . Genetic alterations that inhibit in vivo pressure-overload hypertrophy prevent cardiac dysfunction despite increased wall stress. Circulation 2002;105:85-92. https://doi.org/10.1161/hc0102.101365 .
Trombitás K, Granzier H. Actin removal from cardiac myocytes shows that near Z line titin attaches to actin while under tension. Am J Physiol 1997;273:C662-70. https://doi.org/10.1152/ajpcell.1997.273.2.C662 .
Taegtmeyer H, Sen S, Vela D. Return to the fetal gene program: a suggested metabolic link to gene expression in the heart. Ann N Y Acad Sci 2010;1188:191-8. https://doi.org/10.1111/j.1749-6632.2009.05100.x .
El Gebeily G, El Khoury N, Mathieu S, Brouillette J, Fiset C. Estrogen regulation of the transient outward K(+) current involves estrogen receptor α in mouse heart. J Mol Cell Cardiol 2015;86:85-94. https://doi.org/10.1016/j.yjmcc.2015.07.013 .
Zhu Y, Ai X, Oster RA, Bers DM, Pogwizd SM. Sex differences in repolarization and slow delayed rectifier potassium current and their regulation by sympathetic stimulation in rabbits. Pflugers Arch 2013;465:805-18. https://doi.org/10.1007/s00424-012-1193-9 .
Chu SH, Goldspink P, Kowalski J, Beck J, Schwertz DW. Effect of estrogen on calcium-handling proteins, beta-adrenergic receptors, and function in rat heart. Life Sci 2006;79:1257-67. https://doi.org/10.1016/j.lfs.2006.03.037 .
Liu XK, Katchman A, Whitfield BH, Wan G, Janowski EM, Woosley RL, et al. In vivo androgen treatment shortens the QT interval and increases the densities of inward and delayed rectifier potassium currents in orchiectomized male rabbits. Cardiovasc Res 2003;57:28-36. https://doi.org/10.1016/s0008-6363(02)00673-9 .
Michels G, Er F, Eicks M, Herzig S, Hoppe UC. Long-term and immediate effect of testosterone on single T-type calcium channel in neonatal rat cardiomyocytes. Endocrinology 2006;147:5160-9. https://doi.org/10.1210/en.2006-0186 .
Author notes
Dirección para correspondencia: Samuel Sclarovsky. E-mail: samuel_s@netvision.net.il