RESUMEN
Introducción: Con el objetivo de establecer el diagnóstico de amiloidosis cardíaca por transtiretina (AC-TTR) en etapas precoces, en los últimos años, se lograron identificar ciertas señales de alerta o ¨banderas rojas¨ para orientar la sospecha. Sin embargo, hasta el momento, contamos con escasa evidencia acerca de la sensibilidad y especificidad diagnóstica de cada bandera roja o de si existe alguna combinación de variables que pueda predecir en forma confiable la presencia de AC-TTR.
Objetivo: Desarrollar un modelo de predicción basado en variables clínicas, electrocardiográficas y/o ecocardiográficas que permita establecer una escala de puntuación para guiar el diagnóstico de la AC-TTR.
Material y métodos: Se analizaron las historias clínicas de 342 pacientes con centellograma cardíaco (CC) por sospecha de AC-TTR: 171 pacientes con diagnóstico positivo fueron comparados con igual número de pacientes con diagnóstico negativo. Se analizaron datos clínicos, electrocardiográficos y ecocardiográficos, los cuales fueron incluidos en modelos de regresión logística uni y multivariados. Se construyó una escala de puntuación de 0-8 y se generó una curva de característica operativa del receptor (ROC). Posteriormente, se calculó el área bajo la curva (AUC) con su IC del 95%.
Resultados: En modelos de regresión logística uni y multivariados, se identificaron como predictores de AC-TTR: el septum interventricular (SIV) ≥16mm (OR 3,6, IC 95% 1,8-7,1), sexo masculino (OR 7,9, IC 95% 3,6-17,1),, disfunción diastólica grado II y III con patrón de relajación seudonormal o restrictivo (OR 12,7, IC 95% 6,1-26,3) y el antecedente de túnel carpiano bilateral, TCB (OR 24,4, IC 95% 6,0-97,8). En función de los OR obtenidos se creó la escala de puntuación que mostró un AUC 0,88 (IC 95% 0,84-0,91; p< 0,001) y se identificó el valor ≥3, con alta sensibilidad y especificidad para predecir AC-TTR (AUC 0,82, IC 95% 0,77-0,87).
Conclusión: El modelo de predicción obtenido permitió desarrollar una escala de puntuación que demostró una alta sensibilidad y especificidad para orientar fuertemente el diagnóstico de AC-TTR.
Palabras clave: Prealbúmina, Cardiomiopatía Restrictiva, Insuficiencia Cardíaca Diastólica, Insuficiencia Cardíaca Sistólica.
ABSTRACT
Background: To verify the diagnosis of transthyretin cardiac amyloidosis (ATTR-CA) in its early stages, certain warning signs or "red flags" have been lately identified to guide suspicion. However, to date, there is little evidence regarding the diagnostic sensitivity and specificity of each red flag or whether there is any combination of variables that can reliably predict the presence of ATTR-CA.
Objective: The aim of this study was to develop a prediction model based on clinical, electrocardiographic and/or echocardiographic variables to establish a scoring scale to guide the diagnosis of ATTR-CA.
Methods: The medical records of 342 patients with cardiac scintigraphy (CS) for suspected ATTR-CA were analyzed: 171 patients with a positive diagnosis were compared with the same number of patients with a negative diagnosis. Clinical, electrocardiographic and echocardiographic data were analyzed and included in univariate and multivariate logistic regression models. A 0-8 scoring scale was built and a receiver operating characteristic (ROC) curve was generated. The area under the curve (AUC) with its 95% CI was then calculated.
Results: The following variables were identified as predictors of ATTR-CA in univariate and multivariate logistic regression models: interventricular septum (IVS) ≥16 mm (OR 3.64, 95% CI 1.87-7.1), male gender (OR 7.91, 95% CI 3.7-17.1), grade II or III diastolic dysfunction with pseudonormal or restrictive relaxation pattern (OR 12.7, 95% CI 6.1-26.3), and history of bilateral carpal tunnel syndrome (CTS) (OR 24.4, 95% CI 6.1-97.9). Based on the OR obtained, a scoring scale was created showing an AUC of 0.88 (95% CI 0.84-0.91, p<0.001), and a value ≥3, with high sensitivity and specificity, was identified to predict ATTR-CA (AUC 0.82 95% CI 0.77-0.87).
Conclusions: The prediction model allowed the development of a scoring scale that demonstrated high sensitivity and specificity to strongly guide the diagnosis of ATTR-CA.
Key words: Prealbumin, Restrictive Cardiomyopathy, Diastolic Heart Failure, Systolic Heart Failure.
ARTÍCULO ORIGINAL
Amiloidosis cardíaca por transtiretina. Desarrollo de un modelo de predicción y escala de puntuación para el diagnóstico: score deteCTTAR
Transthyretin Cardiac Amyloidosis. Development of a Prediction Model and Scoring Scale for Diagnosis: the deteCCTAR Score
Received: 06 November 2024
Accepted: 09 December 2024
La amiloidosis cardíaca por transtiretina (AC-TTR) es una miocardiopatía infiltrativa, que se origina por el depósito extracelular de amiloide, como consecuencia de la disgregación y/o mal plegamiento de la transtiretina. (1)
Si bien su prevalencia continúa siendo incierta, en ciertos escenarios clínicos tales como la miocardiopatía hipertrófica (MCH), la estenosis aórtica grave (EAo) o la insuficiencia cardíaca con fracción de eyección ventricular izquierda (FEVI) preservada (IC-FEp) suele ser más frecuente, con cifras entre el 13% y el 17%. (2,3,4,5)
En los últimos años, el surgimiento del centellograma cardíaco (CC) con fosfonatos como método diagnóstico no invasivo, junto con la aparición de nuevos fármacos para una terapia específica, llevaron a un creciente interés en esta patología, lo que generó un incremento notable en el diagnóstico. (6)
Un gran avance en este sentido fue la determinación de ciertas variables clínicas, electrocardiográficas e imagenológicas como señales de alerta o ¨banderas rojas¨ para orientar la sospecha e intentar identificar a los pacientes en etapas más precoces de la enfermedad. Sin embargo, hasta el momento, contamos con escasa evidencia acerca de la sensibilidad y especificidad diagnóstica de cada bandera roja, o de si existe alguna combinación de variables que pueda predecir en forma confiable la presencia de AC-TTR. (7)
Es sabido que la AC-TTR es una enfermedad lenta y progresiva, con un largo período asintomático o subclínico. Es justamente en estas etapas donde el diagnóstico precoz puede ser crucial para mejorar la evolución clínica y el pronóstico de quienes la padecen. Las imágenes de CC con fosfonatos son altamente sensibles y específicas para el diagnóstico, cuando se realizan en el contexto clínico adecuado. Sin embargo, la delimitación de cuándo es apropiado realizarlo y cuando no, sigue siendo un desafío.
Realizamos este estudio con el objetivo de desarrollar un modelo de predicción y posteriormente una escala de puntuación, basado en variables clínicas, electrocardiográficas y ecocardiográficas, para orientar el diagnóstico precoz de AC-TTR.
El diseño del estudio fue unicéntrico y retrospectivo. Se analizaron las historias clínicas electrónicas de 342 pacientes remitidos a nuestro servicio entre enero de 2016 y abril de 2024, para la realización de CC con Tc99m- hidroximetilen- difosfonato (HMDP) por sospecha de AC-TTR. Los CC con HMDP fueron realizados acorde a las guías vigentes. Las imágenes obtenidas fueron analizadas en forma cualitativa según la escala de Perugini. Se consideró diagnóstico positivo de AC-TTR a la presencia de captación cardíaca con HMDP grado 2 o 3 (en ausencia de cadenas livianas en suero y orina). Se consideró diagnóstico negativo para AC-TTR, la captación cardíaca grado 0. (8,9) Fueron excluidos del análisis aquellos pacientes sin consultas y/o estudios previos en nuestra institución.
Un total de 171 pacientes con diagnóstico positivo de AC-TTR, fueron comparados con igual número de pacientes con diagnóstico negativo, seleccionados al azar de un total de 564 CC con HMDP con captación grado 0 de nuestra base de datos. Las poblaciones no fueron emparejadas por sexo ni por edad, ya que ambas variables demostraron ser predictoras en otras escalas de puntuación previamente publicadas.
Se analizaron en ambos grupos datos clínicos, electrocardiográficos y ecocardiográficos. Todas las banderas rojas fueron incluidas, a excepción de proteinuria, strain longitudinal global y realce tardío con gadolinio, que fueron excluidas del análisis por alta pérdida de datos.
Se definió al patrón de relajación del ventrículo izquierdo de acuerdo con los siguientes parámetros ecocardiográficos: (10,11)
-disfunción diastólica grado I: relación E/A≤ 0,8 + Onda E ≤ 50 cm/s, y la ausencia de 2 o 3 de los siguientes parámetros: (a) relación E/e’ > 14, (b) velocidad del jet de insuficiencia tricuspídea (IT) > 2,8 m/s, y (c) volumen de la aurícula izquierda (AI) indexado > 34 mL/m2;
-disfunción diastólica grado II: relación E/A≤ 0,8 + Onda E > 50 cm/s, o relación E/A > 0,8 y < 2, y la presencia de 2 o 3 de los parámetros (a), (b) y (c) citados en el apartado anterior;
- disfunción diastólica grado III: relación E/A ≥ 2
- disfunción diastólica indeterminada cuando no cumple con los criterios antes mencionados.
Se definió hipertrofia del septum interventricular (SIV) al espesor del tabique interventricular medido en diástole ≥ 12mm (12), y túnel carpiano bilateral (TCB) a los antecedentes quirúrgicos o a la presencia de síntomas actuales compatibles con dicho síndrome. (13)
El patrón de seudoinfarto se definió como la presencia de complejos QS en las derivaciones V1-V2, en ausencia de antecedente de infarto de miocardio, y microvoltaje a la presencia de complejos QRS < 5mV en derivaciones frontales o < 10mV en las precordiales.
Las variables cuantitativas se expresaron como mediana con su correspondiente rango intercuartílico (RIC) y fueron comparadas con prueba de Mann-Whitney. Las variables cualitativas se expresaron como porcentaje y fueron comparadas mediante test de chi cuadrado múltiple.
Todos los datos recopilados, fueron incluidos en modelos de regresión logística univariados. Aquellos que mostraron significación estadística, fueron posteriormente incluidos en modelos de regresión logística multivariados para evaluar su valor predictivo en el diagnóstico de AC-TTR.
Las variables identificadas como predictoras en los modelos, se utilizaron para construir una escala de predicción con una puntuación de 0-8. Según los OR obtenidos, se asignó 1 punto para los OR entre 1 y <7; 2 puntos para los OR comprendidos entre 7 y 21, y 3 puntos para los OR >21.
La calibración de la muestra fue evaluada por la prueba estadística de Hosmer-Lemeshow. Para determinar la capacidad predictiva de la escala, se generó una curva de característica operativa del receptor (ROC) y como medida de discriminación se calculó el área bajo la curva (AUC) con su IC del 95%.
Se estableció el nivel de significación estadística como p <0,05.
El software utilizado fue SPSS Statistics versión 26.
El estudio fue aprobado por el Comité de Investigación de nuestra institución y por un Comité de Ética independiente.
En la Tabla 1 se resumen las características basales de ambos grupos con las variables incluidas en el análisis univariado.
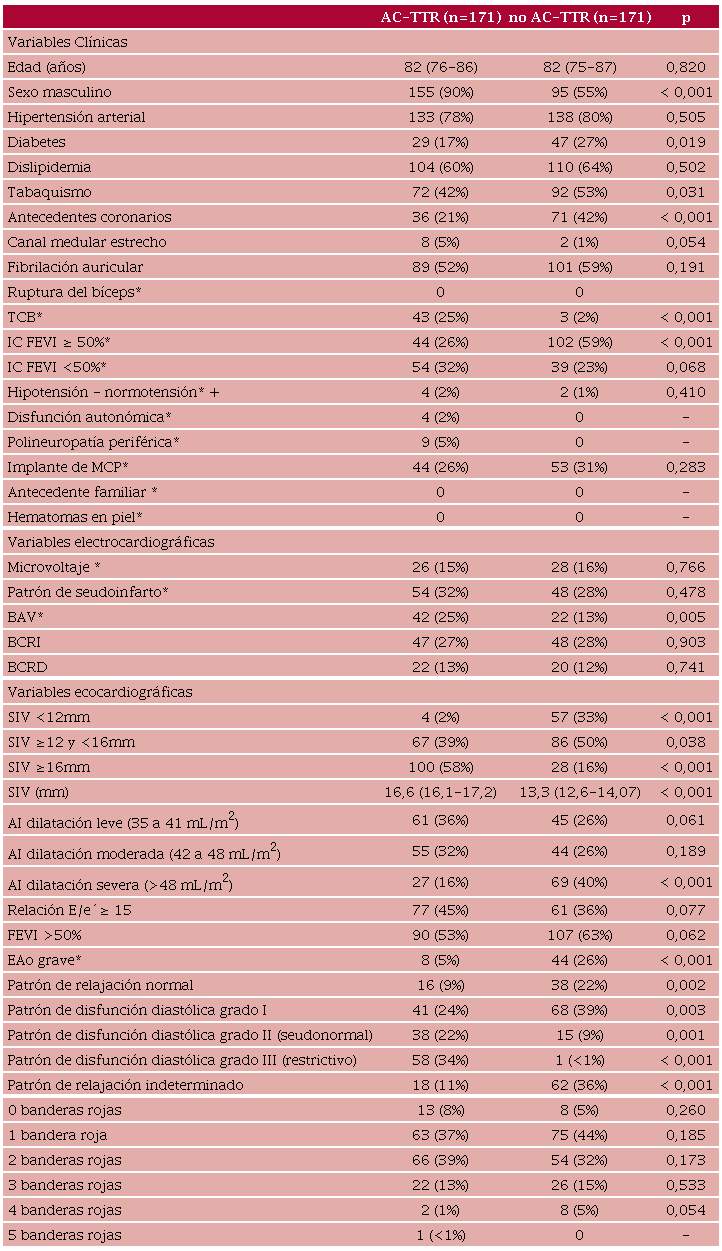
En el grupo AC-TTR fueron significativamente más prevalentes el sexo masculino, la incidencia de TCB, la polineuropatía periférica, el bloqueo aurículo-ventricular y el patrón de disfunción diastólica grado II o III. En el grupo sin AC-TTR fueron más significativamente más prevalentes la diabetes, el tabaquismo, los antecedentes coronarios, la IC con FEVI ≥50%, la dilatación marcada de la AI, y la EAO grave.
También se observaron diferencias estadísticamente significativas en el espesor del SIV: la mayoría de los pacientes sin AC-TTR tenían un espesor < 12mm o entre 12 y 16mm, con una mediana de 13,3 mm (RIC 12,6-14,07), mientras que en el grupo con AC-TTR la mayoría mostró un espesor del SIV ≥16mm, con una mediana de 16,6 mm (RIC 16,1-17,2).
En nuestro análisis, el microvoltaje y el patrón de seudoinfarto (variables predictoras de AC-TTR en otros modelos) no mostraron diferencias significativas entre ambos grupos.
No tuvimos pacientes con captación cardíaca grado 1, ni pacientes con captación grado 0 y cadenas livianas en suero y orina positivas.
Dentro del grupo con AC-TTR positiva, 13 pacientes (8%) tenían un espesor del SIV≥ 12mm sin ninguna bandera roja. Otros 3 pacientes (2%) si bien tenían banderas rojas, no presentaban espesor del SIV aumentado y, además, un paciente no presentaba ninguna de las dos condiciones.
Cuatro pacientes presentaron prueba genética positiva (AC-TTR hereditaria), siendo la mutación más frecuente la Val50Met y sólo uno de ellos presentó la variante Val142Ile.
En la Tabla 2 se detallan las variables con significancia estadística en el análisis univariado. En la Tabla 3 se muestran las variables que se identificaron como predictores de AC-TTR en el análisis multivariado y el puntaje asignado a cada una de ellas, para la confección de nuestra escala de predicción (score deteCTTAR).
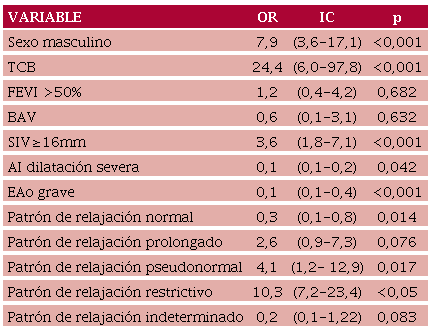
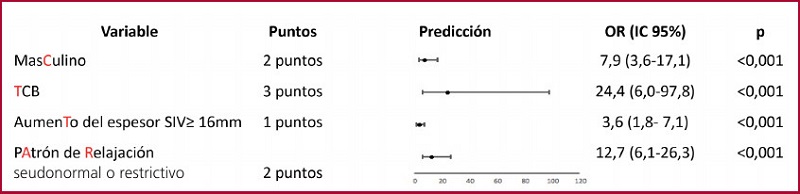
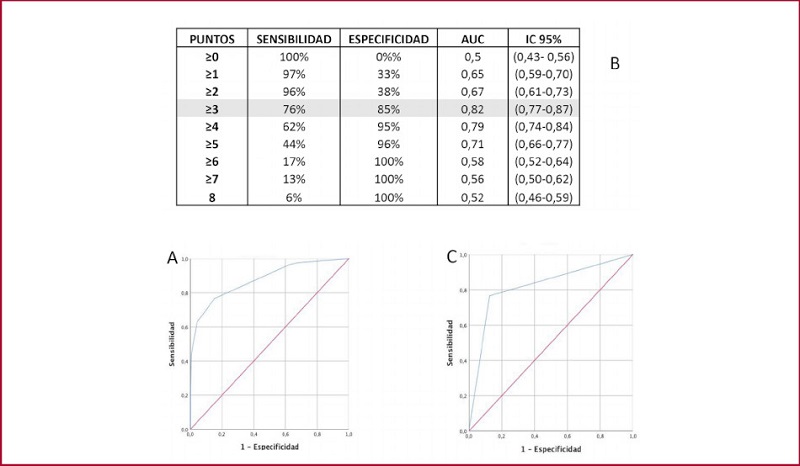
En el análisis de la curva ROC la escala mostró un AUC 0,88 (IC 95% 0,84-0,91, p< 0,001) (Fig. 1A). Se identificó el valor ≥3 como el de mejor combinación de sensibilidad y especificidad para predecir AC-TTR, con un AUC 0,82 (IC 95% 0,77-0,87) (Fig. 1B y C), con OR 22,9 (IC 95% 12,3- 42,5 p<0,001) para padecer la enfermedad.
No se evidenciaron diferencias significativas en la cantidad de banderas rojas presentes entre los grupos, ni que un mayor número de ellas conlleve un mayor riesgo de padecer AC-TTR.
En nuestro trabajo, el sexo masculino, el espesor del SIV ≥ 16 mm, la disfunción diastólica grado II o III (también conocidos como patrón de relajación seudonormal o restrictivo) y el TCB, fueron predictores de AC-TTR.
La falta de diferencias en la cantidad de banderas rojas entre los pacientes con y sin la patología confirma la baja especificidad que presentan estas condiciones para arribar al diagnóstico.
En los últimos años, fueron publicadas dos escalas de puntuación para el diagnóstico precoz de AC-TTR. Una de ellas (ATTR- CM score) realizó la búsqueda de AC-TTR entre pacientes con hipertrofia del SIV e IC con FEVI ≥ 40%. (14)
Sin embargo, según nuestros resultados, del total de los pacientes con diagnóstico positivo de AC-TTR, sólo 44 pacientes (26%) presentaban IC- FEp, 73 pacientes (42%) no mostraban signos/síntomas de IC, mientras que 54 (32%) tenían FEVI disminuida.
Si bien es sabido que la AC- TTR es una patología relacionada históricamente con la IC-FEp, cabe recordar que la evolución natural de la enfermedad sin tratamiento específico, lleva al deterioro progresivo de la histoarquitectura y función miocárdica. Inicialmente, el depósito aislado de fibrillas de amiloide afecta la función diastólica, pero posteriormente, con la acumulación excesiva se afecta el acople de las unidades sarcoméricas y ello afecta la función sistólica. (15)
Por lo tanto, en nuestro trabajo el hallazgo de pacientes con FEVI disminuida, podría ser consecuencia de la evolución natural de la enfermedad (y por ende, un diagnóstico realizado en forma tardía) o podría deberse en algunos casos, a la coexistencia de otras patologías. Es importante recalcar que dentro de este subgrupo de pacientes, el 21% presentaba antecedentes coronarios. Esto remarca que la búsqueda de AC-TTR no solo debe centrarse en miocardiopatías de etiología inexplicable, ya que la coexistencia con miocardiopatía isquémico-necrótica puede ser frecuente.
En la otra escala (T-Amylo score), para realizar la determinación de riesgo de presentar AC- TTR, los pacientes debían presentar como condición necesaria un SIV≥12mm asociado a una o más banderas rojas. (16) Sin embargo, en nuestro trabajo, 17 pacientes (10%) con diagnóstico de AC-TTR, no tenían aumento del espesor del SIV o banderas rojas.
Si bien la presencia de AC-TTR en pacientes que no presentan engrosamiento del SIV no está tan ampliamente difundida, un trabajo encontró una prevalencia de la enfermedad del 5% en pacientes con IC-FEp y SIV <12mm. (17) Esto podría explicarse de manera análoga a lo que ocurre con la cascada isquémica, en que los métodos moleculares pueden detectarla incluso antes de que se hagan evidentes cambios en el electrocardiograma, alteraciones de la motilidad o síntomas.
Ambos fenómenos (isquemia miocárdica y AC-TTR) tienen un largo período subclínico, en el cual el diagnóstico precoz es fundamental para cambiar el pronóstico de la enfermedad. (18)
Posiblemente, en el caso de la AC-TTR, si esperamos a reunir más condiciones de sospecha (mayor espesor del SIV o mayor número de banderas rojas), el diagnóstico se logre con la enfermedad más avanzada y con un daño miocárdico ya establecido. A esto debe sumarse que los nuevos fármacos aprobados en nuestro país no remueven los depósitos miocárdicos de amiloide, sino que estabilizan a la molécula de TTR para evitar su disgregación, evitando así su mayor acumulación. Todo esto nos lleva a la necesidad de tratar de establecer un diagnóstico precoz, incluso antes de que se haga evidente el aumento del espesor del SIV. (19)
De manera que el score deteCTTAR podría resultar más abarcativo que el T-Amylo score y el ATTR-CM score, ya que pudo discriminar el riesgo entre los pacientes de padecer AC-TTR, independientemente de si cumplían o no con las señales de alarma clásicas para la sospecha y del valor de la FEVI (Fig. 2 y 3).
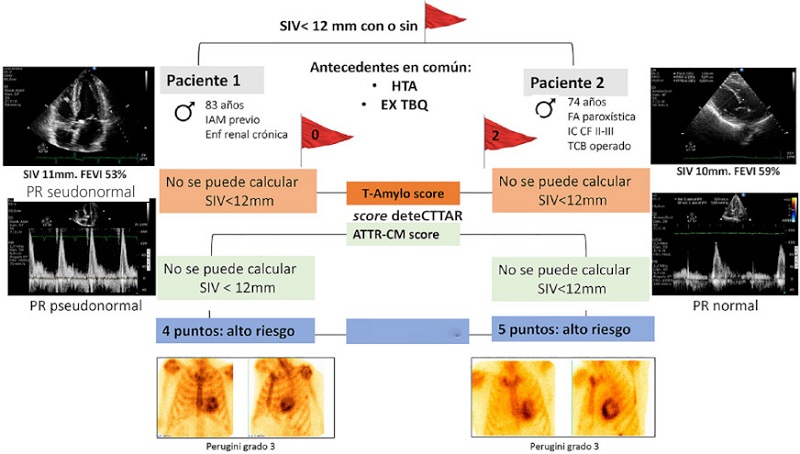
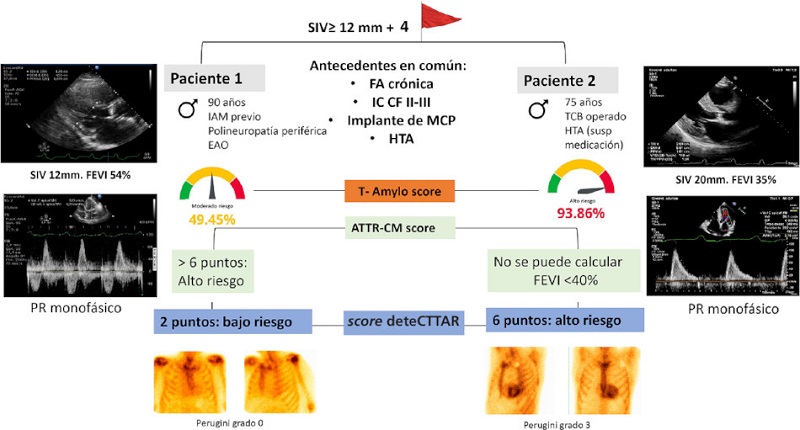
Es sabido que el CC con fosfonatos presenta una alta sensibilidad y especificidad para el diagnóstico no invasivo de AC-TTR. Sin embargo, no existe actualmente acuerdo en la bibliografía acerca de cuándo es apropiado realizarlo.
Algunas guías proponen que debiera llevarse a cabo directamente en ciertos escenarios clínicos, sin necesidad de aplicar escalas de puntuación que determinen el riesgo de cada paciente. Para otras el CC debería solicitarse solo ante la existencia de aumento del espesor del SIV asociada a una o más banderas rojas, IC-FEp o EAo grave. (20,21,22,23)
Si bien entre los pacientes mayores de 65 años con IC-FEp y EAo grave es más frecuente encontrar AC-TTR que en la población general, estas variables no mostraron por sí solas, ser predictores de la enfermedad. (2,3,4,5,24,25,26)
En cuanto al espesor del SIV, no cabe duda de que si está gravemente aumentado, la diferencia que pudiera existir en la medición entre diferentes operadores o equipos no tendría demasiada repercusión. Sin embargo, en valores cercanos a 12mm, un error en la medición (por mala técnica, mala ventana acústica o poca experiencia del operador) según las escalas de puntuación vigentes hasta el momento, significaría descartar la sospecha diagnóstica de AC-TTR.
Previamente a los scores ATTR-CM y T-Amylo, se publicaron otros modelos de predicción pero que, a diferencia de éstos, sólo incluían parámetros ecocardiográficos y/o electrocardiográficos. (27,28) Sin embargo, en nuestro trabajo, la mayoría de las variables incluidas en estos modelos, no resultaron predictores de AC-TTR, a excepción del patrón de relajación y el espesor del SIV.
En cuanto a los antecedentes clínicos, incluidas las banderas rojas tales como disautonomía, polineuropatía periférica, hipotensión-normotensión, etc., el único que mostró relación con el diagnóstico fue padecer TCB.
En nuestro score una puntuación ≥3 aumenta considerablemente el riesgo de padecer AC-TTR, por lo que solo en estos casos estaría indicado realizar un CC con fosfonatos. En aquellos pacientes con un puntaje entre 0-2, no sería necesario realizarlo, debiendo considerarse un diagnóstico alternativo (Fig. 4). Si la sospecha clínica persiste, podría optarse por realizar una resonancia magnética cardíaca, ya que su alto valor predictivo negativo, descartaría finalmente la enfermedad.
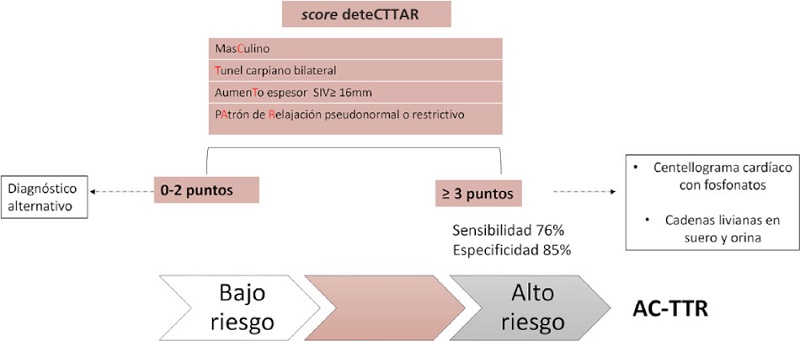
Según nuestra escala, la sola presencia de TCB (3 puntos), sería condición suficiente para solicitar un CC con fosfonatos. En estos casos en particular, debe considerarse el tiempo desde el diagnóstico y/o cirugía, ya que la infiltración del nervio mediano por amiloide suele preceder a la afectación cardiaca en 5 a 9 años. De manera que un CC negativo puede no excluir la enfermedad si fue realizado en forma temprana, por lo que sería adecuado un seguimiento cardiológico estricto. (29)
Debe destacarse que el mayor desafío que encuentran todas las escalas de puntuación para AC-TTR son los pacientes con MCH. En el diagnóstico diferencial con esta entidad, la experiencia del médico a la hora de la sospecha resulta fundamental, ya que la epidemiología, los antecedentes familiares y la mayoría de las veces el electrocardiograma, pueden contribuir a diferenciarlas, sin necesidad de aplicar las escalas.
El score deteCTTAR constituye la primera escala para la predicción de AC-TTR desarrollada con pacientes de nuestro país. Puede ser aplicado en el consultorio a cualquier paciente sin la necesidad de esperar a reunir condiciones (banderas rojas) que puedan demorar el diagnóstico, utilizando datos extraídos del interrogatorio y de un ecocardiograma basal.
El diseño del estudio fue unicéntrico, retrospectivo, con una base de datos relativamente pequeña, por lo que podría existir un sobreajuste del modelo.
El bajo número de pacientes genera que los IC 95% de algunos predictores sean muy amplios, lo cual implica menor precisión en la predicción.
Si bien nuestros datos son alentadores, requieren de una validación externa en el futuro con una muestra mayor de pacientes.
La presencia de un aumento del espesor del SIV asociado a una o más banderas rojas no fue condición necesaria para el diagnóstico de AC-TTR.
El modelo de predicción obtenido permitió desarrollar una escala de puntuación que demostró una alta sensibilidad y especificidad para orientar fuertemente el diagnóstico de AC-TTR.
Una puntuación ≥3 en el score deteCTTAR, aumenta considerablemente el riesgo de padecer AC-TTR.
Dirección para correspondencia: Magali Gobbo. Correo electrónico: magaligobbo28@gmail.com






