EDITORIAL
Nuevas variantes genéticas asociadas a miocardiopatía dilatada adquirida
New Genetic Variants Associated with Acquired Dilated Cardiomyopathy
En 2003 el Proyecto Genoma Humano reveló la primera secuencia del mismo: un “manual de instrucciones” contenido en el ácido desoxirribonucleico (ADN) una molécula presente en el núcleo de todas las células, formado por 4 nucleótidos o bases, citosina (C), guanina (G), timina (T) y adenina (A), en una secuencia de 3300 millones de ellas, que determina el código genético. (1) Así nació la era de la medicina genómica.
Genómica es el estudio científico del ADN. Toda la información para “fabricar” un ser humano y mantener sus funciones representa sólo el 1 % del ADN. Llamamos genes a “segmentos” del ADN con instrucciones para fabricar proteínas. Creemos que los humanos tienen 25000 genes separados por grandes cantidades de ADN intergénico. La genética es el estudio de cada gen.
La tecnología de secuenciación de próxima generación o NGS (Next Generation Sequencing) redujo los costos significativamente y aumento la eficiencia, permitiendo su utilización en lo que hoy se conoce como la era de la medicina postgenómica.
La medicina postgenómica usa información del ADN de miles de individuos de diferentes razas para crear “patrones de referencia” de secuencias “normales”, actualmente basados en datos de población europea.
En 2017, el Proyecto HapMap reveló que los humanos comparten el 99,9 % de la secuencia genética, es decir, son “casi idénticos”.
Existen diferentes tipos de variantes genéticas. La más común es la sustitución de un nucleótido por otro. Si esta variante tiene una frecuencia mayor del 1 % en la población, se denomina variación de nucleótido único, en inglés Single Nucleotide Polymorphism (SNP).
Algunas variaciones genéticas del ADN determinan la apariencia, otras la respuesta a drogas, algunas protegen o predisponen a padecer condiciones, o son directamente responsables de provocar enfermedades. De muchas aún no sabemos su implicancia.
La cardiología genética estudia la asociación entre una variante genética de un paciente o población con la expresión génica o fenotipo. Si la variante se asocia con el fenotipo se demuestra la causalidad genética de la enfermedad. Estas variantes son conocidas como mutaciones; sin embargo la denominación correcta es “variantes genéticas patogénicas”.
Este modelo “gen + mutación= enfermedad” puede seguir un patrón de expresión y de herencia mendeliana autosómica dominante; en este caso un portador de la mutación en general va a desarrollar la enfermedad con diferentes grados de gravedad, y tiene un riesgo del 50% de transmitirla a su descendencia sin importar el sexo. Estas mutaciones son poco frecuentes y son responsables de las enfermedades “monogénicas autosómico dominantes”, las más estudiadas e importantes en cardiología, especialmente dentro del grupo de las miocardiopatías dilatadas genéticas antes llamadas “idiopáticas o no isquémicas”.
Los estudios del genoma o Genome Wide Association Studies (GWAS) incorporaron un paradigma diferente configurado según el esquema del “riesgo poligénico”. Este riesgo contempla muchos SNPs, frecuentes en la población general, en distintos genes que combinados pueden ejercer de manera aditiva gran efecto sobre la expresión de una condición. (2)
La combinación de los efectos de todos estos SNPs capta gran parte de la heredabilidad genética y puede utilizarse para construir modelos de predicción o scores de riesgo poligénico (SRP), los que se consideran una medida cuantitativa de la susceptibilidad genética para calcular una “probabilidad individual”. (Figura 1)
Dado que el genotipo germinal no se modifica, ello excluye la causalidad reversa, indicando que los SRP idealmente representan una medida estable no afectada por la edad ni por el medio ambiente. Pueden calcularse por única vez en cualquier momento y superan muchos obstáculos asociados a otros biomarcadores o modificadores del riesgo. La mayoría incluyen cientos y a veces miles de SNPs.(3)
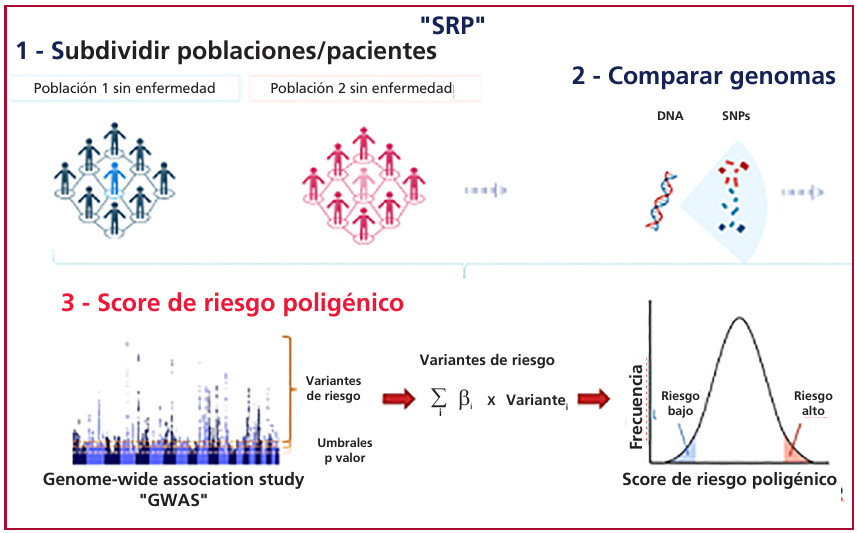
DNA: ácido desoxirribonucleico; GWAS: estudios de asociación del genoma completo; SNP:polimorfismo de nucleótido único; SRP: score de riesgo poligénico
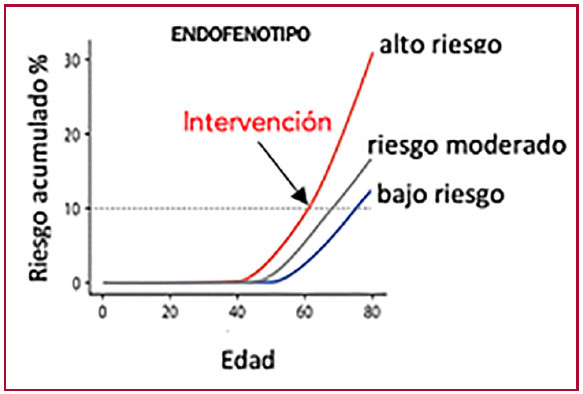
Un SRP ideal permitirá predecir una condición con una variabilidad interindividual acorde con la variabilidad del rasgo estudiado, definiendo el endofenotipo, una posición intermedia en la vía “genotipo-endofenotipo-fenotipo”, reflejo de la predisposición genética individual. Un SRP ideal discrimina los endofenotipos en riesgo bajo, moderado o alto. (4)
Comprender la arquitectura altamente poligénica de trastornos con una complejidad etiológica inherente, como aquellos con gran interacción entre factores ambientales y estilos de vida, puede permitir cambios en estos o un tratamiento farmacológico temprano en quienes presenten un endofenotipo con riesgo elevado. (5) (Figura 2)
El valor de los SRP en prevención secundaria está cobrando mucho interés. (6) Como en el trabajo de Principato y cols. lo es la función sistólica del ventrículo izquierdo, (7) el desafío es que el desenlace con el que se quiere medir el valor pronóstico del score esté definido de manera inequívoca. Los autores utilizan la fracción de eyección, que presenta una alta dependencia tanto de la geometría ventricular como del operador; tal vez en el futuro la valoración mediante resonancia magnética y el uso de la inteligencia artificial pueda mitigar este escollo. Cabe mencionar la importancia de que este trabajo además de incorporar el SRP, incluya algoritmos de inteligencia artificial. Sin embargo, sería deseable ampliar los criterios utilizados en la selección de los SNPs estudiados.
En esta población con etnia del sur de Bolivia y norte argentino es de esperar frecuencias alélicas diversas, cuya consideración a futuro mejoraría la estimación permitiendo ajustar estadísticamente con la información ancestral. (8) Además, la inclusión de otros factores de riesgo como obesidad, tabaquismo, dislipemias, medio socioeconómico y acceso a la atención sanitaria de la población podrían optimizar la uniformidad dentro de la muestra. Se requerirá de nuevos estudios multicéntricos con selección aleatoria de los participantes para una validación externa posterior que evalúe el ajuste del modelo en otras poblaciones, con estrictos criterios de selección de pacientes.
La utilización de los SRP para predecir una propensión causal genéticamente determinada e independiente de los factores de riesgo tradicionales que hasta ahora no han demostrado poder de detección en estadios presintomáticos o preclínicos, está aportando importantes conocimientos a la investigación de las enfermedades cardiovasculares, en especial de las miocardiopatías.
No hay precedentes de estudios de SRP en miocardiopatía chagásica, y ello destaca la importancia de este trabajo, en la intención de la detección precisa de individuos que podrían beneficiarse de una intervención precoz, y la de tener datos locales.
El potencial de los SPR ha llevado recientemente a los documentos de posicionamiento de la American Heart Association (9) y de la European Society of Cardiology. (10) Ambas desaconsejan el uso rutinario de SRP ya que aún existen muchos desafíos. Por ejemplo, los scores actuales solo evalúan SNPs “comunes”, sin investigar el potencial de incluir variantes raras como aquellas responsables de enfermedades monogénicas.
Es fundamental llevar a cabo estudios prospectivos en poblaciones heterogéneas, garantizando el cumplimiento de estrictos estándares de calidad en el procesamiento e informe de datos, con protocolos rigurosos de control y marcos de referencia uniformes, que aseguren la validez y reproducibilidad de los resultados.
La información genética, debido a su lenguaje poco familiar para los cardiólogos es menos intuitiva que cualquiera de los factores de riesgo, datos clínicos o de imágenes tradicionales, pero su correcta incorporación en nuestros modelos de predicción puede influir en la fuerza y la dirección de las decisiones compartidas para mejorar la calidad de la atención médica en la era de la medicina personalizada y de precisión.
Dirección para correspondencia: Marianna Guerchicoff. Correo electrónico: mguerchicofflemcke@gmail.com

DNA: ácido desoxirribonucleico; GWAS: estudios de asociación del genoma completo; SNP:polimorfismo de nucleótido único; SRP: score de riesgo poligénico
