RESUMEN
Introducción: La insuficiencia cardíaca con fracción de eyección ventricular izquierda reducida (FEVIr) es una de las patologías cardiovasculares con mayor mortalidad. La existencia de una predisposición genética para el desarrollo de esta patología ante la presencia de una noxa es aún incierta.
Objetivos: El objetivo de este estudio fue identificar asociaciones entre variantes genéticas en alelos polimórficos, polimorfismos de nucleótido único (SNPs) con la presencia de FEVIr y de trastornos de conducción intraventricular (TCIV), en un modelo de miocardiopatía adquirida como es la chagásica.
Material y métodos: Se incluyó como modelo de estudio a pacientes seropositivos para enfermedad de Chagas con data de infección de más de 20 años, un grupo con FEVIr (FEVI ≤35 %) y otro con FEVI preservada, FEVIp (≥50 %). Se realizó una toma de sangre que fue procesada para la obtención del ácido desoxirribonucleico (ADN), que se envió a un laboratorio in ternacional de genotipado. Se preparó un panel de SNPs de genes utilizando la base internacional The Genome Aggregation Database (GnomAD), eligiendo SNPs con una frecuencia en la población del 10 % al 40 %. Los SNPs elegidos están relacio nados con genes responsables del proceso de contracción y relajación ventricular (TTN, BAG3, MTSS1), el metabolismo mio cárdico (PPARGC1A, SIRT1, AKT1 mTOR, AMPK), receptor adrenérgico beta 1 (ADRB1), receptor colinérgico muscarínico 2 (CHRM2), receptor de angiotensina II tipo 1 (AGTR1B), y el péptido natriurético auricular (NPPA). Mediante diversos modelos de inteligencia artificial para aprendizaje supervisado (Regresión Logística, Máquinas de Vectores de Soporte, Redes Neuronales Artificiales, Naive Bayes, Árboles de Clasificación y Random Forest) se evaluaron 68 SNPs como predictores de la presencia de dos fenotipos: FEVIr, y TCIV. El desempeño de los modelos para la predicción de la FEVIr se evaluó mediante la técnica de validación cruzada (cross-validation), con la métrica F1 como medida de precisión para seleccionar el mejor modelo.
Resultados: Se incluyeron 182 pacientes, con una mediana de edad de 62 años, el 39,6 % hombres. El 31 % presentó FEVIr y el 53 % algún TCIV. El modelo con el mejor desempeño fue la regresión logística (F1 = 0,85), por lo que se la utilizó para ex presar la asociación mediante el Odds Ratio y su IC del 95%. Se observó que las variantes rs2076300, rs61772962 y rs7071853 fueron predictores independientes de reducción de la FEVI, mientras que, para la presencia de TIVC, el único predictor fue el SNP rs72840788. El SNP rs61772962 corresponde al gen PRKAA2, que codifica a la subunidad catalítica alfa-2 de la proteína quinasa activada por 5’-AMP. Por su parte el rs7071853 y el rs72840788 corresponden al gen que codifica a la proteína BAG3 (regulador 3 de chaperona). Finalmente el SNP rs2076300 corresponde al gen DSP que codifica una desmoplaquina, proteína de la placa de unión de los desmosomas.
Conclusiones: En este modelo de derivación, en un conjunto de pacientes con serología positiva para Chagas se identificaron 3 SNPs predictores de reducción de la FEVI y un SNP predictor de TCIV. La reproducibilidad de estos resultados debería ser confirmada en un modelo de validación con una mayor muestra de individuos. Además, este hallazgo podría ser de utilidad en miocardiopatías dilatadas de otras etiologías.
Palabras clave: Miocardiopatìa dilatada, Insuficiencia cardíaca, Genética, Enfermedad de Chagas.
ABSTRACT
Background: Heart failure with reduced left ventricular ejection fraction (HFrEF) is one of the cardiovascular pathologies with the highest mortality. The existence of a genetic predisposition for the development of this pathology in the presence of a noxa is still uncertain.
Objectives: The aim of this study was to identify associations between genetic variants in polymorphic alleles, single nucleotide polymorphisms (SNPs) with the presence of rEF and intraventricular conduction disorders (IVCD) in a model of acquired cardiomyopathy such as chagasic cardiomyopathy.
Methods: A study model including patients seropositive for Chagas disease with a history of infection of more than 20 years, one group with rEF (≤35%) and another group with preserved LVEF (pEF, ≥50%). A blood collection was performed and processed to obtain deoxyribonucleic acid (DNA), which was sent to an international genotyping laboratory. A panel of gene SNPs was prepared using the international TheGenomeAggregationDatabase (GnomAD), choosing SNPs with a frequency in the population of 10% to 40%. The SNPs chosen are related to genes responsible for the process of ventricular contraction and relaxation (TTN, BAG3, MTSS1), myocardial metabolism (PPARGC1A, SIRT1, AKT1 mTOR, AMPK), adrenergic receptor beta 1 (ADRB1), cholinergic receptor muscarinic 2 (CHRM2), angiotensin II type 1 receptor(AGTR1B), and atrial natriuretic peptide (NPPA) Using various artificial intelligence models for supervised learning (Logistic Regression, Support Vector Machines, Artificial Neural Networks, NaiveBayes, Classification Trees, and RandomForest) 68 SNPs were evaluated as predictors of the presence of two phenotypes: rEF, and IVCD. The performance of the models for the prediction of rEF was evaluated by cross-validation technique, with the F1 metric as a measure of accuracy to select the best model.
Results: One hundred and eighty-two patients were included, with a median age of 62 years, 39.6 % men. Thirty-one percent had rEF and 53% had some IVCD. The model with the best performance was logistic regression (F1=0.85), so it was used to express the association by Odds Ratio and its 95% CI. It was observed that the variants rs2076300, rs61772962 and rs7071853 were independent predictors of rEF, whereas the only predictor for IVCD was the SNP rs72840788. The SNP rs61772962 corresponds to the PRKAA2 gene, which encodes the alpha-2 catalytic subunit of 5'-AMP-activated protein kinase. On the other hand, rs7071853 and rs72840788 correspond to the gene encoding the BAG3 protein (chaperone regulator 3). Finally, the SNP rs2076300 corresponds to the DSP gene encoding a desmoplakin, a protein of the desmosome binding plate.
Conclusions: In this derivation model, in a set of patients with positive serology for Chagas disease, 3 SNPs predictive of rEF and one SNP predictive of IVCD were identified. The reproducibility of these results should be confirmed in a validation model with a larger sample of individuals. Furthermore, this finding could be useful in dilated cardiomyopathies of other etiologies.
Key words: Cardiomyopathy, Dilated, Heart Failure, Genetics, Chagas Disease.
ARTÍCULO ORIGINAL
Nuevas variantes genéticas asociadas a miocardiopatía dilatada adquirida. Hacia un nuevo panel poligénico predisponente
New Genetic Variants Associated with Acquired Dilated Cardiomyopathy. Towards a New Predisposing Polygenic Panel
Received: 27 October 2024
Accepted: 03 January 2025
La insuficiencia cardíaca con fracción de eyección ventricular izquierda reducida (FEVIr) representa una de las patologías con mayor mortalidad. Entre sus principales etiologías se destaca la miocardiopatía dilatada (MCD). Los predictores del desarrollo y pronóstico de la MCD están sujetos a continua investigación. A pesar de los avances en el entendimiento de los mecanismos fisiopatológicos subyacentes, las razones por las cuales ciertas condiciones predisponen a la evolución hacia la miocardiopatía dilatada aún no se comprenden completamente. (1)
Se han identificado alteraciones genotípicas (familiares) responsables de un pequeño grupo de casos con el fenotipo de dilatación ventricular.
Un aspecto notable es que la misma noxa puede generar efectos variables entre distintos pacientes. Esto sugiere la posible existencia de una predisposición genética que influiría en una evolución clínica diferenciada. En este contexto, los polimorfismos de nucleótido único (SNPs) podrían desempeñar un papel clave en la variabilidad de la respuesta de los pacientes ante una misma noxa.
Para investigar la existencia de variantes genéticas asociadas con la predisposición a la MCD utilizamos la enfermedad de Chagas como modelo. (2)
La enfermedad de Chagas es responsable de la MCD con mayor morbilidad y mortalidad. Presenta dos fases clínicas: una aguda, que suele ser asintomática en el 95 % de los pacientes, y una fase crónica, con un período de latencia prolongado de 10-30 años. En este grupo, entre el 25% y el 30% de los individuos, desarrollan signos o síntomas de afectación cardíaca (miocardiopatía chagásica). (3)
La miocardiopatía chagásica crónica (MCC) se ha considerado como la causa más frecuente de miocardiopatía no isquémica en Argentina. Sin embargo, no existe consenso sobre los indicadores de riesgo para el desarrollo de esta afección y otros eventos cardiovasculares, independientemente del efecto de los factores de riesgo tradicionales. (4)
El objetivo de nuestro estudio fue determinar las variantes genéticas relacionadas con la presencia de MCD realizando un análisis de asociación con SNPs.
Estudio unicéntrico prospectivo que incluyó pacientes desde junio de 2016 hasta enero de 2020.
Se incluyeron pacientes de 21 a 80 años, seropositivos para enfermedad de Chagas con MCD, provenientes de las provincias del noroeste argentino y sur de Bolivia, y otros serológicamente positivos de edad similar, procedentes de las mismas áreas geográficas sin MCD, como grupo control.
Todos debían contar con una antigüedad conocida por el paciente de la infección de más de 20 años certificada por médico tratante, análisis serológico y abandono del área endémicas por más de 20 años. Los pacientes debían tener una FEVI medida dentro de los 12 meses previos a su inclusión, ≤ 35% o ≥ 50%.
Se excluyeron pacientes que rechazaron firmar el consentimiento informado, aquellos con patologías conocidas graves (excluida la cardiovascular) que generen una expectativa de vida menor a un año, y aquellos que estuvieran participando en protocolos de investigación en los 30 días previos a la toma de la muestra. También se rechazaron aquellos en los que no se podía asegurar su contacto personal o telefónico, aquellos con abuso de alcohol o drogas en los últimos 6 meses, con clínica y laboratorio de insuficiencia hepática (valor de transaminasas x3 y bilirrubina total >2 mg/dL), con FEVI entre 36% y 49 % (el objetivo fue separar los grupos evitando el cruce de pacientes), y los que recibían drogas de conocida acción sobre los parámetros cardiovasculares (inmunosupresores, nitratos, estrógenos). También se excluyó a los pacientes con enfermedad coronaria en etapa aguda o crónica, con indicación de revascularización o con angioplastia coronaria o cirugía de revascularización miocárdica en los 6 meses anteriores, pacientes con insuficiencia renal (creatinina sérica >2,5 gr / dL), con enfermedad pulmonar obstructiva grave, con MCD de otras etiologías (ej.: artritis reumatoidea, diabetes, hipertensión arterial), con enfermedades valvulares significativas (excepto las secundarias a dilatación del anillo valvular mitral y/o tricuspídeo), con marcapasos con estimulación mayor al 50%, o con patologías autoinmunes (lupus, esclerodermia, hepatitis C, etc.).
Los pacientes que cumplieron con los criterios de inclusión y no presentaron criterios de exclusión fueron divididos en 2 grupos:
Grupo 1: pacientes con FEVI ≤ 35%.
Grupo 2: individuos con FEVI ≥ 50%.
Luego de la firma del consentimiento informado se les realizó una historia clínica y examen físico completos, acorde con su patología de base y los procedimientos diagnósticos y pronósticos correspondientes.
Se efectuó un ecocardiograma para confirmar el valor de FEVI y un ECG de 12 derivaciones. Según los resultados del ECG, los pacientes se clasificaron en dos grupos: con trastornos de la conducción intraventricular (TCIV), cuando tenían uno o más de los siguientes criterios: bloqueo de rama derecha, bloqueo de rama izquierda, hemibloqueo anterior izquierdo y hemibloqueo posterior izquierdo; o sin TCIV.
Los pacientes fueron codificados con un sistema alfanumérico para garantizar la identidad de los grupos.
Personal capacitado realizó una toma de sangre de 10 mL para la determinación genómica. La muestra fue colocada en tubos con presencia de ácido etilendiaminotetraacético (EDTA) según normas ISO para evitar su coagulación, y conservada a -20ºC hasta su procesamiento. Esta muestra fue procesada para la obtención del ácido desoxirribonucleico (ADN) correspondiente, en un centro especializado de nuestro país, quedando muestras de seguridad.
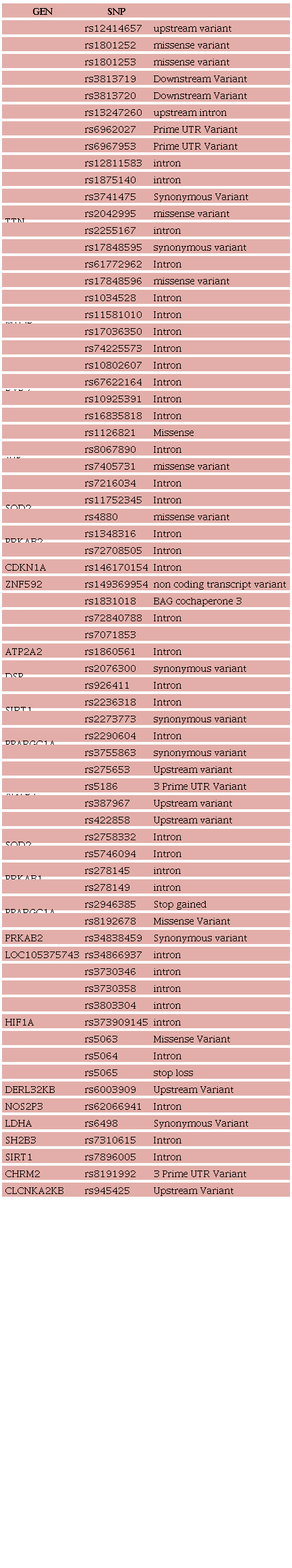
El ADN se envió vía un courier autorizado por legislación internacional a tal fin al laboratorio internacional Xenética Cardiovascular, Instituto de Investigación Sanitaria de Santiago, laboratorio nº1, Complexo Hospitalario Universitario de Santiago de Compostela, donde se realizó el genotipado y su análisis (Tabla 1). El laboratorio permaneció ciego respecto a qué grupo pertenecían los pacientes. Esto era solamente conocido por el equipo estadístico al momento del análisis.
Se preparó un panel de SNPs de genes relacionados con:
El proceso de contracción y relajación ventricular (TTN, BAG3, MTSS1). (5,6,7)
El metabolismo miocárdico (PPARGC1A, SIRT1, AKT1 mTOR, AMPK, PRKAA2).
El receptor colinérgico muscarínico 2 (CHRM2).
El receptor de angiotensina II tipo 1 (AGTR1B).
El péptido natriurético auricular (NPPA).
Reguladores del ciclo celular (CDKN1A, RYR2)
Estructura sarcomérica (ATP2A2, DSP, JUP)
Energía celular (PRKAB2, PRKAB1)
Actividad mitocondrial (SOD 2)
Apoptosis (AKT1)
Regulador de la hipoxia celular (HIF1A)
Cadena respiratoria (LDHA, lactato deshidrogenasa (LDH))
Óxido Nítrico (NOS1, NOS2P3)
Factores de crecimiento e inflamación (SH2B3)
Se utilizó la base internacional The Genome Aggregation Database (GnomAD) eligiendo SNPs con una frecuencia del 10 % al 40 % en la población incorporada a esta base de datos.
Finalmente se seleccionaron 68 SNPs para su análisis, los cuales se hallan detallados en la tabla S1.
La tecnología utilizada fue iPLEX Gold. Se realizó el script en SNPassoc para evaluar si cumplían el estado de equilibrio H-W toda la población.
Se evaluó la asociación entre estos dos fenotipos, como variables binomiales codificadas como SI = 1 y NO = 0, con los SNPs codificados como una variable ordinal según la siguiente convención: 0 para homocigotos del alelo tipo salvaje, 2 para homocigotas del alelo alternativo y 1 para los heterocigotos.
Para la evaluación de la relación entre los diferentes SNPs en estudio y la presencia de una FEVI reducida, se utilizaron diversos modelos de inteligencia artificial para aprendizaje supervisado. Se evaluó el desempeño de 1) Regresión Logística, 2) Máquinas de Vectores de Soporte, 3) Redes neuronales artificiales, 4) Naive Bayes, 5) Árboles de decisión y 6) Random Forest, con la colaboración del equipo de Inteligencia Artificial de genomIT.
La evaluación del desempeño de los distintos modelos para la predicción de la FEVI reducida, se efectuó mediante la técnica de validación cruzada, cross-validation, utilizando la métrica F1 como medida de precisión para seleccionar el mejor modelo.
Para la evaluación de la relación entre cada SNP y la presencia de TCIV se evaluó un modelo de regresión logística univariado con la presencia de FEVI reducida y TCIV como desenlaces y cada SNP como predictor. Se seleccionaron los SNPs con un p valor asociado < 0,05, para la evaluación de su efecto mediante un modelo de regresión logística multivariado, seleccionando aquellos SNPs con un valor p < 0,05, a través de la estrategia backward selection con el método stepwise regression. La magnitud de la asociación entre cada SNP y el desenlace en estudio se expresó como el Odds Ratio y su respectivo intervalo de confianza del 95 % (IC95%). La performance predictiva del modelo fue evaluada usando el área bajo la curva. El mismo procedimiento se aplicó con la utilización de regresión logística de los SNPs con FEVI reducida.
Los análisis se efectuaron con el software R ® (versión 4.1.1, R Development Core Team/R Foundation for Statistical Computing, Vienna, Austria).
Se generó además, un Manhattan plot con los diferentes modelos de herencia para todos los SNPs analizando el nivel nominal de significancia y el nivel de Bonferroni.
Consideraciones éticas: El estudio fue desarrollado según los principios de la Declaración de Helsinki y aprobado por el Comité de Docencia e Investigación de la institución.
Se estudiaron 182 pacientes con serología positiva para Chagas oriundos del sur de Bolivia y Noroeste de Argentina.
La mediana de edad de la población fue de 62 años. El 39,6 % fueron hombres. Cincuenta y siete de ellos (31 %), presentaron FEVIr y 95 (53 %) presentaron algún TCIV (Tabla 1).
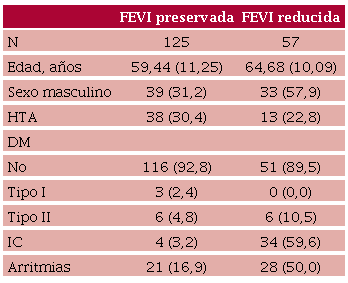
Entre los diferentes modelos de clasificación supervisada evaluados, el modelo que utiliza 7 K folds y un clasificador de Regresión Logística obtuvo una puntuación de F1 = 0,85, y fue el mejor modelo obtenido, por lo que se reportan los resultados obtenidos con el mismo.
El análisis univariado de la relación entre cada SNP (en el eje horizontal) y la presencia de una FEVI reducida y TCIV respectivamente efectuado mediante regresión logística se presenta en las Figuras 1 A y 1 B
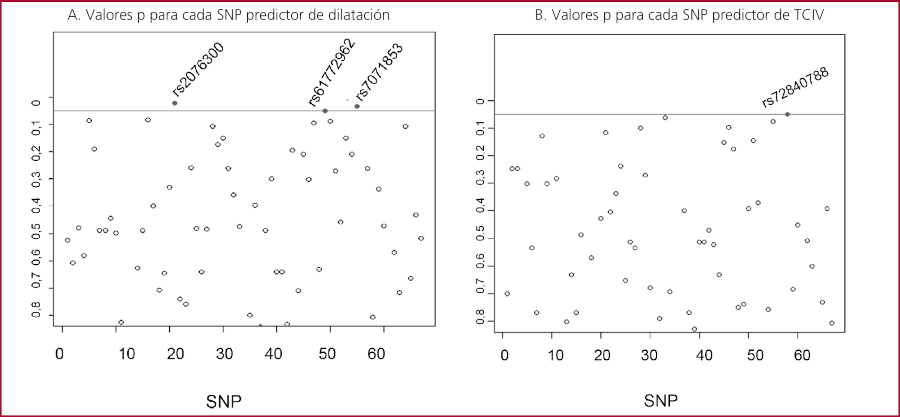
SNP: polimorfismo de nucleótido único; TCIV: trastorno de conducción intraventricular
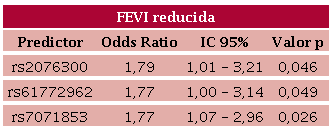
Se realizó un análisis multivariado en el cual se evidencio la asociación con el fenotipo de FEVI reducida y TCIV. (Figuras 2 A y B, Tablas 2 y 3).
Se observó que las variantes rs2076300, rs61772962 y rs7071853 fueron predictores independientes de reducción de la FEVI. Mientras que, para la presencia de bloqueos, el único predictor fue el SNP rs72840788, como se indicó en el análisis univariado.
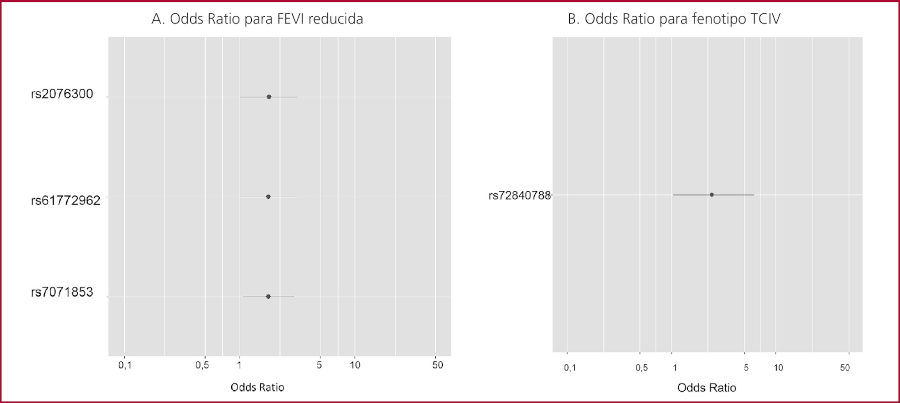
FEVI: fracción de eyección ventricular izquierda; IC 95%: intervalo de confianza del 95%; SNP: polimorfismo de nucleótido único; TCIV: trastorno de conducción intraventricular

En cada uno de los tres SNPs que resultaron predictores de MCD, se analizó la proporción de variantes homocigota salvaje, heterocigota y homocigota del alelo alternativo de cada uno, según la presencia de una FEVI reducida o no y de TCIV. (Figuras 3 A, B y C, Figura 4)
Se evidencia el desempeño predictivo del modelo para la presencia de FEVI reducida mediante el área bajo la curva ROC (0,662) y su IC 95 % (0,580 - 0,745) (Figura 5)
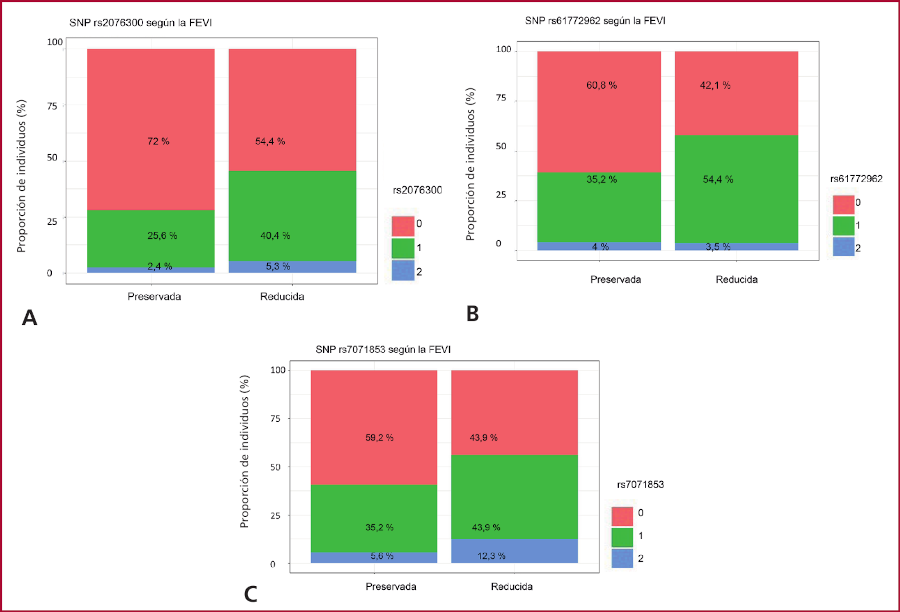
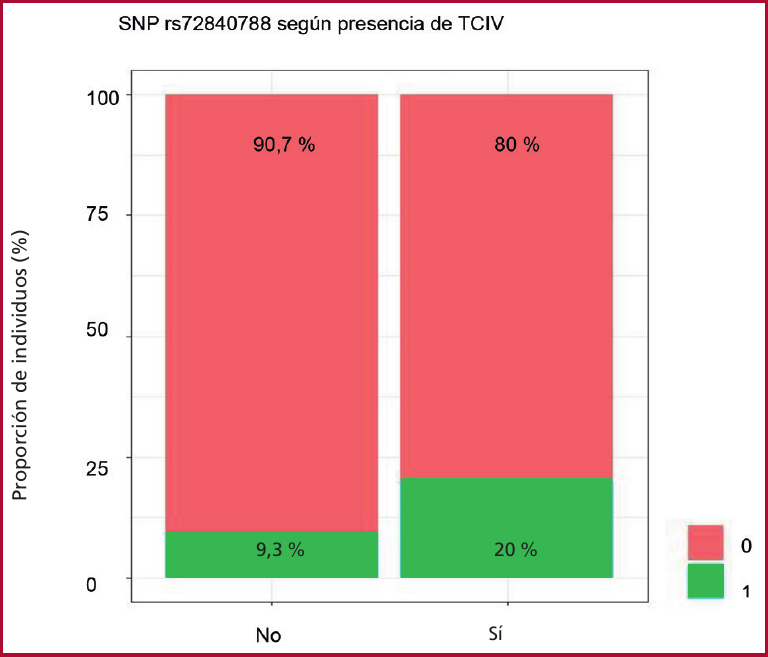
SNP: polimorfismo de nucleótido único 0: homocigotos del alelo tipo salvaje 1: heterocigotos
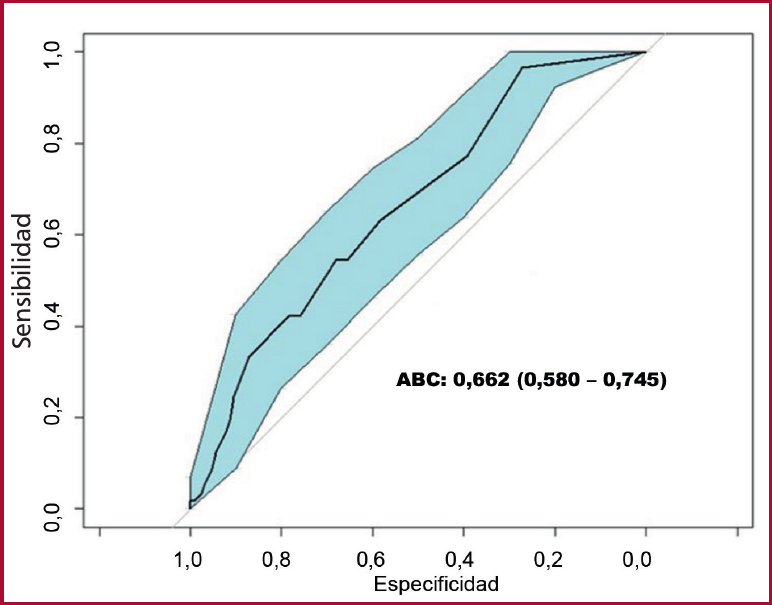
ABC: área bajo la curva; FEVI: fracción de eyección ventricular izquierda; IC 95%: intervalo de confianza del 95%;
Respecto del desempeño de la red neuronal para la predicción de FEVI reducida con los tres SNP identificados, el mejor modelo fue el de una red neuronal con 2 capas ocultas de 6 y 3 neuronas respectivamente, con una tasa de error (proporción de fallas de predicción) de 0,33 y una tasa de exactitud (proporción de aciertos de predicción) de 0,67. (Figura 6)
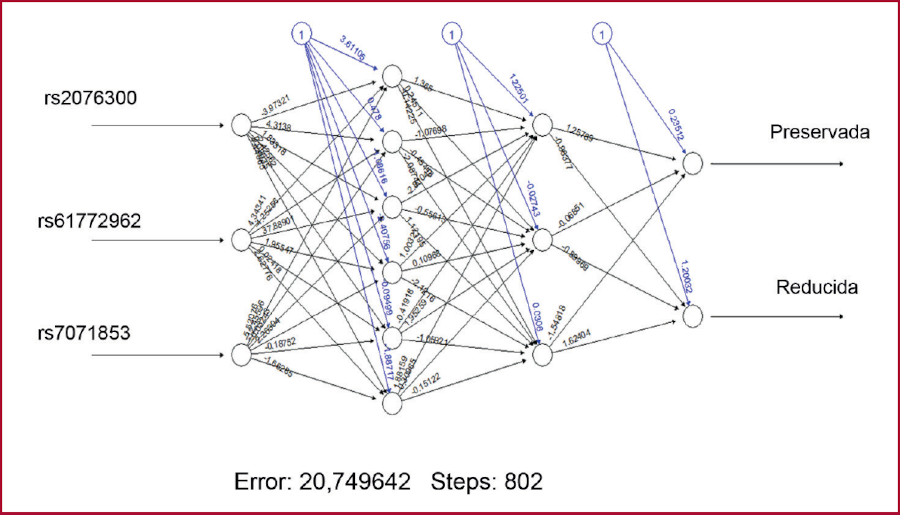
FEVI: fracción de eyección ventricular izquierda SNP: polimorfismo de nucleótido único
La insuficiencia cardíaca (IC) es una enfermedad de proporciones epidémicas, que representa la etapa final de diversas patologías. Su prevalencia se incrementa de dos a tres veces al incluir a los pacientes con disfunción sistólica asintomática. (12,13,14)
Inicialmente, el 60-70% de los pacientes con IC presentaba una alta mortalidad dentro de los cinco años posteriores al diagnóstico, acompañada de una elevada tasa de hospitalización por IC descompensada. Sin embargo, con el advenimiento de nuevos fármacos, se ha evidenciado una significativa disminución de la morbimortalidad. (15,16,17,18,19,20,21)
La IC con FEVIr es un trastorno progresivo que generalmente se inicia después de que una noxa o un evento dañino afecta el músculo cardíaco, resultando en la pérdida de miocitos funcionales o en la disminución de la capacidad contráctil del miocardio. En la mayoría de los casos, inicialmente se presenta una fase asintomática debido a mecanismos compensadores que se activan y modulan la función del VI dentro de límites fisiológicos por un período de tiempo determinado. No obstante, la activación sostenida de los sistemas neurohormonal y de citocinas provoca una serie de cambios en el miocardio, conduciendo al remodelado ventricular y a la eventual aparición de IC sintomática.
Los sistemas neurohumorales incluyen el sistema nervioso simpático (SNS), a través de la activación del receptor Beta 1, y el sistema renina-angiotensina (SRA), mediado por la acción persistente de la angiotensina II (AT2) y la aldosterona sobre el miocardio.
La inhibición parasimpática también contribuye a la patogenia de la IC, al reducir las concentraciones de óxido nítrico (NO) con el consiguiente aumento de la inflamación y remodelado ventricular. (22)
La mayoría de los genes implicados en el desarrollo de MCD e IC participan en los procesos de producción y regulación de energía, así como en la señalización del calcio y la regulación de la transcripción. Los descriptos principalmente son los genes de las proteínas del sarcómero (MYH7, TNNT2, TNNI3, TNNC, TPM1, MYBPC3, TTN, ACTC, MYL3, MYL2), de las proteínas del disco Z (VCL, LDB3, TCAP, MYOZ2), proteínas del citoesqueleto o la membrana celular (DES, DAG1, SGCA, LMNA, FLNC), proteínas del desmosoma (JUP, DSP, DSG2, DSC2, PKP2,RYR2, PLN), del canal de sodio (SCN5A), proteínas metabólicas (PRKAG2, GLA, LAMP2, GAA) y proteínas reguladoras (RMB20, BAG3, TGFB3) entre otros.
Mediante estudios de asociación del genoma completo (GWAS) se han descripto ciertos SNPs asociados con el riesgo de desarrollo de IC.
Uno de los más ampliamente estudiado es la variante responsable del cambio de arginina por glicina (Arg389Gly) en el receptor Beta 1. En la población general, el polimorfismo Arg389Gly no se asoció significativamente con IC, pero en el análisis de subgrupos según la etnia, en los pacientes asiáticos la presencia de Gly389 demostró aumentar un 35% el riesgo de IC en comparación con portadores Arg389 (RR 1,35; IC95%: 1,16-1,57; p <0,001). En un análisis más detallado de subgrupos, se encontró que los homocigotos Arg389 se asociaron con una mejoría de la FEVI en los asiáticos del este (IC95% 1,85-3,40; p <0,001) y población mixta (IC 95% 0,72-2,91; p <0,001); mientras que, entre los pacientes blancos, los homocigotos Arg389 tuvieron una mejora del diámetro sistólico del VI. La mejora fue significativamente mayor que la de los Gly389 (IC 95% 0,04-0,36, p=0,001). (23,24,25,26)
En el caso de genes de renina, se analizaron los polimorfismos del G/AI 9-83 en pacientes con MCD. La forma heterocigota se encontró sólo en 37,5% de los sujetos control. Este estudio no mostró participación de los polimorfismos de renina A/G en la patogénesis de la IC. (27)
Los pacientes con MCD pueden presentar hipertrofia y fibrosis. Se observó una asociación del receptor de angiotensina II tipo 1 y los polimorfismos del gen (AGTR1, A1166C) en la hipertrofia ventricular izquierda (HVI) mediada por la enzima convertidora de angiotensina (ECA) en deportistas de resistencia, por lo que sería una variante para estudiar en el futuro en la MCD. (28)
Por otra parte, en diversos estudios, se ha reportado, en el gen de la Titina (TTN), dos SNPs (rs763361 y rs727088) en el último exón del CD226 que han sido asociados con un incremento en el riesgo de MCD. (29)
Otro gen para considerar es el MMP2. Se analizaron SNPs de este gen para evaluar su asociación con el desarrollo de MCD y se encontraron tres de ellos relacionados tanto con el riesgo de padecerla, como con su peor pronóstico. (30)
Dado que no hay consenso sobre las variantes que podrían predisponer al desarrollo de MCD en respuesta a factores nocivos que afectan al miocardio, decidimos establecer un panel de análisis. Éste incluye estructuras relacionadas tanto con sistemas neurohumorales como con aspectos del metabolismo energético que podrían estar implicados en el desarrollo de MCD. Utilizamos la base internacional The Genome Aggregation Database (GnomAD) eligiendo SNPs con una frecuencia del 10 % al 40 % en la población mundial. Así pues, quedaron los SNPs que se detallan en la Tabla S1.
En nuestro análisis pudimos observar que las variantes rs61772962, rs7071853 y rs2076300 fueron predictoras independientes de reducción de la FEVI en nuestra población de pacientes con miocardiopatía chagásica crónica.
El SNP rs61772962 corresponde a una variante intrónica del gen PRKAA2. Este gen codifica la subunidad catalítica alfa-2 de la proteína quinasa activada por 5'-AMP. Esta proteína, AMPK, es una importante enzima sensora de energía celular. En respuesta al estrés metabólico celular, la AMPK se activa y, por lo tanto, fosforila e inactiva la acetil-CoA carboxilasa (ACC) y la beta-hidroxi beta-metilglutaril-CoA reductasa (HMGCR), enzimas claves involucradas en la regulación de la biosíntesis de novo de ácidos grasos y colesterol. (31) La variante AMPKα2 es necesaria para el metabolismo energético de los cardiomiocitos. (32)
Los genes RNF207 y PRKAA2, conocidos por su participación en los potenciales de acción cardíacos, la homeostasis energética y la morfología, han sido postulados como candidatos de modelos de MCD luego del estudio en canes y seguimiento en humanos. (33)
Las mutaciones dominantes en la subunidad reguladora γ2 de la proteína quinasa activada por AMP (AMPK), codificada por el gen PRKAG2 causan en ratones mutantes miocardiopatía por almacenamiento de glucógeno. (34)
El rs7071853 corresponde al gen de la proteína reguladora BAG3 (posición chr10:119552094 (GRCh38.p14). Por su parte rs72840788 se asoció con la predicción de trastornos de conducción corresponde a la posición intrónica de dicha proteína. La proteína BAG3 desempeña un papel importante en el mantenimiento de la homeostasis miocárdica y en el acoplamiento excitación-contracción y es un mecanismo adaptativo para mantener la homeostasis celular bajo estrés. Se expresa de manera más prominente en el corazón, el músculo esquelético y en muchas formas de cáncer. En el corazón, actúa como acompañante de las proteínas de choque térmico para facilitar la autofagia. Las mutaciones en BAG3 se han asociado con una variedad de fenotipos, incluida la miocardiopatía hipertrófica/restrictiva y la dilatada. (35,36,37,38,39,40,40)
El rs2076300 forma parte del gen DSP que codifica para la desmoplaquina, una proteína calcio dependiente de la familia de las cadherinas esencial para los desmosomas, estructuras multiproteicas involucradas en la comunicación de señales entre las células y en la coordinación de las contracciones del músculo cardíaco. Los desmosomas son uniones intercelulares críticas para la integridad mecánica y eléctrica de los tejidos, particularmente en el miocardio y los tejidos epiteliales. Las mutaciones en el gen DSP se asocian típicamente con la cardiomiopatía arritmogénica. Sin embargo, también pueden causar miocardiopatía dilatada, que se presenta con una mayor incidencia de arritmias ventriculares y un riesgo incrementado de muerte súbita. Este hallazgo es significativo, ya que demuestra que una proporción de pacientes con diagnóstico clínico de miocardiopatía dilatada albergan mutaciones en genes que codifican proteínas de los discos intercalados. (41,42,43,44,45)
Al intentar confirmar estos resultados con otros métodos estadísticos usando el “umbral de Bonferroni” los resultados no pudieron ser reproducibles. Dado que la mayoría de los efectos de un SNP único está en el rango de un 10 a un 15 % de modificación del riesgo basal de presentar un determinado fenotipo, el ajuste de Bonferroni para la evaluación de 70 SNP, conservando el nivel alfa global de 0,05 y una potencia de 80%, determina que el rechazo de la hipótesis nula para cada prueba se podría efectuar solo con un valor p < 0,0007, lo cual implica, bajo el efecto más optimista de un aumento del riesgo del 15 % (RR = 1,15), la necesidad de reclutar de 6280 individuos. Es por ello por lo que creemos que no pudieron confirmarse los resultados con otras pruebas, debido al tamaño de la muestra utilizada.
En este modelo de derivación, en un conjunto de pacientes con serología positiva para Chagas, se identificaron 3 SNPs predictores de reducción de la FEVI (rs2076300, rs61772962 y rs7071853) y uno predictor de trastornos de conducción (SNP rs72840788).
Al intentar confirmar estos resultados con otros métodos estadísticos usando el “umbral de Bonferroni” los resultados no pudieron ser reproducibles, debido al tamaño de la muestra utilizada. Esto refuerza que se debe continuar en esta línea de análisis, incrementando el número de pacientes. Es fundamental continuar explorando la hipótesis de que, incluso en ausencia de antecedentes familiares de MCD y de variantes patogénicas en estudios genéticos, pueden existir polimorfismos que predispongan al desarrollo de dilatación ventricular frente a factores desencadenantes.
Este enfoque resultaría muy útil en el futuro, no solo para identificar con premura los pacientes predispuestos a presentar MCD e IC, sino también para anticiparse en el tratamiento, pudiendo así mejorar tanto la morbilidad como la mortalidad de nuestros pacientes. Creemos que esto podría abrir nuevas perspectivas en farmacogenómica aplicada a la IC.
Este estudio busca ser un punto de partida que promueva futuras investigaciones y estrategias. Su intención es establecer una línea de investigación que, al incorporar un mayor número de pacientes y continuar con el análisis, permita alcanzar un mayor poder estadístico.
Dirección para correspondencia: Mario B. Principato. Correo electrónico: mbprincipato@yahoo.com.ar


SNP: polimorfismo de nucleótido único; TCIV: trastorno de conducción intraventricular

FEVI: fracción de eyección ventricular izquierda; IC 95%: intervalo de confianza del 95%; SNP: polimorfismo de nucleótido único; TCIV: trastorno de conducción intraventricular




SNP: polimorfismo de nucleótido único 0: homocigotos del alelo tipo salvaje 1: heterocigotos

ABC: área bajo la curva; FEVI: fracción de eyección ventricular izquierda; IC 95%: intervalo de confianza del 95%;

FEVI: fracción de eyección ventricular izquierda SNP: polimorfismo de nucleótido único
