IMÁGENES EN CARDIOLOGÍA
Aorta shaggy: sustrato ideal para la fatalidad
Shaggy Aorta: Ideal Substrate for Disaster
La aorta, así como los vasos de mediano y pequeño calibre, es susceptible de desarrollar aterosclerosis debido a una combinación de factores adquiridos, hereditarios, relacionados con el sexo y la edad. Además de obstruir mecánicamente el flujo sanguíneo, la placa ateromatosa plantea riesgos de rotura que conducen a una trombosis vascular obstructiva o embólica. La aorta shaggy (AS), término inglés que se traduce como desgreñado, enmarañado, peludo, representa una manifestación extrema de la aterosclerosis aórtica, caracterizada por una enfermedad ateromatosa, extendida y grave que presenta úlceras dispersas, restos blandos débilmente adheridos, una capa arterial media debilitada y tendencia a la formación de trombos. 1 Aunque la etiología precisa de la mayor vulnerabilidad de la aorta continúa sin ser clara, se cree que implica complejas interacciones entre los patrones hidrodinámicos que afectan a la aorta y la predisposición genética a la aterogénesis. 2 La importancia clínica de esta patología radica en los diversos síndromes que pueden desarrollarse a partir de su etiopatogenia, que generan una gran morbilidad y mortalidad en los individuos afectados, y en su papel como factor de riesgo de mortalidad operatoria. El avance de las herramientas diagnósticas subraya la importancia de la multimodalidad de imágenes para lograr diagnósticos oportunos y precisos, y facilitar la toma de decisiones adecuadas en el manejo del paciente. En este contexto, presentamos tres casos clínicos que ejemplifican la naturaleza de esta enfermedad y el espectro de diferentes síndromes asociados a la AS. También destacamos las diversas herramientas de imagen que nos permitieron realizar el diagnóstico y su manejo.
Caso 1: Una paciente de 80 años ingresó en urgencias por presentar durante 3 días un dolor torácico retroesternal opresivo, intenso y autolimitado, asociado a palpitaciones y síntomas neurovegetativos, tras un esfuerzo físico moderado. La historia clínica incluía hipertensión y dislipidemia.
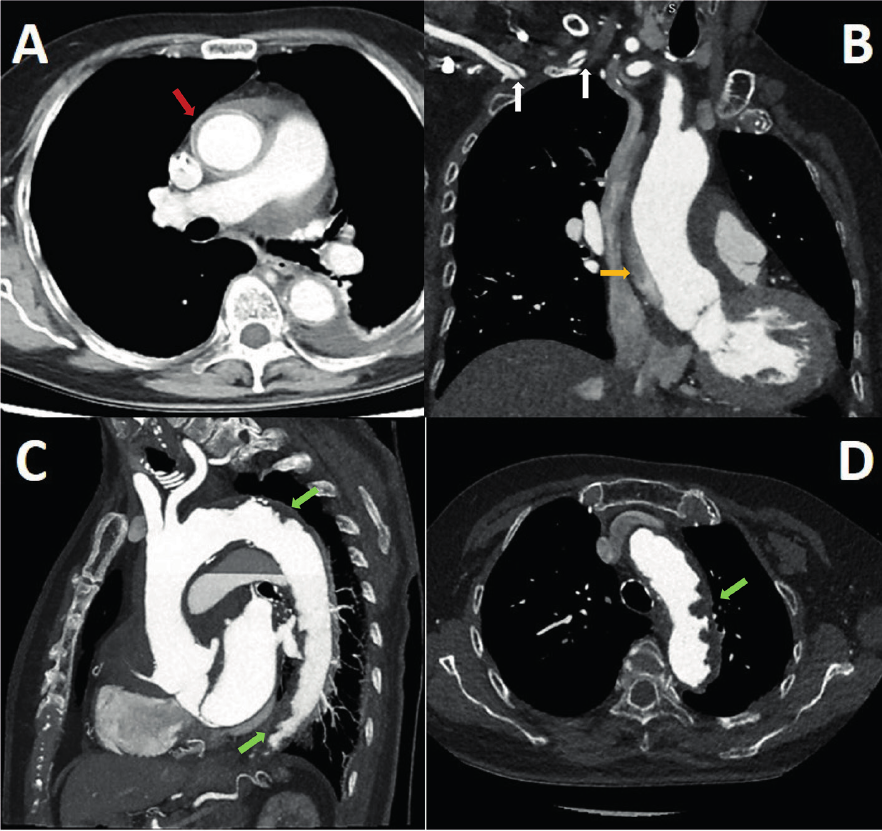
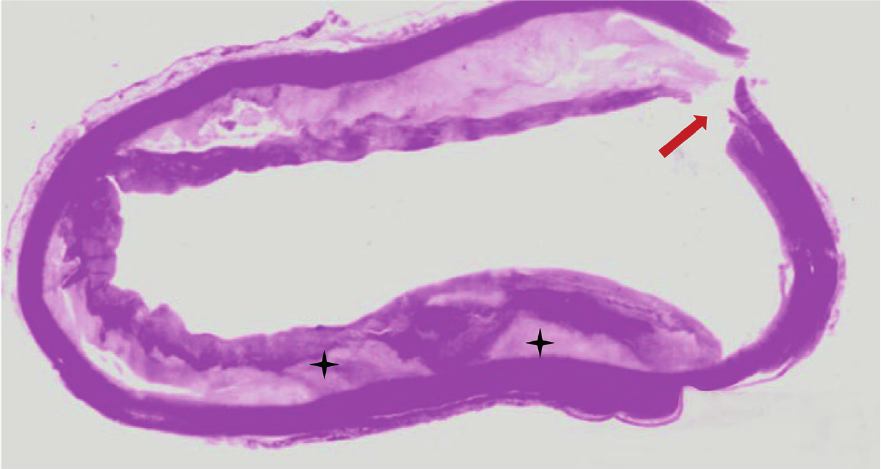
En la exploración física, la paciente estaba taquicárdica con todas las demás constantes vitales conservadas. La auscultación cardíaca reveló ruidos rítmicos de intensidad conservada sin soplos ni ruidos agregados. Además, no se encontró ingurgitación yugular ni reflujo hepatoyugular. El electrocardiograma reveló ritmo sinusal con elevación del segmento ST > 1 mm en V1-V4 y ondas T bifásicas de V1-V4 . Las pruebas de laboratorio revelaron elevación de troponina I de 3113 ng/mL (VN <0,028 ng/mL). La paciente fue ingresada con el diagnóstico de infarto anterior de 3 días de evolución. Durante su hospitalización desarrolló recrudecimiento del dolor torácico asociado a inversión de ondas T en derivaciones precordiales (V1-V6) y nueva movilización de troponina, por lo que se realizó angiografía. Durante el intento de canulación de la arteria coronaria izquierda, con un catéter JL 3.5 5F, se detectó retención de contraste en la aorta ascendente. La angiotomografía mostró doble luz en la aorta ascendente con presencia de colgajo de disección en la unión sinotubular (sin comprometer el ostium de las arterias coronarias) con trayectoria ascendente hasta el arco aórtico proximal (Figura 1), con extensión por el tronco braquiocefálico hasta el segmento proximal de la arteria subclavia (a nivel de la cabeza humeral). También se observó ateromatosis difusa en el arco aórtico con una imagen sugestiva de trombo intraluminal. Se realizó un diagnóstico de aorta shaggy, disección aórtica Stanford “A”, y disección del tronco braquiocefálico y de la arteria subclavia derecha. Se indicó tratamiento quirúrgico de urgencia, pero lamentablemente la paciente falleció durante la intervención. Se realizó un estudio histopatológico de la aorta ascendente afectada (Figura 2), que mostró ateromatosis circunferencial y el colgajo de entrada de la disección aórtica.
Caso 2: Se presentó un hombre de 76 años con antecedentes de hipertensión arterial, tabaquismo, aleteo auricular, aneurisma de aorta abdominal tratado con bypass aortofemoral bilateral, que refería claudicación intermitente de miembros inferiores a predominio izquierdo al caminar menos de 100 metros (estadio IV, según la clasificación de Fontaine). Fue ingresado de forma ambulatoria para revascularización periférica.
En el examen físico presentó signos vitales conservados, extremidades inferiores adelgazadas, frías, pálidas y con cambios tróficos. En la auscultación cardíaca los ruidos eran arrítmicos, de buena intensidad, asociados a un soplo holosistólico III/VI localizado en foco mitral, irradiado a axila. La exploración vascular reveló ambos pulsos femorales conservados; sin embargo, los pulsos de las arterias poplítea, tibial posterior y pedia estuvieron ausentes bilateralmente. El resto de la exploración física fue normal. El electrocardiograma mostró ritmo de aleteo auricular, bloqueo completo de rama izquierda y extrasístoles ventriculares. La evaluación prequirúrgica se complementó con ecocardiografía transesofágica (ETE) debido a la mala ventana acústica en el abordaje transtorácico. Los hallazgos relevantes fueron disfunción sistólica biventricular (fracción de eyección ventricular izquierda, FEVI, 38%, y fracción de cambio de área del ventrículo derecho, CAF, 29%) debida a hipoquinesia global difusa, dilatación de ambas aurículas (volumen de la aurícula izquierda 54 mL/m2, área de la aurícula derecha 20 cm2) e insuficiencia mitral severa (área del orificio regurgitante efectivo 0,4 cm2, volumen regurgitante 65 ml, fracción regurgitante 68%). Asimismo, la evaluación de la aorta mostró múltiples placas ateromatosas complejas distribuidas circunferencialmente, que se extendían desde el arco aórtico hasta la aorta descendente (Figura 3). La angiotomografía aórtica mostró múltiples placas de ateroma ulceradas dispuestas en tándem a lo largo de todo el arco aórtico y la aorta descendente, asociadas a imágenes de baja atenuación sugestivas de trombos (Figura 4). Las arterias ilíacas comunes presentaban múltiples placas calcificadas internas y externas que condicionaban estenosis severas predominantemente a la izquierda y bypass aortofemoral permeable.
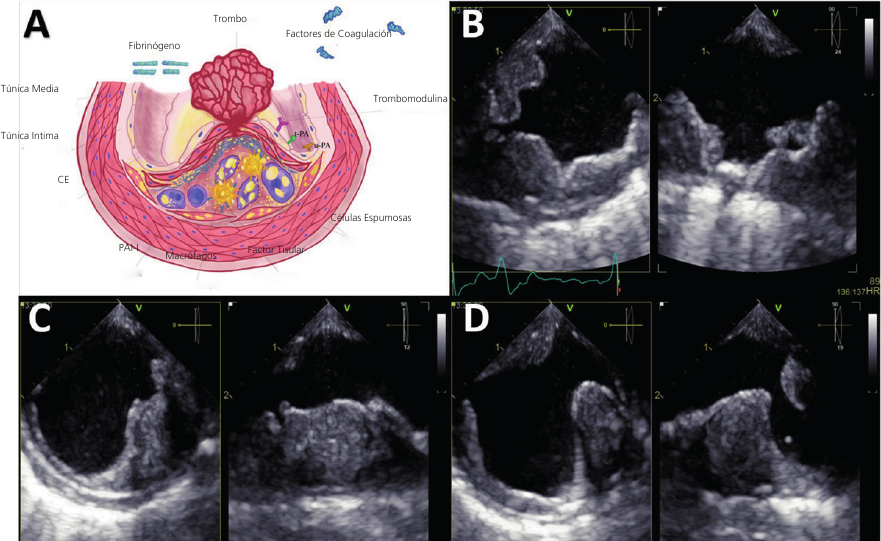
CE: célula endotelial; PAI-1: inhibidor del activador del plasminógeno tipo 1; t-PA: activador del plasminógeno de tipo tisular; u-PA: activador del plasminógeno de tipo urocinasa.
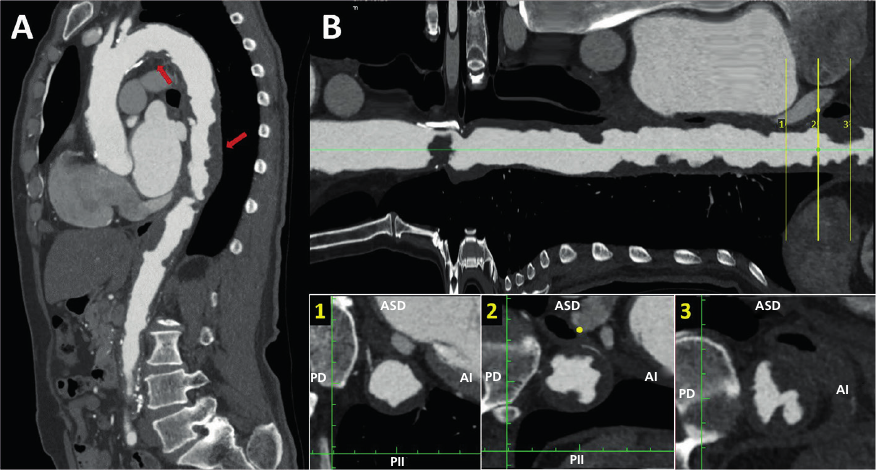
AI: anterior izquierdo; ASD: anterior y superior derecho: PD: posterior derecho; PII: posterior e inferior izquierdo; UH: unidades Hounsfield.
Debido a estos hallazgos, se decidió revascularización coronaria y reemplazo valvular mitral con posterior revascularización periférica. Sin embargo, el paciente no toleró la cirugía cardíaca y falleció durante el procedimiento.
Caso 3: Un paciente varón de 84 años ingresó en urgencias con diarrea aguda asociada a dolor abdominal difuso intenso. Su historia clínica incluía hipertensión, diabetes mellitus, enfermedad renal crónica y demencia senil.
El examen físico reveló taquicardia, piel pálida y terrosa, sudoración y relleno capilar >2 seg. Los ruidos cardiacos eran rítmicos y taquicárdicos, y no se identificaron soplos. En la auscultación pulmonar, el murmullo vesicular estaba conservado en ambos campos pulmonares. Las pruebas de laboratorio mostraron anemia grave (Hb: 6,9 mg/dL), leucocitosis con desviación a la izquierda, azotemia elevada (creatinina: 3,11 mg/dL, urea: 134 mg/dL) e hiperlactacidemia. Se solicitó una angiotomografía toracoabdominal, y se encontró una AS con calcificación parietal grave asociada a un aneurisma de aorta abdominal de hasta 85 mm, con presencia de trombosis mural (Figura 5). Se sospechó isquemia mesentérica, con fuente embolígena procedente de placas aórticas ateromatosas complejas o aneurisma aórtico abdominal. El paciente ingresó en el quirófano para una laparotomía exploratoria. Sin embargo, falleció durante el procedimiento quirúrgico.
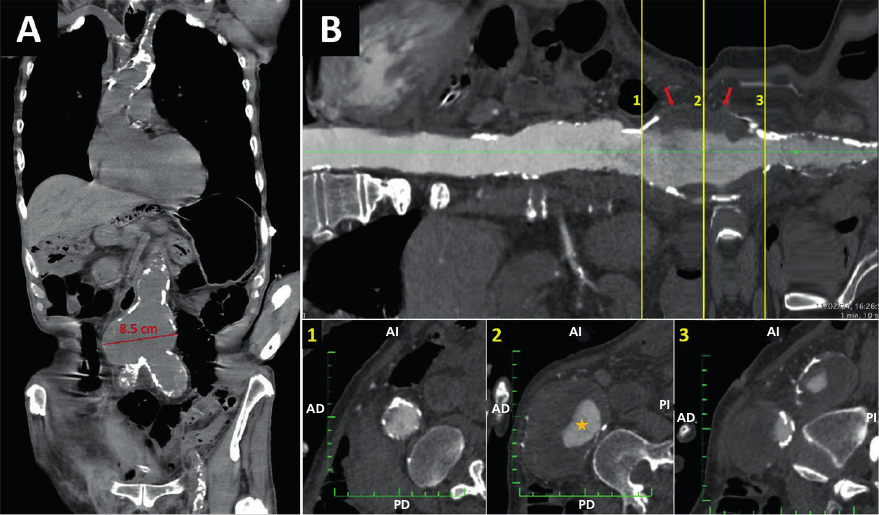
AD: anterior derecho; AI: anterior izquierdo; PD: posterior derecho; PI: posterior izquierdo.
La definición uniforme de la AS no se ha establecido claramente debido a los diferentes métodos diagnósticos utilizados. Sin embargo, se han postulado algunas definiciones. Aorta shaggy es un término descriptivo que se ha utilizado para los segmentos aórticos ateroscleróticos, que muestran irregularidad localizada o difusa e imágenes obstructivas y espiculadas típicas que se visualizan en diferentes herramientas diagnósticas. El aspecto shaggy se debe a complicaciones en forma de ulceraciones multifocales, calcificación y/o trombos superpuestos. 3 Otra definición utilizada para la AS es la aparición de una especie de pelusa similar al cáñamo en la superficie interna de la aorta debido a lesiones ateroscleróticas difusas graves. Clínicamente, suele referirse a un hallazgo de imagen de tomografía computarizada (TC) con contraste o ecografía. 1
Se desconoce la prevalencia e incidencia de la AS en la población general. Sin embargo, existen algunos informes en ciertos grupos de riesgo. Así, en un estudio se observó que 48/447 pacientes (11%) sometidos a reparación electiva de aneurisma aórtico abdominal presentaban AS. Igualmente, la incidencia de complicaciones graves y mortalidad fue 4,1 veces superior en los pacientes con AS que en los pacientes sin aorta aterosclerótica grave. 4 En otro estudio, se observó que la prevalencia de AS en los pacientes sometidos a reemplazo total del arco aórtico era del 19%. 5 Asimismo, se ha observado que la mayoría de los pacientes con AS son ancianos, predominantemente varones, con afecciones comórbidas como hipertensión, diabetes mellitus, enfermedad pulmonar obstructiva crónica, arteriopatía coronaria y periférica y accidente cerebrovascular. 3
La degeneración aterosclerótica grave de la aorta es un proceso multifactorial en el que intervienen diversos factores de riesgo modificables y del propio organismo (no modificables). Se desconoce el acontecimiento inicial que da lugar a la formación del ateroma; sin embargo, la hipótesis de la “respuesta a la lesión” considera la aterosclerosis como una respuesta crónica de inflamación y cicatrización en la pared arterial tras una lesión endotelial con posterior evolución del ateroma debido a la interacción de lipoproteínas modificadas, el sistema inmunitario y las células lisas de la pared arterial. 6
Tras la acumulación de partículas de lipoproteínas en el espacio subintimal y su unión a proteoglicanos, estas partículas se ven afectadas por el estrés oxidativo (oxidación y glicación). Estas lipoproteínas modificadas inducen la síntesis de citoquinas que promueven la quimiotaxis de células inflamatorias (monocitos y linfocitos T), fagocitando este material. Estos macrófagos (células espumosas) son fuente de nuevos mediadores que favorecen la migración de células musculares lisas hacia la íntima, las cuales son responsables de la elaboración de la matriz extracelular que se acumula dentro de la placa aterosclerótica, permitiendo su crecimiento. 2
La heterogeneidad espacial de las lesiones ateroscleróticas en pacientes con AS ha sido difícil de explicar. Se cree que no sólo es el resultado de una respuesta a los diferentes patrones hidrodinámicos que afectan a la aorta (el flujo laminar pulsátil normal genera una mayor fuerza de cizallamiento que se asocia a una menor aterogenicidad), sino también de una predisposición genética específica del individuo. Así, aquellos con mayor expresión de genes que codifican las enzimas superóxido dismutasa, óxido nítrico sintasa y el factor 2 de tipo Kruppel están menos predispuestos a la degeneración aterosclerótica grave, al reducir la formación de radicales libres de oxígeno, inhibir el NF-kB (proinflamatorio) y favorecer la vasodilatación. 2
La importancia clínica de esta patología radica en los diversos síndromes que pueden desarrollarse a partir de su etiopatogenia, los cuales generan una gran morbimortalidad en los individuos afectados. Así, la presencia de degeneración aterosclerótica severa en la aorta se asociará a un mayor riesgo de desarrollar aneurismas aórticos, disección aórtica, tromboembolismo o embolización ateromatosa periférica (al aparato digestivo, renal, médula espinal o miembros periféricos), manifestada como síndrome AS, accidente cerebrovascular isquémico y úlcera aterosclerótica penetrante. 7 (Ilustración central). Asimismo, la AS es un factor de riesgo independiente y significativo de mortalidad operatoria.
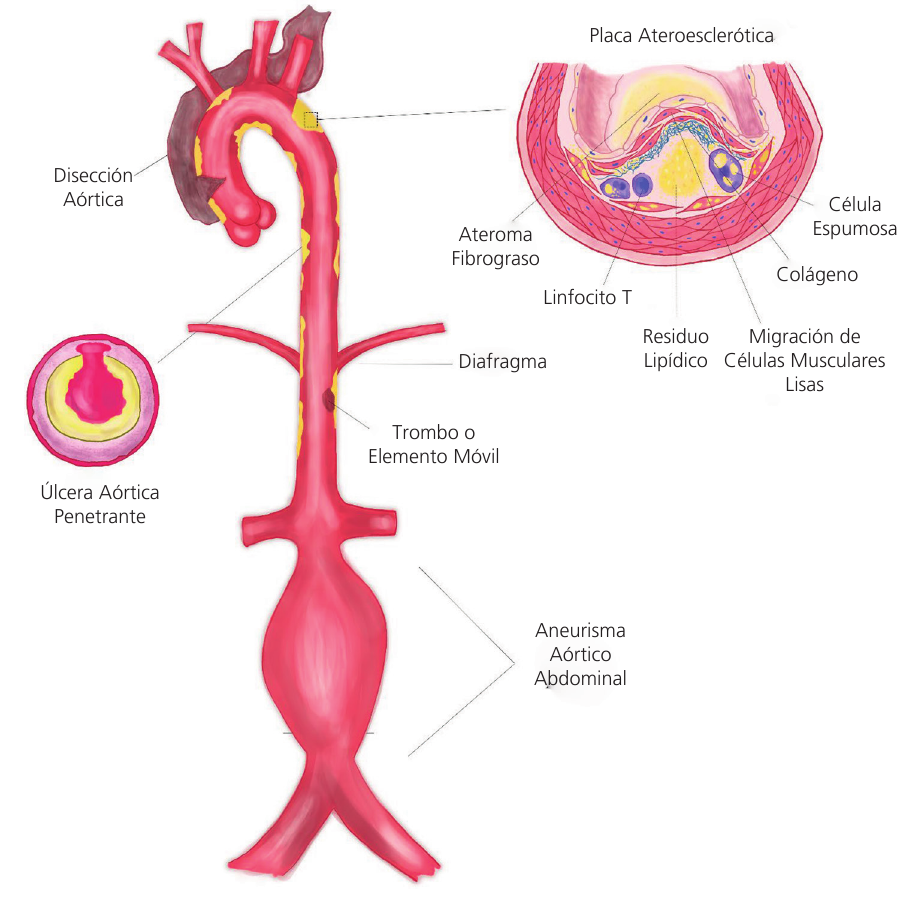
La predisposición al desarrollo de aneurismas y disección aórtica tiene una base multifactorial en la que intervienen la inflamación crónica y la isquemia de la pared aórtica, que generan remodelado y aumento de la susceptibilidad. La presencia de aterosclerosis grave se asocia a una mayor expresión local de proteinasas que contribuyen a la destrucción tisular, la necrosis celular y la apoptosis. 8,9 Por otra parte, el aporte sanguíneo de la aorta se realiza por difusión simple (2/3 interno) y a través de los vasa vasorum (1/3 externo), excepto en la aorta infrarrenal, que carece de un aporte vascular independiente, 10 por lo que la presencia de ateromas favorece la isquemia de la media con la consiguiente apoptosis de las células musculares lisas y debilitamiento de la pared. 11 Este fenómeno, junto con un estímulo estresante simultáneo que supera la resistencia de la pared aórtica, aumenta la susceptibilidad al desarrollo de aneurismas y/o disección aórtica.
Otro de los síndromes asociados a la AS es la embolia, central o periférica, de trombos o cristales de colesterol. La estabilidad de la placa será el resultado del equilibrio entre la resistencia mecánica y las fuerzas que afectan al revestimiento. Así, las placas inestables se caracterizarán por la presencia de una fina placa fibrosa, con escasas células musculares lisas, que recubre un gran núcleo lipídico con abundantes células espumosas y factor tisular. 12 La fractura de la vaina expondrá el factor tisular del ateroma a las proteínas de coagulación sanguínea, iniciándose así la cascada de la coagulación y la formación de trombos ricos en fibrina (Figura 4), que embolizarán al cerebro o a órganos periféricos. Asimismo, la exposición de cristales de colesterol, contenidos en el núcleo lipídico, puede embolizar hacia los órganos periféricos o las extremidades dando lugar al síndrome de AS (embolización ateromatosa difusa). 13
Las úlceras ateroscleróticas penetrantes (UAP) están causadas por la ulceración de la placa aterosclerótica con extensión a la media produciendo una excrecencia en forma de hongo. Se presentan como lesiones unifocales o multifocales en aortas difusamente ateroscleróticas, sobre todo en la porción media y el tercio distal de la aorta descendente. Su diagnóstico a tiempo es esencial, ya que las UAP grandes (> 20 mm), con una profundidad superior a 10 mm, son responsables del 2-7% de los casos de síndrome aórtico agudo. 3,14
A la hora de evaluar la patología aórtica, el método de elección dependerá de la sospecha diagnóstica, las comorbilidades del paciente y la disponibilidad del método. Entre ellos se incluyen la ecocardiografía transtorácica (ETT), la ETE, la TC y la resonancia magnética (RM). Generalmente se utilizará más de una herramienta diagnóstica, destacando la importancia de la multimodalidad para un correcto diagnóstico, y su elección dependerá de la individualización de cada caso.
La ETT permite visualizar la raíz aórtica, la unión sinotubular (UST), la aorta ascendente (AoA), la porción distal del arco y la porción proximal de la aorta descendente (AoD). Sin embargo, esto está limitado por la ventana acústica de cada paciente. En cambio, la ETE permite visualizar, con mayor resolución espacial, de la AoA, el arco aórtico y la AoD torácica, con la excepción de un “punto ciego” situado en la unión de la AoA y el arco aórtico. 15 La mayor resolución espacial se debe a la proximidad del transductor esofágico a la aorta y a la mayor frecuencia de onda. Por este motivo, la ETE es la modalidad de imagen de elección para diagnosticar placas en la aorta torácica y especificar sus características morfoestructurales. 15 Así, la placa aórtica se define como un engrosamiento irregular de al menos 2 mm de grosor con aumento de la ecogenicidad respecto a la superficie intimal adyacente. Una placa aórtica compleja, definida por un grosor ≥4 mm, ulcerada o con componente móvil, está asociado con un aumento del riesgo de enventos cardiovasculares o cerebrovasculares y mortalidad. 16
La TC permite visualizar la aorta en su totalidad, detectar placas calcificadas, tortuosidad, aneurisma y evaluar los órganos adyacentes. La visualización de la luz requiere el uso de medios de contraste, que permiten definir con exactitud la pared aórtica, realizar mediciones precisas, identificar y caracterizar las placas aórticas, así como sus complicaciones (trombos endoluminales y las diferentes formas de síndrome aórtico agudo). 16 Por ello, ante la sospecha de síndrome aórtico agudo, se lo considera el primer estudio diagnóstico, siempre y cuando esté contrastado y gatillado. Sus principales limitaciones radican en el uso de radiación y contraste yodado.
La RM caracteriza perfectamente la composición de la placa aórtica (casquete fibroso y núcleo lipídico) e identifica trombos adheridos a la placa. 17 Su capacidad diagnóstica es superior a la ETE, sobre todo en AoA y el arco; sin embargo, la ETE tiene mejor calidad de imagen en lo que se refiere a la aorta descendente. 18 Además, permite valorar la función cardiaca y valvular, información de interés en la patología aórtica. A pesar de estas ventajas, su elevado coste, limitada disponibilidad, mayor tiempo de adquisición y el uso ocasional de contraste, la convierten en un método poco recomendable para el diagnóstico y seguimiento.
Aunque no existe una indicación clara para el tratamiento aórtico endovascular de la aorta abdominal o torácica en pacientes con AS, sabemos que estos pacientes presentan un mayor riesgo de embolización y de desarrollo de complicaciones aórticas agudas y crónicas. La evidencia sugiere que la endarterectomía ''profiláctica'' de una aorta aterosclerótica grave por ateroma protruyente como complemento de un procedimiento cardiaco no está recomendada debido a la alta incidencia de accidente cerebrovascular intraoperatorio. 19 No obstante, los pacientes con embolización periférica o visceral recurrente y presencia de aorta Shaggy con características anatómicas favorables para la reperfusión endovascular pueden someterse a dicho tratamiento (clase de recomendación IIb, nivel de evidencia C). 20 Por otro lado, el tratamiento de las complicaciones asociadas a la AS queda fuera del alcance de esta revisión.
La AS se refiere a la degeneración aterosclerótica grave de la superficie aórtica, que es extremadamente friable y predispone a diversas complicaciones, como aneurismas, síndromes aórticos agudos y embolización periférica. Se desconoce la incidencia y prevalencia de la AS en la población mundial, pero se calcula que es del 10-20%. Las bases fundamentales para el desarrollo de la AS y sus complicaciones son la inflamación crónica, la isquemia, el estrés de cizallamiento de la pared aórtica y la susceptibilidad genética individual. Por otro lado, la multimodalidad de imágenes es esencial para la oportuna y correcta identificación y caracterización de las placas ateroscleróticas aórticas, especialmente las complejas, que son típicas de la AS. Cada una de estas herramientas diagnósticas tiene unas características que favorecen o limitan su utilidad. Finalmente, no existe consenso en cuanto al manejo intervencionista o quirúrgico de la AS, pero su hallazgo constituye un importante factor de riesgo de mortalidad operatoria y a largo plazo.
Dirección para correspondencia: Kevin Velarde-Acosta Email: kevin_velarde.93@hotmail.com



CE: célula endotelial; PAI-1: inhibidor del activador del plasminógeno tipo 1; t-PA: activador del plasminógeno de tipo tisular; u-PA: activador del plasminógeno de tipo urocinasa.

AI: anterior izquierdo; ASD: anterior y superior derecho: PD: posterior derecho; PII: posterior e inferior izquierdo; UH: unidades Hounsfield.

AD: anterior derecho; AI: anterior izquierdo; PD: posterior derecho; PI: posterior izquierdo.
