CARTA AL EDITOR
Miocardiopatía y enfermedad coronaria obstructiva: ¿causalidad o casualidad?
Cardiomyopathy and Obstructive Coronary Artery Disease: Causality or Chance?
Miocardiopatía y enfermedad coronaria obstructiva: ¿causalidad o casualidad?
Revista argentina de cardiología, vol. 93, no. 1, pp. 69-72, 2025
Sociedad Argentina de Cardiología
Received: 20 October 2024
Accepted: 28 November 2024
La detección de enfermedad coronaria es esencial en el estudio de pacientes con miocardiopatía dilatada y es una práctica común en nuestro entorno. Sin embargo, es importante destacar que la presencia de enfermedad coronaria obstructiva, incluso cuando es extensa, no necesariamente indica que la miocardiopatía sea isquémico-necrótica. Puede tratarse simplemente de una coexistencia sin relación causal. (1)
Bawaskar et al. publicaron recientemente un registro que incluyó a 3023 pacientes que se sometieron a una resonancia magnética cardíaca tras la documentación de enfermedad coronaria obstructiva mediante coronariografía (estenosis ?αμπ;#8805;70 % en ?αμπ;#8805;1 de las arterias descendente anterior, circunfleja, coronaria derecha, o estenosis ?αμπ;#8805;50 % en el tronco de la arteria coronaria izquierda). En este estudio, el 9,3 % de los pacientes presentaban miocardiopatía no coronaria, y este subgrupo mostró un mayor riesgo de eventos cardiovasculares durante el seguimiento. (2)
ESTUDIOS QUE EVALUARON REVASCULARIZACIÓN EN MIOCARDIOPATÍA ISQUÉMICA
En el estudio STICH, publicado en 2011, pacientes con fracción de eyección del ventrículo izquierdo (FEVI) menor o igual al 35 % y enfermedad coronaria extensa revascularizable por cirugía, fueron asignados aleatoriamente a cirugía de revascularización frente a tratamiento médico, sin encontrarse diferencias significativas en la mortalidad por cualquier causa a los 56 meses. (3) Entre las posibles causas de la falta de respuesta a la revascularización identificadas en el subestudio de viabilidad, se encontraron la utilización de métodos diferentes a la resonancia magnética cardíaca (RMC) para la evaluación de la viabilidad, y la probable inclusión de pacientes con remodelado ventricular con baja probabilidad de reversibilidad, evidenciada por los elevados volúmenes ventriculares registrados. (4)
En el estudio REVIVED, publicado en 2022, pacientes con FEVI menor o igual al 35 %, enfermedad coronaria extensa revascularizable por angioplastia y viabilidad en al menos 4 segmentos, fueron asignados aleatoriamente a angioplastia coronaria frente a tratamiento médico óptimo, sin encontrarse diferencias significativas en el combinado de muerte por cualquier causa o insuficiencia cardíaca a los 41 meses. Aunque el 70 % de la evaluación de viabilidad se realizó mediante RMC, nuevamente no se excluyeron pacientes con volúmenes excesivamente elevados y se consideró viable cualquier segmento disfuncional en su motilidad con menos del 25 % del espesor transmural con realce tardío con gadolinio. (5)
UN CASO QUE NOS PLANTEA UNA PREGUNTA INQUIETANTE
En un paciente con enfermedad de 3 vasos y un ventrículo izquierdo dilatado con hipoquinesia global y deterioro grave de la función sistólica, la ausencia de secuela de necrosis en la RMC (Figura 1) sugiere que el miocardio se encuentra viable en su totalidad. Sin embargo, la posibilidad de mejora de la función ventricular post revascularización, es poco probable, ya que la posibilidad de que la etiología de la miocardiopatía sea de origen coronario es muy baja.
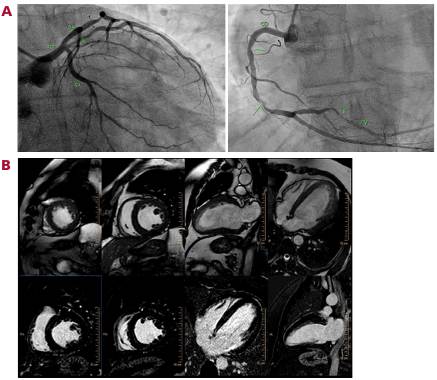
Fig. 1
Imágenes de un paciente de 64 años, internado por insuficiencia cardíaca congestiva. A. Coronariografía (CCG) que muestra enfermedad de tres vasos: afectación grave en la arteria descendente anterior (DA), Ramus intermedio (RI) y coronaria derecha (CD). B. Resonancia magnética cardíaca (RMC) que revela un ventrículo izquierdo dilatado con hipoquinesia global, espesores parietales normales y ausencia de realce tardío con gadolinio (RTG), interpretado como miocardiopatía no isquémica necrótica.
Ahora imaginemos que estamos reclutando pacientes para el estudio REVIVED. ¿Hay algún criterio de inclusión o exclusión que impida que este paciente sea considerado? Este caso representa un claro ejemplo de un paciente con miocardiopatía no coronaria que podría haber sido incluido en el estudio.
ACLARANDO CONCEPTOS BÁSICOS
¿Miocardiopatía, cardiopatía isquémica o mecanismo dual?
Por definición, se considera una miocardiopatía como aquel trastorno del miocardio en el que el músculo cardíaco presenta anomalías estructurales y funcionales, en ausencia de enfermedades de las arterias coronarias, hipertensión, valvulopatías o cardiopatías congénitas que puedan explicar la disfunción cardíaca. (6) Es fundamental destacar que las miocardiopatías pueden coexistir con enfermedad isquémica, valvular o hipertensiva; y que por ende, la presencia de una no excluye la otra. Por lo tanto, es esencial no solo evaluar la existencia de enfermedad coronaria obstructiva, sino también demostrar que justifica el grado de deterioro de la función ventricular.
¿De qué hablamos cuando hablamos de viabilidad?
El miocardio viable se define como el tejido miocárdico con disfunción reversible provocada por enfermedad coronaria. (7) Existen dos mecanismos principales a través de los cuales puede presentarse un miocardio disfuncional en reposo, pero viable: el atontamiento y la hibernación. (8,9) El atontamiento miocárdico es un fenómeno en el cual la contractilidad del miocardio se reduce durante cortos episodios de isquemia, aunque eventualmente se restablece. Durante el período transitorio en que la perfusión se ha normalizado pero el miocardio sigue siendo disfuncional, se considera que está en un estado de “atontamiento”. (10) Un ejemplo común en la práctica clínica, es la disfunción ventricular transitoria que ocurre tras la reperfusión de un síndrome coronario agudo.
El miocardio hibernado, en cambio, resulta de una hipoperfusión sostenida en reposo, asociada a una demanda metabólica del miocardio que excede la reserva de flujo coronario. Este tipo de miocardio presenta una disfunción persistente en reposo debido a un flujo coronario crónico insuficiente, y puede ser parcial o totalmente reversible tras la revascularización. (11) Un ejemplo típico de hibernación en la práctica clínica podemos verlo en oclusiones coronarias crónicas con circulación colateral y poco tejido necrótico.
¿Podemos hablar de miocardio viable en ausencia de hibernación o atontamiento?
Esta pregunta nos lleva a uno de los errores conceptuales que más impactan tanto en la práctica diaria como en el establecimiento de criterios para la selección de poblaciones en estudios aleatorizados: el miocardio isquémico no suele considerarse en la búsqueda de miocardio viable. El miocardio isquémico se caracteriza por presentar motilidad, metabolismo y perfusión normal en reposo, y disfunción al someterse a un estrés, derivado del compromiso vascular. Si entendemos este concepto, resulta obvio que un segmento miocárdico que no presenta secuela de necrosis puede estar isquémico. La única forma de determinarlo entonces, es realizando un protocolo de estrés que evoque isquemia, ya sea mediante resonancia estrés, SPECT gatillado o ecocardiograma estrés.
En consecuencia, si en los estudios STICH y REVIVED no registraron cuantificación de isquemia, ¿cómo podemos diferenciar disfunción ventricular debida a enfermedad coronaria de miocardiopatía con anatomía coronaria obstructiva asociada?
¿Podemos hablar de miocardio vivo pero no viable?
La hibernación y la isquemia evocada representan diferentes espectros de compromiso miocárdico por enfermedad coronaria crónica. (12) Por lo tanto, deben ser tenidos en cuenta dentro del espectro de lo que llamamos viabilidad clínicamente significativa. Es decir, una masa de miocardio que vale la pena revascularizar. Ahora bien, si en el contexto de un ventrículo izquierdo dilatado y globalmente comprometido encontramos un porcentaje significativo de miocardio que no está necrótico, pero tampoco presenta hibernación ni isquemia, podemos decir que estamos frente a miocardio vivo (no necrótico) pero no viable, ya que la etiología de esta disfunción no es coronaria y por lo tanto no mejorará con la revascularización.
UNA PROPUESTA PARA FACILITAR LA PRÁCTICA DIARIA
Las evaluaciones de viabilidad constituyen aproximadamente el 5 % de los pedidos de resonancias cardíacas en nuestro país, según el Registro Nacional Argentino de Resonancia Cardíaca (RENAREC). (13) Con el objetivo de maximizar la utilidad de este recurso, de difícil acceso en nuestro entorno, proponemos la adopción de una terminología unificada y de fácil aplicación. Esta terminología podría facilitar la comprensión del cardiólogo clínico que deriva a sus pacientes para estudios de cardio-imágenes destinados a evaluar la viabilidad miocárdica. Sugerimos referirse a viabilidad clínicamente significativa. O sea, miocardio hibernado o isquémico, excluyendo al miocardio vivo pero no comprometido por enfermedad coronaria (véase Tabla 1).
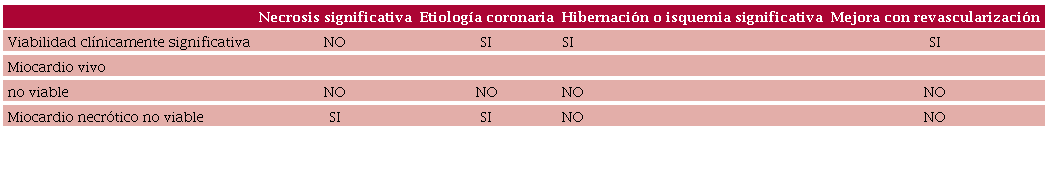
Vale la pena aclarar -como se mencionó previamente- que salvo algunas excepciones, el atontamiento es un fenómeno generalmente relacionado con la disfunción post reperfusión tras un síndrome coronario agudo. Este fenómeno es poco frecuente en casos de disfunción ventricular coronaria crónica, por lo que la viabilidad miocárdica en contexto ambulatorio se refiere principalmente a situaciones de hibernación o isquemia.
COMENTARIO FINAL
Al referirnos al miocardio viable o a la viabilidad clínicamente significativa, asumimos que la disfunción ventricular tiene una etiología coronaria. Al igual que otros especialistas médicos, los cardiólogos realizan interpretaciones diagnósticas, las cuales son inherentemente discutibles. Por ello, proponemos hablar de miocardio viable solo si se está interpretando causa coronaria subyacente. Para esto es esencial contar con datos clínico-imagenológicos que respalden nuestra hipótesis de que el miocardio está comprometido por enfermedad coronaria obstructiva (causalidad) y que no se trate de una mera coincidencia entre ambas condiciones (casualidad).
Con este fin, creemos que un enfoque diagnóstico adecuado debe incluir la evaluación de la isquemia miocárdica, y no limitarse únicamente a la ausencia de necrosis en una resonancia con gadolinio o perfusión miocárdica sin fase de estrés.
No podemos pretender una mejoría de la función ventricular post revascularización, sin antes comprender la fisiopatología de la disfunción.
BIBLIOGRAFÍA
FelkerGM, ThompsonRE, HareJM, HrubanRH, ClemetsonDE, HowardDL. Underlying causes and long-term survival in patients with initially unexplained cardiomyopathy. N Engl J Med 2000342:1077-84. https://doi.org/10.1056/NEJM20000413342150210760308
BawaskarP, ThomasN, Ismail K, Guo Y, Chhikara S, Athwal PSS. Nonischemic or Dual Cardiomyopathy in Patients With Coronary Artery DiseaseCirculation 2024;149:807-21. https://doi.org/10.1161/CIRCULATIONAHA.123.067032
Velazquez EJ, Lee KL, Deja MA, Jain A, Sopko G, Marchenko A. Coronary-artery bypass surgery in patients with left ventricular dysfunction. N Engl J Med 2011;364:1607-16. https://doi.org/10.1056/NEJMoa1100356
Panza JA, Ellis AM, Al-Khalidi HR, Holly TA, Berman DS, Oh JK. Myocardial Viability and Long-Term Outcomes in Ischemic Cardiomyopathy. N Engl J Med 2019;381:739-48. https://doi.org/10.1056/NEJMoa1807365
Perera D, Clayton T, O'Kane PD, Greenwood JP, Weerackody R, Ryan M. Percutaneous Revascularization for Ischemic Left Ventricular Dysfunction. N Engl J Med 2022;387:1351-60. https://doi.org/10.1056/NEJMoa2206606
Comments to the 2021 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure. Rev Esp Cardiol 2022;75:458-65. https://doi.org/10.1016/j.recesp.2021.11.012
Allman KC, Shaw LJ, Hachamovitch R, Udelson JE. Myocardial viability testing and impact of revascularization on prognosis in patients with coronary artery disease and left ventricular dysfunction: a meta-analysis. J Am Coll Cardiol 2002;39:1151-8. https://doi.org/10.1016/s0735-1097(02)01726-6
Cleland JG, Pennell DJ, Ray SG, Coats AJ, Macfarlane PW, Murray GD. Myocardial viability as a determinant of the ejection fraction response to carvedilol in patients with heart failure (CHRISTMAS trial): randomised controlled trial. Lancet 2003;362:14-21. https://doi.org/10.1016/s0140-6736(03)13801-9
Barnes E, Hall RJ, Dutka DP, Camici PG. Absolute blood flow and oxygen consumption in stunned myocardium in patients with coronary artery disease. J Am Coll Cardiol 2002;39:420-7. https://doi.org/10.1016/s0735-1097(01)01774-0
Jeroudi MO, Cheirif J, Habib G, Bolli R. Prolonged wall motion abnormalities after chest pain at rest in patients with unstable angina: a possible manifestation of myocardial stunning. Am Heart J 1994;127:1241-50. https://doi.org/10.1016/0002-8703(94)90042-6
Carlson EB, Cowley MJ, Wolfgang TC, Vetrovec GW. Acute changes in global and regional rest left ventricular function after successful coronary angioplasty: comparative results in stable and unstable angina. J Am Coll Cardiol 1989;13:1262-9. https://doi.org/10.1016/0735-1097(89)90298-2
Kitsiou AN, Srinivasan G, Quyyumi AA, Summers RM, Bacharach SL, Dilsizian V. Stress-induced reversible and mild-to-moderate irreversible thallium defects: are they equally accurate for predicting recovery of regional left ventricular function after revascularization?. Circulation 1998;98:501-8. https://doi.org/10.1161/01.cir.98.6.501
Del Castillo S, Jaimovich G, Destefano L, De Zan M, Sciancalepore A, Ricapito P. Registro Nacional Argentino de Resonancia Cardíaca (RENAREC). Rev Argent Cardiol 2022;90:250-6. https://doi.org/10.7775/rac.es.v90.i4.20535
Author notes
Dirección para correspondencia: Lucas San Miguel. Jerónimo Salguero 560. (C1177AEJ). Ciudad Autónoma de Buenos Aires, Argentina. Correo electrónico: lucasanmiguel@gmail.com
Conflict of interest declaration
