RESUMEN
Introducción: En pacientes con estenosis aórtica (EAo) grave se ha propuesto una clasificación en estadios para evaluar la extensión del daño extravalvular (anatómico y funcional) con la idea de mejorar la indicación y pronóstico del reemplazo valvular aórtico con base solo en la presencia de síntomas o fracción de eyección del ventrículo izquierdo (FEVI) < 50 %. Sin embargo, dicha clasificación no considera el componente vascular de la poscarga del VI. Las características de la vasculatura arterial pueden repercutir en la función del VI a través de la alteración de la cupla ventriculoarterial (CVA).
Objetivo: Evaluar la relación entre la CVA y los diferentes estadios de daño extravalvular en la EAo.
Material y métodos: Se estudiaron 205 pacientes, edad promedio 70 ? 11 años, 117 hombres, con EAo grave (área valvular aórtica, AVA, < 1 cm2) con eco Doppler cardíaco. La CVA fue calculada mediante el cociente elastancia arterial efectiva (Ea)/ elastancia de fin de sístole del VI (Efs). Los pacientes fueron divididos en cinco grupos de acuerdo con la clasificación en estadios de daño cardíaco extravalvular: estadio 0, sin daño cardiaco; estadio 1, daño del VI; estadio 2, daño de aurícula izquierda o válvula mitral; estadio 3, hipertensión pulmonar o compromiso de válvula tricúspide y estadio 4, daño ventricular derecho.
Resultados: No hubo pacientes en estadio 0. Los síntomas estuvieron presentes en el 40 % de los pacientes del estadio 1, 85 % del estadio 2 y 100 % de los estadios 3 y 4. La Ea se incrementó desde el estadio 2 al estadio 4 mientras que la Efs no presentó cambios en estos grupos, pero disminuyó del estadio 1 al 2. La CVA aumentó progresivamente del estadio 1 al 4.
Conclusiones: El deterioro de la CVA aumenta a medida que avanza el estadio de daño miocárdico. La alteración de la CVA desde el estadio 2 al 4 se debe al incremento en la Ea sin cambios significativos en el nivel de contractilidad (Efs). La progresión del daño miocárdico extravalvular parece estar relacionado no solo con la enfermedad valvular sino también con las características de la vasculatura arterial.
Palabras claves: Estenosis aórtica, Cupla ventriculoarterial, Elastancia arterial efectiva.
ABSTRACT
Background: A staging classification has been proposed for patients with severe aortic stenosis (AS) to evaluate the extent of extravalvular (anatomical and functional) damage with the aim of improving the indication and prognosis of aortic valve replacement (AVR) based only on the presence of symptoms or left ventricular ejection fraction (LVEF) < 50 %. However, such classification does not consider the vascular component of LV afterload. The characteristics of the arterial vasculature can have implications for LV function by influencing the ventricular-arterial coupling (VAC).
Objective: The aim of the present study was to evaluate the relationship between VAC and the different stages of extravalvular damage in AS.
Methods: We prospectively evaluated 205 patients (mean age 70 ± 11 years,117 men), with severe AS [aortic valve area (AVA) < 1 cm2] using Doppler echocardiography. Ventricular-arterial coupling was calculated as the arterial elastance (Ea) to LV end-systolic elastance (Ees) ratio. Patients were divided into five groups according to the criteria for staging extravalvular cardiac damage: stage 0, no cardiac damage; stage 1: LV damage; stage 2: left atrial or mitral valve damage; stage 3: pulmonary hypertension or tricuspid valve involvement; and stage 4: right ventricular damage.
Results: There were no patients in stage 0. Symptoms were present in 40 % of stage 1 patients, 85 % of stage 2 and 100 % of stages 3 and 4. Ea increased from stage 2 to stage 4 while Ees remained unchanged in these groups but decreased from stage 1 to stage 2. Ventricular-arterial coupling exhibited progressive increase from stage 1 to 4.
Conclusions: As the stage of myocardial damage progresses, the impairment of VAC increases. The alteration of VAC that occurs from stage 2 to 4 is due to an increase in Ea without significant changes in the level of contractility (Ees). The progression of extravalvular myocardial damage appears to be associated not only with valvular disease but also with the characteristics of the arterial vasculature.
Key words: Aortic stenosis, Ventricular-arterial coupling, Effective arterial elastance.
ARTÍCULO ORIGINAL
Relación entre la cupla ventriculoarterial y el estadio de daño extravalvular en la estenosis aórtica
Relationship Between Ventricular-arterial Coupling and Stage of Extravalvular Damage in Aortic Stenosis
Received: 06 January 2025
Accepted: 07 March 2025
La estenosis aórtica (EAo) calcificada del adulto es la valvulopatía que en la actualidad requiere más frecuentemente tratamiento quirúrgico o endovascular debido al aumento de la edad en la población general. (1) De acuerdo con las Guías ACC/AHA (2) y ESC, (3) el reemplazo valvular aórtico (RVAo) está indicado cuando aparecen síntomas (ángor, disnea o síncope), fracción de eyección de ventrículo izquierdo (FEVI) disminuida o cirugía cardíaca por otras causas. Pero la EAo no es una enfermedad circunscripta a la válvula, sino que debe ser considerada una enfermedad sistémica con compromiso de todas las cavidades cardíacas y del sistema vascular pulmonar y sistémico. Siguiendo este razonamiento, en pacientes con EAo grave se ha propuesto una clasificación en estadios para evaluar la extensión del daño extravalvular (anatómico y funcional) con la idea de mejorar la indicación y pronostico del RVAo. (4) Sin embargo, se debe considerar que la poscarga del VI tiene un componente valvular y otro vascular, (5,6) que no es evaluado en la clasificación en estadios. Las características de la vasculatura arterial pueden repercutir en la función del VI a través de la alteración de la cupla ventriculoarterial (CVA), la cual se evalúa mediante la relación entre la elastancia arterial efectiva (Ea) y la elastancia de fin de sístole del VI (Efs). (7,8) Si el valor del cociente Ea / Efs es ≤ 1 existe un acoplamiento adecuado entre el VI y la vasculatura arterial mientras que si el valor es ˃ 1 evidencia desacople entre ambos lo que implica pérdida de la eficiencia mecánica del VI. La Ea es un parámetro de mecánica arterial que está influenciado por la impedancia característica y la resistencia periférica, (9) mientras que la Efs evalúa la contractilidad del VI independientemente de la pre y poscarga. El aumento de la edad de los pacientes con EAo en las últimas décadas ha sido acompañado de un incremento en la prevalencia de hipertensión arterial (HTA), lo cual representa una carga aditiva a la obstrucción valvular para el VI. (10,11)
El objetivo del presente trabajo fue evaluar la relación entre la CVA y los diferentes estadios de daño extravalvular en la EAo.
Se estudiaron prospectivamente 205 pacientes (edad 70 ± 11 años, 117 hombres) con EAo grave (área valvular aórtica, AVA, < 1 cm2) mediante eco Doppler cardíaco. El protocolo fue aprobado por el Comité de Docencia e Investigación del Hospital. Fueron excluidos los pacientes que presentaban calcificación significativa del anillo mitral, insuficiencia aórtica o mitral de grado moderado o grave. Se consideró antecedente de HTA a la necesidad de haber indicado tratamiento antihipertensivo previamente y de cardiopatía isquémica si el paciente había presentado uno o más de los siguientes criterios: 1) antecedentes de infarto agudo de miocardio, angioplastia coronaria o cirugía de revascularización, 2) obstrucciones mayores del 50% en las arterias coronarias determinadas por angiografía y 3) acinesia en el ecocardiograma. A todos los pacientes se les efectuó interrogatorio para detectar la presencia de factores de riesgo coronario y síntomas, examen físico cardiovascular y medición de la presión arterial, registro del pulso carotídeo y ecocardiograma Doppler completo.
Ecocardiograma y Doppler cardíaco: El estudio fue realizado con un ecocardiógrafo ESAOTE MyLab 40 con transductor de 2.5 - 3.5 MHz. Las mediciones en modo M, ecocardiograma bidimensional, cálculo de la fracción de acortamiento endocárdica (FAe) del VI, espesor parietal relativo (EPR), volumen de fin de diástole (VFD) (método de Simpson), volumen de fin de sístole (VFS), FEVI e índice de masa (IM), se realizaron de acuerdo con los criterios de la ASE. (12)
Con Doppler continuo se registró la velocidad máxima transvalvular aórtica, el gradiente pico (GP), el gradiente medio (GM) y la integral de la curva de flujo desde las vistas apical, paraesternal derecha, subxifoidea y supraesternal. Con Doppler pulsado se obtuvo el flujo en el tracto de salida del VI desde la vista de cinco cámaras. El cociente adimensional se estimó como el cociente entre la integral de flujo en el tracto de salida de VI y la integral de flujo Ao. Se calculó el AVA efectiva utilizando la ecuación de continuidad, el índice de AVA (AVA / superficie corporal, SC), la impedancia válvulo-arterial (Zva) y el índice de pérdida de energía (IPE) de acuerdo con la ASE. (13) El volumen sistólico (VS) se calculó como el producto del área del tracto de salida por la integral de flujo a dicho nivel, el índice de VS (IVS) como el VS dividido por la SC y el flujo aórtico como el cociente entre el VS y el período eyectivo del VI. Se registró el flujo transmitral colocando el volumen de muestra del Doppler pulsado a nivel del borde libre de la válvula mitral en la vista de 4 cámaras y se obtuvo la velocidad pico de la onda E y la onda A con lo cual se calculó la relación E/A. (14) Posteriormente se registró el Doppler tisular pulsado del anillo mitral lateral y septal, con medición de la velocidad pico de la onda e´ en las dos localizaciones, y se consignó el promedio de ambas para la determinación de la relación E/e´. (15) Se registró la velocidad pico del jet de insuficiencia tricúspidea con Doppler continuo para estimar la presión sistólica de la arteria pulmonar, adicionando la presión de la aurícula derecha estimada a través del diámetro y colapso de la vena cava inferior. La función sistólica del ventrículo derecho (VD) fue cuantificada mediante la excursión sistólica del plano del anillo tricuspídeo (TAPSE) y la velocidad pico de la onda S del Doppler tisular del anillo tricúspideo lateral. En 168 pacientes se estimó el strain longitudinal del VI con speckle tracking bidimensional utilizando el software provisto por el equipo desde las vistas apicales de cuatro y dos cámaras y eje largo apical.
La presión del pulso (PP) se estimó como la diferencia entre la presión arterial sistólica y diastólica medida con esfigmomanómetro. Se calculó el cociente VS/PP como índice de complacencia arterial (CA), (16,17) y para una mejor comparación entre los grupos se normalizó el VS a la superficie corporal: VSi /PP. (18) La resistencia vascular sistémica (RVS) se calculó como: (80 x PAM) /VM, siendo PAM la presión arterial media y VM el volumen minuto.
Luego del ecocardiograma Doppler se registró el carotidograma con un transductor de pulso TPW - 01 A conectado a un ecocardiógrafo TOSHIBA SSH140A, y se midió la presión arterial con esfigmomanómetro en el brazo derecho del paciente. El carotidograma fue calibrado de acuerdo con el método utilizado en nuestro laboratorio (19,20) para obtener la presión de fin de sístole (PFS) (Figura 1).
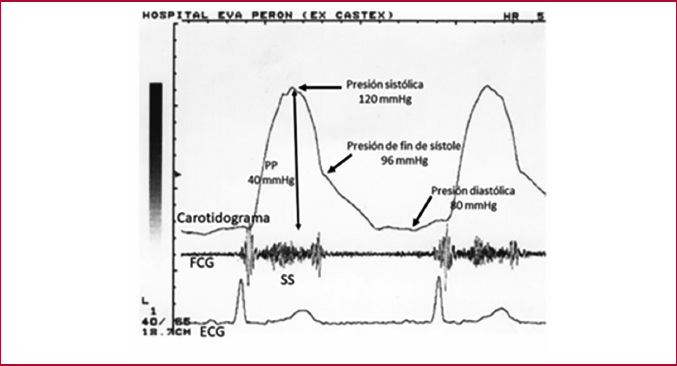
Evaluación de la Efs, Ea y CVA: La Efs fue estimada por el método de Senzaki et al. (21) (ver material suplementario), la Ea se calculó como el cociente entre el VS y la PFS y la CVA como el cociente entre Ea y Efs (Figura 2).
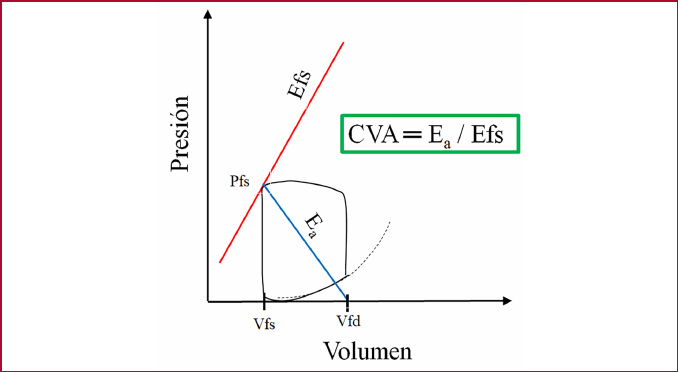
Los pacientes fueron divididos en cinco grupos de acuerdo con la clasificación en estadios de daño cardíaco extravalvular propuesta por Tastet y col. (22):
a) estadio 0, sin daño cardiaco;
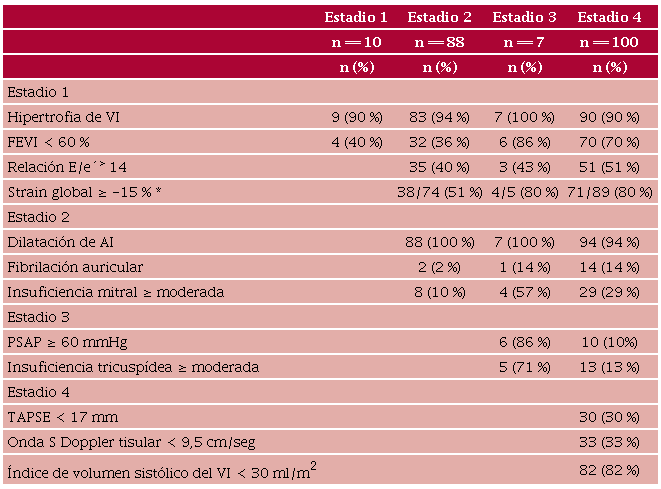
b) estadio 1, daño del VI (n ═ 10): hipertrofia de VI (IM ˃ 115 gr/m2 en hombres y ˃ 95 gr/m2 en mujeres), disfunción diastólica ≥ grado 2 (relación E/e´ ˃ 14), disfunción sistólica subclínica (FEVI < 60 %, strain global de VI ≥ -15%);
c) estadio 2, daño de aurícula izquierda o válvula mitral (n ═ 88): índice de volumen de la aurícula izquierda (IVAI) ˃ 34 ml/m2, insuficiencia mitral ≥ moderada, fibrilación auricular;
d) estadio 3, hipertensión pulmonar o compromiso de válvula tricúspide (n ═ 7): presión sistólica de arteria pulmonar ≥ 60 mmHg, insuficiencia tricuspídea ≥ moderada;
e) estadio 4, daño ventricular derecho o insuficiencia cardíaca subclínica (n ═ 100): disfunción sistólica del VD (TAPSE < 17 mm, onda S del Doppler tisular tricuspídeo < 9,5 cm/seg), bajo flujo moderado a grave (IVS < 30 ml/m2).
En la asignación del grupo a cada paciente se consideró el hallazgo de al menos un criterio en el estadio más avanzado, por ejemplo, un paciente con TAPSE < 17 mm fue considerado del estadio 4 aun en ausencia de hipertensión pulmonar, compromiso de la válvula mitral o FEVI < 60 %.
Análisis estadístico: se realizó con el software SPSS 25. Las variables continuas se expresaron como media ? desviación estándar. Para la comparación de los grupos se utilizó el análisis de la varianza. Como límite de significación se consideró un valor de p < 0,05.
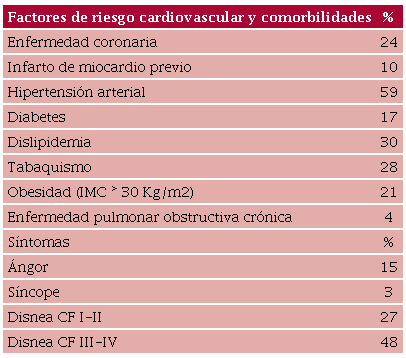
En la Tabla 1 se muestran los factores de riesgo cardiovascular, comorbilidades y síntomas de los pacientes estudiados. No hubo pacientes en estadio 0. La HTA fue el factor de riesgo más frecuente. Los síntomas estuvieron presentes en el 40 % de los pacientes del estadio 1, 85 % del estadio 2 y 100 % de los estadios 3 y 4. La disnea III-IV fue el síntoma más frecuente. Los pacientes del estadio 1 tuvieron una edad menor (57 ± 13 años, p < 0,01) comparados con el resto de los pacientes (Tabla 2). No hubo diferencias significativas entre los distintos grupos al considerar la SC, presión arterial sistólica, diastólica, PFS y frecuencia cardíaca.
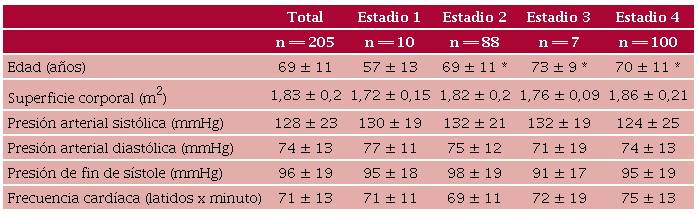
Función sistólica de VI (Tabla 3): se observó aumento significativo de los diámetros y volúmenes ventriculares desde el estadio 2 al 4 al compararlos con el estadio 1. De acuerdo con el IM y el EPR, la hipertrofia concéntrica fue el tipo de geometría que predominó en todos los grupos. La FEVI estuvo disminuida significativamente en los estadios 3 y 4, aunque se detectó disminuida por debajo del 60 % en el 40 % de los pacientes del estadio 1 y 36 % del estadio 2. El strain longitudinal del VI fue disminuyendo progresivamente desde el estadio 2 al 4, con diferencias entre los grupos estadísticamente significativas. El IVS y el flujo aórtico disminuyeron en forma significativa en el estadio 4, hallándose un IVS < 30 ml/m2 en el 82 % de los pacientes de dicho grupo.
Estenosis aórtica: no hubo diferencias significativas entre los pacientes de los estadios 1 al 3 al considerar la velocidad pico transvalvular aórtica, los GP y GM, el AVA, el índice del área valvular aórtica (IAVA), Zva e IPE (Tabla 4). Los pacientes en estadio 4 tuvieron gradientes más bajos pero mayor gravedad de la estenosis aórtica de acuerdo con el AVA, IAVA, Zva e IPE indicando un grado mayor de compromiso de la enfermedad a nivel valvular.
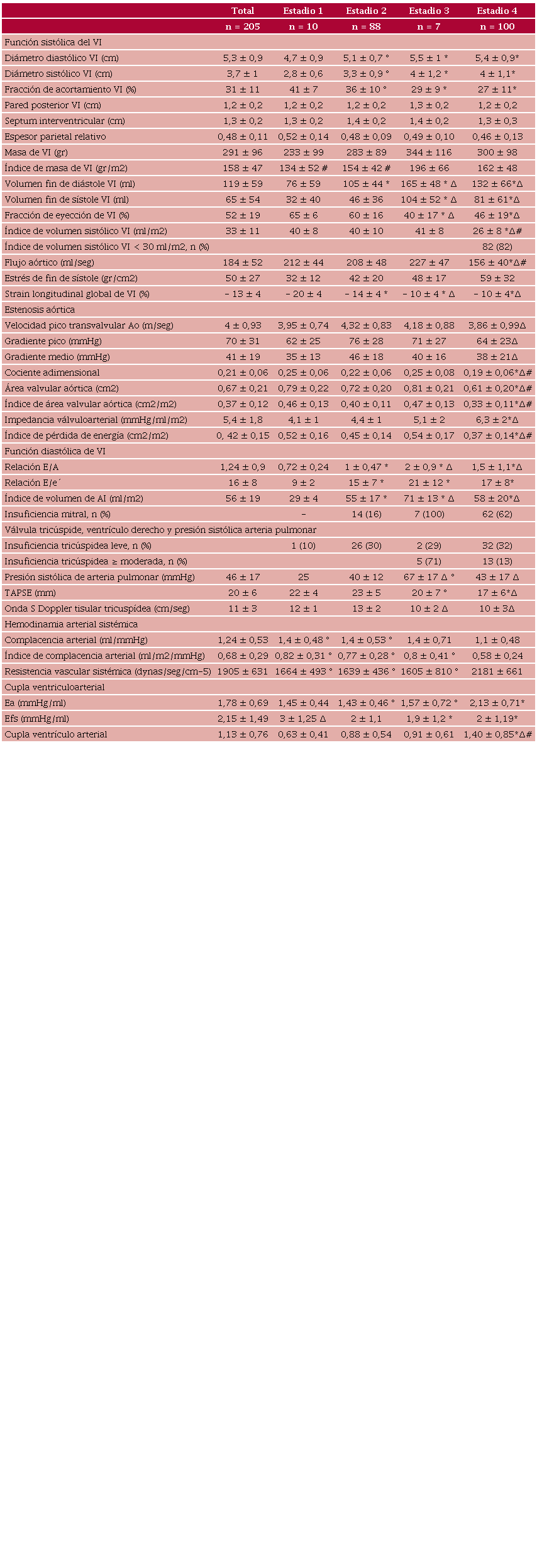
Función diastólica de VI: la relación E/A, E/e´ y el IVAI se incrementaron significativamente desde el estadio 2 al 4.
Insuficiencia mitral: la insuficiencia mitral de grado moderado o mayor se observó más frecuentemente en los estadios 3 y 4.
Insuficiencia tricuspídea, VD y presión sistólica de arteria pulmonar: la insuficiencia tricuspídea de grado leve se registró en un tercio de los pacientes de los estadios 2, 3 y 4, mientras que el grado moderado o grave fue más frecuente en el estadio 3 que en el 4, debido probablemente a que el estadio 3 presentó mayor presión sistólica de arteria pulmonar que el estadio 4. La función sistólica longitudinal del VD evaluada mediante el TAPSE y la onda S del Doppler tisular del anillo tricuspídeo lateral estuvo disminuida en los estadios 3 y 4.
Hemodinamia arterial sistémica: la CA y la RVS estuvieron alteradas solo en el estadio 4, no hallándose diferencias significativas entre los estadios 1, 2 y 3.
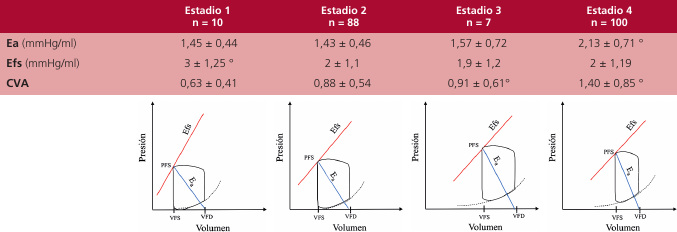
Cupla ventriculoarterial: a diferencia de la CA y la RVS, la Ea se incrementó desde el estadio 2 al estadio 4 indicando aumento de la rigidez arterial y por lo tanto de la carga vascular. La Efs, que evalúa la contractilidad del VI, no presentó cambios en estos grupos (valor mayor de 1 en todos los estadios) evidenciando contractilidad preservada, aunque disminuyó del estadio 1 al 2 (3 ± 1,25 vs 2 ± 1,1, p < 0,01). La CVA se alteró progresivamente del estadio 1 al 4 como consecuencia fundamentalmente del aumento de la Ea (Figura 3).
El principal hallazgo del presente trabajo es que la progresión del daño extravalvular en la EAo se relaciona con la alteración de la CVA, lo cual sugiere que dicho daño no se debe solamente al componente valvular, sino también a las características de la vasculatura arterial sistémica. Généreux y col. (5) describieron una clasificación en cinco estadios de daño extravalvular (anatómico y funcional) en la EAo en 1661 pacientes de los estudios PARTNER 2A y 2B en los cuales se realizó RVAo. Posteriormente los mismos autores publicaron el impacto de la determinación del estadio de daño extravalvular luego del año del RVAo (23) y la correlación con la calidad de vida de acuerdo con el cuestionario de miocardiopatías de Kansas. (24) Para definir mejor el compromiso de la función del VI se incorporó el strain longitudinal global, con lo que se demostró un incremento en el valor pronóstico de la clasificación descripta previamente. (25) Nosotros utilizamos la clasificación en estadios propuesta por Tastet y col. (9) que adopta como punto de corte para la FEVI un valor menor de 60 % para el estadio 1, ya que consideramos que es más adecuado que menos de 50 % en presencia de hipertrofia concéntrica, geometría que exagera el movimiento del endocardio con el cual se calcula la FEVI. (26,27) En los trabajos mencionados los pacientes del estadio 4 representan entre el 7,1 % y el 8,7 % del total mientras que en nuestro estudio fue del 49 %, sin pacientes en el estadio 0. Dicha diferencia puede deberse a falta de diagnóstico precoz, ya que la mayoría de los pacientes con insuficiencia cardíaca desconocían la existencia de su valvulopatía, hecho frecuente de observar en los hospitales públicos.
Con respecto a la gravedad de la EAo, no hubo diferencias entre los estadios 1 al 3 al compararla a través de los gradientes, AVA, IAVA y el IPE, por lo que puede considerarse que la carga valvular fue la misma en los tres estadios. No ocurrió lo mismo con el estadio 4, que evidenció mayor gravedad de la EAo. Sin embargo, la CVA se alteró progresivamente desde el estadio 2 al 4 a expensas del aumento de la Ea, sin estar disminuida la contractilidad del VI (Efs) (Figura 3).
Se debe considerar que en la EAo la relación con la poscarga es más compleja que lo esperado, (28,29,30) ya que al efecto de la obstrucción al tracto de salida (carga valvular) se agregan las fuerzas que se oponen a la eyección, dependientes de las características físicas de las arterias (carga vascular), (31) como la impedancia arterial, determinada por la relación fásica entre la presión y el volumen aórtico, la RVS, la rigidez de la pared aórtica, (32) y las propiedades de la inercia sanguínea y de las ondas de reflexión que se producen en las bifurcaciones arteriales. (33,34,35) De los índices que evalúan la mecánica arterial, la Ea parece ser más adecuada que la CA, porque incorpora la impedancia característica, resistencia, complacencia y longitud del ciclo. (36,37) Un parámetro que evalúa la carga global (valvular y vascular) en la EAo es la Zva ; sin embargo, a pesar de estar incrementada - debido a la alta prevalencia de hipertensión arterial -, no mostró diferencias significativas entre los diferentes estadios, excepto en el estadio 4.
La alteración de la CVA se correlaciona con la aparición de los síntomas e insuficiencia cardíaca, predominando el aumento de la Ea sobre la disminución de la Efs. (38) En el presente estudio la FEVI estuvo disminuida sobre todo en los estadios 3 y 4 (86 % y 70 % respectivamente) a pesar de estar la contractilidad preservada según la Efs, lo cual se explica por el “mismatch” o sea el desacople entre la poscarga y el inotropismo existente entre la función de cámara (FEVI) y la función muscular (Efs) en la EAo. (16,39) El mismo concepto podría aplicarse para el strain, que disminuyó progresivamente desde el estadio 2 al 4 anticipándose a la disminución de la FEVI, ya que el strain se correlacionó positivamente con el aumento de la Ea (r ═ 0,43 p<0,001 y ═ 0,0715 . x + 2) evidenciando su dependencia de la poscarga como todo índice que evalúa el acortamiento de la fibra. Por lo tanto, se debe considerar que la disminución del strain o la FEVI no se debe solo a la carga valvular sino también a la carga vascular.
El deterioro de la CVA aumenta a medida que avanza el estadio de daño miocárdico. La alteración de la CVA desde el estadio 2 al 4 se debe al incremento de la Ea sin cambios significativos en el nivel de contractilidad (Efs). La progresión del daño miocárdico extravalvular parece estar relacionado no solo con la enfermedad valvular sino también con las características de la vasculatura arterial.
Dirección para correspondencia: Ricardo A. Migliore, Moreno 3518 4° E, San Martín (1650), Provincia de Buenos Aires, Argentina. Correo electrónico: rmigliore@intramed.net






