RESUMEN
Introducción: Entre 3% y 20% de los pacientes con cirugía de Fontan-Kreutzer (CF) desarrollarán enteropatía perdedora de proteína (EPP), con alto impacto en la sobrevida. Se ha propuesto la técnica de embolización selectiva de conductos linfáticos hepatoduodenales (ESLHD) como un novedoso blanco terapéutico.
Objetivo: Evaluar la factibilidad, complicaciones y el resultado clínico analítico de la ESLHD en pacientes con CF y EPP.
Material y métodos: Serie de casos de pacientes con CF, retrospectiva, unicéntrica, que incluyó 5 pacientes con EPP, a los que se les realizó ESLHD por vía percutánea.
Resultados: Se incluyeron 5 pacientes con CF realizada a una mediana de edad de 4 años (rango: 3,5-4,3), quienes desarrollaron EPP a una mediana de tiempo postquirúrgico de 7 años (rango 2,3-15,3). Se realizaron 7 ESLHD, con linfografía por cateterismo, bajo control ecocardiográfico. En los 5 pacientes se hallaron conductos linfáticos hepatoduodenales dilatados y tortuosos que drenaban en el intestino delgado, y se logró su embolización de manera efectiva en todos los casos. Post procedimiento inmediato todos incrementaron el nivel sérico de albúmina. Durante una mediana de seguimiento de 20 meses (rango 12-43) 4 pacientes mantuvieron los niveles de albúmina, mientras que un p requirió dos nuevas embolizaciones por hipoalbuminemia persistente. Un paciente requirió intervención quirúrgica por defecto residual anatómico. En todos los pacientes se evidenció mejoría clínica. No hubo complicaciones mayores relacionadas con el procedimiento; 3 pacientes presentaron episodio autolimitado de melena.
Conclusiones: La ESLHD fue una herramienta segura y beneficiosa. El procedimiento permitió mejorar los niveles séricos de albúmina y sintomatología en todos nuestros pacientes.
Palabras clave: Enteropatía perdedora de proteínas, cirugía de Fontan-Kreutzer, embolización linfática selectiva.
ABSTRACT
Background: Between 3% and 20% of Fontan-Kreutzer surgery (FS) patients will develop protein-losing enteropathy (PLE), with high impact on survival. Selective hepatoduodenal lymphatic duct embolization (SHDLE) technique has been proposed as a novel therapeutic target.
Objective: The aim of this study was to evaluate the feasibility, complications and analytical clinical outcome of SHDLE in patients with FS and PLE.
Methods: A retrospective, single-center, case series of patients with FS was carried out, including 5 patients with PLE, who underwent percutaneous SHDLE.
Results: Five patients who underwent FS at a median age of 4 years (range: 3.5-4.3), developed PLE at a median postoperative time of 7 years (range 2.3-15.3). Seven SHDLE were performed, with catheter lymphography, under echocardiographic control. In all 5 patients dilated and tortuous hepatoduodenal lymphatic ducts draining into the small intestine were found, and their embolization was effectively achieved in all cases. Immediately after the procedure all these patients increased their serum albumin level. During a median follow-up of 20 months (range 12-43) 4 patients maintained their albumin levels, while one patient required two new embolizations due to persistent hypoalbuminemia. One patient required surgical intervention due to residual anatomical defect. All patients showed clinical improvement. There were no major complications related to the procedure; 3 patients presented a self-limited episode of melena.
Conclusions: SHDLE was a safe and beneficial tool. The procedure allowed improving serum albumin levels and symptoms in all our patients.
Keywords: Protein-losing enteropathy, Fontan-Kreutzer surgery, Selective lymphatic embolization..
ARTÍCULO BREVE
Embolización linfática de la enteropatía perdedora de proteínas en la circulación Fontan Kreutzer. Serie de casos
Lymphatic Embolization of Protein-losing Enteropathy in the Fontan Kreutzer Circulation. Case series
Received: 23 December 2024
Accepted: 30 March 2025
La cirugía de Fontan- Kreutzer (CF) para pacientes con fisiología univentricular consiste en la generación de un circuito “en serie”, con un único ventrículo sistémico como bomba pulsátil que mantiene el gasto cardíaco, y que conecta directamente el retorno venoso sistémico a la arteria pulmonar sin interposición de un ventrículo subpulmonar funcional. (1,2) Con el paso del tiempo, este frágil modelo hemodinámico, caracterizado por la elevación de la presión venosa central y el estado de bajo gasto crónico, tiene efectos deletéreos sobre múltiples órganos. (3,4)
Un 3% a 20% de los pacientes desarrollarán enteropatía perdedora de proteína (EPP), que tiene alto impacto en la sobrevida. La EPP se define como una pérdida grave de albúmina y otras proteínas en la luz intestinal. Se sospecha a partir de la historia del paciente y el examen físico, y se confirma con la presencia de hipoalbuminemia y un elevado nivel de alfa 1 antitripsina (AT) en la materia fecal. (5) La sobrevida a los cinco años desde el diagnóstico fue descripta inicialmente tan baja como 50%; sin embargo, con los recientes avances en el diagnóstico precoz y nuevos tratamientos, actualmente la sobrevida a 5 y 10 años es del 88% y 72% respectivamente. (6,7,8)
La fisiopatología de la EPP, aunque ampliamente investigada, sigue siendo motivo de controversia y no está completamente dilucidada. Sin duda, el aumento crónico de la presión venosa sistémica sostenido en el tiempo es un factor determinante, pero por sí solo no explica completamente todos los fenómenos que conducen a la pérdida de proteínas hacia la luz intestinal. Dos observaciones clave han impulsado la búsqueda de nuevas respuestas: primero, aunque todos los pacientes con circulación de Fontan-Kreutzer presentan una presión venosa sistémica elevada, no todos desarrollan esta complicación; segundo, los estudios publicados no han mostrado una relación directa entre el valor de la presión venosa central y la severidad de la enteropatía. Se ha encontrado una mejor correlación en aquellos pacientes que, además de la presión venosa aumentada, presentan un gasto cardíaco notablemente disminuido, que determina un aumento de la resistencia periférica, con compromiso especialmente de los órganos "no vitales", como el sistema gastrointestinal. En los pacientes con EPP el flujo diastólico en la arteria mesentérica se encuentra marcadamente disminuido o incluso ausente. (9,10) Este mecanismo "compensador" resulta en una reducción significativa del flujo de perfusión y, a nivel celular, apoptosis, lo que compromete la integridad de la barrera intestinal y facilita la pérdida de proteínas. (11) La EPP ocurre en enfermedades inflamatorias gastrointestinales o sistémicas (como la enfermedad de Crohn o el lupus eritematosos sistémico) y responde favorablemente a los corticoides, lo que sugiere adicionalmente un componente inflamatorio en su fisiopatología. (12,13) De manera similar, el tratamiento con heparina ha mostrado cierta efectividad, actuando por su estructura química como una barrera para el paso de proteínas en el enterocito, dado que ambas son moléculas con carga negativa. (14) Finalmente, la reducción de la presión oncótica debido a la pérdida de proteínas provoca edema generalizado, incluso en la pared intestinal, lo que dificulta aún más la absorción adecuada de nutrientes, creando un círculo vicioso que agrava el estado clínico ya existente.
En los últimos años y con el advenimiento de nuevas modalidades de imágenes, como la linfografía por resonancia magnética nuclear o cateterismo, se ha demostrado también la dilatación patológica de los conductos linfáticos hepatoduodenales, linfangiectasias, colateralización del sistema linfático e inclusive la presencia el flujo linfático retrógrado hacia cavidades de menor presión, como los bronquios o el intestino. Estos hallazgos sugieren proponer la existencia de algún defecto congénito presente en el sistema linfático de los pacientes afectados, que actúe como otro factor predisponente para el desarrollo de esta entidad. (15,16,17,18,19,20) A partir de estas observaciones, se ha propuesto la técnica de embolización de estos conductos como un novedoso blanco terapéutico específico con resultados alentadores, inicialmente descripto por Itkin et al. (19,20,21).
El objetivo de este estudio fue evaluar la factibilidad, complicaciones y el resultado clínico-analítico de la embolización selectiva de linfáticos hepatoduodenales (ESLHD) en pacientes con circulación Fontan- Kreutzer y EPP.
Realizamos una revisión retrospectiva de la historia clínica de pacientes con CF que evolucionaron con EPP y fueron sometidos a un procedimiento de ESLHD. Definimos EPP a la presencia de signos y síntomas compatibles (edema de tejidos blandos, diarrea y ascitis) acompañada de niveles séricos de albúmina disminuidos (< 3,2 gr/dL) y elevación del clearance (Cl) de alfa 1 AT en materia fecal (Cl 24 hs > 20 mL). La técnica de linfografía y embolización percutánea se realizó según la descripción de Itkin et al. Evaluamos los niveles de albúmina sérica a los 10 días y a los 4 meses del procedimiento, y en el último control de cada paciente.
En este estudio se incluyeron cinco pacientes (P1 a P5) con CF realizada a una mediana de edad de 4 (rango 3,5-4,3) años. Tres pacientes desarrollaron el cuadro clínico característico de EPP, y en dos pacientes la presentación fue subclínica, en ambos casos con hallazgos de laboratorio de rutina. Uno se presentó con hipoalbuminemia aislada, y el otro con aumento del clearance de alfa 1 AT en la materia fecal, con proteínas y albúmina normales. Este último caso se interpretó como una EPP incipiente. Los pacientes incluidos presentaron el diagnóstico de EPP a una mediana de 7 (rango 2,3-15,3) años desde la realización de la CF.
Las características de los pacientes se encuentran en la Tabla 1.
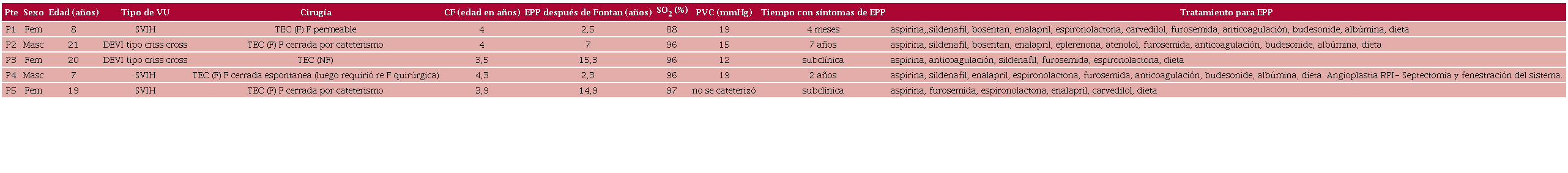
Tres pacientes tenían signos clínicos evidentes de disfunción del sistema Fontan- Kreutzer, con edemas generalizados, incluyendo ascitis, y uno de ellos edema escrotal invalidante. Dos pacientes se presentaron con formas subclínicas, el paciente P3 con leves edemas en miembros inferiores y el paciente P5 con deposiciones desligadas y edemas intermitentes en miembros inferiores. En todos los pacientes fue insuficiente el tratamiento médico instaurado para la reversión del cuadro. Los pacientes con presentación clínica más grave requirieron régimen transfusional con albúmina.
Cuatro pacientes fueron cateterizados previamente a la realización de la linfografía, para evaluar el funcionamiento del sistema Fontan. En el paciente P5, a quien solo se le objetivó aumento del clearance de alfa 1 AT, sin hipoalbuminemia, no se realizó cateterismo previo. Solamente en un paciente con restricción al flujo a nivel interauricular, el cateterismo demostró sustrato hemodinámico subyacente tratable. Este paciente requirió septectomia y fenestración del sistema. El resto de los pacientes no necesitaron procedimientos intervencionistas o quirúrgicos para optimizar el cuadro. La presión venosa central (PVC) se encontró elevada en todos los pacientes, con una mediana de 15 (rango 12-19) mmHg (Tabla 1).
Se realizaron un total de 7 procedimientos en 5 pacientes. Se logró en los cinco hallar los conductos linfáticos hepatoduodenales dilatados y tortuosos drenando en el intestino delgado. En solo un paciente se realizó además previamente linfografía por resonancia magnética, en el resto de los pacientes se realizó linfografía por cateterismo. En todos se logró la realización de la ESLHD de manera efectiva (Figura 1)
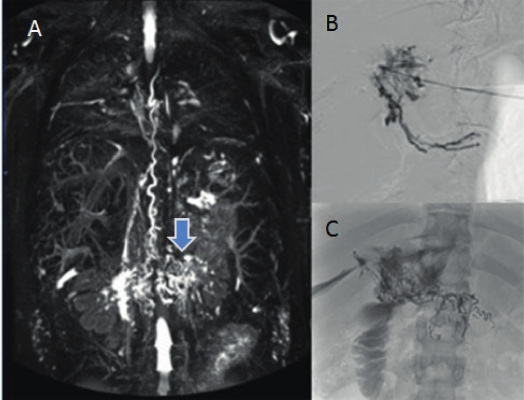
En sala de intervencionismo, bajo anestesia general se realiza la linfografía por cateterismo. Con control y guía ecográfica se accede al parénquima hepático, se coloca una aguja Chiba de 10 cm y calibre de 22 G y se la ubica cerca de la vena porta. Se asume que por anatomía los vasos linfáticos están en contigüidad a la misma. Bajo guía radioscópica se inyecta suavemente material de contraste yodado soluble en agua, mientras se retrae la aguja hasta lograr la visualización de los conductos linfáticos hepáticos que drenan a la luz del duodeno. Cuando se logra opacificar adecuadamente los linfáticos, y con la aguja en el parénquima hepático, se realiza inyección de material de contraste para confirmar cómo los linfáticos drenan gran cantidad de volumen de linfa a la luz intestinal. Luego se procede a la embolización de los linfáticos inyectando 1 a 2 mL de pegamento de n-butilcianoacrilato (n-BCA) diluido en aceite etilado (1/6) a través del mismo acceso hepático, para sellar las ramas linfáticas que van desde el hígado al duodeno.
Luego de la primera embolización todos los pacientes demostraron buena respuesta inmediata, con incremento en los valores de albúmina, en controles de laboratorio realizados dentro de los primeros diez días del procedimiento. Los pacientes P1, P3 y P5 permanecieron en su evolución con valores de albúmina dentro del rango normal, hasta el último control de cada uno respectivamente, con un seguimiento medio de 27,4 (rango 12-43) meses. (Tabla 2 y Figura 2).
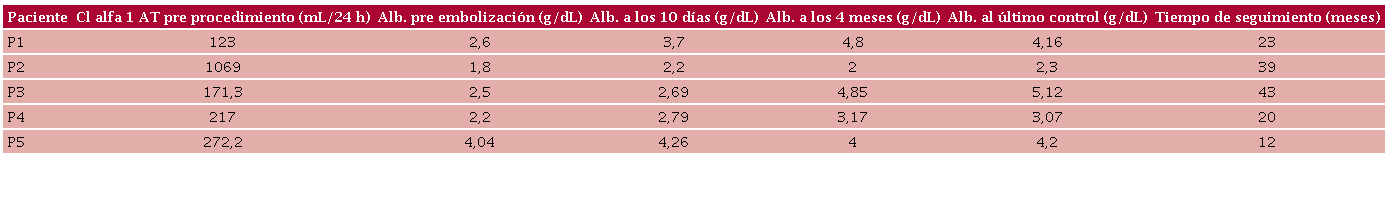
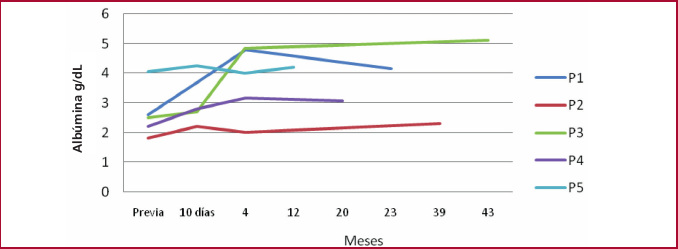
El paciente P2 requirió 2 nuevas embolizaciones por no alcanzar valores deseables de albuminemia y persistir con edemas y ascitis. Estos se realizaron a los 29 y 39 meses posteriores al primer procedimiento respectivamente. Este paciente no alcanzó valores normales de albúmina en su evolución, pero sí logró disminuir los edemas.
Al paciente P4 se le indicó septectomía auricular con fenestración del sistema concomitantemente con la ESLHD. En la actualidad permanece con valores de albúmina sérica levemente disminuidos, cercanos a la normalidad.
Clínicamente todos los pacientes demostraron mejoría franca en la calidad de vida, con disminución de los edemas, inclusive el paciente con hipoalbuminemia persistente y los dos casos subclínicos, quienes refirieron mejoría en la autopercepción de la piel, y calce de sus ropas.
Todos continúan con el mismo esquema farmacológico previo a la embolización, con suspensión de corticoides a partir del tercer mes de iniciado.
No se observaron complicaciones mayores intra o periprocedimiento. En cuanto a complicaciones menores, 3 pacientes presentaron episodio de melena leve autolimitada post procedimiento inmediato.
La EPP es una complicación grave en los pacientes con circulación Fontan, con gran impacto en la supervivencia; inicialmente se reportó 50% de sobrevida a los cinco años tras el diagnóstico. Sin embargo, gracias a los avances en diagnóstico precoz y tratamiento de la última década, la tasa de mortalidad ha disminuido significativamente; la sobrevida reportada a 5 años del diagnóstico asciende al 88%, prolongando el momento para la indicación final de trasplante cardíaco. (6,7,8)
La incidencia de EPP en la CF descripta en la bibliografía varía entre el 3% y el 20%. (6,7,8) En nuestra casuística fue del 5%. El mecanismo fisiopatológico subyacente a esta condición es complejo y multifactorial. (9,10,11) En su serie inicial, en 2017, Itkin et al. demostraron en 8 pacientes que factores como la alta presión venosa central, la dilatación y la anatomía predisponente de las conexiones linfáticas hepatoduodenales, juegan un papel crucial en su desarrollo. Estas observaciones han dado lugar a un nuevo enfoque sobre la importancia de la circulación linfática, ofreciendo un nuevo paradigma para el manejo de esta complicación de difícil tratamiento. Obliterar estas conexiones linfáticas resultó en una reducción efectiva de la fuga de proteínas en el intestino, mejorando así el estado clínico del paciente. (21) En nuestro servicio iniciamos la experiencia en 2019, con resultados inicialmente favorables, si bien el número de pacientes tratados ha sido limitado, similar a lo que se observa en cohortes internacionales.
Según la literatura disponible, esta complicación puede manifestarse tanto en el período postquirúrgico inmediato como después de muchos años. (9) En nuestra serie de pacientes, la EPP se presentó con una mediana de 7 años tras la realización de la CF. Clínicamente, dos pacientes diagnosticados de forma temprana mostraron formas leves o subclínicas de la enfermedad, mientras que los otros tres presentaron síntomas evidentes con afectación grave en su clase funcional y calidad de vida. La gravedad de la hipoalbuminemia coincidió con la de los síntomas clínicos, aunque no se observó una correlación similar con los niveles de clearance de alfa 1 AT; los pacientes más graves no mostraron niveles más elevados de esta proteína en las heces. Esto podría deberse a una disminución en la síntesis de proteínas hepáticas en los casos más graves. Cabe destacar que ninguno de nuestros pacientes presentó alteraciones en el hepatograma durante la evolución. Estas observaciones subrayan la necesidad indispensable de una detección precoz de esta complicación en todos los pacientes con CF, mediante un interrogatorio detallado y controles analíticos seriados de albúmina sérica y alfa 1 AT en heces.
Al igual que Itkin et al., (21) y Maleux et al., (22) quienes han publicado las series de casos más extensas (con 8 y 7 pacientes respectivamente), en nuestra serie también logramos demostrar, mediante linfografía por resonancia magnética o linfografía por cateterismo, la presencia de flujo linfático retrógrado desde el hígado hacia una red linfática dilatada peri intestinal en los 5 pacientes que se presentaron con EPP. Coincidentemente con esos grupos, en la mayoría de los pacientes intervenidos se lograron niveles adecuados de albúmina sérica tras la primera embolización. Sin embargo y al igual que en los grupos mencionados, en ocasiones fueron necesarios procedimientos adicionales. En nuestra experiencia un paciente requirió dos nuevas embolizaciones durante el seguimiento debido a hipoalbuminemia persistente, lo que reveló desarrollo de nuevas conexiones linfáticas. Las potenciales complicaciones más graves descriptas incluyen la progresión del material utilizado para la embolización hacia la arteria o vena hepática, las vías biliares, las venas o arterias sistémicas, o la arteria pulmonar. Además, se podría esperar el desarrollo de hipertensión portal durante la evolución y se podrían presentar sangrados locales graves. (21) Ninguna de estas complicaciones se evidenció en nuestros pacientes. Los eventos adversos luego de los procedimientos fueron todos menores, en su mayoría sangrado intestinal, manifestado como melena leve y autolimitada. Ningún paciente falleció en el seguimiento.
Algunos interrogantes que surgen en nuestro equipo de trabajo a partir de la implementación de este nuevo tratamiento incluyen:
¿Por cuánto tiempo se mantendrán los beneficios de la embolización en cada paciente, teniendo en cuenta que las mismas condiciones hemodinámicas se mantendrán en el tiempo?
¿Cuándo es el momento adecuado para suspender el tratamiento médico instaurado desde el diagnóstico de la EPP?
¿Cuándo es el momento óptimo para realizar la embolización? ¿Serán mejores los resultados cuanto más precoz la intervención?
¿Es necesario implementar linfografías adicionales de rutina durante el seguimiento para evaluar conexiones linfáticas persistentes o de nuevo establecimiento?
¿Cuándo es el momento preciso para evaluar al paciente como candidato para un trasplante cardíaco?
Debido al bajo porcentaje de incidencia de la EPP en la CF y a lo novedoso de la técnica propuesta, el número de pacientes tratados en nuestra serie fue limitado quedando inconclusas las respuestas a esos interrogantes.
La EPP es una complicación devastadora en los pacientes con circulación Fontan con gran impacto en la calidad de vida y sobrevida. El mapeo por resonancia y/o la linfografía por cateterismo fueron claves para delinear la anatomía linfática, el patrón de flujo linfático y planificar un abordaje intervencionista para su embolización.
Si bien se trata de una pequeña muestra, los resultados obtenidos tanto en aumento de los niveles séricos de albúmina, mejoría clínica y seguridad del procedimiento, resultaron promisorios para los pacientes con esta complicación. Estudios de mayor escala serán necesarios para definir la evolución a largo plazo.
Dirección para correspondencia: Carla Pasinato, dirección de mail: carlapasinato2@gmail.com



