Artículos
Recepción: 06 Agosto 2021
Aprobación: 06 Noviembre 2021
Publicación: 30 Diciembre 2021
Resumen: Los objetivos de este estudio fueron identificar y estimar a los potenciales polinizadores de Fragaria ananassa Duch., mediante el análisis del polen transportado en sus cuerpos. El estudio se llevó a cabo en una finca comercial de Las Pampitas, situada en los valles de Perico, provincia de Jujuy (Argentina). Se muestrearon e identificaron visitantes florales y otros artrópodos y se analizó la diversidad de los mismos. Las muestras de los insectos seleccionados para la obtención de polen transportado fueron procesadas siguiendo la técnica de acetólisis. Los potenciales polinizadores del cultivo de la frutilla se estimaron mediante el cálculo del índice de probabilidad de polinización. Los visitantes florales correspondieron a representantes de Hymenoptera, Diptera, Hemiptera, Lepidoptera, Coleoptera e incluso Araneae. Apis mellifera L. fue el visitante floral más frecuente y presentó más polen de frutilla que los otros insectos seleccionados. El índice de probabilidad de polinización estimó que dicha especie tuvo una alta probabilidad de ser una polinizadora. Otros polinizadores como Allograpta exotica Wiedemann, Halictidae, Meliponini e incluso Thripidae podrían complementar la acción de la abeja melífera. Este es el primer aporte al conocimiento de la polinización de F. ananassa en agroecosistemas de Jujuy.
Palabras clave: Agroecosistemas, Biodiversidad, Entomopalinología, Frutilla, Polen.
Abstract: The aims of this study were to identify and estimate the potential pollinators of Fragaria ananassa Duch. “strawberry”, through the analysis of pollen carried out on their bodies. The study was carried out on a commercial farm in Las Pampitas, located in the Perico valleys, Jujuy province (Argentina). Floral visitors and other arthropods were sampled and identified, and their diversity was analyzed. The samples of insects selected to obtain the pollen carried were processed following the acetolysis technique. The potential pollinators of the strawberry crop were estimated by calculating the pollination probability index. The floral visitors corresponded to representatives of Hymenoptera, Diptera, Hemiptera, Lepidoptera, Coleoptera and even Araneae. Apis mellifera L. was the most frequent floral visitor and presented more strawberry pollen than other selected insects. The pollination probability index estimated that this species had a high probability of being a pollinator. Other pollinators such as Allograpta exotica Wiedemann, Halictidae, Meliponini and even Thripidae could complement the action of the honeybee. This is the first contribution to the knowledge of the pollination of F. ananassa in the agroecosystems of Jujuy.
Keywords: Agroecosystems, Biodiversity, Entomopalynology, Pollen, Strawberry.
INTRODUCCIÓN
La polinización por insectos (Insecta) es la responsable de la fecundación de la mayoría de las plantas de producción alimentaria (Reyes Tirado & Johnston, 2013). Más del 75% de las principales especies de cultivos del mundo dependen, o al menos se benefician, de los polinizadores (Klein et al., 2007), constituyendo un servicio ecosistémico muy importante, pero también gravemente amenazado (Potts et al., 2010) y subestimado o incluso ignorado en las políticas nacionales o internacionales (Klatt et al., 2014).
La “frutilla” (Fragaria ananassa Duch.) (Rosaceae) es una especie surgida del cruce accidental de F. virginiana Mill y F. chiloensis (L.) Mill (Miserendino, 2010). Su fruto es agregado y cada receptáculo floral contiene múltiples carpelos (Free, 1993). Aunque sus variedades comerciales se autofecundan de manera espontánea o por acción del viento, los insectos también son importantes agentes (Nye & Anderson, 1974), al transportar el polen entre flores de diferentes plantas, promoviendo la polinización cruzada (Jaycox, 1970; Zebrowska, 1998).
Varios estudios han destacado el potencial de los insectos como polinizadores de la frutilla. Nye & Anderson (1974) encontraron que la abeja melífera, Apis mellifera L., transportó más polen que otros visitantes florales, por lo que sus visitas florales tenían un efecto positivo en el desarrollo de los frutos. Por su parte, Malagodi Braga (2002) también registró a A. mellifera y abejas sin aguijón (Meliponini) transportando polen, mientras que Albano et al. (2009a; b) categorizaron a los potenciales polinizadores, en función de la frecuencia y la actividad en las flores, en tres grupos principales: A. mellifera, Syrphidae o “moscas de las flores” (Diptera) y abejas nativas, principalmente Halictidae. Apis mellifera ha sido considerada la especie polinizadora más importante de monocultivos en el mundo (Klein et al., 2007), inclusive en la Argentina, ya sea domesticada o silvestre (Sáez et al., 2014). Los Syrphidae son insectos vistosos que adoptan la apariencia de abejas o avispas (Maza et al., 2014). Sus larvas son agentes de control biológico y los adultos son polinizadores (Díaz et al., 2020). Por su parte, Halictidae es una familia relativamente diversa de abejas con distintos grados de sociabilidad, potencialmente utilizables para la polinización de cultivos (Dalmazzo, 2012).
En la Argentina, los polinizadores nativos adquieren más relevancia e interés. Tal es el caso de Bombus pauloensis Friese, “abejorro”, (antes conocido como Bombus atratus Franklin) en Tucumán, por su tamaño, pilosidad, polinización vibrátil, atracción por la frutilla y forrajeo a temperaturas bajas (Díaz et al., 2013), y más recientemente, de Plebeia catamarcensis (Holmberg), en Santa Fe, por la abundancia de colonias en áreas urbanas y suburbanas, y su naturaleza inofensiva, a diferencia de la abeja melífera y el abejorro (Vossler et al., 2018). No obstante, faltan estudios dirigidos hacia otros potenciales polinizadores, tradicionalmente “no manejables”, pero que pueden estar presentes de manera espontánea en los cultivos, como “moscas” (Diptera), “mariposas” (Lepidoptera), “escarabajos” (Coleoptera), “chinches” (Hemiptera) e incluso “trips” (Thysanoptera). Además, la dependencia de un único polinizador en todo el mundo es una preocupación internacional, ya que sus poblaciones se han visto amenazadas por múltiples factores y están en declive (Potts et al., 2010). Esto propicia aún más a la búsqueda e identificación de potenciales polinizadores en regiones donde la intensificación agrícola desestabiliza aún más la situación de los polinizadores nativos, como el noroeste argentino (NOA).
El polen es un recurso forrajeado por los polinizadores, dado que les proporciona cerca del 20% de los carbohidratos que necesitan y el total de proteínas (Ricou et al., 2014). Nates Parra (2005) revisó la importancia de las abejas nativas en la polinización y destacó que los requisitos que definen a un buen polinizador son: la atracción natural hacia las flores, la fidelidad floral, el tamaño corporal y el comportamiento adecuado para remover y transportar polen viable y compatible en grandes cantidades y depositarlo en los estigmas, cuando éstos se hallan receptivos (Freitas, 1998). El polen disperso por todo el cuerpo del insecto es considerado como el más importante para la polinización y, por ende, los visitantes “contaminados” con polen son los que tienen más probabilidad de transferir el polen al estigma de las flores (Alves dos Santos et al., 2016). En este sentido, el polen puede ser analizado para distinguir los insectos que transportan una cantidad considerable de polen, y así, estimar su probabilidad de ser polinizadores.
La provincia de Jujuy es una de las principales productoras de frutilla en la Argentina. El desarrollo de esta actividad se concentra en los valles de Perico, departamento El Carmen (Fernández et al., 2011; Kirschbaum et al., 2019). Para esta región y el NOA en general, Kirschbaum et al. (2015) citaron especies de plagas frecuentes en frutilla como Tetranychus urticae C.L. Koch “arañuela roja”, Phytonemus pallidus Banks “ácaro del ciclamen”, Frankliniella schultzei (Trybom), Frankliniella gemina Bagnall “trips”, Aphididae “pulgones” y organismos benéficos para el control biológico como Orius insidiosus Say (Hemiptera), Hippodamia convergens Guerin Meneville, Eriopis connexa Germar, Cycloneda sanguinea L. (Coleoptera). Sin embargo, no informan sobre especies como visitantes florales frecuentes o potenciales polinizadores del cultivo. Los objetivos del presente estudio fueron: identificar y estimar a los potenciales polinizadores de F. ananassa mediante el análisis del polen transportado en sus cuerpos y ampliar el conocimiento sobre los artrópodos asociados a F. ananassa, en los valles de Perico de Jujuy.
MATERIALES Y MÉTODOS
Los muestreos se realizaron en una finca comercial de frutilla situada en localidad de Las Pampitas, Perico (24º 23´ 37 0´´S, 65º 04´ 01 1´´O, 905 m), aproximadamente a 35 km de San Salvador de Jujuy, y en los días 16 y 30 de noviembre (F1 y F2), y 7 y 14 de diciembre de 2017 (F3 y F4). La región de los valles de Perico presenta un clima subtropical serrano, templado con estación seca, con veranos moderadamente cálidos (22-24 °C), inviernos frescos (10-12 °C), precipitaciones concentradas en la época estival (550-750 ml) y vientos variables en dirección y velocidad durante todo el año (Brawn Wilke et al., 2001). Fitogeográficamente, la región se encuentra en un ecotono entre las provincias fitogeográficas del Chaco y Yungas, (Cabrera, 1976) con remanentes de vegetación nativa coexistentes con especies exóticas naturalizadas y cultivos de tipo hortícola, ornamental y “tabaco” (Nicotiana tabacum L.).
Trabajo de campo
Para las observaciones directas de los artrópodos visitantes florales, en cada fecha se eligieron al azar cinco grupos de 20 a 25 plantas de frutilla en flor; cada grupo fue observado durante 10 min, entre las 09:00 y 13:00 (Fig. 1 a). Los visitantes se capturaron y se colocaron individualmente en frascos con etanol al 70%. También se efectuaron barridos con red entomológica en transectas en formato “X” y se colocaron trampas de caída bee bowls (Gill & O´Neal, 2015). Cada transecta fue muestreada dos veces, efectuando 10 barridos con la red sobre el follaje, a intervalos de siete pasos (Fig. 1 b). Las muestras obtenidas se colocaron en bolsas de tela y estas a su vez, en frascos mortíferos. Las trampas de caída se elaboraron con envases de plástico de 100 cm. forrados con papel contact celeste y a cada una se le agregó agua con detergente (10 cm. de detergente en un litro de agua). En total se colocaron seis trampas (Fig. 1 c), cada una sobre un soporte de hierro a la altura de las plantas (aproximadamente 30 cm), asegurada con cinta adhesiva y con permanencia durante las cuatro horas de muestreo. Luego se cerraron y etiquetaron para su limpieza y revisión. Todo el material recolectado fue depositado en el Departamento de Entomología del Instituto de Biología de la Altura de la Universidad Nacional de Jujuy (INBIAL-UNJu) para su estudio taxonómico. También se colectaron flores del cultivo, que fueron preservadas según las técnicas convencionales de herborización.
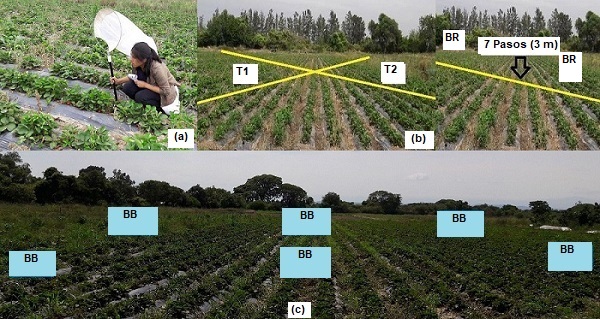
Fig 1. Métodos de muestreo aplicados en el cultivo de Fragaria ananassa, en una finca comercial de Las Pampitas, Jujuy.
a. Observaciones directas. b. Barridos con red en transectas en formato “X”. c. Trampas de caída bee bowls.
T1 = Transecta 1; T2 = Transecta 2; BR = Barridos con red; BB= Trampas de caída bee bowls.
Trabajo de laboratorio
Identificación y selección de ejemplares. El proceso de identificación de los ejemplares recolectados se realizó bajo microscopio estereoscópico Nikon SMZ 800, mediante claves dicotómicas específicas, material bibliográfico (Association of Official Agricultural Chemist, 1965; Roig Juñent et al., 2014) y consultas a especialistas. Los individuos que no pudieron identificarse a nivel de género y/o especie se categorizaron como morfoespecie, de acuerdo al criterio de Weyland & Zaccagnini (2008).
Obtención de muestras del polen transportado. Después de la identificación, los ejemplares de un mismo taxón se individualizaron en un frasco con etanol al 70%, para la preservación del polen asociado al mismo. Posteriormente se seleccionaron aquellos ejemplares pertenecientes a los principales órdenes asociados a la polinización: Hymenoptera, Diptera, Coleoptera, Lepidoptera y Hemiptera. Se extrajeron cabeza, tórax, abdomen y apéndices de los especímenes de un tamaño igual o superior a un centímetro. Este procedimiento se realizó bajo microscopio estereoscópico Leica L2, con pinza y aguja histológica y las partes extraídas se preservaron en vasos de precipitación. Por otra parte, los ejemplares de tamaño inferior a un centímetro no se diseccionaron y fueron colocados en tubos Eppendorf.
Procesamiento y observación de polen. Para la extracción del polen, a todas las muestras de los insectos seleccionados, se les agregó hidróxido de potasio al 10%, con ayuda de una pipeta Pasteur, se maceraron con varillas de vidrio y se expusieron al calor durante 10 min (Kearns & Inouye, 1993). Los vasos de precipitación se calentaron a fuego directo (mechero Bunsen) y los tubos Eppendorf cerrados a baño María. A continuación, se realizó la acetólisis (Erdtman, 1960), técnica convencional de la palinología que permite observar la exina de los granos de pólenes, principal carácter de valor diagnóstico de los tipos polínicos. El polen obtenido de cada taxón seleccionado fue colocado en tubos Eppendorf para su conservación. Para facilitar la identificación del polen de frutilla, se extrajeron las anteras de las flores recolectadas del cultivo y se maceraron en cajas de Petri, siguiendo el protocolo mencionado anteriormente. La obtención y el procesamiento de las muestras de polen se realizó en el Laboratorio de Palinología de la Facultad de Ciencias Agrarias de la Universidad Nacional de Jujuy (LABPAL- UNJu). El polen de frutilla se incorporó a la Palinoteca de Referencia del Laboratorio de Palinología (PAL-JUA).
La observación del polen de frutilla se realizó a través de preparaciones microscópicas de las muestras obtenidas, selladas con parafina, bajo microscopio óptico Leica DM 500 a una magnificación de 400x y 1000x. La identificación de otros tipos polínicos se efectuó con ayuda de la palinoteca de referencia, atlas polínicos (Markgraf & D´Antoni, 1978) y consultas a especialistas. La nomenclatura polínica, es decir, la designación de los nombres a los tipos polínicos, se estableció siguiendo los criterios de Joosten & De Klerk (2002) y De Klerk & Joosten (2007). Las fotografías del polen de frutilla se tomaron con la cámara digital Leica ICC50 incorporada al microscopio.
Análisis estadístico
Como los datos no cumplieron los supuestos de normalidad y homogeneidad, se realizó la prueba no paramétrica de Kruskall Wallis (H), para hallar diferencias significativas entre las fechas de muestreo (P ≤ α), con un nivel de significancia α = 0,05 y la prueba post-hoc por pares de Mann Whitney, con corrección de Bonferroni, para saber cuáles eran las fechas diferentes, utilizando el software estadístico InfoStat (Di Rienzo et al., 2008). De igual modo se procedió para los métodos de muestreo (α = 0,05). Se determinó en ambos casos abundancia (N), riqueza (S), índice de Dominancia (D) y de Shannon Wiener (H´). Asimismo, éstos últimos índices se compararon a través de la prueba . de diversidad. Dichos análisis se efectuaron con el software estadístico PAST versión 4.01 (Hammer et al., 2001).
El análisis de polen se efectuó mediante un conteo de hasta 600 granos de polen en una muestra de polen de cada taxón de insectos procesado. Con este dato se determinó la abundancia y porcentaje de polen de frutilla. Por último, para estimar a los potenciales polinizadores del cultivo de frutilla, mediante el polen transportado, se adaptó el índice de probabilidad de polinización (PPI) de Ne´eman et al. (1999).

Siendo:
PCP: la proporción de polen transportado de frutilla correspondiente a cada taxón de insectos procesado (PtFr), respecto a la suma polínica total del polen transportado de frutilla en todos los taxa procesados (PTFr = ∑PtFr). (PCP = PtFr/PTFr).
PBP: la proporción de individuos de cada taxón de insectos procesado, que presentó polen transportado de frutilla. Como en algunos taxa se procesaron más de un individuo, se consideró que todos ellos transportaron, por lo menos, un grano de polen de frutilla (PBP = 1).
El PPI refleja la probabilidad de un insecto como polinizador. Valores cercanos a 0 indican una baja probabilidad, mientras que valores cercanos a 1 indican una alta probabilidad.
RESULTADOS
Visitantes florales y otros artrópodos en frutilla
Se registraron 547 artrópodos, identificándose ocho órdenes, un suborden, 28 familias, 25 géneros, 31 especies y 59 morfoespecies. Para la clase Insecta se determinaron siete órdenes y 27 familias, y para la clase Arachnidae, sólo el orden Araneae.
Los órdenes que se destacaron por su abundancia fueron: Thysanoptera (286), Hymenoptera (118) y Hemiptera (61), mientras que los mejor representados por su riqueza fueron Hymenoptera (cuatro géneros, cuatro especies y 34 morfoespecies), Coleoptera (ocho géneros, nueve especies y cinco morfoespecies) y Hemiptera (seis géneros, seis especies, cinco morfoespecies y una ninfa indeterminada). A partir del método de observaciones directas se registraron 59 visitantes florales, en su mayoría abejas, pero sólo se capturaron 27. Apis mellifera fue la visitante floral más frecuente, seguida de Allograpta exotica Wiedemann y Geocoris sp. Del método de barridos con red en transectas se recolectaron 229 individuos del follaje, principalmente Gelechiidae, Cicadellidae y Caliothrips phaseoli (Hood). Y con el método de trampas bee bowls se obtuvieron 259 individuos, siendo las especies más relevadas C. phaseoli, Frankliniella australis Morgan y F. schultzei, todas pertenecientes a Thripidae (Tabla I).
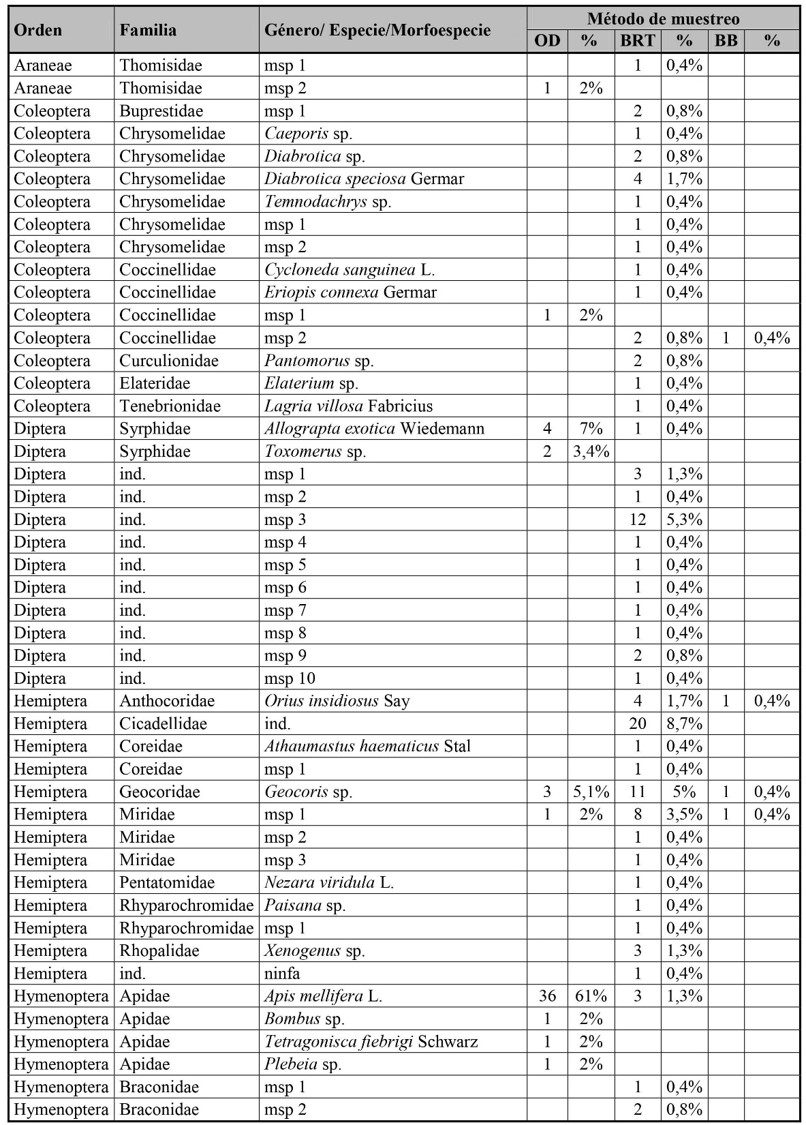
Tabla I. Diversidad taxonómica, abundancia y porcentaje de artrópodos por método de muestreo en el cultivo de Fragaria ananassa, Las Pampitas, Jujuy.
msp = morfoespecie. Método de muestreo: OD = observaciones directas; BRT = barridos con red en transectas; BB = trampas de caída bee bowls; % = porcentaje.
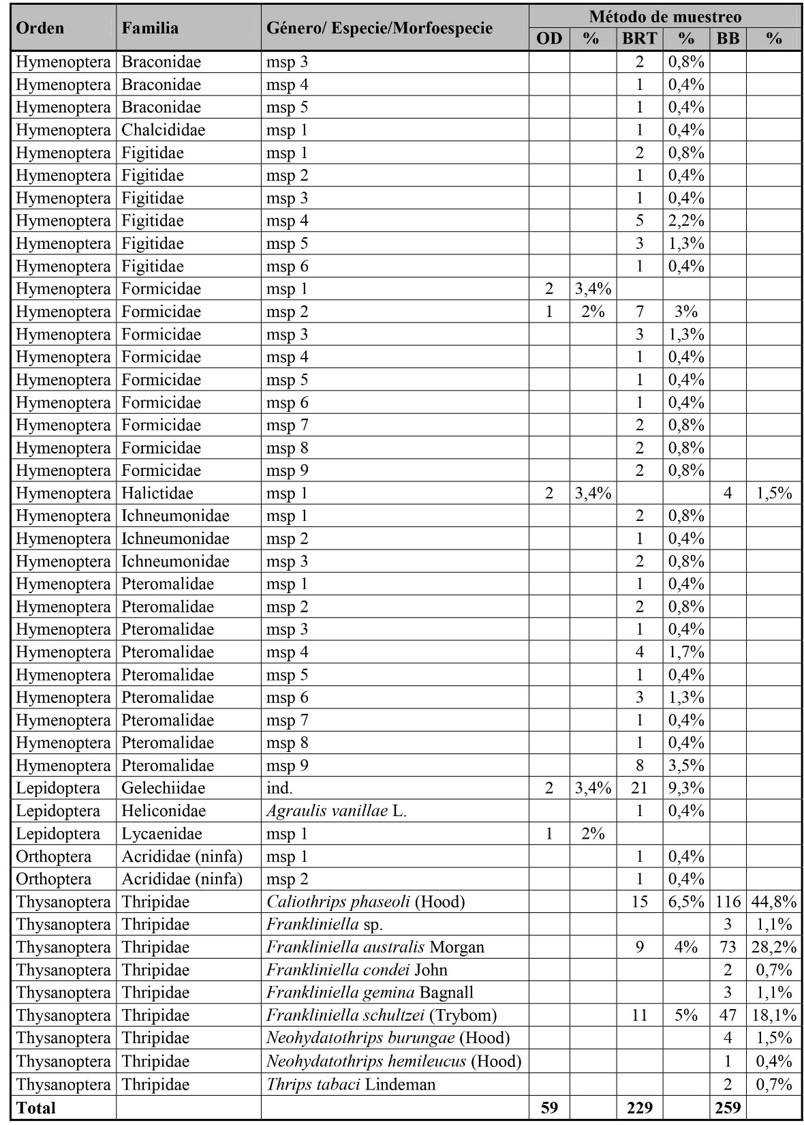
Tabla I (cont.). Diversidad taxonómica, abundancia y porcentaje de artrópodos por método de muestreo en el cultivo de Fragaria ananassa, Las Pampitas, Jujuy.
msp = morfoespecie. Método de muestreo: OD = observaciones directas; BRT = barridos con red en transectas; BB = trampas de caída bee bowls; % = porcentaje.
La prueba de Kruskall Wallis arrojó diferencias significativas entre las fechas (H = 22,89, H corregido = 30,46, P < 0,0001) y entre los métodos de muestreo (H = 82,01, H corregido = 108,4, P < 0,0001). La prueba de Mann Whitney determinó que la fecha 1 fue significativamente diferente de las otras fechas (F1 y F2: P = 0,003, F1 y F3: P < 0,0001, F1 y F4: P < 0,0001). Asimismo, el método de barridos con red en transectas fue significativamente diferente de los otros métodos empleados (OD y BRT: P < 0,0001, BB y BRT: P < 0,0001).
La prueba . de diversidad verificó diferencias significativas entre el índice de Dominancia de la fecha 2 y el de las otras fechas (F2 y F1 . Dominancia = -3,4414, df = 107,93, P = 0,0008; F2 y F3 . Dominancia = 5, 8353, df = 305,97, P < 0,0001; F2 y F4 . Dominancia = 5,4706, df = 308,41, P < 0,0001). También entre el índice de Shannon Wiener de las fechas 1 y 2, y el de las fechas 3 y 4 (F1 y F3 . Shannon Wiener = -4,8522, df = 62,441, P < 0,0001; F1 y F4 . Shannon Wiener = 3,8139, df = 64,317, P = 0,0003; F2 y F3 . Shannon Wiener = -7,1948, df = 370, 82, P < 0,0001; F2 y F4 . Shannon Wiener = -5,8907, df = 345,88, P < 0,0001) (Tabla II).
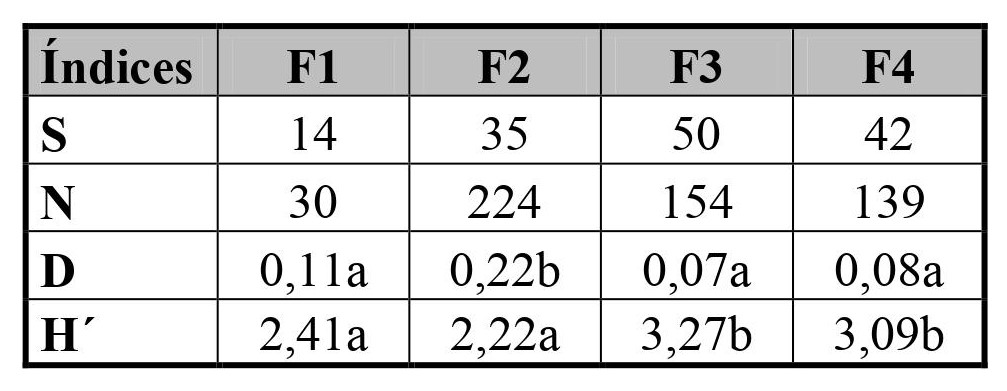
Tabla II. Riqueza, abundancia e índices de diversidad de artrópodos, por fecha de muestreo, en el cultivo de Fragaria ananassa, Las Pampitas, Jujuy.
S = riqueza; N = abundancia; D = índice de Dominancia; H´ = índice de Shannon Wiener; F1 = 16 de noviembre; F2 = 30 de noviembre; F3 = 7 de diciembre; F4 = 14 de diciembre.
Para los métodos de muestreo, la prueba t de diversidad verificó diferencias significativas entre los índices de Shannon Wiener y Dominancia del método de barridos con red en transectas y los de los métodos restantes (BRT y OD . Shannon Wiener = -10,079, df = 77,818, P < 0,0001; BRT y OD . Dominancia = 4,7608, df = 59,392, P < 0,0001; BRT y BB . Shannon Wiener = 22,9, df = 470,31, P < 0,0001; BRT y BB . Dominancia = -15,314, df = 288,64, P < 0,0001). No se observaron diferencias significativas entre los índices de las observaciones directas y las trampas de caída bee bowls (Tabla III).
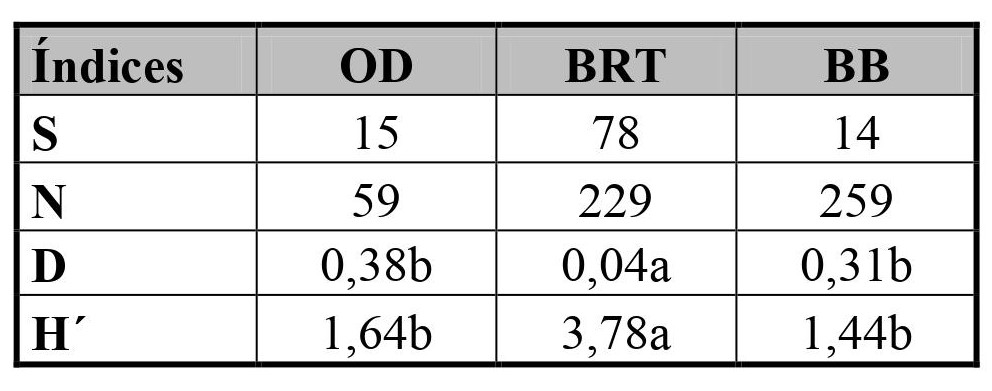
Tabla III. Riqueza, abundancia e índices de diversidad de artrópodos, por método de muestreo, en el cultivo de Fragaria ananassa, Las Pampitas, Jujuy.
S = riqueza; N = abundancia; D = índice de Dominancia; H´ = índice de Shannon Wiener; OD = observaciones directas; BRT = barridos con red en las transectas; BB = trampas de caída bee bowls.
Potenciales polinizadores
De los artrópodos recolectados, se seleccionaron y procesaron 47 insectos pertenecientes a 19 taxa (Tabla IV). Todos los insectos presentaron polen transportado, pero sólo en A. mellifera y A. exotica se alcanzó a contar 600 granos de distintos tipos polínicos, en el resto se encontró escaso polen. En función de los 600 granos de polen contados, los ejemplares de A. mellifera fueron los que presentaron mayor abundancia y porcentaje de polen de frutilla, que el resto de los insectos procesados (Tabla V; Fig. 2). El PPI estimó que, del conjunto de los insectos procesados, A. mellifera fue la especie con la probabilidad más alta de ser una polinizadora del cultivo de frutilla (PPI: 0,72), seguida de Diabrotica speciosa Germar (PPI: 0,14) y Coccinellidae (PPI: 0,03) (Tabla VI).
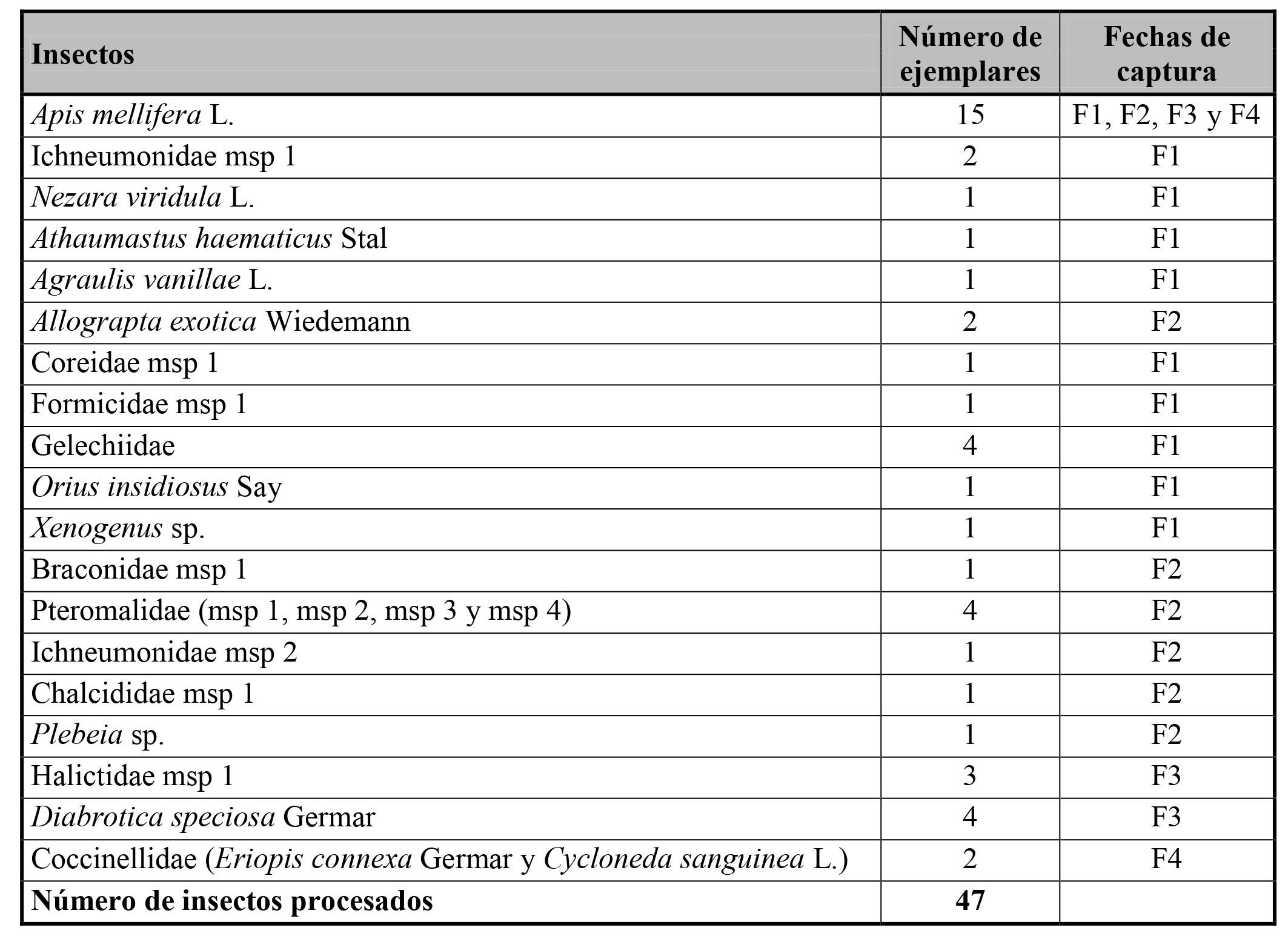
Tabla IV. Insectos seleccionados para el procesamiento de obtención de polen de Fragaria ananassa.
F1 = 16 de noviembre; F2 = 30 de noviembre; F3 = 7 de diciembre; F4 = 14 de diciembre.
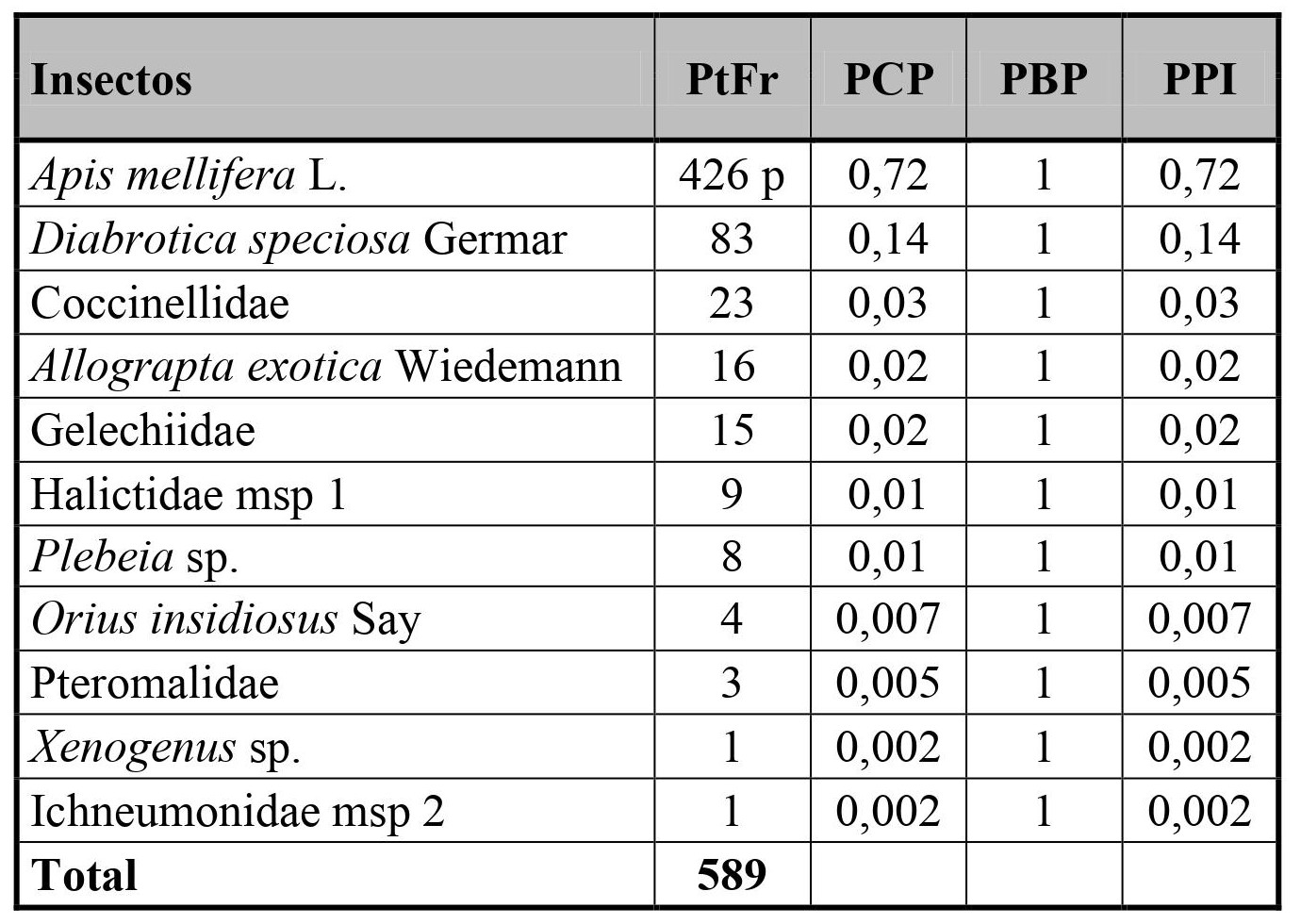
Tabla V. Abundancia y porcentaje de polen transportado de Fragaria ananassa, a partir del conteo de polen en los insectos procesados.
F1 = 16 de noviembre; F2 = 30 de noviembre; F3 = 7 de diciembre; F4 = 14 de diciembre; % = porcentaje.
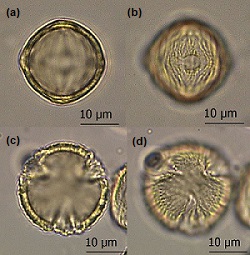
Fig 2. Grano de polen de Fragaria ananassa.
a-b. Vista polar. c-d. Vista ecuatorial. (Escala = 10 µm).
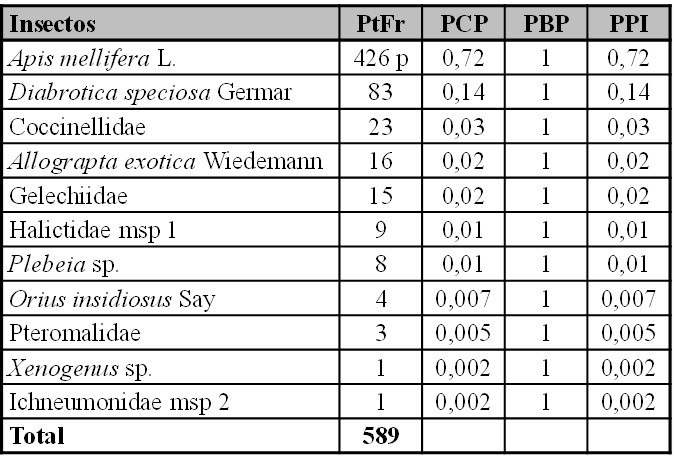
Tabla VI. Potenciales polinizadores del cultivo de Fragaria ananassa, Las Pampitas, Jujuy.
p = promedio de las abundancias de polen de Fragaria ananassa en Apis mellifera; PtFr = polen transportado de Fragaria ananassa correspondiente a cada taxón; PTFr: suma polínica total de Fragaria ananassa de los taxa considerados; PCP: proporción de polen transportado de Fragaria ananassa (PtFr/PTFr); PBP:proporción de individuos que presentó polen transportado de Fragaria ananassa. PPI: (PCP * PBP).
DISCUSIÓN
Los visitantes florales de frutilla en las Pampitas correspondieron a representantes de Hymenoptera, Diptera, Hemiptera, Lepidoptera, Coleoptera e incluso Araneae, señalados también en los estudios de Malagodi Braga (2002) y Albano et al. (2009a) en Brasil y Portugal, respectivamente. Para la Argentina, Olivo et al. (2015) y Kirschbaum et al. (2015) también reportan representantes de dichos órdenes en cultivos de frutilla del NOA, pero no mencionan especies potencialmente polinizadoras. Por lo tanto, este estudio aporta los primeros registros de visitantes florales de frutilla en los valles de Perico de Jujuy.
Las características menos especializadas de la flor de frutilla, como su simetría radial y su forma rotácea, el néctar de fácil acceso y las anteras expuestas permiten la atracción de diversos visitantes florales (Malagodi Braga, 2002). La principal visitante floral fue A. mellifera, ampliamente reportada en diversos estudios como la principal especie polinizadora de frutilla, tanto por su alta capacidad de transportar polen (Nye & Anderson, 1974; Malagodi Braga, 2002) como por su alta frecuencia en las flores (Albano et al., 2009a; b), rasgos propios de la especie que también se constataron en este estudio. Svensson et al. (1991) aseguran que la abeja melífera, y las abejas en general, distribuyen el polen de forma homogénea en los receptáculos, aumentando el número de aquenios fecundados por fruto. Su probabilidad estimada en este estudio para ser una polinizadora (PPI) fue de 0,72, igual a la proporción de polen conespecífico (PCP: 0,72), ya que todos los ejemplares analizados presentaron polen de frutilla (PBP: 1). Para los valles de Perico, se interpreta que, de los insectos analizados, un ejemplar de A. mellifera puede transportar un 72% de polen de frutilla, una cantidad que satisface el desarrollo del fruto, el cual, requiere de un 70 u 80% de pistilos fertilizados (Carew et al., 2003).
Por su parte, A. exotica fue la visitante floral más frecuente, después de A. mellifera. En los que respecta a las moscas de las flores, estudios mencionan a las del género Eristalis (Nye & Anderson, 1974; Albano et al., 2009a; b) y a Episyrphus balteatus (De Geer) y Eupeodes latifasciatus (Macquart) (Hodgkiss et al., 2018), como polinizadoras de frutilla. Sin embargo, en la Argentina, A. exotica, junto con Toxomerus son abundantes en los sistemas hortícolas y agroecosistemas (Maza, 2018; Díaz et al., 2020; Torretta et al., 2021). La probabilidad estimada para A. exotica fue de un 2%, muy inferior a la de la abeja melífera, posiblemente por los escasos ejemplares recolectados y procesados. Otra explicación puede ser el hábito de la especie de “limpiar” su cuerpo (acicalamiento) para recolectar todo el polen adherido y luego consumirlo; sumado a esto, la escasa pilosidad que presenta y que no permite la adhesión de una importante cantidad de polen (Zamora Carrillo et al., 2011). No obstante, las visitas florales combinadas de especies de moscas poco pilosas en la frutilla pueden producir un aumento de pistilos fertilizados (Hodgkiss et al., 2018).
Otros visitantes poco frecuentes y con escaso polen de frutilla fueron las Apoidea nativas Halictidae y Plebeia sp., también reconocidas como polinizadoras (Dalmazzo, 2012; Vossler et al., 2018). Al respecto, se indagó que hay un efecto complementario en la polinización de la frutilla, cuando diversas especies de apoideos visitan sus flores. Chagnon et al. (1993) explicaron este efecto en la deposición del polen en el receptáculo: los apoideos de tamaño medio, al pivotar en la parte superior del receptáculo, polinizan los pistilos de la región apical, mientras que, los de tamaño pequeño, al circular en los estambres, polinizan los pistilos de la región basal. Comportamientos similares en ambos grupos también fueron observados por Albano et al. (2009b) para A. mellifera y otros apoideos más grandes como Andrenidae y Megachilidae, en la región apical del receptáculo y para los apoideos pequeños como Halictidae, en la región basal.
Por su parte, Gelechiidae, que presentó escaso polen de frutilla, reúne a especies perjudiciales de microlepidópteros de importancia agrícola (Urretabizkaya, 2010). Las “chinches ojonas” del género Geocoris, registradas como visitantes florales, son especies que actúan como depredadoras de plagas de frutilla (Lemme et al., 2000; Gómez Martínez, 2006; Salas Araiza et al., 2014; Olivo et al., 2015), lo cual explicaría sus visitas a las flores. Diabrotica speciosa, E. connexa y C. sanguinea, conocidas como “mariquitas”, no fueron observadas como visitantes florales y para los escasos individuos analizados, se obtuvo una baja probabilidad de polinización (PPI: 0,14 y 0,03, respectivamente). Los Coleoptera polinívoros pueden permanecer más tiempo en las flores de frutilla, a diferencia de otros insectos que son más activos al visitar flores, como las abejas (Albano et al., 2009a), lo cual indica su bajo potencial como polinizador. Sin embargo, de las especies mencionadas, E. connexa y C. sanguinea se destacan por ser enemigos naturales de plagas de frutilla (Lemme et al., 1996; Kirschbaum et al., 2015), por lo que, al ser especies benéficas, deben ser igualmente valoradas en el cultivo.
Caliothrips phaseoli, la especie más abundante de los artrópodos recolectados, fue hallada como una de las principales plagas de frutilla en Salta (Olivo et al., 2015). Con este registro, se amplía el complejo de trips asociados al cultivo de frutilla en Jujuy, conformado por Scirtidothrips torquatus (Hood) encontrado en hojas, y F. schultzei con F. gemina, en las flores (Kirschbaum et al., 2015; Zamar et al., 2018). Los trips pueden inducir la polinización, al transportar cientos de granos de polen (Williams et al., 2001). Al respecto, especies del género Frankliniella sp. son citadas como potenciales polinizadores del “mango” (Mangifera indica L.) al acarrear granos de polen tanto en estado adulto como en estado inmaduro (Retana Zalazar & Rodríguez Arrieta, 2015).
Si bien comparar la diversidad de artrópodos entre las fechas y los métodos de muestreo no fue uno de los objetivos propuestos, se observaron diferencias para ambos casos. En la comparación por fecha, la fecha 1 difirió significativamente del resto, esto puede atribuirse a la baja riqueza y abundancia de artrópodos obtenidos en ese día (N = 30, S = 14). Deben agregarse también los vientos variables comunes en el área de estudio (Brawn Wilke et al., 2001), que afectaron el normal desarrollo de los muestreos. El índice de Dominancia presentó valores cercanos a 0, reflejando que los taxa tenían la misma representatividad y que no había una especie dominante (Moreno, 2001). El índice de Dominancia de la fecha 2 (D = 0,22) difirió significativamente del resto, por la elevada abundancia de Thysanoptera en ese momento. Asimismo, los valores del índice de Shannon Wiener reflejaron una distribución equitativa de artrópodos (Moreno, 2001). Sin embargo, las fechas 1 y 2 (H´= 2,41 y 2,22, respectivamente), difirieron significativamente de las fechas 3 y 4 (H´= 3,27 y 3,09), debido a la mayor riqueza de taxa colectados en las dos últimas fechas, aunque las abundancias fueron menores a la de la fecha 2 y mayores a la de la fecha 1. En base a los datos obtenidos, se puede afirmar que la diversidad de artrópodos es alta, pero con una variación diaria o semanal que puede depender de factores vinculados al manejo de la producción, como la aplicación de insecticidas o plaguicidas. Asimismo, Olivo et al. (2015) demostraron que, en un cultivo de frutilla, la comunidad de artrópodos en un mismo predio varía con los años, siendo más diversa en cultivos con plantas de diferentes edades.
Al comparar los métodos de muestreo, el de barridos con red en transectas difirió significativamente del resto, en riqueza (S = 78), dominancia (D = 0,04) y equidad (H´= 3,78). Este método proporcionó una alta y equitativa diversidad de familias, principalmente Thripidae, Diptera, Pteromalidae, Formicidae, Figitidae, Cicadellidae y Geocoridae, pero fue poco efectivo para capturar abejas o moscas de las flores. Como lo afirma Gill & O´Neal (2015), los barridos con red permiten capturar grandes cantidades de artrópodos del follaje. A diferencia de este método, las observaciones de visitantes florales y las trampas de caída bee bowls, se asemejaron en los parámetros medidos (D = 0,38 y 0,31, H´= 1,64 y 1,44, respectivamente), ya que, en cada caso, hubo especies particularmente abundantes. En las observaciones, A. mellifera fue la especie más abundante, además de que pudo ser fácilmente identificada en el momento de su registro. Aunque es probable que se hayan cometido sesgos en este método, porque sólo se registraron los visitantes que se acercaron a las flores y se posaron en ellas, ignorando que otros estuviesen en el interior de las flores, como Thysanoptera y diminutos Hymenoptera (Albano et al., 2009a). Por su parte, las trampas de caída bee bowls tuvieron un efecto distinto a lo esperado; en contraste con su nombre, se comportaron como trampas de Thysanoptera. El color celeste, elegido para las trampas, pudo haber influido en la atracción de C. phaseoli, como lo observado por Bravo Portocarrero et al. (2020) en Frankliniella sp.
Además de polen de frutilla, se registraron otros tipos polínicos, principalmente Fabaceae, Apiaceae, Rapistrum, Senecio, Eucalyptus, Senecio cremeiflorus, Vachellia y Sapium haematospermun, cuyas especies botánicas son de polinización entomófila, mientras que Amaranthaceae-Chenopodiaceae, son de polinización anemófila. Esta riqueza de polen sugiere que los insectos estarían actuando como vectores de polen de otras especies, muchas de ellas, circundantes al cultivo. La importancia de la vegetación de los bordes de cultivos se basa en la provisión de recursos (polen, néctar) y sitios de cría o atracción sexual sobre las flores o inflorescencias o en interior de las mismas (Nicolson et al., 2007). Por lo tanto, pueden albergar a los polinizadores de cultivos y asegurar la continuidad de éstos en los agroecosistemas (Chacoff & Aizen, 2006; Sáez et al., 2014), a través de un manejo adecuado que provea diversas oportunidades acordes a los requerimientos de los polinizadores (Klein et al., 2007).
El sistema de cultivo de frutilla de Jujuy presenta un importante complejo de polinizadores potenciales, identificados mediante la adecuación de la metodología de obtención de polen transportado. Apis mellifera es la especie con mayor probabilidad de polinizar la frutilla, dentro del conjunto de insectos analizados. Otros polinizadores como A. exotica, Halictidae, Meliponini e incluso Thripidae podrían complementar la acción de la abeja melífera. Sin embargo, son necesarias investigaciones que analicen la dinámica estacional de los polinizadores y su comportamiento en las flores, en función de las variedades cultivadas y sus períodos de floración en los Valles de Perico de Jujuy.
AGRADECIMIENTOS
A los proyectos PUE 22920170100027CO (INECOA CONICET JUJUY), A/0192 y F/0026 (SECTER-UNJu). A la Dra. Noelia Maza (Facultad de Agronomía y Zootecnia, UNT, Tucumán), al Dr. Leopoldo Álvarez (División Entomología, Museo de La Plata, UNLP, La Plata) y a los equipos de Entomología del INBIAL-UNJu y del Laboratorio de Palinología de la FCA-UNJu. A los revisores, por los valiosos aportes realizados al trabajo. A la familia Fernández por facilitarnos su finca para la realización de este estudio.
REFERENCIAS
Albano, S., Salvado, E., Borges, P.A.V., & Mexia, A. (2009a) Floral visitors, their frequency, activity rate and Index of Visitation Rate in the strawberry fields of Ribatejo, Portugal: selection of potential pollinators. Part 1. Advances Horticultural Science, 23(4), 238-245.
Albano, S., Salvado, E., Duarte, S., Mexia, A., & Borges, P.A.V. (2009b) Pollination effectiveness of different strawberry floral visitors in Ribatejo, Portugal: selection of potential pollinators. Part 2. Advances in Horticultural Science,23(4), 246-253.
Alves dos Santos, I., Silva, C.I., Pinheiro, M., & Peixoto Kleinert, A.M. (2016) Quando um visitante floral é um polinizador? Rodriguésia, 67(2), 295-307.
Association of Official Agricultural Chemist. (1965) Official methods of analysis. Bioestadística: principios y procedimientos (Steel, R.G.D., & Torrie, J.H.). 2 ed. Mac Graw-Hill.
Bravo Portocarrero, R., Uscamayta, K.Z., & Lima Medina, I. (2020) Eficiencia de trampas pegantes de colores en la captura de insectos de hortalizas de hoja. Scientia Agropecuaria, 11, 61-66.
Brawn Wilke, R., Santos, E.E., Picchetti, L.P., Larran, M.T., Guzmán, G.F., Colarich, C.R., & Casoli, C.A. (2001) Carta de Aptitud Ambiental de la Provincia de Jujuy. Arte-Ciencia. Jujuy en el Presente. REUN. UNJu.
Cabrera, A.L. (1976) Regiones Fitogeográficas Argentinas. Enciclopedia Argentina de Agricultura y Jardinería (ed. Kugler, W.F.), pp. 1-85. ACME, Buenos Aires.
Carew, J.G., Morreniti, M., & Battey, N.H. (2003) Misshapen Fruits in Strawberry. Small Fruits Review, 2(2), 37-50.
Chagnon, M., Gingras, J., & de Oliveira, D. (1993) Complementary aspects of strawberry pollination by honeyand indigenous bees (Hymenoptera). Journal of Economic Entomology, 86(2), 416-420.
Chacoff, N., & Aizen, M.A. (2006) Edge effects on flower-visiting insects in grapefruit plantations premontane subtropical forest. Journal of Applied Ecology, 43, 18-27.
Dalmazzo, M.M. (2012) Biología de abejas silvestres potencialmente utilizables como polinizadores de cultivos. Tesis para la obtención del Grado Académico de Doctor en Ciencias Biológicas. Facultad de Bioquímica y Ciencias Biológicas. Universidad Nacional del Litoral. Argentina.
De Klerk, P., & Joosten, H. (2007) The difference between pollen types and plant taxa: a plea for clarity and scientific freedom. Eiszeitalter and Gegenwart Quarternary Science Journal, 56, 162-171.
Díaz, S.A., Roger, S.L., Yacumo, D.M., Kirschbaum, D.S., & Gennari, G. (2013) Efecto polinizador de Bombus atratus sobre frutilla (Fragaria x ananassa Duch.) en la provincia de Tucumán. En: Resúmenes de trabajos del XXXVI Congreso Argentino de Horticultura, 2013, Tucumán. Argentina, p. 44.
Díaz, B.M., Maza, N., Castresana, J.E., & Martínez, M.A. (2020) Los sírfidos como agentes de control biológico y polinización en horticultura. Ediciones INTA, Estación Experimental Agropecuaria Concordia, Argentina. Disponible en: https://inta.gob.ar/sites/default/files/inta_concordia_sirfidos_como_agentes_de_control biologico_y_polinizacion_en_horticultura.pdf
Di Rienzo, J.A., Casanoves, F., Balzarini, M.G., González, L., Tablada, M., & Robledo, C.W. (2008) InfoStat, versión 2008, Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina.
Erdtman, G. (1960) The Acetolysis Method, a revised description. Svensk Botanisk Tidskrift,54, 561-564.
Fernández, M.T., Villegas, D.R., Alvarado, P., & Kirschbaum, D.S. (2011) Mejoramiento de las condiciones de trabajo y de la rentabilidad de agricultores familiares. Conferencia dictada en las VII Jornadas Interdisciplinarias de Estudios Agrarios y Agroindustriales (FCE-UBA). Buenos Aires, Argentina.
Free, J.B. (1993) Insect pollination of crops. 2nd ed. Academic Press, London, UK.
Freitas, B. (1998) Avaliação da eficiencia de polinizadores potenciais. En: Anais Congresso Brasileiro de Apicultura. pp. 105-107.
Gill, K.A., & O'Neal, M.E. (2015) Survey of Soybean Insect Pollinators: Community Identification and Sampling Method Analysis. Environmental Entomology,44(3), 488-498.
Gómez Martínez, J.A. (2006) Descripción del comportamiento de insectos y enfermedades asociadas al cultivo de fresa (Fragaria spp. L.) en el municipio de La Sabana, Departamento de Madriz. Tesis. Facultad de Agronomía. Universidad Nacional Agraria. Nicaragua. (disponible en: http://repositorio.una.edu.ni/id/eprint/1978).
Hammer, Ø., Harper, D.A.T., & Ryan, P.D. (2001) PAST: Paleontological Statistics Software Package for Education and Data Analysis. Palaeontologia Electronica4(1), 4.
Hodgkiss, D., Brown, M.J.F., & Fountain, M.T. (2018) Syrphine hoverflies are effective pollinators of comercial strawberry. Journal of Pollination Ecology, 22(6), 55-66.
Jaycox, E.R. (1970) Pollination of strawberries. American Bee Journal, 110, 176-177.
Joosten, H., & De Klerk, P. (2002) What's in a name? Some thoughts on pollen classification, identification, and nomenclature in Quaternary palynology. Review of Palaeobotany and Palynology, 122, 29-45.
Kearns, C.A., & Inouye, D.W. (1993) Techniques for Pollination Biologists. University Press of Colorado, USA.
Kirschbaum, D.S., Alderete, G.L., Rivadeneira, M., Borquez, A.M., Mollinedo, V.A., Funes, C.F., Baino, O.M., Reguilón, C., Conci, V.C., et al. (2015) Guía práctica de campo para el reconocimiento de plagas frecuentes, organismos benéficos y enfermedades habituales del cultivo de frutilla en el Noroeste Argentino. INTA PRODERI. Disponible en: https://inta.gob.ar/sites/default/files/intafrutilla.pdf
Kirschbaum, D., Sordo, M.H., Adlercreutz, E.G., Delmazzo, P.R., Cuellas, M.V., Lochbaum, T., Caminiti, A., Miserendino, E.E., Escalier, C., & Choque, L. (2019) Panorama del cultivo de frutilla en Argentina. Boletín de Frutas y Hortalizas, 99, 2-8. Disponible en: http://www.mercadocentral.gob.ar/sites/default/files/docs/boletin-INTA-CMCBA-99-frutilla.pdf
Klatt, B.K., Holzschuh, A., Westphal, C., Clough, Y., Smit, I., Pawelzik, E., & Tscharntke, T. (2014) Bee pollination improves crop quality, shelf life and commercial value. Proceedings of the Royal Society B, 281, 2013-2440.
Klein, A.M, Vaissiere, B.E., Cane, J.H., Steffan Dewenter, I., Cunningham, S.A., Kremen, C., & Tscharntke, T. (2007) Importance of pollinators in changing landscapes for world crops. Proceedings of the Royal Society B, 274, 303-313.
Lemme, M.C., Jaime de Herrero, A.P., Kirschbaum, D.S., & Nasca, A.J. (1996) Artrópodos asociados al cultivo de la frutilla, Fragaria x ananassa, en Tucumán, Argentina. Vedalia, 3, 51-52.
Lemme, M.C., Jaime De Herrero, A.P., Nasca, A.J., Ajmat, M.V., & Kirschbaum, D.S. (2000) Hemípteros asociados al cultivo de frutilla (Fragaria x ananassa Duch.) en Tucumán, Argentina. Revista Industrial y Agrícola de Tucumán, 77(1-2), 13-21.
Malagodi Braga, K.S. (2002) Estudo de agentes polinizadores em cultura de morango (Fragaria x ananassa Duchesne-Rosaceae). Tese (Doutorado). Instituto de Biociências da Universidade de São Paulo, Departamento de Ecología, São Paulo.
Markgraf, V., & D'Antoni, H. (1978) Pollen Flora of Argentina. Modern Spore and Pollen Types of Pteridophyta, Gymnospermae and Angiospermae. The University of Arizona Press, Tucson.
Maza, N., Sopena, Y.N., Assaf, M.J.T., Paz, M.R., & Jaime, A.P. (2014) Las “moscas de las flores” (Diptera: Syrphidae) en Lules, Tucumán. Revista Agronómica del Noroeste Argentino, 34(2), 234-235.
Maza, N. (2018) Potencialidad de sírfidos (Diptera: Syrphidae) como agentes de control biológico de plagas en cultivos de pimiento en invernadero. Tesis doctoral. Facultad de Agronomía y Zootecnia. Universidad Nacional de Tucumán.
Miserendino, E.E. (2010) Posibilidades de producción de frutillas en Bariloche. Presencia, 55, 16-20.
Moreno, C.E. (2001) Métodos para medir la biodiversidad. M&T-Manuales y Tesis SEA, Zaragoza.
Nates Parra, G. (2005) Abejas silvestres y polinización. Manejo Integrado de Plagas y Agroecología, 75, 7-20.
Ne'eman, G., Dafni, A., & Potts, S.G. (1999) A new pollination probability index (PPI) for pollen load analysis as a measure for pollination effectiveness of bees. Journal Apicultural Research, 38 (1-2), 19-23.
Nicolson, S.W., Nepi, M., & Pacini, E. (2007) Nectaries and Nectar. Springer Verlag, Dordrecht.
Nye, W.P., & Anderson, J.L. (1974) Insect pollinators frequenting strawberry blossoms and effect of honey bees on yield and fruit quality. Journal American Society Horticultural Science, 99, 40-44.
Olivo, V.I., Corronca, J.A., & González Reyes, A.X. (2015) Dinámica de la comunidad de artrópodos asociada a cultivos de frutilla con plantas de diferentes edades en el noroeste de la Argentina. Agriscientia,32, 29-39.
Potts, S.G., Biesmeijer, J.C., Kremen, C., Neumann, P., Schweiger, O., & Kunin, W.E. (2010) Globall pollinator declines: trends, impacts and drivers. Trends in Ecology & Evolution, 25(6), 345-353.
Retana Zalazar, A.P., & Rodríguez Arrieta, J.A. (2015) Especies potenciales de thrips (Insecta: Thysanoptera: Thripidae) en la polinización del mango (Mangifera indica L.) en Costa Rica. Revista Gaditana de Entomología, 6, 103-112.
Reyes Tirado, G.S., & Johnston, P. (2013) El declive de las abejas. Peligros para los polinizadores y la agricultura de Europa. Unidad Científica de Greenpeace, Rev. 1. Greenpeace International.
Ricou, C., Schneller, C., Amiaud, B., Plantureux, S., & Bockstaller C. (2014) A vegetation-based indicator to assess the pollination value of field margin flora. Ecological Indicators,45, 320-331.
Roig Juñent, S., Claps, L.E., & Morrone, J.J. (Directores). (2014) Biodiversidad de artrópodos argentinos. Volumen 3. Editorial Sociedad Entomológica Argentina.
Sáez, A., Sabatino, M., & Aizen, M. (2014) La diversidad floral de borde afecta la riqueza y abundancia de visitantes florales nativos en cultivos de girasol. Ecología Austral, 24, 94-102.
Salas Araiza, M.D., Salazar Solís, E., Martínez Jaime, O.A., & Guzmán Mendoza, R. (2014) Insectos benéficos en el cultivo de fresa en Irapuato, Guanajuato, México. Entomología Mexicana, 1, 289-294.
Svensson, B. (1991) The importance of honeybee-pollination for the quality and quantity of strawberries (Fragaria x ananassa) in Central Schweden. Acta Horticulturae, 288, 260-264.
Torretta, J.P., López, M.C., & Marrero, H.J. (2021) Las moscas de las flores (Diptera: Syrphidae) en agroecosistemas pampeanos: un caso de estudio. Revista de la Sociedad Entomológica Argentina, 80(2), 23-34.
Urretabizkaya, N., Vasicek, A., & Saini, E. (2010) Insectos perjudiciales de importancia agropecuaria: 1. Lepidópteros. Ediciones INTA. Buenos Aires. (disponible en: https://inta.gob.ar/sites/default/files/script-tmp-inta_lepidopteros.pdf).
Vossler, F.G, Blettler, D.C., Fagúndez, G.A., & Dalmazzo, M. (2018) Stingless Bees as Potential Pollinators in Agroecosystems in Argentina: Inferences from Pot Pollen Studies in Natural Environments. Pot Pollen in Stingless Bee Melittology (ed. Vit, P., Pedro, S., & Roubik, D.), pp. 155-175. Springer, Cham.
Weyland, F., & Zaccagnini, M.E. (2008) Efecto de las terrazas sobre la diversidad de artrópodos caminadores en cultivos de soja. Ecología Austral, 18(3), 357-370.
Williams, G., Adams, P., & Mound, L.A. (2001) Thrips (Thysanoptera) pollination in Australian subtropical rainforests, with particular reference to pollination of Wilkiea huegeliana (Monimiaceae). Journal of Natural History, 35, 1-21.
Zamar, M.I., Funes, C., Kirschbaum, D., Tapia, S., & Alejo, G. (2018) Nuevos registros de Thripidae (Thysanoptera: Terebrantia) del noroeste de Argentina. Acta Zoológica Lilloana, 52(2), 1-11.
Zamora Carrillo M., Amat García, G.D., & Fernández Alonso, J.L. (2011) Estudio de las visitas florales de las moscas de las flores (Diptera: Syrphidae) en Salvia bogotensis (Lamiaceae) en el Jardín Botánico José Celestino Mutis (Bogotá, D.C.-Colombia). Caldasia, 33(2), 433-450.
Zebrowska, J. (1998) Influence of pollination modes on yield components in strawberry (Fragaria x ananassa Duch.). Plant Breeding, 117(3), 255-260.
Notas de autor
lalei344@gmail.com
