Artículos
Actividad forrajera y de mantenimiento de nido de la hormiga cortadora de hojas Acromyrmex lobicornis (Hymenoptera: Formicidae) en un viñedo orgánico inserto en el desierto de Monte en Mendoza, Argentina
Foraging and nest maintenance activity of the leafcutter ant Acromyrmex lobicornis (Hymenoptera: Formicidae) in an organic vineyard in the Monte desert of Mendoza, Argentina
Actividad forrajera y de mantenimiento de nido de la hormiga cortadora de hojas Acromyrmex lobicornis (Hymenoptera: Formicidae) en un viñedo orgánico inserto en el desierto de Monte en Mendoza, Argentina
Revista de la Sociedad Entomológica Argentina, vol. 80, núm. 4, 2021
Sociedad Entomológica Argentina
Recepción: 27 Mayo 2021
Aprobación: 11 Noviembre 2021
Publicación: 30 Diciembre 2021
Resumen: Exclusivas del Neotrópico, las hormigas cortadoras de hojas son consideradas plagas agrícolas, aunque pueden tener también un efecto positivo sobre las plantas. En los viñedos mendocinos la biodiversidad vegetal es mínima, por lo cual cortan el recurso vegetal más disponible. Acromyrmex lobicornis Emery es mayoritariamente nocturna y forrajea en función de la temperatura. Se midió la actividad de forrajeo y de mantenimiento en 14 colonias durante todo un día por mes desde octubre de 2019 a marzo de 2020 a intervalos de cuatro horas. Acromyrmex lobicornis mostró patrones estacionales de actividad de forrajeo diferentes entre sí entre horarios de muestreo. La intensidad de forrajeo fue máxima durante enero y febrero, menor durante diciembre y baja durante octubre y noviembre. Se observó un patrón bimodal, forrajeando tanto de día como de noche evitando las horas de más calor. Recolectó mayor cantidad de fragmentos en el intervalo de 10 y 19 °C, menor entre 20 – 39 °C, mínimo entre 40 y 49 °C y nulo entre 0 – 9 °C. La actividad de mantenimiento fue máxima entre 20 y 29 °C, menor entre 30 – 39 °C, mínimo entre 40 - 49 °C y nulo entre 0 – 20 °C.
Palabras clave: Actividad de forrajeo, Actividad de mantenimiento de nido, Attini.
Abstract: Exclusive to the Neotropical region, leaf cutter ants are considered agricultural pests, although they can also have a positive effect on plants. In Mendoza vineyards, vegetal biodiversity is minimal, therefore they cut off this plant as a feeding resource. Acromyrmex lobicornis Emery it is mostly nocturnal and forages according to temperature. Foraging and maintenance activity was measured monthly in 14 colonies, throughout a full day at four-hour intervals, from October 2019 to March 2020. Acromyrmex lobicornis showed different seasonal patterns of foraging activity. Foraging intensity was highest throughout January and February, intermediate during December, and lowest in October and November. A bimodal feeding pattern was observed, foraging both day and night avoiding the hottest hours. The maximum collection of fragments was observed in the range of 10 and 19 °C, less between 20 - 39 °C, minimum between 40 - 49 °C and null between 0 - 9 °C. The nest - maintenance activity was maximum between 20 - 29 °C, less between 30 - 39 ° C, minimum between 40 - 49 °C and null between 0 - 20 °C.
Keywords: Attini, Foraging activity, Nest maintenance activity.
INTRODUCCIÓN
Las hormigas cortadoras de hojas son exclusivas del Neotrópico y son consideradas uno de los herbívoros más importantes en esta región (Fowler et al., 1986; Hölldobler & Wilson, 1990; Fowler et al., 1991; Armani & Quirán, 2007). Al utilizar vegetales frescos que cortan de la vegetación circundante, son capaces de aprovechar la mayoría de las especies cultivadas, por lo que generalmente son consideradas plagas agrícolas y forestales (Della Lucía, 2003; Moreno Kiernan et al., 2019). Sin embargo, la actividad forrajera de estas hormigas puede tener un efecto positivo sobre las plantas ya que también remueven semillas y frutos, facilitando su dispersión (Farji-Brener & Silva, 1996; Pizo & Oliveira, 2001; Wirth et al., 2003; Rico-Gray & Oliveira, 2007; Nobua-Behrmann, 2014).
Las mismas pertenecen a la tribu Attini y comprenden tres géneros Atta Fabricius, Acromyrmex Emery y Amoimyrmex Cristiano, Cardoso & Sandoval, que se caracterizan por su amplia distribución y elevada densidad (Diehl-Fleig, 1995).
Las Attini cultivadoras de hongos cortan fragmentos de hojas, flores y frutos (Beattie & Hughes, 2002) así como también tallos y pequeños trozos de ramas (Gamboa, 1975). Pueden afectar a las comunidades de plantas mediante la herbivoría y a través del movimiento de grandes cantidades de suelo para construir sus nidos (Wirth et al., 2003; Rico-Gray & Oliveira, 2007; Nobua-Behrmann, 2014). Éstos llegan a ser de hasta 5 m de diámetro y 2 m de profundidad (Della Lucía, 1993). Están casi siempre construidos superficialmente (Della Lucía, 2003; Bollazzi et al., 2010), con poca tierra suelta, aunque varias especies depositan sobre ellos vegetales secos, o los construyen en espacios entre piedras, troncos de árboles, en cimientos de construcciones, etc. (Della Lucía, 1993).
Acromyrmex lobicornis Emery y Amoimyrmex striatus Cristiano, Cardozo & Sandoval, son especies simpátricas que conviven en el desierto de Monte (Nobua-Behrmann, 2014). Son generalistas ya que consumen tanto monocotiledóneas como dicotiledóneas (Bucher & Montenegro, 1974; Pilati et al., 1997; Claver, 2000; Armani & Quirán, 2007; Nobua-Behrmann, 2014).
Acromyrmex lobicornis se distribuye en todo el territorio argentino hasta Santa Cruz (Cuezzo & Larrea, 2021) marcando los límites de distribución latitudinal y altitudinal de las hormigas cortadoras pertenecientes a la tribu Attini en la Argentina. Habita en ambientes con grandes variaciones térmicas como montes, desiertos y estepas (Farji-Brener & Ruggiero, 1994; Navas Romero et al., 2018). Esta especie prefiere temperaturas moderadas y sus nidos frecuentemente presentan basureros externos grandes y conspicuos (Farji-Brener, 2000) y generalmente con un domo que minimiza la variabilidad climática ambiental (Farji-Brener & Sasal, 2003; Navas Romero et al., 2018). Suelen encontrarse debajo de algún árbol o arbusto, con sus caminos de forrajeo mayormente a la sombra (Farji-Brener, 2000; Nobua-Behrmann, 2014).
La actividad de selección, corte y transporte hacia el nido se denomina forrajeo (Weber, 1972; Fowler & Stiles, 1980; Alma, 2017; Moreno Kiernan et al., 2019). La cantidad de material vegetal que una colonia puede acumular por día depende del número de obreras que se encuentran forrajeando en cada momento del día, así como del número de horas diarias que una colonia forrajea activamente (Wirth et al., 2003). La temperatura toma particular relevancia para los organismos que habitan los desiertos, ya que en estos sistemas existen amplias variaciones térmicas diarias y estacionales. Las hormigas que habitan en desiertos suelen tener preferencias para forrajear en función de la temperatura del suelo (Pol & López de Casenave, 2004; Azcárate et al., 2007; Nobua-Behrmann, 2014). Los patrones de forrajeo y mantenimiento de nido de las hormigas cortadoras de hojas son muy variados. Algunas forrajean exclusivamente durante el día en los meses de invierno y en la noche durante el verano como por ejemplo Acromyrmex versicolor Pergande (Gamboa, 1975). Otras como Atta cephalotes L. y Atta colombica Guérin-Méneville, poseen forrajeo nocturno en la época seca (para evitar las altas temperaturas diurnas) y diurno en la época húmeda (Rockwood, 1975; Farji-Brener, 1993). Por otra parte, estos patrones pueden variar a lo largo del año en respuesta al tamaño de la colonia (Hölldobler & Wilson, 1990; Jofré & Medina, 2012), cambios en la temperatura (Gamboa, 1975; Pilati et al., 1997; Claver, 2000; Jofré & Medina, 2012; Nobua-Behrmann, 2014), las precipitaciones (Rockwood, 1975), la humedad relativa del ambiente, la intensidad de la luz y la presión atmosférica (Lewis et al., 1974b), el estado reproductivo, los requerimientos nutricionales (Lewis et al., 1974a; Jofré & Medina, 2012), la presencia de insectos parasitoides (Wetterer, 1995), la cantidad de senderos (Elizalde & Farji-Brener, 2012) y la disponibilidad de recursos (De Vasconcelos, 1990). Nobua-Behrmann et al. (2017) encontraron que A. lobicornis en el desierto de Monte forrajea por las noches en primavera y verano, cuando las temperaturas son muy elevadas, mientras que en otoño e invierno tiene una actividad diurna. Así mismo, existen factores bióticos que pueden regular la actividad de forrajeo como las interacciones con especies competidoras (Sanders & Gordon, 2000; Nobua-Behrmann, 2014), la disponibilidad de alimento (Steinberger et al., 1992; Sanders & Gordon, 2000; Nobua-Behrmann, 2014) y la presencia de depredadores (Mehlhop & Scott, 1983; Nobua-Behrmann, 2014) y parasitoides (Orr, 1992; Nobua-Behrmann, 2014).
La actividad de mantenimiento de nido consiste en extraer de las cámaras internas todo el material residual (material vegetal, hongo agotado y cadáveres de hormigas). Este trabajo es realizado por las obreras más viejas, las cuales entran en contacto con la basura sin tener acceso al jardín de hongo evitando así la contaminación del mismo (Marinho et al., 2006).
Existen muchos trabajos que estudian los patrones de forrajeo y cosecha de hormigas cortadoras en ambientes naturales (Farji-Brener, 1993; Pilati et al., 1997; Bollazzi & Roces, 2002; Nobua-Behrmann et al., 2017) y urbanos (Jofré & Medina, 2012). Sin embargo, son pocos los que analizan la actividad de forrajeo de las hormigas cortadoras en agroecosistemas (Nickele et al., 2016; Jiménez, 2019; Dagatti et al., 2019) como los viñedos. Así mismo, no hay trabajos donde se estudie la actividad de mantenimiento del nido en función de la temperatura.
En la región Neotropical, las hormigas cortadoras de hojas atacan cultivos de café (Coffea arabica L.), cacao (Theobroma cacao L.), citrus (Citrus spp.), maíz (Zea mays L.) y algodón (Gossypium hirsutum L.) y provocan intensos daños a los cultivos estimándose una importante pérdida de la producción (Montoya-Lerna, 2012). En los sistemas productivos de la provincia de Entre Ríos, Argentina, los daños por hormigas cortadoras consisten en pérdidas de plantas, que afectan principalmente la etapa inicial de los cultivos (girasol, maíz, lino, sorgo), las praderas y los pastizales naturales (Dans, et al. 2009). Así mismo, en Pinus spp. y Eucalyptus spp., ocasionan pérdidas económicas de gran magnitud (Sabattini, 2017). Acromyrmex lobicornis es considerada una de las principales plagas en la agricultura y silvicultura argentina (Pilati et al., 1997; de Coll, 2003; Montoya-Lerna, 2012). Las tasas de defoliación están en el rango de 2,5 a 8,5 Kg/colonia/año, más altas que cualquier otra especie de Acromyrmex (Pilati et al., 1997). En Argentina, esta especie ha sido reportada causando graves daños económicos en forestales de Corrientes y Misiones (de Coll, 2003), en viñedos de San Juan (Amatta et al., 2015) y Mendoza (Dagatti, 2016) y es una plaga potencial en forestales de la Patagonia (Pérez, 2009; Sánchez-Restrepo et al., 2018).
El control de hormigas cortadoras en viñedos se hace mayormente por remoción manual y extracción mecánica de sus nidos y/o la aplicación de productos fitosanitarios de síntesis química o biológica (Amatta et al., 2015). En un agroecosistema vitícola, la biodiversidad vegetal en los interfilares del cultivo es mínima, debido a las labores culturales que realizan los viticultores para evitar las heladas. Por lo tanto, las hormigas cortadoras adquieren un status de plaga al cortar el recurso vegetal más disponible, la vid, convirtiéndose en un problema recurrente para los productores vitícolas. No obstante, no existen trabajos publicados en la actualidad que cuantifiquen el daño que estas hormigas ocasionan en el viñedo.
La importancia de conocer las fluctuaciones diarias y estacionales en las cuales A. lobicornis se encuentra más activa removiendo mayor cantidad de material vegetal es fundamental para plantear estrategias de manejo y control en el viñedo, sobre todo en el sistema de producción orgánico. Es por ello que nos planteamos como objetivos (1) conocer las variaciones de la actividad forrajera y de mantenimiento diaria de A. lobicornis en los meses donde se encuentra más activa, y (2) determinar si la temperatura del suelo es un factor determinante de sus patrones de actividad.
MATERIAL Y MÉTODOS
Área de estudio
Mendoza está situada al pie de la Cordillera de los Andes y se extiende en el Centro-Oeste argentino, entre los 32° y 37°35´de latitud Sur y los 66°30´y 70°35´de longitud Oeste. Esta provincia argentina se encuentra en la Ecorregión de Monte (Cabrera, 1976; Pol et al., 2005) con clima cálido, árido y seco, con gran variación térmica diaria y estacional (Norte, 2000; Pol et al., 2005). El agua es un factor limitante en este ecosistema donde las precipitaciones suelen ser escasas y poco predecibles (Nobua-Behrmann, 2014). El trabajo se realizó en la temporada 2019-2020 en una parcela de vid orgánica de 3 has. cv. Malbec de La Consulta, San Carlos, Mendoza, Argentina. La parcela presentaba riego por goteo, sistema de conducción por espaldero y cobertura vegetal interfilar. Como contexto ecológico, la parcela en estudio estaba rodeada por vegetación natural (Monte).
Metodología
El diseño de muestreo original consistía en visitar 14 colonias, elegidas al azar, en cada día de muestreo, de manera de poder seguir sus tendencias individuales. Del total de nidos, nueve estaban inmersos dentro del cultivo y cinco en el campo natural aledaño. Sin embargo, algunas de las colonias cesaron su actividad o mudaron su nido entre visitas, por lo cual en esos casos se incluyeron nuevas colonias. Las colonias estaban situadas con una distancia de al menos 50 metros entre sí dentro del viñedo y de 100 metros afuera del mismo, en el monte natural. Cada nido fue identificado con una estaca de madera con el número de hormiguero y marcado con cinta de color para no ser removido ni pisado. Se midió la actividad de forrajeo y de mantenimiento de las colonias a intervalos de cuatro horas durante todo un día por mes desde octubre de 2019 a marzo de 2020. Para ello, se realizó un círculo imaginario de aproximadamente 30 cm de diámetro alrededor del nido, con centro en la boca principal del mismo, para delimitar la zona de recuento de hormigas que ingresaban y egresaban de la colonia durante cinco minutos. Estos registros se tomaron en cada día de muestreo en seis horarios diarios (0, 4, 8, 12, 16 y 20 horas). Se registró la temperatura superficial adyacente a la entrada de cada nido con un termómetro digital soterrado unos pocos milímetros debajo de la superficie del suelo. Para estudiar la relación entre la actividad de forrajeo y la temperatura del suelo se usaron dos aproximaciones complementarias: primero se estudió la influencia de la temperatura sobre el estado de la colonia (con o sin actividad) y luego su influencia sobre los niveles de actividad en las colonias activas (el número de obreras que se encuentran forrajeando y realizando tareas de mantenimiento de nido). Para estudiar la relación entre los niveles de actividad y la temperatura del suelo se tuvo en cuenta el número de obreras que regresaban al nido con carga cuando las colonias estaban activas, así como también la cantidad de hormigas que egresaban del nido realizando tareas de mantenimiento.
La matriz de los datos de la actividad forrajera y de mantenimiento se construyó con las medias del número de hormigas que ingresaban con material vegetal (actividad de forrajeo) y egresaban con sedimentos (actividad de mantenimiento) y las medias de las temperaturas del suelo para cada horario de muestreo y por cada mes. Posteriormente se realizó el test no paramétrico Kruskal-Wallis, con el Software InfoStat 2016 (Di Rienzo et al., 2016) para examinar si existían diferencias entre horarios de muestreo, entre sitios (viñedo y monte natural) y entre meses de colecta de acuerdo a la temperatura del suelo.
RESULTADOS
Actividad de forrajeo
En general, en ambos sitios de muestreo, A. lobicornis mostró patrones estacionales de actividad de forrajeo marcadamente diferentes entre sí entre horarios de muestreo durante la temporada en estudio. Las obreras forrajearon activamente durante casi todo el día en octubre de 2019. En todos los meses, excepto en noviembre 2019, A. lobicornis forrajeó mayormente en el horario de las 8 de la mañana (Fig. 1). Durante el mes de octubre la actividad de forrajeo registrada fue de 16 horas, en noviembre de 8 horas y desde diciembre a febrero la actividad de forrajeo se limitó a tres horarios: a las 0, 8 y 20 horas. La intensidad de forrajeo fue máxima durante febrero (promedio de 213,83 obreras con carga en un lapso de 5 minutos) y enero (promedio de 191,58 obreras/5 min), menor durante diciembre (promedio de 103,76 obreras/5 min.) y baja durante octubre y noviembre (menos de 40 obreras/5 min). La actividad forrajera presentó un patrón bimodal, forrajeando tanto de día como de noche evitando las horas de más calor del mediodía y las primeras horas de la tarde hasta las 20 horas donde la actividad forrajera comenzó nuevamente, excepto en noviembre (Fig. 1).
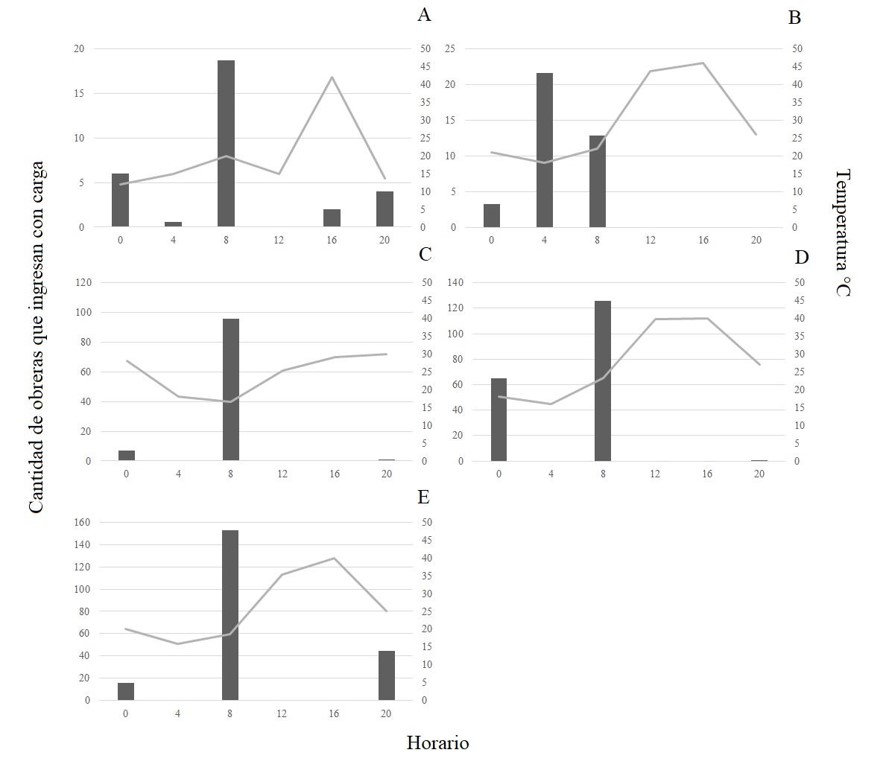
Fig. 1. Cantidad total de obreras que ingresan al nido con carga (actividad de forrajeo) durante cinco minutos a lo largo del día en los 14 hormigueros estudiados en: A) octubre 2019, B) noviembre 2019, C) diciembre 2019, D) enero 2020 y E) febrero 2020 en las colonias de Acromyrmex lobicornis. Se muestra la temperatura promedio del suelo (línea gris).
Nótese que los valores de la escala del eje y cambian entre los meses de estudio.
Al comparar ambos sitios de muestreo (viñedo y monte natural) se puede observar que las colonias de A. lobicornis que se encontraban fuera del cultivo, acarrearon mayor cantidad de fragmentos vegetales hacia los nidos en todos los meses, excepto en febrero donde la actividad forrajera fue mayor dentro del viñedo (Fig. 2). Sin embargo, esta diferencia no fue significativa (H=0,05; p=0,76) pero sí lo fue en relación a los horarios de muestreo (H=124,6; p<0,0001) (Fig. 3) y a los meses de colecta (H= 8,02; p=0,0085) (Fig. 4) con un α=0,05.
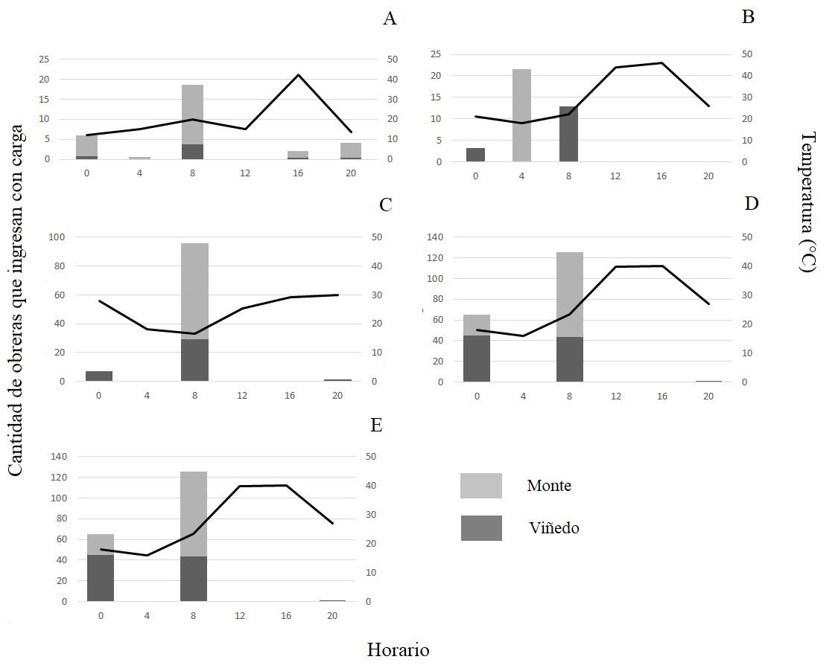
Fig. 2. Cantidad total de obreras que ingresan al nido con carga (actividad de forrajeo) durante cinco minutos en los nueve hormigueros del viñedo y en los 5 del monte natural aledaño a lo largo del día en: A) octubre 2019, B) noviembre 2019, C) diciembre 2019, D) enero 2020 y E) febrero 2020 en las colonias de Acromyrmex lobicornis insertas en el viñedo y fuera de él, en el monte natural.
Se muestra la temperatura promedio del suelo (línea negra). Nótese que los valores de la escala del eje y cambian entre los meses de estudio.
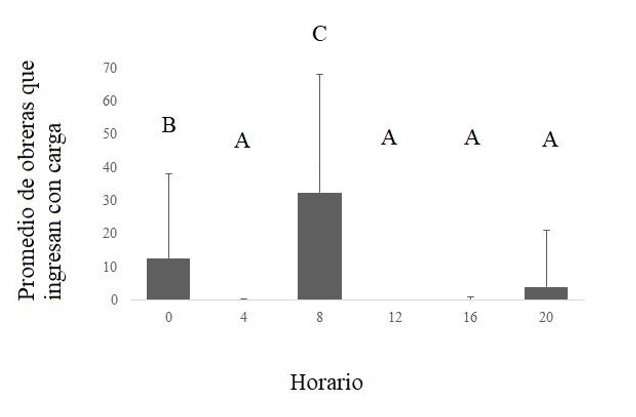
Fig. 3. Cantidad promedio de obreras que ingresan al nido con carga (actividad de forrajeo) durante cinco minutos a lo largo del día en las 14 colonias de Acromyrmex lobicornis insertas dentro del viñedo y fuera de él, en el monte natural.
Las barras indican el error estándar. Diferentes letras indican diferencias significativas (p<0,05).
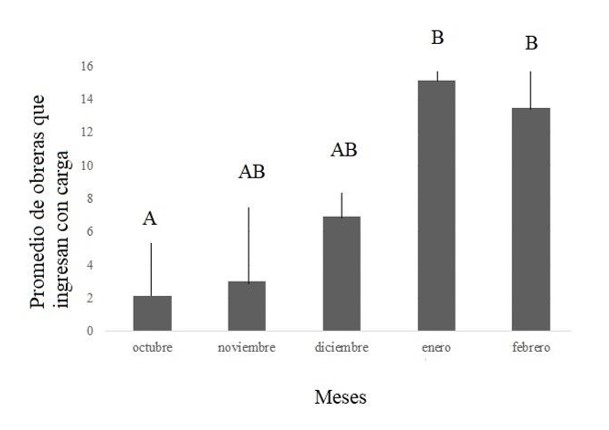
Fig. 4. Cantidad promedio de obreras que ingresan al nido con carga (actividad forrajera) durante cinco minutos a lo largo de la temporada en estudio en las 14 colonias de Acromyrmex lobicornis insertas dentro del viñedo y fuera de él, en el monte natural.
Las barras indican el error estándar. Diferentes letras indican diferencias significativas (p<0,05).
Respecto a las temperaturas óptimas de forrajeo, se observó que tanto en las colonias insertas dentro del viñedo, así como en aquellas que se encontraban en el monte natural, las obreras de A. lobicornis recolectaron mayor cantidad promedio de fragmentos cuando la temperatura media del suelo fue de entre 10 y 19 °C, menor en el intervalo de temperatura de 20 – 39 °C, mínimo entre 40 y 49 °C y nulo entre 0 – 9 °C (Tabla I).
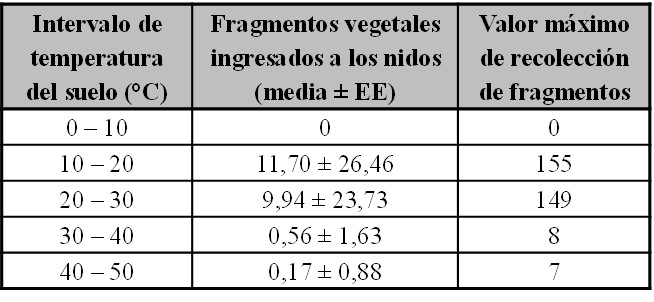
Tabla I. Cantidad promedio y error estándar (EE) de fragmentos vegetales acarreados por las obreras de Acromyrmex lobicornis hacia los nidos en diferentes intervalos de temperatura del suelo.
Actividad de mantenimiento.
En relación a la actividad de mantenimiento de la colonia, ésta fue cambiando a lo largo de la temporada en estudio. En febrero a las 8 a.m., se registró la mayor cantidad de obreras saliendo del nido con tareas de limpieza.
Los patrones mensuales de actividad de mantenimiento del nido fueron, en términos generales, similares a los de la actividad de forrajeo. En las colonias de A. lobicornis el patrón de actividad de mantenimiento fue máximo en el horario de las 8 y durante 20 horas en el mes de octubre, 8 a.m. en noviembre y de 12 horas durante diciembre, enero y febrero (Fig. 5).
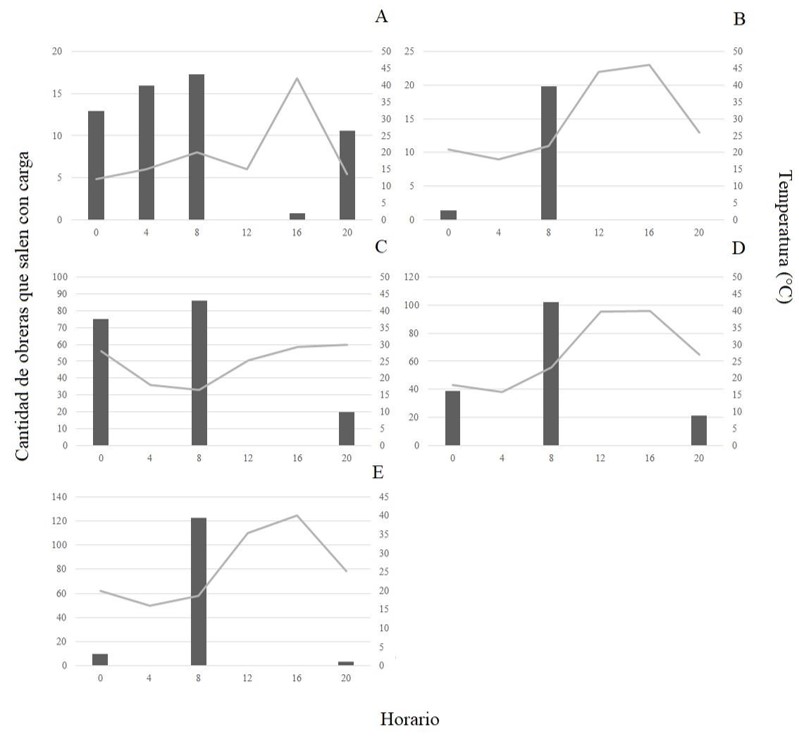
Fig. 5. Cantidad total de obreras que salen del nido (actividad de mantenimiento) con carga durante cinco minutos a lo largo del día en los 14 hormigueros estudiados en: A) octubre 2019, B) noviembre 2019, C) diciembre 2019, D) enero 2020 y E) febrero 2020 en las colonias de Acromyrmex lobicornis. Se muestra la temperatura promedio del suelo (línea gris).
Nótese que los valores de la escala del eje y cambian entre los meses de estudio.
Al comparar ambos sitios de muestreo (viñedo y monte natural), no hubo diferencias entre sitios de estudio (H=0,27; p=0,499) en cuanto a la actividad de mantenimiento en las colonias de A. lobicornis (Fig. 6). Respecto a los horarios de muestreo entre los sitios de estudio, hubo diferencias significativas (H=117,22; p<0,0001) (Fig. 7), así como también en los meses de recolección (H=7,04; p=0,0193) (Fig. 8), con un α=0,05.
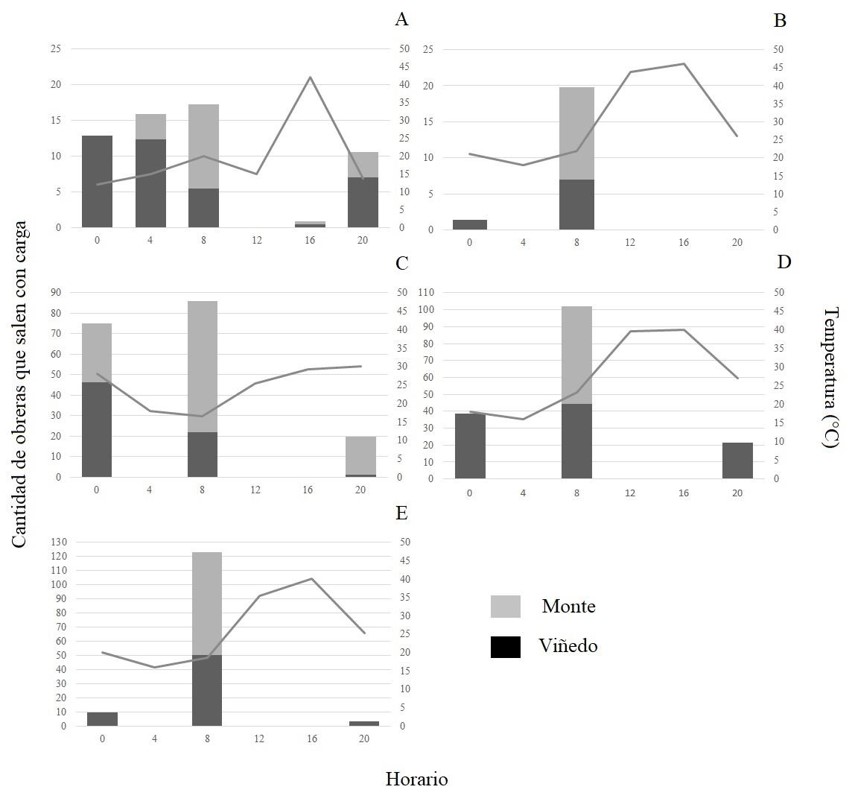
Fig. 6. Cantidad total de obreras que salen del nido (actividad de mantenimiento) con carga durante cinco minutos a lo largo del día en los 14 hormigueros estudiados en: A) octubre 2019, B) noviembre 2019, C) diciembre 2019, D) enero 2020 y E) febrero 2020 en las colonias de Acromyrmex lobicornis insertas en el viñedo y fuera de él, en el monte natural. Se muestra la temperatura promedio del suelo (línea gris).
Nótese que los valores de la escala del eje y cambian entre los meses de estudio.
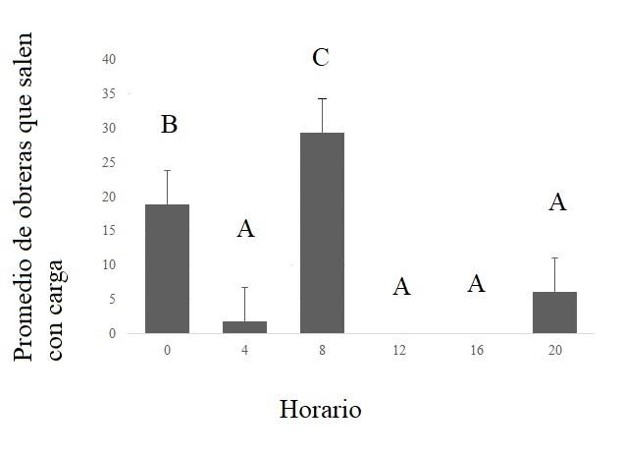
Fig. 7. Cantidad promedio de obreras que salen del nido con carga durante cinco minutos a lo largo del día en las 14 colonias de Acromyrmex lobicornis insertas dentro del viñedo y fuera de él, en el monte natural.
Las barras indican el error estándar. Diferentes letras indican diferencias significativas (p<0,05).
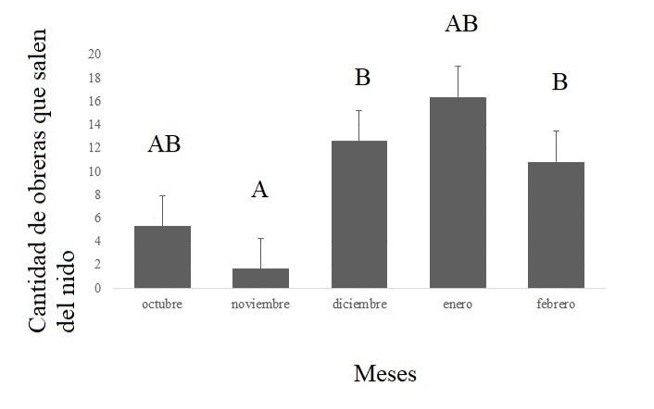
Fig. 8. Cantidad promedio de obreras que salen del nido con carga durante cinco minutos a lo largo de la temporada en estudio en las 14 colonias de A. lobicornis insertas dentro del viñedo y fuera de él, en el monte natural.
Las barras indican el error estándar. Diferentes letras indican diferencias significativas (p<0,05).
Respecto a las temperaturas óptimas de mantenimiento, se observó que tanto en las colonias insertas dentro del viñedo, así como en aquellas que se encontraban en el monte natural, las obreras de A. lobicornis sacaron mayor cantidad promedio de sedimentos cuando la temperatura media del suelo era de entre 20 y 29 °C, menor en el intervalo de temperatura de 30 – 39 °C, mínimo entre 40 y 49 °C y nulo entre 0 – 20 °C (Tabla II).
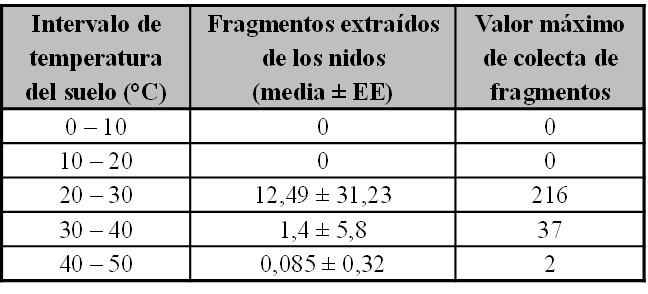
Tabla II. Cantidad promedio y error estándar (EE) de sedimentos acarreados por las obreras de A. lobicornis desde los nidos en diferentes intervalos de temperatura del suelo.
DISCUSIÓN
En el viñedo estudiado, así como en la vegetación de monte aledaña, A. lobicornis presentó un patrón de forrajeo bimodal, es decir que las colonias se mantuvieron activas durante el día y la noche, evitando las horas de más calor del mediodía y las primeras horas de la tarde, al igual que lo observado por Nobua-Behrmann y colaboradores (2017) para la misma especie en el desierto de Monte. Estos autores concluyeron que, en estas horas de calor intenso, las obreras de A. lobicornis se limitan a realizar tareas dentro del nido, dejando de buscar alimento.
Los patrones diarios de actividad forrajera y de mantenimiento están asociados, entre otros factores, a la variación de la temperatura del suelo, lo que no solo determina si las colonias están activas o no, sino también su nivel de actividad. Así mismo, los cambios en los patrones diarios de actividad son un tipo de respuesta comportamental que les permite a las hormigas explotar más eficientemente sus rangos de temperatura preferidos (Nobua-Behrmann, 2014). Coincidiendo con los resultados de Jofré & Medina (2012), así como los de Nobua-Behrmann (2014), la máxima intensidad de forrajeo observada ocurrió durante la noche en los horarios de 0 y 8 a.m., siendo nula a las 4 a.m., donde la temperatura baja considerablemente. Los meses más cálidos, enero y febrero, fueron los que presentaron mayor actividad de forrajeo tanto dentro del viñedo como en monte natural aledaño al mismo.
El rango de temperaturas óptimo de suelo para A. lobicornis en el desierto de Monte fue de 15 – 35 °C, de acuerdo a los resultados obtenidos por Nobua-Behrmann (2014). En el viñedo, así como en el monte aledaño al mismo, la máxima actividad de forrajeo ocurrió en el intervalo de 10 – 19 °C. Esto indica la gran plasticidad térmica de esta especie, así como también una mayor capacidad de adaptarse a los cambios del ambiente. De acuerdo con Farji-Brener & Silva (1996), ésta sería la causa por la cual A. lobicornis se ha expandido hacia el sur de Argentina en las últimas décadas.
Los patrones de actividad de mantenimiento del nido fueron principalmente nocturnos y hasta las 8 de la mañana donde fue máximo. En las horas de más calor, ya no había obreras realizando tareas de mantenimiento y esta tarea era realizada en la noche. Al ser animales ectotermos, su temperatura corporal cambia de acuerdo con las variaciones de temperatura. Por lo tanto, en las estaciones más frías las hormigas solo pueden realizar actividades de limpieza y mantenimiento de nido durante el mediodía, cuando las temperaturas son más elevadas. Así mismo, en las estaciones más cálidas, la actividad de forrajeo y mantenimiento es nula en el horario del mediodía y las primeras horas de la tarde. Estos resultados son coincidentes con los obtenidos por Nobua-Behrmann (2014) en el Monte central para la misma especie. En nuestro trabajo, el rango de temperatura óptimo fue de 20 – 29 °C.
AGRADECIMIENTOS
Al grupo de bodegas Vinodinámicos por el financiamiento otorgado para este estudio, especialmente a los Ings. Mauricio Castro y Facundo Bonamaizón quienes participaron activamente de este proyecto. A la Ing. Mag. María Eugenia Herrera por las lecturas y correcciones realizadas.
REFERENCIAS
Alma, M. A. (2017) Resolución de problemas en hormigas cortadoras de hojas: factores implicados en la resolución individual versus colectivo. Tesis doctoral. Universidad Nacional del Comahue, San Carlos de Bariloche, Argentina. 245 pp.
Amatta, E., Calcaterra, L., & Gianonni, S. (2015) Daño causado por las hormigas cortadoras de hojas en relación a la fenología de la vid, el sistema de cultivo y la densidad de hormigueros. En: Actas y Trabajos del X Congreso Argentino de Entomología, Mendoza. pp. 406.
Armani, A., & Quirán, E. (2007) Evaluación cualitativa y cuantitativa de la oferta y cosecha de biomasa herbácea por Acromyrmex striatus Roger (Hymenoptera: Formicidae) en la provincia de La Pampa, Argentina. Gayana, 71, 203-206.
Azcárate, F. M., Kovacs, E., & Peco, B. (2007) Microclimatic conditions regulate surface activity in harvester ants Messor barbarus. Journal of Insect Behavior, 20, 315-329.
Beattie, A. J., & Hughes, L. (2002) Ant-plant interactions. In: Plant-Animal Interactions – An Evolutionary Approach (ed. Herrera, C. M. & Pellmyr, O.), pp. 211-235, Blackwell Science, Oxford, USA.
Bollazzi, M., & Roces, F. (2002) Thermal preference for fungus culturing and brood location by workers of the thatching grass-cutting ant Acromyrmex heyeri. Insectes Sociaux, 49 (2), 153-157.
Bollazzi, M., & Roces, F. (2010) Leaf-cutting ant workers (Acromyrmex heyeri) trade off nest thermoregulation for humidity control. Journal of Ethology, 28 (2), 399-403.
Bucher, E. H., & Montenegro, R. (1974). Hábitos forrajeros de cuatro hormigas simpátridas del género Acromyrmex (Hymenoptera, Formicidae). Ecología, 2, 47–53.
Cabrera, V. E. (1976) Regiones fitogeográficas argentinas. Editorial ACME, Buenos Aires, Argentina.
Claver, S. (2000) Ecología de Acromyrmex lobicornis (E.) (Hymenoptera: Formicidae) en la Reserva de Biosfera de Ñacuñán, provincial Biogeográfica del Monte. Tesis doctoral. Universidad Nacional de La Plata, Buenos Aires, Argentina.
Cristiano, M. P., Cardoso, D. C., Sandoval-Gómez, V. E. & Simoes-Gomes, F. C. (2020) Amoimyrmex Cristiano, Cardoso & Sandoval, gen. nov. (Hymenoptera: Formicidae): a new genus of leaf‐cutting ants revealed by multilocus molecular phylogenetic and morphological analyses. Austral Entomology, 59, 643-676.
Cuezzo F., & Larrea, D. (2021) Formicidae (Hymenoptera) species from Argentina and Uruguay. [fecha de acceso: 15-01-21]. < https://biodar.unlp.edu.ar/formicidae/ >
Dagatti, C. (2016) Diversidad de hormigas (Hymenoptera: Formicidae) en el cultivo de la vid con manejo orgánico y tradicional en Mendoza [disertación]. Mendoza (Argentina): Universidad Nacional de Cuyo.
Dagatti, C., Bernabé, A., Rossi, L., & Becerra, V. (2019) Actividad forrajera de Acromyrmex striatus (Roger,1863) (Formicidae: Attini) en un viñedo orgánico en Mendoza, Argentina. Revista de Investigaciones Agrícolas, 45 (2), 191-195.
Dans, D., Anglada, M., & Maidana, A. (2009) Caracterización del daño de hormigas cortadoras en el cultivo de sorgo (Sorghum spp.). Revista Científica Agropecuaria,13(1), 7-15.
de Coll O. (2003) Detección y control de hormigas cortadoras (Hymenoptera-Formicidae) en plantaciones forestales en Misiones y noreste de Corrientes. Tesis doctoral. Universidad Nacional del Nordeste, Corrientes, Argentina.
Della Lucia, T. M. C. (2003) Introducción a la ecología de las hormigas. En: Fernández, F. (ed). (2003). Introducción a las hormigas de la región Neotropical. Bogotá, Colombia. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt.
De Vasconcelos, H. (1990) Foraging activity of two species of leaf-cutting ants (Atta) in a primary forest of the Central Amazon. Insectes socieux, 37 (2), 131-145.
Diehl-Fleig, E. (1995) Formigas: organizaçao social e ecologia comportamental. Editorial Unisinos, São Leopoldo, Brazil.
Di Rienzo, J. A.; Casanoves, F.; Balzarini, M.G.; Gonzalez L.; Tablada, M. & Robledo, C. W. (2016) InfoStat versión 2016. Grupo InfoStat. Universidad Nacional de Córdoba, Argentina.
Elizalde, L., & Farji-Brener. A. (2012) To be or not to be faithful: flexible fidelity to foraging trails in the leaf-cutting ant Acromyrmex lobicornis. Ecological Entomology, 37(5), 370-376.
Farji-Brener, A. G. (1993) Influencia de la estacionalidad sobre los ritmos forrajeros de Atta laevigata (Hymenoptera: Formicidae) en una sabana tropical. Revista de Biología Tropical, 41 (3), 897-899.
Farji-Brener, A. G., & Ruggiero, A. (1994) Leaf-cutting ants (Atta and Acromyrmex) inhabiting Argentina: Patterns in species richness and geographical range sizes. Journal of Biogeography, 21, 391-399.
Farji-Brener, A. G., & Silva, J. F. (1996) Leaf-cutter ants’ (Atta laevigata) aid to the estabishment success of Tapirira veluntinifolia (Anacardiaceae) seedlings in a parkland savanna. Journal of Tropical Ecology, 12, 163-168.
Farji-Brener, A. G. (2000) Leaf-cutting ant nests in temperate environments: mounds, mound damages and mortality rates in Acromyrmex lobicornis. Studies on Neotropical Fauna and Environment,35, 131-138.
Farji-Brener, A., & Sasal, Y. (2003) Is dump material an effective small-scale deterrent to herbivory by leafcutting ants? Ecoscience, 10, 151-154.
Fowler, H. G., & Stiles, E. W. (1980) Conservative resource management by leafcutting ants. The role of foraging territories and trails, and environmental patchiness. Sociobiology, 5, 24-42.
Fowler, H. G., Forti, L. C., Pereira-da-Silva, V., Saes, N. B. (1986) Economics of grass-cutting ants. In: Fire ants and leaf-cutting ants: biology and management (ed. Lofgren, C. S., Vander Meer, R. K., pp. 28-35, Westview Press, Boulder, Colorado.
Fowler, H. G., Forti, L. C., Brandao, C. R., Delabie, J. H & Vasconcelos, H. L. (1991) Ecologia nutrizional de formigas. En: Ecologia nutricional de insectos e suas implicacoes no manejo de pragas (eds., Panizzi, A. R. & Parra, R. P.) Editora Manole LTDA, San Paulo, Brazil.
Gamboa, G. (1975) Foraging and leaf-carrying of the desert gardening ant Acmmrmex manglar manglar (Hymenoptera, Formicidae). Oecologia,20,102-110.
Hölldobler, B., & Wilson, E. O. (1990) The Ants. Cambridge, Harvard University Press, USA.
Jiménez, N. (2019) Patrones de herviboría y co-ocurrencia de hormigas cortadoras de hojas en forestaciones y áreas naturales del Bajo delta del Río Paraná, Argentina. Tesis doctoral, Universidad Nacional de Buenos Aires, Argentina.
Jofré, L., & Medina, A. (2012) Patrones de la actividad forrajera y tamaño de nido de Acromyrmex lobicornis (Hymenoptera: Formicidae) en una zona urbana de San Luis, Argentina. Revista de la Sociedad Entomológica Argentina, 71 (1-2), 37-44.
Lewis T., Pollard, G. & Dibley, G. (1974a) Rhythmic foraging in the leaf-cutting ant Atta erhalgtgs. Journal of Animal Ecology, 43,129-141.
Lewis T., Pollard, G. & Dibley, G. (1974b) Micro-environmental factors affecting diet patterns of foraging in the leaf-cutting ant Atta cephalotes. Journal of Animal Ecology, 43,143-153.
Marinho, C., Della Lucia, T., & Pianco, M. (2006) Fatores que deficultam o controle das formigas cortadeiras. Revista Bahia Agricola, 7 (2), 18-21.
Mehlhop, P., & Scott, N. J. (1983) Temporal patterns of seed use and availability in a guild of desert ants. Ecological Entomology, 8, 69-85.
Montoya-Lerma, J., Giraldo-Echeverrib, C., Armbrechta, I., Farji-Brener, A. & Calleb, Z. (2012) Leaf-cutting ants revisited: Towards rational management and control. International Journal of Pest Management, 58 (3), 225-247.
Moreno Kiernan, A., García Lastra, M., Culebra Mason, S., Margaria, C., & Ricci, M. (2019) Actividad de forrajeo de hormigas de hormigas Acromyrmex lundi (Guérin Méneville) (Hymenoptera: Formicidae) en áreas urbanas. Resúmenes de Jornadas Entomología Agrícola Investigación Joven, 6 (2).
Navas Romero, A., Moratta Herrera, M., & Zuliani, M. (2018) Efecto de los nidos de Acromyrmex lobicornis (Formicidae: Myrmicinae) sobre la descomposición de hojarasca, en el desierto del Monte. Boletín de la Sociedad Argentina de Botánica, 53 (4), 633-640.
Nickele, M. A., Reis Filho, W., Pie, M. R., & Penteado, S. D. R. C. (2016) Daily foraging activity of Acromyrmex (Hymenoptera: Formicidae) leaf-cutting ants. Sociobiology, 63 (1), 645-650.
Nobua Behrmann, B. E. (2014) Interacciones tróficas entre dos especies simpátricas de hormigas cortadoras y el ensamble de plantas en el Monte central. Tesis doctoral. Facultad de Ciencias Exactas y Naturales. Universidad de Buenos Aires, Argentina.
Nobua-Behrmann, B. E., López de Casenave, J., Milesi, F.A., & Farji-Brener, A. (2017) Coexisting in harsh environments: temperatura-based foraging patterns of two desert leafcutter ants (Hymenoptera: Formicidae: Attini). Mymercological News, 25, 41-49.
Norte, F. (2000) Mapa climático de Mendoza, Argentina. En: Recursos y Problemas Ambientales de las Zonas Áridas. Primera parte. Provincias de Mendoza, San Juan y La Rioja. Tomo I: Caracterización Ambiental, (eds. Abraham, E. M., & Martínez, F. M.), Mendoza, pp. 25-27.
Orr, M. R. (1992) Parasitic flies (Diptera: Phoridae) influence foraging rhythms and caste division of labor in the leaf-cutter ant, Atta cephalotes (Hymenoptera: Formicidae). Behavioral Ecology and Sociobiology, 30, 395-402.
Pérez, S. (2009) Riesgo potencial de la hormiga cortadora de hojas Acromyrmex lobicornis para las plantaciones forestales de la Patagonia. Serie técnica: “Manejo Integrado de Plagas Forestales” (ed. Villacide, J., & Corley, J.), INTA Ediciones, Bariloche, Argentina.
Pilati, A., Quirán, E. M., & Estelrich, H. D. (1997) Actividad forrajera de Acromyrmex lobicornis Emery (Hymenoptera: Formicidae) en un pastizal natural semiárido de la provincia de La Pampa (Argentina). Ecología Austral, 7, 49-56.
Pizo, M. A., & Oliveira, P. S. (2001) Size and lipid content of nonmyrmecochorous diaspores: effects on the interaction with litter-foraging ants in the Atlantic rain forest of Brazil. Plant Ecology, 157, 37-52.
Pol, R., & López de Casenave, J. (2004) Activity patterns of harvester ants Pogonomyrmex pronotalis and Pogonomyrmex rastratus in the central Monte desert, Argentina. Journal of Insect Behavior, 17, 647-661.
Pol, R.; Carmín, S., & Astié, A. (2005) Ecorregiones del Monte. En: La Situación Ambiental Argentina (eds. Brown, A., Martínez Ortiz, U.; Acerbi, M., & Corcuera, J.) pp. 227-233, Fundación Vida Silvestre. Buenos Aires, Argentina.
Rico-Gray, V. & Oliveira, P. S. (2007) The Ecology an Evolution Ant-Plant Interactions. The University of Chicago Press, USA.
Rockwood, L. (1975) The effects of seasonality on foraging in two species of leaf-cutting ants (Atta) in Guancaste Province, Costa Rica. Biotropica,7,176-193.
Sabattini, J. (2017) Impacto de hormigas cortadoras de hojas en ecosistemas implantados de Sudamérica. Trabajo final integrador. Universidad Nacional del Nordeste, Corrientes, Argentina.
Sánchez-Restrepo, A., Jiménez, N., Confalonieri, V., & Calcaterra, L. (2018) Distribution and diversity of leaf-cutting ants in Northeastern Argentina: species most associated with forest plantations. International Journal of Pest Management, DOI: 10.1080/09670874.2018.1555343.
Sanders, N. J., & Gordon, D.M. (2000) The effects of interspecific interactions on resource use and behavior in a desert ant. Oecologia, 125, 436–443.
Steinberger, Y., Leschner, H., & Shmida, A. (1992) Activity pattern of harvester ants (Messor spp.) in the Negev desert ecosystem. Journal of Arid Environments, 23, 169–176.
Weber, N. (1972) The Attines: the fungus cutting ants. American Scientist,60, 448-456.
Wirth, R., Herz, R., Ryel, R.J., Beyschlag, W., & Hölldobler, B. (2003) Herbivory of leaf-cutting ants: a case study on Atta colombica in the tropical rainforest of Panama. Springer Verlag, Berlín. Alemania.
Notas de autor
dagatti.carla@inta.gob.ar