Artículos científicos
Toxicidad de plaguicidas convencionales en los servicios ecosistémicos de la artropofauna terrestre en el cultivo de cacao (Theobroma cacao) en San Martín, Perú
Toxicity of conventional pesticides on the ecosystem services of terrestrial arthropod fauna in cocoa (Theobroma cacao) cultivation in San Martin, Peru.
Toxicidad de plaguicidas convencionales en los servicios ecosistémicos de la artropofauna terrestre en el cultivo de cacao (Theobroma cacao) en San Martín, Perú
Revista de la Sociedad Entomológica Argentina, vol. 81, núm. 4, 2022
Sociedad Entomológica Argentina
Recepción: 16 Marzo 2022
Aprobación: 09 Agosto 2022
Resumen: Se evaluó la toxicidad de cuatro plaguicidas en los servicios ecosistémicos de la artropofauna terrestre en el cultivo de cacao. Se aplicó cipermetrina (T1), carbofurano (T2), oxicloruro de cobre (T3) y clorpirifos (T4) en una finca de cacao en San Martín, Perú. Se colocaron cuarenta trampas de caída por cada tratamiento para capturar a la artropofauna terrestre en cuatro evaluaciones. Se concluye que las familias que presentaron mayor abundancia de individuos fueron Formicidae, Entomobryidae y Poduridae. Para la evaluación global, se encontraron diferencias significativas en los depredadores para el índice de riqueza específica, siendo T3 el que presentó los números más bajos; mientras que para el índice de Margalef, el valor más bajo fue T3. Para el análisis por evaluaciones se encontraron diferencias significativas en los detritívoros durante la segunda evaluación para el número de individuos, siendo T4 el número más bajo. También se encontraron diferencias significativas en los depredadores durante la primera evaluación en el índice de Margalef, observándose en T4 el valor más bajo. El gremio trófico que permitió evaluar la toxicidad de forma más eficiente fueron los depredadores, la T1 es el plaguicida más compatible con los artrópodos terrestres asociados a cultivo de cacao y, los índices de diversidad alfa mostraron diferencias significativas entre los plaguicidas aplicados.
Palabras clave: Artrópodos, Diversidad alfa, Gremios tróficos, Trampas de caída.
Abstract: Toxicity of four pesticides in ecosystem services of terrestrial arthropofauna in cocoa cultivation was evaluated. Cypermethrin (T1), carbofuran (T2), copper oxychloride (T3) and chlorpyrifos (T4) were applied in a cocoa farm in San Martín, Peru. Forty pitfall traps were placed for each treatment to capture terrestrial arthropofauna in four evaluations. It is concluded that the families that presented the greatest abundance of individuals were Formicidae, Entomobryidae and Poduridae. For the global evaluation, significant differences were found in the predators for the specific richness index, being T3 the one that presented the lowest numbers; while for the Margalef index, the lowest value was T3. For the analysis by evaluations, significant differences were found in the detritivores during the second evaluation for the number of individuals, with T4 being the lowest number. Significant differences were also found in the predators during the first evaluation in the Margalef index, with the lowest value being observed in T4. The trophic guild that allowed the most efficient evaluation of the toxicity were the predators, T1 is the most compatible pesticide with the terrestrial arthropods associated with cocoa cultivation, and the alpha diversity indices showed significant differences between the applied pesticides.
Keywords: Alpha diversity, Arthropods, Pitfall traps, Trophic guilds.
INTRODUCCIÓN
El cultivo de cacao (Theobroma cacao) en el Perú, aporta una gran cantidad de beneficios, al poseer cualidades terapéuticas y nutricionales que son útiles para la fabricación de otros productos como cacao en polvo, manteca, pasta y chocolate (Esenarro et al., 2021), y del que dependen económicamente más de 100000 familias. Este cultivo debe cumplir los estándares internacionales para que se posicione mundialmente (MINAGRI, 2019).
Uno de los mayores problemas en la agricultura y, por ende, en el cultivo de cacao es el uso indiscriminado de plaguicidas, debido a que los contaminantes derivados de esta actividad antropogénica se liberan a la atmósfera y posteriormente, se almacenan en la superficie del suelo (Abt & Robin, 2020).
Las principales plagas que afectan al cultivo de cacao como mazorca negra (también conocida como pudrición parda), escoba de bruja, moniliasis, mazorquero del cacao , etc., son controladas de forma tradicional; sin embargo, el control de éstas también es acompañado de sustancias químicas convencionales como la cipermetrina, carbofurano, oxicloruro de cobre y clorpirifos, cuyas categorías toxicológicas son moderadamente peligrosa, extremadamente peligroso, ligeramente peligroso y moderadamente peligroso, respectivamente (Gomero, 2014). Se ha determinado que estas sustancias químicas pueden afectar a la fauna benéfica no objetivo, y, por ende, a los servicios ecosistémicos que estos brindan, lo que provoca un impacto ecológico negativo para el ecosistema (Caja-Molina & Iannacone, 2021; Dellafredad & Iannacone, 2021; Pérez et al., 2021).
La toxicidad de los plaguicidas en base a las mezclas químicas detectadas en el medio ambiente puede evaluarse mediante comparaciones con valores de calidad ambiental y efectos ecotoxicológicos en especies bioindicadoras clave (Iannacone & Lamas, 2002; Lin et al., 2021; Pérez et al., 2021). Se ha señalado que la toxicidad permite hallar la naturaleza y la trascendencia del riesgo del contaminante, en este caso los agroquímicos convencionales, empleando los contextos más graves y de peor exposición en el ecosistema (Peñafiel-Sandoval & Iannacone, 2020).
Para determinar la toxicidad procedente de la aplicación de plaguicidas, es común utilizar a la artropofauna terrestre como un indicador de calidad ambiental (Davis et al., 2001; Pérez et al., 2021). Los insectos cumplen un papel significativo en este tipo de ecosistemas debido a que proporcionan servicios ecosistémicos diversos (Chowdhury et al., 2017). Para identificar los servicios ecosistémicos de la artropofauna terrestre, se clasifica a los insectos según su grupo trófico a nivel de familia y a partir de ello se le asigna a un gremio determinado (EFSA, 2016; Sánchez et al., 2019; Greenop et al., 2021). Para estimar la diversidad de estos individuos según su gremio trófico, se realiza la medición de la diversidad alfa utilizando índices comunitarios (Şentürk & Özkan, 2017; Cole et al., 2020).
Es por ello que el objetivo principal del presente estudio fue evaluar la toxicidad de la aplicación de cuatro plaguicidas convencionales en los servicios ecosistémicos de la artropofauna terrestre en el cultivo de cacao en San Martín, Perú.
MATERIALES Y MÉTODOS
Área Experimental
El estudio se realizó en un cacaotal localizado a la altura del km 19 de la carretera Pelejo Papaplaya, centro poblado de Sangamayoc, distrito de Barranquita, provincia de Lamas, departamento de San Martín, Perú (06° 16′ 02.21″ S 76° 08′ 50.34″ O) y a una altitud de 169 msnm.
El área experimental tuvo una extensión de 1000 m. (50 m x 20 m), la cual estuvo dividida en diez parcelas (10 m x 10 m) (Avelino & Deheuvels, 2008) y cada parcela estuvo dividida en cuatro subparcelas (Iannacone & Murrugarra, 2000) (5 m x 5 m), se tuvo en cuenta el efecto borde, por lo que se consideró dos metros lineales de separación entre la ubicación de las trampas de caída de cada subparcela con distintos tratamientos. El área control fue de 250 m. (25 m x 10 m), la cual estuvo dividida en diez subparcelas.
Se realizó una sola aplicación de los plaguicidas convencionales en el inicio del estudio. Los cuatro tratamientos (T), cipermetrina (T1), carbofurano (T2), oxicloruro de cobre (T3) y clorpirifos (T4), fueron aplicados en diez subparcelas cada uno. Cada parcela varió en el orden de la aplicación de los tratamientos siguiendo el sentido de las agujas del reloj, a excepción de las dos últimas parcelas de cada fila cuya distribución fue de forma aleatoria para evitar repeticiones.
Diseño Experimental
Los plaguicidas tuvieron diez repeticiones cada uno obteniendo un diseño en bloque completamente aleatorio (DBCA) de 4 x 40 (4 plaguicidas convencionales x 40 repeticiones). Los plaguicidas o tratamientos seleccionados fueron cuatro: (1) cipermetrina 250 g IA (ingrediente activo) L-1 (insecticida) (Bulltrim® EC) cuya dosis aplicada de cada productos comercial (PC) fue de 250 mL / 200 L, (2) carbofurano 480 g IA L-1 (insecticida) (Farmadan® SC), 1380 mL de PC / 200 L, (3) Oxicloruro de cobre 500 g IA Kg-1 (fungicida) (Cupravit® OB 21 WP), 0,92 Kg de PC / 200 L, (4) clorpirifos 480 g IA L-1 (insecticida) (Tifon® 4E EC), 460 mL de PC / 200 L. Las dosis fueron seleccionadas con base a las dosis de aplicación habitualmente empleadas en el cultivo de cacao e indicadas en las hojas técnicas de cada uno de los plaguicidas. Además, se empleó alcohol polivinílico (Stick Water®) (Perú Productos Agrícolas SAC-Inveragro), el cual se combinó con los plaguicidas utilizados según la dosis indicada en la ficha técnica por tipo de plaguicida (100-150 mL / 200 L), con el objetivo de que los cuatro plaguicidas se adhieran de mejor manera al cultivo de cacao debido a las lluvias constantes que se presentan los meses de verano (enero a marzo), ya que coinciden con la época de mayor intensidad de precipitación en la zona. El control estuvo conformado por 40 repeticiones y usó únicamente agua con alcohol polivinílico a 125 mL/ 200 L.
Muestreo de Campo
Se colocaron 200 trampas “pit fall” o de caída en cada evaluación, estos envases de plástico cuyas dimensiones fueron: diámetro: 8,5 cm y alto: 12 cm, de 430 mL que se llenaron a ¾ partes de su capacidad con una solución de formol al 3%, y combinado con detergente en poca cantidad (Siewers et al., 2014) y se distribuyeron de la siguiente manera: cada una de las 40 subparcelas presentaron cuatro trampas en la que se aplicaron los plaguicidas convencionales, las trampas pit fall fueron instaladas cada quince días, con una frecuencia de recojo de tres días o 72 h de exposición (Alvarado & Iannacone, 2010; Montgomery et al., 2021). Se realizaron en total cuatro evaluaciones durante el 2019 con una separación de quince días aproximadamente: primera evaluación (del 1 al 3 de enero), segunda evaluación (del 16 al 18 de enero), tercera evaluación (del 31 de enero al 2 de febrero) y cuarta evaluación (del 15 al 17 de febrero). El control presentó 10 suparcelas con cuatro trampas pit fall cada una, y evaluado durante la primera evaluación con el fin de asegurar el inicio estándar en comparación a los otros cuatro tratamientos con los plaguicidas convencionales. Siendo que el propósito del estudio fue comparar los cuatro plaguicidas convencionales entre sí en base a seis índices de diversidad alfa que por sí solos tienen su interpretación, en base a un entorno agrícola real de cacaotal de naturaleza comercial, el diseño experimental empleado de solo comparación entre plaguicidas convencionales siguió lo propuesto por Krauss et al. (2011) y Sattler et al. (2020). Por razones éticas, el agricultor dueño de cacaotal autorizó el estudio en la que emplearon los cuatro plaguicidas convencionales en el área experimental en las cuatro evaluaciones con ausencia de un control sin aplicación de plaguicidas.
Las muestras de artropofauna terrestre fueron recolectadas al tamizar el contenido de cada trampa a través de tamiz fino de 500 µm de diámetro de abertura. Los individuos obtenidos fueron almacenados en frascos herméticos, cuyo contenido fue recolectado de las cuatro trampas “pit fall” que conformaban cada subparcela. A cada uno de los frascos se le adicionó alcohol etílico al 70% y después estos envases fueron codificados (Iannacone & Montoro, 2002; Montgomery et al., 2021). Se utilizaron frascos herméticos nuevos para el almacenamiento en cada evaluación.
Análisis de laboratorio
En el laboratorio se analizó cada frasco, los individuos fueron colocados en una placa de Petri grande y se reconocieron utilizando el microscopio estereoscópico, para su manipulación se usaron pinzas y agujas enmangadas y para su limpieza, pinceles y alcohol (Fernández et al., 2017). Para asegurar la correcta determinación de estos individuos recolectados se contó con el apoyo de especialistas en taxonomía del Museo de Historia Natural, Laboratorio de Ecología y Biodiversidad Animal (LEBA), Facultad de Ciencias Naturales y Matemática de la Universidad Nacional Federico Villarreal (UNFV) (Porter et al., 2014). Los códigos de depósito en la colección entomológica fueron Ent002132 a ENT002190. Posteriormente la información que se recopiló fue copiada en el programa Microsoft Office Excel 2013, con la finalidad de crear una base de datos inicial que sirvió para contabilizar la cantidad de individuos por orden y familia (Montaño et al., 2012).
Diseño Estadístico
Después de clasificar a las familias por gremios tróficos (GT), en cada evaluación se calcularon los seis índices de diversidad alfa por tratamiento y evaluaciones utilizando el programa PAST 3.0 (Hammer et al., 2001). Los datos ordenados por índices fueron analizados en el programa SPSS Statistics 22.0. Se utilizó la prueba de normalidad Shapiro–Wilk (tamaño de muestra = 40) y de homogeneidad de varianzas de Levene, para determinar el uso de pruebas paramétricas o no paramétricas (Arias et al., 2017). Posteriormente, estos datos fueron evaluados para determinar la eficacia de los tratamientos y sus repeticiones utilizando la prueba ANOVA y en aquellos casos donde existían diferencias significativas entre tratamientos se utilizó la prueba de comparación multiple de Tukey. En ocasiones donde no se cumplieran las condiciones de las pruebas paramétricas, se utilizó la prueba no paramétrica de Kruskal-Wallis, la cual es equivalente a ANOVA. Para la evaluación global fue empleado el ANOVA de medidas repetidas y su equivalente no paramétrico con base a la prueba de Friedman (Chi.) tomando en consideración la temporalidad de las cuatro evaluaciones entre tratamientos.
Evaluación de la toxicidad
Se empleó esta técnica para determinar la magnitud de la toxicidad del carbofurano (T2), clorpirifos (T4), cipermetrina (T1) y oxicloruro de cobre (T3) sobre los artropofauna de suelo (Iannacone et al., 2009). Se realizó un análisis comparativo entre estos cuatro plaguicidas convencionales en base a los seis índices de diversidad alfa y se determinó que la toxicidad se obtiene cuando se cumplan los siguientes casos en los resultados:
1) Riqueza específica (S): Se observa una mayor toxicidad cuando disminuye el número total de familias agrupadas por GT entre tratamientos en cada evaluación (Alarcón et al., 2018).
2) Número de individuos (N): Se observa una mayor toxicidad cuando disminuye la cantidad total de individuos de cada familia agrupada por GT entre los tratamientos de cada evaluación (Alarcón et al., 2018).
3) Diversidad de Margalef (Dmg): Se nota una mayor toxicidad cuando disminuye el número de familias agrupadas por GT por número de individuos entre tratamientos de cada evaluación (Margalef, 1969).
4) Diversidad de Shannon-Wienner (H´): Se observa una mayor toxicidad cuando disminuye numéricamente este índice en una comunidad en base del número de familias agrupadas por GT (Campo & Duval, 2014).
5) Equidad de Pielou (J´): Se nota una mayor toxicidad cuando disminuye numéricamente este índice en una comunidad en base del número de familias agrupadas por GT (Moreno, 2001).
6) Dominancia de Simpson (D): Se verifica una mayor toxicidad cuando aumenta numéricamente este índice en una comunidad de familias agrupadas por GT (Zarco et al., 2010).
RESULTADOS
Caracterización general de la artropofauna terrestre:
En la evaluación global (cuatro evaluaciones), se recolectó un total de 9036 individuos, distribuidos en 16 órdenes y 89 familias (Tabla I). Los tres órdenes con mayor número de individuos fueron Hymenoptera (44,40%), Collembola (38,70%) y Coleoptera (3,84%); sin embargo, los que presentaron mayor diversidad de familias fueron Coleoptera (19,10%), Diptera (19,10%) y Hemiptera (13,48%). Las familias que presentaron mayor abundancia de individuos fueron Formicidae (44,17%), Entomobryidae (31,67%) y Poduridae (6,47%). Por tratamientos, el número de individuos recuperados en orden creciente fue en el T2 (21,92%), T4 (23,45%), T1 (27,30%) y T3 (27,32%); sin embargo, el número de familias recuperadas en orden creciente fue T2 (57,30% del total de familias), T3 y T4 igualados (60,67% del total de familias) y T1 (70,79% del total de familias) (Tabla I).
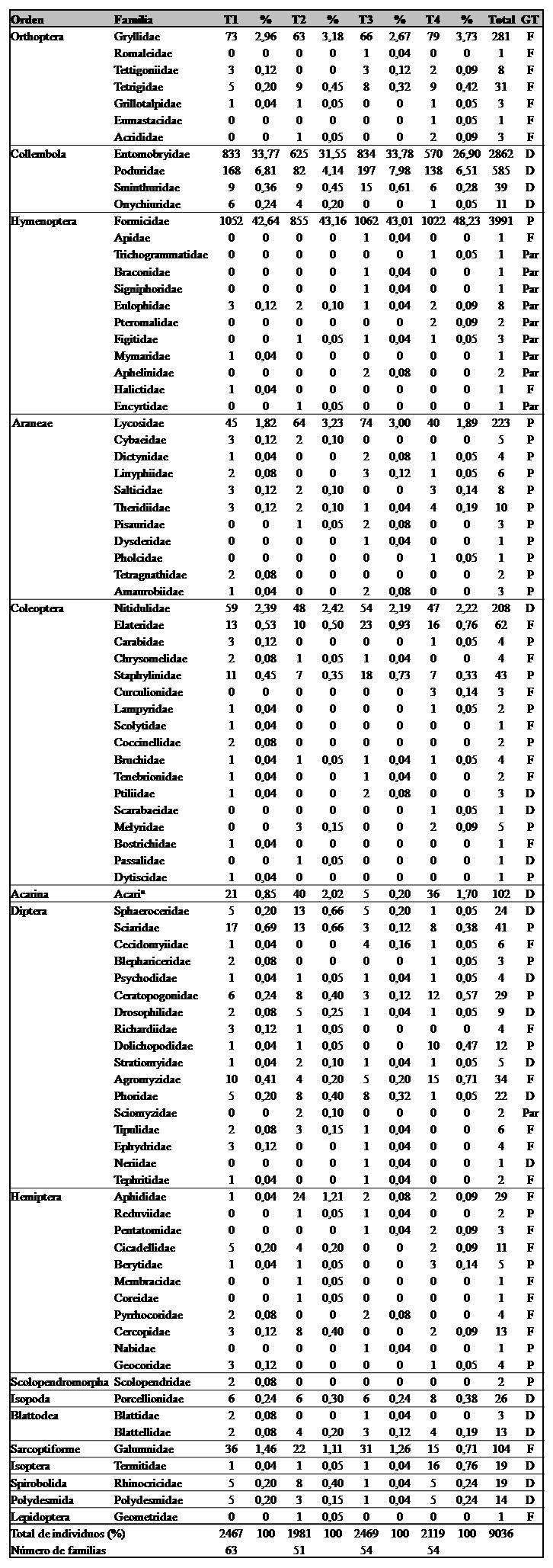
Tabla I.
Órdenes, familias y gremios tróficos de la artropofauna terrestre en el cultivo de cacao en la evaluación global (cuatro evaluaciones) bajo el efecto de cuatro plaguicidas convencionales en el departamento de San Martín, Perú.
T1=Cipermetrina, T2=Carbofurano, T3=Oxicloruro de Cobre, T4= Clorpirifos, GT= Gremio trófico, F= Fitófago, D= Detritívoro, P= Depredador, Par= Parasitoide. a: Taxón que no corresponde al nivel de familia (Acari que no son galumniforme).
Análisis a nivel taxonómico de familia:
Tratamiento Control:
Se recolectaron en total 3430 individuos distribuidos en 38 familias, siendo Entomobryidae (40,36%), Formicidae (28,75%) y Gryllidae (7,14%), las familias que presentaron mayor abundancia de individuos.
Primera Evaluación
Se recolectaron en total 3566 individuos distribuidos en 71 familias, siendo Entomobryidae (36,32%), Formicidae (32,61%) y Poduridae (10,77%) las familias que presentaron mayor abundancia de individuos. Por tratamientos, la abundancia de individuos en orden creciente fue el siguiente: T2 con un total de 760 individuos distribuidos en 40 familias; T4, 824 individuos distribuidos en 34 familias; T1, 990 individuos distribuidos en 42 familias y T3, 992 individuos distribuidos en 38 familias. En el análisis de los seis índices de diversidad alfa no se encontró diferencias (S: F=0,04, p=0,96; Individuos: F=0,07, p=0,97; Dmg: F=0,29, p=0,86; H’: F=0,01, p=0,94; J`: F=0,09, p=0,94; D: F=0,06, p=0,79).
Segunda Evaluación
Se recolectaron en total 2760 individuos distribuidos en 57 familias, siendo Formicidae (57,28%), Entomobryidae (25,76%) y Poduridae (3,15%) las familias que presentaron mayor abundancia de individuos. Por tratamientos, la abundancia de individuos en orden creciente fue el siguiente: T2 con un total de 620 individuos distribuidos en 27 familias; T4, 622 individuos distribuidos en 28 familias; T3, 741 individuos distribuidos en 26 familias y T1, 777 individuos distribuidos en 36 familias. En el análisis de los seis índices de diversidad alfa no se encontró diferencias significativas entre tratamientos (S: F=0,02, p=0,99; Individuos: F=0,03, p=0,99; Dmg: F=0,22, p=0,89; H’: F=0,05, p=0,98; J`: F=0,11, p=0,93; D: F=0,14, p=0,91).
Tercera Evaluación
Se recolectaron en total 634 individuos distribuidos en 35 familias, siendo Formicidae (41,01%), Entomobryidae (21,77%) y Poduridae (9,46%) las familias que presentaron mayor abundancia de individuos. Por tratamientos, la abundancia de individuos en orden creciente fue el siguiente: T2 con un total de 129 individuos distribuidos en 17 familias; T3, 148 individuos distribuidos en 13 familias; T1, 175 individuos distribuidos en 16 familias y T4, 182 individuos distribuidos en 23 familias. En el análisis de los seis índices de diversidad alfa no se encontró diferencias significativas entre tratamientos (S: F=0,06, p=0,97; Individuos: F=0,08, p=0,96; Dmg: F=0,20, p=0,90; H’: F=0,12, p=0,92; J`: F=0,13, p=0,91; D: F=0,14, p=0,90).
Cuarta Evaluación
Se recolectaron en total 2076 individuos distribuidos en 42 familias, siendo Formicidae (47,54%), Entomobryidae (34,59%) y Gryllidae (4,82%) las familias que presentaron mayor abundancia de individuos. Por tratamientos, la abundancia de individuos en orden creciente fue el siguiente: T2 con un total de 472 individuos distribuidos en 21 familias; T4, 491 individuos distribuidos en 21 familias; T1, 525 individuos distribuidos en 27 familias y T3, 588 individuos distribuidos en 22 familias. En el análisis de índices de diversidad alfa no se encontró diferencias significativas entre tratamientos (S: F=0,08, p=0,96; Individuos: F=0,03, p=0,99; Dmg: F=0,31, p=0,84; H’: F=0,10, p=0,93; J`: F=0,11, p=0,91; D: F=0,12, p=0,92).
En ninguna de las cuatro evaluaciones se obtuvieron diferencias significativas para los seis índices de diversidad alfa analizados, por lo que la evaluación a nivel de familia sin separar por servicios ecosistémicos con base de los GT no permitió determinar si existe toxicidad sobre la artropofauna terrestre derivado de la aplicación de los cuatro plaguicidas estudiados. Es por ello que se procedió a realizar el análisis a nivel de GT, lo cual si permitió determinar la toxicidad.
Análisis descriptivo a nivel de gremios tróficos:
En la evaluación global, el número de familias encontradas por GT en orden creciente fue: parasitoides (11,24%), detritívoros (23,60%), depredadores (30,34%) y fitófagos (34,83%). Sin embargo, el número de individuos recolectados en orden creciente fue: parasitoides (0,24%), fitófagos (6,97%), detritívoros (43,95%) y depredadores (48,84%).
Análisis global a nivel de gremios tróficos de los índices de diversidad de la artropofauna
En la evaluación global, de los cuatro GT evaluados en esta investigación, solo en el gremio trófico depredador se registró diferencias significativas para los índices S (Chi.=7,23; p=0,04) y Dmg (Chi.=3,57; p=0,02) entre los tratamientos evaluados. Para el índice S el T1, fue estadísticamente igual al T2 y T4, pero diferente al T3. En el caso de Dmg el T3 presentó el valor más bajo en el índice Dmg, aunque estadísticamente igual al T2 y T4, pero diferente al T1. En los demás índices evaluados como el N, H`, J´ y D no se registró diferencias estadísticas para cada uno de ellos entre los cuatro tratamientos (Tabla II). Los GT detritívoro (S: F=0,56, p=0,64; Individuos: F=2,98, p=0,06; Dmg: F=0,34, p=0,79; H’: F=0,88, p=0,46; J`: F=1,97, p=0,37; D: F=0,94, p=0,43), fitófago (S: Chi.=3,75, p=0,24; Individuos: Chi.=1,92, p=0,57; Dmg: F=0,85, p=0,47; H’: F=1,08, p=0,37; J`: F=0,61, p=0,61; D: F=0,97, p=0,42) y parasitoide (S: Chi.=1,08, p=0,11; Individuos: Chi.==2,03, p=0,16; Dmg: Chi.==0,23, p=093; H’: Chi.=0,07, p=0,98; J`: Chi.=0,002, p=0,99; D: Chi.=0,23, p=0,93) no mostraron diferencias globales entre los cuatro tratamientos.
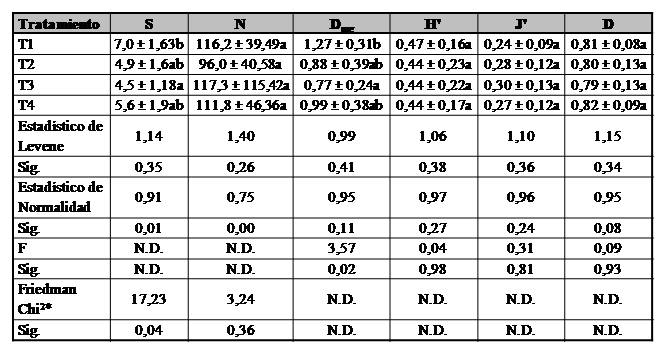
Tabla II.
Valores promedios de los índices de diversidad alfa del gremio trófico depredador en el cultivo de cacao en la evaluación global bajo el efecto de cuatro plaguicidas convencionales en el departamento de San Martín, Perú.
T1=Cipermetrina; T2=Carbofurano; T3=Oxicloruro de Cobre; T4=Clorpirifos; S=Riqueza Específica; N=Número de Individuos; Dmg=Margalef; H’=Shannon-Wienner; J’=Equidad de Pielou; D=Dominancia de Simpson; X ± DE=Media ± Desviación estándar; Sig.=Nivel de Significancia; F=Estadísticos de Fisher del ANOVA de muestras repetidas; Chi2*=Estadísticos de Friedman; N.D.=No Determinado; Letras minúsculas iguales en una misma columna indican que el efecto entre tratamientos es estadísticamente igual (p ≥ 0.05). La evaluación global incluye la variabilidad entre repeticiones y temporal.
Análisis por cada una de las cuatro evaluaciones a nivel de gremios tróficos de los índices de diversidad de la artropofauna
Gremio Trófico detritívoro
De las cuatro evaluaciones realizadas en esta investigación, solo en la segunda se registró diferencias estadísticamente significativas para el índice N entre los tratamientos evaluados. En el tratamiento T4 se observó un numero significativamente menor de individuos que en los tratamientos T1 y T3, mientras que no hubo diferencias con el tratamiento T2 (F=5,26, p=0,01). En los demás índices evaluados no se registró diferencias estadísticamente significativas entre cada uno de ellos por tratamiento (F=0,63-2,51, p=0,08-0,60) (Tabla III). No se observaron diferencias en la primera, tercera y cuarta evaluación para el GT detrítivoro en los seis índices de diversidad alfa (S: H=0,41-2,42, p=0,49-0,94; Individuos: H=0,87-3,96, p=0,11-0,83; Dmg: H=0,25-4,03, p=0,26-0,97; H´: F=0,27-1,71, p=0,18-0,97; J´: F=0,35-1,15, p=0,08-0,79; D: F=0,16-1,45, p=0,24-0,98).
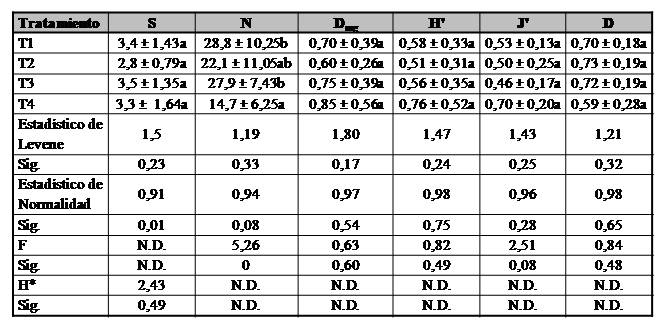
Tabla III.
Valores promedios de los índices de diversidad alfa del gremio trófico detritívoro en el cultivo de cacao en la segunda evaluación bajo el efecto de cuatro plaguicidas convencionales en el departamento de San Martín, Perú.
T1=Cipermetrina; T2=Carbofurano; T3=Oxicloruro de Cobre; T4=Clorpirifos; S=Riqueza Específica; N=Número de Individuos; Dmg=Margalef; H’=Shannon-Wienner; J’=Equidad de Pielou; D=Dominancia de Simpson; X ± DE=Media ± Desviación estándar; Sig.=Nivel de Significancia; F=Estadísticos de Fisher del ANOVA; H*=Estadísticos de contraste de Kruskal-Wallis; N.D.=No Determinado. Letras minúsculas iguales en una misma columna indican que el efecto entre tratamientos es estadísticamente igual (p ≥ 0,05).
Gremio Trófico depredador
De las cuatro evaluaciones realizadas en esta investigación, solo en la primera se encontró diferencias estadísticamente significativas para el índice Dmg entre los tratamientos evaluados. En el tratamiento T4 se observó un numero significativamente menor de individuos que en el tratamiento T1, mientras que no hubo diferencias con los tratamientos T2 y T3 (F=3,30, p=0,03). En los demás índices evaluados no se registró diferencias estadísticamente significativas entre cada uno de ellos por tratamiento (H=0,90-6,38, p=0,09-0,82) (Tabla IV). No se observaron diferencias en la segunda, tercera y cuarta evaluación para el GT depredador en los seis índices de diversidad alfa (S: H=0,18-7,43, p=0,06-0,98; Individuos: H=2,03-2,26, p=0,22-0,57; Dmg: H=0,62-0,92, p=0,20-0,89; H´: H=0,71-2,78, p=0,42-0,97; J´: F=0,37-1,01, p=0,41-0,77; D: F=0,14-0,36, p=0,55-0,94).
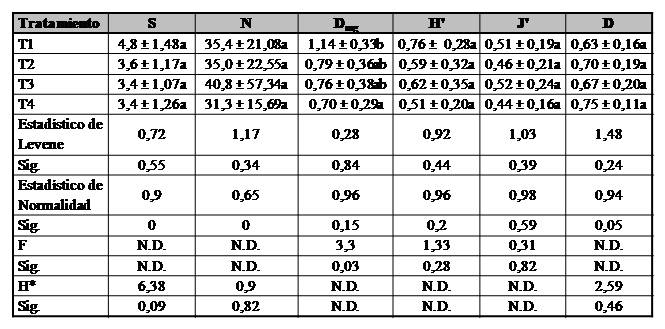
Tabla IV.
Valores promedios de los índices de diversidad alfa del gremio trófico depredador en el cultivo de cacao en la primera evaluación bajo el efecto de cuatro plaguicidas convencionales en el departamento de San Martín, Perú.
T1=Cipermetrina; T2=Carbofurano; T3=Oxicloruro de Cobre; T4=Clorpirifos; S=Riqueza Específica; N=Número de Individuos; Dmg=Margalef; H’=Shannon-Wienner; J’=Equidad de Pielou; D=Dominancia de Simpson; X ± DE=Media ± Desviación estándar; Sig.=Nivel de Significancia; F=Estadísticos de Fisher del ANOVA; H*=Estadísticos de contraste de Kruskal-Wallis; N.D.=No Determinado; Letras minúsculas iguales en una misma columna indican que el efecto entre tratamientos es estadísticamente igual (p ≥ 0,05).
Gremio Trófico fitófago y parasitoide:
De las cuatro evaluaciones realizadas en esta investigación, en ninguna se registró diferencias estadísticamente significativas entre sus tratamientos en los seis índices de diversidad alfa analizados para los fitófagos (S: H´=1,17-5,82, p=0,12-0,60; Individuos: H=0,16-7,40, p=0,06-0,98; Dmg: F=0,14-2,23, p=0,10-0,93; H´: H=1,14-2,48, p=0,10-0,78; J´: H=1,38-7,76, p=0,06-0,71; D: H=1,10-2,07, p=0,12-0,80) y para los parasitoides (S: H=1,02, p=0,80; Individuos: H=1,12, p=0,77; Dmg: H=0,97, p=0,81; H’: H=0,97, p=0,81; J`: H=2,00, p=0,37; D: H=0,81, p=0,81).
DISCUSIÓN
Los estudios realizados en el cultivo de cacao en el Perú se han enfocado primordialmente en identificar las principales plagas y enfermedades como: “Mazorquero” (Helicoverpa zea), “moniliasis” (Moniliophthora roreri), “escoba de bruja” (Moniliophthora perniciosa) y “pudrición parda” (Phytophthora palmivora) (Cabezas et al., 2017). Además, se conoce que el número de estudios asociados a la identificación de artrópodos terrestres realizados en campo en el Perú es escaso (Giraldo, 2014). El presente estudio evaluó la diversidad alfa de la artropofauna terrestre al nivel taxonómico de familia y de GT (Sánchez et al., 2019). Los resultados han demostrado la eficacia de evaluar la toxicidad por la aplicación de plaguicidas convencionales en los servicios ecosistémicos que brindan estos insectos a nivel de GT.
La familia más abundante fue Formicidae (44,17%), esto coincide con lo obtenido en un estudio en Colombia, el cual indica que el árbol de cacao sirve como nicho de anidamiento y alimento para hormigas de los géneros Solenopsis, Paratrechina, Brachymyrmex y Camponotus, debido que estos árboles cuentan con particularidades como rajaduras en la parte superficial del leño, orificios entre las hojas y raíces, gran número de frutos y hojas anchas (Vergara et al., 2007). Además, una de las condiciones que favoreció a la presencia de hormigas es la sombra de los árboles de cacao, lo cual coincide con lo indicado en un estudio de realizado en Brasil, donde se demuestra que este factor ayuda a conservar la diversidad de estos artrópodos terrestres, y, por lo tanto, a preservar los servicios ecosistémicos que brindan como depredadores de insectos fitófagos (Delabie et al., 2007). Las hormigas pueden presentar una abundancia dominante en los ambientes terrestres y, debido a sus múltiples funciones, se encuentran en muchos ecosistemas desempeñando un papel ecológico importante como ingenieros de ecosistemas (Flores-Maldonado et al., 2021).
La segunda y tercera familia más abundante fueron Entomobryidae (31,67%) y Poduridae (6,47%), los cuales pertenecen al orden Collembola. La presencia de Entomobryidae se ve favorecida en condiciones donde existe material vegetal en descomposición producido por la humedad, lo cual coincide con las condiciones del presente estudio realizado durante la temporada de lluvias (Allasi, 2016). Además, un estudio realizado en el cultivo de cacao en Brasil ha señalado que la presencia de Entomobryidae está relacionada a la presencia de nidos de hormigas (Castaño-Meneses et al., 2014). En el cultivo de maíz en Colombia, los Poduromorpha, los cuales incluyen a la familia Poduridae, presentaron el mayor número de individuos capturados por trampas de caída afectados por insecticidas, al igual que los resultados obtenidos en el cacao, por lo que se puede determinar que esta familia es representativa en investigaciones donde que aplican plaguicidas y evalúan la artropofauna de suelo (Castaño-Meneses et al., 2014).
Para la evaluación de la toxicidad por aplicación de cuatro plaguicidas sobre la artropofauna en base a los GT en el cultivo de cacao, los índices S, N y Dmg mostraron diferencias entre algunos de los cuatro tratamientos con plaguicidas. El análisis a nivel de GT evaluó la toxicidad por la aplicación de plaguicidas convencionales en los servicios ecosistémicos de la artropofauna terrestre. La evaluación de la diversidad alfa de la artropofauna a nivel de familia sin analizar en base a los GT no mostró diferencias entre los cuatro plaguicidas convencionales. Pocos estudios han evaluados el efecto de los plaguicidas en los GT del suelo, y cómo estos plaguicidas pueden afectar las comunidades de fauna del suelo en múltiples GT como los detritívoros, herbívoros, mixtos y depredadores, y los procesos del suelo que regulan. En conjunto, estos resultados sugieren que los plaguicidas convencionales pueden alterar la abundancia, riqueza y diversidad de los GT de la fauna del suelo no objetivo (Atwood et al., 2018).
El GT depredador fue el que presentó los mejores indicadores por la aplicación de los plaguicidas utilizados. El GT depredador en la evaluación global para el índice S obtuvo en el T3 el menor valor, y los valores más altos en T1; mientras que en el índice Dmg, el T3 registró el menor valor y el T1 el valor más alto. El GT depredador en la primera evaluación para el índice Dmg obtuvo en el T4, el menor valor promedio, y en el T1, el valor más alto. Atwood et al. (2018) argumentan que, además, del efecto directo de los plaguicidas en la mortalidad de un artrópodo podría ocurrir un efecto indirecto o secundario por una exposición vía ingestión. De esta manera en el GT depredador, los resultados pudieran sugerir que al alimentarse de especies herbívoras afectadas por los plaguicidas carbofurano y oxicloruro de cobre, podrían experimentar un “envenenamiento secundario” y alterar su capacidad depredadora o incluso morir al alimentarse de las especies impactadas con estos plaguicidas. Sin embargo, no explicarían adecuadamente los efectos secundarios de la cipermetrina sobre el GT depredador. Otra explicación pudiera afectar a la artropofauna depredadora sería que el contacto con plaguicidas adsorbidos en las partículas del suelo y en los residuos vegetales, la disolución de los plaguicidas en agua, el transporte como partículas de polvo y en exudados como savia (Atwood et al., 2018). En todos estos casos, los cambios en las poblaciones de artrópodos en los diferentes tratamientos son también el resultado de interacciones ecológicas entre las especies de la artropofauna afectada (Sánchez-Bayo, 2021). Los resultados de nuestra investigación concuerdan con la evaluación de los índices de diversidad alfa como el H`, Dmg y D en la artropofauna de suelo en el cultivo de quinua que mostraron menores efectos de la cipermetrina en comparación a otros plaguicidas como el teflubenzuron, benzoato de emamectina e imidacloprid (Cruces et al., 2021).
El GT detritívoro en la segunda evaluación para el índice N obtuvo en el T4, el menor valor promedio. Otras investigaciones sugieren un mayor efecto tóxico del clorpirifos en comparación a otros plaguicidas como la deltametrina y el dimetoato sobre los microartrópodos detritívoros de suelo como Folsomia candida y en comparación al bifentrin, pyriproxyfen, benzoato de emamectina, y spinosad sobre Isotoma decorata (Kamoun et al., 2018; Carniel et al., 2020; Ahmed et al., 2021). Se han mostraron reducciones drásticas en los microartrópodos de suelo por la acción del clorpirifos en los cultivos de algodón y Capsicum (Suresh et al., 2021). Según la clasificación toxicológica de los plaguicidas de la OMS (2020), el clorpirifos es un neurotóxico que puede disminuir la actividad de la acetilcolinesterasa y se presenta con base a su ingrediente activo una DL50 oral (mg/kg) para la rata y se ubica en la clase II al ser inferior a 200 mg. Por lo tanto, se considera moderadamente peligroso (Mora-Gutiérrez et al., 2021). Lo cual concuerda con los resultados del presente trabajo sobre el GT detritívoro.
Los plaguicidas que representaron un mayor efecto en la fauna de suelo fueron el clorpirifos con base a Dmg para los depredadores, el carbofurano y el oxicloruro de cobre con base a S y Dmg para los detritívoros en comparación a la cipermetrina. Otras investigaciones muestran ausencia de efectos por el clorpirifos y alta toxicidad del carbofurano en la microfauna de suelo evaluadas por trampas pit fall (Ghosal & Hati, 2019). Muchos plaguicidas como el clorpirifos, carbofurano y el oxicloruro de cobre suelen reducir la abundancia de la artropofauna al aumentar directamente la mortalidad o reducir la fecundidad de la fauna componente del suelo (Sánchez-Bayo, 2021).
La cipermetrina es el plaguicida más compatible en comparación al clorpirifos, carbofurano y oxicloruro de cobre con los artrópodos terrestres asociados a cultivo de cacao. Este insecticida que pertenece al grupo de los piretroides es un modulador no persistente de los canales de sodio, caracterizado por un amplio espectro de actividad. El compuesto actúa por contacto directo en los insectos, provocando una hiperexcitación neuronal junto al axón. Debido a sus efectos residuales relativamente cortos y a su precio más bajo, este plaguicida es comúnmente utilizado por los productores de cacao (Cruces et al., 2021).
El carbofurano fue uno de los plaguicidas que presentó un mayor impacto para la S del GT depredador debido a que fue uno de los tratamientos donde se obtuvo una menor S de la artropofauna terrestre muestreada en forma global en comparación a los otros tratamientos. Se han realizado bioensayos con carbofurano en cinco artrópodos acuáticos y terrestre resultando tóxico con base a la CL50 (Concentración letal media) que fluctuaron entre 0,023 mg IA/L y 0,45 mg IA/L. Se puede determinar que este plaguicida carbámico presenta riesgo ecológico en artrópodos en base al método determinístico y empleando los cocientes de riesgo que relacionan la toxicidad y la exposición en base a 0,43 para organismos acuáticos y 2,88 para organismos terrestres, debido a que presenta efectos por ingestión en artrópodos plagas, y en especies no objetivo (Iannacone et al., 2011). Iannacone & Tejada (2007) mostraron efectos en la regeneración de la planaria de agua dulce Girardia festae a 1,17 mg/L y 2,34 mg/L de carbofurano. Sin embargo, en el presente estudio, a nivel de familia sin separar por GT no se presentaron diferencias significativas entre los índices de diversidad alfa y los tratamientos, por lo tanto, no detectó diferencias en la toxicidad por los plaguicidas.
En el GT detritívoro, encontró que Collembola fue uno de los órdenes con mayor presencia en el cultivo de maíz en Colombia bajo de la aplicación del insecticida clorpirifos (Mojocoa, 2004). En su estudio clasifica a los Collembola en Entomobryomorpha y Poduromorpha, que incluyen a las familias Entomobryidae y Poduridae respectivamente, capturados con trampas de caída. Este resultado está relacionado con lo encontrado en el presente estudio, ya que estas mismas familias fueron la segunda y tercera más abundantes a lo largo de las cuatro evaluaciones; sin embargo, aunque estadísticamente en la segunda evaluación se encontró diferencias significativas en el índice N entre el T4 y el T3, la cantidad de individuos pertenecientes a este GT sigue siendo alta para el T4.
En el GT depredador, en un estudio realizado en el cultivo de cocona en Tingo María, Perú se ha demostrado en sus resultados que los insectos capturados pertenecientes a la familia Formicidae presentaron una alta abundancia de individuos a pesar de la aplicación del plaguicida clorpirifos (Castañeda, 2015). Este resultado respalda lo encontrado en el presente estudio, donde esta misma familia fue la más abundante del GT depredador, aunque no presentó diferencias significativas entre los cuatro tratamientos para el índice N en las cuatro evaluaciones.
En el cultivo de algodón en Lima, Perú, las arañas, capturadas con trampas de caída, disminuyeron en su número de individuos después de aplicar el plaguicida clorpirifos (Cruz et al., 2019). Lo mismo ocurrió con las familias pertenecientes al orden Araneae de este estudio, ya que el número de individuos al aplicar el mismo plaguicida en la primera evaluación es menor (19) en comparación a los otros tratamientos (T1=29, T2=56 y T3=48). En el presente estudio se encontró que el plaguicida clorpirifos tuvo el valor más bajo en comparación con los otros tratamientos para el índice Dmg a nivel de GT depredador en la primera evaluación.
La diferencia significativa que se produjo entre los tratamientos en los índices de diversidad alfa N y Dmg para los GT detritívoro y depredador respectivamente, se dio en el periodo de quince a treinta días y pudo deberse a que el tiempo de persistencia de los plaguicidas disminuye por las condiciones a las que se les exponga, como el pH del suelo, presentando la Región San Martín, un suelo de tipo alcalino (Arévalo et al., 2016). Con relación al tiempo de vida media de los plaguicidas, el clorpirifos tiene un promedio de 25 días, disminuyendo en medios alcalinos (Watts, 2012). El carbofurano tiene un promedio de 149 días en medios alcalinos, por lo que al aplicarse en el suelo de San Martín su impacto en el número de individuos de la artropofauna terrestre evaluada a nivel de familia pudo observarse en las evaluaciones (Secretaría del Convenio de Rotterdam sobre el procedimiento de consentimiento fundamentado previo aplicable a ciertos plaguicidas y productos químicos peligrosos objeto de comercio internacional, 2017).
En el cultivo de café en Montenegro, Colombia, se ha demostrado que los artrópodos capturados pertenecientes a la familia Lycosidae, incluidos en el orden Araneae, estuvieron presentes a pesar de la aplicación del plaguicida T3 (Rueda & Varela, 2016). En el presente estudio, se obtuvo en la evaluación global que esta misma familia clasificada dentro del GT depredador, fue la que tuvo mayor cantidad de individuos en comparación con las otras familias que forman parte del mismo orden y el mismo tratamiento. Se obtuvo que este mismo plaguicida tuvo el un valor más medio en comparación con los otros tratamientos para el índice de diversidad alfa Dmg. Estos resultados pudieron deberse a que el tiempo de vida media de este plaguicida en el suelo es de 1 600 días (Bedmar et al., 2015) debido a que el cobre, el cual es un metal pesado, no se degrada de forma microbiológica ni química y, generalmente, permanece unido a los coloides del suelo (Mansilla, 2017).
Se concluye que las familias que presentaron mayor abundancia de individuos fueron Formicidae, Entomobryidae y Poduridae. Para la evaluación global, se encontraron diferencias significativas en los depredadores para el índice de riqueza específica, presentando el oxicloruro de cobre, el valor más bajo; mientras que para el índice de Margalef, el valor más bajo fue para el oxicloruro de cobre. Para el análisis por evaluaciones se encontraron diferencias significativas en los detritívoros durante la segunda evaluación para el número de individuos, siendo clorpirifos el que presentó el valor más bajo. También se encontraron diferencias significativas en los depredadores durante la primera evaluación en el índice de Margalef, siendo clorpirifos el que observó el valor más bajo. El gremio trófico que permitió evaluar la toxicidad de forma más eficiente fueron los depredadores, la cipermetrina es el plaguicida más compatible con los artrópodos terrestres asociados a cultivo de cacao, y los índices de diversidad alfa para la artropofauna de suelo con base a la riqueza de especies, Margalef y número de individuos mostraron diferencias significativas entre los plaguicidas aplicados.
Agradecimientos
Se contó con el financiamiento de la Dirección General de Investigación, Desarrollo e Innovación de la Universidad Científica del Sur y el soporte del Laboratorio de Ecología y Biodiversidad Animal (LEBA) de la Facultad de Ciencias Naturales y Matemáticas de la Universidad Nacional Federico Villarreal a través del uso de los equipos requeridos para el análisis de las muestras y el apoyo de sus integrantes para la identificación taxonómica de los insectos recolectados.
REFERENCIAS
Abt, E., & Robin, L.P. (2020). Perspective on cadmium and lead in cocoa and chocolate. Journal of Agricultural and Food Chemistry, 68, 13008–13015.
Ahmed, S., Asif, M.U., & Hassan, B. (2021). Toxicity of soil accumulated insecticides on the survival of Isotoma decorata (Brown, 1923) in laboratory. International Journal of Pest Management, doi: 10.1080/09670874.2021.1973689
Alarcón, G., Alvariño, L., & Iannacone, J. (2018). Arañas (Arachnida: Araneae) asociadas a formaciones vegetales en el refugio de vida Silvestre Pantanos de Villa, Lima, Perú. Biotempo, 15, 201-214.
Allasi, E. (2016). Composición taxonómica, distribución y abundancia de la clase hexápoda, asociada a la flora del Santuario Nacional Lagunas de Mejía (julio-setiembre 2014) (Tesis de pregrado). Universidad Nacional de San Agustín. Arequipa, Perú.
Alvarado, L., & Iannacone, J. (2010). Entomofauna de la palmera Ceroxylon parvifrons (Aimé Bonpland, 1804) en el área Las Palmas (Leymebamba, Amazonas, Perú). Boletín el Zarcillo, ., 1-13.
Arévalo, E., Obando, M., Zúñiga, L., Arévalo, C., Baligar, V., & He, Z. (2016). Metales pesados en suelos de plantaciones de cacao (Theobroma cacao L.) en tres regiones del Perú. Ecología Aplicada,15, 81-89.
Arias, J., Silva, G., Figueroa, I., Fischer, S., Robles, A., Rodríguez, C., & Lagunes A. (2017). Actividad insecticida, repelente y antialimentaria del polvo y aceite esencial de frutos de Schinus molle l. para el control de Sitophilus zeamais (motschulsky). Chilean Journal of Agricultural & Animal Sciences, 33, 93-104.
Atwood, L.W., Mortensen, D.A., Koide, R.T., & Smith, R.G. (2018). Evidence for multi-trophic effects of pesticide seed treatments on nontargeted soil fauna. Soil Biology and Biochemistry, 125, 144–155.
Avelino, J., & Deheuvels, O. (2008). Caracterización de diferentes dominios agroecológicos para enfermedades, productividad y biodiversidad. Proyecto Cacao Centroamérica (PCC), CATIE-Turrialba Costa Rica. 47 pp.
Bedmar, F., Gianelli, V., Angelini, H., & Viglianchino, L. (2015). Riesgo de contaminación del agua subterránea con plaguicidas en la cuenca del arroyo El Cardalito, Argentina. Revista de Investigaciones Agropecuarias,41, 70-82.
Cabezas, O., Gil, J., Gómez, R., Dávila, C., Morón, S., & Ramírez, C. (2017). Estado fitosanitario en la producción de cacao (Theobroma cacao L.) en la Región de Huánuco (Perú): Incremento del Impacto de Carmenta foraseminis Eichlin. 2017 International Symposium on Cocoa Research (ISCR). Simposio llevado a cabo en Lima, Perú.
Caja-Molina, A.V., & Iannacone, J. (2021). Evaluación del riesgo ambiental por petróleo crudo en las especies acuáticas Lemna minor, Daphnia magna y Danio rerio. Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales, 45(176), 777-794.
Campo, A., & Duval, V. (2014). Diversidad y valor de importancia para la conservación de la vegetación natural. Parque Nacional Lihué Calel (Argentina). Anales de Geografía, 34, 25-42.
Carniel, L.S.C., Niemeyer, J.C., Oliveira-Filho, L.C.I., Alexandre, D., Gebler, L., & Klauberg-Filho, O. (2020). Are there any risks of the disposal of pesticide effluents in soils? Biobed system meets ecotoxicology ensuring safety to soil fauna. Ecotoxicology, 29, 1409–1421.
Castañeda, D. (2015). Diversidad biológica y aspectos morfo-etológicos, de formícidos asociados al cultivo de cocona (Solanum sessiliflorum Dunal) en el ecotipo CT2 en Tulumayo (Tesis de pregrado). Universidad Nacional Agraria de la Selva. Tingo María, Perú.
Castaño-Meneses, G., Palacios-Vargas, J. G., Delabie, J. H., Santos, R. D. J., & Mariano, C. S. (2014). Springtails (Collembola) from nests of Ponerinae (Hymenoptera: Formicidae) ants in Brazilian cacao plantations. Florida Entomologist, 97, 1862-1864.
Chowdhury, G., Datta, U., Zaman, S., & Mitra, A. (2017). Ecosystem services of insects. Biomedical Journal of Scientific & Technical Research, ., 1-3.
Cole, R.J., Selmants, P., Khan, S., & Chazdon, R. (2020). Litter dynamics recover faster than arthropod biodiversity during tropical forest succession. Biotropica, 52, 22-33.
Cruces, L., de la Peña, E., & De Clercq, P. (2021). Field evaluation of cypermethrin, imidacloprid, teflubenzuron and emamectin benzoate against pests of quinoa (Chenopodium quinoa Willd.) and their side effects on non-target species. Plants, 10, 1788.
Cruz, L., Silva, D., & Vergara, C. (2019). Composición y fluctuación poblacional de la araneofauna en el algodonero de la Universidad Nacional Agraria La Molina, Lima, Perú. Revista peruana de biología,26, 63-80.
Davis, A., Hollowary, J., Huijbregts, H., Krikken, J., Kirk-Spriggs, A., & Sutton, S. (2001). Dung beetles as indicators of change in the forests of northern Borneo. Journal of Applied Ecology, 38, 593–616.
Delabie, J., Jahyny, B., Cardoso, I., Mariano, C., Lacau, S., Campiolo, S., Philpott, S., & Leponce, M. (2007). Contribution of cocoa plantations to the conservation of native ants (Insecta: Hymenoptera: Formicidae) with a special emphasis on the Atlantic Forest fauna of southern Bahia, Brazil. Biodiversity and Conservation, 16, 2359-2384.
Dellafredad T.C.N., & Iannacone, J. (2021). Efecto ecotoxicológico de la mezcla de Aroclor 1254 y Plomo en el bioindicador Daphnia magna. Revista Lasallista de Investigación, 18, 144-161.
European Food Safety Authority [EFSA] Scientific Committee. (2016). Guidance to develop specific protection goals options for environmental risk assessment at EFSA, in relation to biodiversity and ecosystem services. EFSA Journal, 14, 44-99.
Esenarro, D., Rodriguez, C., Arteaga, J., Garcia, G., & Flores, F. (2021). Sustainable use of natural resources to improve the quality of life in the Alto Palcazu population Center, Iscozazin-Peru. International Journal of Environmental Science and Development, 12, 146-150.
Fernández, I., Fontenla, J., Hidalgo-Gato, M., Cruz, D., Rodríguez D., Neyra, B., Mestre, N., & Gutiérrez, E. (2017). Insectos terrestres. pp. 224-253. En: Diversidad biológica de Cuba: métodos de inventario, monitoreo y colecciones biológicas (C. A. Mancina y D. D. Cruz, Eds.). Editorial AMA, La Habana, 502 pp.
Flores-Maldonado, K.Y., Rodríguez-De-León, I.R., Guzmán-Díaz, L., & Rosas-Mejía, M. (2021). Myrmecological diversity (Hymenoptera: Formicidae) in Tamaulipas, México. Revista de la Sociedad Entomológica Argentina, 80, 81–99.
Ghosal, A., & Hati, A. 2019. Impact of some new generation insecticides on soil arthropods in rice maize cropping system. The Journal of Basic and Applied Zoology, 80, 6.
Giraldo, A. (2014). Algunas sugerencias para realizar evaluaciones biológicas de artrópodos terrestres en el Perú. Ecología Aplicada,13, 57-66.
Gomero, L. (2014). Evaluation report and action plan for the safer use of pesticides (PERSUAP). Alternative Development Program (ADP).
Greenop, A., Woodcock, B.A., Outhwaite, C.L., Carvell, C.C., Pywell, R.F., Mancini, F., Edwards, K.K., Andrew C., Johnson, A.C., & Isaac, N.J.B. (2021). Patterns of invertebrate functional diversity highlight the vulnerability of ecosystem services over a 45-year period. Current Biology, 31, 4627–4634.
Hammer, Ø., Harper, D., & Ryan, P. (2001). PAST: Paleontological statistics software package for education and data analysis. Palaeontología Electrónica, ., 1- 9.
Iannacone, J., & Lamas, G. (2002) Efecto de dos extractos botánicos y un insecticida convencional sobre el depredador Chrysoperla externa. Manejo Integrado de Plagas y Agroecología, 65, 92-101.
Iannacone, J., & Montoro, I. (2002). Impacto de dos productos botánicos bioinsecticidas (azadiractina y rotenona) sobre la artropofauna capturada con trampas de suelo en el tomate en Ica, Perú. Revista Colombiana de Entomología,28, 191-198.
Iannacone, J., & Tejada, M. (2007). Empleo de la regeneración de la planaria de agua dulce Girardia festae (Borelli, 1898) (Tricladida: Dugesiidae) para evaluar la toxicidad del carbofurano. Neotropical Helminthology, ., 7-13.
Iannacone, J., & Murrugarra, Y. (2000). Efecto en las poblaciones del predador Metacanthus tenellus (Heteroptera: Berytidae) por los insecticidas botánicos Rotenona y Neem en el cultivo de tomate en el Perú. Revista Colombiana de Entomología,26, 89-97.
Iannacone, J., Alvariño, L., & Paredes, C. (2009). Evaluación del riesgo ambiental del arseniato de plomo en bioensayos con ocho organismos no destinatarios. Journal of the Brazilian Society of Ecotoxicology, 4(1-3), 73-82.
Iannacone, J., Alvariño, L., Paredes, C., Alayo, M., Mamani, N., Bonifacio, J., Mariano, M., & Miglio, M. (2011). Evaluación del riesgo ambiental de carbofurano en bioensayos con organismos no blanco. Acta Toxicológica Argentina,19, 19-31.
Kamoun, I.J., Jegede, O.O., Owojori, O.J., Bouzid, J., Gargouri, R., & Römbke, J. (2018). Effects of deltamethrin, dimethoate, and chlorpyrifos on survival and reproduction of the collembolan Folsomia candida and the predatory mite Hypoaspis aculeifer in two African and two European soils. Integrated Environmental Assessment and Management, 14, 92-104.
Krauss, J., Gallenberger, I., & Steffan-Dewenter, I. (2011). Decreased functional diversity and biological pest control in conventional compared to organic crop fields. PLoS ONE, 6(5), e19502.
Lin, B.L., Meng, Y., Kamo, M., & Naito, W. (2021). An All-in-one Tool for Multipurpose Ecological Risk Assessment and Management (MeRAM) of Chemical Substances in Aquatic Environment. Chemosphere, 268, 128826.
Mansilla, C. (2017). Impacto ambiental de la aplicación de plaguicidas en siete modelos socio-productivos hortícolas del Cinturón Verde de Mendoza (Tesis de pregrado). Universidad Nacional de Cuyo. Mendoza, Argentina.
Margalef, R. (1969). El ecosistema pelágico del Mar Caribe. Memoria de la Sociedad de Ciencias Naturales La Salle,29, 5-36.
Ministerio de Agricultura y Riego (MINAGRI). (2019). En el Perú más de 100 mil familias se dedican al cultivo de cacao en 16 regiones. Disponible en https://www.gob.pe/institucion/minagri/noticias/52030-minagri-en-el-peru-mas-de-100-mil-familias-se-dedican-al-cultivo-de-cacao-en-16-regiones.
Mojocoa, M. (2004). Efecto del uso de clorpirifos en maíz (Zea Mays L.) sobre los artrópodos no-blanco del suelo (Tesis de pregrado). Universidad del Tolima. Ibagué, Colombia.
Montgomery, G.A., Belitz, M.W., Guralnick, R.P., & Tingley, M.W. (2021) Standards and best practices for monitoring and benchmarking insects. Frontiers in Ecology and Evolution, ., 579193.
Montaño, M., Meza, A., & Dias, L. (2012). La colección entomológica CEBUC y su potencial como colección de referencia de insectos acuáticos. Boletín Científico Centro de Museos Museo de Historia natural, 16, 173–184.
Mora-Gutiérrez, A., Rubio, C., Romero-López, Á. A., & Rubio-Osornio, M. (2021). Neurotoxic effects of insecticides Chlorpyrifos, Carbaryl, Imidacloprid, in different animal species. In (Ed.), Neurotoxicity - New Advances [Working Title]. IntechOpen. https://doi.org/10.5772/intechopen.100527
Moreno, C. (2001). Métodos para medir la biodiversidad. M&T–Manuales y Tesis SEA. Zaragoza, España. 84 p.
Organización Mundial de la Salud (OMS). (2020). Clasificación recomendada por la OMS de los plaguicidas por el peligro que presentan y directrices para la clasificación de 2019. [WHO recommended classification of pesticides by hazard and guidelines to classification, 2019 edition]. Ginebra. Organización Mundial de la Salud. 99 p.
Peñafiel-Sandoval, Z.B., & Iannacone, J. (2020). Effect of urea on lead absorption in corn (Zea mays L.), spinach (Spinacia oleracea L.) and cabbage (Brassica oleracea L.). Agronomía Colombiana, 38, 205-217.
Pérez, D.J., Iturburu, F.G., Calderon, G., Oyesqui, L.A.E., De Gerónimo, E., & Aparicio, V.C. (2021). Ecological risk assessment of current-use pesticides and biocides in soils, sediments and surface water of a mixed land-use basin of the Pampas region, Argentina. Chemosphere, 263, 128061.
Porter, T., Gibson, J., Shokralla, S., Baird, D., Golding, G., & Hajibabae, M. (2014). Rapid and accurate taxonomic classification of insect (class Insecta) cytochrome . oxidase subunit 1 (COI) DNA barcode sequences using a naïve Bayesian classifier. Molecular Ecology Resources,14, 929-942.
Rueda, D., & Varela, A. (2016). Distribución espacial, composición y densidad de edafofauna en hojarasca de bosque y cafetal (Montenegro, Colombia). Acta biológica Colombiana,21(2), 399-412.
Sattler, C., Gianuca, A. T., Schweiger, O., Franzén, M., & Settele, J. (2020). Pesticides and land cover heterogeneity affect functional group and taxonomic diversity of arthropods in rice agroecosystems. Agriculture, Ecosystems and Environment, 297, 106927.
Sánchez, P., Alvariño, L., & Iannacone, J. (2019). Diversidad de insectos terrestres en cuatro comunidades vegetales del Área de Conservación Regional (ACR) Humedales de Ventanilla, Callao, Perú. The Biologist (Lima),17(1), 73-94.
Sánchez-Bayo, F. (2021). Indirect effect of pesticides on insects and other arthropods. Toxics, ., 177.
Secretaría del Convenio de Rotterdam sobre el procedimiento de consentimiento fundamentado previo aplicable a ciertos plaguicidas y productos químicos peligrosos objeto de comercio internacional. (2017). Convenio de Rotterdam Aplicación del procedimiento de consentimiento fundamentado previo aplicable a productos químicos prohibidos o rigurosamente restringidos Documento de orientación para la adopción de decisiones Carbofurano. Conferencia de las Partes. Conferencia llevada a cabo en Ginebra, Suiza.
Şentürk, Ö., & Özkan, K. (2017). Calculating landscape diversity with alpha diversity índices. Journal of Environmental Biology,38, 931-936.
Siewers, J., Schirmel, J., & Buchholz, S. (2014). The efficiency of pitfall traps as a method of sampling epigeal arthropods in litter rich forest habitats. European Journal of Entomology,111, 69-74.
Suresh, P., Jyothilaxmi, A., Reddy, K.S., Mahesh, T., & Balakrishna, D. (2021). Effect of chlorpyrifos and imidacloprid pesticides toxicity on soil microarthropod population in different crop fields of Narsampet Mandal, Warangal district (T.S.). Uttar Pradesh Journal of Zoology, 42, 72-78.
Vergara, E., Echavarría, H., & Serna, F. (2007). Hormigas (Hymenoptera Formicidae) asociadas al arboretum de la Universidad Nacional de Colombia, sede Medellín. Boletín Sociedad Entomológica Aragonesa,40, 497−505.
Watts, M. (2012). Clorpirifos: Un Posible COP a nivel global. Pesticide Action Network Norteamérica (PANNA).
Zarco, V., Valdez, J., Ángeles, G., & Castillo, O. (2010). Estructura y diversidad de la vegetación arbórea del Parque Estatal Agua Blanca, Macuspana, Tabasco. Estructura y diversidad de una selva mediana perennifolia,26, 1-17.
Notas de autor
joseiannacone@gmail.com