Artículos
Avispas parasitoides (Hymenoptera) y control biológico en Chile: Aplicaciones y Potencialidades
Parasitic wasps (Hymenoptera) and Biological Control in Chile: Applications and Potentials
Avispas parasitoides (Hymenoptera) y control biológico en Chile: Aplicaciones y Potencialidades
Revista de la Sociedad Entomológica Argentina, vol. 82, núm. 4, 2023
Sociedad Entomológica Argentina
Recepción: 13 Diciembre 2022
Aprobación: 29 Noviembre 2023
Resumen: La disminución global de la biodiversidad y la contaminación, junto con el cambio climático, amenazan directamente la seguridad alimentaria y la soberanía. Las prácticas insostenibles en la agricultura industrial, incluida la introducción de insectos no nativos, agravan esta crisis ambiental. Estos pueden invadir hábitats nativos y causar pérdida de biodiversidad. Creamos una base de datos de especies de avispas parasitarias utilizadas para el control biológico en Chile, examinando el porcentaje de especies introducidas y nativas, los plazos de introducción y las interacciones con los huéspedes. Un total del 73 % de los himenópteros corresponden a especies exóticas. También identificamos casos en los que especies parasitarias nativas e introducidas comparten los mismos huéspedes, lo que podría provocar un efecto de desbordamiento. Dado el alto endemismo de Chile en su entomofauna, la introducción de especies exóticas podría tener consecuencias perjudiciales para la biodiversidad local y los ecosistemas agrícolas. La excesiva dependencia de controladores de plagas no nativos obstaculiza la utilización de especies nativas, aumentando la vulnerabilidad a las plagas adaptadas a agentes de control biológico ampliamente utilizados. Abogamos por priorizar avispas controladoras nativas para garantizar la producción agrícola sostenible en Chile, al tiempo que mitigamos los impactos negativos de las especies exóticas.
Palabras clave: Agroecología, Control biológico de conservación, Insectagedón.
Abstract: Global biodiversity decline and pollution, along with climate change, directly threaten food security and sovereignty. Unsustainable practices in industrial agriculture, including the introduction of non-native insects exacerbate this environmental crisis. These can invade native habitats and disrupt the ecological balance, leading to biodiversity loss. We created a database of parasitic wasp species used for biological control in Chile, examining the percentage of introduced and native species, introduction timelines, and host interactions. A total of 73% of the Hymenoptera used for biological control in Chile are exotic species. This trend has grown over decades as new species were continuously introduced, resulting in an increasing accumulation of exotic species. We also identified instances of native and introduced parasitoid species sharing the same hosts, potentially causing a spillover effect. Given Chile's high endemism in its insect population, the massive introduction of exotic species could have detrimental consequences for local biodiversity and agricultural ecosystems. Overreliance on non-native pest controllers impedes the use of existing native biological control species, increasing vulnerability to pests adapted to widely used biological control agents. We advocate for prioritizing local and native parasitic wasps to ensure long-lasting, and sustainable agriculture production in Chile while mitigating the negative impacts of exotic species.
Keywords: Agroecology, Conservation biological control, Insectageddon.
INTRODUCCIÓN
Bajo el contexto de la crisis ambiental global se proyecta la agudización del problema de la producción y abastecimiento de alimentos a nivel planetario (Mace et al., 2014; Picó et al., 2020); se están experimentado aumentos en la inseguridad y pérdida sostenida de soberanía alimentaria (McKay, 2017). La actividad agroforestal industrializada ha impactado negativamente en la biodiversidad del planeta, afectando las contribuciones de la naturaleza a las personas, o “servicios ecosistémicos”, que ésta provee (Vanbergen et al., 2020). El cambio de uso del suelo, la alteración del paisaje, la contaminación con fertilizantes y plaguicidas (Tscharntke et al., 2012) y la introducción de especies exóticas con fines aplicados a la producción agrícola (Karp et al., 2012; Garibaldi et al., 2017), han sido señaladas como las externalidades negativas involucradas en la pérdida de hábitats nativos y degradación de las funciones ecosistémicas. Un caso relevante de este último tipo de problemáticas corresponde al uso de controladores biológicos de plagas (CBPs) exóticos a la zona de aplicación (He et al., 2021).
Los controladores biológicos pueden definirse como cepas o variedades de microorganismos u organismos multicelulares, principalmente invertebrados como nematodos y artrópodos (e.g., arácnidos e insectos) (Kogan, 1998; MacQuarrie et al., 2016), que son capaces de reducir la incidencia y la gravedad del daño provocado por enemigos naturales de plantas (e.g. hierbas invasivas, patógenos vegetales, organismos herbívoros, entre otros) (Abrol & Shankar, 2015).
El uso de controladores biológicos de plagas forma parte de la estrategia de manejo integrado incluso desde antes de la invención de los insecticidas organofosforados en la década de 1940 (Funasaki et al., 1988). Se ha propuesto que este manejo se basaría en el adecuado conocimiento de la biología del organismo plaga y las condiciones que pudieran disminuir su impacto en los cultivos (Kogan, 1998), existiendo al menos tres variantes mayoritariamente empleadas: i) el control biológico clásico donde se introduce un “enemigo natural” de la plaga a controlar en el nuevo hábitat que ha sido colonizado por la especie plaga, vale decir un organismo antagonista, comúnmente depredador, parásito o parasitoide, que normalmente ha co-evolucionado en interacción con el organismo plaga que consume en su lugar de origen (Howarth, 1995), ii) el control biológico aumentativo, en el que sucesivas introducciones de un enemigo natural son realizadas con la intención de garantizar el establecimiento del controlador (van Lenteren et al., 2003; Collier & Van Steenwyk, 2004), y iii) el control biológico de conservación, en el que no se liberan enemigos naturales, sino que se modifica el ambiente o las prácticas culturales con el objetivo de proteger y favorecer a los enemigos naturales ya existentes que pudieran controlar a la especie plaga (Barbosa, 1998; Tscharntke et al., 2007).
El uso de organismos para controlar plagas se incrementó a mediados de la década de 1960 (Kogan, 1998) al comenzar a salir a la luz las primeras evidencias con relación a los efectos negativos de las formulaciones químicas que se estaban aplicando como plaguicidas agrícolas y forestales (Carson, 1962). Dentro de estas primeras consecuencias detectadas en ese momento se destacaban el desarrollo de resistencias en las especies objetivo o blanco, la reaparición de plagas primarias, el surgimiento de otras plagas secundarias, además de los graves efectos en la salud y los ecosistemas derivados de la contaminación ambiental con estos productos (Davis, 2014).
Distintas evaluaciones del control biológico clásico y aumentativo han detectado problemas de efectividad y seguridad en este tipo de manejos (Simberloff & Stiling, 1996; Collier & Van Steenwyk, 2004). La incorporación de un controlador biológico exótico a un ecosistema determinado implica el riesgo de que esa especie introducida expanda su nicho empleando recursos de hábitats nativos adyacentes al agroecosistema donde es liberado, fenómeno conocido como “efecto de derrame” o “spillover” en inglés (Donoso et al., 1999). De esta forma, los organismos introducidos pueden afectar a herbívoros nativos no blanco (Howarth, 2000; Kenis et al., 2009). En esta situación, el controlador biológico puede llegar a atacar a otras especies nativas no consideradas como blancos o a obtener sus recursos alimentarios complementarios (e.g. néctar) de especies de plantas nativas (Van Lenteren et al., 2006). De esta forma podría expandir su rango de hospederos, pudiendo superponer su nicho trófico al de especies depredadoras o parasitoides locales que incluso podrían resultar desplazadas (Bennett, 1993). Además, en el caso de expandir sus presas u hospederos a especies de artrópodos nativos, esto podría generar una presión de depredación/parasitismo que podría mermar las poblaciones de especies locales. Así, resultan alteradas no solo las capacidades de control sino las funciones ecológicas de los organismos involucrados (Brown et al., 2022). De esta forma la introducción de especies exóticas podría generar asociaciones ecológicas emergentes del agente controlador biológico exótico con la biota local, desencadenar daños a las cadenas tróficas locales y promover la expansión de las especies exóticas controladoras biológicas como potenciales especies invasivas (Rand et al., 2006). En ambos casos, el efecto “spillover” podría gatillar efectos ecosistémicos en cascada, la homogeneización biótica, generar problemas de conservación y de pérdida de servicios ecosistémicos adicionales provistos por el hábitat nativo adyacente (Tscharntke et al., 2007; Seymour & Veldtman, 2010). Además, desde el punto de vista del control biológico clásico, esto repercutiría disminuyendo la eficiencia de su aplicación, dado que se espera que el organismo introducido se perpetúe en el tiempo y disperse sobre el cultivo de interés para ampliar su acción controladora (van Lenteren et al., 2003). Esta evidencia podría relativizar la relevancia y eficiencia de introducir especies o variantes exóticas adicionales de control biológico como “insumos externos” estrictamente necesarios para la producción agrícola (Fortuna et al., 2022). Este problema podría ser más agudo aún en el caso de la introducción de CBPs en zonas del planeta que presentan un alto endemismo con relación a su biodiversidad, y economías donde la agricultura corresponde a una actividad clave, como es el caso de Chile (Panez et al., 2020; Henríquez‐Piskulich et al., 2021).
En Chile, el primer registro que se tiene de importación de especies exóticas para control biológico corresponde a la avispa parasitoide Aphelinus mali (Haldeman, 1851) (Hymenoptera: Aphelinidae), que fue importada desde California en 1888 para el control del pulgón lanígero del manzano, Eriosoma lanigerum (Hausmann, 1802) (Hemiptera: Aphididae) (Lavandero & Domínguez, 2010). La siguiente introducción relevante ocurrió en 1915, con el ingreso de parasitoides de la familia Pteromalidae (Hymenoptera) Dinotiscus colon (Linnaeus, 1758) y Rhaphitelus maculatus (Walker, 1834) para el control del escólito del durazno, Scolytus rugulosus (Müller, 1818) (Coleoptera: Curculionidae) (Zúñiga, 1985). La introducción de este tipo de controladores biológicos ha continuado, siendo en las primeras décadas del siglo XXI una práctica extendida y frecuente (Williams & Polaszek, 1996; Radrigan et al., 2021). Desde entonces, la incorporación de controladores biológicos exóticos se ha expandido exponencialmente hasta las últimas décadas, principalmente a través de la importación desde Estados Unidos (Rojas, 2005; Barra-Bucarei et al., 2020). Además, al utilizar insectos parasitoides como enemigos naturales resulta relevante considerar su nivel de especificidad a diferentes hospederos (i.e. familia, género, especie), dado que, de introducirse especies polífagas, con diversos hospederos conocidos o gran plasticidad, éstas tenderán a ampliar aún más su rango de hospederos en los nuevos ambientes (Parry, 2009), generando, potencialmente, problemas de eficiencia de control y ambientales. Lo anterior es posible de considerar y evaluar bajo las directrices de la Convención Internacional de Protección Fitosanitaria (IPPC, por sus siglas en inglés), donde se establecen entre otros aspectos, las organizaciones responsables y la necesidad de llevar a cabo un análisis de riesgo de plagas antes de la introducción de una nueva especie, y la necesidad de monitorear su establecimiento y dispersión luego de la liberación, específicamente en las Normas Internacionales para Medidas Fitosanitarias 3 NIMF 3, (ISPM 3, por sus siglas en inglés) (FAO, 2005).
Esta estrategia resultaría relativamente positiva si implicara una reducción de las aplicaciones de insecticidas químicos (Murdoch et al., 1985); sin embargo, en paralelo con el incremento de especies exóticas introducidas para su uso como CBPs en Chile, el número de formulaciones de plaguicidas también ha experimentado un constante incremento desde los años ochenta y hasta las últimas décadas (González, 1998; Zúñiga-Venegas et al., 2021). Por ejemplo, para el año 2019, las ventas reportadas por el Servicio Agrícola y Ganadero (SAG) alcanzaron los 9.778.970 Kg/l de productos agrupados en la lista 1000, una clasificación interna del mencionado Servicio, que incluye insecticidas, acaricidas, nematicidas y otros (SAG, 2019), representando un aumento del 20 % respecto a los 8.179.730 Kg/l del año 2010 (SAG, 2010). Este incremento sigue la tendencia internacional de aumento de la carga de plaguicidas y la toxicidad de las formulaciones empleadas en los agroecosistemas a nivel mundial (Sharma et al., 2019), con las subsecuentes consecuencias para el medioambiente y la salud de las personas (Vale, 2008; Grube et al., 2011; Sharma et al., 2019; Silva et al., 2019).
Por otro lado, las constantes importaciones de especies exóticas para controlar plagas fitosanitarias asumen una mayor eficiencia de las especies que se ha hipotetizado que han co-evolucionado con la plaga objetivo, siguiendo los principios del control biológico clásico expuesto anteriormente. Uno de los argumentos que se emplea para promover la constante importación de insectos tanto depredadores cuanto parasitoides exóticos, como ocurre en Chile, es que las plagas de herbívoros a las cuales controlarán son también exóticas y usualmente se asume que los controladores a importar habrían co-evolucionado en sus lugar de origen empleado éstos herbívoros como presas y/o hospederos, por lo que al aplicarse a nuevas agrícolas del planeta donde los herbívoros plaga han expandido su distribución, se propone que serían más eficientes en su control que la fauna local (Howarth, 1995).
Sin embargo, aprovechar la variación intraespecífica de especies de controladores nativas o endémicas, ya sea seleccionando líneas que muestren un mejor control (selección de cepa o variedad) o individuos con características específicas para ser los progenitores de la próxima generación (selección artificial), permitiría emplear, también, a estas últimas como controladores biológicos eficientes (Kruitwagen et al., 2018).
Esta alternativa de control biológico de conservación aprovecha el uso de insumos internos agroecológicos como controladores biológicos locales (Barbosa, 1998; Tscharntke et al., 2007). Sin embargo, para llevar a la práctica lo anterior se debe superar, como primera medida, el desconocimiento de la entomofauna local, tanto a nivel taxonómico como de su biología y relaciones tróficas. Además, debiera propenderse hacia un manejo de paisaje agrícola tipo “land sharing”, en el cual éste convive con las áreas destinadas a la conservación y no del tipo “land sparing”, en el que ambos están claramente separados (Grass et al., 2019).
Debido a lo antes expuesto y, basados en los postulados presentados, este trabajo busca, a partir de una revisión de la literatura disponible sobre control biológico en Chile, i) informar sobre las diversas especies de avispas parasitoides empleadas como controladores biológicos en Chile a la fecha, ii) determinar el porcentaje de avispas parasitoides que corresponden a especies nativas y las que han sido introducidas para efectos de control de plagas fitosanitarias, iii) conocer la amplitud de hospederos a los cuales se sabe que están asociadas dichas plagas, iv) determinar qué porcentaje de estos hospederos son usados por especies nativas y que porcentaje son usados por especies introducidas y, en el caso de estas últimas, se reporta, además, la zona propuesta como origen, fechas de introducción a Chile y si han logrado establecerse en los agroecosistemas nacionales. Esta información se analiza y discute en torno a las potencialidades y riesgos del manejo integrado de plagas y la constante y en incremento introducción de especies foráneas a lo largo del tiempo para su aplicación como control biológico (van Lenteren et al., 2003).
MATERIALES Y MÉTODOS
Fuentes para obtener los trabajos a revisar
Se realizó una revisión bibliográfica a partir de167 artículos recuperados de la búsqueda en ISI Clarivate Web of Science®, Londres, Reino Unido (2023), relacionados con avispas parasitoides usadas y/o colectadas en sistemas agrícolas en Chile. Se utilizaron adicionalmente 59 artículos diferentes de los antes mencionados encontrados a través de Researchgate® (2023) GmbH, Berlín, Alemania, y 68 adicionales al emplear Google Scholar ® (2023) California, Estados Unidos. Estos correspondieron a artículos históricos, capítulos de libros disponibles en repositorios de información sobre biodiversidad como la Biodiversity Heritage Library (BHL, 2015) y la colección de revistas digitalizadas de la Revista de la Sociedad de Entomología de Chile (Sociedad de Entomología de Chile, 2019).
Trabajos de especial interés
Dentro de la literatura consultada, se consideró una actualización y ampliación del trabajo de Zúñiga (1985), que revisa los proyectos realizados por el Instituto de Investigaciones Agropecuarias (INIA) desde el año 1903 hasta 1984. En virtud de la importancia como centro de investigación y difusión, se concedió especial importancia a las publicaciones de INIA, las cuales normalmente discuten el tema del control biológico dentro de los documentos dedicados a especies en particular. En lo referente a plagas forestales, la publicación de Baldini et al. (2005), apoyado por la Corporación Nacional Forestal (CONAF) y la Fundación para la Innovación Agraria (FIA) fue un referente.
Palabras clave utilizadas en la búsqueda
Entre las palabras empleadas en la búsqueda bibliográfica destacan “parasitoid”, “biological control” y “Chile”. Complementariamente, se revisó la información disponible para las especies de parasitoides, distribución y hospederos disponibles en el repositorio de información de biodiversidad del Global Biodiversity Information Facility, GBIF (GBIF, 2022) y en la base de datos del Centre for Agricultural Bioscience International (CAB International, 2010). Adicionalmente, se accedió a literatura física no digitalizada disponible en SAG e Instituto de Entomología UMCE, Santiago, Chile.
Análisis de los datos
A partir de los datos recopilados se construyó una base de datos actualizada de las especies de parasitoides empleadas en los agroecosistemas de Chile, su condición de origen (nativo o introducido) y los hospederos que atacan según los registros. A partir de los datos obtenidos se realizaron distintas pruebas estadísticas, paramétricas y no paramétricas, según el objetivo y tipo de datos relacionados.
Para conocer la diversidad de especies de avispas parasitoides empleadas (nativas y exóticas), se calculó el índice de biodiversidad de Shannon (H’) para la especies exóticas y nativas, utilizando el programa Past4® (Hammer et al., 2001). Este índice está basado en la teoría de la información e indica la incertidumbre en predecir a que especie corresponderá un individuo desconocido. Este índice toma valores entre 0, cuando existe una sola especie y logaritmo del número de especies (S) (Moreno, 2001), cuando todas las especies están representadas por el mismo número de individuos. Se entiende que, en una situación poco diversa, donde existe una o pocas especies dominantes, es más fácil predecir a que especie corresponderá un individuo y el valor de H’ será más cercano a cero (Moreno, 2001). Se compararon los valores de H’ así obtenidos mediante una prueba t utilizando el programa R-Studio ® (RStudio Team, 2020).
Para comparar proporción de himenópteros controladores de plaga nativos vs exóticos y la proporción de éstos que atacaban herbívoros plaga en sistemas agrícolas chilenos se empleó Prueba-z para una proporción. La prueba de Mann-Whitney de igualdad de medianas se realizó para determinar la existencia de diferencias entre los parasitoides nativos y exóticos, debido a la ausencia de normalidad en los datos, utilizando el programa R-Studio ® (R Studio Team, 2020).
RESULTADOS
Se determinó la existencia de 192 especies de parasitoides empleados en control biológico de plagas, correspondientes a 15 familias del orden Hymenoptera (Tabla I). De las 191 especies registradas por esta investigación, una mayoría significativa (70 %) correspondió a especies exóticas (z= 5.528; N= 191, p< 0.001). Este contraste fue marcado a nivel de familias, donde el 86 % correspondió a linajes exóticos, siendo el 14 % restante nativo (Tabla I). Adicionalmente, se encontró que ha existido una introducción constante de nuevas especies exóticas como controladores biológicos que muestra una ligera alza después del año 1975, mostrando una tendencia a la acumulación creciente y progresiva de especies exóticas en los últimos 100 años (Fig. 1).
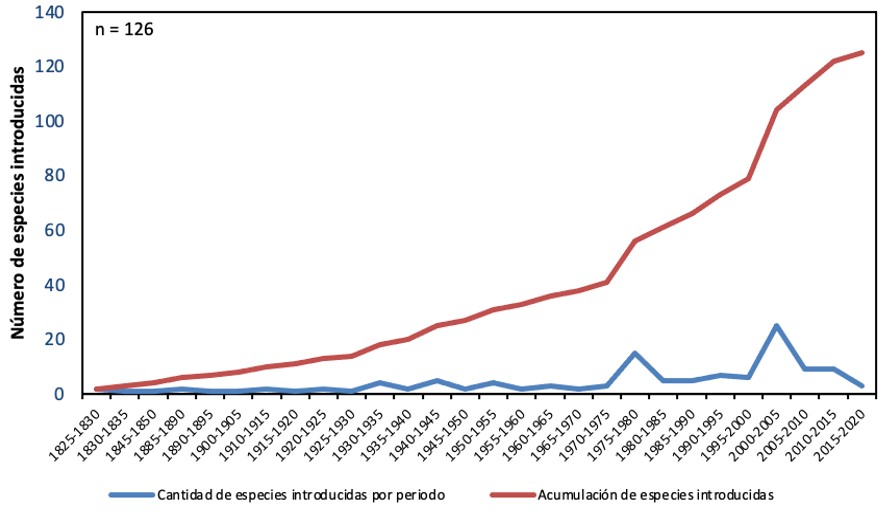
Fig. 1.
Número de especies de parasitoides introducidas a Chile desde el siglo pasado a la fecha (línea azul), considerando intervalos de cinco años y la acumulación de número de especies a través del tiempo (línea roja).
Respecto a los hospederos, se encontró que, de las 85 familias de hospederos usadas por los parasitoides, 56 % eran atacadas sólo por especies exóticas y un 44 % sólo por especies nativas (Fig. 2).
Existen familias de parasitoides que sólo estaban representadas en los registros agrícolas por especies introducidas tales como Bethylidae, Chrysididae, Diapriidae, Ibaliidae, Perilampidae y Pteromalidae, sin perjuicio que pudieran existir especies nativas correspondientes a estos linajes (Tabla I).
De las 15 familias de Hymenoptera empleadas en el campo chileno, 14 incluyen especies exóticas y nueve especies nativas (Tabla I). Al comparar a través de pruebas no paramétricas no se observaron diferencias estadísticamente significativas en el uso de hospederos por parte de las especies exóticas vs. el uso de hospederos por parte de las especies nativas (Prueba de Mann Whitney, z= 1,719, N= 71, p. 0,085). De la misma forma, tampoco se observaron diferencias significativas al comparar ambos grupos en términos del número de especies según origen, o utilizando como indicador de la biodiversidad de ambos grupos el índice de Shannon (H’) (Prueba de t de Índices de Biodiversidad, t= 1,926, gl= 92, 82, p= 0,05).
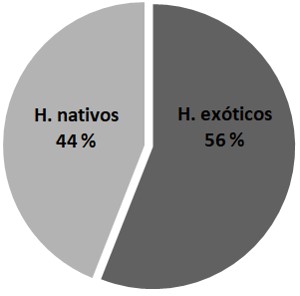
Fig. 2.
Proporción del número de familias de herbívoros plagas que son utilizadas como hospederos por parasitoides nativos y exóticos introducidos.
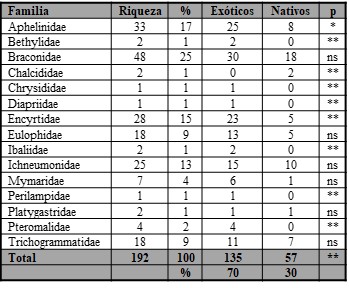
Tabla I.
Riqueza porcentual y representación en la entomofauna exótica y nativa de las especies de avispas parasitoides usadas en Chile en control biológico.
Las diferencias estadísticas menores a p= 0,05 están representadas con un asterisco, mientras que las menores a p= 0,005 con dos asteriscos. Cuando no existen diferencias entre los grupos exótico y nativo con relación a la proporción de especies de cada familia se representa con las siglas “ns” (no significativo).
DISCUSIÓN
Encontramos que, a la fecha, más de la mitad de los parasitoides que están siendo empleados para controlar insectos herbívoros considerados plaga en los sistemas agrícolas chilenos corresponden a especies exóticas introducidas. Del total de especies controladoras registradas, las exóticas corresponden al 70 % de los registros. A nivel de familias de herbívoros plagas a los cuales atacan, este porcentaje corresponde a un 56 % que es atacado por especies exóticas. A través del registro temporal la cantidad de especies exóticas ha solamente aumentado a través de los últimos 100 años, experimentándose en décadas recientes el mayor aumento de estas introducciones. Es interesante destacar que a pesar de la extensa historia de introducción de avispas parasitoides para fines de control biológico desde 1888 y hasta 1983 en Chile, solo un 55 % de las especies logró establecerse (Zúñiga, 1985). La baja eficiencia del establecimiento de las especies exóticas empleadas en Chile como controladores biológicos llama a reflexionar sobre las dimensiones de las relaciones ecológicas y el contexto de la agricultura intensiva donde está inmersa la introducción de estas especies exóticas (Rioja Soto, 2022).
Actualmente, existen propuestas metodológicas y protocolos para disminuir los potenciales impactos negativos de la introducción de especies exóticas a un nuevo ecosistema. En éstas, se evalúan aspectos ecológicos como la capacidad de establecimiento, de dispersión o el rango potencial de hospederos de la nueva especie (Howarth, 2000; van Lenteren et al., 2003). Sin embargo, las primeras introducciones a Chile no cumplían dichas normas y solo se basaban en la efectividad de control teórica del parasitoide sobre la plaga (Zúñiga, 1985). Lo anterior implica el riesgo de efecto de derrame o “spillover” y el desplazamiento de los parasitoides nativos, aunque algunos estudios (e.g., Luck & Podoler, 1985; Bennett, 1993; Murdoch et al., 1985, 1996) citados por Parry (2009), señalan que los parasitoides desplazados podrían ser, a su vez, parasitoides “previamente introducidos” y no nativos. Esta afirmación es difícil de evaluar en ausencia de estudios previos acerca de la entomofauna nativa de la zona donde se liberó la nueva especie exótica. Sin embargo, resulta cuestionable considerando que la estructuración trófica de las comunidades de insectos en los ecosistemas terrestres considera comúnmente un tercer y cuarto nivel trófico donde se sostienen parasitoides e hiperparasitoides nativos a cada hábitat (Rodríguez et al., 2019; Pedroso et al., 2021). Por lo tanto, asumir que el desplazamiento de especies por introducción de especies solo afectaría a especies exóticas previamente establecidas es poco probable y resulta especialmente delicado si se considera que el objetivo de tales liberaciones es el establecimiento del nuevo controlador, al menos en el control biológico clásico. Por otro lado, la intensidad del efecto “spillover” podría verse aumentada debido a la estructura fragmentada del paisaje y el aumento de la superficie dedicada a la agricultura, en detrimento de las áreas naturales. Esto podría provocar que especies de parasitoides se desarrollen en gran número en las áreas agrícolas, debido a la cantidad de presas disponibles y luego migren a las zonas naturales vecinas cuando las condiciones cambien, (e.g. al terminar el ciclo de un cultivo), aumentando la presión sobre los herbívoros de dichas áreas (Rand et al., 2006).
Adicionalmente, el uso de parasitoides como controladores biológicos puede representar una disminución en el uso de plaguicidas, lo que tampoco es claro de acuerdo con lo mencionado por Zúñiga-Venegas et al. (2021). Desafortunadamente, mientras que para Chile existe un registro de productos fitosanitarios que son aplicados, como es el caso de las formulaciones de pesticidas empleadas en el país (AFIPA, 2023), no existe disponible a la fecha un catálogo nacional asociado a una normativa de registro que regule la aplicación de depredadores y parasitoides como controladores biológicos de libre acceso. Particularmente grave es la situación de la aplicación de este tipo de control en zonas extremas del país donde se ha reportado falta de capacitación y apoyo para la adecuada liberación y conservación de los controladores biológicos en los agroecosistemas (Rioja Soto, 2022). En estas zonas productivas se ha informado de errores de manejo con relación a enemigos naturales enviados para controlar plagas objetivo, como uso de agentes biológicos no adaptados a las condiciones climáticas locales, y aplicación simultanea masiva de pesticidas en cultivos adyacentes a las zonas de liberación de controladores. Estas deficiencias en el manejo intensivo estarían relacionadas a la escasa diversidad presente en los monocultivos de estas localidades (Rioja Soto, 2022).
Además de problemas relacionados con dificultades de manejo, la introducción de especies exóticas y su potencial expansión podría significar la contaminación de huertos o zonas productivas manejadas bajo un sistema no intensivo industrializado, menos dependientes en “insumos externos” como pesticidas y controladores exóticos, como son la agricultura orgánica y agroecológica. Por ejemplo, estudios a escala global recientes han demostrado que la agricultura orgánica es capaz de permitir una mayor diversidad de abejas nativas en comparación con el enfoque industrializado intensivo, pudiendo esto estar ocurriendo también para otros insectos beneficiosos como controladores biológicos nativos y exóticos ya establecidos. Además, tanto bajo el enfoque de la estrategia de producción agroecológica como el del control biológico por conservación, se plantea la promoción de los servicios ecosistémicos que proveen los organismos locales como “insumos internos” para la producción agrícola, así se emplean los polinizadores nativos y controladores locales (exóticos y nativos) (Barbosa, 1998; Altieri, 2018; Henríquez-Piskulisch et al., 2021). Por lo tanto, prácticas de introducción masiva de controladores exóticos causantes de efectos de derrame podrían perjudicar estas estrategias de agricultura más sostenible, simplificando y homogenizando la comunidad de insectos presentes en los campos independientemente del tipo de manejo. En última instancia, se ha propuesto que esto pudiera generar una presión sobre los organismos plaga, usualmente también exóticos, promoviendo la evolución de resistencias hacia este controlador exótico, volviéndolo finalmente inefectivo y requiriéndose nuevamente introducir un agente más “eficiente” (Goldson et al., 2014).
Sintetizando, es posible sugerir que es necesario un reenfoque de los manejos agrícolas empleados en Chile para sacar partido a la entomofauna local (exótica establecida y nativa) que podría prestar servicios como “insumos internos” para el control biológico de plagas (Rojas, 2005), antes de seguir destinando recursos en incorporar nuevas especies exóticas para estos fines. Esto dado que, al revisar la situación histórica y actual de este manejo agrícola, la práctica actual representa un alto riesgo de spillover (Donoso; et al., 1999). Por el contrario, de continuar este enfoque cortoplacista se estará generando un daño a la sostenibilidad de la actividad agrícola y la biodiversidad chilena al desperdiciar los potenciales beneficios que la entomofauna local brinda a esta actividad humana (Tscharntke et al., 2007; Petit et al., 2020).
Para finalizar, sería importante destacar que, para proteger los recursos naturales y la biodiversidad del país, urge establecer políticas y una legislación que regule la utilización con fines comerciales de recursos naturales o conocimientos nativos sin el correspondiente beneficio para el Estado o las comunidades depositarias de ese saber. Chile es un país que ha seguido una estrategia de introducción de controladores exóticos, sin poner en valor los agentes presentes naturalmente (Gerding, 2011; Barra-Bucarei et al., 2020). Un caso que ejemplifica negativamente lo anterior y da sustento a esta propuesta, es la utilización en diversos países del mundo (Argentina, Estados Unidos y la Península Ibérica) del parasitoide de áfidos nativo Lysiphlebus testaceipes (Cresson) (Braconidae: Aphidiinae) como controlador de áfidos. La investigación de esta microavispa en Chile es muy escasa (Gerding, 1992; Starý et al., 1993: Vargas & Ubillo, 2001) y aspectos básicos tales como su ciclo biológico, distribución o estado de conservación, a nuestro mejor entender, en Chile no han sido estudiados. Esto dificulta comenzar a promover este insecto como controlador a pesar de los buenos resultados obtenidos en otros lugares del mundo de clima mediterráneo donde se ha utilizado (Satar et al., 2019). Otro punto importante en el fomento de la utilización de biocontroladores nativos es la necesidad de un marco regulatorio y una plataforma que permita la consulta de información sobre la comercialización de estos organismos (Gerding, 2011). Por lo tanto, Chile presenta un potencial en el uso de controladores biológicos de plagas nativos, pero que carece de herramientas que fomenten el uso de estos a escala país.
REFERENCES
Abrol, D., & Shankar, U. (2015) Integrated Pest Management. Breeding Oilseed Crops for Sustainable Production (ed. Gupta, S.K.), pp. 523-549. Academic Press, San Diego.
AFIPA (2023) Registro de productos fitosanitarios. AFIPA Chile. https://www.afipa.cl/registro-y-uso-de-productos-fitosanitarios/ (acceso 10 de octubre 2022).
Altieri, M.A. (2018) Agroecology: The Science of Sustainable Agriculture. Second Edition. CRC Press Taylor & Francis Group, New York, USA. https://doi.org/10.1201/9780429495465
Baldini, A.U., Cogollor, G.M., Sartori, A.R., & Aguayo, J.S. (2005) Control Biológico de Plagas Forestales de Importancia Económica en Chile. Corporación Nacional Forestal y Fundación para la Innovación Agraria, Santiago de Chile, Chile.
Barbosa, P.A. (1998) Conservation Biological Control. Academic Press, San Diego.
Barra-Bucarei, L., Moreno, L.D., & Iglesias, A.F. (2020) Biological control in Chile. Latin America and the Caribbean: Its Rich History and Bright Future (ed. van Lenteren, J.C., Bueno, V.H.P., Luna, M.G., & Colmenarez, Y.C.) pp. 108-123. CABI Invasives Series, CABI, Wallingford UK.
Bennett, F.D. (1993) Do Introduced Parasitoids Displace Native Ones? The Florida Entomologist, 76, 54-63.
BHL (Biodiversity Heritage Library) (2015) Smithsonian Libraries and Archives, USA. URL https://www.biodiversitylibrary.org/ (acceso 10 de octubre 2022).
Brown, P.M.J., Zaviezo, T., Grez, A., Adriaens, T., San Martin, G., Roy, H.E., & Soares, A.O. (2022) Invasive intraguild predators: Evidence of their effects, not assumptions. Ecological Entomology, 47, 249-252. https://doi.org/10.1111/een.13116
CAB International (2010) Centre for Agricultural Bioscience International, CAB International, Reino Unido. https://www.cabidigitallibrary.org/journal/cabicompendium (acceso 10 octubre 2022).
Carson, R. (1962) Silent Spring. The Riverside Press Cambridge, Cambridge, MA, USA.
Collier, T., & Van Steenwyk, R. (2004) A critical evaluation of augmentative biological control. Biological Control, 31, 245-256.
Davis, F.R. (2014) Banned: a history of pesticides and the science of toxicology. Yale University Press, New Haven, CT, London, UK.
Donoso, G., Cancino, J., & Magri, A. (1999) Effects of agricultural activities on water pollution with nitrates and pesticides in the Central Valley of Chile. Water Science & Technology, 39, 49-60.
FAO (2005) Directrices para la exportación, el envío, la importación y liberación de agentes de control biológico y otros organismos benéficos. Normas Internacionales para Medidas Fitosanitarias NIMF 3, Roma.
Fortuna, T.M., Le Gall, P., Mezdour, S., & Calatayud, P.A. (2022) Impact of invasive insects on native insect communities. Current opinion in insect science, 51, 100904. https://doi.org/10.1016/j.cois.2022.100904
Funasaki, G.Y., Po-Yunf, L., Nakahara, L.M., Beardsley, J.W., & Ota, A.K. (1988) A Review of Biological Control Introductions in Hawaii: 1890 to 1985. Proceedings, Hawaiian Entomological Society, 28, 105-160.
Garibaldi, L.A., Gemmill-Herren, B., D’Annolfo, R., Graeub, B.E., Cunningham, S.A., & Breeze, T.D. (2017) Farming Approaches for Greater Biodiversity, Livelihoods, and Food Security. Trends in Ecology and Evolution, 32, 68-80. https://doi.org/10.1016/j.tree.2016.10.001
GBIF (2022) Global Biodiversity Information Facility. Copenhagen Ø Denmark. https://www.gbif.org/ (acceso 10 de octubre 2022).
Gerding, M. (1992) Control biológico de áfidos en cereales. Serie Quilamapu. https://hdl.handle.net/20.500.14001/39092 (acceso 6 noviembre 2023).
Gerding, M. (2011) Desafíos en la implementación y comercialización de controladores biológicos en Chile. En: 12 (SINCOBIOL) Simposio de Controle Biológico: Mudanças climáticas e sustentabilidade: quebra de paradigmas. Sao Paulo, Brasil.
Goldson, S., Tomasetto, F., & Popay, A. (2014) Biological control against invasive species in simplified ecosystems: its triumphs and emerging threats. Current Opinion in Insect Science, 5, 50-56. https://doi.org/10.1016/j.cois.2014.09.003
González, S. (1998) Uso racional de pesticidas en Chile. Estado actual y perspectivas futuras. Racionalización Del Uso de Pesticidas en El Cono Sur (ed. Stachetti, G.), pp. 51-58. PROCISUR-IICA, Montevideo, Uruguay.
Google Scholar (2023) https://scholar.google.ca/scholar?hl=en&inst=8192625893198780794 (acceso 5 mayo de 2023).
Grass, I., Loos, J., Baensch, S., Batáry, P., Librán-Embid, F., Ficiciyan, A., Klaus, F., Riechers, M., Rosa-Schleich, J., Tiede, J., Udy, K., Westphal, C., Wurz, A., & Tscharntke, T. (2019) Land-Sharing/-Sparing Connectivity Landscapes for Ecosystem Services and Biodiversity Conservation. People and Nature, 1(2),262-72. https://doi.org/10.1002/pan3.21
Grube, A., Donaldson, D., Kiely, T., & Wu, L. (2011) Pesticides Industry Sales and Usage: 2006 and 2007 Market Estimates. U.S. Environmental Protection Agency, 1-41. https://www.epa.gov/sites/production/files/2015-10/documents/market_estimates2007.pdf (acceso 10 mayo 2022).
Hammer, Ø., Harper, D.A.T., & Ryan, P.D. (2001) PAST (4.0). Windows. Oslo, University of Oslo.
He, D., He, M., Amalin, D.M., Liu, W., Alvindia, D.G., & Zhan, J. (2021) Biological Control of Plant Diseases: An Evolutionary and Eco-Economic Consideration. Pathogens, 10, 1-15.
Henríquez‐Piskulich, P.A., Schapheer, C., Vereecken, N.J., & Villagra, C. (2021) Agroecological strategies to safeguard insect pollinators in biodiversity hotspots: Chile as a case study. Sustainability (Switzerland), 13(12), 6728. https://doi.org/10.3390/su13126728
Howarth, F.G. (1995) Environmental Impacts of Classical Biological Control. Annual Review of Entomology, 36, 485-509.
Howarth, F.G. (2000) Non-target Effects of Biological Control Agents. Biological Control: Measures of Success. (ed. Gurr, G., & Wratten, S.), pp. 369-403. Springer, Netherlands, Dordrecht.
ISI Web of Science® Clarivate (2023) Web of Science Core Collection. Clarivate, London, UK. https://www-webofscience-com.uchile.idm.oclc.org/wos/woscc/basic-search (acceso 10 de octubre 2022).
Karp, D.S., Rominger, A.J., Zook, J., Ranganathan, J., Ehrlich, P.R., & Daily, G.C. (2012) Intensive agriculture erodes β-diversity at large scales. Ecology Letters, 15, 963-970. https://doi.org/10.1111/j.1461-0248.2012.01815.x
Kenis, M., Auger-Rozenberg, M.A., Roques, A., Timms, L., Péré, C., Cock, M.J.W., Settele, J., Augustin, S., & Lopez-Vaamonde, C. (2009) Ecological effects of invasive alien insects. Biological Invasions, 11, 21-45. https://doi.org/10.1007/s10530-008-9318-y
Kogan, M. (1998) Integrated pest management: Historical perspectives and contemporary developments. Annual Review of Entomology, 43, 243-270. https://doi.org/10.1146/annurev.ento.43.1.243
Kruitwagen, A., Beukeboom, L.W., & Wertheim, B. (2018) Optimization of native biocontrol agents, with parasitoids of the invasive pest Drosophila suzukii as an example. Evolutionary Application, 11, 1473-1497.
Lavandero, B., & Domínguez, M. (2010) Isolation and characterization of nine microsatellite loci from Aphelinusmali (Hymenoptera: Aphelinidae), a parasitoid of Eriosomalanigerum (Hemiptera: Aphididae). Insect Science, 17, 549-552.
Luck., R.F., & Podoler, H. (1985) Competitive Exclusion of Aphytis lingnanensis by .. melinus: Potential Role of Host Size. Ecology, 66(3), 904-13. https://doi.org/10.2307/1940553
Mace, G.M., Reyers, B., Alkemade, R., Biggs, R., Chapin, F.S., Cornell, S.E., Díaz, S., Jennings, S., Leadley, P., Mumby, P.J., Purvis, A., Scholes, R.J., Seddon, A.W.R., Solan, M., Steffen, W., & Woodward, G. (2014) Approaches to defining a planetary boundary for biodiversity. Global Environmental Change, 28, 289-297. https://doi.org/10.1016/j.gloenvcha.2014.07.009
McKay, B.M. (2017) Agrarian Extractivism in Bolivia. World Development, 97, 199-211. https://doi.org/10.1016/j.worlddev.2017.04.007
MacQuarrie, C.J.K., Lyons, D.B., Lukas Seehausen, M., & Smith, S.M. (2016) A history of biological control in Canadian forests, 1882-2014. Canadian Entomologist, 148, S239-S269. https://doi.org/10.4039/tce.2015.66
Moreno, C.E. (2001). Métodos para medir la biodiversidad. M&T– Manuales y Tesis SEA. CYTED, ORCYT, UNESCO & SEA, Zaragoza, España.
Murdoch, W.W., Briggs, C.J., & Nisbet, R.M. (1996) Competitive Displacement and Biological Control in Parasitoids: A Model. The American Naturalist, 148(5), 807-26. https://doi.org/10.1086/285957
Murdoch, W.W., Chesson, J., & Chesson, P.L. (1985) Biological Control in Theory and Practice. American Naturalist, 125, 344-366.
Panez, A., Roose, I., & Faúndez, R. (2020) Agribusiness facing its limits: The re-design of neoliberalization strategies in the exporting agriculture sector in Chile. Land, 9(3), 66. https://doi.org/10.3390/land9030066
Parry, D. (2009) Beyond Pandora’s Box: Quantitatively Evaluating Non-Target Effects of Parasitoids in Classical Biological Control. Biological Invasions, 11(1), 47-58. https://doi.org/10.1007/s10530-008-9319-x
Pedroso, B.M., Morales-Silva, T., & Faria, L.D.B. (2021) Dominant parasitoid species diminishes food web structural complexity and function. Journal of Insect Conservation, 25, 671-682. https://doi.org/10.1007/s10841-021-00336-5
Petit, S., Muneret, L., Carbonne, B., Hannachi, M., Ricci, B., Rusch, A., & Lavigne, C. (2020) Landscape-scale expansion of agroecology to enhance natural pest control: A systematic review. Advances in Ecological Research, 63, 1-48. https://doi.org/10.1016/bs.aecr.2020.09.001
Picó, Y., Alvarez-Ruiz, R., Alfarhan, A.H., El-Sheikh, M.A., Alshahrani, H.O., & Barceló, D. (2020) Pharmaceuticals, pesticides, personal care products and microplastics contamination assessment of Al-Hassa irrigation network (Saudi Arabia) and its shallow lakes. Science of the Total Environment, 701, 135021. https://doi.org/10.1016/j.scitotenv.2019.135021
Radrigan, C., Beers, E., Alvear, A., & Fuentes-Contreras, E. (2021) Acute toxicity of lethal and sublethal concentrations of neonicotinoid, insect growth regulator and diamide insecticides on natural enemies of the woolly apple aphid and the obscure mealybug. Chilean Journal of Agricultural Research, 81, 398-407.
Rand, T.A., Tylianakis, J.M., & Tscharntke, T. (2006) Spillover edge effects: The dispersal of agriculturally subsidized insect natural enemies into adjacent natural habitats. Ecology Letters, 9, 603-614. https://doi.org/10.1111/j.1461-0248.2006.00911.x
ResearchGate (2023) https://www.researchgate.net/ (acceso 5 de mayo 2023).
Rioja Soto, T.C. (2022) Control Biológico En Agroecosistemas de Zonas Áridas de Chile. Idesia (Arica), 40(3), 3-6. https://doi.org/10.4067/S0718-34292022000300003
Rodríguez, A., Pohjoismäki, J.L.O., & Kouki, J. (2019) Diversity of forest management promotes parasitoid functional diversity in boreal forests. Biological Conservation, 238, 108205. https://doi.org/10.1016/j.biocon.2019.108205
Rojas, S. (2005) Control biológico de plagas en Chile: historia y avance. Instituto de Investigaciones Agropecuarias (Chile). Ministerio de Agricultura, La Cruz, Chile.
RStudio Team (2020) RStudio: Integrated Development for R. RStudio, PBC, Boston, MA. http://www.rstudio.com/ (acceso 10 de octubre 2022).
Satar, G., Karacaoğlu, M., Uygun, N., & Satar, S. (2019) Some Demographic Parameters of Lysiphlebus confusus, L. fabarum, and .. testaceipes (Hymenoptera: Braconidae: Aphidiinae). Journal of Economic Entomology, 112(3), 1105-1111. https://doi.org/10.1093/jee/toz041
SAG (2010) Declaración de ventas de plaguicidas de uso agrícola año 2010. https://www.sag.cl/content/declaracion-de-venta-de-plaguicidas-de-uso-agricola-ano-2010 (acceso 10 de octubre 2022).
SAG (2019) Declaración de ventas de plaguicidas de uso agrícola año. https://www.sag.gob.cl/content/declaracion-de-ventas-de-plaguicidas-de-uso-agricola-2019 (acceso 10 de octubre 2022).
Seymour, C., & Veldtman, R. (2010) Ecological role of control agent, and not just host-specificity, determine risks of biological control. Austral Ecology, 35, 704-711. https://doi.org/10.1111/j.1442-9993.2009.02077.x
Sharma, A., Kumar, V., Shahzad, B., Tanveer, M., Sidhu, G.P.S., Handa, N., Kohli, S.K., Yadav, P., Bali, A.S., Parihar, R.D., Dar, O.I., Singh, K., Jasrotia, S., Bakshi, P., Ramakrishnan, M., Kumar, S., Bhardwaj, R., & Thukral, A.K. (2019) Worldwide pesticide usage and its impacts on ecosystem. SN Applied Sciences, ., 1-16. https://doi.org/10.1007/s42452-019-1485-1
Silva, V., Mol, H.G.J., Zomer, P., Tienstra, M., Ritsema, C.J., & Geissen, V. (2019) Pesticide residues in European agricultural soils - A hidden reality unfolded. Science of the Total Environment, 653, 1532-1545. https://doi.org/10.1016/j.scitotenv.2018.10.441
Simberloff, D., & Stiling, P. (1996) How Risky is Biological Control? Ecology, 77, 1965-1974.
Sociedad de Entomología de Chile (2019) Revista de la Sociedad Chilena de Entomologia. http://www.insectachile.cl/revista/ (acceso 10 de octubre 2022).
Starý, P., Gerding, I.M., Norambuena, I.H., & Remaudière, G. (1993) Environmental research on aphid parasitoid biocontrol agents in Chile (Hym., Aphidiidae; Hom., Aphidoidea). Journal of Applied Entomology, 115(1‐5), 292-306.
Tscharntke, T., Bommarco, R., Clough, Y., Crist, T.O., Kleijn, D., Rand, T.A., Tylianakis, J.M., Nouhuys, S. van, & Vidal, S. (2007) Conservation biological control and enemy diversity on a landscape scale. Biological Control, 43, 294-309. https://doi.org/10.1016/j.biocontrol.2007.08.006
Tscharntke, T., Clough, Y., Wanger, T.C., Jackson, L., Motzke, I., Perfecto, I., Vandermeer, J., & Whitbread, A. (2012) Global Food Security, Biodiversity Conservation and the Future of Agricultural Intensification. Biological Conservation, 151(1), 53-59. https://doi.org/10.1016/j.biocon.2012.01.068.
Vale, J.A. (2008) Poisoning due to neonicotinoid insecticides. Clinical Toxicology, 46, 404-405.
van Lenteren, J., Babendreier, D., Bigler, F., Burgio, G., Hokkanen, H., Kuske, S., Loomans, A.J.M., Menzler-Hokkanen, I., van Rijn, P.C.J., Thomas, M.B., Tommasini, M.G., & Zeng, Q.-Q. (2003) Environmental risk assessment of exotic natural enemies used in inundative biological control. BioControl, 48, 3-38.
van Lenteren, J.C., Bale, J., Bigler, F., Hokkanen, H.M.T., & Loomans, A.J.M. (2006) Assessing risks of releasing exotic biological control agents of arthropod pests. Annual Review of Entomology, 51, 609-634. https://doi.org/10.1146/annurev.ento.51.110104.151129
Vanbergen, A.J., Aizen, M.A., Cordeau, S., Garibaldi, L.A., Garratt, M.P.D., Kovács-Hostyánszki, A., Lecuyer, L., Ngo, H.T., Potts, S.G., Settele, J., Skrimizea, E., & Young, J.C. (2020) Transformation of agricultural landscapes in the Anthropocene: Nature’s contributions to people, agriculture and food security. Advances in Ecological Research, The Future of Agricultural Landscapes, Part I. (ed. Bohan, D.A., & Vanbergen, A.J.), pp. 193-253. Academic Press. https://doi.org/10.1016/bs.aecr.2020.08.002
Vargas, R., & Ubillo, A. (2001). Toxicidad de pesticidas sobre enemigos naturales de plagas agrícolas. Agricultura Técnica, 61(1), 35-41.
Williams, T., & Polaszek, A. (1996) A re-examination of host relations in the Aphelinidae (Hymenoptera: Chalcidoidea). Biological Journal of the Linnean Society, 57, 35-45.
Zúñiga, E. (1985) Ochenta años de control biológico en Chile. Agricultura Técnica, 43, 175-183.
Zúñiga-Venegas, L., Saracini, C., Pancetti, F., Muñoz-Quezada, M.T., Lucero, B., Foerster, C., & Cortés, S. (2021) Pesticide exposure in Chile and population health: urgency for decision making. Gaceta Sanitaria, 35, 480-487. https://doi.org/10.1016/j.gaceta.2020.04.020
Notas de autor
cristian.villagra@umce.cl