Artículos
Márgenes de ruta como reservorios de biodiversidad: el rol ecosistémico de los insectos
Roadside margins as biodiversity reservoirs: the ecosystem role of insects
Márgenes de ruta como reservorios de biodiversidad: el rol ecosistémico de los insectos
Revista de la Sociedad Entomológica Argentina, vol. 83, núm. 1, 2024
Sociedad Entomológica Argentina
Recepción: 08 Junio 2023
Aprobación: 07 Marzo 2024
Resumen: Los márgenes de las rutas que contienen vegetación natural brindan condiciones biológicas estables y promueven la biodiversidad. Estas áreas son importantes para mejorar los servicios ecosistémicos en los paisajes agrícolas. Los objetivos de este estudio fueron i) evaluar la diversidad de insectos como visitantes florales (excluyendo apiformes), y la riqueza de especies de plantas en los márgenes de las rutas, ii) determinar los Grupos Funcionales de insectos registrados como visitantes florales en los márgenes de rutas, y iii) analizar el rol ecológico de los insectos presentes en ocho márgenes de rutas ubicados en la región centro-este de la provincia de Santa Fe, Argentina. El estudio se realizó a lo largo de cuatro rutas provinciales (N°. 6, 10, 62 y 64) y la ruta nacional N°. 19; de noviembre de 2013 a septiembre de 2015. Se registraron un total de 1614 insectos, Oxysarcodexia varia (Walker) (Diptera: Sarcophagidae), Allograpta exotica (Wiedemann) (Diptera: Syrphidae) y Harmonia axyridis (Pallas) (Coleoptera: Coccinellidae), fueron las especies más abundantes. Las familias Brassicaceae, Apiaceae y Asteraceae recibieron el mayor número de visitas de insectos. Se registraron un total de 225 interacciones planta-insecto. Se discute la importancia de los márgenes de ruta con vegetación natural para proporcionar alimento y refugio a insectos polinizadores, depredadores, parasitoides, herbívoros y descomponedores.
Palabras clave: Diversidad, Grupos funcionales, Interacciones tróficas, Visitantes florales.
Abstract: The roadside margins that contain natural vegetation provides biological stable conditions and promote biodiversity. These areas are important to enhance ecosystem services in agricultural landscapes. The aims of this study were i) to assess the diversity of insects as floral visitors (excluding apiformes), and plant species richness in roadside margins, ii) to determine the Functional Groups of insects recorded as floral visitors of roadside margins, and iii) to analyze the ecological role of insects presents in eight roadside margins located in the central-eastern region of the Santa Fe province. The study was conducted along four provincial roads (No. 6, 10, 62, and 64) and the national road No. 19, on November 2013 to September 2015. A total of 1614 insects were recorded. Oxysarcodexia varia (Walker) (Diptera: Sarcophagidae), Allograpta exotica (Wiedemann) (Diptera: Syrphidae) and Harmonia axyridis (Pallas) (Coleoptera: Coccinellidae), were the most abundant species. The families Brassicaceae, Apiaceae, and Asteraceae received the highest number of insect visits. A total of 225 plant-insect interactions were recorded. The importance of roadside margin with natural vegetation to provide food and shelters for pollinators, predators, parasitoids, herbivores, and decomposers insects is discussed.
Keywords: Diversity, Functional groups, Floral visitors, Trophic interactions.
INTRODUCCIÓN
La intensificación agrícola impulsó transformaciones significativas en los paisajes, caracterizadas por la reducción o eliminación de hábitats naturales y seminaturales (Hendrickx et al., 2007; Tilman et al., 2011; Ganser et al., 2019). Este proceso de cambio en el paisaje conlleva a una creciente homogeneización, fragmentación, y significativa pérdida de biodiversidad (Tscharntke et al., 2005, Haddad et al., 2015, Fardila et al., 2017). De manera especial, la disminución en la cantidad de especies de insectos es motivo de preocupación, ya que estos desempeñan un rol crucial en el mantenimiento de servicios ecosistémicos en los ambientes (Wagner, 2020). Los insectos, al ser el grupo más diverso y abundante dentro del reino animal, realizan servicios ecosistémicos, que incluyen la descomposición, la polinización y el control biológico, entre otros. Estos servicios ecosistémicos son fenómenos estrictamente ecológicos, vinculados a la estructura, los procesos y las funciones de los ecosistemas, independientemente de su valor o beneficio para los humanos (Altieri & Nicholls, 2004; Spangenberg et al., 2014; Landis, 2017). Para evaluar la calidad de estos servicios ecosistémicos en los ambientes, es esencial contar con conocimiento sobre la diversidad de insectos (Losey & Vaughan, 2006; Öckinger & Smith, 2007; Schowalter, 2013; Molina et al., 2014, 2016; Garibaldi et al., 2020). Las especies que cumplen un mismo rol dentro de las funciones de un ecosistema, o que utilizan un recurso de manera similar, son consideradas como parte de un grupo funcional (Torretta & Poggio, 2013). La gran diversidad entomológica y de grupos funcionales, se ve reflejada en los visitantes florales que no son exclusivamente polinizadores. Estos insectos buscan en las flores alimento, refugio, camuflaje o un lugar esporádico de descanso (Valladares et al., 2019). Estas relaciones interespecíficas se registran tanto en flores silvestres como en especies cultivadas (Corbet, 2006).
Las prácticas agrícolas relacionadas con la lechería y ganadería pueden ser compatibles con el mantenimiento de la biodiversidad y beneficiosas para diferentes poblaciones de insectos. Esto se debe a que las pasturas para alimentar ganado, en general, son de ciclo largo (como por ejemplo la alfalfa) y emplean menor número de agroquímicos que otras actividades de producción agrícola (Hallmann et al., 2017, Wang et al., 2019). En las últimas décadas la frontera agrícola, en el centro de la provincia de Santa Fe, se ha expandido y en consecuencia el 54 % de los establecimientos dedicados a la ganadería de carne y el 48 % de los dedicados al tambo abandonaron la actividad (Plá, 2022; Sandoval et al., 2023). En este contexto, los remanentes naturales o semi naturales que se encuentran en los márgenes de rutas aportan heterogeneidad al ambiente, proporcionando alimento y refugio a insectos (Armsworth et al., 2007; Sáez et al., 2014; Phillips et al., 2020). Estos espacios presentan condiciones más estables y promueven una mayor diversidad y complejidad en la estructura de la comunidad vegetal, amortiguando las perturbaciones en los agroecosistemas (Poggio et al., 2010, 2013; Park et al., 2015; Molina et al., 2016). Estas áreas son importantes para conservar la diversidad de especies, de grupos funcionales y de interacciones interespecíficas que proporcionan servicios ecosistémicos a los cultivos aledaños (Marshall & Moonen, 2002; Tscharntke et al., 2008; Medan et al., 2011; Diehl et al., 2013; Holzschuh et al., 2016, Molina et al., 2014, 2016; Lindgren et al., 2018). Se ha reportado que mientras más diverso sea el agroecosistema las interacciones tróficas aumentan, desarrollándose sinergismos que promueven la estabilidad poblacional de los insectos (Southwood & Way, 1970; Larson et al., 2006; Garibaldi et al., 2011). Por lo tanto, la simplificación del paisaje afecta indirectamente a los servicios de los ecosistemas y sus interacciones al reducir la riqueza de los organismos proveedores de los mismos (Dainese et al., 2019). Los objetivos del presente trabajo son i) conocer la diversidad de especies de Visitantes Florales (VF) y la riqueza de especies vegetales en los márgenes de rutas; ii) determinar los Grupos Funcionales (GF) de insectos presentes en estos ambientes; iii) analizar el rol ecológico de las especies de visitantes florales presentes sobre márgenes de ruta en el centro-este de la provincia de Santa Fe (Argentina).
MATERIALES Y MÉTODOS
Sitio de estudio
El estudio se llevó a cabo en la región central de la Provincia de Santa Fe, precisamente en los Departamentos Castellanos, Las Colonias y La Capital. Estos departamentos están situados en zonas de alta producción, tanto agrícola como lechera, debido a las condiciones climáticas favorables y suelos fértiles (Torres, 2021). En ellos, según el último Censo Agropecuario, el total de superficie implantada fueron 632.050,06 ha, de las cuales el 66,5 % correspondió a cultivos anuales, 30,4 % a forrajeras (anuales y perennes), el 3,1 % restante correspondió a bosques y montes implantados (Instituto Nacional de Estadísticas y Censos de la República Argentina (INDEC), 2021).
Los muestreos se desarrollaron sobre los márgenes de las Rutas Provinciales (N.º 6, 10, 62 y 64) y la Ruta Nacional N.°19, entre noviembre de 2013 y septiembre de 2015, sumando un total de 10 muestreos por sitio. La frecuencia de muestreo fue bimestral, a excepción de los meses de invierno en los que se realizó un muestreo trimestral.
Para la elección de los sitios de muestreo se realizó una campaña exploratoria previa, en la cual se tuvo en cuenta si el margen conservaba vegetación de crecimiento espontáneo, descartando aquellos que presentaban algún tipo de manejo (desmalezado o cultivado). Durante el periodo de muestreo, en los lotes aledaños a los sitios de colecta los cultivos presentes eran de maíz, soja, arveja, girasol, entro los que se encontraron pasturas como alfalfa y avena, coincidentes con la época de siembra de cada especie. Solo se muestrearon los márgenes con vegetación espontánea sin tener en cuenta el cultivo contiguo.
Se determinaron ocho sitios de muestreo (Fig. 1):
● Sitio A: -31,88505, -61,46472 (Ruta Prov. N.º 64)
● Sitio B: -31,832, -61,29503 (Ruta Prov. N.º 10)
● Sitio C: -31,29375, -61,22352 (Ruta Prov. N.º 10)
● Sitio D: -31,54608, -60,92619 (Ruta Prov. N.º 6)
● Sitio E: -31,00683, -61,32333 (Ruta Prov. N.º 62)
● Sitio F: -31,86797, -61,56833 (Ruta Prov. N.º 64)
● Sitio G: -31,29377, -60,85741 (Ruta Prov. N.º 6)
● Sitio H: -31,63886, -60,96102 (Ruta Nac. N.º 19)

Fig. 1.
Sitios de muestreo. a. Sitios de muestreo en Rutas Provinciales: N.º 64 (sitios “a” y “f”); 10 (sitios “b” y “c”); 6 (sitios “d” y “g”); 62 (sitio “e”); y Nacional N° 19 (sitio “h”), en los tramos de la región central de Santa Fe. b-d. ejemplos de márgenes de ruta en el centro oeste de la provincia de Santa Fe
Muestreo de insectos y plantas
Para conocer la riqueza y registrar las visitas de los visitantes florales se utilizó la metodología propuesta por Chacoff et al. (2012). En cada sitio se recorrió una transecta de 200 m trazada al azar. En cada parche floral atravesado por la transecta se registraron durante cinco minutos las especies de insectos presentes sobre las flores y la identidad taxonómica de dicha planta visitada. Las colectas fueron realizadas entre las 8:00 a.m. y 15:00 p.m. rotando el recorrido de manera de abarcar todos los horarios en cada sitio. Las observaciones se realizaron bajo condiciones climáticas óptimas para la actividad de los insectos (temperatura superior a 15 ºC, viento moderado y días soleados). Se recolectaron tanto los visitantes florales, como las plantas que no pudieron ser identificados a campo, para su posterior determinación en laboratorio mediante el uso de claves dicotómicas, comparación con colecciones de referencia (colección de la Cátedra de Entomología de la Facultad de Humanidades y Ciencias (FHUC-UNL), Museo Provincial de Ciencias Naturales Florentino Ameghino (MFA) y Museo Argentino de Ciencias Naturales Bernardino Rivadavia (MACN) y consulta con especialistas (ver agradecimientos). En aquellos casos en los que no se pudo determinar los ejemplares a nivel de especie, los mismos fueron clasificados como morfoespecies. Los especímenes fueron depositados en las colecciones de FHUC-UNL, MFA y MACN.
Analisis de datos
Diversidad de especies de visitantes florales: Para estimar la diversidad de especies, se analizaron los datos con los números efectivos de especies de la comunidad (Hill, 1973), para esto se aplicó q= 1 (Diversidad de Shannon y Riqueza de especies, Colwell et al., 2012; Chao et al., 2014). Este análisis es una modificación de los índices comúnmente utilizados que permite, por un lado, comparar directamente la magnitud de la diferencia en la diversidad de dos o más comunidades, lo cual no es posible con índices tradicionales de diversidad (Jost & González-Oreja, 2012), por otro lado, aporta mayor robustez matemática (Moreno et al., 2011). Con q= 1, todas las especies son incluidas con un peso exactamente proporcional a su abundancia (Hill, 1973; Moreno et al., 2011; Jost & González-Oreja, 2012). Para evaluar diferencias estadísticamente significativas (p < 0,5) entre sitios seguimos el procedimiento sugerido por Chao et al. (2014) y comparamos las curvas de rarefacción y extrapolación de diversidad de especies y los intervalos de confianza (95 %). Se utilizó el paquete iNEXT 2.0.20 (Hsieh et al., 2016) del software RStudio (RStudio Team, 2022) para el cálculo de q= 1 y los gráficos.
Determinación de los Grupos Funcionales: Para evaluar el rol ecológico que cumplen los visitantes florales colectados en estos ambientes, los mismos fueron clasificados en cinco grupos funcionales (modificado de Torretta & Poggio, 2013): polinizadores (especies que visitan flores para alimentarse de polen y néctar); depredadores (especies que capturan otros artrópodos para alimentarse o alimentar a sus larvas); parasitoides (especies que desarrollan su ciclo larvario en insectos vivos y que matan a su huésped al eclosionar); herbívoros (especies que se alimentan de tejidos de plantas vivas); y descomponedores (especies cuyo ciclo larvario se desarrolla en materia orgánica de origen animal o vegetal en descomposición).
Para la clasificación de las especies dentro de estas cinco categorías se consideró el principal componente de la dieta a lo largo del ciclo de vida completo del individuo (desde 1er estadio larval hasta adulto). Esto fue inferido de la bibliografía (Morrone & Coscarón, 1998; Cordo et al., 2004; Johnson & Triplehorn, 2004; Claps et al., 2008; Roig-Juñet et al., 2014), partiendo de ejemplares adultos (no se colectaron ni registraron inmaduros). En el caso de las morfoespecies, estas fueron clasificadas según la información bibliográfica disponible para el taxa superior en el que fueron identificadas. En el presente estudio se excluyeron todos los registros de abejas (Apoidea, Anthophila), ya que las especies de este grupo de insectos especializados realizan más visitas que el resto de los VF (Aguado Martín et al., 2015), eclipsando las abundancias de las demás especies en una comunidad.
Redes de interacción: Para construir la red cuantitativa de interacciones planta-visitante floral se confeccionó una matriz bi-dimensional en la cual las filas representan especies de plantas, las columnas especies visitantes florales y los valores de las celdas indican la suma de los registros obtenidos de los censos durante todo el periodo de muestreo. Para obtener la red se utilizó el paquete bipartite (Dormann, 2020) del software RStudio.
RESULTADOS
Diversidad de insectos y riqueza floral
Se registraron un total 1614 individuos representando 44 especies/morfoespecies, (Mat. sup. Anexo I), de 29 familias y 5 órdenes de insectos. El número de registros de insectos visitantes florales observados en cada sitio osciló entre 111 y 292 (Tabla I). Tomando en cuenta la totalidad de los registros, el 63 % de la abundancia total de los insectos estuvo representada por el orden Diptera; 31 % Coleoptera; 3 % Hymenoptera; 2 % Lepidoptera y 1 % Hemiptera. En cuanto a la diversidad de especies (q= 1) por sitio, se pueden observar dos grupos que difieren significativamente entre sí, por un lado, los sitios “f” y “d” y por otro, el resto de sitios muestreados (“a”, “b”, “c”, “e”, “g” y “h”; Fig. 2). El sitio de muestreo “d” es el único sitio donde la curva de rarefacción tiene una tendencia hacia la asíntota y no llega a la misma, el resto de los sitios alcanzaron la asíntota (Fig. 2). El sitio de muestreo “g” presentó el mayor registro de insectos (292 registros de visita) y el sitio “d” tiene el mayor valor de diversidad q=1 (13,42) (Tabla I).

Fig. 2.
Curva de números efectivos de especies (q1) para cada sitio de muestreo sobre márgenes de ruta en el centro-este de la provincia de Santa Fe (Argentina). La curva q= 1 representa el exponencial de índice de Shannon. La superficie sombreada representa el intervalo de confianza (95 %) para cada punto de la curva.
La riqueza de especies dentro de cada familia de insectos varió entre 1 y 5, el 37 % de las familias presentaron más de una especie (Mat. sup. Anexo I). La familia con mayor riqueza de especies fue Syrphidae del orden Diptera (5 especies/morfoespecies), seguida por Chrysomelidae y Coccinellidae, ambas del orden Coleoptera, con 4 y 3 especies respectivamente.
Entre las especies registradas, Oxysarcodexia varia Walker (Sarcophagidae: Diptera) presentó el mayor número de individuos (350 registros), seguida por Allograpta exotica Wiedemann (Syrphidae: Diptera) con 298 registros de individuos y Harmonia axyridis Pallas (Coccinellidae: Coleoptera) con 252 registros.
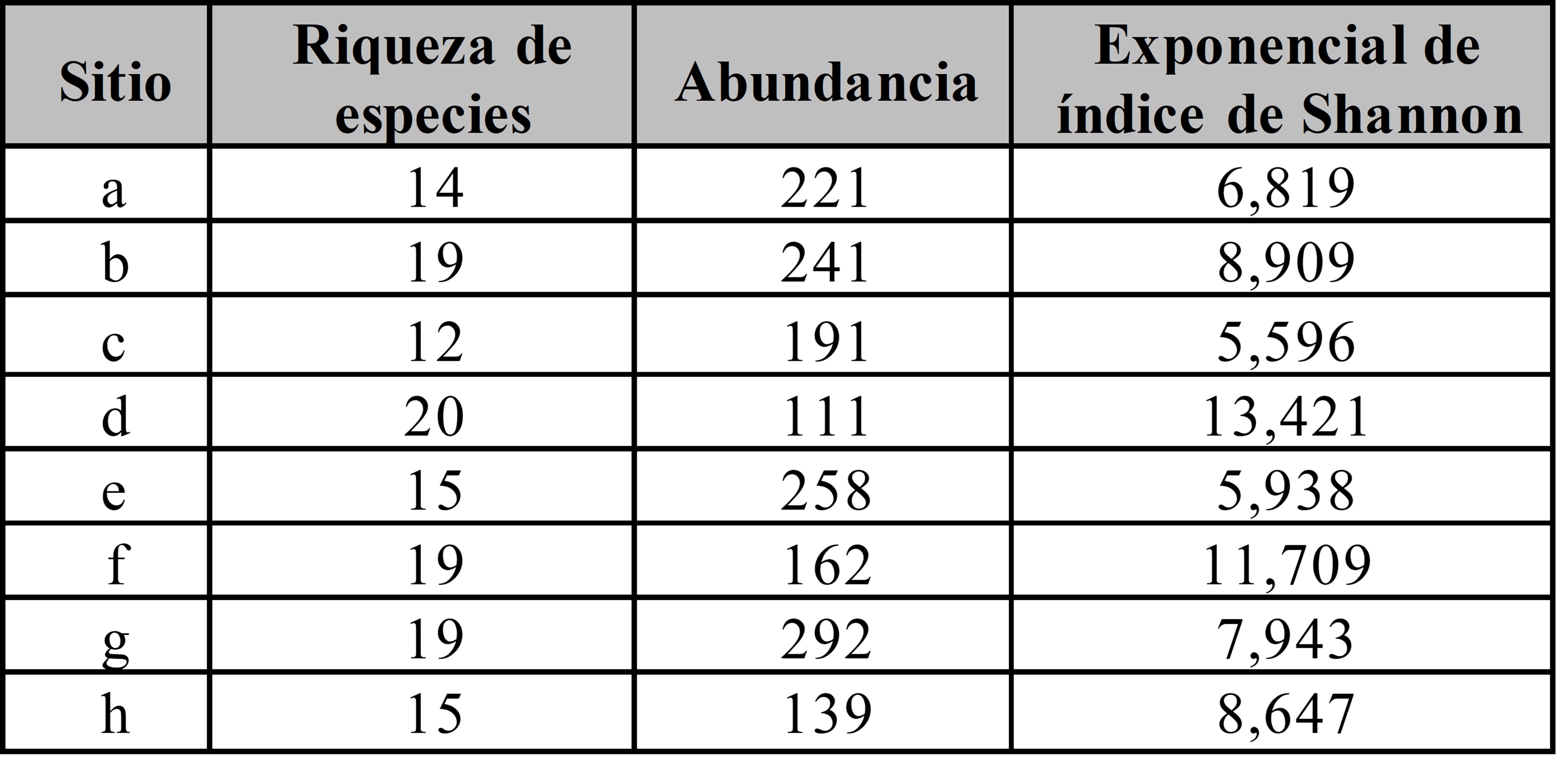
Tabla I.
Riqueza, abundancia y estimación de diversidad asintótica (q= 1) de visitantes florales para cada sitio de muestreo sobre márgenes de ruta en el centro-este de la provincia de Santa Fe (Argentina).
En cuanto a la vegetación de los márgenes de ruta, se registraron un total de 48 especies/ morfoespecies de plantas asociadas a los insectos registrados, pertenecientes a 18 familias vegetales. Para el 55,6 % de las familias vegetales, sólo se registró una especie, mientras que el 44,4 % restante presentó más de 2 especies de plantas. La familia con mayor riqueza de especies fue Asteraceae (16 especies), seguida por Apiaceae y Fabaceae ambas con 5 especies (Mat. sup. Anexo II).
Grupos funcionales
Los insectos registrados fueron clasificados en 5 grupos funcionales (GF): polinizadores, descomponedores, herbívoros, depredadores y parasitoides (Fig. 3).

Fig. 3.
Número de visitas de insectos visitantes florales agrupados por Grupos Funcionales, considerando todos los sitios de muestreos sobre márgenes de ruta en el centro-este de la provincia de Santa Fe (Argentina).
En primer lugar, los extractos de DCM, AcOEt y MeOH extraídos de estragón, mostraron una fuerte actividad antialimentaria, todos con valores de (IA) medianos del 100 %, y significativamente diferentes respecto al control (test de Conover-Inman, p< 0,05). En segundo lugar, el extracto de MeOH de lavanda, tuvo una fuerte actividad antialimentaria (valor IA mediano= 100 %) y significativamente diferente del control (test de Conover–Inman, p< 0,05). Por último, el extracto de AcOEt de copete y tomillo, tuvieron una fuerte actividad antialimentaria, ambos con valores de (IA) medianos del 100 % y significativamente diferentes del control (test de Conover-Inman, p< 0,05).
Los polinizadores fueron el grupo con mayor registro de visitas a lo largo de los márgenes de ruta, correspondiendo al 35 % del total de los individuos registrados. De las 5 especies/morfoespecies de polinizadores registradas todas pertenecieron a la familia Syrphidae, del orden Diptera. Allograpta exótica Wiedemann registró 298 visitas florales, siendo la especie de la familia Syrphidae con mayor número de registros. Los descomponedores representaron el 27,1 % de los insectos registrados, siendo Diptera el único orden registrado para este GF y O. varia la especie más abundante (80,1 % de los registros). El GF herbívoros representó el 20 % de los insectos registrados, siendo el GF que presentó el mayor número de especies diferentes (20 especies) y destacándose Chauliognathus scriptus Germar (Cantharidae: Coleoptera) por presentar alta abundancia (116 individuos). Los depredadores representaron el 17 % de los registros con 6 especies, de estas el 94 % de los registros de visita correspondieron a H. axyridis. Por último, el GF parasitoides registró 12 visitas (1 % del total) y 5 especies fueron catalogadas dentro del grupo.
Grupos funcionales de insectos
En nuestro estudio se observaron patrones interesantes en cuanto a la composición de los grupos funcionales de insectos. Los polinizadores representaron el 35 % de las visitas registradas en las plantas entomófilas de los márgenes de la ruta; todos los registros correspondieron a la familia Syrphidae, que presentó una riqueza de 5 especies. Sin embargo, en trabajos similares realizados en la región Pampeana registraron más de 20 especies de esta familia (Torretta & Poggio, 2013; Torretta et al., 2021). Algunas especies de esta familia son de especial interés en los cultivos, ya que prestan servicios ecosistémicos a lo largo de todo su ciclo de vida. Por ejemplo, pueden actuar como depredadores o descomponedores cuando están en estado larval y como polinizadores cuando son adultos, transportando polen como Apis mellifera L. (Rader et al., 2009, 2011; Dunn et al., 2020). El 52 % de los registros de esta familia correspondieron A. exotica, la cual también presentó altos porcentajes de registro en estudios de agroecosistemas similares (Bortolotto et al., 2016; Medeiros et al., 2018; Torretta et al., 2021). Los insectos del grupo funcional descomponedores fueron los segundos con mayor abundancia de registros de visitas en los márgenes de ruta. No obstante, se registraron 8 especies descomponedoras de las que O. varia fue la que más visitas realizó. Los insectos descomponedores se encuentran en gran parte de los ecosistemas terrestres y ayudan a mantener el equilibrio en el suelo, debido a que aseguran el reciclaje de nutrientes presentes en los tejidos de plantas y animales, fragmentando y mineralizando elementos como el fósforo y nitrógeno que son usados por la vegetación (Putman, 1983; Galante & Marcos-Garcia, 1997; Fragoso et al., 2001). Por otro lado, la mayor riqueza de especies se registró en el GF de herbívoros (20 especies), estos insectos suelen relacionarse con daños en los cultivos; sin embargo, se ha encontrado que comunidades diversas de herbívoros sostienen comunidades más diversas de enemigos naturales (Dyer & Letourneau, 2003; Rusch et al., 2017; Muneret et al., 2018). Es decir, que una mayor diversidad y abundancia de herbívoros podría beneficiar a los insectos que ejercen control biológico (Langer & Hance, 2004; Gómez-Martínez et al., 2018). El GF depredadores representó el 16.6 % de los registros de visitas sobre plantas entomófilas y H. axyridis presentó la mayor abundancia dentro de este grupo funcional (252 individuos). Esta especie puede ser considerada un buen agente controlador de áfidos, ya que tiene altas tasas de consumo de especies de pulgones que se encuentran con frecuencia en cultivos hortícolas (Rocca et al., 2017, 2022).
Por último, se registraron dos especies del orden Diptera (Tachinidae) y tres especies del orden Hymenoptera para el GF parasitoides (0,7 % del total de los VF registrados). Trichopoda giacomelli Blanchard (Tachinidae: Diptera) fue responsable del 33 % de los registros. Esta especie se considera un importante enemigo natural de adultos de Nezara viridula L. (Pentatomidae: Hemiptera), ya que reduce la longevidad y disminuye la capacidad reproductiva de estos insectos perjudiciales en los cultivos agrícolas (Liljesthröm, 1992; Coombs & Khan, 1997; Massoni & Frana, 2006). Además, se registró Campsomeris bistrimacula (Lepeletier) (Hymenoptera: Scoliidae), reconocidos como parasitoides de larvas Scarabaeidae que se desarrollan en el suelo (Cao, 2023). Sería recomendable tener en cuenta el manejo de los márgenes de ruta como refugio para estas especies. La baja representatividad de este GF tanto a nivel de especies como en abundancia podría deberse a que los muestreos fueron realizados en plantas en flor, y estos insectos solo utilizan las flores como complemento en su dieta. Este sesgo en el muestreo podría considerarse una limitante en nuestro estudio, y sería interesante profundizar en el estudio de este GF en los márgenes de ruta con el objetivo de conservar aquellas especies vegetales que benefician a los parasitoides.
Redes de interacción
Sobre las flores de los márgenes de ruta se registraron 225 interacciones planta-insecto diferentes (Fig. 4). La familia vegetal Brassicaceae registró mayor número de visitas de insectos (463 registros), el 49,5 % de estas visitas fueron realizadas por los GF polinizadores y 25,3 % por descomponedores; Apiaceae fue la segunda familia vegetal con mayores visitas de insectos (412 registros), 38,8 % por el GF polinizadores, 34,5 % por herbívoros y 15,5 % por depredadores. Por último, la familia Asteraceae registró 336 visitas, de las cuales el 37,8 % correspondió a herbívoros, 22,3 % a polinizadores y 22,3 % depredadores. Las especies vegetales más visitadas fueron Rapistrum rugosum L. All (Brassicaceae: Brassicales) (26 % de las visitas y 51 % de las especies registradas), Ammi majus L. (Apiaceae: Apiales) (10 % de las visitas y 20 % de las especies registradas) y Melilotus officinalis (L.) Pall. (Fabales: Fabaceae) (9 % de las visitas y 40 % de las especies registradas). En total, estas tres especies vegetales soportaron al 44 % de los individuos y el 67 % de las especies de visitantes florales registradas en el estudio. El 37,11 % de los registros de visitas fueron para los polinizadores, principalmente sobre flores de la familia Asteraceae; los descomponedores (25,52 %) fueron registrados en 12 familias vegetales; los herbívoros representaron el 20,1 % de las visitas totales, visitaron 12 familias vegetales. Depredadores y parasitoides el 17,27 % restante, estos dos últimos grupos se registraron principalmente sobre flores de la familia Asteraceae.
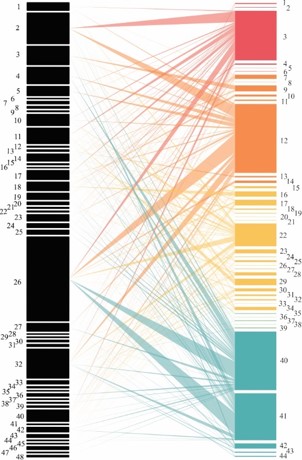
Fig. 4.
Red de interacciones mutualistas planta-insecto visitante floral obtenida a partir de muestreos sobre márgenes de ruta en el centro-este de la provincia de Santa Fe (Argentina). Las especies están representadas por rectángulos cuyo ancho es proporcional a la suma de interacciones que las involucran. Los colores indican los grupos funcionales en los que se clasificaron a los insectos (rojo: depredadores; naranja: descomponedores; amarillo: herbívoros; verde: parasitoides; azul: polinizadores). En negro están las especies de plantas de los márgenes de rutas y caminos. La identidad taxonómica de las especies se presenta en material suplementario.
DISCUSIÓN
En este estudio se analizó la riqueza de especies vegetales de crecimiento espontáneo y los grupos funcionales de insectos que las visitan, en los márgenes de rutas del Centro de la provincia de Santa Fe, donde se sitúa la cuenca lechera más importante del país. Los resultados muestran una diversidad taxonómica de insectos similar a la de otros ambientes de la región, según lo reportado en estudios previos (Montero, 2008; Pacini, 2010). Sin embargo, este estudio es el primero en explorar la diversidad y la composición de la comunidad de insectos presentes en los márgenes de rutas en la Provincia de Santa Fe, lo que representa una importante contribución para el conocimiento de la biodiversidad de la región.
Insectos en márgenes de rutas
El muestreo se realizó desde noviembre de 2013 hasta diciembre de 2015 y se registraron 29 familias de insectos representadas por 45 especies/morfoespecies. El orden de insectos con mayor cantidad de registros fue Diptera (68,5 %), probablemente debido al método del muestreo sobre plantas entomófilas y al elevado número de especies que utilizan estas plantas como fuente de alimento y cría. La gran cantidad de individuos de O. varia registrados en este estudio, ofrece una interesante relación con el entorno y las actividades propias de esta región, entre ellas la producción lechera. Esta especie, utiliza el excremento vacuno como medio de cría y fuente de alimento (Hernández, 1987), y su abundancia sugiere la presencia de materia orgánica en descomposición en el ambiente estudiado. Estos resultados pueden tener implicancias relevantes en términos del ciclo de nutrientes en la cuenca lechera. La presencia de organismos descomponedores como O. varia puede desempeñar una función importante en la descomposición de la materia orgánica y la liberación de nutrientes en el suelo, procesos importantes para la fertilidad y la calidad del suelo en la región.
Para el Orden Coleoptera, se registraron 14 especies, y la familia Coccinellidae presentó el mayor número de visitas (16,2 % del total de las visitas registradas). Los representantes de esta familia son frecuentes visitantes florales debido a que necesitan consumir néctar y polen como complemento alimenticio (Aguiar-Menezes & Aquino, 2005). De las visitas registradas para esta familia, el 97 % fueron realizadas por H. axyridis, este coleóptero es una especie importante en el control biológico de plagas por su capacidad depredadora (Hodek et al., 2012; Greco & Rocca, 2020).
El análisis de la diversidad de especies en márgenes de rutas de la provincia de Santa Fe permitió distinguir dos sitios con mayor diversidad que los seis restantes. Estos sitios presentan la particularidad de encontrarse a 1600 metros del centro de la localidad de San Martín de las Escobas (sitio “f”) y lindero a la estación de cobro de peaje de la ruta provincial Nº 6 (sitio “d”). En la provincia de Santa Fe, la Ley 11.273, prohíbe la aplicación de productos fitosanitarios en el sector comprendido entre los 500 m (clase toxicológica C y D) y los 3000 m (clase toxicológica A y B) de las zonas urbanas. Es posible que en estos sitios (“f” y “d”) se cumpla la regulación de la aplicación de agroquímicos y esto favorezca la presencia de mayor riqueza de especies. Asimismo, sería de interés conducir estudios que midan el efecto directo de la aplicación de agroquímicos sobre la entomofauna en estos ambientes.
Importancia de familias vegetales en márgenes de rutas
Los márgenes de ruta son áreas clave en la implementación de prácticas agrícolas sostenibles e importantes en la conservación de especies vegetales que sustentan poblaciones viables de insectos benéficos (Ashby, 2018; Bartual et al., 2019; Monasterolo et al., 2020). Entre las familias más relevantes registradas en este estudio se encuentra la familia Asteraceae, esta familia estuvo representada por 15 especies en los márgenes de ruta, y recibieron visitas principalmente de los GF herbívoros, depredadores y polinizadores (21 % de las visitas totales). Las Asteráceas son de gran interés debido a su capacidad para proporcionar polen de alta calidad nutricional para los insectos. Asimismo, Apiaceae, fue la segunda familia con mayor abundancia de visitas (25,5 % de visitas totales), sin embargo, solo se registraron 5 especies. Por último, sobre la vegetación espontánea de la familia Brassicaceae (3 especies vegetales) se registraron visitas principalmente de polinizadores, además, esta fue la familia vegetal con mayor registro de visitas (28,7 % de visitas totales). Las especies de estas tres familias concentran el 75,3 % del total de las visitas de insectos relevadas, posiblemente, por presentar periodos de floración prolongados (desde mediados de invierno hasta fin del otoño. Consecuentemente, estas familias vegetales fomentan la diversidad de insectos benéficos, como polinizadores, depredadores y herbívoros neutrales, lo que contribuye al control biológico de plagas y a un aumento en la productividad de los cultivos (Nicholls, 2006; Montero, 2008; Ahuja et al., 2011; Manfrino et al., 2011, Rowe et al., 2021).
Importancia de los márgenes como reservorios de biodiversidad
La simplificación del paisaje reduce la riqueza de polinizadores y de enemigos naturales, lo que produce consecuencias indirectas para la polinización y el control de plagas disminuyendo la producción en los cultivos (Dainese et al., 2019). Los márgenes de ruta cubren grandes áreas a nivel mundial, a menudo superando las áreas de los remanentes naturales (Jeusset et al., 2016; Gardiner et al., 2018). Por lo tanto, estos márgenes podrían estar aportando a los insectos recursos (polen y néctar, presas, sitios de nidificación, etc.) que no están disponibles en los cultivos aledaños. Esto los convierte en posibles corredores biológicos para la entomofauna. Varios autores han informado que la diversidad de especies aumenta con la heterogeneidad del paisaje (Tscharntke et al., 2005; Devictor & Jiguet, 2007; Fahrig et al., 2011; Phillips et al., 2020). Los márgenes de las rutas donde se conserva la vegetación de crecimiento espontáneo podrían aumentar la conectividad entre parches naturales, permitir el intercambio de visitantes florales entre el margen y los cultivos aledaños, y aportar heterogeneidad al ambiente. Además, en vastas extensiones de campos cultivados, los márgenes de rutas son los únicos ambientes que brindan refugio a especies vegetales y sus insectos asociados.
CONCLUSIONES
Los márgenes de las rutas proporcionan refugio y alimento a los visitantes florales, creando ambientes para insectos con roles ecológicos clave. Nuestros resultados muestran que las especies de las familias vegetales Brassicaeae, Apiaceae y Asteraceae podrían usarse para enriquecer estos márgenes, desarrollando especies nativas para manejar estos ambientes, ya que, recibieron el mayor porcentaje de visitas de polinizadores y depredadores. Aunque se ha estudiado el uso de los bordes de los cultivos como reservorios de insectos benéficos, se ha explorado poco el uso de los márgenes de las rutas para esta función. Este tipo de corredores son comunes en el paisaje de la cuenca lechera del centro de la provincia de Santa Fe, y hemos demostrado su importancia para la conservación de insectos y la flora asociada.
Sugerimos seguir avanzando en la implementación de planes de conservación y manejo de los márgenes de rutas y caminos de la región con el fin de conservar y promover la biodiversidad de especies vegetales e insectos. Es importante reconocer la función que estos ambientes pueden desempeñar como corredores biológicos, conectando parches de hábitats fragmentados y proporcionando recursos para la fauna silvestre. Esto podría incluir medidas como la promoción de prácticas agrícolas más sostenibles y la restauración de hábitats naturales a través de la restauración ecológica y la reforestación de áreas degradadas. Por último, es apremiante fomentar paisajes agrícolas más diversificados, con presencia de vegetación espontánea y nativa, que puedan aportar a la producción de alimentos, por un lado, y por otro conservar la biodiversidad de manera equilibrada y sostenible.
Materiales suplementarios
material suplementario (pdf)
Agradecimientos
A los Dres. P. Mulieri, L. Patitucci, J. P. Torretta y J. Frana, por su colaboración en la identificación de insectos de los Ordenes Diptera y Coleóptera. Al Dr. G. Marino por la identificación de las especies vegetales. Este estudio fue financiado por proyectos CAI+D 2020 (cod. 50520190100159LI) de la Universidad Nacional del Litoral y PICT 2019 (Cod: 2019-02478) de la Agencia Nacional de la Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación.
REFERENCIAS
Aguado Martín, L.O., Viñuela Sandoval, E., & Fereres Castiel, A. (2015) Guía de campo de los polinizadores de España. Ediciones Mundi-Prensa, Madrid, España.
Aguiar-Menezes, E.L., & Aquino, A.M. (2005) Coleoptera terrestre e sua importância nos sistemas agropecuários. Embrapa Agrobiologia, Seropédica, Brasil
Ahuja, I., Rohloff, J., & Bones, A.M. (2011) Defence mechanisms of Brassicaceae: implications for plant-insect interactions and potential for integrated pest management. Sustainable Agriculture, 2, 623-670.
Altieri, M.A., & Nicholls, C.I. (2004) Una base agroecológica para el diseño de sistemas diversificados de cultivo en el Trópico. The Haworth Press, Binghamton, NY, USA.
Armsworth, P.R., Chan, K.M., Daily, G.C., Ehrlich, P.R., Kremen, C., Ricketts, T.H., & Sanjayan, M.A. (2007) Ecosystem‐service science and the way forward for conservation. Conservation Biology, 21(6), 1383-1384. https://doi.org/10.1111/j.1523-1739.2007.00821.x
Ashby, M.A. (2018) Enhancing the benefits to biodiversity and ecosystem services within arable field margins. Lancaster University, UK.
Bartual, A.M., Sutter, L., Bocci, G., Moonen, A.C., Cresswell, J., Entling, M., & Albrecht, M. (2019) The potential of different semi-natural habitats to sustain pollinators and natural enemies in European agricultural landscapes. Agriculture, Ecosystems & Environment, 279, 43-52. https://doi.org/10.1016/j.agee.2019.04.009
Bortolotto, O.C., Menezes Júnior, A.D.O., Hoshino, A.T., & Campos, T.A. (2016) Distance from the edge of forest fragments influence the abundance of aphidophagous hoverflies (Diptera: Syrphidae) in wheat fields. Acta Scientiarum. Agronomy, 38, 157-164. https://doi.org/10.4025/actasciagron.v38i2.27711
Cao, J.A. (2023) Aporte de Campsomeris bistrimaculata (Hymenoptera: Scoliidae) como polinizador nativo en el cultivo de colza en el centro sur bonaerense. Tesis de Grado. Universidad Nacional del Sur. Bahía Blanca, Argentina. https://repositoriodigital.uns.edu.ar/handle/123456789/6417
Chacoff, N.P., Vázquez, D.P., Lomascolo, S.B., Stevani, E.L., Dorado, J., & Padron, B. (2012) Evaluating sampling completeness in a desert plant–pollinator network. Journal of Animal Ecology, 81(1), 190-200. https://doi.org/10.1111/j.1365-2656.2011.01883.x
Chao, A., Chiu, C.H., & Jost, L. (2014) Unifying species diversity, phylogenetic diversity, functional diversity, and related similarity and differentiation measures through Hill numbers. Annual review of ecology, evolution, and systematics, 45, 297-324. https://doi.org/10.1146/annurev-ecolsys-120213-091540
Claps, L.E., Debandi, G., & Roig-Juñet, S. (2008) Biodiversidad de Artrópodos Argentinos. Volumen 2. Editorial Sociedad Entomológica Argentina, Mendoza.
Colwell, R.K., Chao, A., Gotelli, N.J., Lin, S.Y., Mao, C.X., Chazdon, R.L., & Longino, J.T. (2012) Models and estimators linking individual-based and sample-based rarefaction, extrapolation and comparison of assemblages. Journal of Plant Ecology, 5(1), 3-21. https://doi.org/10.1093/jpe/rtr044
Coombs, M., & Khan, S.A. (1997) New host/parasitoid records for Australian Pentatomidae, Tachinidae and Braconidae. The Australian Entomologist, 24(2), 61-64. https://search.informit.org/doi/10.3316/informit.094082002298383
Corbet, S.A. (2006) A typology of pollination systems: implications for crop management and the conservation of wild plants. Plant-pollinator interactions. From specialization to generalization. The University of Chicago Press, Chicago.
Cordo, H.A., Logarzo, G., Braun, K., & Di Iorio, O. (2004) Catálogo de los insectos fitófagos de la Argentina y sus plantas asociadas. Editorial Sociedad Entomológica Argentina, Buenos Aires, Argentina.
Dainese, M., Martin, E.A., Aizen, M.A., Albrecht, M., Bartomeus, I., Bommarco, R., & Steffan-Dewenter, I. (2019) A global synthesis reveals biodiversity-mediated benefits for crop production. Science Advances, 5(10), eaax0121. https://doi.org/10.1126/sciadv.aax0121
Devictor, V., & Jiguet, F. (2007) Community richness and stability in agricultural landscapes: the importance of surrounding habitats. Agriculture, Ecosystems & Environment, 120(2-4), 179-184. https://doi.org/10.1016/j.agee.2006.08.013
Diehl, E., Sereda, E., Wolters, V., & Birkhofer, K. (2013) Effects of predator specialization, host plant and climate on biological control of aphids by natural enemies: a meta‐analysis. Journal of Applied Ecology, 50(1), 262-270. https://doi.org/10.1111/1365-2664.12032
Dormann, C.F. (2020) Using bipartite to describe and plot two-mode networks in R. https://cran.r-project.org (Accessed 17 March 2024)
Dunn, L., Lequerica, M., Reid, C.R., & Latty, T. (2020) Dual ecosystem services of syrphid flies (Diptera: Syrphidae): pollinators and biological control agents. Pest Management Science, 76(6), 1973-1979. https://doi.org/10.1002/ps.5807
Dyer, L.A., & Letourneau, D. (2003) Top‐down and bottom‐up diversity cascades in detrital vs. living food webs. Ecology Letters, 6(1), 60-68. https://doi.org/10.1046/j.1461-0248.2003.00398.x
Fahrig, L., Baudry, J., Brotons, L., Burel, F.G., Crist, T.O., Fuller, R.J., Sirami, C., Siriwardena, G.V., & Martin, J.L. (2011) Functional landscape heterogeneity and animal biodiversity in agricultural landscapes. Ecology letters, 14(2), 101-112. https://doi.org/10.1111/j.1461-0248.2010.01559.x
Fardila, D., Kelly, L.T., Moore, J.L., & McCarthy, M.A. (2017) A systematic review reveals changes in where and how we have studied habitat loss and fragmentation over 20 years. Biological Conservation, 212, 130-138. https://doi.org/10.1016/j.biocon.2017.04.031
Fragoso, C., Castillo, P.R., & Rojas, P. (2001) La importancia de la biota edáfica en México. Acta Zoológica Mexicana (nueva serie), 1, 1-10. https://doi.org/10.21829/azm.2001.8401842
Galante, E., & Marcos-García, M.A. (1997) Detritívoros, coprófagos y necrófagos. Los Artrópodos y el Hombre. Sociedad Aragonesa de Entomología. Zaragoza, 20, 57-64.
Ganser, D., Knop, E., & Albrecht, M. (2019) Sown wildflower strips as overwintering habitat for arthropods: effective measure or ecological trap? Agriculture, Ecosystems & Environment, 275, 123-131. https://doi.org/10.1016/j.agee.2019.02.010
Gardiner, M.M., Riley, C.B., Bommarco, R., & Öckinger, E. (2018) Rights‐of‐way: a potential conservation resource. Frontiers in Ecology and the Environment, 16(3), 149-158. https://doi.org/10.1002/fee.1778
Garibaldi, L.A., Steffan‐Dewenter, I., Kremen, C., Morales, J.M., Bommarco, R., Cunningham, S. A., Carvalheiro, LG., Chacoff, N.P., Dudenhöffer, J.H., Greenleaf, S.S., Holzschuh, A., Isaacs, R., Krewenka, K., Mandelik, Y., Mayfield, M.M., Morandin, L.A., Potts, S.G., Ricketts, T.H., Szentgyörgyi, H., Viana, B.F., Westphal, C., Winfree, R., & Klein, A.M. (2011) Stability of pollination services decreases with isolation from natural areas despite honey bee visits. Ecology Letters, 14(10), 1062-1072. https://doi.org/10.1111/j.1461-0248.2011.01669.x
Garibaldi, L.A., Sáez, A., Aizen, M.A., Fijen, T., & Bartomeus, I. (2020) Crop pollination management needs flower‐visitor monitoring and target values. Journal of Applied Ecology, 57(4), 664-670. https://doi.org/10.1111/1365-2664.13574.
Gómez-Martínez, M.A., Jaques, J.A., Ibáñez-Gual, M.V., & Pina, T. (2018) When the ground cover brings guests: is Anaphothrips obscurus a friend or a foe for the biological control of Tetranychus urticae in clementines? Journal of Pest Science, 91(2), 613-623. https://doi.org/10.1007/s10340-017-0926-0
Greco, N.M., & Rocca, M. (2020) Depredadores. Control biológico de plagas en horticultura. Experiencias argentinas de las últimas tres décadas (ed. Polack, L.A., Lecuona, R.E., & Lopez, S.N), pp. 33-74. Ediciones INTA, Ciudad Autónoma de Buenos Aires, Argentina.
Haddad, N.M., Brudvig, L.A., Clobert, J., Davies, K.F., Gonzalez, A., Holt, R.D., & Townshend, J.R. (2015) Habitat fragmentation and its lasting impact on Earth’s ecosystems. Science Advances, 1(2), e1500052. http://dx.doi.org/10.1126/sciadv.1500052
Hallmann, C.A., Sorg, M., Jongejans, E., Siepel, H., Hofland, N., Schwan, H., Stenmans, W., Müller, A., Sumser, H., Hörren, T., Goulson, D., & De Kroon, H. (2017) More than 75 percent decline over 27 years in total flying insect biomass in protected areas. PloS one, 12(10), e0185809. https://doi.org//10.1371/journal.pone.0185809
Hendrickx, F., Maelfait, J.P., Van Wingerden, W., Schweiger, O., Speelmans, M., Aviron, S., Augenstein, I., Billeter, R., Bailey, D., Bukacek, R., Burel, F., Diekötter, T., Dirksen, J., Herzog, F., Liira, J., Roubalova, M., Vandomme, V., Bugter, R., & Bugter, R.O.B. (2007) How landscape structure, land‐use intensity and habitat diversity affect components of total arthropod diversity in agricultural landscapes. Journal of Applied Ecology, 44(2), 340-351. https://doi.org/10.1111/j.1365-2664.2006.01270.x
Hernández, M.C. (1987) Dípteros coprófagos: Oxysarcodexia varia (Walker) (Diptera, Sarcophagidae). Descripción de estadíos larvales. Revista de la Sociedad Entomológica Argentina, 46(1-4), 141-145.
Hill, M.O. (1973) Diversity and evenness: an unifying notation and its consequences. Ecology, 54(2): 427-432. https://doi.org/10.2307/1934352
Hodek, I., Honek, A., & Van Emden, H.F. (2012) Ecology and behaviour of the ladybird beetles (Coccinellidae). John Wiley & Sons, New Jersey, USA.
Holzschuh, A., Dainese, M., González‐Varo, J.P., Mudri‐Stojnić, S., Riedinger, V., Rundlöf, M., & Steffan‐Dewenter, I. (2016) Mass‐flowering crops dilute pollinator abundance in agricultural landscapes across Europe. Ecology Letters, 19(10), 1228-1236. https://doi.org/10.1111/ele.12657
Hsieh, T.C., Ma, K.H., & Chao, A. (2016) iNEXT: an R package for rarefaction and extrapolation of species diversity (Hill numbers). Methods in Ecology and Evolution, 7(12), 1451-1456. https://doi.org/10.1111/2041-210X.12613
INDEC (Instituto Nacional de Estadística y Censos de la República Argentina) (2021) Censo Nacional Agropecuario 2018: resultados definitivos. Ciudad Autónoma de Buenos Aires, Buenos Aires. Argentina.
Jeusset, A., Vargac, M., Bertheau, Y., Coulon, A., Deniaud, N., Flamerie De Lachapelle, F., & Sordello, R. (2016) Can linear transportation infrastructure verges constitute a habitat and/or a corridor for biodiversity in temperate landscapes? A systematic review protocol. Environmental Evidence, 5(1), 1-11. https://doi.org/10.1186/s13750-016-0056-9
Johnson, N., & Triplehorn, C.A. (2004) Borror and DeLong’s introduction to the study of insects (7th ed.). Brooks/Cole. Florence, KY.
Jost, L., & González-Oreja, J. (2012) Midiendo la diversidad biológica: más allá del índice de Shannon. Acta Zoológica Lilloana, 56(1-2), 3-14.
Landis, D.A. (2017) Designing agricultural landscapes for biodiversity-based ecosystem services. Basic and Applied Ecology, 18, 1-12. https://doi.org/10.1016/j.baae.2016.07.005
Langer, A., & Hance, T. (2004) Enhancing parasitism of wheat aphids through apparent competition: a tool for biological control. Agriculture, Ecosystems & Environment, 102(2), 205-212. https://doi.org/10.1016/j.agee.2003.07.005
Larson, D.L., Royer, R.A., & Royer, M.R. (2006) Insect visitation and pollen deposition in an invaded prairie plant community. Biological Conservation, 130(1), 148-159. https://doi.org/10.1016/j.biocon.2005.12.009
Lindgren, E., Almqvist, M.S., & Elmqvist, T. (2018) Ecosystem services and health benefits an urban perspective. Oxford textbook of nature and public health: The role of nature in improving the health of a population (ed. Van den Bosch, M., & Bird, W.), pp. 257-263. Oxford University Press, Oxford.
Liljesthröm, G. (1992) Distribución de los ataques del parasitoide Trichopoda giacomellii (Diptera: Tachinidae) sobre una población de Nezara viridula (Hemiptera: Pentatomidae). Ecología Austral, 2(1), 029-037.
Losey, J.E., & Vaughan, M. (2006) The economic value of ecological services provided by insects. Bioscience, 56(4), 311-323. https://doi.org/10.1641/0006-3568(2006)56[311:TEVOES]2.0.CO;2.
Medeiros, H.R., Hoshino, A.T., Ribeiro, M.C., Morales, M.N., Martello, F., Neto, O.C.P., & de Oliveira Menezes Junior, A. (2018) Non-crop habitats modulate alpha and beta diversity of flower flies (Diptera, Syrphidae) in Brazilian agricultural landscapes. Biodiversity and conservation, 27, 1309-1326. https://doi.org/10.1007/s10531-017-1495
Manfrino, R.G., Salto, C.E., & Zumoffen, L. (2011) Estudio de las asociaciones áfidos-entomófagos sobre Foeniculum vulgare (Umbelliferae) y Conyza bonariensis (Asteraceae) en la región central de Santa Fe, Argentina. Revista de la Sociedad Entomológica Argentina, 70(1-2), 99-109.
Marshall, E.J.P., & Moonen, A.C. (2002) Field margins in northern Europe: their functions and interactions with agriculture. Agriculture, Ecosystems and Environment, 89(1-2), 5-21. https://doi.org/10.1016/S0167-8809(01)00315-2.
Massoni, F., & Frana, J. (2006) Enemigos naturales del complejo de chinches fitófagas y evaluación de su acción ecológica en un cultivo de soja. Publicación Miscelánea INTA EE Rafaela, 106, 163-165.
Medan, D., Torretta, J.P., Hodara, K., de la Fuente, E.B., & Montaldo, N.H. (2011) Effects of agriculture expansion and intensification on the vertebrate and invertebrate diversity in the Pampas of Argentina. Biodiversity and Conservation, 20, 3077-3100. https://doi.org/10.1007/s10531-011-0118-9.
Molina, G.A., Poggio, S.L., & Ghersa, C.M. (2014) Epigeal arthropod communities in intensively farmed landscapes: effects of land use mosaics, neighbourhood heterogeneity, and field position. Agriculture, Ecosystems and Environment, 192, 135-143. https://doi.org/10.1016/j.agee.2014.04.013.
Molina, G.A., Poggio, S.L. & Ghersa, C.M. (2016) Structural complexity of arthropod guilds is affected by the agricultural landscape heterogeneity generated by fencerows. Annals of Applied Biology, 168, 173-184. https://doi.org/10.1111/aab.12253.
Monasterolo, M., Poggio, S.L., Medan, D., & Devoto, M. (2020) Wider road verges sustain higher plant species richness and pollinator abundance in intensively managed agroecosystems. Agriculture, Ecosystems & Environment, 302, 107084. https://doi.org/10.1016/j.agee.2020.107084
Montero, G.A. (2008) Comunidades de artrópodos en vegetación de áreas no cultivadas del sudeste de Santa Fe. MSc Tesis. Maestría en Manejo y Conservación de Recursos Naturales. Facultad de Ciencias Agrarias. Universidad Nacional de Rosario. Zavalla, Argentina. https://www.researchgate.net/publication/282186980
Moreno, C.E., Barragán, F., Pineda, E., & Pavón, N.P. (2011) Reanálisis de la diversidad alfa: alternativas para interpretar y comparar información sobre comunidades ecológicas. Revista Mexicana de Biodiversidad, 82(4), 1249-1261. https://doi.org/10.22201/ib.20078706e.2011.4.745
Morrone, J.J., & Coscarón, S. (1998) Biodiversidad de artrópodos argentinos: una perspectiva biotaxonómica. Ediciones Sur. La Plata, Argentina.
Muneret, L., Mitchell, M., Seufert, V., Aviron, S., Djoudi, E.A., Pétillon, J. & Rusch, A. (2018) Evidence that organic farming promotes pest control. Nature Sustainability, 1(7), 361-368. https://doi.org/10.1038/s41893-018-0102-4
Nicholls, C. (2006) Bases agroecológicas para diseñar e implementar una estrategia de manejo de hábitat para control biológico de plagas. Agroecología, 1, 37-48.
Öckinger, E., & Smith, H.G. (2007) Semi‐natural grasslands as population sources for pollinating insects in agricultural landscapes. Journal of Applied Ecology, 44(1), 50-59. https://doi.org/10.1111/j.1365-2664.2006.01250.x
Pacini, A. (2010) Servicios ecosistémicos generados por las interacciones planta- insecto visitante floral en el Departamento San Cristóbal, Provincia de Santa Fe, perteneciente a la Región Parque Chaqueño. Tesina de Grado. Licenciatura en Biodiversidad. Facultad de Humanidades y Ciencias, Universidad Nacional del Litoral. Santa Fe, Argentina.
Park, M.G., Blitzer, E.J., Gibbs, J., Losey, J.E., & Danforth, B.N. (2015) Negative effects of pesticides on wild bee communities can be buffered by landscape context. Proceedings of the Royal Society B: Biological Sciences, 282, 1809. https://doi.org/10.1098/rspb.2015.0299
Phillips, B.B., Bullock, J.M., Osborne, J.L., & Gaston, K.J. (2020) Ecosystem service provision by road verges. Journal of Applied Ecology, 57(3), 488-501. https://doi.org/10.1111/1365-2664.13556
Plá, J.M. (2022) El impacto del modelo de agronegocios sobre el modelo de producción agropecuaria argentino desde una perspectiva socio-jurídica. El caso de la industria lechera en la provincia de Santa Fe. MSc Tesis. Maestría en Sistemas Ambientales Humanos. Centro de Estudios Interdisciplinarios. Universidad Nacional de Rosario. Rosario, Argentina. https://rephip.unr.edu.ar/items/3a7c152f-332d-434a-9e2c-e51907dc8043
Poggio, S.L., Chaneton, E.J. & Ghersa, C.M. (2010) Landscape complexity differentially affects alpha, beta, and gamma diversities of plants occurring in fencerows and crop fields. Biological Conservation, 143, 2477-2486. https://doi.org/10.1016/j.biocon.2010.06.014
Poggio, S.L., Chaneton, E.J., & Ghersa, C.M. (2013) The arable plant diversity of intensively managed farmland: Effects of field position and crop type at local and landscape scales. Agriculture, Ecosystems and Environment, 166, 55-64. https://doi.org/10.1016/j.agee.2012.01.013
Putman, R.J. (1983) Carrion and dung: the decomposition of animal wastes. Edward Arnold. London, UK.
Rader, R., Howlett, B.G., Cunningham, S.A., Westcott, D.A., Newstrom‐Lloyd, L.E., Walker, M.K., & Edwards, W. (2009) Alternative pollinator taxa are equally efficient but not as effective as the honeybee in a mass flowering crop. Journal of Applied Ecology, 46(5), 1080-1087. https://doi.org/10.1111/j.1365-2664.2009.01700.x
Rader, R., Edwards, W., Westcott, D.A., Cunningham, S.A., & Howlett, B.G. (2011) Pollen transport differs among bees and flies in a human‐modified landscape. Diversity and Distributions, 17(3), 519-529. https://doi.org/10.1111/j.1472-4642.2011.00757.x
RStudio Team (2022). RStudio: Integrated Development for R. RStudio, PBC, Boston, MA. http://www.rstudio.com/ (Accessed 17 March 2024)
Rocca, M., Rizzo, E., Greco, N., & Sánchez, N. (2017) Intra‐and interspecific interactions between aphidophagous ladybirds: the role of prey in predator coexistence. Entomologia Experimentalis et Applicata, 162(3), 284-292. https://doi.org/10.1111/eea.12527
Rocca, M., Díaz Lucas, M.F., & Greco, N.M. (2022) Effect of spatiotemporal association and trophic interactions between aphidophagous coccinellids toward aphid control. Environmental Entomology, 51(1), 44-51. https://doi.org/10.1093/ee/nvab127
Roig-Juñet, S., Claps L.E., & Morrone, J.J. (2014) Biodiversidad de Artrópodos Argentinos. Volúmenes 3-4. Editorial Sociedad Entomológica Argentina. San Miguel de Tucumán, Argentina.
Rowe, L., Gibson, D., Landis, D.A., & Isaacs, R. (2021) Wild bees and natural enemies prefer similar flower species and respond to similar plant traits. Basic and Applied Ecology, 56, 259-269. https://doi.org/10.1016/j.baae.2021.08.009
Rusch, A., Bommarco, R., & Ekbom, B. (2017) Conservation biological control in agricultural landscapes. Advances in Botanical Research, 81, 333-360. https://doi.org/10.1016/bs.abr.2016.11.001
Sáez, A., Sabatino, M., & Aizen, M. (2014) La diversidad floral del borde afecta la riqueza y abundancia de visitantes florales nativos en cultivos de girasol. Ecología Austral, 24(1), 94-102. https://doi.org/10.25260/EA.14.24.1.0.41
Sandoval, P.S., Leonardi, R., Pernuzzi, C., & Martins, L. (2023) Transformaciones inducidas por la lógica del sistema agroalimentario. Tenacidad y conflicto: semblantes de la lechería familiar santafesina. (ed. Sandoval, P.S.) pp. 81-96. Ediciones UNL, Santa Fe.
Schowalter, T.D. (2013) Insects and sustainability of ecosystem services. CRC Press. Florida, USA.
Southwood, T.R.E., & Way, M.J. (1970) Ecological background to pest management. Concepts of Pest Management (ed. Rabb, R.L., & Guthrie, F.E), pp. 6-28. North Carolina State University, Raleigh, NC.
Spangenberg, J.H., von Haaren, C., & Settele, J. (2014) The ecosystem service cascade: Further developing the metaphor. Integrating societal processes to accommodate social processes and planning, and the case of bioenergy. Ecological Economics, 104, 22-32. https://doi.org/10.1016/j.ecolecon.2014.04.025
Tilman, D., Balzer, C., Hill, J., & Befort, B.L. (2011) Global food demand and the sustainable intensification of agriculture. Proceedings of the National Academy of Sciences, 108(50), 20260-20264. https://doi.org/10.1073/pnas.1116437108
Torres, C. (2021) El espacio productivo de la cuenca lechera central Argentina y sus paradigmas históricos de desarrollo. Eutopía Revista de Desarrollo Económico Territorial, 20, 32-51. https://doi.org/10.17141/eutopia.20.2021.5084
Torretta, J.P., & Poggio, S.L. (2013) Species diversity of entomophilous plants and flower-visiting insects is sustained in the field margins of sunflower crops. Journal of Natural History, 47(3-4), 139-165. https://doi.org/10.1080/00222933.2012.742162
Torretta, J.P., López, M.C., & Marrero, H.J. (2021) Las moscas de las flores (Diptera: Syrphidae) en agroecosistemas pampeanos: un caso de estudio. Revista de la Sociedad Entomológica Argentina, 80(2), 23-34. http://dx.doi.org/doi.org/10.25085/rsea.800205.
Tscharntke, T., Klein, A. M., Kruess, A., Steffan-Dewenter, I., & Thies, C. (2005) Landscape perspectives on agricultural intensification and biodiversity-ecosystem service management. Ecology Letters, 8, 857-874. https://doi.org/10.1111/j.1461-0248.2005.00782.x
Tscharntke, T., Bommarco, R., Clough, Y., Crist, T.O., Kleijn, D., Rand, T.A., & Vidal, S. (2008) Conservation biological control and enemy diversity on a landscape scale. Biological control, 45(2), 238-253. https://doi.org/10.1016/j.biocontrol.2007.08.006
Valladares, G., Salvo, A., & Degafo, M.T. (2019) Insectos: guía completa para explorar su mundo. Editorial de la UNC, Córdoba, Argentina.
Wagner, D.L. (2020) Insect declines in the Anthropocene. Annual Review of Entomology, 65, 457-480. https://doi.org/10.1146/annurev-ento-011019-025151
Wang, L., Delgado-Baquerizo, M., Wang, D., Isbell, F., Liu, J., Feng, C., Liu, J., Zhong, Z., Zhu, H., Yuan, X., Chang, Q., & Liu, C. (2019) Diversifying livestock promotes multidiversity and multifunctionality in managed grasslands. Proceedings of the National Academy of Sciences, 116(13), 6187-6192. https://doi.org/10.1073/pnas.1807354116
Notas de autor
ghiglionecarla0@gmail.com