Casos Clínicos
Síndrome de Bouveret.
(Bouveret's syndrome)
Síndrome de Bouveret.
Avances en Biomedicina, vol. 8, núm. 2, pp. 83-87, 2019
Universidad de los Andes

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 05 Mayo 2019
Aprobación: 18 Enero 2020
Resumen: El síndrome de Bouveret es una causa rara de íleo biliar proximal con obstrucción del duodeno o de la salida gástrica. Es causada por la impactación de cálculos biliares ectópicos de gran tamaño en el duodeno proximal y es una complicación de la colelitiasis crónica con fístula colecistogástrica o colecistoentérica. Debido a su rareza, y sintomatología inespecífica, en el diagnóstico diferencial apenas se le considera como etiología de la obstrucción de la salida gástrica. Los síntomas clínicos son totalmente vagos. La sintomatología de presentación más común es dolor abdominal epigástrico o en cuadrante superior derecho difuso, náuseas, vómitos, hematemesis y pérdida de peso. Sin un diagnóstico oportuno, puede asociarse con altas tasas de morbilidad y mortalidad, por lo que es importante hacer un diagnóstico y tratamiento temprano. Los hallazgos de la tomografía computada son neumobilia, fístula colecistoduodenal y un cálculo biliar en el duodeno o tríada de Rigler, la cual es patognomónica. El objetivo primordial de la terapia es aliviar la obstrucción mediante la eliminación del cálculo. El tratamiento ideal es endoscópico y si fracasa se debe realizar la cirugía. Presentamos un caso de síndrome de Bouveret.
Palabras clave: Síndrome de Bouveret, Obstrucción de la salida gástrica, Cálculos biliares, Íleo biliar.
Abstract: Bouveret's syndrome is a rare cause of proximal biliary ileus with obstruction of the duodenum or gastric outlet. It is caused by impaction of large ectopic gallstones in the proximal duodenum and is a complication of chronic cholelithiasis with cholecystogastric or cholecystoenteric fistula. Due to its rarity, and non-specific symptomatology, in the differential diagnosis, it is hardly considered as the etiology of the obstruction of the gastric outlet. Clinical symptoms are totally vague. The most common symptomatology is epigastric abdominal pain or diffuse upper right quadrant, nausea, vomiting, hematemesis and weight loss. Without a timely diagnosis, it can be associated with high morbidity and mortality rates, so it is important to make an early diagnosis and treatment. Findings of the computed tomography are pneumobilia, cholecystoduodenal fistula and a gallstone in the duodenum or Rigler's triad, which is pathognomonic. The primary goal of therapy is to relieve the blockage by removing the gallstones. The ideal treatment is endoscopic and if it fails surgery should be performed. We present a case of Bouveret's syndrome.
Keywords: Bouveret syndrome, Obstruction of the gastric outlet, Gallstones, Biliary ileus.
Introducción
El término “malformación arterio-venosa espinal metamérica” (MAVEM) es nuevo en la literatura científica, deriva de otro que involucra encéfalo y cara denominado “malformación arteriovenosa cráneo-facial metamérica” (MAVCM) (1). MAVEM son malformaciones vasculares localizadas en una o varias metámeras, no hereditarias, las cuales se extienden a la médula espinal, a regiones para espinales y otros tejidos de la misma metámeras. El síndrome de Cobb forma parte de las MAVEM y siempre involucra la médula espinal (2). Este síndrome es raro, no hereditario, caracterizado por la presencia de angiomas espinales o malformaciones arteriovenosas (MAV) y lesiones cutáneas de origen vascular presentes en el mismo dermatomo, asociadas con hemorragias y déficits neurológicos (3). La lesión vascular se presenta desde el nacimiento pero no da síntomas hasta varios años después, cuando se extiende e involucra tejidos profundos (4). Puede afectar cualquiera de los 31 segmentos espinales y con frecuencia involucra más de un segmento. El adjetivo “metaméricas” es debido a que afecta el ectodermo, mesodermo y neuro-ectodermo. La importancia de este síndrome reside en el hallazgo de lesiones cutáneas vasculares asociadas a angiomas espinales o MAV medulares.
Berenbuch en 1890 fue el primero en reconocer la enfermedad, pero fue descrita por Stanley Cobb en 1915. El primer caso de Cobb fue tratado por Harvey Cushing, considerado por muchos el padre de la Neurocirugía, en el Peter Bend Brigham Hospital de Boston. Actualmente, se han publicado alrededor de 50 casos de esta patología, pero su incidencia es mayor. Algunos autores consideran que el síndrome debería denominarse síndrome de Cobb-Cushing (5).
El objetivo de nuestro trabajo es presentar una paciente femenina de 24 años que consultó con síntomas progresivos y severos de lumbalgia crónica, deambulación dificultosa, parestesia espástica y trastornos esfinterianos desde los 19 años, posterior a cesárea electiva. Entre sus antecedentes de importancia tenia MAV toracolumbar desde T10 hasta L3, y tratamiento endovascular parcial previo. Al examen físico se observó nevus fenotípico a nivel torácico lateral e inferior derecho. Angiografía espinal demostró permeabilidad de las lesiones malformativas metaméricas múltiples desde T10 a L3. Se practicaron dos sesiones de embolizaciones supra selectivas espinales múltiples en el año 2011 en los niveles de T10 a L1 demostrando oclusión en la mayoría de las malformaciones. Los síntomas mejoraron en forma significativa manteniéndose estable clínicamente hasta los 32 años de edad. Último control fue en marzo del 2018.
Caso Clínico
Se trata de una paciente femenina de 59 años, quien asistió a la emergencia por presentar náuseas y vómitos intensos, repetidos y de color oscuro de 3 días de evolución, acompañado de dolor abdominal difuso en epigastrio e hipocondrio derecho de leve intensidad, difuso, sin acalmias y que no mejoraba con el uso de analgésicos. La paciente tenía antecedentes de diabetes mellitus no insulinodependiente e hipertensión desde hacía 3 y 5 años, respectivamente.
El examen físico reveló palidez cutáneo- mucosa acentuada, signos de deshidratación, hipotensión (100/60 mm de Hg) y frecuencia cardiaca de 110 latidos x minuto. La evaluación abdominal mostró aumento de la sensibilidad en la región epigástrica e hipocondrio derecho, sin signos de distensión, defensa o rigidez abdominal. No se palparon tumoraciones o visceromegalias. Los ruidos hidroaéreos estaban normales en intensidad y frecuencia. En el examen rectal no se palparon anomalías ni tumoraciones. En vista de los hallazgos se colocó una sonda nasogástrica para drenar el contenido gástrico. Las pruebas de laboratorio mostraron los siguientes resultados: cuenta blanca 18.000 células/mm3 y hemoglobina 8,0 g/dL. Las pruebas de perfil de coagulación, funcionalismo hepático y renal estaban dentro de límites normales. Las concentraciones de electrolitos y glicemia estaban dentro de límites normales.
La radiografía de tórax mostró cardiomegalia ligera con ambos campos pulmonares normales y la radiografía de abdomen mostró algunas asas distendidas con niveles de aire y ausencia de neumoperitoneo. La ecografía abdominal mostró que el estómago estaba distendido y lleno de líquido con un túnel de insonación en el duodeno. Las imágenes de tomografía computada revelaron presencia de aire libre en cavidad abdominal, obstrucción de la salida gástrica con presencia de neumobilia, evidencia de colecistitis y una probable fistula colecistoduodenal. Se observó un defecto de llenado con atenuación baja rodeado de material de contraste de alta atenuación en la tercera porción del duodeno, que parecía corresponder a un cálculo biliar (figura 1). Se realizó el diagnóstico de fistula bilioentérica e íleo biliar proximal.
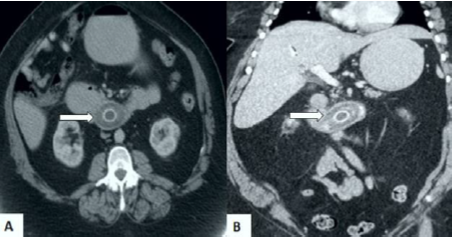
Figura 1
Tomografía computada abdominopélvica. A) Imagen axial que demuestra cálculo biliar (flecha) en la tercera porción del duodeno con el duodeno proximal y el estómago lleno de líquido. B) Imagen coronal que muestra el cálculo biliar en la tercera porción del duodeno (flecha), neumobilia y dilatación del estómago.
La endoscopia gastrointestinal superior confirmó la presencia de un cálculo biliar de gran tamaño impactado en el duodeno. Se intentó la extracción del cálculo con cestas y fórceps, pero no se logró retirar debido a que la zona donde se encontraba y el diámetro del cálculo hicieron imposible la extracción, al igual que la colocación de alambres guías o globos más allá de la ubicación del cálculo en el duodeno. En vista de lo anterior, y dada la posibilidad de perforación por necrosis secundaria a compresión, se decidió realizar laparotomía exploratoria. Se encontró tumoración dura y regular en la tercera porción del duodeno con adherencias fibróticas a la vesícula biliar, Se decidió realizar enterolitotomía y colecistectomía con reparación de la fístula colecistoduodenal. El cálculo en la laparotomía había migrado aproximadamente 30 centímetros en el yeyuno y fue extraído mediante enterotomía. Posteriormente se realizó la colecistectomía y reparación con cierre primario de la fistula que posteriormente fue cubierta con un parche de epiplón y pegamento de fibrina. El cálculo biliar media 9 x 5 centímetros (figura 2). Durante el postoperatorio, la paciente no presentó ninguna complicación y fue dada de alta a los 7 días.
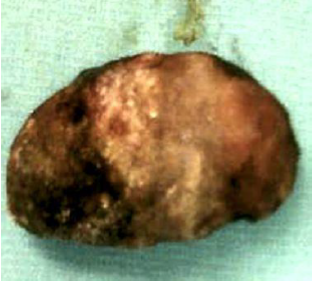
Figura 2
Cálculo biliar de 9 centímetros de largo removido durante la cirugía.
Discusión
El síndrome de Bouveret es una complicación extremadamente rara de la colelitiasis, en la que un cálculo biliar de gran tamaño migra por una fístula bilioentérica (causada por erosión de la vesícula biliar y pared intestinal) hacia el estómago distal o el duodeno proximal que causa obstrucción de la salida gástrica secundario al bloqueo duodenal intraluminal. Después de la migración a través de la fístula, la mayoría de los cálculos biliares pasan sin producir síntomas hasta ser expulsados (1, 4). En raras ocasiones, este puede aumentar de tamaño por la acumulación de sales y materia fecal que se agregan a la superficie y causan íleo biliar al bloquear la luz intestinal. El síndrome ocurre más frecuentemente en mujeres de edad avanzada (7 veces más común en personas mayores de 70 años) (4). A pesar de las mejoras significativas en el diagnóstico y tratamiento, las tasas de morbilidad y mortalidad siguen siendo altas, estimadas en 60% y 12% - 30%, respectivamente (5).
La localización más común de impactación del cálculo es el íleon terminal (cerca del 60% de los casos), seguido por íleon proximal, yeyuno y colon (2, 3). En un número menor de casos se produce en el duodeno causando obstrucción de la salida gástrica. Además del bloqueo intraluminal, la compresión duodenal extrínseca por distensión excesiva de la vesícula biliar con múltiples cálculos también puede ocasionar obstrucción de la salida gástrica, que se describe como síndrome de pseudo-Bouveret (6).
La sospecha clínica es esencial para el diagnóstico del síndrome de Bouveret, ya que tiene características clínicas inespecíficas. Existen informes que indican que la sintomatología más común incluye: náuseas, vómitos, dolor abdominal difuso en epigastrio y cuadrante superior derecho, pérdida de peso, anorexia, aumento de la sensibilidad abdominal, signos de deshidratación y distensión abdominal. Además de la obstrucción de la salida gástrica, el cálculo biliar impactado puede causar perforación duodenal secundaria a necrosis por compresión, hematemesis debido a síndrome de Mallory-Weiss, rotura esofágica distal debido a vómitos intensos repetidos (síndrome de Boerhaave) y formación de bezoares gástricos (7, 8).
Las modalidades de imágenes permiten que el diagnóstico sea relativamente sencillo. La radiografía simple de abdomen tiene bajo valor diagnóstico y es relativamente inespecífica en casos de síndrome de Bouveret (4, 7). La presencia de obstrucción del intestino delgado y estómago dilatado, neumobilia (aire en el árbol biliar) y cálculos biliares ectópicos, conocido como tríada de Rigler, pueden sugerir el diagnóstico en 10% - 50% de los casos. (1, 7). Los niveles de líquido aire doble en el cuadrante superior derecho, que representan el estómago y la vesícula biliar, también puede sugerir la presencia de fístula bilioentérica. La ecografía permite realizar el diagnóstico en 60% de los casos al mostrar estómago lleno de líquido, evidencia de colecistitis crónica, cálculo biliar calcificado ectópico, neumobilia y signo de doble arco, pero puede ser técnicamente difícil de realizar e interpretar, debido a la distensión intestinal o aire dentro de la vesícula biliar (8, 9). El cálculo biliar de gran tamaño puede detectarse; no obstante, la ubicación precisa (ectópica u ortotópica) puede ser difícil de establecer, especialmente cuando la vesícula biliar se descomprime o contrae. La fístula bilioentérica puede visualizarse directamente, pero en ocasiones se confunde con el conducto biliar común si no se considera en el momento del estudio (10).
Las imágenes de tomografía computada abdominal con contraste también pueden ser útiles para establecer el diagnóstico del síndrome de Bouveret, ya que puede definir la presencia de la tríada de Rigler. Sin embargo, en 15% - 25% de los casos, el cálculo biliar puede quedar oculto por líquido o bilis circundante en el duodeno (10, 11). En esos casos, la colangiopancreatografía por resonancia magnética es la modalidad de diagnóstico más efectiva, ya que permite delinear el cálculo y detectar los trayectos fistulosos. También es útil en pacientes con alergia al contraste oral. La endoscopia gastrointestinal superior permite identificar la causa exacta de la obstrucción de la salida gástrica y establecer las características macroscópicas del cálculo biliar impactado, pero este es visible solamente en 70% de los casos, probablemente porque la mucosa puede recubrirlo (8, 9, 12).
Las opciones terapéuticas para tratar el síndrome de Bouveret incluyen endoscopia, cirugía laparoscópica o abierta. El objetivo terapéutico primordial es aliviar la obstrucción mediante la eliminación del cálculo. El tratamiento endoscópico se considera la opción terapéutica de primera línea en pacientes con alto riesgo de complicaciones perioperatorias, a pesar que tiene una tasa de éxito baja (aproximadamente el 10%). En general, la tasa de éxito depende del tamaño del cálculo, ya que aquellos de más de 2,5 centímetros de diámetro son difíciles de extraer (13). Aquellos cálculos biliares densamente adheridos al duodeno pueden necesitar fragmentación in situ con litotricia de onda de choque extracorpóreo, mecánico o con ayuda de láser previo a la recuperación endoscópica (12). No obstante, uno de los inconvenientes de este método es que el cálculo fragmentado puede producir obstrucción distal, incrementando las posibilidades de cirugía (14).
La cirugía es necesaria en 90% de los pacientes. La enterolitotomía laparoscópica es una técnica útil en pacientes de edad avanzada con comorbilidades (15). Sin embargo, la cirugía abierta es una opción luego del fracaso de la endoscopia para retirar el cálculo, migración distal o falta de disponibilidad, conocimientos y/o instalaciones para realizar el procedimiento laparoscópico. La cirugía consiste en laparotomía, duodenotomía longitudinal, remoción del cálculo y cierre transversal de la duodenotomía en forma de piloroplastia (3, 15). Algunos autores recomiendan realizar la colecistectomía y la reparación de la fístula bilioentérica en una cirugía posterior en pacientes con comorbilidades significativas o en estado crítico. En muchas ocasiones el cierre de la fistula puede producirse espontáneamente, en especial cuando el conducto cístico es amplio - permeable y no existen cálculos en la vesícula biliar (2, 14, 15).
En conclusión, el síndrome de Bouveret es una complicación extremadamente rara de la colelitiasis y la fístula biliar que puede presentar desafíos diagnósticos y terapéuticos para los médicos tratantes, principalmente debido a su baja frecuencia y manifestaciones clínicas inespecíficas. El manejo endoscópico y quirúrgico de este proceso es importante para los pacientes.
Referencias
1. Yu YB, Song Y, Xu JB, Qi FZ. Bouveret's syndrome: A rare presentation of gastric outlet obstruction. Exp Ther Med. 2019; 17(3): 1813-1816. [PubMed] [Google Scholar]
2. Gallego Otaegui L, Sainz Lete A, Gutiérrez Ríos RD, Alkorta Zuloaga M, Arteaga Martín X, Jiménez Agüero R, Medrano Gómez MÁ, Ruiz Montesinos I, Beguiristain Gómez A. A rare presentation of gallstones: Bouveret´s syndrome, a case report. Rev Esp Enferm Dig. 2016; 108(7): 434-6. [PubMed] [Google Scholar]
3. Palomeque-Jiménez A, Calzado-Baeza S, Reyes-Moreno M. Bouveret syndrome: an infrequent presentation of gallstone ileus. Rev Esp Enferm Dig. 2012; 104(6): 324-5. [PubMed] [Google Scholar]
4. Al-Habbal Y, Ng M, Bird D, McQuillan T, Al-Khaffaf H. Uncommon presentation of a common disease - Bouveret's syndrome: A case report and systematic literature review. World J Gastrointest Surg. 2017; 9(1): 25-36. [PubMed] [Google Scholar]
5. Englert ZP, Love K, Marilley MD, Bower CE. Bouveret syndrome: gallstone ileus of the duodenum. Surg Laparosc Endosc Percutan Tech. 2012; 22(5): e301-3. [PubMed] [Google Scholar]
6. Reinhardt SW, Jin LX, Pitt SC, Earl TM, Chapman WC, Doyle MB. Bouveret's syndrome complicated by classic gallstone ileus: progression of disease or iatrogenic? J Gastrointest Surg. 2013; 17(11): 2020-4. [PubMed] [Google Scholar]
7. Marini M, Panyor G, Rubertà F, Marini AM, Zefelippo A, Avesani EC. Endoscopic versus surgical treatment for a rare form of gallstone ileus: Bouveret's syndrome. Two case reports and review of the literature. Ann Ital Chir. 2018; 89: 162-167. [PubMed] [Google Scholar]
8. Pickhardt PJ, Friedland JA, Hruza DS, Fisher AJ. Case report. CT, MR cholangiopancreatography, and endoscopy findings in Bouveret's syndrome. AJR Am J Roentgenol. 2003; 180(4): 1033-5. [PubMed] [Google Scholar]
9. Harmon L, Abernathy S, Regner J, Isbell T. An uncommon presentation of gastric outlet obstruction: Bouveret's Syndrome. Am Surg. 2016; 82(2): E49-51. [PubMed] [Google Scholar]
10. Kalwaniya DS, Arya SV, Guha S, Kuppuswamy M, Chaggar JG, Ralte L, Chejera R, Sharma A. A rare presentation of gastric outlet obstruction (GOO) - The Bouveret's syndrome. Ann Med Surg (Lond). 2015; 4(1): 67-71. [PubMed] [Google Scholar]
11. Gijón-de-la-Santa L, Camarero-Miguel A, Pérez-Retortillo JA, Ramia-Ángel JM. Bouveret's syndrome: evaluation with multidetector CT. Rev Esp Enferm Dig. 2014; 106(4): 283-4. [PubMed] [Google Scholar]
12. Avci A, Gögenur I, Bulut M. Bouveret's syndrome treated with endoscopic electrohydraulic lithotripsy. BMJ Case Rep. 2019; 12(2). pii: e228316. [PubMed] [Google Scholar]
13. Nickel F, Müller-Eschner MM, Chu J, von Tengg-Kobligk H, Müller-Stich BP. Bouveret's syndrome: presentation of two cases with review of the literature and development of a surgical treatment strategy. BMC Surg. 2013; 13: 33. [PubMed] [Google Scholar]
14. Yang D, Wang Z, Duan ZJ, Jin S. Laparoscopic treatment of an upper gastrointestinal obstruction due to Bouveret's syndrome. World J Gastroenterol. 2013; 19(40): 6943-6. [PubMed] [Google Scholar]
15. Chang KC, Chen WM, Wei KL. Endoscopic treatment of Bouverets syndrome in an extremely elderly patient with Holmium: YAG laser. Ann Saudi Med. 2016; 36(6): 436-439. [PubMed] [Google Scholar]
Información adicional
Conflictos de Interes: Los autores declaran no tener ningún conflicto de interés.