Artículos Originales
Factores que afectan la densitometría óseo en niños y adolescentes obesos.
(Factors that affect bone densitometry in obese children and adolescents)
Factores que afectan la densitometría óseo en niños y adolescentes obesos.
Avances en Biomedicina, vol. 8, núm. 2, pp. 73-81, 2019
Universidad de los Andes

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 08 Septiembre 2019
Aprobación: 30 Abril 2020
Resumen: El objetivo de la investigación fue determinar los factores que afectan la densitometría ósea en niños y adolescentes obesos. La investigación se realizó entre enero de 2015 y mayo de 2019 y se seleccionaron 178 niños y adolescentes obesos que asistieron al Hospital San Vicente de Paul, Ibarra, Ecuador. Todos se sometieron a un examen físico completo (altura, peso y evaluación de la etapa puberal), determinación del porcentaje de grasa corporal y masa ósea de la columna lumbar (vértebras L2-L4) y fémur proximal (cuello del fémur y trocánter). No se encontraron diferencias significativas en edad, peso, altura, índice de masa corporal, porcentaje de grasa corporal total y distribución de cambios puberales entre niños y adolescentes de sexo femenino y masculino (p> 0.05). Las niñas y adolescentes tenían valores más altos de contenido mineral óseo lumbar en comparación con los niños y adolescentes varones (p <0.001). Se observaron correlaciones positivas y significativas entre los parámetros antropométricos y el porcentaje de grasa corporal con el área, el contenido mineral óseo, la densidad mineral ósea y la longitud de la columna vertebral y el fémur proximal (p <0,05). El sexo femenino, el aumento de la edad y el progreso de los cambios puberales se asociaron con cambios en el contenido mineral óseo y la densidad de la columna lumbar, el cuello femoral y el trocánter (p <0,05). Se concluye que la edad, el sexo y los cambios en la pubertad pueden afectar independientemente la densitometría ósea de la columna lumbar y el fémur en niños y adolescentes obesos.
Palabras clave: Obesidad, Niños, Adolescentes, Densitometría ósea.
Abstract: The objective of the research was to determine factors that affect bone densitometry in obese children and adolescents. The research was conducted between January 2015 and May 2019 and 178 obese children and adolescents were selected who attended to Hospital San Vicente de Paul, Ibarra, Ecuador. All underwent a complete physical examination (height, weight, and evaluation of the pubertal stage), determination of the percentage of body fat and bone mass of the lumbar spine (L2-L4 vertebrae) and proximal femur (neck of the femur and trochanter). No significant differences were found in age, weight, height, body mass index, percentage of total body fat and distribution of pubertal changes among children and adolescents of female and male sex (p > 0.05). Female girls and adolescents had higher values of lumbar bone mineral content compared to male boys and adolescents (p < 0.001). Positive and significant correlations were observed between anthropometric parameters and percentage of body fat with the area, bone mineral content, bone mineral density, and length of the spine and proximal femur (p < 0.05). Female sex, age increase, and progress pubertal changes were associated with changes in bone mineral content and density of the lumbar spine, femoral neck and trochanter (p < 0.05). It is concluded that age, sex, and pubertal changes can independently affect the bone densitometry of the lumbar spine and femur in obese children and adolescents.
Keywords: Obesity, Children, Adolescents, Bone mineral density, bone mineral content, Densitometry.
Introducción
La osteoporosis es un problema de salud cada vez más frecuente en el mundo. Existe consenso general que aquellos sujetos que pueden alcanzar la masa ósea máxima más alta posible presentan menor riesgo de sufrir fracturas osteoporóticas al envejecer (1). Diferentes estudios han demostrado que la masa ósea máxima se alcanza entre el final de la primera e inicio de la segunda década de vida y en las mujeres ese momento posiblemente ocurre antes que en los hombres (2).
Los estudios de los efectos de la obesidad infantil sobre la masa ósea total han llegado a conclusiones contradictorias, en gran parte relacionadas a los diferentes enfoques utilizados para evaluar las mediciones por densitometría ósea con respecto a edad, tamaño del hueso y peso - talla de los niños y adolescentes. Algunos estudios han demostrado que contenido óseo puede ser normal (3) o estar aumentado en niños y jóvenes obesos (4), mientras que otras investigaciones concluyeron que los niños obesos presentan disminución de la masa ósea total en relación con su talla - peso corporal (5).
La necesidad de evaluaciones más precisas de los potenciales efectos de la obesidad sobre la el contenido de minerales óseos y la densidad ósea está basada en informes con resultados opuestos sobre los efectos del aumento de la masa corporal total y el índice de masa corporal durante la infancia y adolescencia sobre el riesgo de fracturas en la vida adulta (6,7). El objetivo de este estudio fue determinar los factores que afectan la densitometría ósea en niños y adolescentes obesos.
Materiales y métodos
Selección de pacientes.
Se realizó un estudio prospectivo, transversal con un diseño cuasi-experimental entre enero de 2015 y mayo de 2019 para el cual fueron seleccionados 178 niños y adolescentes obesos con edades comprendidas entre 7 y 16 años que asistieron a las consultas de Endocrinología, Nutrición - Dietética y Pediatría del Hospital San Vicente de Paúl, Ibarra, Ecuador. Solo se incluyeron participantes con obesidad simple, sin causa orgánica, en buen estado físico, con exposición normal a la luz solar. Los niños y adolescentes fueron considerados obesos si presentaban valores del índice de masa corporal superior al percentil 95 según las tablas de crecimiento. Se obtuvo consentimiento informado de los padres / representantes a quienes se les explico sobre los riesgos y beneficios del estudio. La investigación fue aprobada por el Comité de Ética del Hospital.
Se excluyeron aquellos niños y adolescentes que presentaban antecedentes de trastornos metabólicos, endocrinos o cualquier otra patología conocida que pudiera afectar el metabolismo óseo (enfermedad renal, hepática, diarrea crónica o cirugía gastrointestinal), que no hubiesen sido tratados con regímenes dietéticos para la reducción de peso antes del estudio. También fueron excluidos niños y adolescentes que recibieran suplementación con vitamina D o calcio en los 6 meses previos al estudio y aquellos que tomaban medicamentos que afectan el metabolismo óseo (antiepilépticos, rifampicina, colestiramina o tratamiento crónico con esteroides).
Mediciones antropométricas y de densitometría ósea.
A todos los participantes se les realizó examen físico completo que incluyó la medición de talla, peso, porcentaje de grasa corporal y evaluación de la etapa puberal. El peso (Kilogramos) fue medido al 0, 5 kg más cercano mientras el sujeto usaba ropa ligera sin zapatos, con el uso de una balanza clínica estándar (SECA® 704s, Alemania). La altura (centímetros) fue medida usando estadiómetro al 0,1 centímetro más cercano montado en la pared mientras el sujeto estaba parado sin zapatos. El índice de masa corporal se calculó con la formula índice de masa corporal peso (Kg) / altura (m2). El estado puberal fue clasificado según el método de Tanner (8).
| Promedio +/- Niñas y Niños y p desviación estándar Adolescentes Adolescentes femeninas masculinos (n = 89) (n = 89) Edad (años) 12,75 +/- 3,2 11,82 +/- 4,3 0,1150 Peso (Kilogramos) 71,3 +/- 29,2 73,2 +/- 20,9 0,6183 Talla (centímetros) 147,7 +/- 13,9 151,4 +/- 17,7 0,1227 Indice de masa corporal (Kg/m2) 35,3 +/- 5,2 36,6 +/- 5,6 0,1103 Porcentaje de grasa corporal 40,7 +/- 8,1 38,6 +/- 9,6 Escala de Tanner, n(%) 1 36 (40,4) 35 (39,3) 2 12 (13,4) 15 (16,8) 3 11 (12,3) 13 (14,6) 0,9383 4 7 (7,8) 5 (5,6) 5 23 (25,8) 21 (23,5) |
El porcentaje de grasa corporal fue medido usando un monitor de grasa corporal (Omron®-BF306, Alemania). Todas las mediciones se realizaron de acuerdo con las instrucciones del fabricante. La masa ósea en la columna lumbar anteroposterior (vértebras lumbares L2-L4) y del fémur proximal (cuello del fémur y trocánter) fue medida utilizando densitometría ósea con combinación de lápiz y haz de abanico con software pediátrico adaptado por el fabricante (Discovery® QDR®, Hologic, EE.UU.). Las mediciones de densitometría se analizaron para generar medidas del área ósea lumbar y de cadera proyectada (cm2), contenido mineral óseo (gramos) y densidad mineral ósea en el área (g/cm2). La densidad mineral ósea de la columna lumbar y fémur, que se calculó como contenido mineral óseo / área ósea, se utilizó como estimación de la densidad mineral ósea volumétrica (9). Todas las mediciones en los sujetos fueron realizadas en las máquinas previamente citadas utilizando las técnicas de posicionamiento estandarizadas.
Análisis estadístico
Los datos de la investigación se presentan como valores absolutos (promedio +/- desviación estándar) y relativos (porcentajes). Para la evaluación estadística los participantes fueron divididos de acuerdo al sexo. Las comparaciones fueron realizadas con la prueba t de Student para muestras independientes o no relacionadas. La prueba de correlación de Pearson fue utilizada para establecer la correlación entre las variables de absorciometría ósea con las variables antropométricas. Las pruebas de regresión logística múltiple permitieron realizar un modelo para evaluar cuales factores podían afectar el contenido y la densidad mineral ósea de cada una de las regiones estudiadas. La significancia estadística fue fijada en p < 0,05. Todos los análisis fueron realizados utilizando el programa estadístico SPSS para Windows versión 22.
Resultados
Las características de los participantes seleccionados para la investigación se muestran en la tabla 1. No se encontraron diferencias estadísticamente significativas en edad, peso, talla e índice de masa corporal entre niños y adolescentes de sexo femenino y sexo masculino (p > 0,05). Tampoco se encontraron diferencias significativas en el porcentaje de grasa corporal total y en la distribución del estado puberal evaluado por la escala de Tanner (p> 0,05).
Con respecto a las mediciones óseas por densitometría entre los participantes femeninos y masculinos (tabla 2), se observó que las niñas y adolescentes femeninas tenían un menor puntaje Z de columna vertebral, mientras que el puntaje Z de cadera era mayor comparado con niños y adolescentes masculinos. No obstante, estas diferencias no fueron significativas (p = 0,1122 y p = 0,2435, respectivamente). Las niñas y adolescentes femeninas presentaron valores significativamente más altos de contenido mineral óseo comparado con niños y adolescentes masculinos (31,5 +/- 12,9 comparado con 24,3 +/- 7,3; p < 0,001). El resto de las mediciones de columna vertebral, cuello de fémur y trocánter no mostraron diferencias entre los grupos (p > 0,05).
| Promedio +/- | Niñas y | Niños y | p |
| desviación estándar | adolescentes | adolescentes | |
| femeninas | masculinos | ||
| (n = 89) | (n = 89) | ||
| COLUMNA LUMBAR | |||
| Puntaje Z | 0,22 +/- 0,24 | 0,32 +/- 0,54 | 0,1122 |
| Área L2-L4 (cm2) | 35,9 +/- 6,9 | 37,5 +/- 5,6 | 0,0912 |
| Contenido mineral ósea L2-L4 (g) | 31,5 +/- 12,9 | 24,3 +/- 7,3 | 0,0001 |
| Densidad mineral ósea L2-L4 (g/cm2) | 0,78 +/- 0,21 | 0,63 +/- 0,14 | 0,0633 |
| Longitud L2-L4, cm | 8,8 +/- 1,2 | 8,6 +/- 1,1 | 0,2480 |
| CADERA | |||
| Puntaje Z | 2,2 +/- 0,4 | 2,1 +/- 0,7 | 0,2435 |
| Área de la cuello del fémur (cm2) | 4,3 +/- 0,9 | 4,5 +/- 1,1 | 0,1088 |
| Contenido mineral óseo del cuello del fémur (g) | 3,7 +/- 1,3 | 4,0 +/- 1,1 | 0,0983 |
| Densidad mineral ósea del cuello del fémur (g/cm2) | 0,83 +/- 0,16 | 0,81 +/- 0,12 | 0,3468 |
| Longitud del cuello del fémur, cm | 1,43 +/- 0,21 | 1,37 +/- 0,20 | 0,0525 |
| Área del trocánter (cm2) | 9,3 +/- 3,7 | 8,6 +/- 3,6 | 0,2025 |
| Contenido mineral óseo del trocánter (g) | 6,9 +/- 3,8 | 6,1 +/- 1,9 | 0,0774 |
| Densidad mineral ósea del trocánter (g/cm2) | 0,72 +/- 0,11 | 0,70 +/- 0,12 | 0,2480 |
Con respecto a las correlaciones entre las medidas antropométricas y las mediciones óseas (tabla 3) se observaron correlaciones positivas entre el índice de masa corporal y el porcentaje de grasa corporal con área, contenido mineral óseo, densidad mineral ósea y longitud de columna lumbar, cuello del fémur y trocánter (p < 0,05). La única correlación que no fue significativa fue la correlación entre área de la columna lumbar y porcentaje de grasa corporal (r = 0,101; p > 0,05).
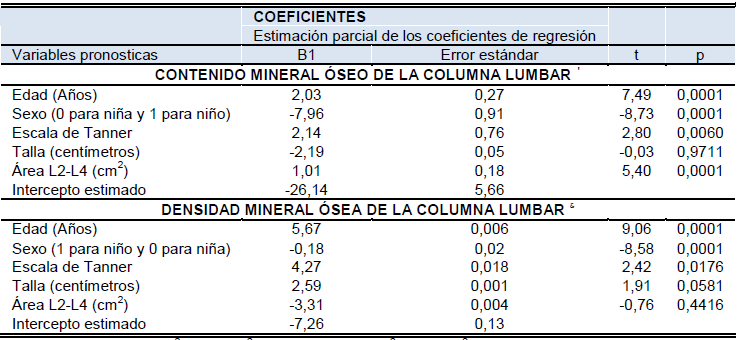
Para realizar el modelo de regresión múltiple fueron incluidas todas las variables edad, sexo, escala de Tanner, talla y área de las vértebras lumbares L2-L4 para la densidad y contenido mineral óseo de la columna vertebral y área del cuello y del trocánter para la densidad y contenido mineral óseo de fémur. En las tablas 4, 5 y 6 se muestran los modelos resultantes. El sexo femenino puede modificar el contenido y densidad mineral ósea de la columna lumbar (p < 0,0001), contenido mineral óseo del cuello del fémur (p = 0,0318) y densidad mineral ósea del trocánter, respectivamente (p = 0,0111). El aumento de la edad también puede modificar el aumento de la densitometría ósea de la columna lumbar y del trocánter (p < 0,0001). El progreso del estado puberal puede explicar los cambios en el contenido y densidad mineral ósea de columna vertebral (p = 0,0060 y p = 0,0176, respectivamente) y del trocánter (p < 0,0001 y p = 0,0016, respectivamente). La talla no presentó ningún efecto en la predicción de la densitometría ósea de la columna lumbar, cuello del fémur y trocánter (p > 0,05).
| Indice de masa corporal | Porcentaje de grasa corporal | |
| COLUMNA LUMBAR Área L2-L4 | 0,421* | 0,101 |
| Contenido mineral óseo | 0,629* | 0,288* |
| Densidad mineral ósea | 0,563* | 0,353* |
| Longitud L2-L4 | 0,574* | 0,481* |
| CADERA Área de la cuello del fémur | 0,361* | 0,368* |
| Contenido mineral óseo del cuello del fémur | 0,519* | 0,393* |
| Densidad mineral ósea del cuello del fémur | 0,497* | 0,251* |
| Longitud del cuello del fémur | 0,516* | 0,412* |
| Área del trocánter | 0,393* | 0,170* |
| Contenido mineral óseo del trocánter | 0,582* | 0,309* |
| Densidad mineral ósea del trocánter | 0,495* | 0,431* |
Coeficiente de correlación de Pearson. * p < 0,05.
R2 = 0,89, R2 ajustado = 0,86. & R2 = 0,85, R2 ajustado = 0,82
Discusión
Los resultados de la presente investigación demuestran que factores como la edad, sexo, cambios puberales pueden afectar la densitometría ósea de la columna lumbar y el fémur en niños y adolescentes obesos. Durante la infancia y adolescencia, la acumulación de mineral óseo es el resultado de aumentos específicos relacionados al sexo y la maduración en las dimensiones corticales y la densidad trabecular (10-12). Las personas con masa ósea máxima más alta después de la adolescencia tienen ventajas protectoras cuando las pérdidas en la masa ósea que se asocian con el aumento de la edad aumentando el riesgo de fracturas. La masa ósea máxima está fuertemente asociada a factores genéticos, pero este potencial genético para alcanzar la máxima masa ósea solo puede alcanzarse si se optimizan nutrición, actividad física y otros factores del estilo de vida (2).
En la infancia, y a medida que aumenta la edad, existe aumento en la densitometría ósea relacionado al crecimiento y la producción de hormona del crecimiento. Durante la pubertad, las concentraciones de hormona del crecimiento y de esteroides sexuales aumentan y ambos tienen efectos positivos en la densitometría ósea, contribuyendo a la acumulación de material (13,14). Además, existen mecanismos potenciales que intervienen en los cambios de la masa ósea en niños y jóvenes obesos. Factores hormonales, como el aumento de las concentraciones circulantes de leptina o el incremento en la conversión periférica de androstenediona a estrógenos, pueden tener algún papel en las modificaciones descritas (15). La leptina actúa como un factor de crecimiento en los condrocitos ubicados en los centros de crecimiento esquelético, a través de la expresión del receptor del factor de crecimiento I similar a la insulina. Por lo tanto, puede contribuir, en forma potencial, al crecimiento lineal e incremento de la masa esquelética observada en la obesidad infantil (16). La influencia de la pubertad sobre la densidad mineral ósea es mayor en niñas que en niños. Estudios en animales demostraron un papel más importante de los estrógenos que de los andrógenos en la mineralización del esqueleto (13). Los estrógenos son un determinante fundamental de la densidad mineral ósea en las niñas durante la pubertad, ya que promueven la acumulación de masa ósea en la superficie endosteal y en el hueso trabecular. Además, tanto los estrógenos como los andrógenos estimulan la absorción y retención de calcio, dando como resultado un balance neto positivo en el hueso, lo que contribuye a la acumulación en el hueso (17).
| COEFICIENTES | ||||
| Estimación parcial de los coeficientes de regresión | ||||
| Variables pronosticas | B1 | Error estándar | t | p |
| CONTENIDO MINERAL ÓSEO DEL CUELLO DEL FÉMUR ' | ||||
| Edad (Años) | -5,46 | 0,07 | -0,76 | 0,4410 |
| Sexo (0 para niña y 1 para niño) | -0,30 | 0,14 | -2,10 | 0,0381 |
| Escala de Tanner | 0,10 | 0,15 | 0,68 | 0,4958 |
| Talla (centímetros) | 7,57 | 0,01 | 0,62 | 0,5302 |
| Área del cuello del fémur (cm2) | 1,05 | 0,16 | 6,28 | 0,0001 |
| Intercepto estimado | -1,55 | 1,40 | ||
| DENSIDAD | MINERAL ÓSE | A DEL CUELLO DEL FÉMUR & | ||
| Edad (Años) | -1,02 | 0,01 | -0,70 | 0,4812 |
| Sexo (1 para niño y 0 para niña) | -5,60 | 0,02 | -1,91 | 0,0590 |
| Escala de Tanner | 3,36 | 0,03 | 1,04 | 0,3005 |
| Talla (centímetros) | -2,22 | 0,01 | -0,01 | 0,9931 |
| Área del cuello del fémur (cm2) | 7,33 | 0,03 | 2,13 | 0,0325 |
| Intercepto estimado | 0,57 | 0,28 | ||
R2 = 0,80, R2 ajustado = 0,78. & R2 = 0,33, R2 ajustado = 0,31.
Los resultados de este estudio confirman el papel conocido de variables como edad, estadio puberal y sexo en los valores de densitometría ósea en niños y adolescentes (12,18). Las diferencias entre estos resultados pueden deberse probablemente a la elección de las variables para evaluar el tamaño y porcentaje de tejido graso corporal total en esas investigaciones. Una investigación no reportó diferencias en las mediciones óseas al comparar sujetos obesos con controles después del ajuste por talla, peso, masa muscular y masa grasa (10). Otro estudio comparó tanto el contenido mineral como la densidad mineral ósea con relación al peso de niños con sobrepeso y obesidad y no encontró que estos parámetros se adaptaran al aumento del peso corporal en ese grupo de sujetos estudiados (11). No obstante, son necesarios más estudios para determinar el efecto de estas diferencias en el riesgo de fractura y si los cambios en el contenido mineral óseo de la columna vertebral y la cadera persisten en la edad adulta.
Las diferencias entre sexos de la distribución de grasa regional (subcutánea o visceral) también pueden producir efectos sobre las mediciones óseas por densitometría (19). En este estudio, esto no se observó diferencias en los valores óseos regionales entre niñas y niños, excepto en la columna vertebral, en las cuales las niñas presentaron contenido mineral óseo significativamente más alto. La ausencia de diferencias puede atribuirse a las características de los participantes seleccionados, en los cuales las similitudes en talla y desarrollo puberal no estaba asociadas a la influencia hormonal marcada en la distribución grasa de ambos sexos.
El aumento del contenido de minerales óseos es importante en la producción de las fracturas. Estudios sobre el efecto del porcentaje de grasa total y el índice de masa corporal sobre el riesgo de fracturas han presentado resultados contradictorios (20). Mientras que el aumento del contenido mineral óseo parece ser benéfico y está asociada a disminución del riesgo de osteoporosis, algunos investigadores lo consideran un factor de riesgo para fracturas óseas. Estudios de biomecánica ósea en ratas macho adultas con obesidad inducida por la dieta demostró mayor resistencia ósea comparado con ratas no obesas controles. Además, la geometría de la sección transversal y la carga de fractura final del fémur fueron mayores en las ratas obesas que en los controles (21). El aumento de las cargas biomecánica secundaria tanto al aumento del peso corporal como al incremento de las fuerzas mecánicas musculares, pueden contribuir al aumento de las dimensiones y masa ósea observadas en los sujetos obesos. Este aumento de la carga sobre los huesos largos lleva a mayor estrés mecánico sobre la superficie y estimula la formación de hueso por expansión subperióstica (22).
El efecto del exceso de peso sobre la carga mecánica ósea ha sido evaluado en adultos. Un estudio longitudinal en menopáusicas demostró que las mujeres con exceso de peso experimentaron aumento significativo en la porción cortical de la cadera por expansión perióstica (23). Otro estudio en niños sanos sugirió que la carga de peso y las tensiones mecánicas son determinantes de la masa ósea cortical, mientras que la densidad ósea trabecular está afectada por factores hormonales asociados al
Tabla 6. Modelo de regresión múltiple de las mediciones oseas por densitometria del cuello del fémur con otras variables.
| Variables pronosticas | B1 | Error estándar | t | p |
| C | CONTENIDO MINE | RAL ÓSEO DEL TROCÁNTER ' | ||
| Edad (Años) | 0,41 | 0,11 | 3,51 | 0,0015 |
| Sexo (0 para niña y 1 para niño) | -0,61 | 0,31 | -1,93 | 0,0562 |
| Escala de Tanner | 0,98 | 0,26 | 3,71 | 0,0001 |
| Talla (centímetros) | -2,09 | 0,02 | -0,83 | 0,4010 |
| Área del cuello del trocánter (cm2) | 0,91 | 0,09 | 9,27 | 0,0001 |
| Intercepto estimado | -1,09 | 2,35 | ||
| DENSIDAD MINE | RAL ÓSEA DEL TROCÁNTER & | |||
| Edad (Años) | 2,86 | 0,01 | 3,04 | 0,0031 |
| Sexo (1 para niño y 0 para niña) | -6,62 | 0,02 | -2,60 | 0,0111 |
| Escala de Tanner | 7,04 | 0,02 | 3,29 | 0,0016 |
| Talla (centímetros) | 4,31 | 0,01 | 2,12 | 0,0374 |
| Área del cuello del trocánter (cm2) | -4,42 | 0,01 | -0,55 | 0,5841 |
| Intercepto estimado | -4,98 | 0,91 | ||
R2 = 0,84, R2 ajustado = 0,83. & R2 = 0,34, R2 ajustado = 0,31.
desarrollo sexual (24). Algunos estudios en niños y jóvenes obesos han propuesto que este aumento del contenido mineral óseo aumenta la resistencia ósea, pero es insuficiente para superar las fuerzas significativamente superiores generadas cuando, por ejemplo, un niño obeso cae sobre el brazo extendido (7).
Una de las deficiencias técnicas de la densitometría ósea está relacionada con el error potencial de las proyecciones al momento de la evaluación de las medidas óseas en población infantil y adolescente, especialmente en la columna vertebral. El esqueleto está compuesto de estructuras en forma tubular (extremidades) y anchas (pelvis) que varían en profundidad y grosor. La medición del área de superficie ósea es poco eficiente para calcular el volumen sobre el cual se distribuye el contenido mineral óseo. El área ósea medida por densitometría es la función de la talla del sujeto y el ancho del hueso. Este hecho debe tenerse en cuenta, ya que los huesos de los niños no crecen y modelan de forma uniforme, lo que puede llevar a sesgos de estimación en niños con mayor talla al compararlos con aquellos de menor talla (25). Para evitar este error, en esta investigación fueron utilizados los valores de densidad mineral ósea, además del contenido mineral óseo como medidas de medición primarias para expresar la cantidad de masa ósea en el esqueleto en crecimiento. El uso de equipos y programas adaptados a niños minimizo estas potenciales fuentes de error.
Una de las limitaciones de esta investigación es que la edad ósea, la cual es un predictor importante de la madurez esquelética y de la masa ósea total, no fue evaluada. En niños, el aumento de la densidad mineral ósea está afectado por el crecimiento y por la cantidad de tejido blando que rodea al hueso, otra variable que cambia en forma significativa con el crecimiento. Aunque el uso de la tomografía computarizada para medir la masa ósea corregiría este problema, la densitometría continúa siendo la técnica más conveniente para evaluar la masa ósea total en niños, debido al corto periodo de exploración y a la baja dosis de radiación utilizada. Aunque se ha sugerido que el uso de contenido mineral óseo evaluado por densitometría, sin corrección de tamaño, es superior para evaluar la masa ósea (26), esto es controversial y no es el procedimiento utilizado en los estudios en población pediátrica (27,28).
En conclusión y sobre la base de los hallazgos de esta investigación, se puede concluir que la edad, sexo y cambios puberales pueden afectar en forma independiente la densitometría ósea de la columna lumbar y fémur en niños y adolescentes obesos.
Referencias
1. Maggio ABR, Martin X, Tabard-Fougère A, Steiger C, Dayer R, Delhumeau C, Ceroni D. Recovery of bone mineral mass after upper limb fractures in children and teenagers. J Pediatr Orthop. 2019; 39: e248-e52. [PubMed] [Google Scholar]
2. Cvijetic S, Baric IC, Satalic Z, Keser I, Bobic J. Influence of nutrition and lifestyle on bone mineral density in children from adoptive and biological families. J Epidemiol. 2014; 24: 209-15. [PubMed] [Google Scholar]
3. Faienza MF, D'Amato G, Chiarito M, Colaianni G, Colucci S, Grano M, Corbo F, Brunetti G. Mechanisms Involved in Childhood Obesity-Related Bone Fragility. Front Endocrinol (Lausanne). 2019; 10: 269. [PubMed] [Google Scholar]
4. Leonard MB, Shults J, Wilson BA, Tershakovec AM, Zemel BS. Obesity during childhood and adolescence augments bone mass and bone dimensions. Am J Clin Nutr. 2004; 80: 514-23. [PubMed] [Google Scholar]
5. Hanusch BC, Tuck SP, McNally RJQ, Wu JJ, Prediger M, Walker J, Tang J, Piec I, Fraser WD, Datta HK, Francis RM. Does regional loss of bone density explain low trauma distal forearm fractures in men (the Mr F study)? Osteoporos Int. 2017; 28: 2877-2886. [PubMed] [Google Scholar]
6. Goulding A, Jones IE, Taylor RW, Williams SM, Manning PJ. Bone mineral density and body composition in boys with distal forearm fractures: a dual- energy x-ray absorptiometry study. J Pediatr. 2001; 139: 509-15. [PubMed] [Google Scholar]
7. Skaggs DL, Loro ML, Pitukcheewanont P, Tolo V, Gilsanz V. Increased body weight and decreased radial cross- sectional dimensions in girls with forearm fractures. J Bone Miner Res. 2001; 16: 1337-42. [PubMed] [Google Scholar]
8. Leite Portella D, Arruda M, Gómez- Campos R, Checkin Portella G, Andruske CL, Cossio-Bolaños MA. Physical growth and biological maturation of children and adolescents: Proposed reference curves. Ann Nutr Metab. 2017; 70: 329-37. [PubMed] [Google Scholar]
9. Chun KJ. Bone densitometry. Semin Nucl Med. 2011; 41: 220-8. [PubMed] [Google Scholar]
10. Manzoni P, Brambilla P, Pietrobelli A, Beccaria L, Bianchessi A, Mora S, Chiumello G. Influence of body composition on bone mineral content in children and adolescents. Am J Clin Nutr. 1996; 64: 603-7. [PubMed] [Google Scholar]
11. El Hage Z, Theunynck D, Jacob C, Moussa E, Baddoura R, Zunquin G, El Hage R. Bone mineral content and density in obese, overweight and normal weight adolescent boys. J Med Liban. 2013; 61: 148-54. [PubMed] [Google Scholar]
12. Zemel B. Bone mineral accretion and its relationship to growth, sexual maturation and body composition during childhood and adolescence. World Rev Nutr Diet. 2013; 106: 39-45. [PubMed] [Google Scholar]
13. Rochira V, Kara E, Carani C. The endocrine role of estrogens on human male skeleton. Int J Endocrinol. 2015; 2015: 165215. [PubMed] [Google Scholar]
14. Ward KA, Roberts SA, Adams JE, Mughal MZ. Bone geometry and density in the skeleton of pre-pubertal gymnasts and school children. Bone. 2005; 36: 1012-8. [PubMed] [Google Scholar]
15. Reid IR, Baldock PA, Cornish J. Effects of leptin on the skeleton. Endocr Rev. 2018; 39: 938-59. [PubMed] [Google Scholar]
16. Kishida Y, Hirao M, Tamai N, Nampei A, Fujimoto T, Nakase T, Shimizu N, Yoshikawa H, Myoui A. Leptin regulates chondrocyte differentiation and matrix maturation during endochondral ossification. Bone. 2005; 37: 607-21. [PubMed] [Google Scholar]
17. Beck BR. Exercise for bone in childhood- hitting the sweet spot. Pediatr Exerc Sci. 2017; 29: 440-9. [PubMed] [Google Scholar]
18. Khadilkar AV, Sanwalka N, Mughal MZ, Chiplonkar S, Khadilkar V. Indian girls have higher bone mineral content per unit of lean body than boys through puberty. J Bone Miner Metab. 2018; 36: 364-71. [PubMed] [Google Scholar]
19. Arfai K, Pitukcheewanont PD, Goran MI, Tavare CJ, Heller L, Gilsanz V. Bone, muscle, and fat: sex-related differences in prepubertal children. Radiology. 2002; 224: 338-44. [PubMed] [Google Scholar]
20. Dennison EM, Harvey NC, Cooper C. Programming of osteoporosis and impact on osteoporosis risk. Clin Obstet Gynecol. 2013; 56: 549-55. [PubMed] [Google Scholar]
21. Bozzini C, Picasso EO, Champin GM, Alippi RM, Bozzini CE. Biomechanical properties of the mid-shaft femur in middle-aged hypophysectomized rats as assessed by bending test. Endocrine. 2012; 42: 411-8. [PubMed] [Google Scholar]
22. Takeda S. Osteoporosis: a neuroskeletal disease? Int J Biochem Cell Biol. 2009; 41: 455-9. [PubMed] [Google Scholar]
23. Kaptoge S, Dalzell N, Loveridge N, Beck TJ, Khaw KT, Reeve J. Effects of gender, anthropometric variables, and aging on the evolution of hip strength in men and women aged over 65. Bone. 2003; 32: 561-70. [PubMed] [Google Scholar]
24. Wren TA, Liu X, Pitukcheewanont P, Gilsanz V. Bone acquisition in healthy children and adolescents: comparisons of dual-energy x-ray absorptiometry and computed tomography measures. J Clin Endocrinol Metab. 2005; 90: 1925-8. [PubMed] [Google Scholar]
25. Fewtrell MS; British Paediatric & Adolescent Bone Group. Bone densitometry in children assessed by dual x ray absorptiometry: uses and pitfalls. Arch Dis Child. 2003; 88: 795-8. [PubMed] [Google Scholar]
26. Nakavachara P, Pooliam J, Weerakulwattana L, Kiattisakthavee P, Chaichanwattanakul K, Manorompatarasarn R, Chokephaibulkit K, Viprakasit V. A normal reference of bone mineral density (BMD) measured by dual energy X-ray absorptiometry in healthy thai children and adolescents aged 5-18 years: a new reference for Southeast Asian Populations. PLoS One. 2014; 9: e97218. [PubMed] [Google Scholar]
27. Kocks J, Ward K, Mughal Z, Moncayo R, Adams J, Högler W. Z-score comparability of bone mineral density reference databases for children. J Clin Endocrinol Metab. 2010; 95: 4652-9. [PubMed] [Google Scholar]
28. Timpson NJ, Sayers A, Davey-Smith G, Tobias JH. How does body fat influence bone mass in childhood? A Mendelian randomization approach. J Bone Miner Res. 2009; 24: 522-33. [PubMed] [Google Scholar]
Información adicional
Conflictos de interés: Declaración de aspectos éticos.Reconocimiento de autoría: Los autores declaramos que hemos realizado aportes a la idea, diseño del estudio, recolección de datos, análisis e interpretación de datos, revisión crítica del contenido intelectual y aprobación final del manuscrito que estamos enviando. Además, somos plenamente responsables de la información que en él se entrega. El material enviado no ha sido publicado en otra revista o publicación de índole científica, nacional o extranjera. Responsabilidades éticas: Protección de personas. Los autores declaramos que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki de 2004. Confidencialidad de los datos: Los autores declaramos que hemos seguido los protocolos establecidos por sus respectivos centros sanitarios para acceder a los datos de las historias clínicas del Hospital San Vicente de Paul, Ibarra, Ecuador, sobre la publicación de datos de pacientes. Derecho a la privacidad y consentimiento informado: Los autores hemos obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo a los fines de poder realizar este tipo de publicación con finalidad de investigación/divulgación en soporte papel y en Internet para la comunidad científica. Este documento obra en poder del autor de correspondencia. Financiamiento: Los autores certificamos que no hemos recibido apoyos financieros, equipos, en personal de trabajo o en especie de personas, instituciones públicas y/o privadas para la realización del estudio. Conflicto de intereses: Los autores declaramos no tener ningún conflicto de intereses.