Revisiones
Sustratos neuroanatómicos y funcionales del córtex prefrontal medial
Neuroanatomical and functional substrates of the medial prefrontal cortex.
Sustratos neuroanatómicos y funcionales del córtex prefrontal medial
Revista Argentina de Ciencias del Comportamiento, vol. 10, núm. 3, pp. 43-53, 2018
Universidad Nacional de Córdoba

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 17 Julio 2018
Aprobación: 10 Octubre 2018
Resumen: Este artículo se presenta como una revisión que buscó integrar el conocimiento actualizado que se tiene sobre los sustratos neuroanatómicos y morfológicos de los circuitos funcionales que el córtex prefrontal medial (mPFC) establece con otras estructuras cerebrales. Diversas investigaciones han descrito las proyecciones emergentes y/o convergentes del mPFC, principalmente tomando como modelo de estudio a los roedores; empleándose la técnica de marcador neuronal como principal técnica de indagación de tales proyecciones, seguido de trabajos que proponen electrofisiografía para develar la conectividad cerebral. Así, se ha descrito la interacción del mPFC con otras estructuras encefálicas, entre las que se destacan principalmente el hipocampo, la sustancia gris periacueductal, el hipotálamo, el núcleo accumbens, la amígdala cerebral, el área tegmental ventral, el núcleo dorsal de Rafe y la habénula lateral del epitálamo, entre otras. Estas investigaciones han ido más allá del componente físico de la conectividad encefálica, extrapolando y posibilitando la comprensión funcional de las vías anatómicas establecidas entre las diferentes regiones interrelacionadas con el mPFC, develando la actividad cognitivo-comportamental de los sujetos de estudio.
Palabras clave: comportamiento, córtex infralímbico, córtex prefrontal medial, córtex prelímbico.
Abstract: This article presents how a revision that was done sought out to integrate the updated knowledge that we have about neuroanatomical and morphological substrates of the functional circuits that the medial prefrontal cortex (mPFC) establishes with other brain structures. Several investigations have described the emergent and/or convergent projections of the mPFC, mainly taking rodents as a study model; using the technique of neuronal marker as the main technique of inquiry to reveal such projections, followed by works that propose electrophysiography to reveal the cerebral connectivity. Thus, the interaction of the mPFC with other brain structures has been described, among which the hippocampus, the periaqueductal gray matter, the hypothalamus, the nucleus accumbens, the cerebral amygdala, the ventral tegmental area, the dorsal nucleus of Rafe and the lateral habenula of the epithalamus, among others. These investigations have gone beyond the physical component of brain connectivity, extrapolating and enabling the functional understanding of the anatomical pathways established between the different regions interrelated with the mPFC, revealing the cognitive-behavioral activity of the study subjects.
Keywords: behavior, infralimbic cortex, medial prefrontal cortex, prelimbic cortex.
Introducción
A lo largo del último cuarto de siglo se han dado progresos significativos en el estudio de las bases biológicas del comportamiento, tanto en modelos animales como humanos. Para esto, grandes avances científicos han acontecido en la comprensión de la estructura anatómica del individuo y las interacciones de los diversos componentes bioquímicos y fisiológicos que lo componen, ampliándose el conocimiento en campos de estudio como la genética, la biología celular y molecular, y con avances relevantes en el desglose y desarticulación de la estructura del sistema nervioso central (SNC), así como las interacciones y correlatos morfo-funcionales de este sistema.
Para llegar al conocimiento de estos mecanismos biológicos, durante los últimos años se han llegado a perfeccionar, con eficiencia y eficacia, las técnicas de estudio desarrolladas décadas atrás y se han propuesto nuevos métodos y modelos de análisis de los datos recolectados; es así que, han surgido y evolucionado las neuroimágenes modernas, la optimización de la electroencefalografía, la electrofisiografía, la estimulación magnética transcraneal y los marcadores químicos de trazado neuronal, entre otros; acompañados de diversas técnicas de laboratorio que han posibilitado revelar la conectividad cerebral y articular la información obtenida.
En particular, las nuevas técnicas y propuestas de investigación relacionadas con el uso de estimulación eléctrica y marcadores químicos de trazado neuronal han permitido establecer con mayor precisión la conectividad nerviosa entre las distintas áreas encefálicas; donde los lóbulos prefrontales han sido una de las regiones de gran interés, por lo que se ha logrado una mayor comprensión del sustrato neuroanatómico de las redes sinápticas y sus correlatos funcionales, esto ha suscitado un mejor entendimiento de la actividad cerebral y su morfología. Estos datos se han divulgado ampliamente a partir del uso de modelos animales y, aunque se ha llegado a trabajar con primates no humanos con el propósito de tener un acercamiento a la estructura y funcionamiento de la biología humana, los roedores siguen siendo el principal modelo de abordaje en laboratorio, por lo que la literatura científica universal ha avanzado significativamente mediante propuestas de estudio con estos animales.
Los lóbulos prefrontales se subdividen anatómicamente en relación con su estructuración morfológica y características funcionales particulares. Específicamente, en la región central del córtex prefrontal (PFC) se encuentra el área ventro-medial o fronto-medial (mPFC), que, en humanos, sus alteraciones se han asociado funcionalmente a síndromes variables que comprenden alteraciones del estado de ánimo con tendencia negativa, cambios comportamentales bruscos, anhedonia, ausencia de respuesta al dolor, fallos en la toma de decisiones, “lagunas mentales” y alteraciones de las memorias de trabajo y de corto plazo, así como síntomas ansiogénicos y de tipo Korsakoff, entre otros. Anatómicamente dentro del mPFC se encuentra el córtex cingulado anterior (ACd) y los córtex prelímbico (PL) e infralímbico (IL) (ver Figura 1), cuyos circuitos neuronales se conectan recíprocamente y se extienden hacia estructuras mediales del encéfalo. Tanto las proyecciones de PL como de IL se correlacionan por compromisos en el circuito cingulado anterior y disfunciones asociadas a regiones posteriores en niveles subcorticales (Ardila & Rosselli, 2007; Roberts et al., 2007; Waxman, 2010; Narayanan & Laubach, 2017). Pese a lo anterior, las vías axonales extendidas desde o hacia el mPFC no presentan una descripción significativa que detalle su “inicio” y “final”, en interacción con las diversas áreas encefálicas a partir de modelos de estudio que empleen primates no humanos para tal fin, por lo que los estudios con modelos animales que emplean roedores siguen siendo los de mayor acceso para el desarrollo de propuestas de investigación que indagan la estructura morfológica y fisiológica del SNC.
En esta vía, este artículo de revisión se desarrolló con el objetivo de integrar el conocimiento que se tiene sobre los sustratos neuroanatómicos y morfológicos de los circuitos funcionales que el córtex prefrontal medial establece con otras estructuras cerebrales. Metodológicamente esto ha sido posible a partir de la búsqueda sistemática de investigaciones publicadas principalmente en los últimos 8 años (en revistas indexadas y bases de datos de alto impacto científico). Por otra parte, se realizó un análisis que integra las descripciones funcionales de la actividad cerebral con aquellas que detallan las proyecciones neuronales convergentes con el mPFC; asimismo, se articula este conocimiento con las visiones e investigaciones clásicas del estudio de la conectividad cerebral, que se han desarrollado a lo largo de las últimas tres décadas sobre el tema; donde los estudios pioneros en el uso de registros electrofisiológicos y la marcación de células nerviosas por medio de trazadores axonales ha sido clave para el desarrollo y evolución de los métodos y técnicas empleados por la neurociencia moderna.
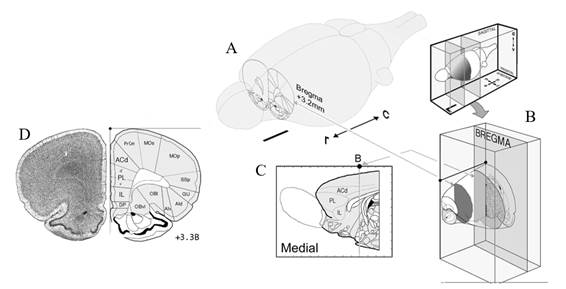
Figura 1
Localización del mPFC y sus subdivisiones anatómicas (Adaptado de Gabbott et al., 2005).
A) Vista transparente del cerebro de rata en orientación rostrocaudal (r-c), posicionando una sección coronal en +3.2 mm (B: Bregma). B) Dibujos que muestran la localización rostrocaudal del bloque de tejido que contienen la corteza prefrontal izquierda. C) Vista lateral de las subdivisiones anatómicas del mPFC: Córtex Cingulado anterior dorsal (ACd), Córtex Pre-límbico (PL) e Infra-límbico (IL) en la pared medial del hemisferio derecho. D) Sección coronal anterior localizando las áreas del PFC en B de +3.3 mm; Área motora precentral (PrCm), Área motora secundaria (MOs), área motora primaria (MOp), Córtex somatosensorial primario (SSp), Área gustaroria del córtex insular (GU), Córtex insular anterior dorsal (AId), Córtex insular anterior ventral (AIv), Córtex orbital lateral (OBl), Córtex orbital ventrolateral (OBvl), Córtex peduncular dorsal (DP).
mPFC y sus interacciones anátomo-funcionales
Diversas investigaciones han estudiado las interacciones de conectividad celular del mPFC a partir del uso de marcadores químicos, empleados principalmente para trazar el recorrido de las células nerviosas, reportando tanto sus aferencias como eferencias, e incluso se ha estudiado desde trabajos que han empleado la electrofisiología como técnica primordial para develar la actividad neuronal. Como se ha mencionado, es amplia la cantidad de investigaciones que emplean roedores como modelo de estudio y que han descrito, a partir de estos, las relaciones morfológicas del mPFC, permitiendo el análisis de la conducta vinculada al sustrato anatómico de base.
Este tipo de experimentación ha posibilitado comprender la funcionalidad de cada una de las conexiones y circuitos establecidos entre el mPFC y otras estructuras del SNC, llegando inclusive a describir con mayor precisión la región del mPFC del cual emergen y/o convergen las fibras nerviosas, siendo particularmente las regiones PL e IL las más estudiadas. Inclusive, se ha detallado en algunos casos si su relación morfológica es con porciones caudales, rostrales, ventrales y/o dorsales de otras estructuras encefálicas.
Entre dichas estructuras con las cuales el mPFC tiene interacciones morfo-funcionales, se destacan principalmente el hipocampo, la sustancia gris periacueductal, el hipotálamo, el núcleo accumbens, la amígdala cerebral, el área tegmental ventral, el núcleo dorsal de Rafé y la habénula lateral del epitálamo, entre otras (ver Figura 2). Por lo anterior, describir la conectividad entre estas regiones encefálicas es primordial cuando se busca comprender las bases neurobiológicas de la actividad cognitivo-comportamental, y más aún si se piensa en la utilidad que este conocimiento tiene para los campos aplicados de la ciencia.
Hipocampo
Se han descrito la existencia de proyecciones neuronales directas desde la porción ventral del hipocampo (vHPC) hacia el mPFC (Jin & Maren, 2015; Knapska et al., 2012; Orsini, Kim, Knapska, & Maren, 2011) específicamente hasta las subdivisiones PL e IL (Hoover & Vertes, 2007; Wang, Jin, & Maren, 2016), siendo mayor el número de proyecciones hacía IL (Wang et al., 2016). De igual forma, el mPFC envía fibras nerviosas hacia el HPC (Bicks, Koike, Akbarian, & Morishita, 2015; Finlay et al., 2015; Ko, 2017; Kogan, Frankland, & Silva, 2000), sin que se hayan descrito puntualmente los centros donde se origina el cuerpo celular. De otro lado, se ha encontrado que en la región CA3 del complejo hipocampal inician fibras neuronales que llegan al mPFC (Avale et al., 2011; Finlay et al., 2015), aun cuando no se describen los centros de recepción de tales fibras (ver Figuras 3 y 4).
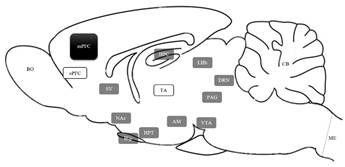
Figura 2.
Localización de los centros subcorticales que interactúan con el mPFC.
Vista sagital medial del cerebro de rata con las principales estructuras (gris) que presentan vínculos anátomo-funcionales con el mPFC. Amígdala cerebral (AM), Área tegmental ventral (VTA), Estriado ventral (SV), Habénula lateral del epitálamo(LHb), Hipocampo (HPC), Hipotálamo (HPT), Núcleo accumbens (NAc), Núcleo dorsal de Rafé (DRN), Tálamo (TA), Sustancia gris periacueductal (PAG); para el contexto de los centros, dentro de la imagen se encuentra el Bulbo olfatorio (BO), Cerebelo (CB), Médula espinal (ME), Córtex órbito-frontal (oPFC) e Hipófisis (Hip). Posiciones anatómicas basadas en el atlas de Paxinos y Watson (2007): The rat brain in stereotaxic coordinates.
Funcionalmente, las proyecciones HPC-mPFC se han asociado a la expresión del miedo (Jin & Maren, 2015; Knapska et al., 2012; Orsini et al., 2011), donde la conexión con PL ejerce un rol relevante en la expresión de las memorias asociadas al miedo (Corcoran & Quirk, 2007; Sierra-Mercado, Padilla-Coreano, & Quirk, 2011), y las neuronas que proyectan hacia IL estarían involucradas en la supresión del condicionamiento al miedo y las respuesta de extinción de este comportamiento (Milad & Quirk, 2012; Zelikowsky et al., 2013). Por su parte, la relación CA3-mPFC se ha vinculado con el enfoque social y la preferencia por la novedad social, y se ha encontrado que la disfunción del receptor en la región dorsal de CA3 altera el enfoque social pero no la preferencia por la novedad social, mientras que las lesiones excitotóxicas de mPFC aumentan la interacción social (Avale et al., 2011; Finlay et al., 2015).
Por lo anterior, es propio que las neuronas de mPFC establezcan conexiones relevantes con el HPC para regular la cognición social en roedores (Bicks et al., 2015; Churchwell & Kesner, 2011; Euston, Gruber, & McNaughton, 2012; Finlay et al., 2015; Kogan et al., 2000), dado el rol crucial del HPC en la formación y consolidación de las memorias; por esto, diversos estudios sugieren que los comportamientos sociales se sincronizan y coordinan entre el mPFC y el HPC durante actividades de la cognición social, donde particularmente el vHPC se ha implicado en la memoria social (Okuyama, Kitamura, Roy, Itohara, & Tonegawa, 2016), así como con comportamientos emocionales como el miedo y la ansiedad (Bannerman, Matthews, Deacon, & Rawlins, 2004; Tovote, Fadok, & Luthi, 2015).
Sustancia Gris Periacueductal e Hipotálamo
De otro lado, existe un solapamiento de las proyecciones de PL e IL hacia la sustancia gris periacueductal (PAG) (Floyd, Price, Ferry, Keay, & Bandler, 2001; Franklin et al., 2017; Gabbott, Warner, Jays, Salway, & Busby, 2005; Ko, 2017). En estas conexiones, varios estudios con modelos animales demostraron que el comportamiento de afrontamiento de amenazas se inicia en las proyecciones del mPFC hacia PAG, exceptuando las circunstancias en que prima el miedo y la ansiedad, en las cuales actúan los circuitos PAG-amígdala (Johansen, Tarpley, LeDoux, & Blair, 2010; Kim et al., 2013; McNally, Johansen, & Blair, 2011; Penzo, Robert, & Li, 2014). De igual forma, PL e IL direccionan fibras hacia el hipotálamo (Floyd et al., 2001; Floyd, Price, Ferry, Keay, & Bandler, 2000; Herry et al., 2008; Ko, 2017; Vertes, 2004); así, mientras que las neuronas de la zona rostral de PL e IL se dirigen hacia el hipotálamo lateral, las de la porción caudal de PL e IL terminan en el hipotálamo dorsal (Floyd et al., 2001); (ver Figuras 3 y 4).
Las conexiones del mPFC con las neuronas del hipotálamo coordinan principalmente la regulación homeostática y el comportamiento social (que está mediado hormonalmente por la interacción con las proyecciones de la hipófisis), como la agresividad, la reproducción y las respuestas defensivas (Herry et al., 2008; Marek, Strobel, Bredy, & Sah, 2013; Tottenham, 2015; Tye & Deisseroth, 2012). También desde el hipotálamo el estrógeno y la oxitocina son importantes para el reconocimiento social, desempeñando roles fundamentales en la regulación del comportamiento dirigido a metas. Así, diversos grupos de neuronas dentro del hipotálamo monitorean y responden de manera diferencial al estado interno y el contexto social del organismo, y transmiten esta información al PFC para la articulación de los procesos motivacionales (Ernst & Fudge, 2009).
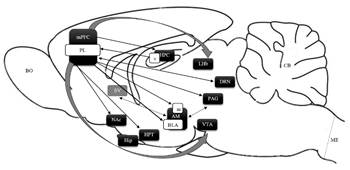
Figura 3.
Direccionalidad de las conexiones neuronales del mPFC (PL) con centros subcorticales.
Aferencias y eferencias del mPFC, desde su región pre-límbica (PL). Amígdala cerebral (AM), Área tegmental ventral (VTA), Estriado ventral (SV), Habénula lateral del epitálamo (LHb), Hipocampo ventral (vHPC), Hipotálamo (HPT), Núcleo accumbens (NAc), Núcleo dorsal de Rafé (DRN), Núcleo basolateral de la amígdala (BLA), Núcleo medial de AM (mAM), Sustancia gris periacueductal (PAG); circuitos PAG-AM y SV-AM interactúan en la regulación de comportamientos asociados al mPFC.
Área tegmental ventral y Núcleo Accumbens
Con relación al área tegmental ventral (VTA), las investigaciones develaron que esta área proyecta hacia la porción IL del mPFC, pero no hacia la zona PL (aunque PL sí proyecta a VTA, ver Figura 3); esta conexión se ha asociado a conductas de hiperlocomoción causadas por la estimulación de recompensa de dopamina. Asimismo, el núcleo accumbens (NAc) presenta proyecciones neuronales hacia el área IL de mPFC (ver Figura 4) y recibe conexiones tanto de PL como de IL, cuyo funcionamiento está vinculado a comportamientos positivos durante la recompensa (Han et al., 2017; Ko, 2017), principalmente por actividad de circuitos cocainérgicos desde NAc hasta mPFC, originados en el locus coeruleous; de igual forma, se ha encontrado que neuronas glutamatérgicas de mPFC proyectan al NAc por vía postsináptica (Schmidt et al., 2017).
Amígdala cerebral y Estriado ventral
En lo que respecta a la amígdala, algunas investigaciones encontraron que las proyecciones emergentes de las subdivisiones (PL e IL) de mPFC se solapan (principalmente las de IL) y convergen con las provenientes de la corteza órbito-frontal (oPFC), prolongándose hacia el núcleo basolateral de la amígdala (BLA) (Chang & Grace, 2016; Chang & Ho, 2017; Likhtik, Stujenske, Topiwala, Harris, & Gordon, 2014; Rempel-Clower, 2007; Sotres-Bayon & Quirk, 2010; Vertes, 2004), sin embargo, en cuanto a proyecciones directas, BLA recibe mayores entradas provenientes de PL (Herving et al, 2017; Vertes, 2004). De igual forma, de PL emergen proyecciones que terminan en la amígdala medial (Anderson, 2012; Allsop, Vander Weele, Wichmann, & Tye, 2014; Ko, 2017; Tottenham, 2015); (ver Figuras 3 y 4). Inclusive, se encontró que el 95% de las neuronas de BLA responden a la estimulación eléctrica realizada en las neuronas de mPFC, y que, ya sea por estimulación eléctrica o farmacológica, la activación de mPFC inhibe la vía lateral-orbital del PFC (Chang & Ho, 2017).
De forma general, la relación directa entre el mPFC y la amígdala cerebral se halla vinculada al control emocional y contingencias asociadas a la regulación del comportamiento, al procesamiento de la información, y a los comportamientos sociales innatos, como la agresión y el apareamiento (Anderson, 2012; Allsop et al., 2014; Choi et al., 2005; Herry et al., 2008; Marek et al., 2013; Sabihi, Dong, Durosko, & Leuner, 2014; Sabihi, Durosko, Dong, & Leuner, 2014; Tottenham, 2015; Tye & Deisseroth, 2012), también se relaciona con el miedo, el aprendizaje, y la extinción de los comportamientos relacionados con la ansiedad (Herry et al., 2008; Tye & Deisseroth, 2012; Marek et al., 2013; Tottenham, 2015).
En lo que respecta a la actividad de la conexión convergente de mPFC/oPFC-Amígdala (ver Figura 4), este circuito se ha relacionado primordialmente con el procesamiento de la información y las emociones, y al igual que el hipocampo, las proyecciones de PL-amígdala se han visto involucradas en la expresión del miedo aprendido, mientras que las de IL-amígdala se asocian a la extinción del recuerdo por condicionamiento al miedo (Milad & Quirk, 2012; Quirk & Mueller, 2008; Sierra-Mercado et al., 2011). De otro lado, también se encontró que la actividad del BLA se conecta con el estriado ventral (ver Figura 3) y estas dos regiones se integran con mPFC en la regulación de sistemas emocionales y comportamientos de tipo respuesta (Gruber & McDonald, 2012), así, la valoración emocional se integra en los circuitos de la toma de decisiones (Herving et al., 2017) a través del mPFC (evaluación del riesgo y control inhibitorio), el BLA (aprendizaje emocional) y el estriado ventral (para información integradora de la recompensa, el contexto y la motivación).
Núcleo dorsal de Rafé
Por otra parte, amplia evidencia sugiere que mPFC está conectado con el núcleo dorsal de Rafé (DRN) por medio de proyecciones monosinápticas recíprocas (Challis & Berton, 2015; Gonçalves, Nogueira, Shammah-Lagnado, & Metzger, 2009; Vázquez-Borsetti, Cortes, & Artigas, 2009). En sus investigaciones, Challis, Beck y Berton (2014) y Petreanu, Huber, Sobczyk y Svoboda (2007) demostraron que neuronas de mPFC establecen sinapsis, particularmente, con neuronas de las porciones rostral y caudal del DRN (ver Figura 4). Desde este núcleo, la serotonina (5-HT) cumple una variedad de funciones cognitivas que incluyen el comportamiento motivacional, la atención, el afrontamiento al estrés, la toma de decisiones basada en valores por recompensa y comportamientos sociales, así como también de aprendizaje y memoria (Nakamura, 2013).
Lo anterior ocurre, porque la 5-HT se sintetiza y libera principalmente en DRN proporcionando importantes aferentes serotoninérgicos al cerebro anterior, particularmente al mPFC (Challis et al., 2014; Challis & Berton, 2015; Michelsen, Prickaerts, & Steinbusch, 2008). De igual forma, la conexión mPFC-DRN, en roedores, se ha visto involucrada en comportamientos similares a estados depresivos (Albert, Vahid-Ansari, & Luckhart, 2014; Hamani et al., 2012; Mahar, Bambico, Mechawar, & Nobrega, 2014; Riga et al., 2014; Veerakumar et al., 2014).
Habénula Lateral
La habénula lateral del Epitálamo, en su porción medial, recibe proyecciones desde PL e IL, así como de las cortezas cingulada anterior e insular (Baker, Oh, Kidder, & Mizumori, 2015). Esta conexión habénula-mPFC (ver Figura 4), transmitiría información del estado emocional interno e influiría en los sistemas de dopamina y 5-HT (Lecourtier, Defrancesco, & Moghaddam, 2008; Sego et al., 2014). También se ha referido que la habénula lateral (LHb) estaría involucrada en el procesamiento olfativo, la ejecución de acciones complejas dirigidas a objetivos, comportamientos de apareamiento y el aprendizaje aversivo o de recompensa (Baker et al., 2015), pese a que su actividad funcional aún ha sido poco estudiada.
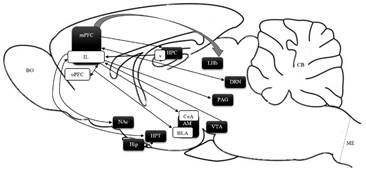
Figura 4
Direccionalidad de las conexiones neuronales del mPFC (IL) con centros subcorticales.
Aferencias y eferencias del mPFC, desde su región infra-límbica (IL). Amígdala cerebral (AM), Área tegmental ventral (VTA), Córtex órbito-frontal (oPFC), Habénula lateral del epitálamo (LHb), Hipocampo ventral (vHPC), Hipófisis (Hip), Hipotálamo (HPT), Núcleo accumbens (NAc), Núcleo dorsal de Rafé (DRN), Núcleo basolateral de la amígdala (BLA), Núcleo central de AM (CeA), Sustancia gris periacueductal (PAG); circuitos HPT-Hip interactúan en la regulación de estados emocionales asociados al mPFC.
En algún sentido, la información del PFC sobre actividades de alta demanda cognitiva se procesaría e integraría junto con eferencias de otras regiones cerebrales que convergen en la LHb, para el aprendizaje encaminado al cumplimiento de metas (Baker et al., 2015). Además, se ha relacionado la conexión LHb-mPFC con el comportamiento de juego social en la interacción de mamíferos jóvenes en pro de facilitar el establecimiento de vínculos y la comunicación social (Baarendse, Counotte, O`Donnell, & Vanderschuren, 2013; van Kerkhof, Damsteegt, Trezza, Voorn, & Vanderschuren, 2013). Lo anterior, parte de la influencia que ejerce la LHb sobre la regulación de la 5-HT y la noradrenalina para modular el comportamiento de juego social (Siviy & Panksepp, 2011; Trezza, Baarendse, & Vanderschuren, 2010). Con relación a esto, Lecourtier, Neijt y Kelly (2004) y van Kerkhof et al. (2013), han postulado que un estado emocional negativo disminuye la actividad de la habénula, para la experiencia positiva del comportamiento de juego social, como, por ejemplo, ante conductas de aislamiento social.
Subdivisiones de PL e IL
Por otra parte, de forma puntual Vertes (2004) describió ampliamente y con mayor precisión las áreas en que emergen las neuronas desde el mPFC, afirmando que las regiones rostrales de IL distribuyen proyecciones más fuertes que las regiones caudales (IL), hacia la corteza insular posterior, la porción externa del núcleo accumbens, el núcleo de la base de la estría terminal, a los núcleos central (CeA) y basolateral de la amígdala (ver Figura 4), el núcleo mediodorsal del tálamo y la corteza entorrinal. De otro lado, la zona caudal de IL proyectaría más neuronas que la porción rostral (IL), hacia el septum lateral, el núcleo horizontal de la banda diagonal, el hipotálamo anterior, el núcleo supramamilar y la PAG del diencéfalo y el mesencéfalo. De forma general se ha referido que estas conexiones de IL (en roedores) cumplen funciones viseromorotas, cuyo funcionamiento es homólogo al de la región oPFC de los primates (Barbas, 1995; 2000; Groenewegen & Uylings, 2000; Neafsey, 1990).
Asimismo, se llegó a detallar (Vertes, 2004), que el área rostral de PL proyecta fuertemente sus neuronas (más que la porción caudal-PL), hacia la corteza insular agranular (profunda y superficialmente), la corteza entorrinal, el centro del núcleo accumbens, a los núcleos CeA y BLA, los núcleos mediodorsal y paraventricular (zona posterior) del tálamo, el núcleo supramamilar y el DRN. Por su parte, la porción caudal de PL presenta mayores proyecciones neuronales que el área rostral (PL) direccionadas a la corteza cingulada anterior (área supracolosal), el septum lateral, el núcleo anterior del hipotálamo, los núcleos anteromedial, interanteromedial, reuniens y mediodorsal del tálamo, y el núcleo supralemniscal.
Adicionalmente, la zona rostral de PL proyecta, selectivamente, fibras a regiones ventrolaterales de PAG, y la región caudal de PL lo hace de igual forma hacia la porción dorsal de PAG. De otro lado, con relación a la región dorsal de PL, ésta distribuye fibras nerviosas hacia la corteza cingulada posterior y retroesplenial, y a la porción lateral del núcleo mediodorsal del tálamo. En lo que respecta al área ventral de PL, ésta traza sus prolongaciones nerviosas hacia la porción horizontal del núcleo de la banda diagonal, el área preóptica medial, y la porción medial del núcleo mediodorsal del tálamo. De forma general, funcionalmente las conexiones neuronales de PL (en roedores) se homologaría con el procesamiento cognitivo que ha sido asociado a la región dorsolateral de la corteza prefrontal de primates (Kolb, 1984; Goldman-Rakic, 1987, 1995; Groenewegen & Uylings, 2000; Vertes, 2004).
Comprensión para el futuro de la investigación
Los resultados de las investigaciones abordados en esta revisión han permitido describir ampliamente la conectividad neuronal del mPFC, tanto de sus vías aferentes como eferentes. Así, la actividad de esta región de los lóbulos prefrontales resalta en importancia como uno de los centros con mayores proyecciones nerviosas vinculadas funcionalmente a procesos emocionales y comportamentales asociados a la cognición social, donde los núcleos de la amígdala y el hipocampo son las estructuras encefálicas que presentan más relaciones morfo-funcionales con el mPFC.
Las interacciones electroquímicas entre los diferentes centros subcorticales del SNC intervienen significativamente en la actividad regulada por el mPFC, por lo que, aunque el córtex prefrontal es considerado el centro ejecutivo de mayor relevancia evolutiva, su actividad metabólica, y los productos cognitivos, emocionales y conductuales del individuo, depende íntegramente de los procesos biológicos desencadenados en niveles internos de la estructura cerebral. A su vez, ha sido claro que, aunque PL e IL comparten aferencias y eferencias con la mayoría de las estructuras abordadas, también presentan proyecciones exclusivas e independientes, lo cual orienta el porqué de la variedad de comportamientos que pueden suscitarse ante la estimulación o daño de circuitos neuronales específicos.
En este sentido, morfológicamente las subdivisiones de los lóbulos prefrontales son las estructuras que más conectividad celular establecen con el resto del sistema nervioso central, tanto cortical como subcorticalmente, y son el centro de convergencia y divergencia de circuitos neuronales que integran la información bioquímica y cognitivo-comportamental del organismo, por lo que, siendo tanto animales como humanos seres sociales por naturaleza, el estudio de la actividad anátomo-funcional asociada al mPFC, y en general al córtex prefrontal, es de gran importancia en la comprensión de la organización psicobiológica del individuo y los correlatos subsecuentes a estos productos de actividad cerebral.
De otro lado, pocos son los estudios que se han interesado por establecer la conectividad celular que tienen las regiones prefrontales con núcleos y centros subcorticales; los cuales presentan gran influencia en la funcionalidad de la actividad cerebral. Aun así, la descripción de sus proyecciones y circuitos neuronales son vagamente conocidas; entre estos, debe profundizarse sobre la habénula lateral del epitálamo y su conectividad con otros centros subcorticales en relación con la actividad del PFC, la interacción Hipófisis/hipotálamo-PFC, y los procesos hormonales del DRN y el VTA con la actividad específica de cada una de las subdivisiones del PFC, entre otros.
Así, se hace evidente la necesidad de continuar el desarrollo de propuestas de investigación que empleen modelos animales como objeto de estudio y, aún más, que propendan por extrapolar en alguna medida la información obtenida hacia la comprensión de la actividad cerebral humana. Para lo anterior, aun cuando el uso de roedores ha reducido la brecha del conocimiento sobre la biología cerebral, es menester incentivar y acrecentar la ejecución de estudios anatomo-fisiológicos y, que propongan e investiguen estas interacciones morfo-funcionales a partir del uso de primates no humanos como objeto de análisis. Pese a que siguen siendo restringidas las investigaciones en las cuales los primates sean el modelo de estudio, su implementación y profundización está marcando la pauta sobre una nueva comprensión de la anatomía, y está orientando el curso de la neurociencia moderna y aplicada.
Referencias
Albert, P., Vahid-Ansari, F., & Luckhart, C. (2014). Serotonin-prefrontal cortical circuitry in anxiety and depression phenotypes: pivotal role of pre and post-synaptic 5-HT1A receptor expression. Frontiers in Behavioral Neuroscience, 8, 199. doi: 10.3389/fnbeh.2014.00199
Allsop, S., Vander Weele, C., Wichmann, R., & Tye, K. (2014). Optogenetic insights on the relationship between anxiety-related behaviors and social deficits. Frontiers in Behavioral Neuroscience, 8, 241. doi: 10.3389/fnbeh.2014.00241
Anderson, D. (2012). Optogenetics, sex and violence in the brain: implications for psychiatry. Biological Psychiatry, 71(12), 1081–1089. doi: 10.1016/j.biopsych.2011.11.012
Ardila, A., & Rosselli, M. (2007). Neuropsicología Clínica. México: Manual Moderno.
Avale, M., Chabout, J., Pons, S., Serreau, P., De Chaumont, F., Olivo-Marin, J., … Granon, S. (2011). Prefrontal nicotinic receptors control novel social interaction between mice. FASEB Journal, 25(7), 2145–2155. doi: 10.1096/fj.10-178558
Baarendse, P., Counotte, D., O`Donnell, P., & Vanderschuren, L. (2013). Early social experience is critical for the development of cognitive control and dopamine modulation of prefrontal cortex function. Neuropsychopharmacology, 38(8), 1485-1494. doi: 10.1038/npp.2013.47
Baker, P., Oh, S., Kidder, K., & Mizumori, S. (2015). Ongoing behavioral state information signaled in the lateral habenula guides choice flexibility in freely moving rats. Frontiers in Behavioral Neuroscience, 9, 295. doi: 10.3389/fnbeh.2015.00295
Bannerman, D., Matthews, P., Deacon, R., & Rawlins, J. (2004). Medial septal lesions mimic effects of both selective dorsal and ventral hippocampal lesions. Behavioral Neuroscience, 118(5), 1033-1041. doi: 10.1037/0735-7044.118.5.1033
Barbas, H. (1995). Anatomic basis of cognitive-emotional interactions in the primate prefrontal cortex. Neuroscience Biobehavioral Review, 19(3), 499–510. doi: 10.1016/0149-7634(94)00053-4
Barbas, H. (2000). Connections underlying the synthesis of cognition, memory, and emotion in primate prefrontal cortices. Brain Research Bulletin, 52(5), 319–330. doi: 10.1016/S0361-9230(99)00245-2
Bicks, L., Koike, H., Akbarian, S., & Morishita, H. (2015). Prefrontal cortex and social cognition in mouse and man. Frontiers in Psychology, 6, 1805. doi: 10.3389/fpsyg.2015.01805
Challis, C., Beck, S., & Berton, O. (2014). Optogenetic modulation of descending prefrontocortical inputs to the dorsal raphe bidirectionally bias socioaffective choices after social defeat. Frontiers in Behavioral Neuroscience, 8, 43. doi: 10.3389/fnbeh.2014.00043
Challis, C., & Berton, O. (2015). Top-down control of serotonin systems by the prefrontal cortex: a path toward restored socioemotional function in depression. ACS Chemical Neuroscience, 6(7), 1040–1054. doi: 10.1021/acschemneuro.5b00007
Chang, C., & Grace, A. (2016). Inhibitory modulation of orbitofrontal cortex on medial prefrontal cortex–amygdala information flow. Cerebral Cortex, 28(1), 1-8. doi: 10. 1093/cercor/bhw342
Chang, C., & Ho, T. (2017). Inhibitory modulation of medial prefrontal cortical activation on lateral orbitofrontal cortex–amygdale information flow. The Jornal of Physiology, 595(17), 6065-6067. doi: 10.1113/JP274568
Choi, G., Dong, H., Murphy, A., Valenzuela, D., Yancopoulos, G., Swanson, L., & Anderson, D. (2005). Lhx6 delineates a pathway mediating innate reproductive behaviors from the amygdala to the hypothalamus. Neuron, 46(4), 647–660. doi: 10.1016/j.neuron.2005.04.011
Churchwell, J., & Kesner, R. (2011). Hippocampal-prefrontal dynamics in spatial working memory: interactions and independent parallel processing. Behavioral Brain Research, 225(2), 389–395. doi: 10.1016/j.bbr.2011.07.045
Corcoran, K., & Quirk, G. (2007). Activity in Prelimbic Cortex Is Necessary for the Expression of Learned, But Not Innate, Fears. Journal of Neuroscience, 27(4), 840-844. doi: 10.1523/JNEUROSCI.5327-06.2007
Ernst, M., & Fudge, J. (2009). A developmental neurobiological model of motivated behavior: anatomy, connectivity and ontogeny of the triadic nodes. Neuroscience Biobehavioral Reviews, 33(3), 367-382. doi: 10.1016/j.neubiorev.2008.10.009
Euston, D., Gruber, A., & McNaughton, B. (2012). The role of medial prefrontal cortex in memory and decision making. Neuron, 76(6), 1057–1070. doi: 10.1016/j.neuron.2012.12.002
Finlay, J., Dunham, G., Isherwood, A., Newton, C., Nguyen, T., Reppar, P., … Greene, R. (2015). Effects of prefrontal cortex and hippocampal NMDA NR1-subunit deletion on complex cognitive and social behaviors. Brain Research, 1600, 70–83. doi: 10.1016/j.brainres.2014.10.037
Floyd, N., Price, J., Ferry, A., Keay, K., & Bandler, R. (2000). Orbitomedial prefrontal cortical projections to distinct longitudinal columns of the periaqueductal gray in the rat. The Journal of Comparative Neurology, 422(4), 556-578. doi: 10.1002/1096-9861(20000710)422:4<556::AID-CNE6>3.0.CO;2-U
Floyd, N., Price, J., Ferry, A., Keay, K., & Bandler, R. (2001). Orbitomedial prefrontal cortical projections to hypothalamus in the rat. The Journal of Comparative Neurology, 432(3), 307-328. doi: 10.1002/cne.1105
Franklin, T., Silva, B., Perova, Z., Marrone, L., Masferrer, M., Zhan, Y., ... Gross, C. (2017). Prefrontal cortical control of a brainstem social behavior circuit. Natural Neuroscience, 20(2), 260–270. doi: 10.1038/nn.4470
Gabbott, P., Warner, T., Jays, P., Salway, P., & Busby, S. (2005). Prefrontal cortex in the rat: projections to subcortical autonomic, motor, and limbic centers. The Journal of Comparative Neurology, 492(2), 145–177. doi: 10.1002/cne.20738
Goldman-Rakic, P. (1987). Circuitry of primate prefrontal cortex and regulation of behavior by representational memory. En: Mountcastle, V., Plum, F., & Geiger, S. (Eds.), Handbook of physiology: section 1: The nervous system. Volume V: Higher functions of the brain (pp. 373–417). Bethesda, MD: American Physiological Society.
Goldman-Rakic, P. (1995). Cellular basis of working memory. Neuron, 14(3), 477–485. doi: 10.1016/0896-6273(95)90304-6
Gonçalves, L., Nogueira, M., Shammah-Lagnado, S., & Metzger, M. (2009). Prefrontal afferents to the dorsal raphe nucleus in the rat. Brain Research Bulletin, 78(4-5), 240–247. doi: 10.1016/j.brainresbull.2008.11.012
Groenewegen, H., & Uylings, H. (2000). The prefrontal cortex and the integration of sensory, limbic and autonomic information. Progress in Brain Research, 126, 3–28. doi: 10.1016/S0079-6123(00)26003-2
Gruber, A., & McDonald, R. (2012). Context, emotion, and the strategic pursuit of goals: interactions among multiple brain systems controlling motivated behavior. Frontiers in Behavioral Neuroscience, 6(50), 1-26. doi: 10.3389/fnbeh.2012.00050.
Hamani, C., Machado, D., Hipólide, D., Dubiela, F., Suchecki, D., Macedo, C., & Nobrega, J. (2012). Deep brain stimulation reverses anhedonic-like behavior in a chronic model of depression: role of serotonin and brain derived neurotrophic factor. Biological Psychiatry, 71(1), 30–35. doi: 10.1016/j.biopsych.2011.08.025
Han, X., Jing, M., Zhao, T., Wu, N., Song, R., & Li, J. (2017). Role of dopamine projections from ventral tegmental area to nucleus accumbens and medial prefrontal cortex in reinforcement behaviors assessed using optogenetic manipulation. Metabolic Brain Disease, 32(5), 1503-1505. doi: 10.1007/s11011-017-0023-3
Herry, C., Ciocchi, S., Senn, V., Demmou, L., Müller, C., & Lüthi, A. (2008). Switching on and off fear by distinct neuronal circuits. Nature, 454(7204), 600–606. doi: 10.1038/nature07166
Herving, M., Hvid, N., Bredo, N., Rydbirk, R., Vestergaard, M., Hay-Schmidt, A., (…) Aznar, S. (2017). Involvement of serotonin 2A receptor activation in modulating medial prefrontal cortex and amygdala neuronal activation during novelty-exposure. Behavioral Brain Research, 326, 1-12. doi: 10.1016/j.bbr.2017.02.050
Hoover, W., & Vertes, R. (2007). Anatomical analysis of afferent projections to the medial prefrontal cortex in the rat. Brain Structure & Function, 212(2), 149-179. doi: 10.1007/s00429-007-0150-4
Jin, J., & Maren, S. (2015). Fear Renewal Preferentially activates ventral hippocampal neurons projecting to both amygdale and prefrontal cortex in rats. Scientific Reports, 5, 8388. doi: 10.1038/srep08388
Johansen, J., Tarpley, J., LeDoux, J., & Blair, H. (2010). Neural substrates for expectation-modulated fear learning in the amygdala and periaqueductal gray. Natural Neuroscience, 13(8), 979-986. doi: 10.1038/nn.2594
Kim, E., Horovitz, O., Pellman, B., Tan, L., Li, Q., Richter-levin, G., & Kim, J. (2013). Dorsal periaqueductal gray-amygdala pathway conveys both innate and learned fear responses in rats. Proceedings of the National Academy of Sciences of the Unites States of America, 110(36), 14795-14800. doi: 10.1073/pnas.1310845110
Knapska, E., Macias, M., Mikosz, M., Nowak, A., Owczarek, D., Wawrzyniak, M., … Kaczmarek, L. (2012). Funtional anatomy of neural circuits regulating fear and extinction. Proceedings of the National Academy of Science of the United States of America, 109(42), 17093-17098. doi: 10.1073/pnas.1202087109
Ko, J. (2017). Neuroanatomical Substrates of Rodent Social Behavior: The Medial Prefrontal Cortex and Its Projection Patterns. Frontiers in Neural Circuits, 11(41), 1-16. doi: 10.3389/fncir.2017.00041
Kogan, J., Frankland, P., & Silva, A. (2000). Long-term memory underlying hippocampus-dependent social recognition in mice. Hippocampus, 10(1), 47–56. doi: 10.1002/(SICI)1098-1063(2000)10:1<47::AIDHIPO5>3.0.CO;2-6
Kolb, B. (1984). Functions of the frontal cortex of the rat: a comparative review. Brain Research Reviews, 8(1), 65–98. doi: 10.1016/0165-0173(84)90018-3
Lecourtier, L., Defrancesco, A., & Moghaddam, B. (2008). Differential tonic influence of lateral habenula on prefrontal cortex and nucleus accumbens dopamine release. The European Journal of Neuroscience, 27(7), 1755–1762. doi: 10.1111/j.1460-9568. 2008.06130.x
Lecourtier, L., Neijt, H., & Kelly, P. (2004). Habenula lesions cause impaired cognitive performance in rats: implications for schizophrenia. The European Journal of Neuroscience, 19(9), 2551–2560. doi:10.1111/j.0953-816x.2004.03356.x
Likhtik, E., Stujenske, J., Topiwala, M., Harris, A., & Gordon, J. (2014). Prefrontal entrainment of amygdala activity signals safety in learned fear and innate anxiety. Natural Neuroscience, 17(1), 106–113. doi: 10.1038/nn.3582
Mahar, I., Bambico, F., Mechawar, N., & Nobrega, J. (2014). Stress, serotonin and hippocampal neurogenesis in relation to depression and antidepressant effects. Neuroscience Biobehavioral Review, 38, 173–192. doi: 10.1016/j.neubiorev.2013.11.009
Marek, R., Strobel, C., Bredy, T., & Sah, P. (2013). The amygdala and medial prefrontal cortex: partners in the fear circuit. Journal of Physiology, 591(10), 2381–2391. doi: 10.1113/jphysiol.2012.248575
McNally, G., Johansen, J., & Blair, H. (2011). Placing prediction into the fear circuit. Trends in Neuroscience, 34(6), 283–292. doi: 10.1016/j.tins.2011.03.005
Michelsen, K., Prickaerts, J., & Steinbusch, H. (2008). The dorsal raphe nucleus and serotonin: implications for neuroplasticity linked to major depression and Alzheimer’s disease. Progress in Brain Research, 172, 233–264. doi: 10.1016/S0079-6123(08)00912-6
Milad, M., & Quirk, G. (2012). Fear Extinction as a Model for Translational Neuroscience: Ten Years of Progress. Annual Review of Psychology, 63(1), 129-151. doi: 10.1146/annurev.psych.121208.131631
Nakamura, K. (2013). The role of the dorsal Raphé nucleus in reward-seeking behavior. Frontiers in integrative Neuroscience, 7, 60. doi: 10.3389/fnint.2013.00060
Narayanan, N., & Laubach, M. (2017). Inhibitory Control: Mapping Medial Frontal Cortex. Current Biology, 27(4), R148-R150. doi: 10.1016/j.cub.2017.01.010
Neafsey, E. (1990). Prefrontal cortical control of the autonomic nervous system: anatomical and physiological observations. Progress in Brain Research, 85, 147–166. doi: 10.1016/S0079-6123(08)62679-5
Okuyama, T., Kitamura, T., Roy, D., Itohara, S., & Tonegawa, S. (2016). Ventral CA1 neurons store social memory. Science, 353(6307), 1536–1541. doi: 10.1126/science.aaf7003
Orsini, C., Kim, J., Knapska, E., & Maren, S. (2011). Hippocampal and prefrontal projections to the basal amygdala mediate contextual regulation of fear after extinction. The Journal of Neuroscience, 31(47), 17269-17277. doi: 10.1523/JNEUROSCI.4095-11.2011
Paxinos, G., & Watson, C. (2007). The rat brain in stereotaxic coordinates (6ta Ed.). UK: Elsevier, Academic Press.
Penzo, M. A., Robert, V., & Li, B. (2014). Fear conditioning potentiates synaptic transmission onto long-range projection neurons in the lateral subdivision of central amygdala. The Journal of Neuroscience, 34, 2432–2437. doi: 10.1523/JNEUROSCI.416613.2014
Petreanu, L., Huber, D., Sobczyk, A., & Svoboda, K. (2007). Channelrhodopsin-2-assisted circuit mapping of long-range callosal projections. Natural Neuroscience, 10(5), 663–668. doi: 10.1038/nn1891
Quirk, G., & Mueller, D. (2008). Neural mechanisms of extinction learning and retrieval. Neuropsychopharmacology, 33(1), 56–72. doi: 10.1038/sj.npp.1301555
Rempel-Clower, N. (2007). Role of orbitofrontal cortex connections in emotion. Annals of the New York Academy of Sciences, 1121(1), 72–86. doi: 10.1196/annals.1401.026
Riga, D., Matos, M., Glas, A., Smit, A., Spijker, S., & Van den Oever, M. (2014). Optogenetic dissection of medial prefrontal cortex circuitry. Frontiers in Systems Neuroscience, 8, 230. doi: 10.3389/fnsys.2014.00230
Roberts, A., Tomic, D., Parkinson, C., Roeling, T., Cutter, D., Robbins, T., & Everitt, B. (2007). Forebrain connectivity of the prefrontal cortex in the marmoset monkey (Callithrix jacchus): an anterograde and retrograde tract-tracing study. The Journal of Comparative Neurology, 502(1), 86-112. doi: 10.1002/cne.21300
Sabihi, S., Dong, S., Durosko, N., & Leuner, B. (2014). Oxytocin in the medial prefrontal cortex regulates maternal care, maternal aggression and anxiety during the postpartum period. Frontiers in Behavioral Neuroscience, 8, 258. doi: 10.3389/fnbeh.2014.00258
Sabihi, S., Durosko, N., Dong, S., & Leuner, B. (2014). Oxytocin in the prelimbic medial prefrontal cortex reduces anxiety-like behavior in female and male rats. Psychoneuroendocrinology, 45, 31–42. doi: 10.1016/j.psyneuen.2014.03.009
Schmidt, K., Schroeder, J., Foster, S., Squires, K., Smith, B., Pitts, E., (…) Weinshenker, D. (2017). Norepinephrine regulates cocaine-primed reinstatement via a1-adrenergic receptors in the medial prefrontal cortex. Neuropharmacology, 119, 134-140. doi: 10.1016/j.neuropharm.2017.04.005
Sego, C., Gonçalves, L., Lima, L., Furigo, I., Donato, J., & Metzger, M. (2014). Lateral habenula and the rostromedial tegmental nucleus innervate neurochemically distinct subdivisions of the dorsal raphe nucleus in the rat. The Journal of Comparative Neurology, 522(7), 1454–1484. doi: 10.1002/cne.23533
Sierra-Mercado, D., Padilla-Coreano, N., & Quirk, G. (2011). Dissociable Roles of Prelimbic and Infralimbic Cortices, Ventral Hippocampus, and Basolateral Amygdala in the Expression and Extinction of Conditioned Fear. Neuropsychopharmacology, 36(1), 529–538. doi: 10.1038/npp.2010.184
Siviy, S., & Panksepp, J. (2011). In search of the neurobiological substrates for social playfulness in mammalian brains. Neuroscience Biobehavioral Reviews, 35(9), 1821–1830. doi: 10.1016/j.neubiorev.2011.03.006
Sotres-Bayon, F., & Quirk, G. (2010). Prefrontal control of fear: more than just extinction. Current Opinion in Neurobiology, 20(2), 231–235. doi: 10.1016/j.conb.2010.02.005
Tottenham, N. (2015). Social scaffolding of human amygdala-mPFC circuit development. Social Neuroscience, 10(5), 489–499. doi: 10.1080/17470919.2015.1087424
Tovote, P., Fadok, J., & Luthi, A. (2015). Neuronal circuits for fear and anxiety. Natural Review in Neuroscience, 16(6), 317–331. doi: 10.1038/nrn3945
Trezza, V., Baarendse, P., & Vanderschuren, L. (2010). The pleasures of play: pharmacological insights into social reward mechanisms. Trends in Pharmacological Science, 31(10), 463–469. doi: 10.1016/j.tips.2010.06.008
Tye, K., & Deisseroth, K. (2012). Optogenetic investigation of neural circuits underlying brain disease in animal models. Natural Review of Neuroscience, 13(4), 251–266. doi: 10.1038/nrn3171
van Kerkhof, L., Damsteegt, R., Trezza, V., Voorn, P., & Vanderschuren, L. (2013). Functional integrity of the habenula is necessary for social play behavior in rats. The European Journal of Neuroscience, 38(10), 3465–3475. doi: 10.1111/ejn.12353
Vázquez-Borsetti, P., Cortes, R., & Artigas, F. (2009). Pyramidal neurons in rat prefrontal cortex projecting to ventral tegmental area and dorsal raphe nucleus express 5-HT2A receptors. Cerebral Cortex, 19(7), 1678–1686. doi: 10.1093/cercor/bhn204
Veerakumar, A., Challis, C., Gupta, P., Da, J., Upadhyay, A., Beck, S., & Berton, O. (2014). Antidepressant-like effects of cortical deep brain stimulation coincide with pro-neuroplastic adaptations of serotonin systems. Biological Psychiatry, 76(3), 203–212. doi: 10.1016/j.biopsych.2013.12.009
Vertes, R. (2004). Differential Projections of the Infralimbic and Prelimbic Cortex in the Rat. Journal SYNAPSE, 51(1); 32–58. doi: 10.1002/syn.10279
Wang, Q., Jin, J., & Maren, S. (2016). Renewal of extinguished fear activates ventral hippocampal neurons projecting to the prelimbic and infralimbic cortices in rats. Neurobiology of Learning and Memory, 134(A), 38-43. doi: 10.1016/j.nlm.2016.04.002
Waxman, S. (2010). Clinical Neuroanatomy. México: McGraw Hill.
Zelikowsky, M., Bissierec, S., Hasta, T., Bennetta, R., Abdipranotod, A., Visseld, B., & Fanselow, M. (2013). Prefrontal microcircuit underlies contextual learning after hippocampal loss. Proceedings of the National Academy of Sciences of the Unites States of America, 110(24), 9938–9943. doi: 10.1073/pnas.1301691110
Notas de autor
alexander.rios@ufrn.edu.br
Información adicional
Citar este artículo como: Ríos-Florez, J. A. (2018). Sustratos neuroanatómicos y funcionales del córtex prefrontal medial. Revista Argentina de Ciencias del Comportamiento, 10(3), 43-53
Enlace alternativo
https://revistas.unc.edu.ar/index.php/racc/article/view/20619/pdf (pdf)