Revisiones de tema
Nutrición en pancreatitis aguda: nuevos conceptos para un viejo problema
Nutrition in acute pancreatitis: new concepts for an old problem
Nutrición en pancreatitis aguda: nuevos conceptos para un viejo problema
Revista Colombiana de Gastroenterologia, vol. 35, núm. 4, pp. 465-470, 2020
Asociación Colombiana de Gastroenterología
Recepción: 10 Julio 2019
Aprobación: 15 Octubre 2019
Resumen: El manejo de la nutrición en pancreatitis aguda ha sido cuestión de debate. Durante muchos años el concepto de reposo pancreático fue generalizado y aceptado en el manejo de la pancreatitis aguda. Actualmente se conoce que la nutrición temprana permite mantener la integridad de la barrera intestinal, que previene la aparición de complicaciones infeccionas y se asocia con una menor estancia hospitalaria, menos complicaciones y un mejor pronóstico. En esta revisión se discuten las principales ventajas de la nutrición temprana en pancreatitis aguda, la seguridad de la misma y la vía de administración.
Palabras clave: Nutrición, reposo pancreático, sonda nasogástrica, sonda nasoyeyunal.
Abstract: Nutrition management in acute pancreatitis has been a matter of debate worldwide. For many years, the concept of pancreatic rest was widespread and accepted to treat acute pancreatitis. However, current knowledge of early nutrition allows maintaining the intestinal barrier’s integrity, preventing the occurrence of infectious complications, which is associated with a shorter hospital stay, fewer complications, and better prognosis. This review presents the main advantages of early nutrition in acute pancreatitis, its safety, and the route of administration.
Keywords: Nutrition, Pancreatic rest, Nasogastric tube, Nasojejunal tube.
Introducción
La pancreatitis aguda (PA) es uno de los trastornos gastrointestinales más frecuentes, sus principales etiologías son los cálculos biliares y el alcohol 1,2.
Según los criterios de Atlanta, para su diagnóstico se requieren dos de los tres siguientes criterios: dolor abdominal compatible con PA, amilasa o lipasa elevados 3 veces sobre el límite superior normal, e imágenes características de PA demostradas por estudios de imagen 3,4.
El 80 % de los casos tiene un curso leve, mientras que un 20 % corresponde a pancreatitis moderadamente grave y grave. De estas, el 33 % presentará una necrosis infectada, alcanzando una mortalidad de aproximadamente 15 %-35 %, siendo la sepsis la principal determinante de la misma. 5.
Consecuencias de la restricción de la dieta
En 1904 el médico ruso Iván Pávlov ganó el premio Nobel en Medicina por sus trabajos en animales, sobre la fisiología de la digestión y la respuesta a los estímulos sobre la secreción de distintas glándulas. Esto fue extrapolado por otros investigadores, quienes asumieron que suprimir el estímulo alimenticio evitaría las distintas fases de la secreción pancreática y, por consiguiente, la liberación de enzimas y mayor daño tisular, teoría que se mantuvo por varios años, incluso actualmente varios médicos ven con recelo administrar alimentos de manera temprana en la PA 6.
Los actuales conocimientos sobre la fisiopatología de la PA han demostrado que la producción de diferentes sustancias proinflamatorias, sumadas a la restricción alimenticia, conducen a una alteración en la motilidad intestinal y en la microbiota sapróbica, facilitando el sobrecrecimiento bacteriano y la alteración de la barrera intestinal, lo que permite la translocación bacteriana mediante los ganglios linfáticos hacia la circulación sistémica, donde las endotoxinas bacterianas provocan la aparición de sepsis y falla multiorgánica 7,8. Esto se observa con mayor detalle en la Figura 1.
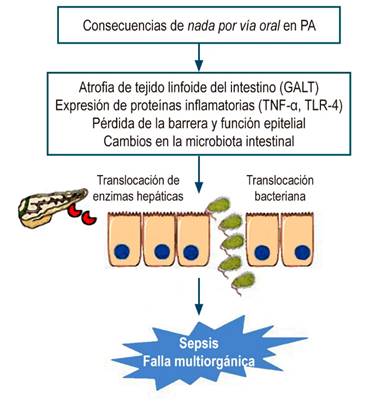
Figura 1
Consecuencias de la suspensión de la vía oral. GALT: tejido linfoide asociado con el intestino; TLR-4: receptor tipo toll-4; TNF-α: factor de necrosis tumoral alfa. Figura realizada por los autores.
Nutrición temprana
Uno de los pilares fundamentales en el tratamiento de la PA durante muchos años fue la restricción de alimentos o el llamado reposo digestivo, mientras “mejoraba” el cuadro de PA, pues se consideraba que los estímulos generados por la alimentación favorecerían la liberación y activación de las enzimas pancreáticas, y generar mayor daño tisular 9. Actualmente, no existen bases que sustenten esta creencia y se ha demostrado en diferentes estudios que el inicio temprano de la nutrición enteral (es decir, en las primeras 24 a 48 horas de haber empezado el cuadro) mejora el balance nitrogenado y disminuye la incidencia de infecciones, la mortalidad y la estancia hospitalaria, y la estimulación pancreática exocrina es mínima 10-12.
Cabe resaltar el alto gasto metabólico producido durante una PA, especialmente en las pancreatitis graves, incrementa los requerimientos de distintos nutrientes encargados de mantener la homeostasis del sistema inmune y la regeneración tisular 13. Según las guías de la European Society for Clinical Nutrition and Metabolism (ESPEN), hasta un 80 % de los casos de pancreatitis aguda grave tiene una pérdida de proteína de 40 g/día llevando hacia un balance nitrogenado negativo 14.
Nutrición enteral frente a la nutrición parenteral
Desde hace aproximadamente 3 décadas se considera que la nutrición parenteral (NP) es la mejor vía de alimentación en PA, principalmente en casos graves, pese a que se conocían sus desventajas como un mayor riesgo de infección del catéter, alteración electrolítica, falla multiorgánica, costo y dificultad de colocación 15,16. Además, se debe considerar la hiperglucemia, la cual está presente en más de la mitad de los casos de NP, y constituye un factor de riesgo adicional para infecciones y mortalidad 17,18.
El conocimiento actual sobre el papel del intestino en la fisiopatología de la PA y la seguridad y tolerabilidad de la nutrición enteral (NE) han desplazado en uso de NP 19. En el metaanálisis de Al-Omran y colaboradores, el cual incluyó a 348 personas, demostró de manera significativa el beneficio de la NE en términos de mortalidad, infección, falla multiorgánica y necesidad de cirugía en comparación con la NP 20. Estos datos fueron corroborados con dos recientes metaanálisis, el primero incluyó a 348 personas y determinó una reducción significativa de la mortalidad y la falla multiorgánica a favor de la NE 21, y el segundo incluyó a 562 personas y determinó que hubo un menor riesgo de infección y necesidad de cirugía con el uso de la NE 22.
Inicio de la nutrición
Recientemente, la Asociación Americana de Gastro-enterología recomendó comenzar la dieta en las primeras 24 horas de iniciado el cuadro, puesto que favorece la integridad y funcionalidad intestinal, mantiene las uniones intercelulares y estimula las enzimas del borde en cepillo, evitando así la translocación bacteriana 23.
En el metaanálisis de Feng y colaboradores que incluyó a 1007 pacientes se determinó el beneficio de la NE en las primeras 48 horas, en términos de falla orgánica y desarrollo del síndrome de respuesta inflamatoria sistémica (SIRS), no encontró diferencia en relación con la mortalidad y la necrosis pancreática 24.
Una reciente revisión sistemática determinó que el inicio temprano de la NE en las primeras 48 horas redujo el riesgo de necrosis infectada, falla orgánica, necesidad de cirugía y mortalidad, comparado con NE tardía y NP 25.
El metaanálisis realizado por Qi y colaboradores determinó que la NE en las primeras 24 horas se asoció con una reducción de complicaciones infeccionas y falla multiorgánica en pancreatitis aguda grave, no se encontró beneficio en pancreatitis leves y moderadamente graves 26.
Una revisión sistemática, realizada en España concluyó que el mejor momento para iniciar la dieta es cuando existe la presencia de ruidos intestinales; además, utilizaron una dieta calórica completa, la cual fue bien tolerada, por lo que se logró reducir la estancia hospitalaria y se mejoró el curso de la PA 27.
Sonda nasogástrica (SNG) frente a la sonda nasoyeyunal (SNY)
Una reciente revisión de Cochrane demostró que no existen diferencias significativas entre el uso de la SNG y SNY, ambas lograron mantener la integridad de la barrea intestinal y la primera demostró ser mejor tolerada 28. En el metaanálisis de Chang y colaboradores no se encontraron diferencias entre el uso de SNG y SNY en términos de eficacia y seguridad 29.
El uso de SNY se reserva para aquellos casos de intolerancia a la SNG, obstrucción al tracto de salida gástrico, obstrucción duodenal y balance energético negativo con el uso de SNG 30. Otro beneficio que demostró el uso de la SNG fue la reducción del dolor, de la necesidad de opioides y de la intolerancia oral 31.
Composición de la dieta
No existe un consenso general sobre la composición ideal y el tipo de dieta, ya que la evidencia actual es limitada. En numerosos estudios se ha demostrado que aquellos que toleran la vía oral se beneficiaron de dietas bajas en grasa de composición sólida o líquida; esto actualmente supondría una ventaja, debido a que la práctica de ir modificando progresivamente la consistencia de la dieta produce un incremento innecesario en los días de estancia hospitalaria 32-35.
En el estudio realizado por Endo y colaboradores en 2018 no se encontró diferencia entre el uso de fórmulas elementales, semielementales y poliméricas 36. Larino-Noia y colaboradores, en un estudio realizado en España, no encontraron diferencias en la tolerancia a la dieta, iniciando la alimentación con una dieta sólida o dieta progresiva 37.
Uso de suplementos
Se ha propuesto el uso de distintos suplementos como probióticos, prebióticos o simbióticos, por su efecto sobre la microbiota y su papel protector, trófico y metabólico; y aunque se ha encontrado que el uso de estos podría asociarse con una disminución de la estancia hospitalaria, todavía no existe evidencia suficiente para recomendar su uso de manera rutinaria 38,39.
Respecto al uso de aminoácidos como arginina y glutamina, los cuales en teoría podrían tener algún beneficio al mantener la integridad intestinal, las guías de la American Society for Parenteral and Enteral Nutrition (ASPEN) no recomiendan su uso rutinario 40.
Los ácidos grasos ω-3, antioxidantes y vitaminas, cuya capacidad antinflamatoria podría suponer un beneficio en la PA, tampoco se han recomendado de manera rutinaria, puesto que se requieren más estudios que respalden su uso 41,42. En la Tabla 1 se resumen las principales recomendaciones de la nutrición en PA.
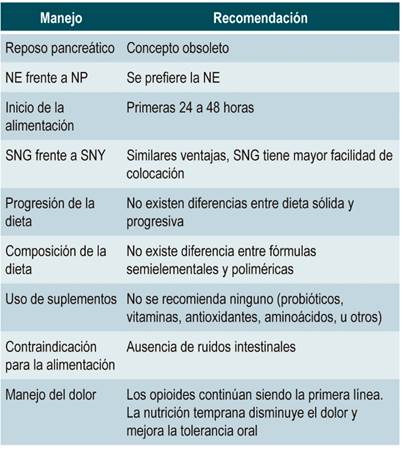
Tabla realizada por los autores.
Conclusiones
El concepto de reposo pancreático actualmente es obsoleto. El inicio temprano de la dieta no causa estimulación ni daño pancreático adicional. El efecto benéfico de la alimentación temprana sobre la barrera intestinal se asocia con una menor translocación bacteriana, menor riesgo de SIRS y menor mortalidad. La vía enteral es ampliamente superior a la parenteral. No existen diferencias entre el uso de SNG y SNY, y en caso de estar indicada, se prefiere la SNG por su facilidad de colocación. El dolor no es una indicación para suspender la dieta, por lo que es necesario optimizar la analgesia con el fin de continuar la alimentación, ya que la misma se asocia con una menor necesidad de opioides y disminución de la intensidad del dolor.
Referencias
1. Peery AF, Crockett SD, Murphy CC, Lund JL, Dellon ES, Williams JL, Jensen ET, Shaheen NJ, Barritt AS, Lieber SR, Kochar B, Barnes EL, Fan YC, Pate V, Galanko J, Baron TH, Sandler RS. Burden and Cost of Gastrointestinal, Liver, and Pancreatic Diseases in the United States: Update 2018. Gastroenterology. 2019;156(1): 254-272.e11. https://doi.org/10.1053/j.gastro.2018.08.063
2. Olson E, Perelman A, Birk JW. Acute management of pancreatitis: the key to best outcomes. Postgrad Med J. 2019;95(1124):328-333. https://doi.org/10.1136/postgradmedj-2018-136034
3. Tenner S, Baillie J, DeWitt J, Vege SS; American College of Gastroenterology. American College of Gastroenterology guideline: management of acute pancreatitis. Am J Gastroenterol. 2013;108(9):1400-15;1416. https://doi.org/10.1038/ajg.2013.218
4. Bollen TL. Acute pancreatitis: international classification and nomenclature. Clin Radiol. 2016;71(2):121-33. https://doi.org/10.1016/j.crad.2015.09.013
5. van Dijk SM, Hallensleben NDL, van Santvoort HC, Fockens P, van Goor H, Bruno MJ, Besselink MG; Dutch Pancreatitis Study Group. Acute pancreatitis: recent advances through randomised trials. Gut. 2017;66(11):2024-2032. https://doi.org/10.1136/gutjnl-2016-313595
6. Petrov MS, Pylypchuk RD, Emelyanov NV. Systematic review: nutritional support in acute pancreatitis. Alim Pharmacol Ther. 2008;28(6):704-712. https://doi.org/10.1111/j.1365-2036.2008.03786.x
7. Singh P, Garg PK. Pathophysiological mechanisms in acute pancreatitis: Current understanding. Indian J Gastroenterol. 2016;35(3):153-66. https://doi.org/10.1007/s12664-016-0647-y
8. Schietroma M, Pessia B, Carlei F, Mariani P, Sista F, Amicucci G. Intestinal permeability and systemic endotoxemia in patients with acute pancreatitis. Ann Ital Chir. 2016;87:138-44.
9. Gupta R, Patel K, Calder PC, Yaqoob P, Primrose JN, Johnson CD. A randomised clinical trial to assess the effect of total enteral and total parenteral nutritional support on metabolic, inflammatory and oxidative markers in patients with predicted severe acute pancreatitis (APACHE II > or =6). Pancreatology. 2003;3(5):406-13. https://doi.org/10.1159/000073657
10. Ramanathan M, Aadam AA. Nutrition Management in Acute Pancreatitis. Nutr Clin Pract. 2019;34 Suppl 1:S7-S12. https://doi.org/10.1002/ncp.10386
11. Vaughn VM, Shuster D, Rogers MAM, Mann J, Conte ML, Saint S, Chopra V. Early Versus Delayed Feeding in Patients With Acute Pancreatitis: A Systematic Review. Ann Intern Med. 2017;166(12):883-892. https://doi.org/10.7326/M16-2533
12. Zhang D, Li H, Li Y, Qu L. Gut rest strategy and trophic feeding in the acute phase of critical illness with acute gastrointestinal injury. Nutr Res Rev. 2019;32(2):176-182.https://doi.org/10.1017/S0954422419000027
13. Pan LL, Li J, Shamoon M, Bhatia M, Sun J. Recent advances on nutrition in treatment of acute pancreatitis. Front Immunol. 2017;8:762. https://doi.org/10.3389/fimmu.2017.00762
14. Gianotti L, Meier R, Lobo DN, Bassi C, Dejong CH, Ockenga J, Irtun O, MacFie J; ESPEN. ESPEN guidelines on parenteral nutrition: pancreas. Clin Nutr. 2009;28(4):428-35. https://doi.org/10.1016/j.clnu.2009.04.003
15. Ziegler TR. Parenteral nutrition in the critically ill patient. N Engl J Med. 2009;361(11):1088-97. https://doi.org/10.1056/NEJMct0806956
16. Storck LJ, Imoberdorf R, Ballmer PE. Nutrition in Gastrointestinal Disease: Liver, Pancreatic, and Inflammatory Bowel Disease. J Clin Med. 2019;8(8). pii: E1098. https://doi.org/10.3390/jcm8081098
17. Pasquel FJ, Spiegelman R, McCauley M, Smiley D, Umpierrez D, Johnson R, Rhee M, Gatcliffe C, Lin E, Umpierrez E, Peng L, Umpierrez GE. Hyperglycemia during total parenteral nutrition: an important marker of poor outcome and mortality in hospitalized patients. Diabetes Care. 2010;33(4):739-741. https://doi.org/10.2337/dc09-1748
18. Petrov MS, Whelan K. Comparison of complications attributable to enteral and parenteral nutrition in predicted severe acute pancreatitis: a systematic review and meta-analysis. Br J Nutr. 2010;103(9):1287-95. https://doi.org/10.1017/S0007114510000887
19. Petrov MS. Gastric feeding and “gut rousing” in acute pancreatitis. Nutr Clin Pract. 2014;29(3):287-90. https://doi.org/10.1177/0884533614528986
20. Al-Omran M, Albalawi ZH, Tashkandi MF, Al-Ansary LA. Enteral versus parenteral nutrition for acute pancreatitis. Cochrane Database Syst Rev. 2010;(1):Cd002837. https://doi.org/10.1002/14651858.CD002837.pub2
21. Yao H, He C, Deng L, Liao G. Enteral versus parenteral nutrition in critically ill patients with severe pancreatitis: a meta-analysis. Eur J Clin Nutr. 2018;72(1):66-68. https://doi.org/10.1038/ejcn.2017.139
22. Wu P, Li L, Sun W. Efficacy comparisons of enteral nutrition and parenteral nutrition in patients with severe acute pancreatitis: a meta- analysis from randomized controlled trials. Biosci Rep. 2018;38(6):pii: BSR20181515. https://doi.org/10.1042/BSR20181515
23. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN; American Gastroenterological Association Institute Clinical Guidelines Committee. American Gastroenterological Association Institute Guideline on Initial Management of Acute Pancreatitis. Gastroenterology. 2018;154(4):1096-1101. https://doi.org/10.1053/j.gastro.2018.01.032
24. Feng P, He C, Liao G, Chen Y. Early enteral nutrition versus delayed enteral nutrition in acute pancreatitis: A PRISMA compliant systematic review and meta-analysis. Medicine (Baltimore). 2017;96(46):e8648. https://doi.org/10.1097/MD.0000000000008648
25. Song J, Zhong Y, Lu X, Kang X, Wang Y, Guo W, Liu J, Yang Y, Pei L. Enteral nutrition provided within 48 hours after admission in severe acute pancreatitis: a systematic review and meta-analysis. Medicine (Baltimore). 2018;97(34):e11871. https://doi.org/10.1097/MD.0000000000011871
26. Qi D, Yu B, Huang J, Peng M. Meta-Analysis of Early Enteral Nutrition Provided Within 24 Hours of Admission on Clinical Outcomes in Acute Pancreatitis. JPEN J Parenter Enteral Nutr. 2018;42(7):1139-1147. https://doi.org/10.1002/jpen.1139
27. Valverde-López F, Wilcox CM, Redondo-Cerezo E. Evaluation and management of acute pancreatitis in Spain. Gastroenterol Hepatol. 2018;41(10):618-628. https://doi.org/10.1016/j.gastrohep.2018.06.012
28. Moggia E, Koti R, Belgaumkar AP, Fazio F, Pereira SP, Davidson BR, Gurusamy KS. Pharmacological interventions for acute pancreatitis. Cochrane Database Syst Rev. 2017;4(4):CD011384. https://doi.org/10.1002/14651858.CD011384.pub2
29. Chang YS, Fu HQ, Xiao YM, Liu JC. Nasogastric or nasojejunal feeding in predicted severe acute pancreatitis: a meta-analysis. Crit Care. 2013;17(3):R118. https://doi.org/10.1186/cc12790
30. Faghih M, Fan C, Singh VK. New Advances in the Treatment of Acute Pancreatitis. Curr Treat Options Gastroenterol. 2019;17(1):146-160. https://doi.org/10.1007/s11938-019-00223-8
31. Petrov MS, McIlroy K, Grayson L, Phillips AR, Windsor JA. Early nasogastric tube feeding versus nil per os in mild to moderate acute pancreatitis: a randomized controlled trial. Clin Nutr. 2013;32(5): 697-703. https://doi.org/10.1016/j.clnu.2012.12.011
32. Li J, Chen J, Tang W. The consensus of integrative diagnosis and treatment of acute pancreatitis-2017. J Evid Based Med. 2019;12(1):76-88. https://doi.org/10.1111/jebm.12342
33. Vege SS, DiMagno MJ, Forsmark CE, Martel M, Barkun AN. Initial medical treatment of acute pancreatitis: American Gastroenterological Association Institute technical review. Gastroenterology. 2018;154(4):1103-1139. https://doi.org/10.1053/j.gastro.2018.01.031
34. Lodewijkx PJ, Besselink MG, Witteman BJ, Schepers NJ, Gooszen HG, van Santvoort HC, Bakker OJ; Dutch Pancreatitis Study Group. Nutrition in acute pancreatitis: a critical review. Expert Rev Gastroenterol Hepatol. 2016;10(5):571-80. https://doi.org/10.1586/17474124.2016.1141048
35. Roberts KM, Nahikian-Nelms M, Ukleja A, Lara LF. Nutritional Aspects of Acute Pancreatitis. Gastroenterol Clin North Am. 2018;47(1):77-94. https://doi.org/10.1016/j.gtc.2017.10.002
36. Endo A, Shiraishi A, Fushimi K, Murata K, Otomo Y. Comparative effectiveness of elemental formula in the early enteral nutrition manage- ment of acute pancreatitis: a retrospective cohort study. Ann Intensive Care. 2018;8(1):69. https://doi.org/10.1186/s13613-018-0414-6
37. Lariño-Noia J, Lindkvist B, Iglesias-García J, Seijo-Ríos S, Iglesias-Canle J, Domínguez-Muñoz JE. Early and/or immediately full caloric diet versus standard refeeding in mild acute pancreatitis: a randomized open-label trial. Pancreatology. 2014;14(3):167-73. https://doi.org/10.1016/j.pan.2014.02.008
38. Tian X, Pi YP, Liu XL, Chen H, Chen WQ. Supplemented Use of Pre-, Pro-, and Synbiotics in Severe Acute Pancreatitis: An Updated Systematic Review and Meta-Analysis of 13 Randomized Controlled Trials. Front Pharmacol. 2018;9:690. https://doi.org/10.3389/fphar.2018.00690
39. Ballesteros Pomar MD, González Arnaiz E. Role of prebiotics and probiotics in the functionality of the microbiota in the patients receiving enteral nutrition. Nutr Hosp. 2018;35(Spec no2):18-26. https://doi.org/10.20960/nh.1956
40. McClave SA, Taylor BE, Martindale RG, Warren MM, Johnson DR, Braunschweig C, McCarthy MS, Davanos E, Rice TW, Cresci GA, Gervasio JM, Sacks GS, Roberts PR, Compher C; Society of Critical Care Medicine; American Society for Parenteral and Enteral Nutrition. Guidelines for the Provision and Assessment of Nutrition Support Therapy in the Adult Critically Ill Patient: Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N.). JPEN J Parenter Enteral Nutr. 2016;40(2):159-211. https://doi.org/10.1177/0148607115621863
41. Lei QC, Wang XY, Xia XF, Zheng HZ, Bi JC, Tian F, Li N. The role of omega-3 fatty acids in acute pancreatitis: a meta-analysis of randomized controlled trials. Nutrients. 2015;7(4):2261-73. https://doi.org/10.3390/nu7042261
42. Jeurnink SM, Nijs MM, Prins HA, Greving JP, Siersema PD. Antioxidants as a treatment for acute pancreatitis: A meta-analysis. Pancreatology. 2015;15(3):203-8. https://doi.org/10.1016/j.pan.2015.03.009
Notas
Notas de autor
*Correspondencia: William Otero-Regino. waoteror@gmail.com
Declaración de intereses
