Comunicaciones
EXPRESIÓN DE UNA PROTEÍNA DE 70 k DA DU R A NTE LA DEGRADACIÓN DE COMBUSTIBLE DIESEL Y ANTRACENO POR Pseudomonas luteola
EXPRESSION OF A 70kDA PROTEIN DURING THE DEGRADATION OF DIESEL FUEL AND ANTHRACENE BY Pseudomonas luteola
EXPRESSÃO DE UMA PROTEÍNA DE 70kDA DURANTE A DEGRADAÇÃO DE COMBUSTIVEL DIESEL E ANTRACENO POR Pseudomonas luteola
EXPRESIÓN DE UNA PROTEÍNA DE 70 k DA DU R A NTE LA DEGRADACIÓN DE COMBUSTIBLE DIESEL Y ANTRACENO POR Pseudomonas luteola
Interciencia, vol. 42, núm. 1, pp. 28-32, 2017
Asociación Interciencia
Recepción: 11/07/2014
Corregido: 01/11/2016
Aprobación: 03/12/2016
Financiamiento
Fuente: Consejo de Desarrollo Científico y Humanístico de la Universidad de Carabobo (CDCH-UC)
Nº de contrato: AM-056-2013
Beneficiario: Valeria Ricoy, Carlos Moreno y Oscar Valbuena
Resumen: La incorporación de nutrientes al citoplasma bacteriano requiere la interacción física entre el sistema membranoso de la célula y las moléculas/iones a ser internalizados. A tal efecto el transporte lo efectúan proteínas (porinas) que actúan como transportadores/canales proteicos. Este trabajo demuestra que durante la degradación del combustible diesel (CD) o antraceno (A) por Pseudomonas luteola PB6, se expresa una proteína de 70kDa ubicada en la fracción membranosa bacteriana. La aparición de p70 en la membrana ocurre a las 4 y 24 h después de su cultivo en medios minerales mínimos suplementados con CD o A como única fuente de carbono, lo cual indica que p70 es un producto inducido por la presencia del hidrocarburo. Mientras p70 esta implicada en el transporte del hidrocarburo a través de la membrana, la metabolización de CD es efectuada por enzimas ubicadas en la fracción citosólica bacteriana, no detectándose actividad en la fracción membranosa de P. luteola.
Palabras clave: Antraceno, Biodegradación, Diesel, P. luteola, Proteínas de Membrana.
Abstract: The passage of nutrients to the bacterial cytoplasm implies an initial physical interaction between the membrane system and the molecules/ions to be internalized. Such an event is mediated by specific proteins (porins), which work as carriers or protein channels. This study shows that during the degradation of diesel fuel (DF) or anthracene (A) by Psuedomonas luteola PB6, a 70kDa membrane-bound protein is expressed. When bacteria are grown in minimal mineral media supplemented with DF or A as the sole carbon source, p70 is detected in the bacterial membrane after 4 and 24h incubation times, respectively, indicating that p70 is induced by the hydrocarbons. Thus, p70 is involved in hydrocarbon transport through the membrane, while the DF metabolization is carried out by enzymes located in the cytosolic fraction, absent from the bacterial membranous fraction.
Resumo: A incorporação de nutrientes ao citoplasma bacteriano requer a interação física entre o sistema membranoso da célula e as moléculas/ions a ser internalizados. A tal efeito o transporte é efetuado por proteínas (porinas) que atuam como transportadores/canais protéicos. Este trabalho demonstra que durante a degradação do combustível diesel (CD) ou antraceno (A) por Pseudomonas luteola PB6, se expressa uma proteína de 70kDa localizada na fração membranosa bacteriana. A aparição de p70 na membrana ocorre às 4 e 24 h após o seu cultivo em meios minerais mínimos suplementados com CD ou A como única fonte de carbono, o qual indica que p70 é um produto induzido pela presença do hidrocarboneto. Enquanto p70 está implicada no transporte do hidrocarboneto através da membrana, a metabolização de CD é efetuada por enzimas localizadas na fração citosólica bacteriana, não sendo detectada atividade na fração membranosa de P. luteola.
Introducción
La incorporación de material nutritivo al citoplasma celular implica una interacción física inicial entre el sistema membranoso de la célula y las moléculas a ser incorporadas (Hearn et al., 2008; Wiener y Horanyi, 2011). En bacterias Gram negativas se han descrito dos barreras membranosas, la membrana externa (ME) y la plasmática (MP); ambas delimitan el espacio periplásmico y la última el contenido citoplásmatico (Prescott et al., 2004). El paso de materiales a través de la ME es efectuado por transportadores o canales proteicos, denominados porinas (Tommassen, 2010), mediante procesos de difusión facilitada. En varios géneros bacterianos se han caracterizado las proteínas implicadas en estos procesos de transporte, diferenciándose transportadores de moléculas hidrofílicas e hidrofóbicas (Hearn et al., 2008; Van den Berg, 2010; Lepore et al., 2011). Cuando las moléculas ingresan al espacio periplásmico (DiRusso y Black, 2004, Van den Berg et al., 2004; Van den Berg., 2005; Hearn et al., 2008), las permeasas ubicadas en la MP incorporan el material al citosol bacteriano, donde tiene lugar su metabolización por sistemas enzimáticos específicos (Black, 2004; Wentzel et al., 2007; Rojo 2009; Kumari et al., 2013). En trabajos previos se ha reportado que Pseudomonas luteola crece en medios mínimos minerales suplementados con combustible diesel (MMMD) o antraceno (MMMA), expresando una proteína de 70kDa (p70) localizada en la fracción membranosa (FM) de la bacteria (Ricoy et al., 2012; Díaz et al., 2013a). En el presente estudio se evaluó la expresión de la p70 en MMMA, se determinó el tiempo de detección de p70 en la membrana al transferirse la bacteria de medio nutritivo a los medios restrictivos MMMD y MMMA y se evaluó la capacidad de degradación del combustible diesel (CD) presente en MMMD, por las fracciones membranosa (FM) y citosólica (FC) de P. luteola.
Materiales y Métodos
Cepa bacteriana
Peudomonas luteola PB6, cepa aislada de suelos contaminados con petróleo, fue suministrada por el Laboratorio de Biotecnología, Departamento de Biología, Facultad de Ciencias y Tecnología, Universidad de Carabobo, Venezuela (Ricoy et al., 2012).
Medios de cultivo
La cepa bacteriana fue cultivada en varios medios de cultivo, de acuerdo a la finalidad de cada experimento. El medio MMMD estuvo compuesto por las siguientes sales minerales (m/v): CaCl2 1%; CuSO4 1%; FeSO4 0,5%; MgSO4 1%; ZnSO4.7H2O 1%; NaCl 1%; (NH4)2SO4 1% disueltas en tampón fosfato 0,1M y pH7,0; y combustible diesel 1% (v/v). El medio MMMA estuvo compuesto por las mismas sales minerales, pero suplementado con antraceno 0,01% (m/v). El medio MMMAP por sales minerales suplementado con antraceno 0,01% (m/v) y peptona 1% (m/v) (HIMEDIA). Para la reactivación bactiana se utilizó medio caldo nutritivo (HIMEDIA) (Díaz et al., 2013a; Ricoy, 2014).
Cultivo de la cepa bacteriana
Para evidenciar la presencia de p70 en la fracción membranosa de la bacteria, P. luteola fue reactivada en caldo nutritivo, transfiriéndose luego 1ml de cultivo a los medios restrictivos, e incubándose con agitación continua (90rpm) a 36ºC durante 3 días en estufa (medio MMMD) o 10 días en baño maría (medio MMMA). Alícuotas (1ml) de los cultivos en MMMD se retiraron a intervalos de 1h hasta completar 8h de incubación; en el caso de cultivos en MMMA, las alícuotas se colectaron cada 24h hasta alcanzar 240h. Finalmente, las alícuotas fueron procesadas para obtener las fracciones FM y FC, y el posterior análisis de los respectivos perfiles polipeptídicos electroforéticos.
Obtención de las fracciones membranosas y citosólicas de P. luteola
Las alícuotas colectadas de los cultivos previamente descritos se centrifugaron durante 30min a 20000g; el sobrenadante se descartó y el sedimento bacteriano se resuspendió en tampón de lisis conteniendo NaCl 500mM, Tris-HCl 20mM, 2-mercaptoetanol 1mM, imidazol 5mM, triton X-100 0,1% (v/v) y EDTA 100mM, pH 8,0 (Sambrook y Russell, 2001), y se sometió a tres ciclos de sonicación (Ultrasonic Cell Disrupter Virsonic 100) en hielo de 45s de duración. Las fracciones citosólicas sobrenadantes (FC) y membranosas sedimentadas (FM) se obtuvieron por centrifugación a 4700g durante 15min. Ambas fracciones fueron analizadas por electroforesis en geles de poliacrilamida para determinar los perfiles polipeptídicos.
Electroforesis en geles de poliacrilamida
Las fracciones FC y FM se mezclaron con 5µl de tampón de aplicación de muestra 4X completándose el volumen final a 20µl con agua destilada estéril y calentándose durante 3min en agua hirviente. Las muestras se depositaron en los pozos de un gel de poliacrilamida al 10% (m/v) y la corrida electroforética se realizó aplicando 100V por 1-2h a temperatura ambiente (Laemmli, 1970). Para la visualización de los polipéptidos, los geles fueron teñidos con plata (Chevallet et al., 2006).
Capacidad degradadora de diesel por las fracciones de P. luteola
Se utilizó 0,5ml de cultivo bacteriano en medio MMMD, que fue transferido a 50ml del mismo medio e incubado durante tres días. Se tomó 2ml de estos cultivos y se centrifugaron, obteniéndose las células bacterianas. Las fracciones FM y FC se obtuvieron por centrifugación y posterior lisis, según lo establecido anteriormente. Las fracciones FC y FM se incubaron individualmente en 50ml de medio MMMD tomándose alícuotas a las 0 y 48h de incubación. El combustible diesel (CD) remanente se determinó por gravimetría, en vasos de precipitados previamente tarados, después de realizar dos ciclos de extracción del cultivo con hexano y evaporar las fases orgánicas a 80ºC. Como sistema control, también se incubó y procesó el medio MMMD, en las mismas condiciones, sin adicionar las fracciones bacterianas.
Resultados
Los patrones polipeptídicos electroforéticos de las fracciones subcelulares FM y FC de P. luteola, en los medios MMMA y MMMD, se muestran en la Figura 1. La proteína p70 se detectó en la fracción FM de ambos cultivos, estando ausente en la fracción FC. El tiempo de aparición de p70 en FM, luego de su transferencia de caldo nutritivo a medios restrictivos, se muestra en la Figura 2, observándose que p70 aparece a las 4h de su cultivo en MMMD; contrariamente, la señal a 70kDa no se detectó en la FM después de su transferencia por 11h al medio MMMA (Figura 3). En vista de este comportamiento en MMMA, se decidió evaluar el efecto que podría ejercer la presencia de una fuente fácilmente metabolizable, como lo es la peptona, en presencia de antraceno (medio MMMAP). A las 11h de incubación no se detectó la p70 (resultados no mostrados); no obstante, al incrementar los tiempos de cultivo en medios MMMA y MMMAP, la p70 fue detectada en la FM a las 24h de cultivo en MMMA (Figura 4) y a las 43h en medio MMMAP (Figura 5).
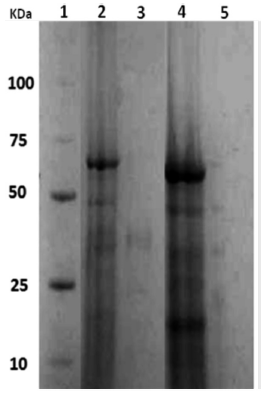
Figura 1
Electroforesis en geles de poliacrilamida de los extractos proteicos de la FM y FC de P. luteola crecida en MMM con CD o con antraceno como única fuente de carbono. 1: marcadores de peso molecular; 2 y 3: FM y FC de P. luteola crecida con CD, respectivamente; 4 y 5: FM y FC de P. luteola crecida con antraceno, respectivamente.

Figura 2
Electroforesis en geles de poliacrilamida de los extractos proteicos de la fracción de membrana de P. luteola crecida en medio con diesel como única fuente de carbono (MMMD) a distintos tiempos de inoculación. 1: marcadores de peso molecular; 2, 3, 4, 5 y 6: incubaciones a 1, 2, 4, 5 y 6h, respectivamente. El asterisco indica la presencia de la proteína p70kDa.

Figura 3
Electroforesis en geles de poliacrilamida de los extractos proteicos de la fracción de membrana de P. luteola crecida con antraceno como única fuente de carbono (MMMA) a distintos tiempos de inoculación. 1: marcador de peso molecular; 2: medio de cultivo no inoculado; 3 al 13: FM de las incubaciones a las 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 y 11h, respectivamente.

Figura 4
Electroforesis en gel de poliacrilamida de los extractos proteicos de la FM de P. luteola crecida en los MMMA, MMMAP a distintos tiempos de inoculación. 1: marcadores de peso molecular; 2, 4 y 6: FM de las incubaciones en MMMA, a las 22, 23 y 24h, respectivamente; 3, 5 y 7: FM de las incubaciones en MMMAP a las 22, 23 y 24h, respectivamente; 8 y 9: medios de cultivo no incubados. El asterisco indica la presencia de la proteína p70kDa.

Figura 5
Electroforesis en geles de poliacrilamida de los extractos proteicos de la fracción de membrana de P. luteola crecida con antraceno y peptona como fuentes de carbono (MMMAP) a distintos tiempos de inoculación. 1: marcadores de peso molecular; 2 al 8: FM de las incubaciones a las 23, 25, 28, 33, 38, 43 y 49h, respectivamente. El asterisco indica la presencia de la proteína p70kDa.
Para evidenciar la capacidad de las fracciones FC y FM para metabolizar el combustible diesel, las fracciones obtenidas de cultivos bacterianos en medio MMMD fueron incubadas en el mismo medio. Luego de la incubación, los patrones polipeptídicos obtenidos a 0 y 48h (Figura 6) mostraron un consumo mayor de CD en la FC (0,11g) y un nivel bajo en la FM (0,01g). En el sistema control (medio MMMD sin células o fracciones subcelulares) incluido en estos experimentos también se detectó un descenso bajo de CD (0,05g) similar al de la FM, probablemente debido a volatilización de algunos componentes del CD (Palittapongarnpim et al., 1998).
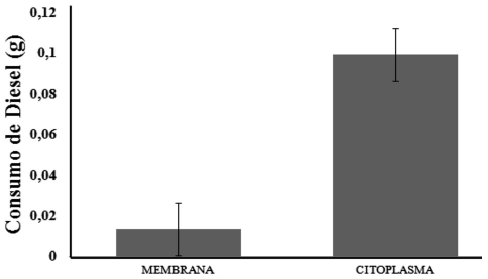
Figura 6
Consumo de CD por fracciones subcelulares de P. luteola.
Discusión
Varios autores han reportado la capacidad degradadora de antraceno por parte de algunos microorganismos (Kanaly y Harayama, 2000; Bracho et al., 2004; Ting et al., 2009; Kumar et al., 2010), así como la del combustible diesel (Singh y Lin, 2008; Adeline et al., 2009; Shukor et al., 2009; Kebria et al., 2009; Olagide y Ogbeifun, 2010; Mayz et al., 2013). En este estudio el crecimiento máximo de P. luteola en medios complementados con A o con CD diesel como única fuente de carbono, fue alcanzado a los 3 y 10 días de cultivo, respectivamente. El perfil polipeptídico de la fracción de membranas evidenció la presencia de la p70 en cultivos suplementados con los hidrocarburos adicionados individualmente, lo cual indica que la p70 esta involucrada en la degradación de moléculas hidrocarbonadas (hidrofóbicas) independientemente de su estructura química, aromática cíclica o parafínica lineal/ramificada. La p70 probablemente es codificada por una secuencia localizada en un plásmido de 11Kpb de P. luteola aislada de suelos contaminados con hidrocarburos (Ricoy et al., 2012), como ha sido reportado por Lacal et al. (2013) y su presencia en la FM bacteriana depende de la disponibilidad de hidrocarburos en el medio de cultivo (Díaz et al., 2013a, b). En ese sentido, p70 es un producto inducible, situación que ha sido reportada para otras cepas bacterianas (Kahng et al., 2000; Rojo, 2009; Gunasekera et al., 2013; Nikolaki et al., 2014).
El tiempo en detectar p70 en la FM varía de acuerdo con la estructura del hidrocarburo. En presencia de CD p70 aparece a las 4h de su transferencia de caldo nutritivo al medio MMMD, mientras que en medio MMMA su presencia se detecta a las 24h de la transferencia. La diferencia en los tiempos de aparición de p70 en la FM podría atribuirse a que A es una molécula pura y CD es una mezcla heterogénea de hidrocarburos, entre ellos alcanos de diferentes pesos moleculares y estructuras; tal vez la aromaticidad/hidrofobicidad de A y CD interaccionan con diferentes afinidades con los elementos moleculares que permiten la transcripción de los genes codificados en el plásmido de 11Kpb de P. luteola, o que las diferentes moléculas presentes en CD actúan interaccionando con varios elementos importantes en la activación de genes, situación no valedera para A. El tiempo de aparición de p70 también depende de la composición del medio de cultivo, fundamentalmente de las fuentes carbonadas (Lâzâroaie, 2008). La presencia simultanea en el medio de cultivo de la peptona (P) y A retarda la aparición de p70 en las membranas, ocurriendo a las 23h en medio MMMA y 43 h en medio MMMAP. El retardo probablemente se debe a que al comienzo de la incubación las células consumen la peptona, material fácilmente metabolizable; una vez agotada esta fuente de carbono, la bacteria debe adaptar su maquinaria enzimática y de transcripción (Hernández-Arranz et al., 2013) para el uso de A, molécula de más difícil metabolización. Otra alternativa podría implicar la represión de transportadores de glucosa asociados a membrana, inducida por compuestos aromáticos y descrita en Pseudomonas putida CSV86 (Shrivastava et al., 2011).
La función transportadora de p70, inferida en trabajos previos (Díaz et al., 2013), fue corroborada mediante la incubación de las fracciones FM y FC en medio MMMD; en estos sistemas el consumo de CD fue mayoritario en la fracción FC, descartando así el posible papel enzimático de p70 en la metabolización de CD. Estos resultados fueron comparados con análisis estadísticos multivariados (datos no mostrados). Similares situaciones han sido observadas en E. coli DH5α transformada con un plásmido de 11Kpb aislado de P. luteola (Ricoy et al., 2012). Finalmente, la proteína p70 ubicada en la fracción membranosa de la bacteria actúa como un transportador/canal proteico específico para hidrocarburos (Van den Berg, 2010; Wiener y Horanyi, 2011), independientemente de la estructura química, aromática cíclica (antraceno) o alifática (alcanos constituyente del combustible diesel) de las moléculas hidrofóbicas a ser transportadas al citoplasma bacteriano.
Agradecimientos
Los autores agradecen el financiamiento otorgado por el Consejo de Desarrollo Científico y Humanístico de la Universidad de Carabobo (CDCH-UC), ayuda menor AM-056-2013, Julio 2013.
REFERENCIAS
Adeline SY, Ting C, Tan Aw CS (2009) Hydrocarbon degradation by isolated Pseudomonas lundensis UTARFP2. Mal. J. Microbiol. 5: 104-108.
Black JG (2004) Microbiology: Principles and Explorations. 6. ed. Wiley. Nueva York, EEUU. pp. 82, 103, 136.
Bracho M, Díaz L, Soto L (2004) Biodegradación de hidrocarburos aromáticos policíclicos hetericíclicos por Pseudomonas spp. Ciencia. 12: 269-275.
Chevallet M, Luche S, Rabilloud T (2006) Silver staining of proteins in polyacrylamide gels. Nat. Protoc. 1: 1852-1858.
Díaz J, Ricoy C, Moreno C, Ricoy V, Pérez V, Valbuena O (2013a) Incorporación de alcanos por bacterias degradadoras de hidrocarburos mediada por una proteína de 70KDa unida a membranas durante la biodegradación de combustible diesel. Interciencia 38: 437-442.
Díaz E, Jimenez JI, Nogales J (2013b) Aerobic degradation of aromatic compounds. Curr. Opin. Biotechnol. 24: 5431-5442.
DiRusso CC, Black PN (2004) Bacterial long chain fatty acid transport. Gateway to a fatty acid responsive signaling system. J. Biol. Chem. 279: 49563-49566.
Gunasekera TS, Striebich RC, Mueller SS, Strobe EM, Ruiz ON (2013) Transcriptional profiling suggests that multiple matabolic adaptations are required for effective proliferaion of Pseudomanas aeruginosa in jet fuel. Environ. Sci. Technol. 47: 13449-13458.
Hearn EM, Patel DR, Van den Berg B (2008) Outer membrane transport of aromatic hydrocarbons as a first step in biodegradation. Proc. Natl. Acad. Sci. USA 105: 8601-8606.
Hernández-Arranz S, Moreno R, Rojo F (2013) The translational repressor Crc controls the Pseudomonas putida benzoate and alkane catabolic pathways using a multi-tier regulation strategy. Environ. Microbiol. 15: 227-241.
Kahng HY, Eyrne AM, Olsen RH, Kukor JJ (2000) Characterization and role of tbux in utilization of toluene by Ralstonia pickettii PK01. J. Bacteriol. 182: 1232-1242.
Kanaly R, Harayama S (2000) Biodegradation of high molecular weight polycyclic aromatic hydrocarbons by bacteria. J. Bacteriol. 182: 2059-2067.
Kebria DY, Khodadadi A, Ganjidoust H, Badkoubs I, Amoozegar MA (2009) Isolation and characterization of a novel native Bacillus straincapable of degrading diesel fuel. Int. J. Environ. Sci. Tech. 6: 435-442.
Kumar G, Singla R, Kumar R (2010) Plasmid associated anthracene degradation by Pseudomonas sp isolated from filling station site. Nat. Sci. 8: 89-94.
Kumari B, Singh SN, Farah D, Sharma M, Pandey V, Singh DP (2013) Elucidation of pyrene degradation pathway in bacteria. Adv. Biores. 4: 151-160.
Lacal, J, Reyes-Darias JA, García-Fontana C, Ramos JL, Krell T (2013) Tactic response to pollutants and their potential increase biodegradation efficiency. J. Appl. Microbiol. 114: 923-933.
Laemmli U (1970) Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature. 227: 680-685.
Lâzâraie MM (2008) Pseudomonas aeruginosa IBBM61 adaptations to high concentrations of hydrocarbons. Elect. J. Biol. 4: 17-26.
Lepore BW, Indic M, Pham H, Hearn EM, Patel DR and Van den Berg B (2011) Ligandgated diffusion across the bacterial outer membrana. Proc. Natl. Acad. Sci. USA 108: 10121-10126.
Mayz J, Manzi L, Laréz A (2013) Isolation, characterization and identification of hydrocarbonoclastic Pseudomonas species inhabitating the rhizosphera of Crotolaria micans Link. Eur. J. Exp. Bio. Sci. 3: 313-321.
Nikolaki A, Papadioti A, Avaniti K, Kassotaki E, Langer JD, Tsiotis G (2014) The membrane complexome of a new Pseudomonas strain during growth on lysogeny broth medium and containing glucose or phenol. EuPA Open Proteom. 4: 1-9.
Olagide PO, Ogbeifun LB (2010) Hydrocarbon biodegrading potentials of Proteus vulgaris strain isolated from fish samples. Amer. J. Appl. Sci. 7: 922-928.
Palittapongarnpim M, Pokethitiyook P, Upatham ES, Tangbanluekal L (1998) Biodegradation of crude oil by soil microorganisms in the tropic. Biodegradation 9: 83-90.
Prescott L, Harley J, Klein D (2004) Microbiología. 5. ed. Mc GrawHill Interamericana. Madrid, España. pp. 95-145.
Ricoy V (2014) Evaluación de la expresión de la proteína p70 de Pseudomonas luteola durante la degradación de combustible diesel y antraceno. Tesis. Universidad de Carabobo. 48 pp.
Ricoy C, Boulé N, Amaíz L, Torcuatt E, Medina L, Valbuena O y Fernández Z (2012) Transferencia de la capacidad degradadora de combustible diesel a Escherichia coli DH5α por plásmidos de bacterias aisladas de suelos contaminados con petróleo. Interciencia 37: 671-677.
Rojo F (2009) Degradation of alkanes by bacteria. Env. Microbiol. 11: 2477-2490.
Sambrook J, Russell DW (2001) A Laboratory Manual. 3. ed. Cold Spring Harbor Laboratory Press. Nueva York, EEUU. 1558 pp.
Shukor MY, Hassan NAA, Jusoh AZ, Perumel N, Shamaan NA, McCormack W, Syed MA (2009) Isolation and characterization of a Pseudomonas diesel degrading strain from Antarct. J. Environ. Biol. 30: 1-6.
Singh C, Lin J (2008) Isolation and characterization of diesel oil degrading indigenous microorganisms in Kwazulu-Natal, South Africa. Afr. J. Biotechnol. 7: 1927-1952.
Shrivastava R, Basu B, Godbole A, Mathew MK, Apte SK, Phale PS (2011) Repression of the glucose-inducible outer membrane protein OprB during utilization of aromatic compounds and organic acids in Pseudomonas putida CSV86. Microbiology 157: 1531-1540.
Ting ASY, Tan CHC, Aw CS (2009) Hydrocarbon degradation by isolated Pseudomonas lundensis UTAR FPE2. Malay. J. Microbiol. 5: 104-108.
Tommassen J (2010) Assambly of outer-membrane proteins in bacteria and mitocondria. Microbiology 156: 2587-2596.
Van den Berg B (2005) The FadL family: unusual transporters for unusual substrate. Review. Curr. Opin. Struct. Biol. 15: 401-407.
Van den Berg B (2010) Going forward laterally: transmembrane passage of hydrophobic molecules through protein cannel walls. Chembiochem. 11: 1339-1343.
Van den Berg B, Black PN, Clemons WMJr, Rapoport TA (2004) Crystal structure of long-chain fatty acid transport FadL. Science 304: 1506-1509.
Wentzel A, Ellingsent T, Kotlar HK, Zotchew SB, Throne-Holts M (2007) Bacterial metabolism of long chain nalkanes. Appl. Microbiol. Biotechnol. 76: 1209-1221.
Wiener M, Horanyi P (2011) Howhydrophobic molecules traverse the outer membranes of Gram negative bacteria. Proc. Natl. Acad. Sci. USA 108: 10929-10930.
Notas de autor