Comunicaciones
PROPIEDADES NUTRACÉUTICAS DE Morchella vulgaris (Pers.) Boud.
NUTRACEUTICAL PROPERTIES OF Morchella vulgaris (Pers.) Boud.
PROPRIEDADES NUTRACÊUTICAS DE Morchella vulgaris (Pers.) Boud.
PROPIEDADES NUTRACÉUTICAS DE Morchella vulgaris (Pers.) Boud.
Interciencia, vol. 42, núm. 7, pp. 423-429, 2017
Asociación Interciencia
Recepción: 29 Marzo 2016
Aprobación: 01 Julio 2017
Resumen: Los hongos poseen un gran potencial para ser usados como medicina natural y representan un importante recurso nutracéutico. Morchella es uno de los géneros de hongos comestibles altamente valorados en el mundo. En este trabajo se evaluaron las propiedades nutracéuticas de M. vulgaris, el cual fue identificado por caracterización macroscópica y por secuenciación de la región ITS del ARNr. Se utilizaron los cuerpos fructíferos del hongo para realizar dos extractos, uno metanólico y otro acuoso. Se encontró que el cuerpo fructífero del hongo contine un 2,6% de vitamina C, 8,2% de proteínas y 25,4% de carbohidratos. Además contiene ácidos linoleico (51,18%), oleico (24,54%) y palmítico con 2,7%. Se realizaron pruebas de actividad biológica sobre 15 cepas bacterianas. El extracto acuoso mostró actividad contra seis cepas y el metanólico contra dos, siendo más sensibles las bacterias Gram positivas. También se evaluó la actividad sobre seis cepas de hongos filamentosos, los que fueron inhibidos por ambos extractos, siendo la más sensible Trichophyton mentagrophytes (CF25= 7,3µg·ml-1). En cuanto a capacidad antioxidante, el extracto metanólico reduce el DPPH (CA50 de 53,17µg·ml-1), mientras que el acuoso obtuvo una CA50 de 43,23µg·ml-1. Se cuantificaron 4,5µg de flavonoides totales por 1g de extracto metanólico, mientras que el extracto acuoso contiene13,25µg·g-1; finalmente, se encontró que el cuerpo fructífero contiene fenoles, ácidos fenólicos, cumarinas y anillos aromáticos con carbonilo unido y una o dos sustituciones. De acuerdo con el Instituto Nacional de Cáncer (NCI) de los EEUU, ninguno de los extractos son tóxicos.
Palabras clave: Antimicrobianos, Hongos comestibles, Nutracéutico.
Abstract: Mushrooms have a great potential to be used as natural medicine and represent an important nutraceutical resource. Morchella is one of the genres of edible mushrooms highly valued in the world. In this study, the nutraceutical properties of M. vulgaris were evaluated. The species was identified by macroscopic characterization and by sequencing of the ITS region from its RNAr. Fruitful bodies of this mushroom were used to produce two extracts, one with methanol and another with water. It was found that the fruiting body of the mushroom contained 2.6% of vitamin C, 8.2% of proteins and 25.4% of carbohydrates. In addition, they contain linoleic acid (51.18%), oleic acid (24.54%) and palmitic acid (2.7%). Biological activity tests on 15 bacterial strains were assayed, the aqueous extract showed activity against 6 strains, whereas the methanol one over 2 of them, Gram-positive bacteria being more sensitive. Activity against 6 strains of filamentous fungi was also assayed and were inhibited by both extracts, Trichophyton mentagrophytes being the most sensitive (CF25= 7.3µg·ml-1). Regarding antioxidant capacity, methanol extract reduces the DPPH (AC50 53.17µg·ml-1) whereas the aqueous one obtained a AC50 of 43.23µg·ml-1. Total flavonoids per g of methanol extract amounted to 4.5µg while the aqueous extract contains 13.25µg·g-1. The fruitin body was found to contain phenols, phenolic acids, coumarins and aromatic rings with attached carbonyl and one or two substitutions. According to the USA National Institute of Cancer (NCI) none of the extracts are toxic.
Resumo: Os fungos possuem um grande potencial para ser usados como medicina natural e representam um importante recurso nutracêutico. Morchella é um dos gêneros de fungos comestíveis altamente valorizados no mundo. Neste trabalho se avaliaram as propriedades nutracêuticas de M. vulgaris, o qual foi identificado por caracterização macroscópica e por sequenciamento da região ITS do rDNA. Utilizaram-se os corpos frutíferos do fungo para realizar dois extratos, um metanólico e outro aquoso. Foi observado que o corpo frutífero do fungo contém 2,6% de vitamina C, 8,2% de proteínas e 25,4% de carboidratos. Além disso contêm ácido linoléico (51,18%), oléico (24,54%) e palmítico com 2,7%. Foram realizadas provas de atividade biológica sobre 15 cepas bacterianas. O extrato aquoso mostrou atividade frente a seis cepas e o metanólico frente a dois, sendo mais sensíveis as bactérias Gram positivas. Também se avaliou a atividade sobre seis cepas de fungos filamentosos, os que foram inibidos por ambos extratos, sendo a mais sensível Trichophyton mentagrophytes (CF25= 7,3µg·ml-1). Em relação à capacidade antioxidante, o extrato metanólico reduz o DPPH (CA50 de 53,17µg·ml-1), enquanto que o aquoso obteve uma CA50 de 43,23µg·ml-1. Quantificaram-se 4,5µg de flavonóides totais por 1g de extrato metanólico, enquanto que o extrato aquoso contém13,25µg·g-1; finalmente, se observou que o corpo frutífero contém fenóis, ácidos fenólicos, cumarinas e anéis aromáticos com carbonila unidos e uma ou duas substituições. De acordo com e o Instituto Nacional de Câncer (NCI) dos EEUU, nenhum dos extratos são tóxicos.
Introducción
Durante miles de años, los hongos han sido valorados por la humanidad como un recurso comestible y medicinal (Wasser, 2002). La aplicación de los hongos como medicamentos se remonta al año 3000 a.C. (Moradali et al., 2007). En la medicina popular mexicana, son varias las especies de hongos macroscópicos que se emplean para el tratamiento de heridas en la piel, hemorragias, disentería, estreñimientos, úlceras, granos, etc. (Díaz-Barriga, 2002). Recientemente los hongos son considerados por ser un buen antioxidante natural, por la variedad de ácidos que contienen (Kalyoncu et al., 2010). Esto es de importancia ya que muchas enfermedades degenerativas son asociadas a que radicales libres provocan estrés oxidativo en el ADN, proteínas y otras macromoléculas, desencadenando reacciones no deseables que pueden conducir al desarrollo de padecimientos como cáncer, problemas cardiovasculares y el natural envejecimiento. Los antioxidantes son compuestos que por su estructura química reducen la formación de radicales libres y previenen o permiten tratar enfermedades causadas por el estrés oxidativo (Tsutani y Takuman, 2008). Además, los hongos pueden ser usados como un buen recurso antibiótico (Kalyoncu et al., 2010), ya que las enfermedades infecciosas representan unas de las causas de mayor mortalidad en los humanos; para el control de los patógenos que las ocasionan se utilizan numerosos antibióticos, sin embargo la resistencia a éstos ha incrementado los problemas de salud pública. La actividad antibiótica de los macromicetos está poco documentada, siendo que desde la antigüedad, en Grecia y Roma, se utilizaban hongos macromicetos como alimento y como medicamento, por lo que estas especies de hongos podrían ser fuentes de nuevos antibióticos (Yamac y Bilgili, 2006).
Por otra parte, la tradición de comer hongos en México tiene raíces ancestrales que datan de la época prehispánica (Guzmán, 1978), ya que éstos tienen un gran potencial para ser usados como una fuente de alimento nutricionalmente óptimo y como una medicina con actividad biológica, fisiológicamente benéfica y no tóxica. Es por esto que los hongos silvestres se están volviendo importantes en la dieta, por sus características nutricionales y farmacológicas (Barros et al., 2007b). Además, tienen importancia etnomicológica porque constituyen un alimento muy estimado por los indígenas de diversos grupos étnicos y, en general, por los campesinos de las regiones donde se desarrollan (Herrera y Ulloa, 1990), y contienen una enorme diversidad de biomoléculas con propiedades nutricionales y/o bioactivas. Debido a estas propiedades, son reconocidos como un alimento funcional, un valioso recurso nutracéutico y de medicina natural (Heleno et al., 2013).
Un nutracéutico puede ser definido como una substancia que puede ser considerada un alimento o parte de un alimento y que provee beneficios, médicos o a la salud, como la prevención y tratamiento de enfermedades (Andlauer y Furst, 2002).
La capacidad de algunos de los alimentos para reducir el riesgo de enfermedades crónicas se ha asociado, al menos en parte, a la ocurrencia de metabolitos secundarios (fitoquímicos) que se ha demostrado ejercen una amplia gama de actividades biológicas. En general, estos metabolitos tienen una baja potencia como compuestos bioactivos en comparación a las drogas farmacéuticas, pero cuando se ingieren con regularidad y en cantidades significativas, como parte de la dieta, pueden tener un efecto fisiológico perceptible a largo plazo (Espin et al., 2007). Se ha reportado que muchos tipos de hongos comestibles y medicinales tienen actividades fisiológicas como antioxidante, antitumorales (He et al., 2012), anti-inflamatoria, y antimicrobiana. Tal es el caso de algunas especies de Morchella (Alves et al., 2012) que han atraído a micólogos debido al alto valor comercial, apariencia y a su buen sabor, con el propósito de aplicarlo como medicina (Prasad et al., 2002), además de ser uno de los géneros de hongos comestibles altamente valorados en el mundo (Heleno et al., 2013). Sin embargo, en México hay pocos estudios acerca de las propiedades medicinales y el contenido nutricional de los hongos y en especial del género Morchella, por lo que es menester realizar más estudios de este tipo para conocer mejor nuestros recursos naturales.
Materiales y Métodos
Obtención de los hongos
Los cuerpos fructíferos de M. vulgaris fueron adquiridos en el mes de octubre de 2014, en Santa Ana Jilotzingo, Estado de México, a un ‘honguero’ local, quien señaló la zona de colecta (19º31’48’’N, 99º26’34’’O). Se realizó el depósito de un ejemplar al Herbario MEXU (Nº 29003).
Identificación del hongo
Para la identificación mediante técnicas moleculares utilizando la región ITS del ARNr, se extrajo el ADN de 10 ejemplares del hongo elegidos al azar, siguiendo el protocolo descrito por MoBio™ con el kit de extracción Ultra Clean Plant DNA Isolation, pulverizando 0,1g de muestra de tejido con nitrógeno. A partir del ADN extraído, se amplificó la región ITS del ARNr del organismo, mediante reacción en cadena de la polimerasa (), con los primers ITS5 G GA AGTA A A AGTCGTA ACAAGG e ITS4 TCCTCCG CTTATTGATATGC (White et al., 1990). La PCR se llevó cabo en un termociclador T100 de BIO-RAD™, bajo las siguientes condiciones: 95ºC 1min; 30 ciclos de 1min a 95ºC, 53ºC 1min, 72ºC 1min; 72ºC 7min; 4ºC (continuo), utilizando 0,125µl de la DNA polimerasa de MyTaq™ (5U/µl), y 5µl de Buffer 5X MyTaq™ (Bioline). Se utilizaron 2µl de una mezcla de los primers ITS 4 e ITS 5 de Sigma Aldrich (10µM) y 1,5µl del ADN aislado en 16,5µl de H2O por reacción
La secuencia del amplicon fue obtenida con el secuenciador ABI/Hitachi 3130XL (16 capilares) de Genetic Analizer en el laboratorio de secuenciación de la Facultad de Estudios Superiores (FES) Iztacala, UNAM). Dicha secuencia se analizó y editó empleando el software Geneious R7. Una vez editada se comparó con las secuencias de la base de datos del Centro Nacional para la Información de la Biotecnología (NCBI, GenBank), mediante la búsqueda BLAST para caracterizar al ejemplar.
Obtención de los extractos
Los extractos del hongo fueron obtenidos por el método de maceración (Domínguez, 1973). Se hizo una extracción secuencial, primero un extracto metanólico y posteriormente uno acuoso. Los cuerpos fructíferos secos (73,95g) se colocaron en trozos en un matraz con metanol (hongo:solvente 1:5; metanol RA 99,9% Fermont), se obtuvo el extracto metanólico crudo, el cual se filtró y destiló a presión reducida en un rotavapor (90rpm, 60ºC; marca IKA HB10). El extracto se colocó en un recipiente de vidrio con la finalidad de completar la evaporación del solvente. Después, la misma cantidad de hongo se maceró con agua, se filtró y se evaporó en una charola de vidrio sobre una parrilla (60ºC) con agitación constante. El rendimiento de los extractos se determinó por diferencia de peso con relación al peso seco del hongo, obteniendo dos extractos: MM: Fracción metanólica y MA: Fracción acuosa.
Cuantificación de carbohidratos
Se realizó la extracción de carbohidratos utilizando 1g del cuerpo fructífero deshidratado y se hizo la cuantificación por el método de Nelson-Somogy (González y Peñalosa, 2000) utilizando 1ml de la muestra problema y glucosa (200µg· ml-1) como patrón.
Determinación de carbohidratos mediante HPLC
Para la determinación de carbohidratos mediante cromatografía líquida de alta resolución (HPLC) se utilizó agua destilada como fase móvil y los patrones glucosa, fructosa, sacarosa, inulina y maltosa (Sigma). La preparación de la muestra consistió en colocar 1mg del cuerpo fructífero seco en 10ml de agua destilada, centrifugar a 14000rpm por 5min e inyectar 20µl en un HPLC marca Agilent series 1100 con detector de índice de refracción y una columna para carbohidratos Supelcogel CA (Sigma Aldrich) de 30cm× 7,8cm de diámetro interno, utilizando como fase móvil agua bidestilada, flujo constante de 13ml·min-1 a 80ºC y tiempo de recorrido total de 15min. Una vez corrida la muestra se comparó y cuantificó la concentración de cada azúcar presente según el área bajo la curva.
Cuantificación de proteínas solubles por el método de Bradford
En este caso se realizó la extracción a partir de 1g del cuerpo fructífero fresco, adicionando 20ml de mezcla metanol/cloroformo/agua 12:5:3 v/v, se homogeneizó el tejido en un mortero frío, y se centrifugó a 5000rpm, colectando el sobrenadante. Se re-extrajo el residuo agitándolo 5min con otros 5ml de mezcla metanol/ cloroformo/agua. Se centrifugó y se juntó este segundo sobrenadante con el primero. Se agregó 1ml de cloroformo y luego 1,5ml de agua; se centrifugó para separar las dos fases y se retiró la fase clorofórmica. El sobrenadante contiene las proteínas, que fueron cuantificación por el método de Bradford, utilizando como patrón albúmina bovina sérica 100µg·ml-1 y un espectrofotómetro a 595nm (González y Peñalosa, 2000).
Determinación de lípidos
Los lípidos fueron determinados utilizando un cromatógrafo de gases Modelo 6850 acoplado a un espectrómetro de masas modelo 5975C, ambos de Agilent Technologies.
Se empleó una columna capilar de 30m × 0,25mm de diámetro con 25μm de película y un f lujo inicial de 1,0ml·min-1; horno a temperatura inicial de 70ºC durante 2min; primer rampa de calentamiento a 250ºC y segunda a 300ºC por un tiempo de 28,25min; modo de inyección split con relación 50,4:1; f lujo del split 49,9ml·min-1; temperatura inicial de 250ºC; detector con 290ºC; impacto electrónico con energía de 70eV; rango de masa: 35 a 600m·z-1; barrido completo; y helio como gas de arrastre.
Se realizó una esterificación de los extractos. El primer extracto fue una muestra de hongo seco que se dejó en hexano durante una semana; se tomó de este 3ml y del extracto metanólico se tomaron 5mg. Los 3ml del extracto hexánico y los 5mg del metanólico por separado se colocaron en 100µl de un estándar interno (ácido heptadecanóico) que se dejó evaporar y se le agregaron 500µl de trifloruro de boro al 12%. La mezcla se calentó en agua hirviendo por 20min. Se le agregaron 500µl de H2O y 500µl de hexano.
La identificación de los compuestos volátiles se realizó, a partir de la inyección de 2µl de la muestra, empleando la base de datos de la biblioteca NIST Versión 8.0
Cuantificación del ácido ascórbico
El ácido ascórbico (vitamina C) fue cuantificado por titulación con el indicador 2,6-diclorofenolindofenol, el cual es reducido por el ácido ascórbico a una forma incolora. Se colocaron 2ml de una solución patrón de ácido ascórbico en un matraz Erlenmeyer de 250ml, se adicionaron 10ml de ácido acético al 10% y 50ml de agua destilada. Se tituló este contenido con la solución del indicador hasta que un color ligeramente rosado persistiera por 15s. Se calcularon los mg de ácido ascórbico equivalentes a 1ml de indicador. Para el cuerpo fructífero se titularon 2ml y se siguió el mismo procedimiento que con el patrón. Se calculó la cantidad de ácido ascórbico en porcentaje por cada g de cuerpo fructífero (Murillo, 2006).
Pruebas biológicas
Evaluación de la actividad antibacteriana. Se utilizaron 14 cepas bacterianas de importancia médica para realizar una evaluación cualitativa, de acuerdo con el método de difusión en agar de Kirby-Baüer. Se ensayaron siete cepas Gram positivas: Streptococcus mutans (ATCC 35668), Staphylococcus aureus (ATCC 12398), Staphylococcus epidermidis (ATCC 35984), Staphylococcus epidermidis (donada por la FES Cuautitlán), Staphylococcus epidermidis (ATCC 12228, donada por la Clínica Universitaria de Salud Integral (CUSI), Iztacala), Actinomyces viscosus (WFCC 449), Enterococcus faecalis (CDBB-B1533) y siete cepas Gram negativas: Pseudomonas aeruginosa (CDBB-B-999), Pantoea agglomerans (CDBB-B-959), Enterobacter aerogenes (CDBBB-958), Proteus miriabilis (caso clínico, donada por el Hospital Ángeles), Escherichia coli (caso clínico, donada por la CUSI-Iztacala), Vibrio cholerae (caso clínico) y Vibrio cholerae (CDC V12 (El Tor)).
En cada caso se impregnaron sensidiscos (Whatman Nº 1; 6mm de diámetro) con 2mg/10ml del extracto a probar; como control positivo se utilizaron sensidiscos con 25µg de cloramfenicol y como control negativo sensidiscos con 10µl del solvente empleado para diluir el extracto a evaluar (Vanden-Berghe y Vlietinck, 1991). Se incubaron durante 24h a 36ºC, para posteriormente determinar la concentración mínima inhibitoria (CMI) y la concentración mínima bactericida (CMB). Se utilizó la microtécnica de dilución en caldo (Müeller-Hinton), en donde las concentraciones empleadas fueron: 12, 10, 8, 6, 4, 2 y 1mg·ml-1. Las cajas se inocularon con 50µl del cultivo bacteriano a una concentración de 1×105 UFC/ml y se incubaron durante 24h a 36ºC (Koneman et al., 1985). Cada bioensayo se realizó por triplicado.
Evaluación de la actividad antifúngica. Se utilizaron seis cepas de hongos filamentosos con importancia médica y agrícola: Fusarium sporotrichioides (NRLL3299) Fusarium moniliforme (CDBBH-265), Trichophyton mentagrophytes (CDBB-H-1112), Aspergillus sp. (donada por Rodolfo de la Torre Almaraz, Laboratorio de Microbiología de la UBIPRO, FES Iztacala), Aspergillus niger (CDBB-H179), y Rhizoctonia lilacina (CDBB-H-306). Se llevó a cabo la evaluación cualitativa con la técnica de inhibición del crecimiento radial, utilizando una concentración de 2mg por sensidisco de los extractos a probar, como control positivo Ketoconazol (7µg) y como control negativo se utilizaron sensidiscos impregnados con 10µl del solvente utilizado para disolver los extractos (Wang y Bun, 2002). Posteriormente se determinó la concentración fungicida media (CF50) y la concentración fungicida mínima (CFM), con el método de inhibición del crecimiento radial (Wang y Bun, 2002) utilizando 6,0; 4,0; 2,0; 1,0; 0,5 y 0,25mg·ml-1 de los extractos a probar. Cada bioensayo se realizó por triplicado.
Capacidad antioxidante
Se evaluó con el método de reducción del radical 2,2-difenil1-picrilhidracil (DPPH). Se determinó la capacidad antioxidante media (CA50), utilizando concentraciones desde 2 a 100µg·ml-1. Como control positivo se utilizó catequina a las mismas concentraciones que el compuesto problema. Como blanco se utilizaron pozos con 200µl de MeOH grado HPLC y la concentración del DPPH fue 0,004%. Se midió la absorbancia a 517nm (Okusa et al., 2007). Cada determinación se realizó con cinco repeticiones. La CA50 se determinó según un modelo lineal, calculando la concentración necesaria del extracto para reducir el 50% del DPPH.
Determinación de metabolitos secundarios
Esta se realizó mediante cromatografía líquida de alta resolución. La preparación de la muestra consistió en pesar 3mg de los extractos y disolverlos en 600µl de agua destilada para inyectar 25µl en el HPLC marca Agilent series 1100, con una columna Allsphere ODS-1 (250×4,6mm), corrida isocrática con mezcla de MeOHacetonitrilo-agua (25-25-50) y flujo de 1ml·min-1. Detector de arreglo de diodos (DAD), longitud de onda de 260nm con barrido completo de 200- 400nm. Una vez corrida la muestra se obtuvieron los cromatogramas y los espectros de absorción UV de cada compuesto detectado, datos con los que se determinó el tipo de compuesto con base a Dey y Harborne (1989).
Flavonoides totales
El contenido de flavonoides totales se determinó usando una curva patrón con quercetina (0-100mg·l-1). Se tomó 10mg de cada extracto en 5ml de metanol y se mezcló 1ml de los problemas con 1ml de cloruro de aluminio (AlCl3), realizando esto por triplicado. Después de 10min de reacción a temperatura ambiente, se determinó la absorbancia a 415nm (Ramamoorthy y Bono, 2007).
Citotoxicidad
La línea de células humanas de carcinoma cervical (Ca Ski), fueron obtenidas de American Tissue Culture Collection. Las células fueron mantenidas en medio DMEM-F12 (Sigma), suplementado con suero fetal bovino al 10% (Gibco), 100μg·ml-1 de anfotericina B (Gibco) y 50μg·ml-1 de fungizona (Gibco). Las células se cultivaron en una incubadora con atmósfera de 5% CO2 a 37ºC. Las células se despegaron utilizando Tripsina-Verseno 0,5%. Se sembraron las células en una placa de cultivo de 96 pozos a una densidad de 15000 células por pozo y se dejaron incubando por 2h antes del tratamiento. Luego, las células fueron tratadas con diferentes concentraciones de los extractos (20-0,019mg·ml-1) de M. Vulgaris. Los ensayos se realizaron por triplicado. Las placas fueron incubadas por 48h en 5% CO2 y 37ºC. La solución inicial del extracto fue obtenida disolviendo la concentración requerida en DMSO. Las diluciones siguientes se realizaron asegurándose que la concentración final de DMSO en cada pozo no fuera superior al 1% (v/v). Como control positivo se utilizó doxorubicina. Al final de la incubación se evaluó la viabilidad celular mediante la tinción con Cristal Violeta (Badisa et al., 2003) y se leyó en un lector de ELISA a 595nm. Se determinó la concentración a la que se inhibe al 50% de la población celular o CI50. Los resultados fueron descritos de acuerdo al criterio del Instituto Nacional de Cáncer (NCI) de EEUU, donde las concentraciones consideradas con efecto citotóxico activo son ≤0,020mg·ml-1.
Pruebas estadísticas
A los resultados de la actividad antibacteriana se les realizó un análisis de varianza (ANOVA de dos factores. Se utilizó el paquete de cómputo estadístico Minitab (versión 16) para determinar si existen diferencias significativas entre los extractos. También se hizo un análisis de regresión lineal para la cuantificación de carbohidratos, proteínas, flavonoides, capacidad antioxidante y porcentaje de mortalidad.
Resultados y Discusión
Identificación del cuerpo fructífero
Se obtuvo una secuencia de 866 pb, de la región ITS (ITS1, 5.8S e ITS2) de Morchella vulgaris, la cual fue dada de alta en el GenBank y se le asignó el número de acceso KJ741329. Esta secuencia tuvo un porcentaje de identidad del 99,7% con la secuencia perteneciente a M. vulgaris con número de acceso JQ691493.1, mediante una búsqueda BLAST en la base de datos del NCBI.
Rendimiento de los extractos
El rendimiento del extracto acuoso (20,418%) fue mayor que el metanólico (15,045%). Estos porcentajes se obtuvieron considerando que el peso de los cuerpos fructíferos en seco, que fue de 73,95g, es el 100%.
Nutrientes
Los carbohidratos representaron el compuesto más abundante en M. vulgaris con 25,4%, ya que por lo general son el componente predominante de los cuerpos fructíferos de diversos hongos, como lo muestran Barros et al. (2007b) y Guzmán et al. (2009) al obtener, en los valores de estudios bromatológicos de diversos hongos comestibles, a los carbohidratos como el macro nutriente predominante seguidos por las proteínas, como lo muestra este trabajo donde se obtuvo 8,2% de proteínas y 2,6% de vitamina C.
Se determinó que el hongo está compuesto por los carbohidratos fructuosa (13,5mg·g-1) y sacarosa (4,56mg·g-1) y por los lípidos ácido oleico (24.54%), ácido 8,11-Octadecadienoico, metil éster (23,5%) para el extracto hexánico y por el ácido linoleico con 51,18%, seguido por el ácido palmítico con un 2,7% para el extracto metanólico (Tabla I).
* TR tiempo de retención
Rezanka et al. (1999) encontraron que el cuerpo fructífero de M. esculenta tiene como más abundante al ácido linoleico con 47,0% seguido por el ácido oleico con 24,1%. También Barros et al. (2007a) encontraron al ácido linoleico como el ácido graso más abundante en cinco hongos silvestres, seguido por el ácido oleico y ácido palmítico, este último ácido obtuvo un porcentaje de 17,08%.
Los carbohidratos desempeñan numerosas funciones esenciales para la vida. Los monosacáridos son la principal fuente de energía para el metabolismo, mientras que los polisacáridos sirven para el almacenamiento de la energía y pueden actuar como componentes estructurales. Por otra parte, otros efectos benéficos para la salud han sido relacionados con estos compuestos, incluyendo su efecto probiótico o de otro tipo menos común, como antioxidante y antiinf lamatorio (Colak et al., 2009).
Las proteínas pueden tener propiedades antibacterianas, antioxidantes, inmunoestimulantes, antitrombótico y actividades anti-inflamatorias, las que podrían ser utilizadas para la prevención y el tratamiento de la hipertensión, la diabetes y la hepatitis, entre otros efectos positivos en el organismo. Todos estos efectos promotores de la salud hacen que estos compuestos sean de gran relevancia como nutracéuticos (Bernal et al., 2011).
Las principales funciones biológicas de los lípidos incluyen almacenamiento de energía, componentes estructurales de las membranas celulares, e importantes moléculas de señalización. Aunque los seres humanos y otros mamíferos utilizan diversas vías de biosíntesis, algunos lípidos esenciales no se pueden obtener de esta manera y deben ser obtenidos a partir de la dieta (Bernal et al., 2011).
Los ácidos grasos insaturados fueron los más abundantes componentes mostrados en comparación con ácidos grasos monosaturados, lo que concuerda con lo encontrado por Heleno et al. (2013). Los ácidos grasos insaturados pueden ejercer un efecto protector contra el desarrollo de enfermedades inflamatorias y cardiovasculares (Barros et al., 2008).
Otros componentes importantes son las vitaminas, ya que constituyen un grupo diverso de compuestos orgánicos esenciales en cantidades traza para el crecimiento y mantenimiento de la vida. Estos compuestos son administrados generalmente como nutracéuticos o alimentos funcionales. La vitamina C (ácido L-ascórbico o L-ascorbato) es soluble en agua y es un nutriente esencial para los seres humanos y otras especies animales (Bernal et al., 2011).
Actividad antibacteriana
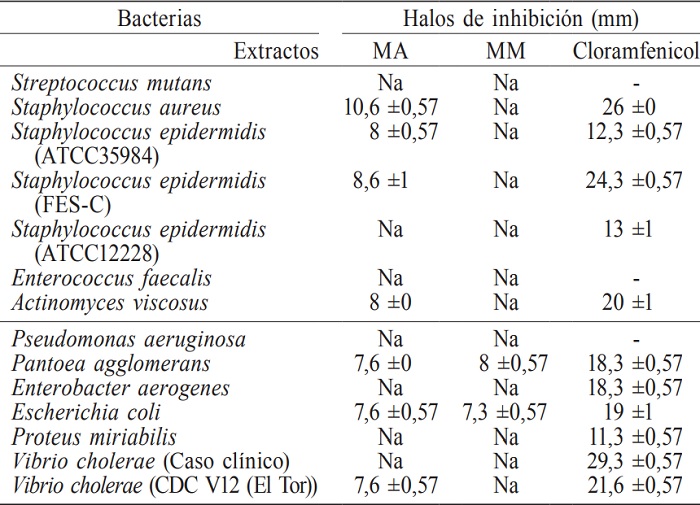
En la prueba cualitativa ambos extractos presentaron actividad antibacteriana, siendo más activo el extracto acuoso, ya que tuvo actividad sobre 7 de las 14 cepas bacterianas analizadas, en comparación con el extracto metanólico que sólo tuvo actividad sobre dos de ellas (Tabla II). S. epidermidis fue la bacteria que mostró los halos de inhibición de mayor diámetro. De acuerdo al análisis estadístico ANOVA factorial, existieron diferencias significativas entre la actividad del extracto acuoso y metanólico (F= 2918,44; P= 0,0001), así como también se mostraron diferencias significativas en la actividad de los extractos sobre el tipo de cepa bacteriana (F= 104,43; P= 0,0001), ya que los halos de inhibición fueron de mayor diámetro en las Gram positivas que en las negativas. E. coli y V. cholera fueron inhibidas por el extracto acuoso, lo que concuerda con Badshah et al., (2012), que al probar el extracto metanólico de M. esculenta, determinaron que tenía actividad contra estas dos bacterias.
MA: extracto acuoso de M. vulgaris, MM: extracto metanólico de M. vulgaris, Na: no tuvo actividad, ±: desviación estándar, - no se tiene. Cloramfenicol: control.
En la determinación de la concentración mínima inhibitoria (CMI) y la concentración mínima bactericida (CBM) de los extractos de M. vulgaris, la bacteria que obtuvo la CMI más baja con el extracto acuoso (MA) fue S. epidermidis FES-C con CMI= 8mg, siendo esta la bacteria más sensible a este extracto, y A. viscosus y E. coli en la concentración más alta probada (12mg·ml-1). Heleno et al., (2013) reporta el efecto de M. esculenta sobre esta última bacteria y obtuvo una medida de 6,31 y 6,44mm con una CMI>10mg·ml-1; en ese trabajo se obtuvo una CMI de 12mg·ml-1 y para S. aureus 7,22 y 6,34mm mientras que en el presente trabajo fue de 10,6mm. Estas diferencias en la actividad antimicrobiana observada en los extractos de Morchella pueden ser atribuidas a factores medio ambientales que pueden interferir en la síntesis de componentes microbiológicamente activos (Heleno et al., 2013). Para las demás bacterias la CMI está por arriba de 12mg·ml-1, lo mismo que para el extracto metanólico para todas las bacterias. Con ningún extracto se pudo determinar la CBM.
Los compuestos fenólicos tienen propiedad antimicrobiana y antiséptica (Celis et al., 2011), por lo que es muy probable que estos compuestos hayan participado en el efecto antibacteriano y antimicótico del extracto, ya que mediante HPLC se corroboró su presencia.
Actividad antifúngica
En la prueba cualitativa se encontró actividad de los dos extractos sobre las seis cepas de hongos filamentosos ensayadas. Posteriormente se obtuvo la CF para el extracto acuoso, ya que para el metanólico no se pudo obtener solo en el caso de F. sporotrichioides y de Rh. lilacina se observó actividad en la concentración más alta (6mg·ml-1), mientras que para los demás hongos no hubo inhibición del crecimiento con ninguna de las concentraciones probadas; sólo A. niger detuvo un poco la esporulación en la concentración más alta (6mg·ml-1). Heleno et al. (2013) observaron que las muestras tratadas con los extractos de M. esculenta mostraron cambios morfológicos, especialmente en A. fumigatis, ya que mostró completa despigmentación del micelio y cambios morfológicos en los conidióforos, determinando que los cultivos probados con este extracto poseen un número inusualmente pequeño de esporas en comparación con el de cultivo sin tratamiento. Quizás por esta razón en este estudio se pudo observar que A. niger detuvo un poco la esporulación.
En el caso del extracto acuoso se calculó la CF25 para T. mentagrophytes, la cual fue de 7,3µg· ml-1, y la CF10 para R. lilacina (2,0693µg·ml-1) y para F. sporotrichoides (2,473µg·ml-1), mientras que para los demás hongos no se logró obtener la CF.
Como se puede observar la actividad antimicrobiana de los extractos de M. vulgaris, no fue relevante, lo cual era de esperarse ya que esta especie de hongo es comestible.
Capacidad antioxidante
El extracto metanólico mostró una actividad antioxidante menor al del extracto acuoso, obteniendo una CA50 de 53,17µg·ml-1, mientras que en el acuoso fue de 43,23µg·ml-1. Kalyoncu et al. (2010), después de analizar la capacidad antioxidante de diez hongos, entre ellos seis especies de Morchella, muestran que los extractos de los hongos silvestres pueden reaccionar con radicales libres, que son el indicador principal de la auto-oxidación, y terminar con la reacción en cadena (Gordon, 1990), lo que es claramente indicativo de que algunas especies de hongos tienen capacidad antioxidante y antimicrobiana significativa. Los porcentajes que obtuvieron de seis extractos etanólicos de especies de Morchella corresponden a 18,95% para M. hortensis, 19,41% para M. esculenta, 27,32% para M.costata, 43,12% M. giganteus y 59,12% para M. elata. En otro estudio, realizado por Gursoy et al. (2009), se obtuvo un porcentaje de 59,22% para M. elata y 43,12% para M. giganteus. Los porcentajes obtenidos en este trabajo, de 53,17% y 43,23% para el extracto metanólico y acuoso, respectivamente, se encuentran entre de los porcentajes mayores en comparación con los trabajos mencionados.
Las propiedades antioxidantes de los hongos suelen estar relacionadas con compuestos de bajo peso molecular, en particular a la de compuestos fenólicos, ácidos fenólicos, flavonoides, etc. (Gursoy et al., 2009), a los que se considera como los principales contribuyentes a la capacidad antioxidante (Chung et al., 1998).
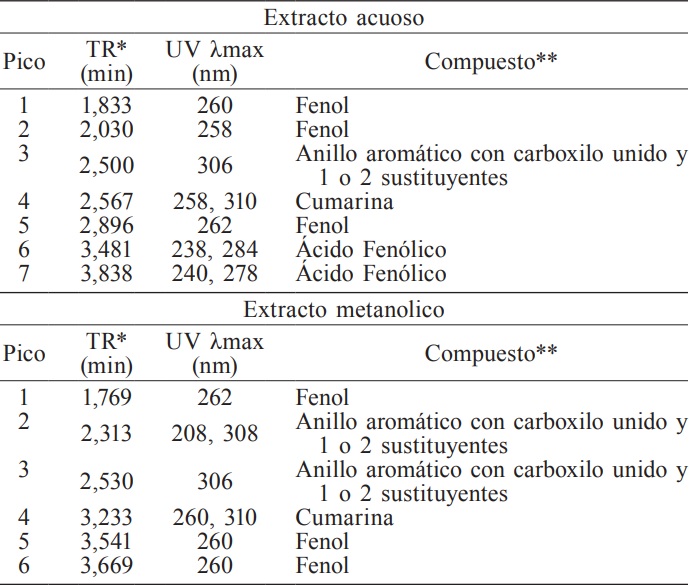
Metabolitos secundarios presentes en los extractos
En los cromatogramas obtenidos en el HPLC se identificó para el extracto acuoso fenoles, ácidos fenólicos, cumarinas y compuestos con anillos aromáticos con carbonilo unido y una o dos sustituciones, mientras que para el metanólico se encuentran los mismos metabolitos con excepción de ácidos fenólicos (Tabla III). Chung et al. (1998) mencionan que estos compuestos son los que contribuyen en la actividad antioxidante. También se encontró la presencia de cumarinas. Todos estos metobolitos secundarios tienen propiedades medicinales; por ejemplo, los fenoles y ácidos fenólicos tienen acción antimicrobiana, antiviral y antifúngica. Se considera que la acción de los fenoles contra los microorganismos se debe a la inhibición enzimática, posiblemente por acción sobre los grupos sulfhidrilos de sus aminoácidos de cisteína o por de reacciones más inespecíficas con proteínas bacterianas. Así mismo, se ha reportado actividad antimicrobiana de las cumarinas (Araujo y Salas, 2008).
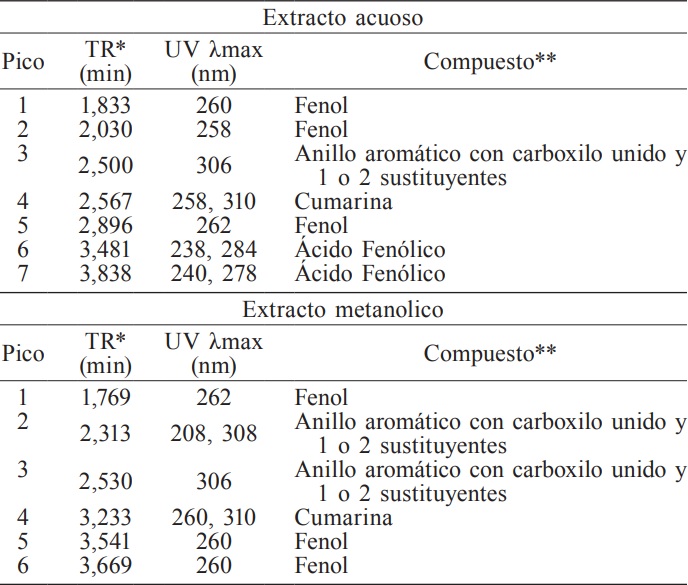
* TR: tiempo de retención.** Identificación de los compuestos con base en Dey y Harborne (1989).
Flavonoides totales
Para el extracto metanólico, se determinó que contiene 4,5µg de flavonoides por 1g de extracto, mientras que el extracto acuoso contiene 13,25µg de flavoniodes por 1g de extracto. Estos valores son altos al compararlos con lo obtenido por Gursoy et al. (2009), ya que para el extracto metanólico de M. rotunda se reportó que contiene 0,59µg de flavonoides.
Los flavonoides poseen propiedades anti-inf lamatorias, antioxidantes, antialérgicas, hepatoprotectoras, antitrombóticas, antivirales y anticarcinogénicas, y representan un amplio grupo de metabolitos secundarios (Tenorio et al., 2006). Son estructuras fenólicas que contienen un solo grupo carbonilo (Fuertes et al., 1998). Estos compuestos orgánicos se sintetizan a partir de aminoácidos, carbohidratos, lípidos, proteínas y ácidos nucleídos (Tenorio et al., 2006)
Los flavonoides lipofílicos pueden perturbar la integridad estructural de la membrana celular (Fuertes et al., 1998). A su vez, parte de los flavonoides inhiben in vitro el crecimiento de V. cholerae, Streptococcus y otras bacterias (Araujo y Salas, 2008). Cabe mencionar que el extracto acuoso de M. vulgaris mostró actividad contra V. cholerae, a diferencia del metanólico que no tuvo actividad, lo cual probablemente se deba a que el extracto acuoso contiene mayor cantidad de flavonoides que el metanólico.
Citotoxicidad de los extractos
Utilizando el porcentaje de mortalidad de las células Ca Ski al someterlas a distintas concentraciones de los extractos de M. vulgaris se obtuvo que la CI50, para el extracto acuoso fue de 622mg·ml-1, mientras que el metanólico obtuvo un valor de 2477mg·ml-1, por lo que se consideró que ninguno de los dos extractos son citotóxicos, ya que de acuerdo con los estándares del Instituto Nacional de Cáncer (NCI) de EEUU, las concentraciones que son consideradas como citotóxicas para extractos son de ≤2 µg·ml-1.
Conclusiones
Se concluye que el cuerpo fructífero de M. vulgaris es un alimento funcional que puede ser utilizado como complemento dietético por contener biomoléculas necesarias para el organismo. Por otro lado, por haber demostrado sus proiedades medicinales (antimicrobiana, antioxidante y no citotóxico) puede se considerado como un producto nutracéutico.
REFERENCIAS
Alves MJ, Ferreira IC, Dias J, Teixeira V, Martins A, Pintado MA (2012) A Review on antimicrobial activity of mushroom (Basidiomycetes) extracts and isolated compounds. Planta Med. 78: 1707-1718.
Andlauer W, Furst P (2002) Nutraceuticals: a piece of history, present status and outlook. Food Res. Int. 35: 171-176.
Araujo JD, Salas AR (2008) Actividad antimicrobiana de plantas. Rev. Científica 6: 6-18.
Badisa RB, Tzakou O, Couladis M, Pilarinou E (2003) Cytotoxic activities of some Greek Labiatae herbs. Phytother. Res. 17: 472-476.
Badshah H, Aleem QR, Khan J, Ullah F, Fahad S, Ullah F, Muhammad KA, Hussain I, Khan N (2012) Pharmacological screening of Morchella esculenta (L) Pers., Calvatia gigantean (Batsch ex Pers.) Lloyd and Astraeus hygrometricus Pers., mushroom collected from South Waziristan (FATA.). J. Medic. Plants Res. 6: 1853-1859.
Barros L, Baptista P, Correia DM, Casal S, Oliveira B, Ferreira IC (2007a) Fatty acid, sugar compositions and nutritional value of five wild edible mushrooms from Northeast Portugal. Food Chem. 105: 140-145.
Barros L, Baptista P, Correia DM, Morais JS, Ferreira IC (2007b) Effects of conservation treatment and cooking on the chemical composition and antioxidant activity of Portuguese wild edible mushrooms. J. Agric. Food Chem. 55: 4781-4788.
Barros L, Cruz T, Baptista P, Estevinho LM, Ferreira IC (2008) Wild and commercial mushrooms as source of nutrients and nutraceutical. Food Chem. Toxicol. 46: 2742- 2747.
Bernal J, Mendiola JA, Ibañez E, Cifuentes A (2011) Advanced analysis of nutraceuticals. J. Pharm. Biomed. Anal. 55: 758-774.
Celis C, García A, Sequeda G, Mendez G, Torrenegra R (2011) Antimicrobial activity of extracts obtained from Anacardium excelsum againts some pathogenic microorganisms. Emir. J. Food Agric. 23: 249-257.
Chung KT, Wong TY, Huang YW, Lin Y (1998) Tannins and human health: a review. Crit. Rev. Food Sci. Nutr. 38: 421-464.
Dey PM, Harborne JB (1989) Methods in Plant Biochemitry. Vol. 1. Plant Phenolics. Academic Press. San Diego, CA, EEUU. pp. 97-98
Colak A, Faiz O, Sesli E (2009) Nutritional composition of some wild edible mushrooms. Turk. J. Biochem. 34: 25-31.
Díaz-Barriga VH (2002) Hongos Macromicetos Comestibles, Venenosos, Medicinales y Destructores de la Madera, de la Reserva de la Biosfera de la Mariposa Monarca, Sierra Chincua, Michoacán, México. Fundación Produce. México. pp. 273-275.
Domínguez AX (1973) Métodos de Investigación Fitoquímica. Limusa. México. pp. 3-17.
Espin JC, Garcia C, Tomás-Barberán FA (2007) Nutraceuticals: facts and fiction. Phytochemistry 68: 2986-3008.
Fuertes C, Roque M, Tristan M (1998) Flavonoides y alcaloides de Lupinus ballianus con actividad antibacteriana y antifúngica. Cienc. Inv. 1: 71-80.
González MS, Peñalosa CI (2000) Biomoléculas (Métodos de Análisis). Universidad Nacional Autónoma de México. 256 pp.
Gordon MH (1990) The Mechanism of Antioxidant Action in vitro. Food Antioxidants. Hudson BJF. Londres, RU. pp. 1-18.
Gursoy N, Sarikukcu C, Cengiz M, Halil SM (2009) Antioxidant activities, metal contents, total phenolics and flavonoids of seven Morchella species. Food Chem. Toxicol. 47: 2381-2388.
Guzmán G (1978) Hongos. Limusa. México. pp. 4, 18-20.
Guzmán BA, Juaréz HE, Sieiro OE, Romero VR, Silencio BJ (2009) Los nutracéuticos, lo que es conveniente saber. Rev. Mex. Pediatr. 76: 136-145.
He P, Geng L, Mao D, Xu C (2012) Production, characterization and antioxidant activity of exopolysaccharides from submerged culture of Morchella crassipes. Bioproc. Biosyst. Eng. 35: 1325-1332.
Heleno SA, Stojkovic D, Barros L, Glamoclija J, Sokoviv M, Martins A, Joao MR, Ferreira IC (2013) A comparative study of chemical composition, antioxidant and antimicrobial properties of Morchella esculenta (L.) Pers. From Portugal and Serbia. Food Res. Int. 51: 236-243.
Herrera T, Ulloa M (1990) El Reino de los Hongos, Micología Básica y Aplicada. Fondo de Cultura Económica. México. 443 pp.
Kalyoncu F, Oskay M, Saglam H, Erdogan TF, Tamer AU (2010) Antimicrobial and antioxidant activities of mycelia of 10 wild mushroom species. J. Med. Food 13: 415-419.
Koneman EW, Allen SD, Dowell VR, Sommers HM (1985) Diagnóstico Microbiológico. Médica Panamericana. México. 909 pp.
Moradali MF, Mostafavi H, Ghods S, Hedjaroude GA (2007) Immunomodulating and anticancer agents in the realm of macromycetes fungi (macrofungi). Int. Immunopharmacol. 7: 701-724.
Murillo F (2006) Actividad antioxidante “in vitro” de las bebidas de frutas. Tecnología (Junio/ Julio): 20-27.
Okusa PN, Penge O, Devleeschouwer M, Duez P (2007) Direct and inderect antimicrobial effects and antioxidant activity of Cordia gilletii De Wild (Boraginaceae). J. Ethnopharmacol. 112: 476-481.
Prasad P, Chauhan K, Kandari LS, Maikhuri RK, Purohit A, Bhatt RP (2002) Morchella esculenta (Guchni): need for scientific intervention for its cultivation in Central Himalaya. Curr. Sci. 82: 1098-1100.
Ramamoorthy PK, Bono A (2007) Antioxidant activity, total phenolic and flavonoid content of Morinda citrifolia fruit extracts from various extraction processes. J. Eng. Sci. Technol. 2: 70-80.
Rezanka T, Rozentsvet OA, Dembitsky VM (1999) Characterization of the hydroxy fatty acid content in Basidiomycotina. Folia Microbiol. 44: 635-641.
Tenorio LF, Del Valle ML, Pastelín HG (2006) Los flavonoides y el sistema cardiovascular: ¿Pueden ser una alternativa terapéutica? Arch. Cardiol. Méx. 76(4): 33-45.
Tsutani K, Takuma H (2008) Regulatory sciences in herbal medicines and dietary supplements. Yakugaku Zasshi 128: 867-880.
Vanden-Berghe DA, Vlietinck AJ (1991) Screening methods for antibacterial agents from higher plants. Dey PM, Harborne, JB, Hostettmann K (Eds.) Methods in Plant Biochemistry. Vol. 6. Assays for Bioactivity. Academic Press. Londres, RU. pp. 47-69.
Wang H, Bun NT (2002) Isolation of an antifungal thaumatin-like protein from kiwi fruits. Phytochemistry 61: 1-6.
Wasser SP (2002) Medicinal mushrooms as a source of antitumor and immunomodulating polysaccharides. Appl. Microbiol. Biotechnol. 60: 258-274.
White TJ, Bruns T, Lee S, Taylor JW (1990) Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. En Innis MA (Ed.) PCR Protocols: A Guide to Methods and Applications. 18: 315-322.
Yamac M, Bilgili F (2006) Antimicrobial activities of fruit bodies and or mycelial cultures of some mushroom isolates. Pharm. Biol. 44: 660-667.