COMUNICACIONES REPORTS COMUNICACOES
Recepción: 10 Marzo 2016
Aprobación: 17 Mayo 2017
Resumen: El monitoreo de la resistencia a los antibióticos en la fauna silvestre de zonas remotas puede ser una valiosa herramienta para evaluar el impacto de la presión antrópica. Se investigó el efecto de la contaminación con arsénico (As), plomo (Pb), cadmio (Cd), cobre (Cu) y zinc (Zn) sobre poblaciones bacterianas aisladas en excretas del pingüino de Humboldt (Spheniscus humboldti). Se estudiaron comunidades bacterianas provenientes de tres lugares importantes de anidación del pingüino de Humboldt en la costa de Chile: Isla Pan de Azúcar, Isla Chañaral e Isla Cachagua. Se evaluaron los patrones de resistencia de bacterias a metales pesados y antibióticos. Hubo diferencias en las bacterias resistentes a metales pesados entre colonias de pingüinos. Todas las cepas bacterianas aisladas de los excrementos de pingüino en las tres localidades mostraron resistencia al Zn. Las cepas bacterianas aisladas de heces en isla Cachagua exhi-bieron la más alta resistencia al As, Cu y Pb, siendo este lugar el que exhibió las más altas concentraciones para estos metales. Las muestras de Isla Cachagua indican que Enterococcus du-rans, E. faecium, Pseudomonas spp. y Brevundimonas vesicula-ris fueron resistentes al Cd. El metal más tóxico fue Cd, seguido por Cu. Todas las bacterias Gram (+) mostraron resistencia a cefapirin, oxitetraciclina, florfenicol, amoxicilina, gentamicina, penicilina y sulfatrimet, mientras que las bacterias Gram (-) fue-ron resistentes a penicilina y sulfatrimet. Las cepas resistentes a metales pesados podrían afectar los ciclos orgánicos e inorgá-nicos en aquellos sitios donde habita el pingüino de Humboldt.
Palabras clave: Antibióticos, Aves Marinas, Contaminación, Metales Pesados, Pingüinos, Resistencia Microbiana, Spheniscus humboldti .
Abstract: Monitoring antibiotic resistance in wildlife from remote areas can be a valuable tool for evaluating the impact of human pressure. We investigated the effect of contamination with arsenic (As), lead (Pb), cadmium (Cd), copper (Cu) and zinc (Zn) on bacterial populations isolated from excreta of the Humboldt penguin (Spheniscus humboldti). Bacterial communities were studied at three important nesting places of the Humboldt penguin on the Chilean coast of Chile: Pan de Azúcar Island, Chañaral Island, and Cachagua Island. Bacteria resistance patterns to heavy metals and antibiotics were evaluated. There were differences in heavy metal-resistant bacteria between colonies of penguins. All bacterial strains isolated from penguin droppings in all three locations showed resistance to Zn. Bacterial strains isolated from feces in Cachagua Island exhibited the highest resistance to As, Cu and Pb, being this location that which exhibited the highest concentrations for these metals. Samples from Cachagua Island indicated that Enterococcus durans, E. faecium, Pseudomonas spp. and Brevundimonas vesicularis were resistant to Cd. The most toxic metal was Cd, followed by Cu. All gram (+) bacteria showed resistance to cefapirin, oxytetracycline, florfenicol, amoxicillin, gentamicin, penicillin, and sulfatrimet, whereas gram (-) bacteria were resistant to penicillin and sulfatrimet. Metal-resistant strains could affect the organic and inorganic cycles at places where Humboldt penguin lives.
Resumo: O monitoramento da resistência aos antibióticos na fauna silvestre de áreas remotas pode ser uma valiosa ferramenta para avaliar o impacto da pressão antrópica. Investigou-se o efeito da contaminação com arsênico (As), chumbo (Pb), câdmio (Cd), cobre (Cu) e zinco (Zn) sobre populações bacterianas isoladas em excretas do pingüim de Humboldt (Spheniscus humboldti). Estudaram-se comunidades bacterianas provenientes de três lugares importantes de anidação do pingüim de Humboldt na costa do Chile: Ilha Pan de Azúcar, Ilha Chañaral e Ilha Cachagua. Avaliaram-se os padrões de resistência de bactérias a metais pesados e antibióticos. Houve diferenças nas bactérias resistentes a metais pesados entre colônias de pingüins. Todas as cepas bacterianas isoladas dos excremento de pingüim nas três localidades mostraram resistência ao Zn. As cepas bacterianas isoladas de fezes em ilha Cachagua exibiram a mais alta resistência ao As, Cu e Pb, sendo este local o que exibiu as mais altas concentrações para estes metais. As amostras de Ilha Cachagua indicam que Enterococcus durans, E. faecium, Pseudomonas spp. e Brevundimonas vesicularis foram resistentes ao Cd. O metal mais tóxico foi Cd, seguido por Cu. Todas as bactérias Gram (+) mostraram resistência a cefapirin, oxitetraciclina, florfenicol, amoxicilina, gentamicina, penicilina e sulfatrimet, enquanto que as bactérias Gram (-) foram resistentes a penicilina e sulfatrimet. As cepas resistentes a metais pesados poderiam afetar os ciclos orgânicos e inorgânicos naquelas regiões onde habita o pingüim de Humboldt.
Introducción
La contaminación del agua, aire y suelo por metales pesa-dos es uno de los problemas ambientales más graves pro-vocados por el hombre (Blais et al., 2007). Las fuentes más comunes de contaminación por dichos metales son los procesos industriales, los ver-tidos municipales y la minería (Muñoz y Becker, 1999). En Chile, como consecuencia del desarrollo minero en el norte y el desarrollo industrial en la zona central, se registra una creciente y preocupante conta-minación ambiental en los ecosistemas costeros por las altas concentraciones de meta-les que afecta desde el sub-suelo hasta la atmósfera, incluyendo suelos y cuerpos de agua (Salamanca et al., 2004). En estas zonas del país se concentran muchas colo-nias de pingüinos de Humboldt, las cuales se ven afectadas por estas activida-des antropogénicas (Celis et al., 2014). El pingüino de Humboldt (Spheniscus hum-boldti) es una especie de ave marina que habita el litoral de las costas del Perú y de Chile; se alimenta en el mar en base a una dieta constitui-da principalmente de peces, complementado con calamares y crustáceos (Martínez y González, 2004). Muchos me-tales pesados son incorpora-dos al organismo a través de la dieta, y una gran parte de ellos son excretados por el pingüino una vez que está en tierra (Celis et al., 2014).La presencia de metales pe-sados en el ambiente puede modificar la f lora microbiana que allí habita, dependiendo de la concentración de estos elementos químicos (Montuelle et al., 1994). Existe evidencia que indica que la contamina-ción con metales pesados pue-de favorecer la resistencia bac-teriana tanto en ambientes marinos como terrestres (Baker-Austin et al., 2006) y que algunos organismos pue-den ser portadores de genes resistentes a los antibióticos (Singer et al., 2006). La resis-tencia a metales pesados en poblaciones bacterianas puede considerase como un fenóme-no ambiental de selección na-tural para la supervivencia de las especies, lo que podría alterar la biota bacteriana au-tóctona de los ecosistemas (Pathak y Gopa, 2005; Baker-Austin et al., 2006). Se ha visto que bacterias nativas del género Pseudomonas que ha-bitan en suelos de ambientes mineros presentan resistencia a metales pesados tales como Cd, Cu y Pb (Monge-Amaya et al., 2008). De este modo, la contaminación de los ecosiste-mas costeros puede tener re-percusiones que van más allá de afectar a la población del pingüino de Humboldt, pues la exposición de bacterias au-tóctonas a altas concentracio-nes de metales pesados podría significar la aparición de ce-pas resistentes, cuyas conscuencias pueden ser graves para el ambiente (Nies, 2003). A nivel mundial se estima que sobre el 70% de las enfermedades infecciosas emergentes tienen su origen en la fauna silvestre, y además de aumentar significativamente con el tiempo, la mayoría de los patógenos que las provocan presentan resistencia a antibióticos (Jones et al., 2008). Esto implica que muchos lugares donde viven especies silvestres podrían estar experimentando los mismos problemas.
La influencia antrópica juega un papel importante en la contaminación de los ecosistemas marinos y terrestres, lo que se ha visto reflejado por la cercanía de las infraestructuras o de núcleos urbanos a los nichos silvestres (Salamanca et al., 2004; Celis et al., 2014). La contaminación por metales pesados sobre la flora microbiana no ha sido cabalmente estudiada en fauna de zonas costeras de Chile (Moraga et al., 2003). La exposición a altas concentraciones de metales pesados podría estar influyendo en la susceptibilidad de las bacterias gastrointestinales de espe-cies como el pingüino de Humboldt. Más aún, ciertos estudios han mostrado que la contaminación con metales en ambientes naturales podría tener un importante rol en la proliferación de la resistencia a antibióticos usados en humanos y en animales (Alonso et al., 2001; Summers, 2002; Rose et al., 2009). Esto ha motivado la realización de algunos estudios sobre susceptibilidad a metales pesados en bacterias que habitan en los ecosistemas costeros de Chile (Mondaca et al., 1993; Moraga et al., 2003). Sin embargo, estos estudios se han realizado sobre la base de matrices abióticas y no sobre matrices bióticas como las excretas, donde las bacterias gastrointestinales de especie silvestres que habitan los ecosistemas costeros podrían tener importancia. No se sabe si la contaminación por metales pesados tiene incidencia sobre la f lora microbiana de estas aves marinas en relación a los hábitats a los que estas especies están vinculadas. En este estudio, se pretende 1) determinar si existe resistencia a metales como Cd, As, Pb, Cu y Zn en bacterias presentes en excretas de colonias de pingüinos de Humboldt que anidan en tres lugares de la costa chilena, y 2) investigar si dichos metales tienen efecto sobre la resistencia bacteriana a algunos de los antibióticos usados en humanos y en veterinaria.
Metodología
Recolección de muestras
Los muestreos se llevaron a cabo entre diciembre 2011 y enero 2012 desde tres lugares del litoral chileno donde habitualmente anidan estas aves (Figura 1): Isla Pan de Azúcar (26º09’S, 70º40’O), Isla Chañaral (29º01’S, 71º34’O) e Isla Cachagua (32º35’S, 71º27’O). Se recolectaron 20 muestras frescas de excretas (~5g cada una) de pingüinos de Humboldt, correspondientes a un grupo de animales de la colonia y no de un individuo en particular, desde los sitios de anidamiento en cada colonia. Para ello, se utilizaron guantes de látex, espátulas de plástico y bolsas de polietileno Ziploc. Cada muestra se almacenó en un contenedor con hielo (~4ºC) hasta su llegada a laboratorio.
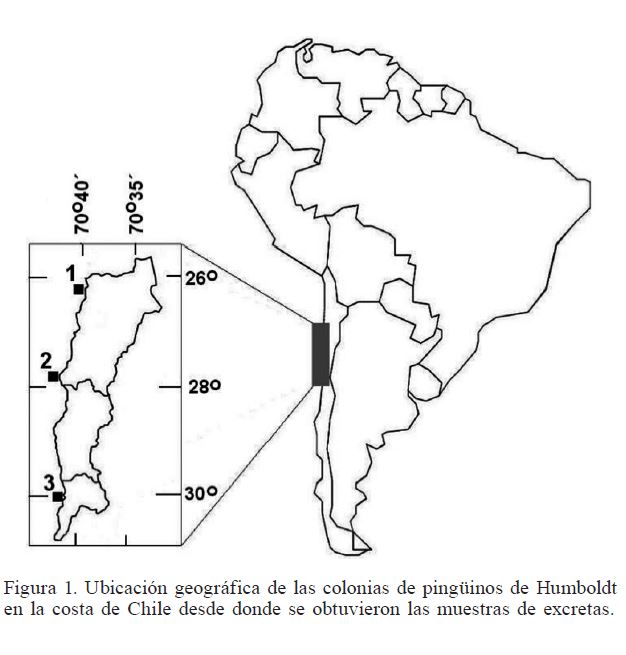
La isla Pan de Azúcar es una isla de forma ovalada (1,5×1km) ubicada en el norte de Chile, a 1km de la costa y a 18km de la bahía de Chañaral, lugar donde desechos de la minería fueron vertidos en gran cantidad entre 1938 y 1974 (Vermeer y Castilla, 1991); allí existe una importante población de pingüinos de Humboldt, con ~5000 individuos. Por su parte, la Isla Chañaral es una isla circular (2km de diámetro) situada a 7km de la costa y a 100km al norte de la bahía de Coquimbo; constituye una de las más grandes colonias de pingüinos de Humboldt en el norte de Chile, con una población estimada de 22000 individuos. Por su parte, Isla Cachagua está ubicada en la zona central de Chile, y es una pequeña área (250×200m) situada a 100m de la costa y a 20km de la Bahía de Quintero, un área altamente industrializada; a pesar del pequeño tamaño de la isla, Cachagua constituye un lugar de anidación importante para los pingüinos de Humboldt, soportando una población de ~2000 individuos (Meza et al., 1998).
Determinación de la resistencia a metales pesados y antibióticos
Las muestras de excretas fueron pesadas para estandarizar una cantidad fija (5g de peso seco) sobre la cual se trabajó en los análisis. A partir de cada muestra, 1g fueron sembrados por esparcimiento superficial en placas de Petri con agar R2A y agar ENDO-C (Merck®), las cuales se incubaron por cinco días a temperatura ambiente (20ºC). Las colonias desarrolladas se caracterizaron de acuerdo a su morfología y las colonias seleccionadas se traspasaron a placas de agar PCA (Merck®) enriquecido con 800μg·ml-1 de CuSO4 (Moraga et al., 2003). La identificación bacteriana a partir de las colo-nias aisladas se basó en estudios de morfología microscópica con tinción Gram y en propiedades bioquímicas. Para la tipificación de las especies identificadas se utilizó un sistema estandarizado de identificación bacteriana (API).
La resistencia a As, Cd, Cu, Pb y Zn se determinó utilizan-do las siguientes soluciones (Merck®): N2AsO4H·7H2O, CdCl2, CuSO4, Pb(NO3)2 y ZnCl2 (Moraga et al., 2003). Para Zn las concentraciones ensayadas fueron 3200, 1600, 800, 400 y 200μg·ml-1, para As, Cu y Pb fueron 1600, 800, 400, 200 y 100μg·ml-1, mientras que para Cd los niveles testeados fueron 400, 200, 100, 50 y 25μg·ml-1 (Mondaca et al., 1993). La resistencia bacteriana se determinó a través de la concentración mínima inhibitoria (CMI) para estos metales (Anisimova et al., 1993). Los ensayos se realizaron en agar PCA suplementado con el metal. Las placas se sembraron con un replicador Steel y fueron incubadas por 48h.
La resistencia a antibióticos se estudió mediante la técnica de difusión en placa, en base a las definiciones dadas por el EuropeanCommittee on Anti-microbial Susceptibility Testing (Matuschek et al., 2013). Se utilizaron los siguientes antibióticos (Merck®): oxitetraciclina (30μg·ml-1), penicilina (10μg·ml-1), gentamicina (10μg· ml-1), f lorfenicol (30μg·ml-1), amoxicilina (20μg· ml-1), sulfatrimet (25μg·ml-1) y cefapirina (30μg·ml-1). Las cepas fueron reactivadas desde partidas congeladas, cultivadas en placa por triplicado y chequeadas para ver crecimiento bacteriano después de 24, 48 y 72h. Se utilizaron tres repeticiones en cada caso. Los resultados se registraron como sensible o resistente; no se consideró el crecimiento intermedio.
Resultados
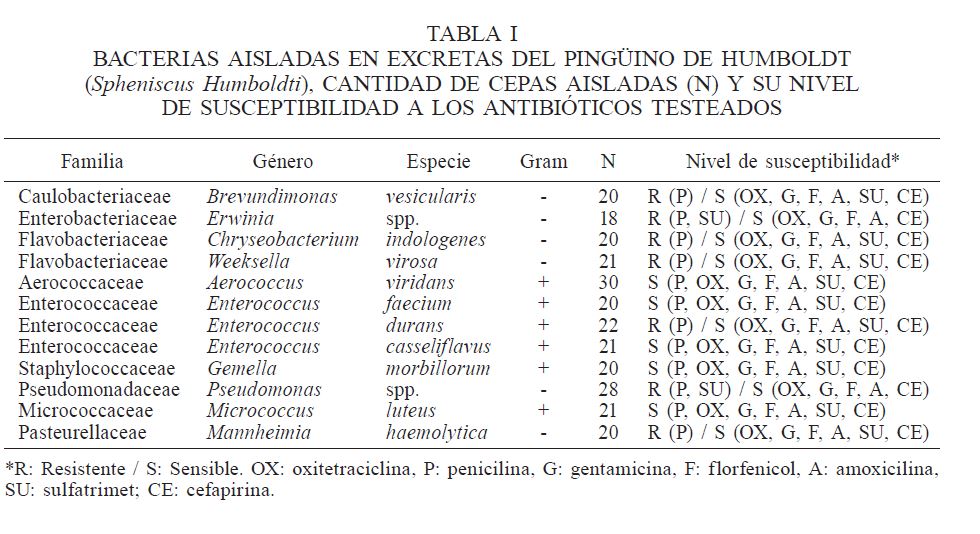
Del análisis de las muestras de excretas obtenidas de las diferentes colonias de pingüinos de Humboldt, se logró identificar diferentes cepas bacterianas (Tabla I). Las bacterias Gram negativas tales como Brevundimonas, Erwinia, Chryseobacterium, Weeksella, Pseudomonas . Mannheimia presentaron resistencia a penicilina, así cono también Ente-rococcus durans, una bacteria Gram positiva. Por su parte, Erwinia y Pseudonoma presentaron resistencia a sulfatrimet y penicilina.
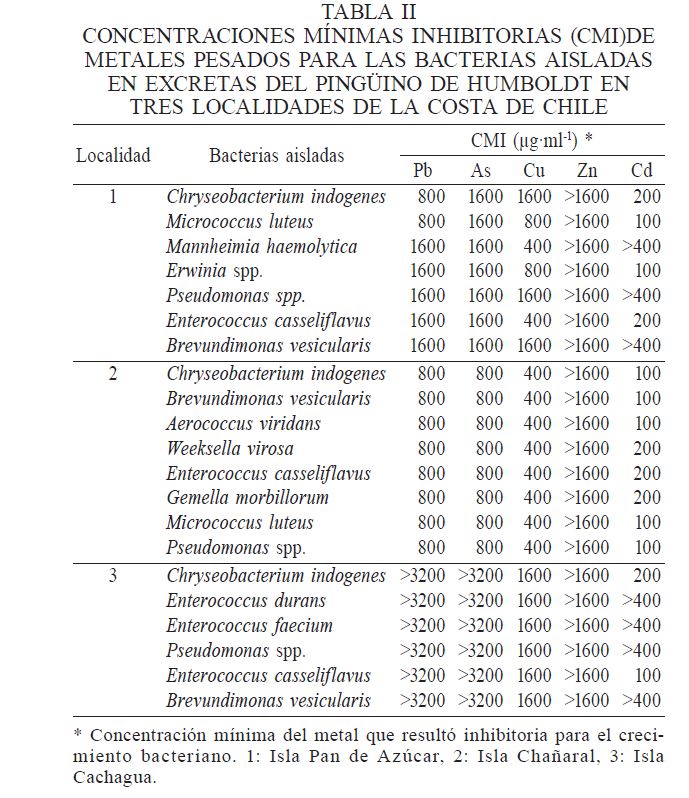
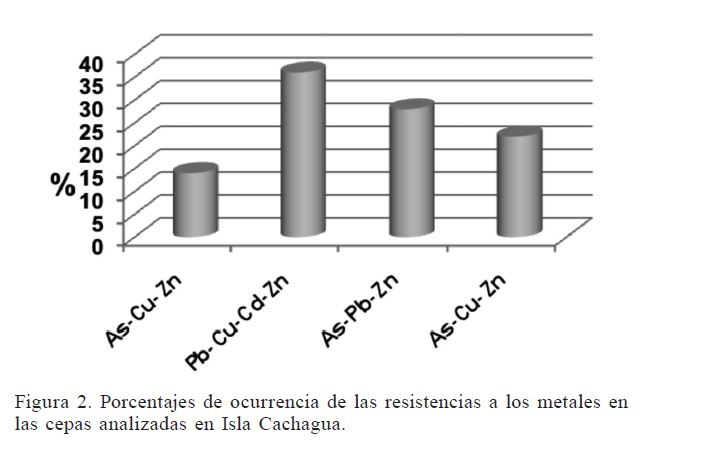
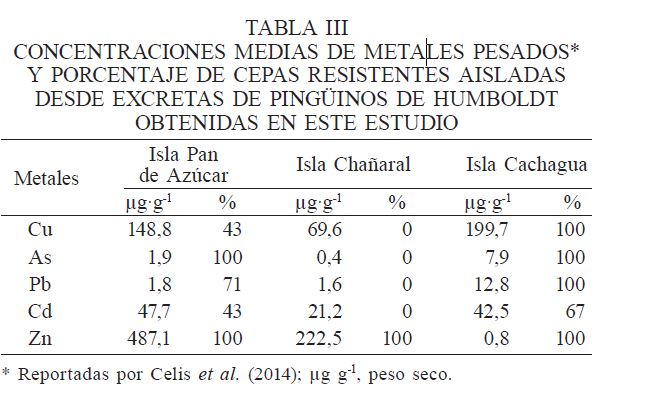
En las pruebas de susceptibilidad a metales, los valores de la concentración mínima inhibitoria (CMI) mostraron que el metal más tóxico (con menor CMI) para todas las cepas aisladas resultó ser el Cd, seguido por el Cu (Tabla II). Se encontró que todas las cepas bacterianas aisladas en las excretas del pingüino de Humboldt de las tres localidades estudiadas fueron resistentes al Zn; en cambio, todas las bacterias aisladas de Isla Chañaral no mostraron ninguna resistencia al Cu, siendo este lugar el más alejado de la costa. Todas las bacterias aisladas de Isla Cachagua y la mayoría de las bacterias de Isla Pan de Azúcar (exceptuando C. indogenes . M. luteus) mostraron resistencia al Pb, mientras que por el contrario las cepas bacterianas de Isla Chañaral no mostraron ninguna resistencia a este metal. Por su parte, E. durans, E. faecium, Pseudo-monas spp. y B. vesicularis aisladas de las excretas obtenidas de Isla Cachagua mostraron resistencia al Cd. Por otra parte, solo M. haemolytica. Pseudomonas spp. de Isla Pan de Azúcar mostraron resistencia al Cd. La mayoría de las cepas de Isla Cachagua e Isla Pan de Azúcar fueron resistentes al As, pero no así las aisladas de Isla Chañaral. Se notó que las cepas resistentes presentaron simultáneamente resistencia a dos o más metales, particularmente en aquellas cepas aisladas de Isla Cacha-gua (Figura 2). Se observó una mayor resistencia al As, Cu y Pb en las cepas bacte-rianas aisladas de las excretas de pingüinos de Humboldt en Isla Cachagua, lo que coincide con las mayores concentraciones de estos metales en las excretas recolectadas desde este lugar (Tabla III).
Discusión
No se encontraron estudios similares de susceptibilidad bacteriana a metales pesados en excretas de pingüinos. Más aún, poco se conoce acerca del impacto de la contaminación con metales sobre las pobla-ciones bacterianas en áreas donde habita el pingüino de Humboldt. Los diferentes valores de CMI encontrados sugieren que las bacterias son capaces de codificar complejos mecanismos de resistencia antimicrobiana, tales como enzimas hidrolíticas, bombas de flujo, mutaciones en porinas de membrana, biofilms y elementos genéticos móviles (Girlich et al., 2007). Entre estos últimos están los plásmidos, los integrones, los transposones y elementos integrativos, los cuales pueden transmitirse entre especies bacterianas mediante procesos de conjugación (Vargas et al., 2010). Cuando un elemento móvil porta simultáneamente genes de resistencia a metales pesados y a algunos antibióticos, la presencia de metales pesados en el entorno claramente favorece la selección de dichos elementos genéticos en las poblaciones bacterianas (Mondaca et al., 1993; Ahmed et al., 2007). El presente estudio revela que existen bacterias gastrointestinales del pingüino de Humboldt resistentes a algunos de los metales pesados estudiados. Moraga et al. (2003) mostraron que bacterias del género Pseu-domonas aisladas en muestras de agua de la bahía de Iquique (760km al norte de Isla Pan de Azúcar), con una gran actividad industrial en su borde costero y cuyas industrias descargan sus residuos líquidos en ella, son resistentes a Pb, As y Cu, y a cefataxima, amikacina, nitrofurantoina y ampicilina. En el presente estudio, la ma-yoría de las bacterias aisladas mostraron resistencia a As, Cu, Pb y Zn. Todas las bacterias Gram negativas aisladas presentaron resistencia a penicilina y algunas a sulfatrimet. En general, las bacterias Gram negativas tales como Chryseo-bacterium y Pseudomonas, presentan resistencia innata a muchos antibióticos (Poole, 2005; Sakurada, 2008), pero no observamos ninguna resistencia a oxitetraciclina, gentamicina, florfenicol, amoxicilina, sulfatrimet o cefapirina.
Las mayores resistencias a Pb, Cu y As fueron observadas en isla Cachagua, la que a diferencia de las otras dos islas estudiadas es la que se encuentra más cercana al litoral y que está más afectada por actividades antropogénicas. Existen estudios que han establecido que la resistencia bacteriana a metales en ecosistemas muy contaminados está asociada a la resistencia a antibióticos (Baker-Austin et al., 2006), como es el caso de la resistencia bacteriana al Hg (Summers et al., 1993) y la resistencia de enterobacterias a la tetraciclina, aún a concentraciones sub-letales de As, Cu y Zn (Chen et al., 2015). Por otro lado, la presencia de metales pesados en las excretas de aves árticas puede inducir cierta resistencia en bacterias que viven en ambientes terrestres (Sjölund et al., 2008). Los trabajos llevados a cabo en suelos muy contaminados por la minería indican que ciertas bacterias nativas en suelos contaminados pueden desarrollar resistencia a Hg y otros metales pesados, así como también a cloranfenicol, ampicilina, tetraciclina, estreptomicina y kanamicina (Rojas et al., 2014). Se ha encontrado que existe una amplia resistencia a Hg, Cu, Pb, Ni, Zn y antibióticos en bacterias que viven inmediatamente bajo la superficie de suelos contaminados (Diptendu y Goutam, 2013). No obstante, y dado que los pingüinos se alimentan en el mar, pueden transportar los metales pesados que ingieren a través de la dieta a los sitios de anidación en tierra, actuando como biovectores de contaminación (Blais et al., 2007). Es allí donde estos contaminantes se concentran, pudiendo aumentar la resistencia de ciertas comunidades bacterianas nativas de estos lugares terrestres. Las excretas son un sustrato ideal para el crecimiento microbiológico y constituyen un medio favorable para que las bacterias estén metabólicamente activas.
B. vesicularis es resistente a sulfametoxazol, trimetropina y ceftazidima (Zhang et al., 2012) y también se ha reportado resistencia a vancomicina por parte de bacterias del género Enterococcus (Cetinkaya et al., 2000). En aves, se ha encontrado que cepas de Pseudomas aisladas de la cloaca del perico bronceado (Brotogerisjugularis) y de cotorra (Aratingapertinax) son resistentes a trimetoprim-sulfametoxazol, cefotaxima y ampicilina (Vargas et al., 2010). Un gran número de bacilos no entéricos Gram negativos, como Pseudomonas, aislados de la cloaca de gaviota argéntea (Larus argentatus) han mostrado resistencia a amikacina, ampicilina, aumentina, carbenicilina, celtiofur, tetraciclina, ticarcilina y tribrissen (Rose et al., 2009). Otro estudio encontró que M. haemolytica es altamente resistente a penicilina y también a f lorfenicol (Pijoan y Aguilar, 2000). La administración de antibióticos de uso veterinario, como florfenicol, celtiofur o tribrissen, puede inducir la selección de bacterias resistentes a los antibióticos en la población animal, que después puede exten-derse a los humanos a través de la cadena alimentaria. La fauna silvestre no se encuentra aislada de la cadena alimentaria y por ende muchos de los problemas en ganadería y clínica humana se están observando en estos animales (Van der Bogaard y Stobbering, 2000).
La resistencia a uno o a varios antibióticos en las bacterias aisladas en animales silvestres es un factor de riesgo para su salud (Vargas et al., 2010). Adicionalmente, el uso de antimicrobianos en la población humana y animal resulta en la liberación de residuos que portan tanto antibióticos como bacterias resistentes a ellos en los ambientes terrestres y marinos (Silbergeld et al., 2008). En nuestro estudio es interesante notar que la mayor resistencia bacteriana se manifestó en los lugares donde hubo mayor concentración con metales pesados, lo que refuerza lo establecido por Montuelle et al. (1994), quienes indican que la resistencia de la flora microbiana depende de la concentración de estos elementos químicos en el ambiente. La Isla Cachagua está ubicada en una zona altamente industrializada y con asentamientos humanos, mientras que Isla Chañaral está alejada de las actividades humanas (Celis et al., 2014). La liberación de As, Cu y Pb al ambiente es el resultado de diferentes actividades antropogénicas, y su presencia en el aire, agua y suelo se debe al uso de combustibles fósiles, a las fundiciones, al uso de pesticidas y fármacos, a las pinturas y a las maderas impregnadas que se usan en las viviendas (Duruibe et al., 2007).
Existe evidencia de que las bacterias resistentes a antibióticos y metales viajan grandes distancias. En ambientes remotos, como el Ártico, se ha encontrado resistencia bacteriana a Hg, Cd, Pb, Cu y Zn, en sedimentos y agua, con una correlación positiva entre metales y antibióticos (Neethu et al., 2015). Otro estudio encontró que bacterias aisladas de excretas de aves árticas presentaron resistencia a ampicilina, trime-tropina, sulfametoxazol, cloranfenicol y tetraciclina (Sjölund et al., 2008). En el norte y zona central de Chile, muchos de los vertidos al mar son aguas residuales industriales que pueden contener metales pesados (Salamanca et al., 2004) y efluentes urbanos que pueden tener metales y compuestos farmacológicos (muchos de ellos conteniendo Hg) debido al aumento del consumo por la población humana y el uso en animales (Jones et al., 2005; Heberer, 2002). En el litoral del norte y centro de Chile las corrientes oceánicas pueden movilizar los metales a grandes distancias (Celis et al., 2014) y podrían llegar hacia los sitios de anidación de los pingüinos de Humboldt si las condiciones climáticas cambiaran, razón por la cual es preciso contar con un monitoreo continuo. La resistencia bacteriana en ecosistemas marinos y terrestres contaminados con metales como Hg, Cu, Pb, Ni y Zn (Rojas et al., 2014; Ball et al., 2007) significaría que la exposición microbiana a tales metales pesados podría resultar en una selección indirecta de bacterias con resistencia a múltiples antibióticos (Baker- Austin et al., 2006; Seiler y Berendonk, 2012). Puesto que los metales pesados son todos similares en sus mecanismos de toxicidad, la tolerancia a múltiples metales es un fe-nómeno común entre las bacterias resistentes a metales (Rajbanshi, 2008). De esta manera, aunque en nuestro estudio no se pudo probar, la exposición a metales pesados podría estimular el desarrollo de cepas bacterianas nativas resistentes a antibióticos y viceversa si las condiciones cambiaran (Rojas et al., 2014). Debido al cambio climático, los sistemas biofísicos y ecológicos están siendo alterados, y como consecuencia de ello se estima que habrá un aumento de las temperaturas en el norte y zona central de Chile (González et al., 2009). Se sabe que las mayores temperaturas promueven la transmisión de patógenos (Patz et al., 2005), lo cual implica que habrá una mayor presión sobre los ecosistemas terrestres y marinos del norte y centro del país. En esas condiciones, existe un escenario propicio para que muchas cepas nativas interactúen con las bacterias gastrointestinales que expulsa el pingüino de Humboldt cuando excreta en los lugares donde anida. El impacto que podrían tener las excretas de los pingüinos de Humboldt en los lugares donde estas aves anidan es un tema que requiere ser más investigado.
Conclusiones
Las cepas resistentes a metales pesados encontradas en este estudio podrían afectar los ciclos orgánicos e inorgánicos en los ambientes del litoral septentrional y central de Chile. A pesar de que no se encontraron evidencias que indiquen que la resistencia bacteriana a metales en los lugares estudiados está fuertemente asociada a la resistencia a antibióticos, se notó cierta tendencia. En general, las cepas bacterianas aisladas de las excretas de pingüino presentan una mayor resistencia a metales pesados en los sectores que se encuentran más cercanos al litoral, los cuales presentan los niveles más elevados de metales pesados como consecuencia de las diferentes actividades antropogénicas. Esto permite localizar las zonas donde las actividades humanas impactan mayormente sobre estas especies de aves marinas, lo que sería un aporte para evaluar el grado de contaminación debida a la actividad antropogénica y que podría estar afectando la fauna del litoral y la salud humana, y ayudará a la toma de decisiones adecuadas que apunten a la reducción de las sustancias contaminantes en el ambiente.
Agradecimientos
Este estudio ha sido financiado por la Vicerrectoría de Investigación de la Univer-sidad de Concepción, a través del proyecto 214.074.051-1.0. Los autores agradecen la colaboración del personal de la Corporación Nacional Forestal (CONAF) y del Servicio Nacional de Pesca (SERNA-PESCA) para la obtención de los permisos para la toma de datos en terreno.
REFERENCIAS
Ahmed AM, Motoi Y, Sato M, Maru-yama A, Watanabe H, Fukumoto Y, Shimamoto T (2007) Zoo animals as reservoirs of Gram-negative bacteria harboring inte-grons and antimicrobial resistan-ce genes. Appl. Environ. Micro-biol. 73: 6686-6690.
Alonso A, Sánchez P, Martínez JL (2001) Environmental selection of antibiotic resistance genes. Environ. Microbiol. 3: 1-9.
Anisimova L, Siunova T, Boronin A (1993) Resistance to metals gram negative bacteria isolated from sewage and soils of indus-trials regions. Microbiology 62: 505-508.
Ball M, Carrero P, Castro D, Yarzábal A (2007) Mercury re-sistance in bacterial strains iso-lated from tailing ponds in a gold mining area near El Callao (Bolívar State, Venezuela). Curr. Microbiol. 54: 149 -154.
Baker-Austin C, Wright M, Stepa-nauskas R, McArthur J (2006) Co-selection of antibiotics and metals resistance. Tre n d s Microbiol. 14: 176 -182 .
Blais J, Macdonald R, Mackey D, Webster E, Harvey C, Smol J (2007) Biologically mediated transport of contaminants to aquatic systems. Environ. Sci. Technol. 41: 1075-1084.
Celis JE, Espejo W, González-Acuña D, Jara S, Barra R (2014) Assessment of trace me-tals and porphyrins in excreta of Humboldt penguins (Sphe-niscus humboldti) in different locations of the northern coast of Chile. Environ. Monit. Assess. 186: 1815-1824.
Cetinkaya Y, Falk P, Mayhall CG (2000) Vancomycin-resistant Enterococci. Clin. Microbiol. Rev. 13: 686 -707.
Chen S, Li X, Sun G, Zhang Y, Su J, Ye J (2015) Heavy metal in-duced antibiotic resistance in bacterium LSJC7. Int. J. Molec. Sci. 16: 23390-23404; doi:10.339 0/ijms161023390.
Diptendu S, Goutam P (2013) Molecular characterization of metal and antibiotic resistance activities in a bacterial popula-tion isolated from waste water sample. Int. J. Biotechnol. Bioeng. Res. 41: 21-30.
Duruibe J, Ogwuegbu M, Egwu-rugwu J (2007). Heavy metal pollution and human biotoxic effects. Int. J. Phys. Sci. 2: 112 -118.
Girlich D, Poirel L, Carattoli A, Kempf I, Lartigue MF, Bertini A, Nordmann P (2007) Exten-ded spectrum beta lactamase CTX-M-1 in Escherichia coliisolates from healthy poultry in France. Appl. Environ. Micro-biol. 73: 4681-4685.
González S, Salazar F, Neuen-schwander A, Arata P, Tessada R, Salas C, Searle JP (2009) Inventarios anuales de gases de efecto invernadero de Chile. Santiago, Chile. http://www2.inia.cl/medios/biblioteca/boleti-nes/ NR35866.pdf
Heberer T (2002) Occurrence, fate, and removal of pharmaceutical residues in the aquatic environ-ment: a review of recent research data. Toxicol. Lett. 131: 5 -17
Jones O, Lester J, Voulvoulis N (2005) Pharmaceuticals: a threat to drinking water? Tre n d s Biotechnol. 23: 163-167
Jones KE, Patel NG, Levy MA, Storeygard A, Balk D, Gittleman JL, Daszak P (2008) Global trends in emerging infectious diseases. Nature 451: 990-994.
Martínez D, González G (2004) Las Aves de Chile: Nueva Guía de Campo. Ediciones del Naturalista. Santiago, Chile. 620 pp.
Matuschek E, Brown DFJ, Kahlmeter G (2013) Development of the EUCAST disk diffusion antimi-crobial testing method and its implementation in routine mi-crobiology laboratories. Clin. Microbiol. Infect. 20: O255-O266.
Meza J, Simeone A, García M, Monsalve B (1998) Censos de Pingüino de Humboldt(Sphenis-cus humboldti) en el Monu-mento Natural Isla Cachagua y Santuario de la Naturaleza Islote Pájaro Niño, 1990-1997. Boletín Técnico 66. Corporación Nacional Forestal. Santiago, Chile.
Mondaca M, Abarzúa M, ParedesK, Maugeri T, Martínez M (1993) Transferencia de resisten-cia a metales pesados en bacte-rias aisladas del río Bío Bío, VII Región, Chile. Rev. Latinoam. Microbiol. 35: 39-43.
Monge-Amaya O, Valenzuela-García J, Acedo-Félix E, Certucha-Barragán M, Almendáriz-Tapia F (2008) Biosorción de cobre en sistema por lote y continuo con bacterias aerobias inmovilizadas en zeolita natural (clinoptilo-lita). Rev. Int. Contam. Amb. 24: 107-115.
Montuelle B, Latour X, Volat B, Gounet A (1994) Toxicity of heavy metals to bacteria in se-diments. Bull. Environ. Contam. Toxicol. 53: 753-758.
Moraga R, Merino C, Mondaca MA (2003) Resistencia a metales pesa-dos en bacterias aisladas de la ba-hía de Iquique. Inv. Mar. 31: 91-95.
Muñoz J, Becker PH (1999) The Kelp Gull as bioindicator of environmental chemicals in the Magellan region. A comparison with other coastal sites in Chile. Sci. Mar. 63: 495-502.
Neethu C, Mujeeb K, Saramma A, Mohamed A (2015) Heavy-metal resistance in gram-negative bac-teria isolated from Kongsfjord, Arctic. Can. J. Microbiol. 61: 429- 435.
Nies DH (2003) Efflux-mediated heavy metal resistance in prokaryotes. FEMS Microbiol. Rev. 27: 313 -339.
Pathak S, Gopa K (2005) Occu-rrence of antibiotic and metal resistance in bacteria from or-gans of river fish. Environ. Res. 98: 100 -103.
Patz JA, Campbell-Lendrum D, Holloway T, Foley JA (2005) Impact of regional climate chan-ge on human health. Nature438: 310 -317.
Pijoan P, Aguilar F (2000) Resis-tencia y sensibilidad a antimi-crobianos en cepas de Pas-teurella haemolytica, P. multo-cida y Haemophilus somnus, aisladas en becerras lecheras en establos de Tijuana. Vet . Mé x . 31: 153-156.
Poole K (2005) Pseudomonas aeru-ginosa. En Frontiers in Antimi-crobial Resistance: A Tribute to Stuart B. Levy. ASM Press. Wa-shington, DC, EEUU. pp. 355-366.
Rajbanshi A (2008) Study on heavy metal resistant bacteria in gu-heswori sewage treatment plant. Our Nat. 6: 52-57.
Rojas M, Botello W, Ball M (2014) Resistencia a antibióticos y me-tales pesados en bacterias aisla-das de subsuelo en la región El Callao, Venezuela. Rev. Col. Biotecnol. 16: 141-149.
Rose JM, Gast RJ, Bogomolni A, Ellis JC, Lentell BJ, Touhey K, Moore M (2009) Occurrence and pat-terns of antibiotic resistance in vertebrates off the Northeastern United States coast. FEMS Microbiol. Ecol. 67: 421- 431.
Sakurada A (2008) Chryseobacterium indologenes. Rev. Chil. Infectol. 25: 446.
Salamanca M, Jara B, Rodríguez T (2004) Niveles de Cu, Pb y Zn en aguas y Perumytilus purpu-ratus en Bahía San Jorge, norte de Chile. Gayana 68: 53-62.
Seiler C, Berendonk T (2012) Heavy metal driven co-selection of antibiotic resistance in soil and water bodies impacted by agri-culture and aquaculture. Front. Microbiol. 3: 399.
Silbergeld EK, Graham J, Price LB(2008) Industrial food animalproduction, antimicrobial resistance,and human health. Annu.Rev. Public Health 29: 151-169.
Singer R, Ward MP, Maldonado G (2006) Can landscape ecology untangle the complexity of anti-biotic resistance? Nat. Rev. Microbiol. 4: 943-952.
Sjölund M, Bonnedahl J, Hernandez J, Bengtsson S, Cederbrant G, Pinhassi J, Kahlmeter G, Olsen B (2008) Dissemination of multidrug-resistant bacteria into the Arctic. Emerg. Infect. Dis. 14: 70-72.
Summers AO (2002) Generally overlooked fundamentals of bacterial genetics and ecology. Clin. Infect. Dis. 34: S85-S92.
Summers AO, Wireman J, Vimy MJ, Lorscheider FL, Marshall B, Levy SB, Bennett S, Billard L (1993) Mercury released from dental silver fillings provokes an increase in mercury-resistant and antibiotic resistant bacteria in oral and intestinal floras of primates. Antimicrob. Agents Chemother. 37: 825-834.
Van der Bogaard A, Stobbering E (2000) Epidemiology of resistance to ant ibiot ics. Links between animals and humans. Int . J. Ant imicrob. Agents 14: 327-335.
Vargas J, Máttar S, Monsalve S (2010) Bacterias patógenas con alta resistencia a antibióticos: estudio sobre reservorios bacterianos en animales cautivos en el zoológico de Barranquilla. Infectio14: 6-19.
Vermeer K, Castilla JC (1991) High cadmium residues observed during a pilot study in shorebirds and their prey downstream from the El Salvador cooper mine, Chile. Bull. Environ. Contam. Toxicol. 46: 242-258.
Zhang C, Hsu H, Li C (2012) Brevun-dimonas vesicularis bacteremia resistant to trimethoprim-sulfamethoxazole and ceftazidime in a tertiary hospital in southern Taiwan. J. Microbiol. Immunol. Infect. 45: 448-45
Notas
e-mail: jcelis@udec.cl
