Artículos
PROTEÍNAS DEL LACTOSUERO: USOS, RELACIÓN CON LA SALUD Y BIOACTIVIDADES
WHEY PROTEIN: USES, RELATION TO HEALTH AND BIOACTIVITIES
PROTEÍNAS DE SORO DO LEITE: USOS, RELAÇÃO COM A SAÚDE E BIOATIVIDADES
PROTEÍNAS DEL LACTOSUERO: USOS, RELACIÓN CON LA SALUD Y BIOACTIVIDADES
Interciencia, vol. 42, núm. 11, pp. 712-718, 2017
Asociación Interciencia
Recepción: 03/11/2016
Aprobación: 24/10/2017
Resumen: El lactosuero (LS) es el subproducto líquido resultante de la coagulación de las proteínas caseicas de la leche durante la preparación del queso; tiene una composición similar a la de la leche desnatada, y está compuesto principalmente de proteínas, lactosa, vitaminas y minerales. Esta revisión resume las características de las proteínas del suero y sus implicacio nes en la salud humana. Se pone de manifiesto que la utilización del LS aporta beneficios a la salud del consumidor, ya que adicional a su alto valor nutritivo presenta propiedades inmunomoduladoras, antioxidantes, antimicrobianas, antivirales, anticancerígenas, antiulcerosas y protege al sistema cardiovascular.
Palabras clave: Bioactividad, Lactosuero, Propiedades Funcionales, Proteínas.
Abstract: Whey is the liquid product resulting from the coagulation of milk casein proteins during the elaboration of cheese; it has a similar composition to skimmed milk, and is mainly composed of proteins, lactose, vitamins and minerals. This review summarizes the characteristics of whey proteins and their implications on human health. It shows that the use of whey brings benefits to consumer health, since in addition to its high nutritional value, it has immunomodulatory, antioxidant, antimicrobial, antiviral, anti-cancer, and anti-ulcer properties, and protects the cardiovascular system.
Resumo: O soro do leite (LS) é o subproduto líquido resultante da coagulação de proteínas de caseína do leite durante a elaboração do queijo; a sua composição é semelhante à do leite magro, e é composta principalmente por proteínas, lactose, vitaminas e minerais. Esta revisão resume as características das proteínas do soro do leite e as suas implicações na saúde humana. Verifica-se que a utilização de LS traz benefícios para a saúde do consumidor, devido a que, para além do seu alto valor nutricional, este possui propriedades imunomoduladoras, antioxidantes, antimicrobianas, antivirais, anticancerígenas e antiulcerosas, protegendo o sistema cardiovascula
El lactosuero (LS) es el líquido remanente que resulta de la coagulación de las proteínas caseicas de la leche durante la elaboración de queso. El LS representa ~90% del volumen total de la leche, y contiene la mayor parte de los componentes solubles en agua, tales como carbohidratos, minerales, vitaminas hidrosolubles y proteínas solubles (Hernández-Ledesma et al., 2008). El LS conserva ~50% del total de los sólidos de la leche y el 20% de las proteínas (Smithers, 2008).
La producción mundial de LS es directamente proporcional al crecimiento de la industria procesadora de queso. El 85% del LS en México es desechado (Panesar et al., 2007). Se estima que anualmente se generan a nivel mundial 118×106t de LS, lo que equivale a ~7×106t de sólidos (Cruz et al., 2009). Los avances tecnológicos han permitido que se utilice ~50% del LS producido, el cual se transforma principalmente en suero en polvo, aislado de proteína de suero, bioetanol, biopolímeros, hidrógeno, metano, electricidad y probióticos (Yadavet al., 2015). El LS remanente se utiliza como alimento para animales, como fertilizante, o es desechado al medio ambiente (Jauregi y Welderufael, 2010). Esto último es consecuencia de la ausencia de métodos económicamente viables que permitan su utilización, lo que ocasiona contaminación ambiental debido a su alta (45000-60000ppm) demanda biológica de oxígeno (Arora et al., 2013). Esta condición ha hecho que el LS sea considerado como uno de los efluentes de mayor importancia en los países en vías de desarrollo (Bainotti et al., 1987).
Las proteínas del lactosuero (PLS) tienen propiedades funcionales y nutricionales únicas, lo cual ha aumentado la demanda no solo del LS; sino también de sus hidrolizados (Jauregi y Welderufael, 2010), ya que actualmente los consumidores están interesados en consumir alimentos funcionales (Ares et al., 2009). Recientemente se ha argumentado que las PLS tienen actividad antiinflamatoria, antitumoral, inmunomodulatoria, hipotensiva, antidiabética, osteoprotectiva, anticancerígena, antihipertensiva y radioprotectiva (Patel, 2015). Además, se indica que participan en la miogénesis (formación de tejido muscular durante el desarrollo de un embrión) y en la disminución del riesgo de padecer obesidad (Drago, 2007; Cruz et al., 2009; Dryakova et al., 2010).
Utilización del Lactosuero en la Industria
El LS es una fuente de proteína de alta calidad económicamente accesible (Luhovyy et al., 2007). El 50% del LS producido a nivel mundial es tratado y transformado en productos alimenticios. El 45% es utilizado directamente en forma líquida, 30% se deshidrata para su uso como polvo, 15% se industrializa para extraer lactosa y con el resto se elabora concentrado proteico de LS en polvo (Panesar et al., 2007).
En países como Nueva Zelanda y Japón, esta materia prima se utiliza en la elaboración de fórmulas lácteas, pastas dentífricas, alimentos nutracéuticos, pomadas antifúngicas y en la industria cosmetológica (Baró et al., 2001). Además, se emplea en la elabo- ración de productos lácteos, cárnicos, panaderia, bebidas, postres, confitería, productos farmacéuticos, formulaciones infantiles y alimentos dietéticos, entre otros (Elpidia, 2013).
Uno de los usos más comunes del LS es como ingrediente en la producción de bebidas (Baccouche et al., 2013; Varghese et al., 2014). Éstas se caracterizan por proporcionar energía, regular la temperatura del cuerpo, evitar la deshidratación y calmar la sed (Shaikh et al., 2001). Como se mencionó, el LS es una fuente barata de proteína y, por lo tanto, la elaboración de bebidas a base de este, a escala comercial, tiene ventajas económicas (Shaikh et al., 2001). Se ha mencionado que esta materia prima, altamente nutritiva, podría sustituir a la leche (Almeida et al., 2009). Otro uso común que se le da a este subproducto en la industria alimentaria, es para la producción de requesón o queso ricotta (Cujano-Guambo, 2016).
Composición Química del Lactosuero
Dada su composición química, el LS está considerado como un subproducto altamente nutritivo (Dragone et al., 2009). Esta composición depende de la etapa de lactancia, especie, alimentación y raza del animal, así como de la estación del año (El-Hatmi et al., 2007) y principalmente de las técnicas de procesamiento empleadas durante la elaboración del queso del cual proviene (Tabla I). Existen dos tipos de suero, el que se origina cuando la fracción de caseína de la leche se separa mediante acción enzimática del resto de las proteínas lácteas, se denomina ‘suero dulce’; por otro lado, el ‘suero ácido’ se obtiene tras la coagulación ácida de las caseínas a un pH<5. Las principales diferencias entre los dos tipos de LS radican en el contenido de minerales, acidez y la composición química de la fracción proteica (Panesar et al., 2007).
La lactosa es el principal componente sólido del LS, éste contiene entre 45 y 50g·l-1, lo cual representa el 50% del total de los sólidos; las proteínas se encuentran entre 6 a 8g·l-1, contiene 0,5g·l-1 de ácido láctico, y cantidades apreciables de ácido cítrico, compuestos nitrogenados no proteicos (urea y ácido úrico) y vitaminas del grupo B (Dragone et al., 2009).
A pesar de sus propiedades nutritivas, en algunos países se le considera un contaminante ambiental (Rathi et al., 2015) ya que en ocasiones es vertido al suelo y/o ríos, afectando seriamente la disponibilidad de oxígeno (Liang et al., 2006). En cuanto al impacto ecológico, se estima que por cada 1000 litros de LS se genera una demanda bioquímica de oxígeno (DBO) de 35kg y una demanda química de oxígeno (DQO) de 68kg, lo que es equivalente a la fuerza contaminante de las aguas negras producidas por 450 personas en un día (Liang et al., 2006).
Proteínas del Lactosuero
El LS constituye 85-90% del volumen de la leche utilizada en la producción de queso. Las proteínas séricas (PS) representan el 55% de los nutrientes de la leche, son proteínas globulares, solubles en agua, no coagulan por cambios de pH y se separan de la cuajada de forma manual, mecánica o por temperatura (McIntosh et al., 1998; Wakabayashi et al., 2006; Sinha et al., 2007). La β-lactoglo- bulina (β-LG) es la PS más abundante y tiene un peso molecular de 18.266Da (Buffoni et al., 2011), presenta dos isoformas (β-LG A y β-LG B) (Ding et al., 2011), que difieren en dos aminoácidos, el ácido aspártico en la posición 64 y la valina en la posición 118 (Guyomarc’h et al., 2014). Por otro lado, la α-lactoalbúmina (α-LA) es la segunda proteína más abundante y posee una cadena polipeptídica de 123 aminoácidos y tiene un peso molecular de 14.2kDa (Zhang et al., 2014).
Las inmunoglobulinas y albúminas, representan el 13 y 7% (P/V), respectivamente. Asimismo, contiene otras proteínas en menor cantidad, entre las cuales están la lactoferrina, lactoperoxidasa y las lisozimas (Kruger et al., 2006)
Las PS son ricas en aminoácidos esenciales (Parra, 2009; Burd y Phillips, 2010), cuya concentración se muestra en la Tabla II. En comparación con otras fuentes de proteínas alimentarias, las PS contienen la mayor concentración de L-leucina, L-valina y L-isoleucina (Goulart et al., 2014). De hecho, éstas poseen un valor biológico elevado en comparación con las proteínas del huevo o la soya (Jáuregui y Welderufael, 2010).
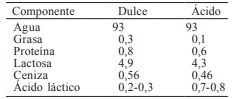
* % pesovolumen Tomado de Dragone et al 2009
Implicaciones de las PLS en la Salud Humana
El papel que la industria alimenticia tiene en la vida cotidiana de los consumidores es innegable, así como lo es la importancia de la dieta en la prevención de enfermedades y su relación con la salud (Komatsu et al., 2013). El consumo de alimentos enriquecidos o elaborados a base de PLS puede modificar o influenciar positivamente la salud de los consumidores, ya que presentan múltiples funciones biológicas y fisiológicas que ayudan a mantener estable los sistemas digestivo, óseo, inmunológico, nervioso, cardiovascular y muscular (Baró et al., 2001).
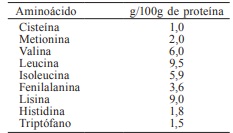
Tomado de Parra (2009)
Sistema digestivo
A nivel digestivo se ha demostrado que la a-lactoalbumina de origen bovino juega un papel central en la síntesis de la lactosa, durante el rápido crecimiento del neonato; aunque esta proteína no es idéntica a la a-lactoalbumina de origen humano, estas presentan una similitud del 72% en su secuencia, por lo que la a-lactoalbumina de origen bovino es ahora adicionada a fórmulas para infantes, para beneficiar a aquellos que se alimentan con estas fórmulas (Ding et al., 2011). Además, se han reportado efectos positivos en el tratamiento de diferentes grados de colitis ulcerosa (Suzuki et al., 2006). También se ha demostrado que al igual que sus hidrolizados ayuda a controlar la ingesta de alimentos, mejora la sensibilidad a la insulina y tiene propiedades insulinotrópicas que provocan una reducción en los niveles de glucosa sanguínea, tanto en sujetos con diabetes mellitus tipo II (DMII), como en individuos sanos (Petersen et al., 2009; Goudarzi y Madadlou, 2013; Jakubowicz y Froy, 2013; Ooi et al., 2015).
Sistema óseo y hematopoyético
Tanto las PLS como los complejos minerales extraídos del LS parecen impactar positivamente la densidad osea (Tsuchita et al., 1993) y en el crecimiento y diferenciación de los osteocitos (Kruger et al., 2006). También pueden ser aprovechadas para promover la biodisponibilidad de hierro y así prevenir la anemia, ya que su estructura peptídica permite ligar cationes di y trivalentes (Kim et al., 2004).
Sistema inmunológico
Los aminoácidos esenciales de la β-LG estimulan la síntesis de glutation, tripéptido conocido por su efecto anticancerígeno a nivel intestinal (Hernández-Ledesma et al., 2008). Otro efecto inmunológico es la portación de ácido retinoico, el cual modula las respuestas linfáticas en caso de infecciones y propagación de tumores (Sharma y Shah, 2010).
Sistema nervioso
Se considera que la α-LA mejora la calidad del sueño, por ser una fuente de triptófano y estimular la formación de serotonina. Al modificar la calidad del sueño, disminuye el nivel de estrés y como consecuencia, mejora el estado de ánimo y el funcionamiento cognitivo (Sharma y Shah, 2010).
Sistema cardiovascular
Actualmente el número de personas con sobrepeso representa un problema de salud a nivel mundial (Sinnot et al., 2009). La concentración de lípidos en la sangre, la obesidad, y el sobrepeso son factores de riesgo en el desarrollo de enfermedades cardiovasculares (Fenkci et al., 2006; Lasker et al., 2008). Las PLS solas o en combinación con aminoácidos, vitaminas y minerales previenen indirectamente las enfermedades cardiovasculares y otros padecimientos metabólicos tales como la DMII, hipertensión y dislipidemia e hiperglucemia (Frestedt et al., 2008; Siddiqui et al., 2008; Pilvi et al., 2009; McGregor y Poppit, 2013; Ooi et al., 2015). Debido a que también disminuyen los niveles de triglicéridos (Hernández-Ledesma et al., 2008; Pal et al., 2010), mejoran la tolerancia en la ingesta de glucosa e incrementan la liberación de colescitoquinina, la cual produce una sensación de saciedad, además de reducir la presión sanguínea, la inflamación y el estrés oxidativo (Shi et al., 2011; Sousa et al., 2012; Tranberg et al., 2015). Por lo anterior, las PLS pueden utilizarse para fortalecer los tratamientos contra la obesidad y la DMII (Sousa et al., 2012).
Péptidos Bioactivos Derivados de las Proteínas del Lactosuero
Las proteínas son consideradas precursores de péptidos bioactivos (PB), los cuales se encuentran encriptados en la secuencia parental de la proteína. Una vez liberados, tienen una gran variedad de actividades biológicas, muchas de ellas capaces de disminuir el riesgo de enfermedades y mejorar la salud (Möller et al., 2008). Hasta el momento, se les han atribuido actividades antioxidante, antimicrobiana, opioide, antitrombótica, acarreadora de minerales, hipolipidémiante, antihipertensiva e inmunomoduladora (FitzGerald y Meisel, 1999; Möller et al., 2008; Cruz et al., 2009; Dryakova et al., 2010; Unal y Akalin, 2012).
En los últimos años se ha incrementado el interés por los PB provenientes de las PLS debido a que en esta matriz se encuentran en grandes cantidades, con alto grado de pureza y a bajo costo (Haque y Chand, 2008). Los PB pue- den ser liberados a través de diferentes procesos hidrolíticos, ya sea mediante el uso de enzimas gastrointestinales o por técnicas fermentativas (Möller et al., 2008; Bhat et al., 2015) basadas principalmente en el uso de bacterias ácido lácticas (Meisel y Bockelmann, 1999). El tamaño de las secuencias peptídicas bioactivas puede variar, siendo éstas de entre 2 a 20 aminoácidos (Haque y Chand, 2008).
Actividad antihipertensiva
La hipertensión es uno de los principales factores de riesgo para un gran número de enfermedades cardiovasculares (Haque y Chand, 2008). Para que los PB ejerzan actividad inhibitoria sobre la enzima convertidora de la angiotensina (ECA) es necesario que las PLS los liberen mediante una hidrólisis enzimática (pepsina, tripsina y quimotripsina) o por medio de microorganismos proteolíticos (Haque y Chand, 2008). La Tabla III muestra los PB que ejercen un efecto inhibitorio sobre la ECA, el cual se traduce en un efecto antihipertemsivo.
Actividad antioxidante
Las PLS son capaces de promover beneficios antioxidantes (Chatterjee et al., 2015), efecto que se relaciona con su capacidad para captar radicales libres, no solo a nivel sistémico, sino también en los productos alimenticios (Landoni et al., 2009; Dryakova et al., 2010; Mann et al., 2015). Algunos de los PB que han sido reportados con actividad antioxidante se presentan en la Tabla IV.
Actividad inmunomodulatoria
La actividad inmunomodulatoria se atribuye a los fragmentos derivados de αs1-CN, β-CN, κ-CN y α-La. El mecanismo de acción no es completamente conocido y la hipótesis más aceptada considera que la unión a los receptores opiáceos en la membrana de los lin focitos, influye en la capacidad inmunoreactiva; el aminoácido arginina en los extremos amino o carboxilo terminal pare- ce ser la zona reconocida por los receptores específicos de la membrana de los linfocitos y los macrófagos (Hernández, 2002).
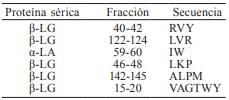
Tomado de Raikos y Dassios (2014)

Tomado de Ricci-Cabello et al. (2012), Hernández-Ledesma et al. (2008).
Se ha reportado que el péptido Tyr-Gly, correspondiente a los fragmentos f(18-19) y f(50-51) de la α-La, y el tripéptido Tyr-Gly-Gly, que corresponde al fragmento f(18-20) de la α-La, modulan in vitro la producción de linfoquinas (sustancias que inhiben o estimulan diferentes aspectos de la respuesta inmunitaria), por lo que se están empleando como coadyugante en el tratamiento del síndrome de la inmunodeficiencia adquirida (SIDA) (Hernández, 2002).
Actividad antimicrobiana
La actividad antimicrobiana in vitro se atribuye a fragmentos de caseínas y a la lactoferrina (Hati et al., 2017). El efecto antimicrobiano de los PB derivados de las PLS parece estar relacionado con la carga neta positiva de estos péptidos (Silva y Malcata, 2005). Los PB derivados de las PLS son la Lacto- ferricina y su fragmento f(17-41), los cuales inhiben a las bacterias Bacillus, Lis- teria, Streptococcus, E. coli, Klebsiella, Salmonella, Proteus y Pseudomonas, y a levaduras como Candida (Hernández, 2002; Meisel, 2001), y algunos péptidos derivados de la b-lactoglobulina correspondientes a las fracciones f(15-20), f(25-40), f(78-83) y f(92-100) que inhiben bacterias gram-positivas (Pellegrini et al., 1999).
Actividad opioide, antitrombótica y acarreadora de minerales
Estas bioactividades han sido poco estudiadas en el LS, aunque si están ampliamente distribuidas en las caseínas. La actividad opioide que resulta de las PLS se debe a la a-lactoalbúmina y la b-lactoglobulina, conocidas como lactorfinas, ya que aumentan el transpote de electrolitos en el epitelio intestinal, además de modular la concentración de insulina postprandial y la liberación del polipéptido pancreático (Aranceta y Serra, 2005). Así mismo, se ha relacionado la actividad antitrombótica con la regulación del sistema cardiovascular; se ha encontrado que las PLS liberan biopeptidos que inhiben enlaces del fibrinógeno y trombina además del factor dependiente de inhibición plaquetaria (Clare y Swais- good, 2000; Jauhiainen et al., 2007). Por otra parte, entre las casoplatelinas, principales péptidos antitromboticos, se encuentra la secuencia peptidica Lys-Arg-AspSer-Glu-Arg-Lys-Arg-Asp-Ser, proveniente de la lactoferrina (Rodríguez-Hernández et al., 2014).
Alergenicidad de las Proteínas del Lactosuero
A pesar de todos sus beneficios, las PLS pueden también ser asociadas con hipersensibilidad alimentaria, no solo en lactantes sino también en niños y adultos (Sampelayo et al., 2006). Las alergias alimentarias son una respuesta inmunológica anormal y representan un problema de salud importante, sobre todo en países industrializados, en los que se ha estimado que afecta entre el 1 y 2% de la población adulta y hasta al 8% de los niños menores de 7 años (Monaci et al., 2006; Cervantes et al., 2007). La evolución del efecto alergénico de las PLS es generalmente favorable, ya que tiene una tasa de remisión del 50% al año de edad, 75% a los 2 años y del 90% a los 3 años (Lozano de la Torre y Lorente Toledano, 1999); sin embargo, alrededor del 15% de los niños permanecen con ella (Monaci et al., 2006). Diversas investigaciones con respecto a la antigenicidad de las proteínas de la leche bovina mencionan que los alérgenos principales son la b-LG y la α-LA (Prioult et al., 2005; Monaci et al., 2006; Lakshman et al., 2011; López-Expósito et al., 2012; Shi et al., 2014)
Se han descrito diferentes métodos de procesamiento dirigidos a disminuir los problemas de alergias asociados con el consumo de PLS, entre ellos se contemplan tratamientos enzimáticos y térmicos (Sampelayo et al., 2006; Micinski et al., 2012, 2013) y/o la combinación de los mismos (Lakshman et al., 2011). Los sistemas enzimáticos utilizados pueden ser de origen vegetal (bromelina), bacteriano (Bifidobacterium lactis, Lactobacillus casei) o gástrico, y pueden utilizarse solos o en combinación (Prioult et al., 2005; Lakshman et al., 2011; Shi et al., 2014).
La hidrólisis enzimática de estas proteínas suele considerarse el proceso más eficiente para reducir su alergenicidad, así como su carga antialergénica y el riesgo de sensibilización, sobre todo en fórmulas lácteas (Fritsché, 2003). El principio de los hidrolizados se basa en la premisa de que las proteínas predigeridas están constituidas por una mezcla de aminoácidos y péptidos que proporcionan nutrientes de forma no alergénica (Ragno et al., 1993).
Otras estrategias incluyen mezclar α-LA y β-LG con maltosa, someterla a una reacción de Maillard en combinación con microondas (200W) a pH ácido (El-Mecherfi et al., 2011). Ello ocasiona una disminución de la antigenicidad de 32,25 a 10,91µg·ml-1 para la α-LA y de 272,4 a 38,17µg·ml-1 para la b-LB (Li et al., 2011).
Lo anteriormente descrito demuestra los efectos positivos que presentan las PLS sobre la salud. Sin embargo, es importante considerar que el efecto biológico atribuido a éstos péptidos debe ser medible, y al mismo tiempo excluirse efectos perjudiciales como toxicidad, alergenicidad y mutagenicidad (Möller et al., 2008).
Conclusiones
Las PLS son una alternativa para el tratamiento y prevención de algunas enfermedades, lo que da valor agregado a los productos alimenticios en los cuales son integradas. A nivel mundial, las grandes cantidades de suero desechado, producido tras la elaboración de quesos, han generado un problema de contaminación ambiental grave, por lo que es recomendable utilizar este subproducto de la industria quesera. Se ha demostrado que éste contribuye al mejoramiento de la salud humana por presentar bioactividades tales como propiedades inmunomoduladoras, antioxidantes, antimicrobianas, antivirales, anticancerígenas, antiulcerosas y proteger al sistema cardiovascular.
REFERENCIAS
Almeida KE, Tamime AY, Oliveira MN (2009) Influence of total solids contents of milk whey on the acidifying profile and viability of various lactic acid bacteria. Food Sci. Technol.-LWT 42: 672-678.
Aranceta J, Serra Ll (2005) Leche, Lácteos y Sa- lud. Médica Panamericana. Madrid, Espa- ña. 71 pp.
Ares G, Giménez A, Gámbaro A (2009) Consu- mer perceived healthiness and willingness to try functional milk desserts: influence of ingredient name and health claim. Food Qual. Pref. 20: 50.56.
Arora S, Shendurse AM, Sharma V, Wadhwa BK, Singh AK (2013) Assessment of stability of binary sweetener blend (aspartame x acesulfame-K) during storage in whey lemon beverage. J. Food Sci. Technol. 50: 770-776.
Baccouche A, Ennouri M, Felfoul I, Attia H (2013) A physical stability study of wheybased prickly pear beverages. Food Hydrocoll. 33: 234-244.
Bainotti AE, Basilico JC, Carrasco de Mendoza MS (1987) Optimización de condiciones para la producción discontinua de proteína unicelular utilizando suero de leche. Rev. Argent. Microbiol. 19: 1-7.
Baró L, Jiménez JJ, Martínez-Férez A, Bouza Y (2001) Bioactive milk peptids and proteins. Ars Pharm. 42: 135-145.
Bhat ZF, Kumar S, Bhat FH (2015) Bioactive peptides of animal origin: a review. J. Food Sci. Technol. 52: 5377-539.
Buffoni JN, Bonizzi I, Pauciullo A, Ramunno L, Feligini M (2011) Characterization of the major whey proteins from milk of Mediterranean water buffalo (Bubalus bubalis). Food Chem. 127: 1515-1520.
Burd NA, Phillips SM (2010) Fast whey protein and the leucine trigger. Nutrafoods 9: 7-11.
Cervantes BR, Snachez PMP, Bacarreza ND, Montijo BE, Zarate MF, Mata RN, Garcia CM, Cadena LJF, Ramirez MJA (2007) Actualidades en alergia a la proteína de leche de vaca. Rev. Enf. Infec. Pediatr. 21: 51-59.
Chatterjee A, Kanawjia SK, Khetra Y, Saini P (2015) Discordance between in silico & in vitro analyses of ACE inhibitory & antioxidative peptides from mixed milk tryptic whey protein hydrolysate. J. Food Sci. Technol. 52: 5621-5630.
Clare DA, Swaisgood HE (2000) Bioactive milk peptides: A prospectus. J. Dairy Sci. 83: 1187-1195.
Cruz AG, Anderson deSS, Macchione MM, Teixeira AM, Schmidt FL (2009) Milk drink using whey butter cheese (queijo manteiga) and acerola juice as a potential source of vitamin C. Food Bioproc.Technol. 2: 368-373.
Cujano-Guambo DC (2016) Determinación de la temperatura y tiempo adecuado para la obtención de requesón deshidratado. Tesis. Universidad Nacional de Chimborazo. Ecua- dor. 134 pp.
Ding X, Yang Y, Zhao S, Li Y, Wang Z (2011) Analysis of α-lactalbumin, β-lactoglobulin A and B in whey protein powder, colostrum, raw milk, and infant formula by CE and LC. Dairy Sci. Technol. 91: 213-225.
Drago S, Maria E (2007) Lactoferrina: Pro- ducción industrial y aplicaciones. Rev. Mex. Cienc. Farm. 38: 30-38.
Dragone G, Mussatto SI, Oliveira JM, Teixeira JA (2009) Characterisation of volatile compounds in an alcoholic beverage produced by whey fermentation. Food Chem. 112: 929-935.
Dryakova A, Pihlanto A, Marnila P, Curda L, Kor- honen HJT (2010) Antioxidant properties of whey protein hydrolysates as measured by three methods. Eur. Food Res. Technol. 230 865-874.
El Mecherfi, KE, Saidi D, Kheroua O, Boudraa G, Touhami M, Rouaud O, Curet S, Choiset Y, Rabesona H, Chobert JM, Haertlé T (2011) Combined microwave and enzymatic treat- ments for β-lactoglobulin and bovine whey proteins and their effect on the IgE immunoreactivity. Eur. Food Res. Technol. 233: 859-867.
El-Hatmi H, Girarde JM, Gaillard JL, Yahyaoui MH, Attia H (2007) Characterisation of whey proteins of camel (Camelus dromedarius) milk and colostrums. Small Rum. Res. 70: 267-271.
Elpidia PE (2013) Whey generalities and potential use as source of calcium from high bioavility. Rev. Chil. Nutr. 40: 397-403.
Fenkci S, Sarsan A, Rota S, Ardic F (2006) Effects of resistance or aerobic exercises on metabolic parameters in obese women who are not on a diet. Adv. Ther. 23: 404-413.
FitzGerald RJ, Meisel H (1999) Lactokinins: whey protein-derived ACE inhibitory peptides. Nahrung 43: 165-175.
Frestedt JL, Zenk JL, Kuskowski MA, Ward LS, Bastian ED (2008) A whey-protein supplement increases fat loss and spares lean muscle in obese subjects: a randomized human clinical study. Nutr. Metab. 5: 1-8.
Fritsché R (2003) Animal models in food allergy: Assessment of allergenicity and preventive activity of infant formulas. Toxicol. Lett. 140-141: 303-309.
Goudarzi M, Madadlou A (2013) Influence of whey protein and its hydrolysate on prehypertension and postprandial hyperglycaemia in adult men. Int. Dairy J. 33: 62-66.
Goulart, AJ, Bassan JC, Barbosa OA, Marques DP, Silveira CB, Santos AF, Garrido SS, Resende FA. Contiero J, Monti R (2014) Transport of amino acids from milk whey by Caco 2 cell monolayer after hydrolytic action of gastrointestinal enzymes. Food Res. Int. 63: 62-70.
Guyomarc’h F, Famelart MH, Henry G, Gulzar M, Leonil J, Hamon P, Bouhallab S, Croguennec T (2014) Current ways to modify the structure of whey proteins for specific functionalities-a review. Dairy Sci. Technol. 95: 795-814.
Haque E, Chand R (2008) Antihypertensive and antimicrobial bioactive peptides from milk proteins. Eur. Food Res. Technol. 227: 7-15.
Hati S, Patel N, Sakure A, Mandal S (2017) Influence of whey protein concéntrate on the production of antibacterial peptides derived form fermented milk by lactic acid bacteria. Int. J. Pept. Res. Ther. https://doi.org/10.1007/ s10989-017-9596-2
Hernández B (2002) Caracterización y Bioacti- vidad de Péptidos Obtenidos a Partir de Proteínas Lácteas Mediante Hidrólisis Enzimática y Procesos Fermentativos. Tesis. Universi- dad Complutense de Madrid. España. 41 pp.
Hernández-Ledesma B, Recio I, Amigo L (2008) β-Lactoglobulin as source of bioactive peptides. Amino Acids 35: 257-265.
Jakubowicz D, Froy O (2013) Biochemical and metabolic mechanisms by which dietary whey protein may combat obesity and Type 2 diabetes. J. Nutr. Biochem. 24: 1-5.
Jauhiainen T, Woulle K, Vapaatalo H, Kerojoki O, Nurmela K, Lowrie C, Korpela, R (2007) Oral absorption, tissue distribution and excretion of radiolabeled analog of a milk-derived antyhipertensive peptide, Ile-Pro-Pro, in rats. Int. Dairy J. 17: 1216-1223.
Jauregi P, Welderufael, FT (2010) Added-value protein products from whey. Nutrafoods 9: 13-23.
Kim SB, Shin HS, Lim JW (2004) Separation of calcium-binding protein derived from enzymatic hydrolysates of cheese whey protein. Asian-Australas. J. Anim. Sci. 17: 712-718.
Komatsu TR, Buriti FCA, Da Silva RC, Lobo AR, Colli C, Gioielli LA, Saad SMI (2013) Nutrition claims for functional guava mousses produced with milk fat substitution by inulin and/or whey protein concentrate based on heterogeneous food legislations. Food Sci. Technol. 50: 755-765.
Kruger MC, Poulsen RC, Schollum L, Haggarty N, Ram S, Palmano K (2006) A comparison between acidic and basic protein fractions from whey or milk for reduction of bone loss in the ovariectomised rat. Int. Dairy J. 16: 1149-1156.
Lakshman PLN, Tachibana S, Toyama H, Taira T, Suganuma T, Suntornsuk W, Yasuda M (2011) Application of an acid proteinase from Monascus purpureus to reduce antigenicity of bovine milk whey protein. J. Ind. Microbiol. Biotechnol. 38: 1485-1492.
Landoni G, Mariani E, Oriani G, Donarini C, Guerrerio T, Iorio EL (2009) Improvement of antioxidant status in women conventionally treated for breast cancer after 12 months of a cow milk whey-based supplementation. A preliminary study. Mediterr. J Nutr. Metab. 2: 127-131.
Lasker DL, Evans EM, Layman DK (2008) Moderate carbohydrate, moderate protein weight loss diet reduces cardiovascular disease risk compared to high carbohydrate, low protein diet in obese adults. Nutr. Metab. 5: 30-39.
Li Z, Luo Y, Feng L (2011) Effects of Maillard reaction conditions on the antigenicity of α-lactalbumin and β-lactoglobulin in whey protein conjugated with maltose. Eur. Food Res. Technol. 233: 387-394.
Liang M, Chen VYT, Chen HL, Chen W (2006) A simple and direct isolation of whey components from raw milk by gel filtration chromatography and structural characterization by Fourier transform Raman spectroscopy. Talanta 69: 1269-1277.
López-Expósito I, Chicón R, Belloque J, LópezFandiño R, Berin MC (2012) In vivo methods for testing allergenicity show that high hydrostatic pressure hydrolysates of β-lactoglobulin are immunologically inert. J.Dairy Sci. 95: 541-548.
Lozano de la Torre MJ, Lorente TF (1999) Mesa Redonda: Alergia e intolerancia alimenta- ria: Aspectos terapéuticos. Bol. Pediatr. 39: 172-180.
Luhovyy BL, Akhavan T, Anderson GH (2007) Whey proteins in the regulation of food intake and satiety. J. Am. Coll. Nutr. 26: 704-712.
Mann B, Kumari A, Kumar R, Sharma R., Prajapati K, Mahboob S, Athira S (2015) Antioxidant activity of whey protein hydrolysates in milk beverage system. J. Food Sci. Technol. 52 3235-3241.
McGregor RA, Poppitt, SD (2013) Milk protein for improved metabolic health: a review of the evidence. Nutr. Metab. 10: 46. doi. org/10.1186/1743-7075-10-46
McIntoch GH, Royle PJ, Le Leu RK, Reegester GO, Johnson MA, Grinsted RL, Kenward RS, Smithers GW (1998) Whey protein as functional food ingredients. J. Dairy Int. 8: 425-434.
Meisel H, Bockelmann W (1999) Bioactive peptides encrypted in milk proteins: Proteolytic activation and thropho-functional properties. Ant. van Leeuwenh. 76: 207-215.
Meisel H (2001) Bioactive peptides from milk pro- teins: a perspective for consumers and producers. Aust. J. Dairy Technol. 56: 83-92.
Micinski J, Kowalski IM, Zwierzchowski G, Szarek J, Pierozyñski B, Zablocka E (2013) Characteristics of cow’s milk proteins including allergenic properties and methods for its reduction. Pol. Ann. Med. 20: 69-76.
Micinski J, Kowalski IM, Zwierzchowski G, Szarek J, Pierozyñski B, Raistenskis J (2012) The effects of bovine milk fat on human health. Pol. Ann. Med. 19: 170-175.
Möller NP, Scholz-Ahrens KE, Roos N, Schre- zenmeir J (2008) Bioactive peptides and proteins from foods: Indication for health effects.Eur. J. Nutr. 47: 171-182.
Monaci L, Tregoat V, Van Hengel AJ, Anklam E (2006) Milk allergens, their characteristics and their detection in food: A review. Eur. Food Res. Technol. 223: 149-179.
Ooi EM, Adams LA, Zhu K, Lewis JR, Kerr DA, Meng X, Solah V, Devine A, Binns CW, Prince RL (2015) Consumption of a whey protein-enriched diet may prevent hepatic steatosis associated with weight gain in elderly women. Nutr. Metab. Cardiovasc. Dis. 25: 388-395.
Pal S, Ellis V, Dhaliwal S (2010) Effects of whey protein isolate on body composition, lipids, insulin and glucose in overweight and obese individuals. Br. J. Nutr. 104: 716-723.
Panesar PS, Kennedy JF, Gandhi DN, Bunko K (2007) Bioutilisation of whey for lactic acid production. Food Chem. 105: 1-14.
Parra HRA (2009) Lactosuero: Importancia en la industria de alimentos. Rev. Fac. Nal. Agron. Medellín 62: 4967-4982.
Patel S (2015) Emerging trends in nutraceutical applications of whey protein and its derivatives. J. Food Sci. Technol. 52: 6847-6858.
Pellegrini A, Thomas U, Bramaz N, Hunziker P, Von Fellenberg R (1999) Isolation and identification of three bactericidal domains in the bovine α-lactalbumin molecule. Biochim. Biophys. Acta 1426: 439-448.
Petersen BL, Ward LS, Bastian ED, Jenkins AL, Campbell J, Vuksan V (2009) A whey protein supplement decreases post-prandial glycemia. Nutr. J. 8: 47. doi: 10.1186/14 75-2891-8-47.
Pilvi TK, Harala S, Korpela R, Mervaala EM (2009) Effects of high-calcium diets with different whey proteins on weight loss and weight regain in high fat-fed C57BL/6J mice. Br. J. Nutr. 102: 337-341.
Prioult G, Pecquet S, Fliss I (2005) Allergenicity of acidic peptides from bovine β-lactoglo- bulin is reduced by hydrolysis with Bifi- dobacterium lactis NCC362 enzymes. Int. Dairy J. 15: 439-448.
Ragno V, Giampietro PG, Bruno G, Businco L (1993) Allergenicity of milk protein hydrolysate formulae in children with cow’s milk allergy. Eur. J. Pediatr. 152: 760-762.
Rathi M, Upadhyay N, Dabur RS, Goyal A (2015) Formulation and physico-chemical analysis of whey-soymilk dahi. J. Food Sci. Technol. 52: 968-975.
Raikos V, Dassios T (2014) Health-promoting properties of bioactive peptides derived from milk proteins in infant food: A review. Dairy Sci. Technol. 94: 91-101.
Ricci-Cabello I, Olalla HM, Artacho R (2012) Possible role of milk-derived bioactive peptides in the treatment and prevention of metabolic syndrome. Nutr. Rev. 70: 241-255.
Rodríguez-Hernández G, Rentería-Monterrubio AL, Rodríguez-Figueroa JC, Chávez-Martí- nez A (2014) Biopéptidos en la leche y sus derivados: funcionamiento y beneficios a la salud. Ecosist. Recurs. Agropec. 3: 281-294.
Sampelayo MRS, Ceballos LS, Osorio MR, Lopez JB (2006) Alergia a las proteínas de la leche ¿Puede considerarse la leche de cabra hipoalergénica respecto a la de vaca? Anales 19: 79-98.
Shaikh SY, Rathi SD, Pawar VD, Agarkar BS (2001) Studies on development of a process for preparation of fermented carbonated whey beverage. Eur. Food Res. Technol. 38: 519-521.
Sharma R, Shah N (2010) Health benefits of whey proteins. Nutrafoods 9. 39-45.
Shi J, Luo Y, Xiao Y, Li Z, Xu Q, Yao M (2014) Effects of fermentation by Lactobacillus casei on the antigenicity and allergenicity of four bovine milk proteins. Int. Dairy J. 35: 75-80.
Shi J, Tauriainen E, Martonen E, Finckenberg P, Ahlroos-Lehmus A, Tuomainen A, Pilvi TK, Korpela R, Mervaala EM (2011) Whey protein isolate protects against diet-induced obesity and fatty liver formation. Int. Dairy J. 21: 513-522.
Siddiqui SMK, Chang E, Li J, Burlage C, Zou M, Buhman KK, Koser S, Donkin SS, Teegarden D (2008) Dietary intervention with vitamin D, calcium, and whey protein reduced fat mass and increased lean mass in rats. Nutr. Res. 28: 783-790.
Silva SV, Malcata FX (2005) Caseins as source of bioactive peptides. Int. Dairy J. 15: 1-15.
Sinha R, Radha C, Prakash J, Kaul P (2007) Whey protein hydrolysate: Functional properties, nutritional quality and utilization in beverage formulation. Food Chem. 101: 1484-1491.
Sinnott RA, Maddela, RL, Nelson ED, Bae S, Singh KP, Anderson JA (2009) The modifying effects of a calcium-rich whey protein supplement on weight loss and waist circumference in overweight subjects. Open Nutraceut. J. 2: 36-41.
Smithers GW (2008) Whey and whey proteins- from ‘gutter-to-gold’. Int. Dairy J. 18. 695-704.
Sousa GT, Lira FS, Rosa JC, De Oliveira EP, Oyama LM, Santos RV, Pimentel GD (2012) Dietary whey protein lessens several risk factors for metabolic diseases: a review. Lip. Health Dis. doi: 10.1186/1476-511X-11-67.
Suzuki A, Mitsuyama K, Koga H, Tomiyasu N, Masuda J, Takaki K, Tsuruta O, Toyonaga A, Sata M (2006) Bifi dogenic growth stimulator for the treatment of active ulcerative colitis: a pilot study. Nutrition 22: 76-81.
Tranberg B, Madsen AN, Hansen AK, Hellgren LI (2015) Whey-reduced weight gain is associated with a temporary growth reduction in young mice fed a high-fat diet.J. Nutr. Biochem. 26: 9-15.
Tsuchita H, Sekiguchi I, Kuwata T (1993) Compa- rison of the effects of whey mineral complexes on bone metabolism in male growing rats. J. Nutr. Sci. Vitaminol. 39: 473-487.
Unal G, Akalin AS (2012) Antioxidant and angiotensin-converting enzyme inhibitory activity of yoghurt fortified with sodium calcium caseinate or whey protein concentrate. Dairy Sci. Technol. 92: 627-639.
Varghese KS, Radhakrishna K, Bawa AS (2014) Moisture sorption characteristics of freeze dried whey- grape beverage mix. J. Food Sci. Technol. 51: 2734-2740.
Wakabayashi H, Yamauchi K, Takase M (2006) Lactoferrin research, technology and applications. Int. Dairy J. 16: 1241-1251.
Yadav JSS, Yan S, Pilli S, Kumar L, Tyagi RD, Surampalli RY (2015) Cheese whey: A potential resource to transform into bioprotein, functional/nutritional proteins and bioactive peptides. Biotechnol. Adv. 33: 756-774.
Zhang H, Yu D, Sun J, Guo H, Ding Q, Liu R, Ren F (2014) Interaction of milk whey protein with common phenolic acids. J. Mol. Struct. 1058: 228-233.