Artículos
EVALUACIÓN DE SUSTRATOS NATURALES PARA LA PRODUCCIÓN DE CONIDIOS DE Beauveria bassiana (BALS.) VUILL. (HYPOCREALES: CORDYCIPITACEAE) EN CULTIVO BIFÁSICO
EVALUATION OF NATURAL SUBSTRATES FOR PRODUCTION OF CONIDIA OF Beauveria bassiana (BALS.) VUILL. (HYPOCREALES: CORDYCIPITACEAE) IN BIPHASIC CULTURE
AVALIAÇÃO DE SUBSTRATOS NATURAIS PARA A PRODUÇÃO DE CONÍDIOS DE Beauveria bassiana (BALS.) VUILL. (HYPOCREALES: CORDYCIPITACEAE) EM CULTIVO BIFÁSICO
EVALUACIÓN DE SUSTRATOS NATURALES PARA LA PRODUCCIÓN DE CONIDIOS DE Beauveria bassiana (BALS.) VUILL. (HYPOCREALES: CORDYCIPITACEAE) EN CULTIVO BIFÁSICO
Interciencia, vol. 42, núm. 11, pp. 739-743, 2017
Asociación Interciencia
Recepción: 30/08/2016
Aprobación: 18/10/2017
Resumen: La búsqueda de nuevas y mejores alternativas para estimular la esporulación de hongos entomopatógenos es básica para el desarrollo de producciones masivas de inóculos destinados al control de algunos insectos plaga que causan pérdidas económicamente importantes. Se evaluó la producción de conidios de dos cepas nativas de Beauveria bassiana (HIB-4 e HIB-7) y una de colección (GHA) en cultivo bifásico utilizando arroz, avena, cebada, maíz, sorgo y trigo como sustratos. La producción de conidios entre los sustratos utilizados se presentó en un rango de 108 conidios/g y no se encontraron diferencias estadísticamente significativas (p≤0,05) entre los diferentes hongos evalua- dos, mientras que para la producción de conidios entre los diferentes sustratos se encontraron diferencias estadísticamente significativas (p≤0,05). La mayor producción se obtuvo con la avena la cual fue de 5,00x108 conidios/g; la menor producción de 1,72x108 conidios/g la presentó la cebada. Con arroz se produjo 3,15x108conidios/g; con sorgo y maíz 2,68; y con trigo 2,38x108 conidios/g, respectivamente. En cuanto a la viabilidad, esta fue >95% para todas las cepas durante cuatro semanas de almacenamiento, tanto a temperatura ambiente como en refrigeración.
Palabras clave: Avena, Beauveria bassiana , Conidios, Cultivo bifásico.
Abstract: The search for new and better ways to stimulate sporulation of entomopathogenic fungi is essential for the development of mass production of inoculants for the control of some insect pests that cause economically important losses. The production of conidia from two native strains of Beauveria bassiana (HIB-4 and HIB-7) and a collection strain (GHA) in biphasic culture using rice, oats, barley, corn, sorghum and wheat as substrates was evaluated. Conidia production on the various substrates used took place in a range of 108 conidia/g and no significant statistical differences (p≤0.05) between the different fungi tested were found, whereas for the production of conidia between different substrates were found statistically significant differences (p≤0.05) were fopund. The highest production was obtained with oat at 5.00x108 conidia/g and the lowest, for bar- ley, was 1.72x108 conidia/g. Rice production was 3.15x108, sorghum and maize 2.68, and wheat 2.38x108 conidia/g, respectively. Viability remained >95% for the storage of all strains for four weeks, both at room temperature and refrigerated.
Resumo: A procura por novas e melhores alternativas para estimular a esporulação de fungos entomopatógenos . fundamental para o de- senvolvimento de produções massivas de inóculos destinados para o controle de alguns insetos praga que causam perdas economicamente importantes. Avaliou-se a produção de conídios de duas cepas nativas de Beauveria bassiana (HIB-4 e HIB-7) e uma de coleção (GHA) em cultivo bifásico utilizando arroz, aveia, cevada, milho, sorgo e trigo como substratos. A produção de conídios entre os substratos utilizados se apresentou em uma faixa de 108 conídios/g e não foram encontradas diferenças estatisticamente significativas (p≤0,05) entre os diferentes fungos avaliados, enquanto que para a produção de conídios entre os diferentes substratos se encontraram diferenças estatisticamente significati- vas (p≤0,05). A maior produção se obteve com aveia, a qual foi de 5,00x108 conídios/g; a menor produção de 1,72x108 conídios/g foi da cevada. Com arroz foi produzido 3,15x108conídios/g; com sorgo e milho 2,68; e com trigo 2,38x108 conídios/g, respectivamente. Quanto à viabilidade, esta foi >95% para todas as cepas durante quatro semanas de armazenamento, tanto em temperatura ambiente quanto com refrigeração.
Introducción
El desarrollo y aplicación de agentes de control biológico de plagas adquiere relevancia como alternativa en el desarrollo de una agricultura sostenible que preserve los recursos naturales y el medio ambiente. La aplicación controlada en agroecosistemas de organismos vivos o sus meta- bolitos para el control de plagas y enfermedades implica el mejoramiento de los cultivos, al proteger las plantas del deterioro producido por agentes patógenos (Gómez et al., 2002). En la naturaleza, los hongos entomopatógenos pueden eliminar plagas o mantenerlas en niveles que no ocasionan daños económicos a los cultivos (Azevedo, 1998). Constituyen, además, el grupo de mayor importancia en el control biológico de insec- tos plaga; prácticamente todos los insectos son susceptibles a algunas de las enfermedades causadas por hongos (López-Llorca y Jansson, 2001). En la actualidad se conocen ~90 géneros y ~700 especies de hongos entomopatógenos. Entre los géneros más importantes se encuentran Metarhizium, Beauveria, Aschersonia, Entomophthora, Zoophthora, Erynia, Hirsutella, Paecilomyces (= Isaria) y Verticillium (=Lecanicillium) (López y Hans Börjes, 2001), aunque solo un número reducido de ellos, incluyendo a Entomophtorales e Hyphomycetes, ha sido bien estudiado (Qazi y Khachatourians, 2008).
Entre los hongos entomopatógenos más conocidos esta Beauveria bassiana, considerada como la especie más ampliamente distribuida de su género en el mundo y que forma parte de los entomopatógenos más destacados debido a su capacidad de infectar a más de 200 especies de nueve órdenes de insectos. Este hongo ha sido aislado, cultivado y ensayado en laboratorio para el control de insectos plaga que atacan a una diversidad de cultivos y, fundamentalmente, es utilizado para el control de lepidópteros, homópteros, coleópteros, hemípteros y dípteros de importancia económica (Zimmermann, 2007). Comprender los aspectos básicos del desarrollo de los hongos entomopatógenos y tener un conocimiento detallado de los requerimientos nutricionales para su crecimiento y esporulación es esencial para emprender su producción masiva y facilitar su comercialización. (Gandarilla- Pacheco et al., 2013a).
La producción de estos hongos para el control de insectos plaga se basa en la multiplicación masiva del hongo de interés y sus estructuras reproductivas en un sustrato natural que proporcione los nutrientes necesarios para la mayor producción de conidios al menor costo. Este procedimiento se ha desarrollado desde hace varias décadas con diversas técnicas de formulación. Actualmente se conocen diferentes métodos de producción de hongos entomopatógenos, artesanal, semi-industrial e industrial, y dicha producción se puede realizar en cultivos líquidos, cultivo mixto ( bifásico) y sólido (Jenkins et al., 1998).
Para la producción masiva de hongos entomopatógenos comúnmente se usa como sus- trato sólido el grano de arroz (Oryza sativa L.) por mantener las condiciones físicas con una adecuada superficie efectiva para el crecimiento micelial, un adecuado balance nutricional y algunas condiciones específicas acordes a los requerimientos del aislamiento en términos de aireación y humedad (Bhanu-Pakrasha et al.,2008). Otros sustratos común- mente utilizados son: cebada, avena, frijol, sorgo, trigo, soya, mijo, cacahuate, garbanzo, lenteja, chícharo, caupí (frijol africano) y estiércol de vaca (Figueroa et al., 2007; Sahayaraj y Namasivayam, 2008; Bhadauria et al., 2012; Gangwar 2013).
Los hongos se han reproducido para su uso como agentes biológicos de plagas desde hace casi un siglo, para lo cual se ha utilizado diferentes métodos de reproducción (Vélez et al., 1997). Para utilizar hongos entomopatógenos como insecticidas deben producirse cantidades masivas del hongo, el cual debe mantener su capacidad infectiva por un período de tiempo considerable. La mayoría de las especies de hongos son producidas en medios sólidos, donde el hongo crece como micelio superficial y produce conidios en hifas aéreas. Por otro lado, la producción de hongos en sustratos sólidos dificulta la automatización del proceso y carece de eficiencia económica, a escala satisfactoria, en la producción de conidios. Este problema puede ser parcialmente resuelto por un proceso de producción de dos fases (cultivo bifásico), en el que los cultivos sumergidos son utilizados para producir una gran cantidad de micelios y/o blastosporas, que es colocada después sobre un sustrato sólido para obtener los conidios necesarios (Jenkins et al., 1998; Wraight et al., 2001).
El objetivo del presente estudio fue evaluar la producción de conidios de dos aislados nativos y una cepa de ..bassiana que han mostrado potencial para el control de insectos plaga en estudios anteriores (Gandarilla-Pacheco et al., 2013b, c), mediante una alternativa de cultivo bifásico utilizando blastosporas como pre-inóculo sobre diferentes sustratos sólidos, específicamente cereales de bajo costo comercial.
Materiales y Métodos
Microorganismos
Los hongos se obtuvieron de la colección del laboratorio L6 del Instituto de Biotecnología, Facultad de Ciencias Biológicas, Universidad Autónoma de Nuevo León (FCB-UANL). Fueron conservados en viales criogénicos con 1ml de glicerol 10% v/v y almacenados en congelación a -80ºC. Los aislados nativos utilizados corresponden a las claves HIB- 4, HIB-7 y la cepa con clave GHA de Beauveria bassiana.
Producción de blastosporas para el precultivo
La cepa y los aislados nativos de B. bassiana se descongelaron por 45min a tempera- tura ambiente (25 ±2ºC) y se cultivaron en agar papa dextrosa. Las cajas se incubaron durante 14 días a 25 ±2º C bajo fotoperiodo 12:12h. Después se prepararon suspen- siones de 5×105 conidios/ml con agua destilada estéril para inocular 10 ml en matra- ces Erlenmeyer bafleados de 500ml conteniendo 90ml de caldo papa dextrosa. Se incubaron por 72h a 28ºC y 250rpm en un incubador con agitación orbital. Al final del tiempo de crecimiento se determinó la concentración total de blastosporas y mediante diluciones seriadas se ajustó la concentración a 1×106 blastos- poras/ml de cada uno de los hongos utilizados para inocular cada uno de los sustratos.
Preparación de los sustratos
Se utilizó arroz (Oryza sativa L.), avena (Avena sativa L.), cebada (Hordeum vulgare L.), maíz quebrado (Zea mays L.), sorgo (Sorghum vulgare L.) y trigo (Triticum sativum L.) como sustratos. Para eliminar la mayor cantidad de partículas ajenas al sustrato cada uno de éstos se lavó por 2min separadamente con agua corriente a presión y se dejó escurrir por 10min sobre el mismo colador donde fue lavado. Después se colocaron 50g (peso húmedo) del sustrato en bolsas de polietileno de alta densidad (HDPE) de 1kg de capacidad y 25ml de agua bidestilada. Las bolsas fueron selladas con grapas metálicas modelo Nº 400, se les colocó una cruz de cinta masking Nº 110, a la cual se denominó sitio de inoculación, en el centro de la bolsa. Todas las bolsas fueron esterilizadas en una autoclave automática a 121 ºC, 15PSI por 15 min.
Inoculación de los sustratos
Una vez esterilizadas, las bolsas se dejaron enfriar durante 24h para ser inoculadas. Para la inoculación de los diferentes hongos se utilizaron jeringas estériles con la que se inyectaron las bolsas en el sitio de inoculación. Todas las bolsas fueron inoculadas aplicando 5ml por bolsa de cada uno de los sustratos con una suspensión de 1×106 blastosporas/ml, asegurándose de esparcir sobre todo el sustrato la suspensión del hongo. Posteriormente se incubaron duran- te 14 días a temperatura ambiente (25 ±2ºC) y se expusieron a la luz blanca de las lámparas del laboratorio (12:12h L:O). Las bolsas fueron agita- das cada tercer día para esparcir las esporas homogéneamente sobre el sustrato. Al final del tiempo de crecimiento se determinó la concentración de conidios y el porcentaje de viabilidad.
Medición de la productividad del sustrato
A los 14 días de incubación se determinó la concentración de conidios por gramo de sus- trato de cada una de las bolsas, tomando 1g de cada uno de los sustratos y agregándolos en tubos de ensayo conteniendo solución estéril Tween 80 al 0,1% (v/v). Se homogenizaron en un agitador vibratorio (vórtex) durante 2min para des- prender los conidios, se realizaron diluciones seriadas y se contaron los conidios usando una cámara de Neubauer.
Determinación de la viabilidad
Como variable de calidad se determinó la viabilidad (super- vivencia) de los conidios producidos sobre avena, ya que fue el sustrato de mayor producción promedio, tanto para la cepa como para los dos aislados nativos de B. bassiana. La prueba se realizó semanalmente durante un mes de almacenaje de las bolsas a una temperatura de 4 ±2ºC (en refrigerador) y 25 ±2ºC (ambiente) en agar papa dextrosa y agar agua.
Análisis de los datos
Los resultados se expresa- ron como valores promedios. Para verificar la normalidad de los datos se realizó la prueba de Kolmogorov Smirnov, previa conversión de los resultados a su logaritmo (log10) para introducirlos en el programa estadístico, y en caso de cumplir con este criterio se realizó un análisis de varianza (ANOVA) y una prueba de Scheffé ( p≤0,05) para las medias. Los datos fueron analizados mediante el programa IBM® SPSS ® v.19.
Resultados y Discusión
La producción de conidios entre los sustratos utilizados se presentó en un rango de 108 conidios por gramo y no se encontraron diferencias esta- dísticamente significativas (p≤0,05) entre los diferentes hongos evaluados (f= 1,84; p= 0,16). Para la cepa GHA la producción promedio fue de 2,55×108, mientras que para los aislados HIB- 4 e HIB-7 rondaron los 2 ,80×108 y 9,44×108 conidios/g, respectivamente (Figura 1). Al evaluar la producción de conidios en- tre los diferentes sustratos se encontraron diferencias esta- dísticamente significativas (p≤0,05). En promedio, la mayor producción se obtuvo con la avena la cual fue de 5,00×108 conidios/g; la menor producción (1.72×108 conidios/g) se presentó en cebada. En arroz hubo una producción de 3,15×108, en sorgo y maíz de 2 ,68×108 , y en t r igo de 2,38/108 conidios/g respectivamente (Figura 2).
Con respecto a la sobrevivencia de los conidios en avena los resultados en temperatura ambiente (25 ±2ºC) y de refrigeración (4±2ºC) para los hongos evaluados en medio papa dextrosa fue de 100% durante las tres primeras semanas y en el medio agar agua fue del 100% durante las primeras tres semanas en refrigeración, mientras que a temperatura ambiente fue muy similar a la registrada en la cuarta semana (Tabla I).
Para la producción masiva de hongos entomopatógenos comúnmente se usa como sus- trato sólido el grano de arroz por mantener las condiciones físicas con una adecuada superficie efectiva para el crecimiento micelial, un adecuado balance nutricional y condiciones específicas acordes a los requerimientos del aislamiento en aireación y humedad (Bhanu et al., 2008; Sahayaraj y Namasivayam, 2008). Sin embargo, existen diferentes estudios en los que se ha bus- cado otras opciones como sus- tratos con el objetivo de reducir costos de producción y/o mejorar los rendimientos en la producción de conidios, reportados por diversos autores en años recientes. Entre los sus- tratos evaluados se encuentran cebada, avena, frijol, sorgo, trigo, soya, mijo, cacahuate, garbanzo, lenteja, chícharo, caupí (frijol africano), estiércol de vaca, por mencionar algunos (Figueroa et al., 2007; Sahayaraj y Namasivayam, 2008; Bhadauria et al., 2012; Gangwar, 2013). En el presente trabajo se utilizaron arroz, avena, cebada, maíz quebrado, sorgo y trigo considerando su bajo costo, fácil adquisición y los trabajos previos a esta investigación
Uno de los problemas más comunes cuando se utiliza un sustrato para la producción de conidios se relaciona con la alta compactación que se ejerce sobre el sustrato. Cortez Madrigal (2007) reporta que en hongos como Lecanicillium lecani, la cantidad de conidios se puede ver afectada por este factor, que evita aireación interna y, por consiguiente, reduce en la producción conidial.
Este problema pudo presentarse en el presente trabajo con B. bassiana, ya que algunos de los sustratos utilizados, como avena, maíz quebrado y principalmente arroz, presentaron dificultades por su tendencia a permanecer apelmazados después de la esterilización debido a un exceso de humedad.
En el presente estudio la producción obtenida fue del orden de 108 conidios/g. Al comparar la producción entre los seis sustratos se obtuvieron diferencias estadistícamente significativas entre ellos, siendo en avena donde se obtuvo los mejores rendimientos en comparación con la cebada, que presentó la menor producción, mientras que el arroz, sorgo, maíz y trigo mostraron resultados similares. Estos resultados coinciden con los reportados por Lucero-Maf la et al., (2004) quienes reportan valores para cepas de B. bassiana de 2,5×108 a 5×109 esporas/g utilizando trigo como sustrato. Sahayaraj y Namasivayam (2008) utilizando trigo, arroz, raghi (mijo africano), sorgo, mijo perla y maíz obtuvieron producciones de 11,76; 11,24; 10,72; 10,24; 9,78 y 9,44×108 conidios/g, respectivamente. La avena es uno de los cereales más completos y de más alto valor nutricional, ya que es rica en carbohidratos complejos, vitaminas del complejo B, minerales y aminoácidos como leucina, treonina, isoleucina y metionina, lo cual coincide con lo señalado en Volcy y Pardo (1994), quienes mencionan que un buen sustrato para la producción de conidios debe poseer un alto contenido de carbohidratos, nitrógeno, microelementos, vitaminas del complejo B y una concentración alta de iones necesarios para el crecimiento y esporulación. Bhadauria et al., (2012) al evaluar quince sustratos diferentes, entre ellos arroz, maíz, sorgo y trigo, encontraron la mayor producción de 9,06×107 conidios/g en caupí (frijol africano, frijol de cabecilla negra), seguido por el chícharo y frijol, en los cuales obtuvieron 8×107 conidios g-1. Posada-Flores (2008) y Gandarilla-Pacheco et al., (2013a) reportan valores menores a 1×1010 conidios/g en medio de cultivo bifásico utilizando arroz como sustrato para B. bassiana. La variabilidad en la producción de conidios entre los diferentes sustratos evaluados en el presente y anteriores trabajos puede deberse en parte a que el rendimiento de esporas por gramo de sustrato también se ve influenciado por la cepa y por el estado de la misma, pudiendo variar entre 5×103 y 2.5×1011 conidios/g de sustrato (Monzón, 2001). Para considerar un sustrato como idóneo a los fines de la producción de conidios de una cepa o aislado de un hongo entomopatógeno debe tomarse en cuenta su bajo costo, fácil adquisición, producción de alta concentración de conidios y capacidad para mantener la virulencia de la cepa (Roberts y Yendol, 1971).
Sin embargo, el rendimiento de la esporulación sobre un sustrato también puede ser influenciado por factores como la técnica de cultivo, concentración del inóculo inicial, condiciones de temperatura, humedad, aireación, y tiempo de incubación (Figueroa et al., 2007), así como las por diferencias nutricionales entre los sustratos.
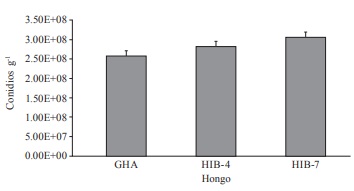
Figura 1
Producción promedio de conidios entre los diferentes hongos evaluados (GHA, HIB-4 e HIB-7) de Beauveria bassiana a los 14 días de incubación bajo condiciones de laboratorio, 25 ±2ºC y fotoperiodo 12:12h. Los tratamientos con diferente letra son significativamente dife- rentes (p≤0,05). Líneas en las barras indican el error estándar.
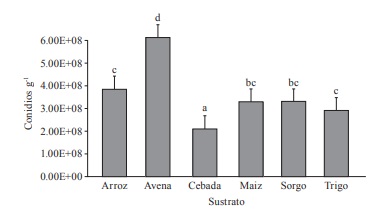
Figura 2
Producción promedio de conidios entre los diferentes sustratos evaluados a los 14 días de incubación bajo condiciones de laboratorio, 25 ±2°C y fotoperiodo 12:12h. Los tratamientos con diferente letra son significativamente diferentes (p≤0,05). Líneas en las barras indican el error estándar.
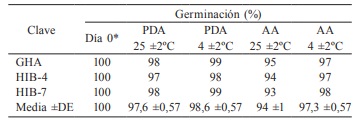
* Corresponde a la sobrevivencia de los conidios a los 14 días de incu bación bajo condiciones de laboratorio 25 ±2ºC y fotoperiodo 1212h PA agar papa dextrosa AA agar agua
Conclusiones
La producción de conidios de los hongos evaluados en los di- ferentes sustratos utilizados se mantuvo en el rango de 108 conidios/g. Sin embargo, estos resultados muestran la capacidad de los hongos evaluados para utilizar la avena como un sustra- to ventajoso para desarrollar su crecimiento y esporulación.
REFERENCIAS
Azevedo JL (1998) Controle micro- biano de insectos pragas e seu melhoramento genético. En Melo IS, Azevedo JL ( Eds.) Controle Biológico. Vol. 1. Embrapa. Jaguariúna, Brasil. pp. 69-96.
Bhadauria BP, Puri S, Singh PK (2012) Mass production of ento- mopathogenic fungi using agri- cultural products. Bioscan 7: 229-232.
Bhanu-Prakasha GVS, Padmaja V, Siva-Kiran RR (2008) Statistical optimization of process variables for the large-scale production of Metarhizium anisopliae conidiospores in solid-state fermentation. BioresourceTechnol. 99: 1530-1537.
Cortez-Madrigal H (2007) Producción de Lecanicillium (=Verticillium) lecanii en diferentes sustratos y patogenicidad. Agric. Técn. Méx. 33: 83-87.
Figueroa LM, Varela A, Corredor D (2007) Evaluación de sustratos naturales para la propagación masiva del hongo entomopatóge- no Paecilomyces fumosoroseus (Deuteromicotina: Hyphomy- cetes). Rev. Invest. 7: 127-131.
Gandarilla-Pacheco FL, Galán-Wong LJ, Arévalo-Niño K, Elías- Santos M, Quintero-Zapata I (2013a) Evaluación de aislados nativos mexicanos de Beauveria bassiana (Báls.) Vuill. (Hypo- creales: Cordycipitaceae) provenientes de zonas citrícolas para su producción masiva en cultivo sumergido y bifásico. Agrocien- cia 47: 255-266.
Gandarilla-Pacheco FL, Galán- Wong LJ, López-Arroyo J I, Rodríguez-Guerra R, Quintero- Zapata I (2013b) Optimization of pathogenicity tests for se- lection of native st rains of entomopathogenic fungi isola- ted from citrus-growing areas of México on adults of Diaphorina citri Kuwayama ( Hemiptera: Liviidae). Fla. Entomol. 96: 187-195.
Gandarilla-Pacheco FL, Galán-Wong LJ, López-Arroyo JI, Quintero- Zapata I (2013c) Patogenicidad de hongos entomopatógenos nativos de la zona citrícola de México sobre ninfas de Diaphorina citri Kuwayama (Hemiptera:Liviidae). Southw. Entomol. 38 :325-338
Gangwar GP (2013) Evaluation of different substrates for mass multiplication of Beauveria bas- siana( Balsamo) Vuillemin . Agric. Sci. Dig. 33: 321-323.
Gangwar GP (2013) Evaluation of different substrates for mass multiplication of Beauveria bas- siana ( Balsamo) Vuillemin . Agric. Sci. Dig. 33: 321-323.
Gómez E, Álvarez RM, San Juan AN, Zayas MA, Hernández J,Lemes T, Croche G, Cruz X (2002) Nematicida a partir del hongo Verticillium lecanii. Terralia 24: 30.
Jenkins NE, Heviefo G, Langewald J, Cherry A, Lomer CJ (1998) Development of mass producc- tion technology for aerial coni- dia for use as mycopesticides. Biocont. News Inf. 19: 21-31.
López-Llorca LV, Jansson HB (2001) Biodiversidad del suelo: control biológico de nemátodos fitopató- genos por hongos nematófagos. Cuad. Biodivers. 6: 12-15.
Lucero-Mafla AM, Peña-Villamil LA, Bacca-Ibarra T (2004) Evaluación de la actividad bio- controladora de Beauveria bas- siana . Metarhizium anisopliae sobre larvas de Ancognatha sca- rabaeiodes (Coleoptera: Scara- baeidae). Corpoica 5: 43-48.
Monzón A (2001) Producción, uso y control de calidad de hongos entomopatógenos en Nicaragua. Manejo Integr. Plagas 63: 95-103.
Posada-Flórez FJ (2008) Production of Beauveria bassiana fungal spores on rice to control the coffee berry borer, Hypothe- nemus hampei in Colombia. J. Insect Sci. 8: 1-13.
Qazi SS, Khachatourians GG (2008) Entomopathogenic fungi: bio- chemistry and molecular biolo- gy. En Brakhage AA, Zipfel PF ( Eds.) Human and Animal Relationships, The Mycota VI. 2a ed. Springer. Berlín, Ale- mania. pp. 33-53.
Roberts DW, Yendol WG (1971) Use of fungi for microbial control of insects. En Burgues H, Hussey N ( Eds) Microbial Control of Insects and Mites. Academic Press. London, RU. pp. 125-149.
Sahayaraj K, Namasivayam SKR (2008) Mass production of ento- mopathogenic fungi using agri- cultural products and byproducts. Afr. J. Biotechnol. 7: 1907-1910.
Vélez PA, Posada FJ, Marín P, Gon- zález MT, Osorio E, Bustillo AE (1997) Técnicas para el Con- trol de Calidad de Formula- ciones de Hongos Entomopa- tógenos. Boletín Técnico Nº 17. Centro Nacional de Investi- gaciones del Café. Manizales, Colombia. 37 pp.
Volcy C, Pardo V (1994) Principios de Micología. 19ª ed. Universidad Nacional de Colombia. 141 pp.
Wraight S, Jackson M, Kock S (2001) Production, stabilization and formulation of fungal bio- control agents. En Butt TM, Jackson C, Magan, N ( Eds.) Fungi as Biological Control Agent: Progress, Problems and Potencial. CABI. Wallingford, RU. pp. 253-280.
Zimmermann G (2007) Review on safety of the entomopathogenic fungi Beauveria bassiana and Beauveria brongniartii. Biocontr. Sci. Technol. 17: 553-596.
Notas de autor
meliassn@uanl.edu.mx