Comunicaciones
ACTIVIDAD PROTEOLÍTICA Y CONCENTRACIÓN PEPTÍDICA EN YOGUR DE LECHE DE CABRA ADICIONADO CON PROBIÓTICOS
PROTEOLYTIC ACTIVITY AND PEPTIDE CONCENTRATION OF GOAT MILK YOGURT ADDED WITH PROBIOTICS
ACTIVIDADE PROTEOLÍTICA DE PÉPTIDOS E CONCENTRAÇÃO NO IOGURTE LEITE DE CABRA COM ADIÇÃO DE PROBIÓTICOS
ACTIVIDAD PROTEOLÍTICA Y CONCENTRACIÓN PEPTÍDICA EN YOGUR DE LECHE DE CABRA ADICIONADO CON PROBIÓTICOS
Interciencia, vol. 43, núm. 1, pp. 50-54, 2018
Asociación Interciencia
Recepción: 13/12/2016
Aprobación: 02/01/2018
Resumen: El yogur es considerado un alimento funcional. La adición de probióticos favorece la actividad proteolítica, liberándose mas péptidos con actividad funcional al medio. El objetivo de este trabajo fue evaluar el efecto de la adición de probióticos sobre la proteólisis y perfil peptídico de yogur de leche de cabra. Para esto se elaboró yogur con leche de cabra adicionado de mezclas de probióticos, se almacenaron a 4ºC y se determinó acidez titulable, concentración peptídica y porcentaje de proteólisis a los 0, 7 y 14 días. La adición de probióticos aumentó la actividad proteolítica de los yogures, sin diferencias significativas de acidez entre tratamientos, ni durante la vida en anaquel.
Palabras clave: Leche de cabra, Péptidos, Probióticos, Proteólisis, Yogur.
Abstract: Yogurt is considered a functional food. The addition of probiotics and prebiotics favors the proteolytic activity, releasing more peptides with functional activity to the medium. The goal of this work was to evaluate the effect of probiotics on proteolysis and peptide profile of goat milk yogurt. To this end, yogurt was elaborated with goat’s milk and probiotic mixtures were added, stored at 4ºC. Titratable acidity, peptide concentration and percentage of proteolysis at 0, 7 and 14 days were determined. The addition of probiotics increased the proteolytic activity of the yogurts, without modifying the acidity of the same.
Resumo: O iogurte é considerado um alimento funcional. A adi ção de probióticos e prebióticos favorecem a atividade proteolítica, libertando mais péptidos com atividade funcional para o meio. O objetivo deste trabalho foi avaliar o efeito dos probióticos sobre a proteólise e o perfil peptídeo do iogurte feito a partir de leite de cabra. Para isso, elaborou-se iogurte com leite de cabra através da adição de misturas de probióticos, armazenados a 4ºC. Acidez titulável, concentração de péptidos e percentuais de proteólise foram determinados a 0, 7 e 14 dias. A adição de probióticos aumentou a atividade proteolítica do iogurte, sem modificar a sua acidez.
Introducción
La leche de cabra es considerada un alimento funcional ya que ejerce funciones nutricionales y terapéuticas (Domagala, 2009; Park, 2009). Comparada con la leche de vaca presenta menor grado de alergenicidad y es más fácil de digerir por la naturaleza de sus proteínas y sus ácidos grasos de cadena corta y mediana (Minervini et al., 2009). Por otra parte, los alimentos funcionales son alimentos o nutrientes que producen un cambio fisiológico benéfico en el cuerpo, como en el caso de los alimentos adicionados con probióticos (Duggan et al., 2002). Se estima que durante la década pasada más de 500 nuevos productos funcionales fueron introducidos al mercado (Silveira et al., 2015). El yogur es un tipo de leche fermentada por la acción simbiótica de dos bacterias termofílicas, Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. bulgaricus, las que deben encontrarse en el producto final en 1x107 UFC/g (Zourari et al., 1992). El suplementar las bebidas lácteas fermentadas con probióticos representa una opción para dar valor agregado a este tipo de productos lácteos (Castro et al., 2013). Por otra parte, se ha comprobado que la adición de probióticos provoca un incremento en la actividad proteolítica, liberándose con esto un mayor número de péptidos (da Costa et al., 2007; Dziuba y Darewicz, 2007).
La proteólisis es la degradación de las proteínas por acción del sistema proteolítico de las bacterias ácido lácticas (BAL), lo que produce pequeños péptidos y aminoácidos libres (Smit et al., 2005). Durante la fermentación de la leche, el sistema proteolítico de los cultivos iniciadores juegan un rol clave (Serra et al., 2009), ya que la proteólisis que lleva a cabo cada microorganismo es iniciada por una sola proteinasa extracelular. Sin embargo, algunas BAL no sintetizan proteinasas extracelulares, dependiendo en este caso de otras cepas que las liberen al medio. La proteólisis en leches fermentadas es entonces de suma importancia por varios aspectos: puede determinar la sobrevivencia de los cultivos iniciadores, contribuye a la formación de compuestos del sabor y olor, confiere propiedades reológicas, así como también permite la formación de péptidos bioactivos (Serra et al., 2009). De los microorganismos que se encuentran frecuentemente formando parte de los cultivos iniciadores, los más estudiados han sido Lactococcus spp. y Lactobacillus spp. (Ebringer et al., 2008). Se ha reportado que algunas especies como Lactobacillus spp. poseen proteinasas que hidrolizan en mayor medida la proteína de leche de cabra (Minervini et al., 2009). El objetivo del presente estudio, fue evaluar el efecto de la adición de probióticos en yogur elaborado a base de leche de cabra, sobre la acidez, concentración peptídica y actividad proteolítica, durante su vida en anaquel.
Materiales y Métodos
Preparación del yogur
Se prepararon, por triplicado, tres tratamientos y un control (Tabla I), siguiendo la metodología descrita por Donkor et al. (2007), con pequeñas modificaciones. La leche fue sometida a tratamiento térmico de 95ºC por 30min, enfriándose posteriormente a 37ºC e inoculándose con 1% de la totalidad de los cultivos, es decir, el control con el 1% del cultivo base para yogur (YO-MIX 495 LYO, Danisco®) y los tres tratamientos con 0,5% de cultivo base y 0,5% de cada cultivo correspondiente según se indica en la Tabla I. Finalmente, se incubaron a 37ºC hasta alcanzar un pH de 4,5. Después de alcanzar este valor, los yogures fueron enfriados y mantenidos en refrigeración (4ºC) por 15 días, tomándose muestras a los 0, 7 y 14 días a fin de determinar la acidez titulable, la concentración peptídica total y el porcentaje de proteólisis.
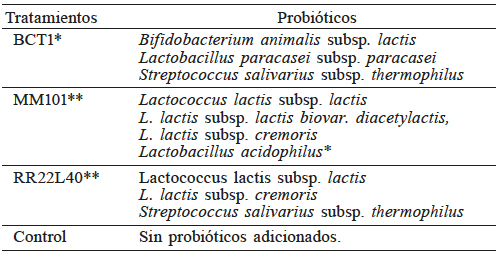
* Marca CHR HANSEN® de México S.A.** Marca Danisco® Mexicana S.A de C.V.
Obtención de los filtrados
La obtención de los filtrados de las bebidas (FB) se llevó a cabo según lo descrito por Donkor et al. (2007). Se tomaron 2,5ml de cada una de las unidades experimentales y se mezclaron con 5ml de ácido tricloroacético 0,75%. La mezcla se pasó a través de papel filtro Whatman Nº 1 de 150mm) y los filtrados fueron congelados a -20ºC hasta su análisis.
Acidez titulable
Ésta se determinó por triplicado, por el método 947.05-1947 de AOAC (1998), el cual se basa en determinar el volumen de NaOH 0,1N necesario para neutralizar los gramos por litro de ácido láctico presentes en la muestra correspondiente. En este caso se empleó 10ml de yogur, 20 ml de agua destilada y dos gotas de fenolftaleína.
Concentración peptídica total
La concentración de los péptidos contenidos en los FB se determinó por triplicado por el método de Bradford (1976). Éste se basa en la reacción de las proteínas con el colorante azul brillante de Comassie G-250 para formar un compuesto colorido que absorbe fuertemente a los 595nm. Para hacer la curva de calibración se prepararon cuatro estándares de albúmina de suero bovino a las concentraciones de 0,009; 0,006; 0,003 y 0,001mg•ml-1). Dicha técnica se emplea para la determinación de proteína total, no obstante en los FB solamente existían los péptidos filtrados. Todos los estándares se prepararon en solución salina 0,15M. Se graficó la curva y se determinó la ecuación de regresión (y= 0,0583x-0,0001, R²= 0,9993). Para el análisis de las muestras se tomaron 0,1ml de los FB o del estándar, y se mezclaron con 1ml del reactivo de Bradford, se agitaron una vez por inmersión y se dejaron reaccionar en la oscuridad a temperatura ambiente por 5min. Posteriormente se leyó la absorbancia a 595nm en un espectrofotómetro (UV-1800 Shimadzu). La medida de absorbancia obtenida se linealizó en la ecuación de regresión de la curva de calibración y se determinó la concentración peptídica de cada uno de los FB.
Actividad proteolítica
La proteólisis de cada uno de los FB se determinó por triplicado según el método de Church et al. (1983), que se basa en la reacción de las aminas primarias (NH3) libres con el O-phthaldialdehido (OPA) y el β-mercaptoetanol. El reactivo OPA se preparó de la siguiente manera: 25ml de tetraborato de sodio 100mM; 2,5 ml de sodio duodecil sulfato 20%; 40mg de OPA en 1ml de metanol; y 100μl de β-mercaptoetanol, aforándose a 50ml con agua tridestilada. Para las lecturas se tomó 50μl de cada FB, y se mezcló con 1ml del reactivo OPA por inversión de la celda de cuarzo, con 2min de incubación a temperatura ambiente y dentro del equipo para evitar la exposición a la luz. Finalmente, se leyó la absorbancia en un espectrofotómetro (UV-1800 Shimadzu) a 340nm. El grado de proteólisis se determinó por diferencia entre las actividades proteolíticas de la muestra control con cada tratamiento (Donkor et al., 2007).
Análisis estadístico
El análisis se realizó con el paquete estadístico SAS System (2006-versión 9.1.3; SAS Institute Inc, Cary, NC, EEUU). Se usó el procedimiento MIXED, por medio de un diseño anidado de bloques al azar con mediciones repetidas a través del tiempo. Se usaron como variables clasificatorias los tratamientos y las repeticiones, y como variables de respuesta los valores de acidez titulable, concentración peptídica y actividad proteolítica. Para determinar las diferencias entre los tratamientos se empleó un análisis de Tukey.
Resultados y Discusión
Acidez titulable
La acidez varió de 7,46 a 12,2g⋅l-1 de ácido láctico en las muestras de yogur monitoreadas durante su vida en anaquel, como se muestra en la Figura 1. No hubo diferencia significativa en el monitoreo de la acidez por efecto de los tratamientos, ni por efecto de la vida en anaquel. No se observaron cambios en los valores de acidez, lo cual coincide con Tranjan et al. (2009), quienes elaboraron bebidas fermentadas con suero de leche de cabra y no registraron diferencias significativas de la acidez titulable durante la vida en anaquel de las bebidas a los 0, 7 y 14 días. Así mismo, Donkor et al. (2007) elaboraron yogur con diferentes mezclas de probióticos: Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. bulgaricus, como base para todos los tratamientos y variaron la adición con L. acidophilus y L. casei, no encontraron diferencias significativas en las concentraciones de ácido láctico producido entre tratamientos y durante su vida en anaquel a los 1, 7 y 14 días, registrando diferencias hasta los 21 y 28 días.
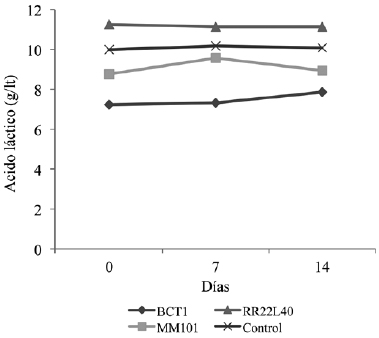
Figura 1
Acidez titulable de las bebidas de yogur durante su vida en anaquel
Todos los tratamientos contenían Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. Bulgaricus; y adicionalmente los tratamientos BCTI, MM101 y RR22L40 (ver Tabla I). Control: sin probiótico adicional.
Concentración peptídica total
La concentración peptídica promedio de las muestras osciló entre 0,005 y 0,006mg⋅l-1 durante su vida en anaquel, como se muestra en la Figura 2. Para este análisis presentaron efecto los tratamientos (p<0,05), la vida en anaquel (p<0,05) y, por lo tanto, la interacción entre ellos (p<0,05), La concentración peptídica, en todos los tratamientos, incluyéndose el control, mostró una tendencia a disminuir con el tiempo; sin embargo, el control y el tratamiento con los cultivos RR22 LYO presentaron siempre la concentración mas alta de péptidos. La concentración más baja la presentó el tratamiento BCT1, observándose esto durante todo el almacenamiento. Además de la importancia de las enzimas proteolíticas/peptidolíticas de las BAL en las propiedades organolépticas del producto final, algunas BAL son conocidas por su contribución a liberar péptidos que promueven la salud mas allá de la nutrición básica (Philanto y Korhonen, 2003). En relación a la concentración peptídica, el control y el tratamiento con los cultivos RA22L4O mostraron los valores mas altos.
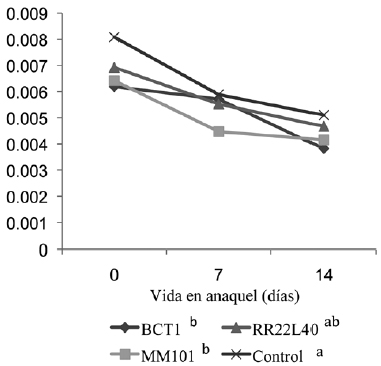
Figura 2
Concentración peptídica total de las bebidas de yogur durante su vida en anaquel
Todos los tratamientos BCTI, MM101 y RR22L40 (ver Tabla I). Control: sin probiótico adicional. ab: Literales diferentes, indican diferencias entre tratamientos (p<0,05).
El sistema proteolítico de las BAL se compone de tres pasos principales, el primero consiste en la proteólisis de las proteínas por proteasas ligada a la pared celular (Prep) para formar una gran cantidad de oligopéptidos (Opp) que, en el segundo paso, son transportados a través de las membranas por el sistema de transporte de Opp; finalmente, una vez dentro de la célula, los péptidos son degradados por diversas peptidasas (PepA, PepE, PepF, PepO, PepX), a pequeños péptidos y aminoácidos libres, y de ahí pasan a desempeñar su función biológica según sea el caso (Bockelmann, 1995). Esta última degradación la llevan a cabo dipeptidasas y tripeptidasas, las cuales varían con respecto a sus propiedades bioquímicas y físicas. Muchas dipeptidasas son también prolinasas o prólidasas, e hidrolizan los péptidos N-C terminal con residuos de prolina. Estas enzimas son necesarias para liberar la mayor cantidad de aminoácidos (Marth y Steele, 2001). El hecho que el control haya presentado la mayor concentración de péptidos pone de manifiesto que el proceso llevado a cabo per se produjo péptidos, lo que pudo deberse al proceso térmico al que se sometió la leche (tratamiento térmico de 95ºC por 30min) y a la acción del cultivo base (Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. bulgaricus).
La proteólisis que ocurre en los yogures resulta de la relación simbiótica entre los dos microorganismos presentes en el cultivo base. L. delbrueckii posee una proteinasa que hidroliza la caseína para liberar polipéptidos, que son posteriormente fraccionados por las peptidasas producidas por S. salivarius (Tamime y Robinson, 2007). Seguido del tratamiento control, el tratamiento con el cultivo RR22L40 fue el que generó mayor concentración de péptidos. Una de las diferencias a resaltar entre las mezclas de cultivos utilizadas es que este tratamiento no contenía lactobacilos como probiótico, contenía dos especies de lactococos y una de estreptococos. Los lactococos poseen una proteinasa extracelular PrtP, que hidroliza la caseína de la leche y produce oligopéptidos suficientes para sostener su crecimiento; sin embargo, se ha reportado que L. Lactis subsp. cremoris no es capaz de degradar di-, triy tetra-péptidos (Tan et al., 1992), lo que pudiera explicar porqué este tratamiento presentó una concentración similar al control. A la fecha, algunas BAL que presentan esta actividad son L. helveticus CP790, L. rhamnosus GG, L. bulgaricus SS1 y L. lactis subsp. cremoris FTA (Gobbetti et al., 2002).
Actividad proteolítica
La actividad proteolítica de las muestras en promedio osciló entre 1,66 a 90,44%, correspondiendo a absorbancias entre 1,01 y 1,65 (Figura 3), presentando efecto los tratamientos (p<0,05) y la vida en anaquel (p<0,05), y por lo tanto la interacción entre ellos (p<0,05). A lo largo de la vida en anaquel, los tratamientos RR22L40 y MM101 fueron los que presentaron mayor actividad proteolítica. Como se muestra en la Tabla II, el primero de ellos con un porcentaje de actividad de entre 17,31 y 53,17 y el segundo entre 1,67 y 76,40 comparados con la actividad proteolítica del control (tomado como 0%, para observar el efecto proteolítico del los probióticos según el tratamiento); no existió diferencia estadística entre ellos. El control presentó la menor actividad proteolítica, siendo ésta estadísticamente diferente a los tres tratamientos. Lo anterior se observó durante toda la vida en anaquel. La adición de probióticos ejerció un incremento (p<0,05) en la actividad proteolítica del yogur.
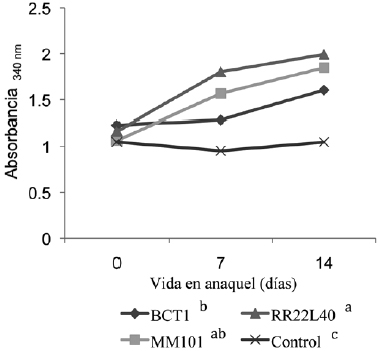
Figura 3
Actividad proteolítica de las bebidas de yogur durante su vida en anaquel
Todos los tratamientos contenían Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. Bulgaricus; y adicionalmente los tratamientos BCTI, MM101 y RR22L40 (ver Tabla I). Control: sin probiótico adicional. ab: Literales diferentes, indican diferencias entre tratamientos (p<0,05).
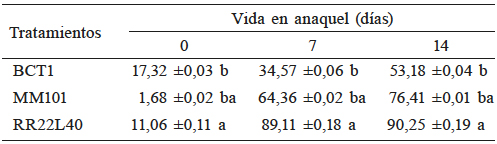
Todos los tratamientos contenían Streptococcus salivarius subsp. thermophilus y Lactobacillus delbrueckii subsp. Bulgaricus; y adicionalmente los tratamientos BCTI, MM101 y RR22L40 (ver Tabla I). Control: sin probiótico adicional. ab: Literales diferentes en una misma columna indican diferencias entre tratamientos (p<0,05).
La producción de yogur es un proceso complejo que involucra muchos cambios físicos y químicos, incluyendo la proteólisis, la cual consiste en la hidrólisis progresiva de las caseínas a polipéptidos, péptidos y aminoácidos libres. La habilidad de las BAL para desarrollarse depende de su sistema proteolítico, que les permite liberar los aminoácidos esenciales para su crecimiento (Christensen et al., 1999). En este estudio los probióticos provocaron un incremento significativo (p<0,05), en la actividad proteolítica de los yogures que los contenían.
Las diferencias en el grado proteolítico de los tratamientos se debe a los diferentes probióticos que contenían, ya que aunque todos sintetizan peptidasas como aminopeptidasas y dipeptidasas, estas difieren entre si en proporciones, puntos de corte, eficiencia, y según las condiciones en las que se encuentren variará su actividad (Shihata y Shah, 2000). Los tratamientos que presentaron mayor actividad proteolítica fueron aquellos que contenían lactococos y estreptococos (RR22L40 y MM101). Los estreptococos metabolizan el exceso de aminoácidos que son liberados, por lo que el grado de proteólisis esta en el balance entre los aminoácidos liberados y utilizados (Rasic y Kurmann, 1978). El tratamiento que presentó mayor grado de proteólisis contenia lactococos y estreptococos; los cocos son capaces de actuar sobre los péptidos liberados de las caseínas por los lactobacilos, y porque mayor cantidad de péptidos y aminoácidos son liberados de los que pueden utilizar (Slocum et al., 1988).
De manera específica, las características más importantes para cada probiótico usado son: Lactococcus lactis sintetiza una proteinasa inicial llamada PrtP, L. acidophilus sintetiza una proteinasa tipo serina (Law y Haandrinkman, 1995), L. paracasei una proteinasa inicial llamada PrtP y S. thermophilus PrtS y peptidasas específicas de prolina (Savijoki et al., 2006) y posee mayor actividad extracelular comparado con los otros (Shihata y Shah, 2000). Las bifidobacterias (como las contenidas en el cultivo BCT-1) tienen una ruta de fermentación de carbohidratos única (Salminen et al., 2004) y su actividad proteolítica es menor al resto (Shihata y Shah, 2000). Debe considerarse también que entre los probióticos empleados se generan diferentes asociaciones simbióticas (Ustok et al., 2007); sin embargo, el grado de actividad proteolítica que se detecte es debida en mayor grado a la simbiósis entre los microorganismos presentes, más que al decremento de la cantidad de proteína que se hidroliza (Salminen et al., 2004).
Conclusiones
Todos los tratamientos elaborados presentaron mayor actividad proteolítica con respecto a la actividad que presentó el control, la cual aumentó del 1,6 al 90,2% al adicionar probióticos a la mezcla básica. Durante el análisis de la vida en anaquel se observaron variaciones significativas en los tratamientos de yogur por efecto de la concentración peptídica y la actividad proteolítica, no observando cambios en la acidez titulable solamente. Se recomienda un estudio posterior para comparar la actividad proteolítica en yogur elaborado con leche de cabra y leche de vaca, así como también una evaluación sensorial para estudiar el grado de aceptación de las bebidas ante los consumidores.
REFERENCIAS
AOAC (1998) Official Method 947.05-1947 Acidity of milk. Titrimetric method. En Food Composition, Additives, Natural Contaminants. Vol II. 16a ed. Official Methods of Analysis of AOAC International. Gaithersburg, MD, EEUU.
Bockelmann W (1995) The proteoly tic system of star ter and non-starter bacteria: components and their importance for cheese ripening. Int. Dairy J. 5: 977-994.
Bradford MM (1976) A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal. Biochem. 72: 248-254.
Castro WF, Cruz AG, Bisinotto MS, Guerreiro LM, Faria JA, Bolini HM, Cunha RL, Deliza R (2013) Development of probiotic dairy beverages: Rheological properties and application of mathematical models in sensory evaluation. J. Dairy Sci. 96: 16-25.
Christensen JE, Dudley EG, Pederson JA, Steele JL (1999) Peptidases and amino acid catabolism in lactic acid bacteria. Ant. van Leeuwenhoek 76: 217-246.
Church FC, Swaisgood HE, Porter DH, Catignani GL (1983) Spectrophotometric assay using ophthaldialdehy de for determination of proteolysis in milk and isolated milk proteins J. Dairy Sci. 66: 1219-1227.
da Costa EL, da Rocha JA, Netto FM (2007) Effect of heat and enzymatic treatment on the antihypertensive activity of whey protein hydrolysates. Int. Dairy J. 17: 632-640.
Domagala J (2009) Instrumental texture, syneresis and microstructure of yoghurts prepared from goat, cow and sheep milk. Int. J. Food Propert. 12: 605-615.
Donkor ON, Nilmini SLI, Stolic P, Vasiljevic T, Shah NP (2007) Survival and activity of selected probiotic organisms in set-type yogurt during cold storage. Int. Dairy J. 17: 657-665.
Duggan C, Gannon J, Walker WA (2002) Protective nutrients and functional foods for the gastrointestinal tract. Am. J. Clin. Nutr. 75: 789-808.
Dziuba M, Darewicz M (2007) Food proteins as precursors of bioactive peptides-classification into families. Food Sci. Technol. Int. 13:393-404.
Ebringer L, Ferencik M, Krajcovi J (2008) Beneficial health effects of milk and fermented dairy products Review. Folia Microbiol. 53: 378-394.
Gobbetti M, Stepaniak L, De Angelis M, Corsetti A, Di Cagno R (2002) Latent bioactive peptides in milk proteins: proteolytic activation and significance in dairy processing. CRC Crit. Rev. Food Sci. Nutr 42: 223-239.
Law J, Haandrikman A (1995) Proteolytic enzymes of lactic acid bacteria. Int. Dairy J. 7: 1-11.
Marth EH, Steele JL (2001) Applied Dairy Microbiology. 2a ed. Dekker. Nueva York, EEUU. 227 pp.
Minervini F, Bilancia MT, Siragusa S, Gobbetti M, Caponio F (2009) Fermented goats’ milk produced with selected multiple starters as a potentially functional food. Food Microbiol. 26: 559-564.
Park YW (2009) Bioactive components in goat milk. Cap. 3 en Park YW Bioactive Components in Milk and Dairy Products. Wiley. Athens, GA, EEUU.
Philanto A, Korhonen H (2003) Bioactive peptides and proteins. Adv. Food Nutr. Res. 47: 175-276.
Rasic JL, Kurmann JA (1978) Yogurt: Scientific Grounds, Technology, Manufacture, and Preparations. Technical Dairy. Copenhage, Dinamarca. 466 pp.
Salminen S, Wrigth AV, Ouwehand AC, Lahtinen S (2004) Lactic acid bacteria: Microbiological and functional aspects. 4a ed. CRC. Boca Ratón, FL, EEUU. pp. 155-156.
Savijoki K, Ingmer H, Varmanen P (2006) Proteolytic systems of lactic acid bacteria. Appl. Microbiol. Biotechnol. 71: 394-406.
Serra M, Trujillo AJ, Guamis B, Ferragut V (2009) Proteolysis of yogurts made from ultra-highpressure homogenized milk during cold storage. J. Dairy Sci. 92: 71-78.
Shihata A, Shah NP (2000) Proteolytic profiles of yogurt and probiotic bacteria. Int. Dairy J. 10: 401-408.
Silveira EO, Lopes-Neto JH, Silva LA, Raposo AES, Magnani M, Cardille HR (2015) The effects of inulin combined with oligofructose and goat cheese whey on the physicochemical properties and sensory acceptance of a probiotic chocolate goat dairy beverage. LWT-Food Sci. Technol. 62. 71: 445-451.
Slocum SA, Jasinski EM, Kilara A (1998) Processing variables affecting proteolysis in yogurt during incubation. Dairy Sci. 71: 596-603.
Smit G, Smit BA, Engels WJ (2005) Flavour formation by lactic acid bacteria and biochemical flavour profiling of cheese products. FEMS Microbiol. Rev. 29: 591-610.
Tamime AY, Robinson RK (2007) Yogurt Science and Technology. 3a ed. Pergamon. Nueva York, EEUU. p. 561-563.
Tan PST, Chapot-Chartier MP, Pos KM, Rousseau M, Boquien CY, Gripon JC, Konings WN (1992) Location of peptidases in lactococci. Appl. Environ. Microbiol. 58: 285-290.
Tranjan BC, Cruz AG, Walter EHM, Faria JAF, Bolini HMA, Moura MRL, Carvalho LMJ (2009) Development of goat cheese whey-flavoured beverages. Int. J. Dairy Technol. 62: 438-443.
Ustok FI, Tari C, Harsa S (2007) Effect of symbiotic relationship of Lactobacillus bulgaricus 77 and Streptococcus thermophilus 95/2 on betagalactosidase and lactic acid production. J. Biotechnol. 131 (Suppl2): S211-S241.
Zourari A, Accolas JP, Desmazeaud MJ (1992) Metabolism and biochemical characteristics of yogurt bacteria. Lait 72: 1-34.
Notas de autor
Autora de correspondencia: América Chávez-Martínez. Dirección: Departamento de Tecnología de Productos de Origen Animal, Facultad de Zootecnia y Ecología, UACH. Periférico Francisco R. Almada km 1 Chihuahua, Chih., México. e-mil: amchavez@uach.mx
Enlace alternativo
https://www.interciencia.net/wp-content/uploads/2018/01/50-CHAVEZ-43_1.pdf (pdf)