COMUNICACIONES
COINÓCULOS BACTERIANOS SOLUBILIZADORES DE FOSFATO Y SU EFECTO EN LA GERMINACIÓN Y DESARROLLO DEL FRIJOL
PHOSPHATE-SOLUBILIZING BACTERIAL CO-INOCULA AND THEIR EFFECT ON GERMINATION AND PLANT GROWTH OF COMMON BEAN
COINÓCULOS BACTERIANOS SOLUBILIZADORES DE FOSFATO E SEU EFEITO NA GERMINAÇÃO E DESENVOLVIMENTO DO FEIJÃO
COINÓCULOS BACTERIANOS SOLUBILIZADORES DE FOSFATO Y SU EFECTO EN LA GERMINACIÓN Y DESARROLLO DEL FRIJOL
Interciencia, vol. 43, núm. 2, pp. 137-143, 2018
Asociación Interciencia
Recepción: 31/05/2017
Corregido: 05/02/2018
Aprobación: 06 Febrero 2018
Financiamiento
Fuente: Instituto Politécnico Nacional
Nº de contrato: SIP 20150735
Financiamiento
Fuente: Instituto Politécnico Nacional
Nº de contrato: SIP 20160846
Descripción del financiamiento: Los autores agradecen al Instituto Politécnico Nacional por el apoyo financiero para realizar este proyecto de investigación mediante los proyectos SIP 20150735 y 20160846
Resumen: Se evaluó el efecto de tres coinóculos bacterianos solubilizadores de fosfato (BSF) en la germinación in vitro, en el crecimiento y desarrollo de plantas de frijol (Phaseolus vulgaris L.) y en la biodisponibilidad de fósforo en el suelo bajo condiciones semicontroladas. Para determinar el efecto en la germinación in vitro se emplearon tres coinóculos BSF (BSF1: Enterobacter sp. + Burkholderia gladioli, BSF2: Enterobacter sp. + Pseudomonas luteola, y BSF3: P. luteola + Aeromonas hydrophila, y dos controles: solución salina estéril (SSE) y agua destilada estéril, combinados con tres tiempos de imbibición de las semillas: 30, 60 y 120min. Para evaluar el efecto de los coinóculos BSF en el crecimiento y desarrollo de plantas de frijol, así como en la biodisponibilidad de fósforo en el suelo se sembraron cuatro semillas en macetas con suelo sin esterilizar en el que se aplicaron cuatro tratamientos (BSF1, BSF2, BSF3 y control sin inocular). Con respecto al control (SSE) las semillas imbibidas en el BSF3 durante 120min presentaron la mayor longitud de radícula e índice de vigor. El peso de 100 semillas de las plantas bajo condiciones semicontroladas incrementó 3,5 y 4,6% con BSF2 y BSF3, respectivamente, respecto al control. El menor valor de pH del suelo y el mayor contenido de P disponible se encontró con el BSF2. BSF2 y BSF3 parecen favorecer la germinación y algunos parámetros biométricos del frijol; sin embargo, se sugiere la evaluación por más de un ciclo de cultivo para confirmar los efectos positivos de estos coinóculos.
Palabras clave: Bioinoculantes , Fósforo disponible , Germinación , Phaseolus vulgaris L..
Abstract: The effect of three phosphate-solubilizing bacterial co-inocula (PSB) on in vitro germination, growth and development of common bean plants (Phaseolus vulgaris L.) and on soil phosphorus bioavailability under semi-controlled conditions was evaluated. In order to determine the effect on in vitro germination, we used three PSB (PSB1: Enterobacter sp. + Burkholderia gladioli; PSB2: Enterobacter sp. + Pseudomonas luteola and PSB3: P. luteola + Aeromonas hydrophila) and two controls, sterile saline solution (SSE) and sterile distilled water, combined with three times of seeds imbibition: 30, 60 and 120min. To evaluate the effect of each PSB co-inoculum on the plant growth and development of common bean plants, as well as on the soil phosphorus bioavailability, four seeds were planted in pots with non-sterile soil in which four treatments were applied (PSB1, PSB2, PSB3 and control without inoculation). With respect to the control (SSE), the seeds dipped in the PSB3 during 120 min presented the greatest length of radicle and vigor index. The weight of 100 seeds of the plants under semi-controlled conditions increased 3.5 and 4.6% with PSB2 and PSB3, respectively, as compared to the control. The lowest soil pH value and the highest available-P content were found with the PSB2. PSB2 and PSB3 seem to favor germination and some biometric parameters of common beans; however, evaluation for more than one crop cycle is suggested to confirm the positive effects of these PSB co-inocula.
Keywords: Bio-inoculants, Phosphorus available, Germination, Phaseolus vulgaris L..
Resumo: Foi avaliado o efeito de três coinóculos bacterianos solubilizadores de fosfato (BSF) na germinação in vitro, no crescimento e desenvolvimento de plantas de feijão (Phaseolus vulgaris L.) e na biodisponibilidade de fósforo no solo sob condições semicontroladas. Para determinar o efeito na germinação in vitro foram utilizados três coinóculos BSF (BSF1: Enterobacter sp. + Burkholderia gladioli, BSF2: Enterobacter sp. + Pseudomonas luteola, e BSF3: P. luteola + Aeromonas hydrophila) e dois controles: solução salina estéril (SSE) e água destilada estéril, combinados com três tempos de embebição das sementes: 30, 60 e 120min. Para avaliar o efeito dos coinóculos BSF no crescimento e desenvolvimento de plantas de feijão, assim como na biodisponibilidade de fósforo no solo, foram planatas quatro sementes em vasos com solo sem esterilizar no qual se aplicaram quatro tratamientos (BSF1, BSF2, BSF3 e controle sem inocular). Em relação ao controle (SSE) as sementes embebidas no BSF3 durante 120min apresentaram o maior comprimento de radícula e índice de vigor. O peso de 100 sementes das plantas, sob condições semicontroladas, incrementou 3,5 e 4,6% com BSF2 e BSF3 respectivamente em relação ao controle. O menor valor de pH do solo e o maior conteúdo de P disponível foi encontrado com BSF2. BSF2 e BSF3 parecem favorecer a germinação e alguns parâmetros biométricos do feijão; no entanto, se sugere a avaliação por mais de um ciclo de cultivo para confirmar os efeitos positivos de estes coinóculos.
Palavras-chave: Bioinoculantes, Fósforo disponível, Germinação, Phaseolus vulgaris L..
Introducción
Dentro de la diversidad de microorganismos edáficos, las bacterias forman parte del grupo más abundante, con una población que oscila alrededor de 5,5×105 UFC/g de suelo, variable de acuerdo con el tipo, el manejo y el contenido de materia orgánica del suelo (Utria et al., 2008). De la población bacteriana total el 0,5% posee la capacidad de solubilizar fosfatos (Kucey, 1983), de las cuales diferentes especies de los géneros Bacillus, Rhizobium y Pseudomonas se han utilizado como inoculantes en diferentes cultivos con resultados favorables. Estos microorganismos pueden secretar al mismo tiempo diferentes reguladores de crecimiento y mostrar un efecto sinérgico al ser aplicados en conjunto con otros microorganismos (Afzal et al., 2009; Collavino et al., 2010; Qureshi et al., 2011). Lara y Negrete (2015) indicaron que las bacterias en consorcios presentan mayor solubilización de fosfato que aquéllas que se encuentran de manera individual, debido a que los consorcios microbianos en muchos casos interactúan de manera sinérgica estimulando algunas actividades físicas o bioquímicas de las bacterias involucradas en las mezclas. Nelly Fernández-Téllez (Comunicación personal, 2016) encontró una mayor cantidad de fósforo (P) disponible en el sustrato con la aplicación de coinóculos bacterianos solubilizadores de fosfato que cuando se aplicaron los mismos géneros y especies bacterianas de manera individual (Bautista-Cruz et al., 2015). Bautista-Cruz et al. (2015) encontraron un aumento de 12,1% en la biomasa aérea seca y de 17,8% en la biomasa radicular seca con respecto al control en plantas de Agave angustifolia Haw. inoculadas con cepas bacterianas individuales solubilizadoras de fosfato. Nelly Fernández-Téllez (Comunicación personal, 2016) también encontró que la biomasa aérea seca fue 14 veces mayor y la biomasa radicular seca fue seis veces mayor en plantas de A. angustifolia cuando se emplearon combinaciones binarias de los mismos géneros y especies bacterianas solubilizadoras de fosfato empleadas por Bautista Cruz et al. (2015) de manera individual.
El fósforo es un macronutriente esencial para las células vegetales, forma parte de su estructura y participa en muchos procesos de crecimiento y desarrollo. Es un elemento relativamente abundante en la corteza terrestre (Cadahia, 2000); sin embargo, solo una pequeña parte se encuentra en la solución del suelo (Cordero et al., 2008) y es frecuente encontrar algún grado de deficiencia de este nutrimento en las plantas (Bernal et al., 2007).
Para la producción de fertilizantes minerales fosfatados es necesaria la utilización de recursos no renovables, principalmente roca fosfórica (Mar y Okasaki, 2012), lo cual eleva su costo (Sequera y Ramírez, 2013). Al mismo tiempo, durante su fabricación se emiten gases con altos contenidos de ácido clorhídrico y fluorhídrico, además de metales pesados como cadmio (Glasser, 2002). Aunado a lo anterior, el uso inadecuado de fertilizantes es una de las principales causas de la salinización del suelo, emisión de gases con efecto invernadero, eutrofización del agua (Savci, 2012) y la acumulación de metales pesados como Cd (Mar y Okasaki, 2012), As, Ni, Pb, Tl y U (Kratz et al., 2016) en los suelos agrícolas.
El frijol (Phaseolus vulgaris L.) es uno de los cultivos más importantes en México y el mundo, al ser la principal leguminosa utilizada como alimento en Latinoamérica, Asia y África (Collavino et al., 2010; Lépiz y Ramírez, 2010). En términos nutricionales, el frijol es una importante fuente de proteínas, minerales y vitaminas (Lépiz y Ramírez, 2010). Este cultivo presenta alta dependencia de la disponibilidad de P soluble en el suelo y es muy sensible a la deficiencia de P, lo que puede ser la principal limitante en su desarrollo y producción (Hernández et al., 1996). Por esta razón, el uso de microorganismos capaces de mejorar los procesos esenciales en la nutrición de este cultivo representa un componente vital en un sistema agrícola sustentable, donde se puedan reducir costos de producción sin demeritar la calidad y rendimiento de los cultivos, propiciando el desarrollo del sector agrícola, tanto en la agricultura de supervivencia como en la comercial (Kaur y Reddy, 2014).
Diferentes estudios se han enfocado en la búsqueda de microorganismos, tanto bacterias como hongos, con capacidad de volver disponibles las reservas de P en el suelo (Kucey, 1983; Fernández et al., 2005); sin embargo, las bacterias han despertado mayor interés como solubilizadoras de fosfato en el cultivo de frijol, en paricular los géneros Burkholderia (Peix et al., 2001; Collavino et al., 2010), Pseudomonas (Valverde et al., 2007; Collavino et al., 2010), Rhizobium (Abril et al., 2007), Sinorhizobium (Ormeño et al., 2007), Enterobacter, Pantoea, Acinetobacter y Exiguobacterium (Collavino et al., 2010). El objetivo de este trabajo fue evaluar el potencial de coinóculos bacterianos solubilizadores de fosfato (BSF) en la germinación in vitro; en el crecimiento y desarrollo de plantas de frijol; y en la biodisponibilidad de P en el suelo bajo condiciones semi-controladas.
Materiales y Métodos
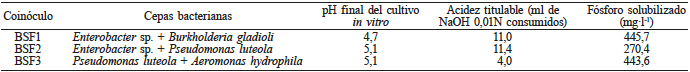
Los coinóculos BSF usados en este estudio se seleccionaron: i) por su eficiente capacidad solubilizadora de fosfato tricálcico in vitro, la cual se determinó cuantitativamente mediante la cantidad de P solubilizado, la producción de ácidos orgánicos y el cambio en el pH del filtrado del cultivo bacteriano (Tabla I) y, ii) por su efecto positivo en el desarrollo y crecimiento de Agave angustifolia Haw. bajo condiciones semi-controladas (Nelly Fernández-Téllez, comunicación personal, 2016). Las cepas bacterianas empleadas en la preparación de estos coinóculos se aislaron de suelos semiáridos cultivados con A. angustifolia en el distrito de Tlacolula, Oaxaca, México (Bautista-Cruz et al., 2015).
Para la obtención del pre-coinóculo se tomó 1ml de cultivo bacteriano de cada cepa solubilizadora de fosfato no antagónica y se inoculó conjuntamente en caldo nutritivo. De cada pre-coinóculo se tomaron 5ml y se inocularon en caldo nutritivo para posteriormente incubarse a 30ºC y 150 opm durante 48h en una incubadora-agitadora. Transcurrido el tiempo de incubación el pre-coinóculo se centrifugó a 10000 rpm durante 10min. El pellet celular obtenido se diluyó con solución salina estéril (SSE) a una concentración de ~15×108 UFC/ml de acuerdo con la escala de McFarland (Perilla et al., 2004). Los tres coinóculos utilizados se describen en la Tabla I.
Se utilizó la variedad mejorada de frijol ‘Negro INIFAP’, la cual fue proporcionada por el Banco de Germoplasma de Especies Nativas de Oaxaca (BAGENO) del Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias (INIFAP), Campo Experimental Valles Centrales, Oaxaca, México. Previo al trabajo experimental se eliminaron las semillas rotas o con daños por insectos o patógenos; las restantes se desinfectaron con una solución de hipoclorito de sodio al 1,5% durante 10min, para después lavarse repetidamente con agua destilada estéril.
Efecto de los coinóculos BSF en la germinación in vitro de semillas de frijol
Las semillas de frijol se embebieron en los tres coinóculos BSF (BSF1, BSF2 y BSF3), en solución salina estéril (SSE) 0,1454M y en agua destilada estéril (ADE) durante 30, 60 y 120min, utilizándose las dos últimas como controles. Posteriormente se colocaron dentro de una caja Petri estéril con algodón y papel filtro humedecidos con 5ml de ADE. Las cajas se sellaron con parafilm y se mantuvieron en cámara de germinación a 25ºC ±5º (Ellis et al., 1985). El hipocótilo y la radícula fueron medidos después de siete días.
El diseño experimental utilizado fue completamente al azar con submuestreo y arreglo bifactorial, donde los factores fueron: a) los tres coinóculos BSF y dos controles (ADE y SSE) y, b) el tiempo de imbibición (30, 60 y 120min), con un total de 15 tratamientos y seis repeticiones (Tabla II). La unidad experimental constó de cinco semillas.
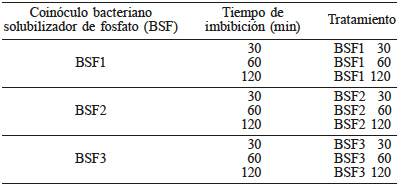
BSF1: Enterobacter sp. + Burkholderia gladioli, BSF2: Enterobacter sp. + Pseudomonas luteola, BSF3: Pseudomonas luteola + Aeromonas hydrophila.
Se consideró germinada la semilla cuando la radícula emergió de la testa. Con la cantidad de semillas germinadas se calculó el porcentaje de germinación (PG) mediante la ecuación

Con la longitud promedio de radícula e hipocótilo se calculó el índice de vigor (IV) mediante la ecuación (Van Staden et al., 2006)
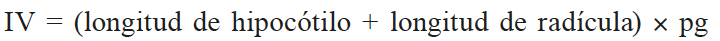
Los resultados obtenidos se analizaron estadísticamente mediante análisis de varianza, prueba de comparación de medias (Tukey 0,05), correlación de Pearson y análisis de componentes principales utilizando el software SAS 9.2®. Previo al análisis de varianza se determinó la homogeneidad de varianza y la normalidad de los datos a través de las pruebas de Hartley y Shapiro-Wilk, respectivamente.
Efecto de los coinóculos BSF en el crecimiento y desarrollo de plantas de frijol
Este experimento se realizó bajo condiciones semicontroladas dentro de un macrotúnel. Como macetas se utilizaron vasos de poliestireno expandido con capacidad de 1 litro, los cuáles se llenaron con suelo sin esterilizar, previamente tamizado con una malla de 2mm de abertura. Entre las propiedades químicas y físicas de este suelo estuvieron: pH 7,6; materia orgánica 2,3%; N total 0,61%; P disponible 2,6mg·kg-1; densidad aparente 1,2g·cm-3; arena 48,6%; limo 25,1%; y arcilla 26,2%.
Se sembraron cuatro semillas de frijol por maceta a una profundidad de 2cm y se regaron hasta el punto de saturación utilizando agua corriente. Cuando las plántulas alcanzaron la etapa V3 (despliegue de la primera hoja trifoliada; Fernández et al., 1986) se realizó el raleo a una plántula por maceta y se agregaron 5ml de cada coinóculo. Después de la inoculación se aplicaron semanalmente 25ml de solución nutritiva Hoagland con P disminuido a la décima parte, hasta la madurez fisiológica de las plantas. Se realizaron riegos periódicos de acuerdo con las necesidades del cultivo.
Las variables medidas fueron floración media, madurez fisiológica, vainas por planta, P foliar por el método vanadato-molibdato amarillo (Cottenie, 1984), semillas producidas, rendimiento, peso de 100 semillas, y contenido de proteína en el grano utilizando el método microKjeldahl. Así mismo, se determinaron, al inicio y al final del experimento, el pH y el P disponible en el suelo (Olsen).
Se utilizó un diseño experimental en bloques completos al azar con cuatro tratamientos (BSF1, BSF2, BSF3 y un control sin inocular) y cinco repeticiones. Las unidades experimentales constaron de cinco macetas. Los resultados obtenidos se analizaron estadísticamente mediante análisis de varianza, prueba de comparación de medias (Tukey 0,05), correlación de Pearson y análisis de componentes principales utilizando el software SAS 9.2®. Previo al análisis de varianza se determinó la homogeneidad de varianza y la normalidad de los datos a través de las pruebas de Hartley y Shapiro-Wilk, respectivamente.
Resultados y Discusión
Efecto de los coinóculos BSF en la germinación in vitro
La longitud de radícula e índice de vigor de las semillas de frijol fueron significativamente diferentes entre los tratamientos evaluados. La longitud de radícula de las semillas tratadas con los coinóculos BSF fue mayor que las del control con SSE (Tabla III). Las semillas imbibidas en el BSF2 y en el BSF3 desarrollaron plántulas con mayor vigor que las del control con SSE. Similarmente, Demissie et al. (2013) reportaron un aumento en el índice de vigor y en la longitud de la radícula durante la germinación de semillas de Vicia faba L. coinoculadas con BSF en comparación con el control. Aipova et al. (2010) también encontraron que la coinoculación con BSF aumentó la longitud de la radícula en semillas de trigo. El efecto positivo en la germinación de las semillas se podría deber a que las bacterias solubilizadoras de fosfato producen hormonas, como las giberelinas, que favorecen la germinación al promover la actividad de enzimas específicas promotoras de la misma, como la α-amilasa, que incrementa la asimilación de almidón (Gholami et al., 2009). Egamberdiyeva (2007) y Sharma et al. (2007) atribuyeron el efecto positivo en la germinación de las semillas a la producción de auxinas por las BSF.
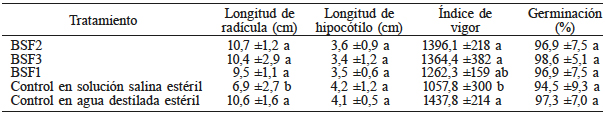
Valor medio ±desviación estándar de cada variable. Letras diferentes en cada columna indican diferencias estadísticas (Tukey 0,05). BSF1: Enterobacter sp. + Burkholderia gladioli, BSF2: Enterobacter sp. + Pseudomonas luteola, BSF3: Pseudomonas luteola + Aeromonas hydrophila).
Las semillas de frijol imbibidas durante 60min mostraron un índice de vigor más alto en comparación con las imbibidas por 30min (Tabla IV), lo que se reflejó en plántulas de mayor tamaño. Es posible que las semillas imbibidas durante un mayor tiempo tengan un mayor periodo para iniciar su metabolismo pre-germinativo y, con ello aumentar su vigor en comparación con aquellas con un menor tiempo de imbibición (Rajjou et al., 2012).
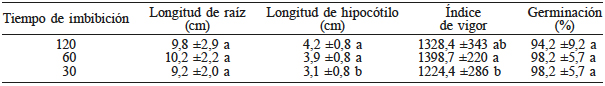
Valor medio ±desviación estándar de cada variable. Letras diferentes en cada columna indican diferencias estadísticas (Tukey 0,05).
Efecto de la interacción coinóculo × tiempo de imbibición
La interacción coinóculo× tiempo de imbibición reveló que las semillas imbibidas durante más tiempo en los coinóculos y ADE desarrollaron plántulas más vigorosas, mientras que en el control (SSE) se observó el efecto opuesto. El tratamiento BSF3 con imbibición durante 120min presentó la mayor longitud de radícula e índice de vigor con respecto al control (SSE) con 60 y 120min de imbibición (Tabla V). Se registró una correlación directa altamente significativa (r= 0,92, p<0,01) entre el índice de vigor y el tamaño de la raíz e hipocótilo de las plántulas, lo que podría indicar que, con las condiciones de este experimento, la longitud de radícula tuvo mayor peso en el vigor de las plántulas.
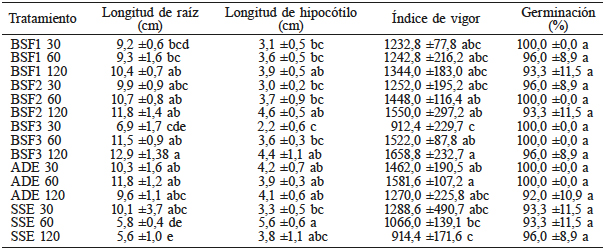
Valor medio ±desviación estándar de cada variable. Letras diferentes en cada columna indican diferencias estadísticas (Tukey 0,05). BSF1 (Enterobacter sp. + Burkholderia gladioli); BSF2 (Enterobacter sp. + Pseudomonas luteola); BSF3 (Pseudomonas luteola + Aeromonas hydrophila); ADE, agua destilada estéril; SSE, solución salina estéril.
Los dos primeros componentes principales explicaron 87,3% de la variación total (Tabla VI). En el primer componente principal las variables más significativas fueron la longitud de la radícula y el índice de vigor, lo que indica que los tratamientos ubicados en el extremo positivo del eje X presentaron plántulas con radículas más largas y de mayor vigor (Figura 1). En el segundo componente principal las variables más sobresalientes fueron el porcentaje de germinación y la longitud de hipocótilo; sin embargo, el vector propio de la longitud de hipocótilo fue negativo, lo cual sugiere que los tratamientos ubicados en extremo positivo del eje Y presentaron mayores porcentajes de germinación, pero hipocótilos cortos.
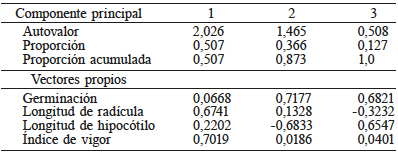
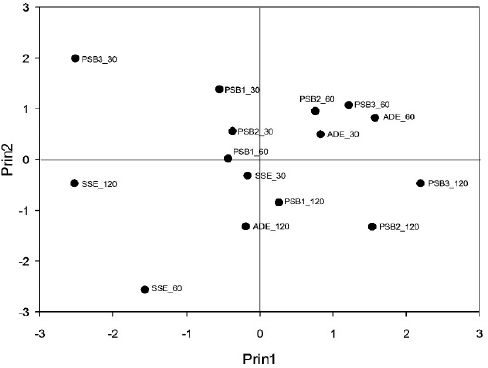
Figura 1
Distribución gráfica de los tratamientos en el estudio de interacción coinóculo × tiempo de imbibición, de acuerdo con los primeros dos componentes principales
PSB1: Enterobacter sp. + Burkholderia gladioli, PSB2: Enterobacter sp. + Pseudomonas luteola, PSB3: Pseudomonas luteola + Aeromonas hydrophila, ADE: agua destilada estéril, SSE: solución salina estéril.
Efecto de los coinóculos BSF en el crecimiento y desarrollo de plantas bajo condiciones semicontroladas
El peso de 100 semillas, el pH del suelo y la cantidad de P disponible fueron significativamente diferentes entre los tratamientos evaluados (Tabla VII). El resto de las variables evaluadas no respondieron significativamente a los tratamientos. La ausencia de efectos significativos de los tratamientos en estas variables podría ser debido a que la habilidad bacteriana de colonizar las raíces de frijol varía de acuerdo con la cepa utilizada (Collavino et al., 2010). También pudo haber influido el que las cepas BSF no son nativas de la rizósfera de plantas de frijol, sino que se aislaron de la rizósfera de A. angustifolia cultivado en suelos con propiedades similares a aquellos donde se cultiva frijol en el estado de Oaxaca, lo cual podría afectar su habilidad para colonizar eficientemente la rizósfera del frijol. Otros autores, como Kaur y Reddy (2014), han encontrado efectos significativos de diferentes inóculos BSF comparados con el suelo sin inocular, hasta el tercer ciclo de cultivo en un sistema orgánico de rotación maíz-trigo, en el mismo suelo.
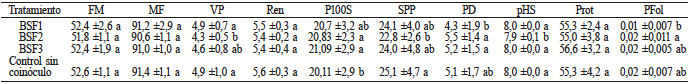
BSF1: Enterobacter sp. + Burkholderia gladioli, BSF2: Enterobacter sp. + Pseudomonas luteola, BSF3: Pseudomonas luteola + Aeromonas hydrophila, FM: floración media (días), MF: madurez fisiológica (días), VP: vainas por planta, Ren: semilla producida (g/planta), P100S: peso de 100 semillas (g), SPP: semillas/planta, PD: fósforo disponible al final del ciclo de cultivo (mg/kg de suelo), pHS: pH del suelo al final del ciclo de cultivo, Prot: contenido de proteína en grano (% peso seco), Pfol: fósforo foliar (mg·kg-1).
Con respecto al control, el peso de 100 semillas fue mayor con BSF2 y BSF3. Se observó un incremento de 4,6% en el peso de las semillas con el BSF3 y de 3,5% con el BSF2 (Tabla VII). Kumar et al. (2016) evaluaron el efecto de una cepa fijadora de nitrógeno (Rhizobium leguminosarum) y dos cepas BSF (Bacillus sp. y Pseudomonas sp.) en plantas de frijol (P. vulgaris) y encontraron que las plantas inoculadas con las cepas BSF presentaron, en promedio, un peso de 100 semillas 35,0% mayor que las plantas sin inocular.
El menor valor de pH del suelo así como el contenido más alto de P disponible se encontró con el BSF2 (Tabla VII). Se registró una correlación directa significativa entre las variables vainas por planta y semillas por planta (r= 0,62, p<0,01); ambas variables también presentaron una correlación inversa significativa con el peso de 100 semillas (r= -0,61, p<0,01) y (r= -0,89, p<0,01), respectivamente. El contenido de proteínas se correlacionó de forma directa con el peso de 100 semillas (r= 0,72, p<0,01), mientras que con la cantidad de vainas y semillas por planta mostró una correlación inversa (r= -0.47, p<0,05) y (r= -0.7, p<0,05), respectivamente. El rendimiento se correlacionó directamente con la cantidad de P disponible en el suelo (r= 0,62, p<0,01). El contenido de P foliar se correlacionó directamente con el peso de 100 semillas (r=0,53, p<0,05). Similarmente, Zafar et al. (2011) encontraron una correlación significativa entre la cantidad de P asimilado y la cantidad de semillas producidas por planta inoculadas con una cepa fijadora de nitrógeno (Bradyrhizobium sp.) y una cepa solubilizadora de fosfato (Agrobacterium sp.).
Los dos primeros componentes principales explicaron 90.2% de la variación total (Tabla VIII). En el primer componente las variables días a madurez fisiológica, vainas por planta, semillas por planta, días a floración, pH del suelo y rendimiento fueron las más significativas, por lo que los tratamientos ubicados en el extremo positivo del eje X mostraron plantas más tardías, con mayor número de vainas por planta y granos por planta, además de que el suelo presentó pH más alcalino. Por el contrario, en el segundo componente principal el contenido de proteína fue la variable que presentó mayor influencia, lo que indica que los tratamientos ubicados en el extremo positivo del eje Y presentaron semillas de mejor calidad (Figura 2).
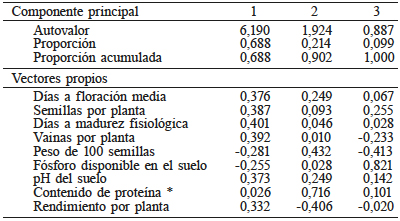
* de las semillas.
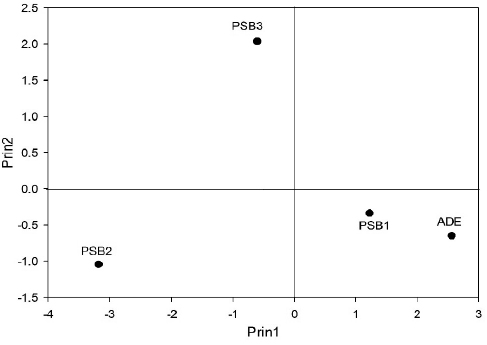
Figura 2
Distribución gráfica de los tratamientos en el crecimiento y desarrollo de plantas de frijol bajo condiciones semi-controladas, de acuerdo con los primeros dos componentes principales
PSB1: Enterobacter sp. + Burkholderia gladioli, PSB2: Enterobacter sp. + Pseudomonas luteola, PSB3: Pseudomonas luteola + Aeromonas hydrophila, ADE: agua destilada estéril.
Conclusiones
Las semillas imbibidas en el BSF3 (Pseudomonas luteola + Aeromonas hydrophila) durante 120min presentaron la mayor longitud de radícula e índice de vigor. El peso de 100 semillas de las plantas de frijol bajo condiciones semi-controladas incrementó con BSF2 (Enterobacter sp. + Pseudomonas luteola) y BSF3. BSF2 disminuyó el pH del suelo y favoreció el incremento de P disponible para la planta. Se sugiere la evaluación por más de un ciclo del cultivo de frijol para confirmar los efectos positivos de estos coinóculos.
Agradecimientos
Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (CONACYT) por la beca otorgada para la realización del posgrado, al Instituto Politécnico Nacional por el apoyo financiero para realizar este proyecto de investigación mediante los proyectos SIP 20150735 y 20160846, y a los ingenieros Alfonso Flores Aguilar y Luis Flores Martínez por facilitar algunos de los materiales utilizados.
Referencias
Abril A, Zurdo-Piñeiro JL, Peix A, Rivas R, Velázquez E (2007) Solubilization of phosphate by a strain of Rhizobium leguminosarum bv. trifolii isolated from Phaseolus vulgaris in El Chaco Arido soil (Argentina). En Velázquez E, Rodríguez-Barrueco C (Eds.) First International Meeting on Microbial Phosphate Solubilization. Salamanca, Spain. Springer. pp. 16-19, 135-138.
Afzal A, Bano A, Fatima M (2009) Higher soybean yield by inoculation with N-fixing and P-solubilizing bacteria. Agron. Sustain. Dev. 30: 487-495.
Aipova R, Aitkeldiyeva SA, Kurmanbayev AA, Sadanov AK, Topalova OB (2010) Assessment of biotechnological potential of phosphate solubilizing bacteria isolated from soils of Southern Kazakhstan. Nat. Sci. 2: 841-845.
Bautista-Cruz A, Martínez-Gallegos V, Martínez-Martínez L, Martínez G (2015) Effect of phosphate solubilizing bacteria on the growth of Agave angustifolia Haw. (maguey espadín). Pak. J. Bot. 47: 1033-1038.
Bernal L, Coello P, Acosta J, Martínez-Barajas E (2007) Efecto de la deficiencia de fósforo en el metabolismo de carbono en plántulas de frijol (Phaseolus vulgaris). Agro. 41: 417-423.
Cadahia LC (2000) Fertirrigación. Cultivos Hortícolas y Ornamentales. 2ª ed. Mundi-Prensa. Madrid, España. 25-62 pp.
Collavino MM, Sansberro PA, Mroginski LA, Aguilar OM (2010) Comparison of in vitro solubilization activity of diverse phosphate-solubilizing bacteria native to acid soil and their ability to promote Phaseolus vulgaris growth. Biol. Fertil. Soils 46: 727-738.
Cordero E, Ortega-Rodés JP, Ortega E (2008) La inoculación de plantas con Pantoea sp., bacteria solubilizadora de fostatos, incrementa la concentración de P en los tejidos foliares. Rev. Col. Biotecnol. 10: 111-121.
Cottenie A (1984) Soil and Plant Testing and Analysis. FAO Soils Bulletin 38/1. Roma, Italia. 96-97 pp.
Demissie S, Muleta D, Berecha G (2013) Effect of phosphate solubilizing bacteria on seed germination and seedling growth of faba bean (Vicia faba L.). Int. J. Agric. Res. 8(3): 123-136.
Egamberdiyeva D (2007) The effect of plant growth promoting bacteria on growth and nutrient uptake of maize in two different soils. Appl. Soil Ecol. 36: 184-186.
Ellis RH, Hong TD, Roberts EH (1985) Handbook of Seed Technology for Genebanks. Vol. 2. Compendium of Specific Germination Information and Test Recommendations. International Board for Plant Genetic Resources. Rome, Italia. 421 pp.
Fernández de C, Gepts FP, López M (1986) Etapas de Desarrollo de la Planta de Frijol Común (Phaseolus vulgaris L.). CIAT. Colombia. 33 pp.
Fernández LA, Zalba P, Gómez MA, Sagardoy MA (2005) Bacterias solubilizadoras de fosfato inorgánico aisladas de suelos de la región Sojera. Cienc. Suelo 23: 31-37.
Gholami A, Shahsavani S, Nezarat S (2009) The effect of plant growth promoting rhizobacteria (PGPR) on germination, seedling growth and yield of maize. World Acad. Sci. Eng. Technol. 49: 19-24.
Glasser G (2002) Air pollution from phosphate fertilizer production. Synth./Regen. 29: 38-40.
Hernández G, Toscano V, Méndez N, Gómez L, Mullings M (1996) Efecto de la concentración de fósforo sobre la asimilación de tres genotipos de frijol común (Phaseolus vulgaris L.). Agron. Mesoam. 7: 80-85.
Kaur G, Reddy MS (2014) Role of phosphate-solubilizing bacteria in improving the soil fertility and crop productivity in organic farming. Arch. Agron. Soil Sci. 60: 549-564.
Kratz S, Schick J, Schnug E (2016) Trace elements in rock phosphates and P containing mineral and organo-mineral fertilizers sold in Germany. Sci. Total Environ. 542: 1013-1019.
Kucey RMN (1983) Phosphate-solubilizing bacteria and fungi in various cultivated and virgin Alberta soils. Can. J. Soil Sci. 63: 671-678.
Kumar P, Pandey P, Dubey RC, Maheshwaria DK (2016) Bacteria consortium optimization improves nutrient uptake, nodulation, disease suppression and growth of the common bean (Phaseolus vulgaris) in both pot and field studies. Rhizosphere 2: 13-23.
Lara C, Negrete JL (2015) Efecto de un bioinoculante a partir de consorcios microbianos nativos fosfato solubilizadores en el desarrollo de pastos Angleton (Dichantium aristatum). Rev. Col. Biotecnol. 17: 122-130.
Lépiz IR, Ramírez DR (2010) Parientes Silvestres del Frijol Común en el Occidente de México. SINAREFI. Universidad de Guadalajara. México. 64 pp.
Mar SS, Okazaki M (2012) Investigation of Cd contents in several phosphate rocks used for the production of fertilizer. Microchem. J. 104: 17-21.
Ormeño E, Torres R, Mayo J, Rivas R, Peix A, Velázquez E, Zúñiga D (2007) Phaseolus lunatus is nodulated by a phosphate solubilizing strain of Sinorhizobium meliloti in a Peruvian soil. En Velázquez E, Rodríguez-Barrueco C (Eds.) First International Meeting on Microbial Phosphate Solubilization. Salamanca, Spain. Springer. pp. 143-147.
Peix A, Mateos PF, Rodríguez-Barrueco C, Martínez-Molina E, Velazquez E (2001) Growth promotion of common bean (Phaseolus vulgaris L.) by a strain of Burkholderia cepacia under growth chamber conditions. Soil Biol. Biochem. 33: 1927-1935.
Perilla MJ, Ajello G, Bopp C, Elliott J, Facklam R, Knapp JS, Popovic T, Wells J, Dowell SF (2004) Manual de Laboratorio para la Identificación y Prueba de Susceptibilidad a los Antimicrobianos de Patógenos Bacterianos de Importancia para la Salud Pública en el Mundo en Desarrollo. Centros para el Control y la Prevención de Enfermedades. Atlanta, GA, EEUU. pp. 226-231. http://apps.who.int/medicinedocs/documents/s16330s/s16330s.pdf
Qureshi MA, Shakir MA, Iqbal A, Akhtar N, Khan A (2011) Co-inoculation of phosphate solubilizing bacteria and rhizobia for improving growth and yield of mungbean (Vigna radiata L.). J. Anim. Plant Sci. 21: 491-497.
Rajjou L, Duva M, Gallardo K, Catusse J, Bally J, Job C, Job D (2012) Seed germination and vigor. Annu. Rev. Plant Biol. 63: 507-533.
Savci S (2012) Investigation of effect of chemical fertilizers on environment. APCBEE Procedia 1: 287-292.
Sequera O, Rámirez R (2013) Roca fosfórica acidulada con ácido sulfúrico y tiosulfato de amonio como fuente de fósforo para frijol en dos tipos de suelo. Bioagro 25: 39-46.
Sharma K, Dak G, Agrawal A, Bhatnagar M, Sharma R (2007) Effect of phosphate solubilizing bacteria on the germination of Cicer arietinum seeds and seedling growth. J. Herbal Med. Toxicol. 1: 61-63.
Utria E, Goffe S, Reynaldo IM, Morales D, Cabrera JA (2008) Los biosólidos de aguas residuales urbanas aplicados con diferentes frecuencias en las propiedades químicas y microbiológicas del suelo, el rendimiento y la calidad de los frutos de tomate (Solanum lycopersicum Mill). Cult. Trop. 29(4): 5-11.
Valverde A, Igual JM, Cervantes E (2007) Polyphasic characterization of phosphate-solubilizing bacteria isolated from rhizospheric soil of the north-eastern region of Portugal. En Velázquez E, Rodríguez-Barrueco C (Eds.) First International Meeting on Microbial Phosphate Solubilization. Salamanca, Spain. Springer. pp. 16-19, 243-276.
Van Staden J, Sparg SG, Kulkarni MG, Light ME (2006) Post-germination effects of the smoke-derived compound 3-methyl-2H-furo[2,3-c] pyran-2-one, and its potential as a preconditioning agent. Field Crops Res. 98: 98-105.
Zafar M, Abbasil MK, Rahim N, Khaliq A, Shaheen A, Jamil M, Shahid M (2011) Influence of integrated phosphorus supply and plant growth promoting rhizobacteria on growth, nodulation, yield and nutrient uptake in Phaseolus vulgaris. Afr. J. Biotechnol. 10(74): 16793-16807.
Notas de autor
Autora de correspóndencia: Doctora en Ciencias Biológicas, Universidad Autónoma Metropolitana, México. Profesora Investigadora, Instituto Politécnico Nacional, CIIDIR-Oaxaca, México. Dirección: Hornos 1003, Xoxocotlán, Oaxaca, México. 71230. e-mail: mbautistac@ipn.mx
Enlace alternativo
https://www.interciencia.net/wp-content/uploads/2018/03/137-BAUTISTA-43_02.pdf (pdf)