Comunicaciones
EL miRNA bta-miR-19a REGULA LA EXPRESIÓN GÉNICA DEL GEN DICER EN BOVINOS
THE miRNA bta-miR-19a REGULATES DICER GENE EXPRESIÓN IN BOVINES
O miRNA bta-miR-19a REGULA A EXPRESSÃO GÊNICA DO GENE DICER EM BOVINOS
EL miRNA bta-miR-19a REGULA LA EXPRESIÓN GÉNICA DEL GEN DICER EN BOVINOS
Interciencia, vol. 44, núm. 1, pp. 43-47, 2019
Asociación Interciencia
Recepción: 17 Septiembre 2017
Corregido: 17 Enero 2019
Aprobación: 18 Enero 2019
Financiamiento
Fuente: CONACYT-México
Nº de contrato: proyecto no. 168991 y por la beca 266887
Beneficiario: Ana Karen Torres-García
Resumen: La activación del genoma embrionario implica la degradación masiva de los RNAm maternos almacenados durante la ovogénesis por acción de miRNAs. DICER es la ribonucleasa encargada de procesar miRNAs para que sean capaces de reconocer el 3’UTR de un RNAm y bloquear su traducción. En bovinos la expresión del gen Dicer tiene el comportamieto de un RNAm materno. El objetivo del presente estudio fue demostrar que el RNAm de Dicer es regulado por un miRNA. Mediante un análisis bioinformático se identificó la región completa del 3’UTR de Dicer bovino y a través del programa miRmap se encontró que el miRNA bta-miR-19a tenie sitios de unión con este 3’UTR. Posteriormente se transfectó un cultivo de células de la granulosa bovina con diferentes concentraciones del bta-miR-19a (10, 30 y 50nM) por 5h; el cultivo celular se mantuvo durante 48h más. Se extrajo el RNA total y se sintetizó el cDNA para medir la expresión del gen Dicer por PCR cuantitativa y de la proteína DICER por western blot con un anticuerpo específico. Los resultados indicaron que no hubo diferencias en el nivel de expresión del RNAm (P>0,05) entre las diferentes concentraciones del bta-miR-19a; sin embargo, por western blot se demostró disminución de la proteína DI- CER (P<0,05) en células transfectadas con 50mM de bta-miR-19a. Estos resultados demuestran que el bta-miR-19a inhibe la traducción del RNAm del gen Dicer, lo que implica que siendo DICER quien genera los miRNAs, es ella misma quien promueve su propia regulación a nivel genómico.
Palabras clave: Bovino, bta-miR-19ª, Dicer, Embrión, Ovocito.
Abstract: Embryonic genome activation implies a massive degradation of maternal mRNAs stored during oogenesis, through miRNAs. DICER is a ribonuclease responsible for processing miRNAs by recognition of 3’UTR mRNA and blockade of its translation. Dicer gene expression has a maternal mRNA function. The goal of the present work was to show that Dicer mRNA is regulated by a miRNA. The complete region of the bovine Dicer 3’UTR was identified by means of bioinformatic tools and, with the miRmap program, it was found that bta-miR19a has binding sites to this 3’UTR. Subsequently, transfection was performed for 5h with different concentrations (10, 30 y 50nM) of bta-miR-19a in a culture of bovine granulosa cells; the cell culture was maintained for 48h more. Total RNA was isolated and cDNA was synthetized to quantify the Dicer gene expression by Real Time PCR and the DICER protein by western blot assay with a specific anti- body. Results indicated that there were no differences in the level of gene expression (P>0.05) between the different concentrations of bta-miR-19a. However, western blot showed a decrease of DICER protein (P<0.05) in transfected cells with 50mM bta-miR-19a. This demonstrates that bta-miR-19a inhibits the translation of the RNAm of the Dicer gene, which implies that, as DICER generates the miRNAs, it promotes its own regulation at a genomic level.
Resumo: A ativação do genoma embrionário implica a degradação massiva dos RNAm maternos armazenados durante a ovogênese por ação de miRNAs. DICER é a ribonuclease encarregada de procesar miRNAs para serem capazes de reconhecer o 3’UTR de um RNAm e bloquear sua tradução. Em bovinos a expressão do gene Dicer tem comportamento de um RNAm materno. O objetivo do presente estudo foi demonstrar que o RNAm de Dicer é regulado por um miRNA. Mediante uma análise bioinformática foi identificada a região completa do 3’UTR de Dicer bovino e através do programa miRmap foi observado que o miRNA bta-miR-19a tem pontos de união com este 3’UTR. Posteriormente foi transfectada uma cultura de células da granulosa bovina com diferentes concentrações do bta-miR--19a (10, 30 e 50nM) por 5h; a cultura celular foi mantida por mais 48h. O RNA total foi extraído e o cDNA foi sintetizado para medir a expressão do gene Dicer por PCR quantitativa e da proteína DICER por western blot com anticorpo específico. Os resultados indicaram que não houve diferenças no nível de expressão do RNAm (P>0,05) entre as diferentes concentrações do bta-miR-19a; no entanto, por western blot ficou demonstrada a diminuição da proteína DICER (P<0,05) em célu- las transfectadas com 50mM de bta-miR-19a. Estes resultados demonstram que o bta-miR-19a inibe a tradução do RNAm do gene Dicer, o qual implica que, sendo DICER aquele que gera os miRNAs, é também quem promove sua própria regulação em nível genômico.
Introducción
La identificación y caracterización de los genes que participan en la regulación del crecimiento del ovocito y de la transición ovocito-embrión, son requeridos para entender los mecanismos de maduración, fertilización y desarrollo embrionario. Los RNAm maternos son transcritos, sintetizados y traducidos en el ovocito durante el proceso de maduración y después de la fertilizacion en la transición ovocito-embrión (Bettegowda et al., 2008). Al inicio de su desarrollo, el ovocito es transcripcionalmente activo y se encuentra almacenando RNAm para ser utilizado en la etapa de maduración hacia la metafase II. Una vez que ocurre arresto en metafase II, se torna transcripcionalmente inactivo y continúa así, aún después de la fecundación. Cuando se encuentra inactivo, los RNAm almacenados son los encargados de mantener el aporte de proteínas necesarias para soportar las primeras etapas el desarrollo embrionario hasta la activación del genoma embrionario (Tesfaye et al., 2009).
En el modelo bovino, se han identificado diversos RNAm maternos; Mater (Pennetier et al., 2006), Nobox (Tripurani et al., 2011), Nmp2 (Lingenfelter et al., 2011) y Zar1 (Brevini et al., 2004), entre otros. Burrola-Barraza et al. (2011) analizaron la expresión, durante el desarrollo embrionario bovino, del gen Dicer que participa en el procesamiento de los miRNAs; encontraron que Dicer se expresa en el ovocito inmaduro, maduro y en el embrión de 2-4 células, para después decaer en el embrión de 8-16 células y volver a expresarse en la mórula, tiempo que coincide con la activación del genoma embrionario en bovino. Este patrón de expresión es similar al que presentan los genes maternos como Mater (Pennetier et al., 2006), lo que sugiere que Dicer tiene un patrón de expresión correspondiente a un RNAm materno.
Los miRNAs son RNAs de ~24 nucleótidos de longitud, codificados a lo largo del genoma dentro de regiones intergénicas o en regiones intrónicas. Una vez expresados son procesados en el citosol por la enzima DICER, luego son ensamblados en un complejo miRISC donde hibridan con el extremo 3’ no traducido (UTR’3) de un RNAm blanco para promover su degradación (Bushati y Cohen, 2007). Diversos estudios han demostrado que los microRNAs participan en la regulación de los RNAm maternos y, por consiguiente, en la activación del genoma embrionario (Bettegowda et al., 2008; Tripurani, 2011). Tokumaru et al. (2008) determinaron que el RNAm de Dicer es el blanco de Let-7a en células humanas cancerosas de páncreas, Hs766T. Por su parte Tao et al. (2012) analizaron la expresión de Dicer en las células T24 (células de cáncer de vejiga de humano) donde encontraron que el microRNA miR-18a disminuyó la expresión de Dicer a nivel de RNAm y proteína. Así mismo en el bovino se ha demostrado que en los RNAm maternos como Nobox y Nmp2 se regulan vía los miRNAs 196a y 181a, respectivamente (Lingenfelter et al., 2011; Tripurani et al., 2011). Con base en estos antecedentes es posible plantear que en el bovino el gen Dicer sea regulado por algún microRNA, de igual manera que sucede en el humano. Por lo anterior, el objetivo de este trabajo fue demostrar que el gen Dicer es un RNAm que es regulado por un microRNA, cuya acción está implicada con el desarrollo embrionario temprano.
Materiales y Métodos
Localización in silico del UTR’3 del RNAm de Dicer
El análisis para la identificación de la región completa del UTR’3 se realizó en el programa BLAST del NCBI (http://www.ncbi.nlm.nih.gov), buscando la homología entre el UTR’3 de Dicer humano (NM_177438.2) en el genoma de Bos taurus (UMD 3.1.1).
Predicción bioinformática del miRNA de unión a Dicer
La predicción del miRNA para regular el gen Dicer se realizó siguiendo el algoritmo computacional del software miRmap (http://mirmap.ezlab.org/), donde cada uno de los 500 miRNAs de bovino almacenados en esta base fueron evaluados para interaccionar con el UTR’3 del RNAm Dicer (Vejnar y Zdobnov, 2012).
Cultivo de células de la granulosa de bovino
Las células de la granulosa fueron aisladas de acuerdo a lo reportado por Grado-Ahuir et al. (2009). Se utilizaron ovarios de vacas adultas provenientes de la Empacadora Ganadera de Chihuahua, S.A. de C.V. TIF-55, los cuales se transportaron al laboratorio en NaCl 0,15M estéril a temperatura ambiente (22-25ºC) en un lapso ≤3h. Una vez en el laboratorio, se lavaron tres veces con solución salina estéril a la misma concentración, luego se sumergieron en etanol 70% por 30s, para ser enjuagados nuevamente en tres ocasiones con solución salina 0,15M estéril. Posteriormente, se seleccionaron folículos pequeños de 1-5mm de diámetro y se aspiraron con aguja de calibre 21G×112” (BD precisión Glide) adaptada a jeringa de 3ml por llenado automático de la punta sin succionar bruscamente, para garantizar la integridad celular. El fluido folicular obtenido se centrifugó a ~291g por 7min a 4ºC, se descartó el sobrenadante, se resuspendió y se lavó tres veces la pastilla celular con 7ml de medio DMEM/Ham’s-F12 (Sigma) libre de suero; durante cada lavado las células se separaron del medio por centrifugación a ~291g por 7min a 4ºC. Después de la última centrifugación, la pastilla celular se resuspendió con 2ml de DMEM/Ham’s-F12 (Sigma) suplementado con 5mg·ml-1 de DNase (Sigma) y 2,5mg·ml-1 de colagenasa (Sigma) para prevenir la aglutinación de las células. Se incubaron 6×105 células viables en cajas de Petri NUNC (8,8cm2) con 3ml de DMEM/Ham’s-F12 suplementado con 5% de suero de fetal bovino (Sigma) y gentamicina 0,12mM, y se mantuvieron a 38,5ºC con una atmósfera de 5% de CO2 por 48h.
Transfección de células de la granulosa con el bta-miR-19a
Para la transfección en el cultivo de células de la granulosa se utilizaron separadamente concentraciones de 10, 30 y 50nM de bta-miR-19a (MC10 649; Applied Biosystems) y un control sin transfección. Se diluyeron 3µl de bta-miR-19a en 50µl de Opti-MEM (Invitrogen™), correspondiente a cada tratamiento, mientras que en otros tubos se diluyeron 3µl de lipofectamina (Invitrogen™) en 50µl de Opti-MEM (Invitrogen™); se mezcló el contenido de ambos tubos y se incubaron por 20min a temperatura ambiente. Al término de la incubación se agregaron los complejos lipofectamina-DNA a cada cultivo celular, incubándolos con esta mezcla durante 5h a 37ºC con 5% de CO2. Al terminar el tiempo de incubación, se descartó el medio Opti-MEM con lipofectamina-DNA y se reemplazó con medio DMEM/Ham’s-F12 para mantener el cultivo celular durante 48h a 37ºC con 5% de CO2. Para retirar las células del cultivo se removió el medio y se lavó la capa celular con PBS 1X, se adicionó 500µl de Tripsina-EDTA 1X (Sigma) incubando en placa de calentamiento a 37ºC por ~5min o hasta que las células se separaron de la superficie del plato de cultivo. Las células en suspensión se centrifugaron a 1000rpm por 5min a 4ºC para descartar el sobrenadante y resuspender la pastilla en 1ml de PBS 1X y centrifugar nuevamente. Para finalizar, la pastilla celular se resuspendió en 500µl de TRIzol (Invitrogen).
Extracción de RNA total de células de la granulosa
Se aisló el RNA total de las células de la granulosa provenientes de cada tratamiento; se lisaron con 500µl del reactivo TRizol, y se transfirieron a tubos de 1,5ml y se incubaron en TRIzol (Invitrogen) durante 5min a temperatura ambiente. Al término de la incubación se añadió 0,10ml de cloroformo y se procedió a dar agitación vigorosa durante 15s para posteriormente incubar 3min a temperatura ambiente; después las muestras se centrifugaron a 3500g durante 30min a 4ºC y la fase acuosa superior se transfirió a un tubo nuevo. Una vez realizado esto, el RNA se precipitó con 0,25ml de alcohol isopropílico, se mezcló manualmente y se incubó por 10min a temperatura ambiente, seguido por centrifugación a 3500g durante 10min a 4ºC; el sobrenadante obtenido se retiró y el sedimento de RNA se lavó con 0,5ml de etanol 70%, después se centrifugó 5min a 3500g a 4ºC, el sobrenadante se eliminó y se dejó secar el precipitado de RNA durante 5min a temperatura ambiente, después al RNA se le adicionó 10µl del buffer TE. El RNA eluido se cuantificó en un espectrofotómetro NanoDrop (ThermoScientific) a una longitud de onda de 260nm. El RNA obtenido se almacenó a -80ºC hasta la síntesis de cDNA.
RT-PCR cuantitativa
La síntesis de cDNA se realizó partiendo de 10ng de RNA total, empleando el kit SuperScript® VILOTM (InvitrogenTM) en un volumen final de 20µl. Las reacciones se colocaron en un termociclador Techne bajo el siguiente programa: temperatura de ajuste de 25ºC por 10min seguida de 60min a 42ºC, para desactivar la enzima a una temperatura de 85ºC por 5min y por último se mantuvo el sistema a 4ºC. El cDNA obtenido se cuantificó en un espectrofotómetro NanoDrop (ThermoScientific) a una longitud de onda de 260nm. Para las recciones de PCR cuantitativa se utilizó el kit TaqMan Gene Expression Assay (Applied Biosystems) que incluye una sonda específica para Dicer (Bt03217754_m1) con el reportero FAM y el quencher MGB-NFQ y se seleccionó el gen RNAr18S como gen endógeno. La mezcla de reacción se realizó usando en todos los casos 100ng de cDNA, 1µl de TaqMan Gene Expression Assay 20X, 10µl del TaqMan Universal Master Mix II y agua libre de nucleasas hasta completar un volumen final de 20µl. Las reacciones se realizaron en el equipo Real Time StepOne (Applied Biosystems) bajo el siguiente programa: activación de la polimerasa a 95ºC por 10min, seguida de 40 ciclos de amplificación constituidos por desnaturalización a 95ºC por 15s y alineamiento/extensión a 60ºC por 1min.
Ensayos de western blot
Posterior a la transfección en el cultivo de células de la granulosa, se retiró el medio de cultivo, se añadieron 400µl de CellLytic M y 20µl de inhibidor de proteasas (GE Healthcare), se incubaron durante 15min en agitación constante, al término se tomó el lisado de células y se procedió a centrifugar por 15min a 12000g; el sobrenadante que contiene el extracto de proteínas se transfirió a un tubo nuevo. Se cuantificaron las proteínas empleando el kit BCA*Protein (Pierce) en un espectrofotómetro Nanodrop (ThermoScientific). Las proteínas se almacenaron a -20ºC hasta su posterior uso. Los extractos de proteínas totales (54µg) se separaron por SDS-PAGE y se transfirieron a una membrana de nitrocelulosa a 4ºC con 100V por 1h, al terminar la transferencia la membrana se tiñó con rojo de Ponceau para confirmar la presencia de las proteínas. Se realizaron lavados con PBS hasta eliminar el colorante y se dejó en solución de bloqueo PBS-Tween20 0,05% y leche Svelty baja en grasa al 5% durante toda la noche a 4ºC con agitación constante. Para la detección de las proteínas se incubó con el anticuerpo policlonal contra DICER (H-212, Santa Cruz Biotecnology) y el anticuerpo policlonal contra ACTINA(H-300, Santa Cruz Biotecnology), ambos con dilución 1:200 y una concentración de 200µg·ml-1, el periodo de incubación fue de 3h a temperatura ambiente y agitación constante, al término se realizaron cinco lavados con PBS-Tween20 al 0,1%. Para realizar la detección del anticuerpo primario se incubó con un segundo anticuerpo de cabra anti-conejo IgG-HRP (Santa Cruz Biotecnolgy) diluido 1:1000 con una concentración de 200µg·ml-1 durante 1h a temperatura ambiente y agitación constante. Al concluir la incubación del segundo anticuerpo se lavaron las membranas con PBS-Tween20 al 0,1% y se procedió al revelado con el kit ECL western blotting substrate (Promega™) siguiendo las especificaciones del fabricante.
Análisis estadístico
Todos los experimentos se realizaron tres veces de forma independiente. Para el análisis de expresión génica se analizó la abundancia relativa del RNAm, la cual se determinó por el método 2-DCT de acuerdo a lo sugerido por Livak y Schittgen (2001), donde el DCT se generó a partir de la diferencia del promedio de los CT del gen de interés normalizado con el promedio de los CT del control interno RNAr18S.
Para el análisis de western blot, posterior a la digitalización en formato JPG de la placa autorradiográfica, la intensidad de cada mancha se estimó seleccionando el área y obteniendo la densidad por pixel (dpp) con el software ImageJ (http://rsbweb,nih.gov/ij/index.html). La cantidad relativa de la proteína DICER se obtuvo normalizando con la dpp obtenidad de la proteína ACTINA.
Para todos los casos se realizó un análisis parámetrico en el programa XLSTAT-Base donde se utilizo la prueba Krustal-Wallis para probar significancia a P<0,05 entre los tratamientos.
Resultados y Discusión
Predicción bioinformática del miRNA de unión a Dicer
La hipótesis de esta investigación fue que en bovinos el gen Dicer es regulado vía degradación por un miRNA. Para probar esto lo primero que se necesitaba tener era la secuencia completa del UTR’3 del RNAm que codifica el gen Dicer en bovinos. Para ello se realizó una búsqueda en la base de datos del Genebank del NCBI, donde se encontró que el RNAm Dicer (NM_203359.1), tiene un tamaño reportado de 5828 bases (b), con una región codificante de 5571 b, lo que deja una longitud de 40 b para la región UTR’3, muy corta si se tiene en cuenta que el extremo UTR’3 de la mayoría de los RNAm tiene una longitud mayor a 1000 b. Dado que el resto de la secuencia que compone el UTR’3 no está reportada como tal, se procedió a la identificación completa de esta región. Teniendo el antecedente que el UTR’3 de Dicer humano (NM_177438.2) sí se encuentra reportado en el Genebank, se realizó un análisis de homología con el programa BLAST en el NCBI, comparando la secuencias del UTR’3 humano (NM_177438.2) contra el genoma de Bos taurus UMD 3.1 reportado en el NCBI. El resultado mostró un 82% de identidad entre el UTR’3 humano con el cromosoma 21 de Bos taurus, (Figura 1a). Una vez que se ubicó la posición exacta en el cromosoma 21, fue posible identificar en el resto del gen Dicer (NM_203359) que ya está reportado, el codón de paro y la señal de poliadenilación, lo que llevó a determinar una región de 4388pb que conforman el UTR’3 del gen Dicer bovino (Figura 1b). Con esta secuencia entonces se procedió a realizar la predicción del miRNA blanco siguiendo el algoritmo del software miRmap, donde se se logró predecir que el bta-miR-19a tiene un sitio de unión que abarca de la posición 291 a la 298 del UTR’3 para Dicer bovino (Figura 2). Los miRNAs se encuentran localizados en exones e intrones de RNA no codificante o en intrones de RNA codificantes (Lugo et al., 2009). Interesantemente, muchos miRNA se localizan en familias de genes policistrónicos, donde a partir de un transcrito primario se generan múltiples miRNAs (Aravin et al., 2003; Altuvia et al., 2005). El bta-miR-19a forma parte de la familia miR-17-92 (Romao et al., 2014), que además del bta-miR19a genera otros cinco miRNAs individuales: miR-17, miR-18a, miR-19a, miR-20a, y miR-92a; donde todos los miembros de esta familia han sido relacionados con procesos oncogénicos (Tao et al., 2012).
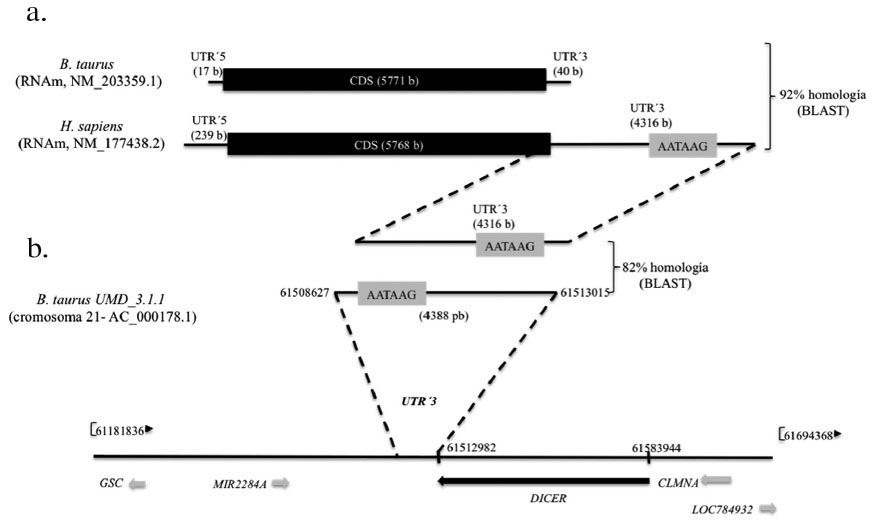
Figura 1
Localización in silico del UTR’3 del RNAm Dicer bovino. A: Esquematización donde se comparan los RNAm del gen Dicer de bovino (B. taurus) y humano (H. sapiens). B: Localización del UTR’3 de Dicer en B. taurus, mediante Blast del UTR’3 de Dicer humano contra el genoma completo de B. taurus. La secuencia AATAAG dentro de la caja gris corresponde a la señal de poliadenilación.

Figura 2
Predicción bioinformática del miRNA de unión al UTR’3 de Dicer. Sitio de unión bta-miR-19a en el UTR’3 de Dicer bovino.
Acción del miRNA bta-miR-19a sobre la expresión de Dicer bovino
Con el fin de comprobar la acción del bta-miR-19a sobre la regulación del RNAm Dicer, este miRNA se introdujo mediante un ensayo de transfección en un cultivo primario de células de la granulosa de origen bovino, las cuales expresan de forma endógena el gen Dicer. Después de transfectar con diferentes concentraciones el bta-miR-19a se encontró (Figura 3) que el bta-miR-19a es capaz de disminuir la expresión del gen Dicer. Aunque no se encontró diferencia estadística significativa (P>0,05) en ninguno de los tratamientos, se observa una clara tendencia a la disminución de la expresión de Dicer al transfectar las células de la granulosa con una concentración de 50nM del bta-miR-19a. Para confirmar que la depresión de la expresión del gen Dicer afectaba la traducción de la proteína, se realizaron ensayos de western blot con extractos proteicos provenientes de células de la granulosa transfectadas con el bta-miR-19a. Los resultados indicaron que en las células de la granulosa transfectadas con 50nM de bta-miR-19a, la presencia de la proteína DICER disminuye en comparación con los otros tratamientos (P<0,05; Figura 4). Esto implica que el Dicer bovino se regula de una forma similar a como lo hace el Dicer humano, con la diferencia que en humanos la represión es mediada por miR-18a (Tao et al., 2012). Es importante señalar que tanto el miR-18a como el bta-miR-19a pertenecen a la familia miR-17-92, lo que convierte a la regulación del RNAm de Dicer en un evento evolutivamente conservado. Sin embargo, diferentes investigaciones realizadas en humano han demostrado que el Dicer es regulado por acción del miRNA let-7 en líneas celulares Hs766T de cáncer de páncreas (Tokumaru et al. 2008) y también por miR-130 en células de cáncer de cérvix (He et al. 2014). Lo anterior implica que Dicer en humano puede ser regulado por varios miRNAs dependiendo del tipo celular en el que se encuentre. Si esto sucede de la misma manera en el bovino es una interrogante interesante de dilucidar. Por lo pronto, los resultados de este estudio coinciden con los obtenidos en humano, donde la expresión del gen Dicer es regulada por la acción de un miRNA. Lo que es intrigante es la proteína DICER, quien genera los miRNAs, ya que entonces pareciera que la misma DICER modula su propia expresión. La activación del genoma embrionario implica la degradación masiva de los RNAm maternos almacenados durante la ovogénesis por acción de miRNAs. De acuerdo a lo reportado por Burrola-Barraza et al. (2011) la expresión del gen Dicer tiene un comportamiento similar a lo reportado para RNAm maternos y, coincidentemente, algunos RNAm maternos como Nobox y Nmp2 también son regulados por miRNAs (Lingenfelter et al., 2011; Tripurani et al., 2011). Integrando esto, proponemos que en el bovino el gen Dicer, al ser un RNAm materno es regulado vía la acción del miRNA bta-miR-19a, y modula su propia expresión.
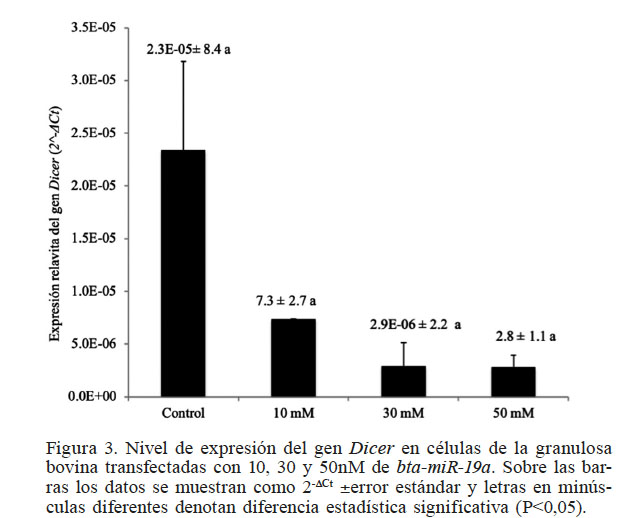
Figura 3
Nivel de expresión del gen Dicer en células de la granulosa bovina transfectadas con 10, 30 y 50nM de bta-miR-19a. Sobre las barras los datos se muestran como 2-DCt ±error estándar y letras en minúsculas diferentes denotan diferencia estadística significativa (P<0,05).
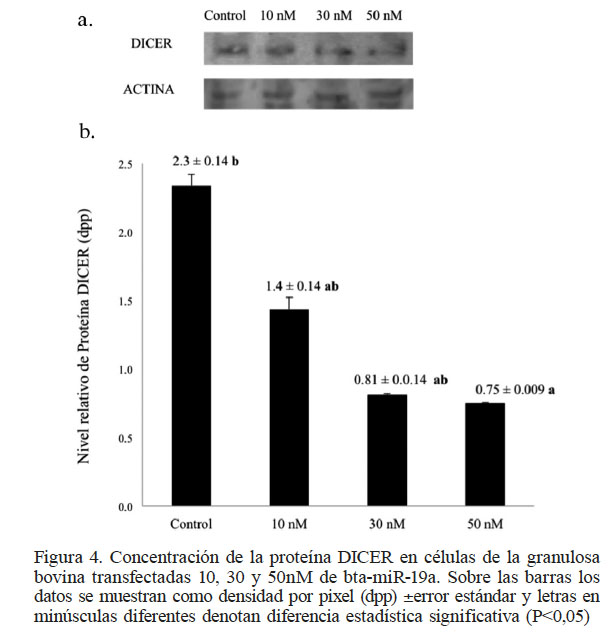
Figura 4
Concentración de la proteína DICER en células de la granulosa bovina transfectadas 10, 30 y 50nM de bta-miR-19a. Sobre las barras los datos se muestran como densidad por pixel (dpp) ±error estándar y letras en minúsculas diferentes denotan diferencia estadística significativa (P<0,05)
Agradecimientos
Los autores agradecen el financiamiento otorgado por el CONACYT-México a través del proyecto no. 168991 y por la beca 266887 otorgada a Ana Karen Torres-García.
Referencias
Altuvia Y, Landgraf P, Lithwick G, Elefant N, Pfeffer S, Aravin A, Brownstein MJ, Tuschl T, Margalit H (2005) Clustering and conservation patterns of human microRNAs. Nucl. Acids Res. 33: 2697-2706.
Aravin AA, Lagos-Quintana M, Yalcin A, Zavolan M, Marks D, Snyder B, Gaasterland T, Meyer J, Tuschl T (2003) The small RNA profile during Drosophila melanogaster development. Dev. Cell 5: 337-350.
Bettegowda A, Patel OV, Lee KB, Park -E, Salem M, Yao J, Ireland JJ, Smith GW (2008) Identification of novel bovine cumulus cell molecular markers predictive of oocyte competence: functional and diagnostic implications. Biol. Reprod. 79: 301-309.
Brevini TAL, Cilo F, Colleoni S, Lazzari G, Galli C, Gandolfi F (2004) Expression pattern of the maternal factor zygote arrest 1 (Zar1) in bovine tissues, oocytes, and embryos. Mol. Reprod. Dev. 78: 375-380.
Burrola-Barraza M, Hernández-Seáñez R, Barceló-Fimbres M, Rodríguez-Almeida F, GonzálezRodríguez E, García-Quiñónez S, Grado-Ahuir J, Moreno-Brito V (2011) Dicer gene expression during early bovine embryo development. Mol. Reprod. Dev. 78: 622-622.
Bushati N, Cohen SM (2007) microRNA functions. Annu. Rev. Cell Dev. Biol. 23: 175-205.
Grado-Ahuir J, Aad P, Ranzenigo G, Caloni F, Cremonesi F, Spicer L (2009) Microarray analysis of insulin-like growth factor-I-induced changes in messenger ribonucleic acid expression in cultured porcine granulosa cells: possible role of insulin-like growth factor-I in angiogenesis. J. Anim. Sci. 87: 1921-1933.
He L, Wang H, Zhang L, Huang L, Li J, Xiong Y, Zhang M, Jia W, Yun J, Luo R (2014) Prognostic significance of low DICER expression regulated by miR-130a in cervical cancer. Cell Death Dis. 5: 1205-1215.
Lingenfelter BM, Tripurani SK, Tejomurtula J, Smith GW, Yao J (2011) Molecular cloning and expression of bovine nucleoplasmin 2 (NPM2): a maternal effect gene regulated by miR-181a. Reprod. Biol. Endocrinol. 9: 40-48.
Livak KJ, Schmittgen TD (2001) Analysis of relative gne expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) Method. Methods 25: 402-208.
Lugo Trampe Á, Trujillo Murillo KdC (2009) MicroRNAs: reguladores clave de la expresión génica. Med. Univ. 11: 187-192
Pennetier S, Perreau C, Uzbekova S, Thélie A, Delaleu B, Mermillod P, Dalbiès-Tran R (2006) MATER protein expression and intracellular localization throughout folliculogenesis and preimplantation embryo development in the bovine. BMC Dev. Biol. 6: 26-35.
Romao JM, Jin W, He M, McAllister T (2014) MicroRNAs in bovine adipogenesis: genomic context, expression and function. BMC Genomics 15: 137-152.
Tao J, Wu D, Li P, Xu B, Lu Q, Zhang W (2012) microRNA-18a, a member of the oncogenic miR-17-92 cluster, targets Dicer and suppresses cell proliferation in bladder cancer T24 cells. Mol. Med. Rep. 5: 167-172.
Tesfaye D, Worku D, Rings F, Phatsara C, Tholen E, Schellander K, Hoelker M (2009) Identification and expression profiling of microRNAs during bovine oocyte maturation using heterologous approach. Mol. Reprod. Dev. 76: 665-677.
Tokumaru S, Suzuki M, Yamada H, Nagino M, Takahashi T (2008) let-7 regulates Dicer expression and constitutes a negative feedback loop. Carcinogenesis 29: 2073-2077.
Tripurani SK, Lee KB, Wang L, Wee G, Smith GW, Lee YS, Latham KE, Yao J (2011) A novel functional role for the oocyte-specific transcription factor newborn ovary homeobox (NOBOX) during early embryonic development in cattle. Endocrinology 152: 1013-1023.
Vejnar CE, Zdobnov EM (2012) MiRmap: comprehensive prediction of microRNA target repression strength. Nucl. Acids Res. 40: 11673-11683.
Notas de autor
mburrola1@uach.mx