Comunicaciones
LIBERAÇÃO DO PARASITOIDE Cotesia flavipes (HYMENOPTERA: BRACONIDAE) EM Diatraea saccharalis (LEPIDOPTERA: CRAMBIDAE) NA CANA-DE-AÇÚCAR
LIBERACIÓN DEL PARASITOIDE Cotesia flavipes (HYMNOPTERA: BRACONIDAE) EN Diatraea saccharalis (LEPIDOPTERA: CRAMBIDAE) EN UNA PLANTACIÓN DE CAÑA DE AZÚCAR
RELEASE OF THE PARASITOID Cotesia flavipes HYMENOPTERA: BRACONIDAE) ON Diatraea saccharalis (LEPIDOPTERA: CRAMBIDAE) IN A SUGAR CANE PLANTATION
LIBERAÇÃO DO PARASITOIDE Cotesia flavipes (HYMENOPTERA: BRACONIDAE) EM Diatraea saccharalis (LEPIDOPTERA: CRAMBIDAE) NA CANA-DE-AÇÚCAR
Interciencia, vol. 44, núm. 5, pp. 287-290, 2019
Asociación Interciencia
Recepção: 31 Agosto 2017
Corrected: 21 Maio 2019
Aprovação: 22 Maio 2019
Resumo: Diatraea saccharalis (Lepidoptera: Crambidae) é considerada uma das principais pragas da cultura da cana-de-açúcar. O método mais eficiente para o controle desse inseto é a liberação no campo do inimigo natural, Cotesia flavipes(Hymenoptera: Braconidae). No entanto, uma série de fatores pode afetar a eficiência do controle, sendo a temperatura um dos mais importantes. Grandes oscilações de temperatura são observadas nos horários em que se realizam as liberações de C. flavipes. O objetivo foi avaliar o parasitismo de duas linhagens da C. flavipes em diferentes horários de liberação e identificar as melhores condições para essas liberações. Para isso, internódios de cana-de-açúcar contendo lagartas de quarto ínstar de D. saccharalis foram distribuídos em um canavial, sendo posteriormente liberados os parasitoides nas 6:00, 7:00, 8:00, 9:00 e 10:00, permanecendo os colmos no campo por 24h. Após esse período, os internódios com as lagartas foram levados para o laboratório para avaliar o parasitismo. As maiores taxas de parasitismo ocorreram nos horários entre 7:00 e 9:00, quando a temperatura média foi de 24ºC no interior do canavial.
Palavras-chave: Broca , Controle Biológico , Emergência , Inimigo Natural , Pragas .
Resumen: Diatraea saccharalis (Lepidoptera: Crambidae) es considerada como una de las principales plagas del cultivo de la caña de azúcar. Para el control de ese insecto el método más eficiente de control es a través de la liberación del parasitoide Cotesia flavipes (Hymenoptera: Braconidae). Sin embargo, una serie de factores pueden afectar la performance de ese enemigo natural, siendo la temperatura un factor importante. En regiones de cultivo de la caña de azúcar se verifican grandes oscilaciones de temperatura en los horarios en que se realizan las liberaciones de C. flavipes. El objetivo de este trabajo fue evaluar el parasitismo en diferentes horarios de liberación de dos linajes del parasitoide, de manera semejante a lo que se realiza en las haciendas e identificar las mejores condiciones para esas liberaciones. Internodios de caña de azúcar que contenían orugas de cuarto instar de la broca fueron distribuidos en un cañaveral, siendo posteriormente liberados los parasitoides a los 6:00, 7:00, 8:00, 9:00 y 10:00. permaneciendo Los internodos permanecieron en el campo por 24h. Después de ese período, los internodios con las orugas fueron llevados al laboratorio para evaluar el parasitismo. Las mayores tasas de parasitismo fueron observadas cuando la temperatura media en el interior del cultivo de la caña de azúcar fue de 24ºC, en los horarios entre 7:00 y 9:00.
Abstract: Diatraea saccharalis (Lepidoptera: Crambidae) is considered as one the most important pest for sugarcane plantations. Biological control, through the release of Cotesia flavipes (Hymenoptera: Braconidae), is the most efficient means of controlling this insect pest. However, several factors can affect the performance of the natural enemy, being the temperature one of the most important. In sugarcane plantations, great oscillations of temperature can be observed during the time of release of C. flavipes. The aim of the work was to ascertain the degree of parasitism by two strains of this parasitoid at the different times of release that are used by the farmers and identify the best liberation moment. Internodes of sugarcane containing fourth instar caterpillars of D. saccharalis were distributed among plants in a cane field, and parasitoids were released at different times (6:00, 7:00, 8:00, 9:00 and 10:00). The internodes remained in the field for 24h. After this period, all of them were taken to the laboratory to evaluate the parasitism. The highest rate of parasitism was observed when inside of the sugarcane plantation the medium temperature was 24ºC and the release was done between 7:00 and 9:00.
Introdução
O Brasil se destaca por ser o maior produtor de cana-de-açúcar (Saccharum officinarum L.) com uma produção de 688×106t em uma área plantada de ~10,1×106ha (IBGE, 2019). Diatraea saccharalis (Fabricius) (Lepidoptera: Crambidae) é considerada uma das principais pragas da cultura (Dinardo-Miranda et al., 2012) sendo capaz de causar perdas de biomassa, morte do meristema apical e redução de açúcar e álcool (Rossato et al., 2013). Segundo Dinardo-Miranda et al. (2011), a cada 1% de intensidade de infestação da broca, ocorrem perdas de 0,49% de açúcar, 0,28% de álcool e 1,50% na produtividade de colmos.
O controle da D. saccharalis através de método químico não é eficiente, devido a lagarta ficar protegida no colmo. Dessa forma, o controle biológico com parasitoides é o método mais utilizado (Oliveira et al., 2012a). Segundo Pinto et al. (2006), o sucesso do controle biológico da broca da cana se deve a existência de grande diversidade de parasitoides e predadores, que atuam principalmente sobre as fases de ovo e larva da praga. O controle biológico desse inseto-praga nos canaviais brasileiros é realizado principalmente pelo parasitoide larval e exótico Cotesia flavipes (Cameron, 1891) (Hymenoptera: Braconidae) (Carvalho et al., 2007; Arroyo et al., 2012). O uso de C. flavipes para o controle da Diatraea spp. é considerado um dos maiores programas de controle biológico em nível mundial, com uma área tratada em torno de 3×106ha (Vacari et al., 2012).
Fatores bióticos, como hospedeiro de criação, qualidade, quantidade e idade dos parasitoides são importantes e influenciam na eficiência desses insetos benéficos em campo, visando o controle biológico de pragas. A baixa qualidade desses insetos pode resultar em falhas no controle, comprometendo a atividade canavieira. Por isso a identificação de linhagens e/ou espécies e a avaliação da adaptação ao hospedeiro-alvo são fundamentais para garantir o sucesso de liberações de parasitoides em campo (Oliveira et al., 2005;Pratissoli et al., 2006).
Fatores abióticos como o clima afetam as interações entre espécies, como plantas-herbívoros, predador-presa e parasitoide-hospedeiro (Tylianakis e Binzer, 2014). Os parasitoides dependem de uma série de adaptações, de acordo com a ecologia e a fisiologia dos seus hospedeiros e plantas hospedeiras, para sua sobrevivência e, portanto, é provável que sejam altamente suscetíveis as mudanças nas condições ambientais (Hance, et al., 2007). A capacidade de um parasitoide procurar seu hospedeiro depende de sua tolerância às variações climáticas, como a temperatura, que exerce influência sobre a biologia, metabolismo, reprodução e a interação parasitoide/hospedeiro (Pereira et al., 2011; Oliveira et al., 2012b; Selvaraj et al., 2013).
Em Dourados, Mato Grosso do Sul, Brasil, registros climáticos obtidos da estação meteorológica da Embrapa Agro-pecuária Oeste demonstram variações de temperaturas de até 10ºC em um único dia, podendo afetar a performance de inimigos naturais no campo (Oliveira et al., 2012a). Assim, os objetivos deste trabalho foram avaliar o parasitismo de C. flavipes em diferentes horários de liberação, de maneira semelhante ao que é realizado nas lavouras, e identificar as melhores condições para essas liberações.
Material e Métodos
O experimento foi realizado em cultivo da cana-de-açúcar localizado no município de Dourados/MS, Brasil. As lagartas da broca da cana D. saccharalis foram obtidas da criação do laboratório de Entomologia da Embrapa Agropecuária Oeste.
Multiplicação de Diatraea saccharalis
Ovos de D. saccharalis foram tratados com sulfato de cobre 1% e mantidos em placas de Petri (10cm diâmetro e 1,5cm altura) vedados com papel filme e incubados em câmara climatizada a 25 ±1ºC e fotofase de 12h. Após eclosão, as lagartas foram transferidas para tubos de vidro (8,5cm altura x 2,5cm diâmetro) contendo dieta artificial modificada de Hensley e Hammond (1968) à base de farelo de soja, germe de trigo, vitaminas e sais minerais (Parra, 2007), sendo as mesmas mantidas nestas condições até a fase de pupa. As pupas foram retiradas da dieta, sexadas e acondicionadas em gaiolas de PVC (10cm diâmetro e 22cm altura), revestidas internamente com folha de papel sulfite como substrato para oviposição e fechadas com tecido do tipo ‘voil’ e elástico. Um total de 24 pupas (12 fêmeas e 12 machos) foram acondicionadas por gaiola, onde permanecem até a fase adulta. Os adultos foram alimentados com solução aquosa de mel 10%. Após o acasalamento, as fêmeas realizaram as posturas nas folhas, iniciando um novo ciclo.
Obtenção de Cotesia flavipes
Para a realização do experimento foram utilizadas duas linhagens do parasitoide, que foram fornecidos por um laboratório de controle biológico localizado no município de Dourados/MS (Linhagem 1) e por uma usina sucroalcooleira (provenientes de um laboratório de São Paulo/SP) (Linhagem 2). Os parasitoides foram enviados pelos laboratórios na fase de pupa e permaneceram em laboratório da Embrapa Agro-pecuária Oeste a 25ºC, até 24h após a emergência, quando foram levados para a área experimental.
Informações climáticas
Dados de temperatura e umidade foram obtidos da Estação Meteorológica da Embrapa Agropecuária Oeste (informações externas a área experimental com a cana), e por um termômetro digital (Datalogger Extech 135 RHT10) (informações dentro da área experimental instalada no canavial).
Bioensaio - Horário de liberação sobre o parasitismo de C. flavipes
Para o desenvolvimento do experimento, uma lagarta de D. saccharalis de quarto instar foi introduzida em um orifício aberto em internódios de cana-de-açúcar com ~25cm. Esses internódios foram protegidos com papel alumínio e foram mantidos em laboratório durante 24h, com o objetivo de que a lagarta se adaptasse ao interior do internódio. Após esse período, esses internódios foram levados para campo e amarrados em plantas de um canavial em uma altura de ~1,20cm, que estava com seis meses de idade e se tratava de cana soca em quarto corte em uma área experimental com ~2,9ha (29.160m2), localizada a 22º16'50.10''S e 55º07’36. 95''O.
Quatro internódios infestados com a broca foram dispostos a uma distância de 2m de cada ponto de liberação, seguindo a distribuição dos pontos cardeais e os pontos de liberação tinham 29m de distância entre si, visando assegurar uma distância suficiente para que os parasitoides liberados em um ponto não influenciassem no parasitismo do outro ponto de liberação.
As duas linhagens de C. flavipes estavam com ~24h de emergência e foram liberadas nos horários 6:00, 7:00, 8:00, 9:00 e 10:00. A quantidade de parasitoides liberados foi de 1500 por ponto.
Após 24h das liberações, os colmos foram levados para o laboratório, e as lagartas foram colocadas novamente em dieta artificial e mantidas em sala climatizada (25ºC, umidade relativa de 60%, fotofase de 12h), para verificar a porcentagem de parasitismo.
Para cada uma das linhagens, o delineamento experimental foi em blocos casualizados, com cinco tratamentos (horários de liberação) e quatro repetições (blocos), sendo que a unidade experimental (parcela) consistiu de quatro colmos ao redor do ponto de liberação. Os resultados para cada linhagem foram submetidos à análise de regressão a partir do modelo polinomial, para estabelecer o melhor horário de liberação. Os experimentos com cada linhagem foiram realizado simultaneamente, na mesma lavoura e em área contígua.
A escolha da equação que melhor se ajustou aos dados foi baseada no coeficiente de determinação (R2) e na significância dos coeficientes de regressão (βi) e da regressão pelo teste F (<0,05).
Resultados e Discussão
O ponto máximo de parasitismo para a Linhagem 1 foi às 7h e 44min, com uma média de 39,8% das brocas parasitadas, e para Linhagem 2, que apresentou 55,3% de parasitismo, o horário que proporcionou maior parasitismo foi às 8h e 19min (Figura 1). Botelho e Macedo (2002) relataram, índices de até 38,89% de parasitismo de D. saccharalis por C. flavipes em liberações realizadas no Estado de São Paulo entre os anos de 1990 a 1999, em mais de 1,8×106ha. Esses valores são semelhantes ao obtidos com a Linhagem 1, mas são menores que os obtidos pela Linhagem 2. Esses índices máximos obtidos para cada uma das linhagens podem estar diretamente relacionados com a qualidade do parasitoide, onde fatores no processo de criação podem afetar a performance do inimigo natural e poderia explicar esses melhores resultados obtidos no presente trabalho. O que também pode explicar esses melhores resultados é o fato de que eles são referentes ao que foi identificado como melhor horário (temperatura para liberação) e os resultados relatados por Botelho e Macedo (2002) não levam em consideração os horários e temperaturas durante a liberação.
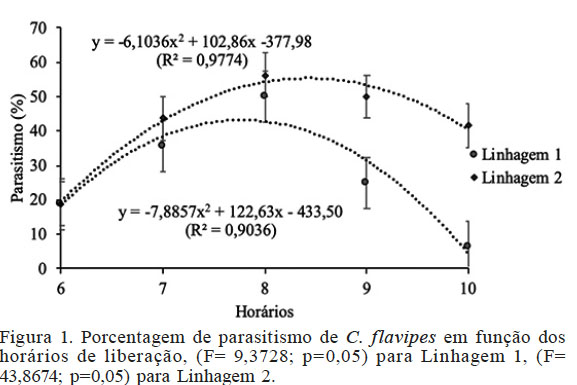
Figura 1
Porcentagem de parasitismo de C. flavipes em função dos horários de liberação, (F= 9,3728; p=0,05) para Linhagem 1, (F= 43,8674; p=0,05) para Linhagem 2.
A temperatura máxima no interior do canavial nos horários de liberação foi de 25,8ºC e a mínima 23,7ºC, sendo que nos horários entre 7:00 e 9:00 foi onde se verificaram as melhores taxas de parasitismo a temperatura média foi de 24ºC (Tabela I). Vale destacar que mesmo em épocas mais frias (liberação realizada no mês de maio), a temperatura no interior dos talhões tem menor oscilação (Tabela I), favorecendo a performance do parasitoide.
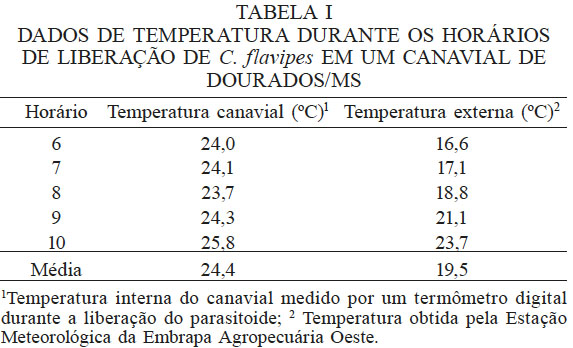
1 Temperatura interna do canavial medido por um termômetro digital durante a liberação do parasitoide; 2 Temperatura obtida pela Estação Meteorológica da Embrapa Agropecuária Oeste.
O ambiente interfere no controle biológico, uma vez que sua liberação é um aspecto importante na redução de pragas agrícolas; por isso, oscilações de temperatura durante o dia têm uma forte influência sobre o desempenho de parasitoides (Firake e Khan, 2014). Furlong e Zalucki (2017) indicam que o metabolismo, crescimento, movimento, reprodução e interação hospedeiro-parasitoide dependem da temperatura.
Trabalhos realizados com C. flavipes têm demonstrado que a temperatura é um dos mais importantes fatores que afetam o desempenho desse parasitoide (Potting et al., 1997). Estudos também relatam que para C. flavipes, a faixa considerada favorável para o desenvolvimento situa-se entre 20 e 30ºC (Botelho e Macedo, 2002).
É importante conhecer essa dinâmica que influencia a performance de cada parasitoide, visando buscar informações que contribuam para melhoria de programas de liberação, pois Bittencourt e Berti-Filho (2004) relatam que temperatura de 30ºC afeta negativamente Palmistichus elaeisis Delvare & LaSalle (Hymenoptera: Eulophidae) em diferentes hospedeiros, causando mortalidade no estágio de pré-pupa e sugerindo que 22ºC é a temperatura mais adequada para seu desenvolvimento. Já Glaeser et al. (2016) relataram que para Trichospilus diatraeae Cherian & Margabandhu (Hymenoptera: Eulophidae) não houve alterações na sobrevivência, longevidade, parasitismo e emergência desse parasitoide quando exposto a temperatura de até 33ºC.
Conclusão
Os horários de liberação estão relacionados com as temperaturas no momento de liberação. Verificou-se que os melhores horários de liberação de C. flavipes devem ocorrer em temperaturas próximas a 24ºC. A menor oscilação de temperatura no interior do canavial se mostrou um importante fator no momento das liberações, oferecendo um microclima favorável para na performance do parasitoide.
Agradecimentos
Os autores agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pela concessão da bolsa de Mestrado ao primeiro autor.
LIBERAÇÃO DO PARASITOIDE Cotesia flavipes (HYMENOPTERA: BRACONIDAE) EM Diatraea saccharalis (LEPIDOPTERA: CRAMBIDAE) NA CANA-DE-AÇÚCAR
Arroyo BM, Filho CCF, Lima JA, Pinto AS (2012) Predação de “massas” de Cotesia flavipes na técnica de liberação por espalhamento de pupas no canavial. VI Workshop Agroenergia, Ribeirão Preto, São Paulo, Brasil, ISBN 978-85-85564-24-7.
Bittencourt MAL, Berti Filho E (2004) Exigências térmicas para o desenvolvimento de Palmistichus elaeisis (Hyme-noptera: Eulophidae) em pupas de cinco espécies de lepidópteros. Iheringia Sér. Zool. 94: 321-323.
Botelho PSM, Macedo N (2002) Cotesia flavipes para o controle de Diatraea saccharalis. Em Parra JRP, Botelho PSM, Corrêa-Ferreira BS, Bento JMS (Eds.) Controle Biológico no Brasil: Parasitoides e Predadores. Manole. São Paulo, Brasil. p. 409-425.
Carvalho JS, Viel SR, Vacari AM, Proença DC, Pereira LCG, Bortoli SA (2007) Parâmetro para controle de qualidade de Cotesia flavipes (Cameron, 1891) (Hymenoptera: Braconidae). Anais VIII Cong. de Ecologia do Brasil. Sociedade de Ecologia do Brasil. Caxambu, MG, Brasil.
Dinardo-Miranda LL, Anjos IA, Costa VP, Fracasso JV (2012). Resistance of sugarcane cultivars to Diatraea saccharalis. Pesq. Agropec. Bras. 47: 1-7.
Dinardo-Miranda LL, Fracasso JV, Perecin D (2011) Variabilidade espacial de populações de Diatraea saccharalis em canaviais e sugestão de método de amostragem. Bragantia 70: 577-585.
Firake DM, Khan MA (2014) Alternating temperatures affect the performance of Trichogramma species. J. Insect Sci. 14: 1-14.
Furlong, MJ, Zalucki, MP (2017) Climate change and biological control: the consequences of increasing temperatures on host-parasitoid interactions. Curr. Opin. Insect Sci. 20: 39-44.
Glaeser DF, Oliveira HN, Moreira SC, Rodas PL (2016) Impacto das oscilações de temperatura sobre o parasitoide pupal Trichospilus diatraeae (Hymenoptera: Eulophidae). Cad. Agroecol. 11: 1-8.
Hance T, Baaren JV, Vernon P, Boivin G (2007) Impact of extreme temperatures on parasitoids in a climate change perspective. Annu. Rev. Entomol. 52: 107-126.
Hensley SD, Hammond AH (1968) Laboratory techniques for rearing the sugar cane borer on an artificial diet. J. Econ. Entomol. 61: 1742-1743.
IBGE (2019) Levantamento Sistemático da Produção Agrícola. 25: 127. Instituto Brasileiro de Geografia e Estatística. Rio de Janeiro, Brasil. https://sidra.ibge.gov.br/home/lspa/brasil
Oliveira HN, Colombi CA, Pratissoli D, Pedruzzi EP, Dalvi LP (2005) Capacidade de parasitismo de Trichogramma exiguum Pinto & Platner, 1978 (Hymenoptera: Trichogrammatidae) criado em dois hospedeiros por diversas gerações. Ciênc. Agrotec. 29: 284-288.
Oliveira HN, Glaeser DF, Bellon PP (2012a) Recomendações para Obter um Controle Biológico Eficaz da Broca-da-Cana de Açúcar. Comunicado Técnico 181. Embrapa Agropecuária Oeste. Dourados, Brasil. ISSN 1679-0472.
Oliveira HN, Bellon PP, Santana DRS (2012b) Critérios para determinação da idade ideal de liberação de Cotesia flavipes. Cad. Agroecol. 7: 1-4.
Parra JRP (2007) Técnicas de Criação de Insetos para Pro-gramas de Controle Biológico. 6ª ed. USP/ESALQ. Piracicaba, Brasil, pp.134.
Pereira FF, Zanuncio JC, Oliveira HN, Grance ELV, Pastori PL, Gava-Oliveira MD (2011) Thermal requirements and estimate number of generations of Palmistichus elaeisis (Hyme-'noptera: Eulophidae) in different Eucalyptus plantations regions. Braz. J. Biol. 71: 431-436.
Pinto AS, Garcia JF, Botelho PSM (2006) Controle biológico de pragas da cana-de-açúcar. Em Pinto AS, Nava DE, Rossi MM, Malerbo Souza DT Controle Biológico de Pragas na Prática. Piracicaba, SP, Brasil. pp. 287.
Potting, RPJ, Vet, LEM, Overholt, WA (1997) Geographic variation in host behavior and reproductive success in the stemborer parasitoid C. flavipes (Hymenoptera: Braconidae). Bull. Entomol. Res. 87: 515-524.
Pratissoli D, Thuler RT, Silva AF, Dalvi LP, Tamanhoni T (2006) Características biológicas de linhagens de Trichogramma pretiosum, criados em ovos de Tuta absoluta, em diferentes temperaturas. Científica 34: 210-216.
Rossato JAS, Costa GHG, Madaleno LL, Mutton MJR, Higley LG, Fernandes A (2013) Characterization and impact of the sugarcane borer on sugarcane yield and quality. Agron. J. 105: 643-648.
Selvaraj S, Ganeshamoorthi P, Pandiaraj T (2013) Potential impacts of recent climate change on biological control agents in agro-ecosystem: A review. Int. J. Biodivers. Conserv. 5: 845-852.
Tylianakis JM, Binzer A (2014) Effects of global environmental changes on parasitoid-host food webs and biological control. Biol. Control. 75: 77-86.
Vacari AM, Genovez GS, Laurentis VL, Bortoli SA (2012) Fonte proteica na criação de Diatraea saccharalis e seu reflexo na produção e no controle de qualidade de Cotesia flavipes. Bragantia 71: 355-361.
Autor notes
prih_davis@hotmail.com