Resumen: Recientemente, la industria alimentaria ha incrementado el interés de sustituir el uso de colorantes sintéticos por pigmentos naturales como las betalaínas, las cuales se utilizan principalmente por el color rojo que imparten. Además, las betalaínas son sustancias que poseen actividad antioxidante y anti degenerativa frente a diversas enfermedades. Son pigmentos nitrogenados solubles en agua, derivados del ácido betalámico: betacianinas (rojo-violeta) y betaxantinas (amarillo-naranja). Sin embargo, el uso de dichos pigmentos se ha visto restringido por su inestabilidad a diversos factores, tales como temperatura, pH, luz, actividad de agua y enzimática, así como a la presencia de oxígeno y/o metales. El objetivo de esta revisión fue sintetizar los avances sobre la estabilidad que presentan las betalaínas frente a diversos factores fisicoquímicos.
Palabras clave:BetalaínasBetalaínas,EncapsulaciónEncapsulación,EstabilidadEstabilidad,PigmentosPigmentos.
Abstract: Recently, the food industry has increased the interest to replace the use of synthetic dyes with natural pigments such as betalains, which are mainly used for the red color they impart. In addition, betalains are substances that have antioxidant and anti-degenerative activity against various diseases. They are water-soluble nitrogenated pigments, betalamic acid derivatives: betacyanines (red-violet) and betaxanthines (yellow-orange). However, the use of said pigments has been restricted due to its instability to various factors, such as temperature, pH, light, water and enzymatic activity, as well as the presence of oxygen and / or metals. The aim of this review was to synthesize the advances on the stability of betalains in the presence of diverse physicochemical factors.
Resumo: Recentemente, a indústria alimentícia aumentou o interesse em substituir o uso de corantes sintéticos por pigmentos naturais, como as betalaínas, que são utilizados principalmente para a cor vermelha que eles transmitem. Além disso, betalínas são substâncias que têm atividade antioxidante e anti-degenerativa contra várias doenças. Elles são pigmentos nitrogenados hidrossolúveis, derivados do ácido betalâmico: betacianinas (vermelho-violeta) e betaxantinas (amarelo-laranja). No entanto, o uso dos referidos pigmentos tem sido restringido por sua instabilidade a vários fatores, tais como temperatura, pH, luz, água e actividade enzimática, bem como a presença de oxigênio e / ou metais. O objetivo desta revisão é sintetizar os avanços na estabilidade que se apresentam diante de diversos fatores físico-químicos.
Artículos
ESTRUCTURA Y ESTABILIDAD DE LAS BETALAÍNAS
STRUCTURE AND STABILITY OF BETALAINES
ESTRUTURA E ESTABILIDADE DAS BETALAÍNAS
Asociación Interciencia
Recepción: 21 Enero 2019
Corregido: 31 Mayo 2019
Aprobación: 03 Junio 2019
Las betalaínas son los principales pigmentos de la raíz del betabel o remolacha (Beta vulgaris sp.) y de otras especies, como la espinaca malabar (Basella sp.), el amaranto (Amaranthus sp.), la pitaya (Cereus, Hylocereus y Selenicereus spp.) y la pera del cactus (Opuntia sp.) comúnmente conocida como tuna (Stintzing et al., 2003; García-Cruz et al., 2012; Kumar et al., 2014; Güneşer, 2016; Celli y Brooks, 2017;Shaaruddin et al., 2017; Ciriminna et al., 2018).
La raíz del betabel representa la principal fuente comercial de betalaínas concentrado o en polvo (Delgado-Vargas et al., 2000; Soriano-Santos et al., 2007; Rodriguez-Amaya, 2016). Dichos compuestos tienen aplicación como colorantes naturales (Herbach et al., 2005, 2006b) en la industria farmacéutica, cosmética y alimentaria (Mereddy et al., 2017). La betanina es el compuesto responsable del color rojo autorizado y clasificado como colorante natural de los alimentos (Esatbeyoglu et al., 2015), bajo el código E162 por la Unión Europea (UE) (Kapadia y Subba, 2013; Carocho et al., 2015;EFSA-ANS, 2015) y por la Administración de Drogas y Alimentos de EUA (FDA) designado con el numero 73.40 (Martínez et al., 2006; Rodriguez-Amaya, 2016). En las últimas décadas se han estudiado las propiedades saludables de estos compuestos, entre las que se pueden destacar su actividad antioxidante, antidiabética, antiinflamatoria y anticancerígena (Kanner et al., 2001; Kapadia et al., 2003; Gandía-Herrero y García-Carmona, 2013; Gandía-Herrero et al., 2013,2016; Kapadia y Subba, 2013;Mikołajczyk-Bator y Pawlak, 2016). Las betalaínas por naturaleza son inestables en presencia de luz (von Elbe et al., 1974), temperatura (Huang y von Elbe, 1985), pH (Penfield y Campbell, 1990), actividad enzimática (Slimen et al., 2017), y presencia o ausencia de oxígeno y metales (Tabla I) (von Elbe y Schwartz, 1996; Azeredo, 2009; Castillo-Garrido, 2013). Debido a la baja estabilidad, que conlleva la pérdida de sus propiedades saludables, se ha restringido su uso como ingredientes en la formulación de alimentos (Serris y Biliaderis, 2001; Herbach et al., 2006a; Stintzing et al., 2006). Por consiguiente, resalta la importancia de estudiar y comprender cómo los factores intrínsecos de un alimento, o bien las condiciones de empaque y/o almacenamiento benefician o afectan la estabilidad de las betalaínas. El objetivo del presente trabajo fue establecer el estado del arte de cómo los factores fisicoquímicos alteran la estabilidad de las betalaínas.
FACTORES QUE INFLUYEN EN LA ESTABILIDAD DE LAS BETALAÍNAS

Adaptado de Herbach et al. (2006) y Esatbeyoglu et al. (2015).
Se realizó una búsqueda de artículos que citaban las palabras clave de esta revisión: ‘betalaínas’, ‘pigmentos’, ‘estabilidad’ y ‘encapsulación’ en las bases de datos CONRYCIT (Consorcio Nacional de Recursos de Información Científica y Tecnológica), NCBI (National Center for Biotechnology Information) y Google Académico. Se analizó cada uno de los artículos encontrados en dichas bases de datos y se elaboró una síntesis de la informacion para presentar el estado del arte.
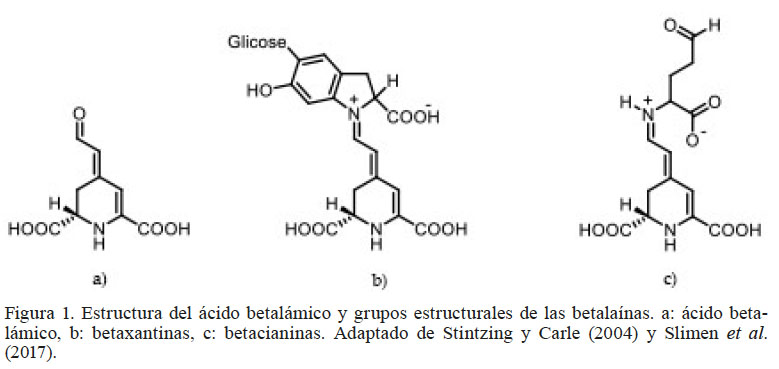
Figura 1.
Estructura del ácido betalámico y grupos estructurales de las betalaínas. a: ácido betalámico, b: betaxantinas, c: betacianinas. Adaptado de Stintzing y Carle (2004) y Slimen et al. (2017).
Stintzing y Carle (2004) y Slimen et al. (2017).
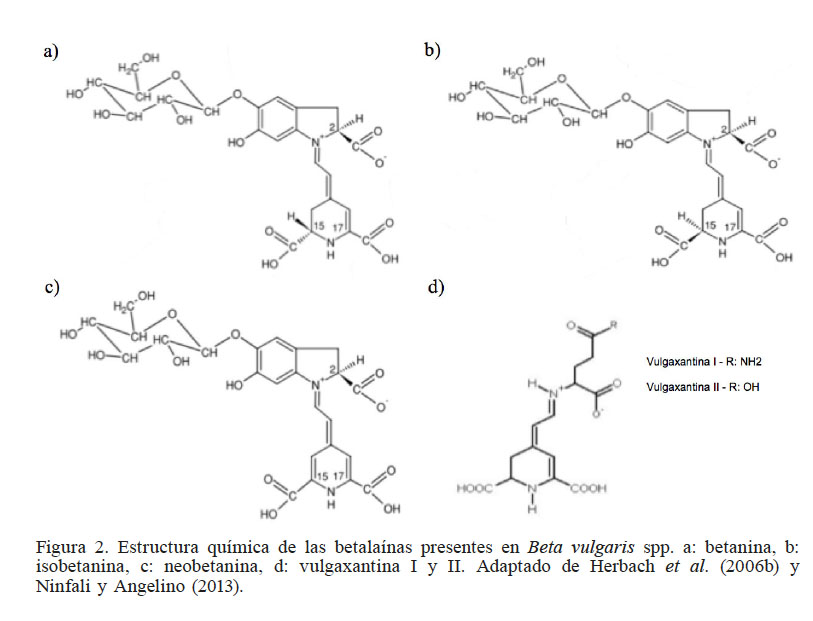
Figura 2
Estructura química de las betalaínas presentes en Beta vulgaris spp. a: betanina, b: isobetanina, c: neobetanina, d: vulgaxantina I y II. Adaptado de Herbach et al. (2006b) y Ninfali y Angelino (2013).
Herbach et al. (2006b) y Ninfali y Angelino (2013).
La degradación de las betalaínas depende de la temperatura y sigue una cinética de reacción de primer orden, dependiente del pH (Huang y von Elbe, 1985, 1987; Castellar et al., 2003;Azeredo, 2005,2009). El factor más importante en la estabilidad de las betalaínas durante el procesamiento y almacenamiento de alimentos es la temperatura (Huang y von Elbe, 1985; Herbach et al., 2005; Azeredo, 2009; Reshmi et al., 2012). Durante los procesos térmicos las betalaínas pueden degradarse por isomerización, desglicosilación, hidrolisis, deshidrogenación y descarboxilación (von Elbe et al., 1974;Huang y von Elbe, 1985; von Elbe y Schwartz, 1996;Herbach et al., 2004b, 2005, 2007; Azeredo, 2009; Castillo-Garrido, 2013; Ruiz-Gutiérrez et al., 2014). La aparición de pardeamiento lleva a una reducción de color gradual, de rojo característico de estos pigmentos hasta llegar a color marrón claro (Huang y von Elbe, 1985). Se ha demostrado que las betalaínas tienen mayor estabilidad a temperaturas bajas (Herbach et al., 2005), siendo 4°C la temperatura que permite mantener la estabilidad de los compuestos betalámicos, comparado con temperaturas más altas (Herbach et al., 2005;González-Sánchez et al., 2010; Janiszewska, 2014). El ácido betalámico (amarillo brillante) y ciclodopa-5-O-glucosido (sin color) son productos resultantes de la descarboxilación de betanina durante tratamientos térmicos (Huang y von Elbe, 1985, 1987). Cuando la betanina sufre deshidrogenación se genera otro compuesto betalámico, la neobetanina, observándose un cambio de color rojo a amarillo (Reshmi et al., 2012). Así mismo, el proceso térmico del jugo de betabel causa la degradación de las betalaínas dando como resultado diferentes tipos de betacianinas mono, di y tricarboxiladas (Wybraniec, 2005). Cabe mencionar que la adición de ácido cítrico es capaz de proteger la estabilidad de las betalaínas ante factores como temperatura, luz y oxígeno (Hernández-Rodríguez y Salazar-Tjerino, 2017).
Las betalaínas son estables en soluciones en un rango de pH de 3,0 a 6,0. Por fuera de este rango los compuestos presentan una degradación rápida que va acompañada de una perdida de color (Delgado-Vargas et al., 2000; Castellar et al., 2003; Stintzing et al., 2005; Gandía-Herrero et al., 2007,2013; Herbach et al., 2007; Gandía-Herrero y García-Carmona, 2013). Bajo condiciones alcalinas la betanina se degrada a ácido betalámico y ciclodopa-5-O-glucosido (von Elbe y Schwartz, 1996). Las betacianinas se consideran con mayor estabilidad a pH ácido, mientras que las betaxantinas son más resistentes en medios neutros (Reshmi et al., 2012). El pH ideal para la estabilidad de los pigmentos del betabel en condiciones anaerobias es de 4,0-5,0 pero si las betalaínas se encuentran en un medio con presencia de oxígeno el pH óptimo sería 5,5-5,8 (Huang y von Elbe, 1985; Herbach et al., 2006b).
La estabilidad de las betalaínas es afectada por luz; la degradación de color es causada por la absorción de ondas UV (Manchali et al., 2013; Janiszewska, 2014). Sin embargo, Herbach et al. (2004) señalan que la degradación de los pigmentos por la luz depende de la presencia de oxígeno, puesto que ésta no se da en condiciones anaerobias. Este tipo de degradación se puede evitar mediante la utilización de ácido ascórbico (Herbach et al., 2004a, 2004b,2005). La presencia de luz y de oxígeno tienen un efecto sinérgico. La luz causa una degradación de color del 15,6% y el oxígeno 14,6%, mientras que la combinación de ambos causa una degradación del 28,6% (von Elbe et al., 1974). Manchali et al. (2013) mencionan que no todas las fuentes de luz generan la degradación de las betalaínas, sino que la luz de diferentes longitudes de onda puede causar un efecto aditivo de color en las betalaínas. De tal forma, Shin et al. (2003) sugieren que la luz azul en combinación con la luz infrarroja inducen a una mayor acumulación de betacianinas.
Oxígeno
Las betalaínas reaccionan con el oxígeno y cuando son almacenadas en presencia de oxígeno sufren una degradación de color (von Elbe et al., 1974; Herbach et al., 2006b,2006c). Sin embargo, se ha demostrado que niveles bajos de oxígeno favorecen la recuperación del pigmento después de sufrir dicha degradación (Huang y von Elbe, 1987). La eliminación de oxígeno disuelto aumenta la estabilidad de los compuestos betalámicos (von Elbe et al., 1974). El oxígeno juega un papel crucial en la degradación de las betalaínas, y más aún si dichos compuestos se encuentran almacenados por encima de los 4ºC y en presencia de luz (von Elbe et al., 1974;Schwartz et al., 1983;Schwartz y von Elbe, 1983; Herbach et al., 2004b; Azeredo, 2009; Manchali et al., 2013).
Los metales son otro factor a considerar en la degradación de los pigmentos betalámicos. Cobre, hierro, aluminio y estaño afectan la estabilidad de la betanina acelerando la pérdida de su color (Pasch y von Elbe, 1979;Attoe y Vol Elbe, 1981,1984; von Elbe y Attoe, 1985). Para reducir la degradación de color en los pigmentos por iones metálicos, algunos autores recomiendan utilizar ácido cítrico como agente quelante (Stintzing y Carle, 2007,2008;Hernández-Rodríguez y Salazar-Tijerino, 2017).
Se ha observado una mayor estabilidad de las betalaínas cuando la actividad de agua (aw) es <0,63. La aw afecta la estabilidad de los compuestos betalámicos puesto que el agua favorece la ruptura del enlace aldimina del compuesto (Herbach et al., 2006a, b, c). Diversos autores reportan que la estabilidad de estos compuestos aumenta cuando se aplican métodos para reducir el contenido de agua, tales como liofilización y secado por atomización, entre otros (Castellar et al., 2003;Herbach et al., 2004b,2005, 2006a,b, c;Pitalua et al., 2010; Ruiz-Gutiérrez et al., 2014).
Otra causa de inestabilidad de los compuestos betalámicos es la inactivación inadecuada de enzimas tales como las glucosidasas, polifenoloxidasas y peroxidasas (Herbach et al., 2006b;Castillo-Garrido, 2013). Las glucosidasas afectan la estabilidad de las betalaínas por la formación de agliconas, las peroxidasas forman radicales y las polifenoloxidasas oxidan principalmente los compuestos fenólicos sin color, todo esto dando como resultado la inactivación de las betalaínas y por consiguiente la decoloración de los compuestos betalámicos (von Elbe y Schwartz, 1996; Stintzing y Carle, 2008; Castillo, 2013).
Se ha demostrado que la encapsulación de betalaínas y su aplicación en diferentes matrices comestibles pueden aumentar la estabilidad de estos compuestos (Tabla II), y por ende conservan las actividades antioxidantes y antirradicales (Gandía-Herrero et al., 2009;López et al., 2012). La microencapsulación se ha utilizado para proteger a los compuestos fitoquímicos (colorantes, saborizantes, antioxidantes, bactericidas, vitaminas, aceites esenciales, etc.) contenidos en alimentos (López et al., 2012; Vergara, 2013;Xue et al., 2013, Luna-Guevara et al., 2016). Es un proceso mediante el cual las sustancias bioactivas se recubren con una película delgada de un material protector denominado agente encapsulante (Parra-Huertas, 2011; Arrazola et al., 2014; Flores-Belmont y Jiménez-Munguía, 2013; Gallo-Nunura y Cevallos-Vera, 2014; Manjunatha y Raju, 2015;Diaz et al., 2017), y tienen así mayor aplicación en la industria alimentaria, ya que aumentan su estabilidad, incrementan la vida útil y son más fáciles de manejar (Azeredo, 2005, 2009;Azeredo et al., 2007; Azeredo et al., 2009; Gandía-Herrero et al., 2007; Pitalua et al., 2010; López et al., 2012; Janiszewska, 2014; Ibraheem et al., 2015; Diaz et al., 2017). Existe una gran variedad de técnicas para encapsular los alimentos y algunos autores las han clasificado como químicas y físicas o mecánicas (Guevara-Breton y Jimenez-Munguia, 2008). Entre los métodos químicos se encuentran la polimerización interfacial, gelificación iónica, cristalización, coacervación compleja, incompatibilidad polimérica y atrapamiento de liposomas (Pedroza-Islas, 2002; Azeredo, 2005,2009; Flores-Belmont y Jiménez-Munguía, 2013). Dentro de las técnicas físicas o mecánicas aparecen el secado en lecho fluidizado, extrusión, liofilización y secado por atomización (Madene et al., 2006), siendo estas últimas las más utilizadas (Azeredo, 2005; Azeredo et al., 2009;Oberoi y Sogi, 2015; Araujo-Diaz et al., 2017;Shaaruddin et al., 2017; Shishir y Chen, 2017).
AGENTES ENCAPSULANTES Y CONDICIONES DE ENCAPSULACIÓN UTILIZADOS PARA ESTABILIZAR BETALAÍNAS
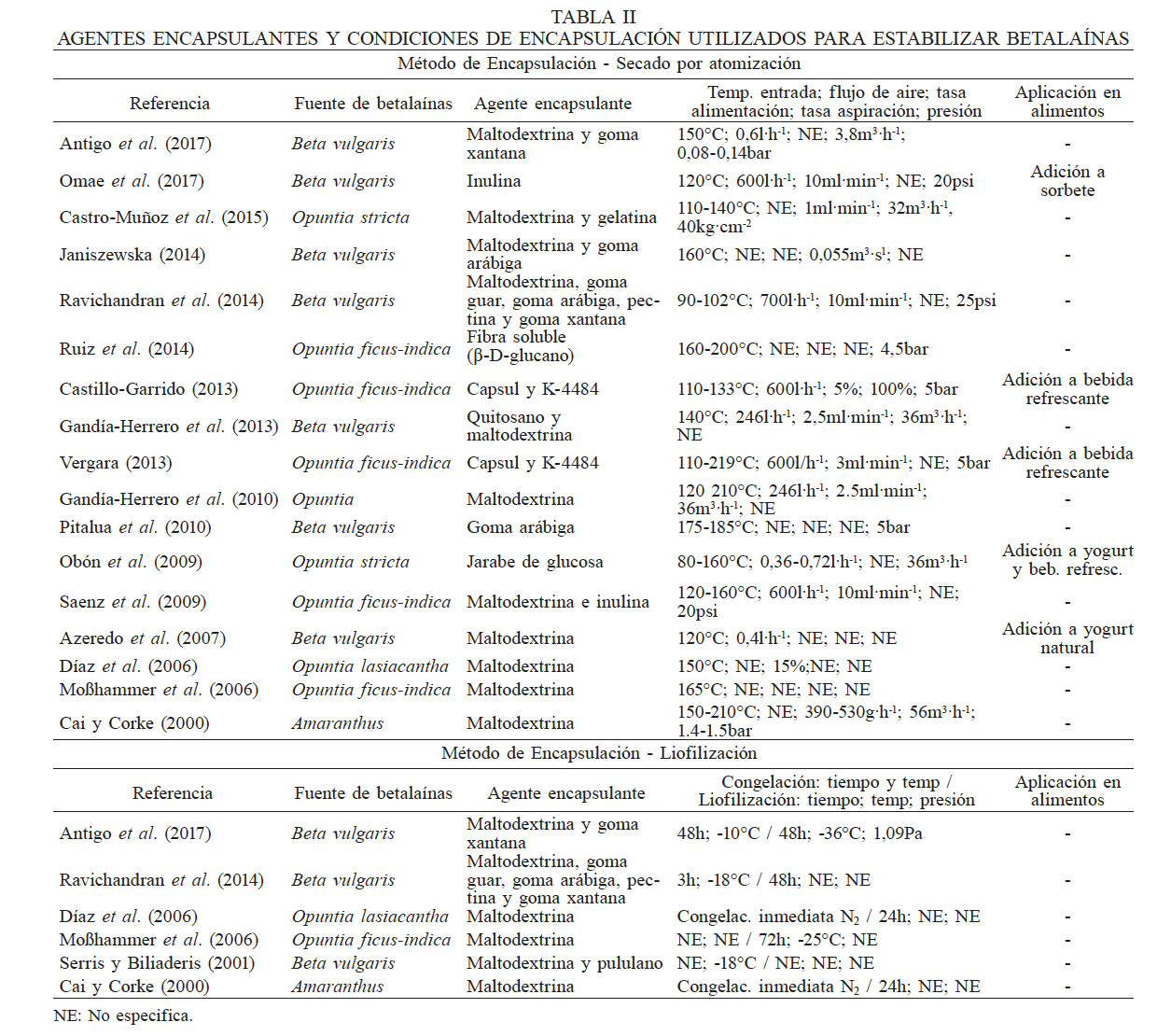
NE NE: No especifica.
Existen diferentes tipos de agentes encapsulantes (Sandoval-Peraza et al., 2016), también llamados acarreadores, entre los que se encuentran carbohidratos, lípidos, proteínas y polímeros de grado alimenticio (Guevara-Breton y Jimenez-Munguia, 2008; Gallo-Nunura y Cevallos-Vera, 2014; Ibraheem et al., 2015; Antigo et al., 2017). En el grupo de los carbohidratos se incluyen los almidones, alginatos, carrageninas, goma arábiga, goma guar, goma xantana, sacarosa, glucosa, maltodextrina, inulina, jarabe de maíz, pectina, carboximetil celulosa y quitosano, entre otros (Barbosa et al., 2005; Pitalua et al., 2010;Ravichandran et al., 2014;Manjunatha y Raju, 2015;Diaz et al., 2017;Shishir y Chen, 2017; Slimen et al., 2017). Entre los lípidos se ubican las ceras de abeja, carnauba y candelilla, diestearato de glicerol y grasas naturales y modificadas (Pedroza-Islas et al., 1999;Sandoval et al., 2016). En las proteínas se puede destacar como agentes encapsulantes a la gelatina, caseínas como el caseinato de sodio, proteínas del suero de soja y proteínas de trigo (Gandía-Herrero y García-Carmona, 2013). En los polimeros de grado alimenticio se destacan el polipropileno, polivinilacetato, poliestireno y polibutadieno, entre otros (Guevara-Breton y Jimenez-Munguia, 2008). Cada grupo de materiales acarreadores tienen ventajas y desventajas, por lo que los recubrimientos en su mayoria son formulaciones compuestas de todos los anteriores (Tabla II) (Madene et al., 2006).
Cai y Corke (2000) y Gandía-Herrero et al. (2010, 2013) reportan que la estabilidad de las betalaínas aumenta cuando son encapsuladas (secado por atomización) con maltodextrina, manteniendo la coloración rojo-púrpura de los polvos. Una investigación realizada por Castro-Muñoz et al. (2015) sugiere que la mezcla de maltodextrina con gelatina (75:25) es una opción viable para la encapsulación de compuestos alimentarios como las betalaínas. Azeredo et al. (2007) indican que el uso de diferentes proporciones de maltodextrina en la encapsulación mediante el secado por atomización de betacianinas aumenta su estabilidad.
Por su parte, Ravichandran et al. (2014) mencionan que la encapsulación de las betalaínas secado por atomización con diferentes mezclas (maltodextrina con pectina, con goma arábiga y con goma xantana) incrementan la estabilidad de las betalaínas en comparación con el uso exclusivo de maltodextrina (6, 6 y 21% respectivamente). Así mismo el estudio señala que las betalaínas encapsuladas por liofilización con goma xantana aumentan hasta un 65% del contenido de betalaínas respecto al control con maltodextrina únicamente. De igual forma, Moßhammer et al. (2006) y Antigo et al. (2017) señalan que la liofilización de extracto de betabel mezclado con maltodextrina y goma xantana presenta una mayor estabilidad en contenido de betalaínas, en relación al secado por pulverización.
Por otro lado, se ha demostrado que la estabilidad de las betalaínas aumenta cuando se lleva a cabo el secado por atomización utilizando como agente encapsulante la goma arábiga en relación con la maltodextrina, debido a su menor higroscopicidad (Janiszewska, 2014). También, se ha determinado que el uso de inulina (Omae et al., 2017), goma guar (Ravichandran et al., 2014), quitosano (Gandía-Herrero et al., 2013), fibra soluble β-D-glucano (Ruiz-Gutiérrez et al., 2014), jarabe de glucosa (Obón et al., 2009), cápsula y K4484 (Castillo-Garrido, 2013;Vergara, 2013) como agentes encapsulantes en secado por atomización, aumenta la estabilidad de betalaínas en contraste con el extracto sin agentes. Estos métodos y agentes de encapsulación han sido utilizados para diversas fuentes de betalaínas, tales como Beta vulgaris, Opuntia (ficus, lasiacantha, stricta, etc) y Amaranthus, entre otras (Tabla II).
La aplicación comercial de los pigmentos del betabel (betalaínas) esta limitada por su inestabilidad; sin embargo, diferentes técnicas de encapsulación han resultado ser eficaces para aumentar su estabilidad. Los factores más importantes a considerar durante la encapsulación de los compuestos betalámicos son el proceso empleado (liofilización, extrusión, secado por atomización, etc.), la temperatura y el agente encapsulante, econtrándose resultados óptimos cuando se emplean mezclas de agentes encapsulantes tales como maltodextrina y goma xantana, y se emplea liofilización. Por lo anterior, los métodos de encapsulación representan una alternativa para conservar las propiedades fisicoquímicas de las betalaínas, de tal forma que estos compuestos puedan utilizarse para la elaboración de una gran variedad productos alimenticios. La demanda de alimentos formulados con ingredientes naturales ha aumentado en los ultimos años, por lo que el uso de betalaínas como colorantes naturales es una alternativa prometedora, ya que ademas de impartir color, son compuestos con excelentes propiedades saludables. No obstante, hace falta investigar sobre su estabilidad estructural y ampliar el panorama de las ventajas y/o beneficios que pueden aportar a la salud de quien las consume.
amchavez@uach.mx
FACTORES QUE INFLUYEN EN LA ESTABILIDAD DE LAS BETALAÍNAS

Adaptado de Herbach et al. (2006) y Esatbeyoglu et al. (2015).

Figura 1.
Estructura del ácido betalámico y grupos estructurales de las betalaínas. a: ácido betalámico, b: betaxantinas, c: betacianinas. Adaptado de Stintzing y Carle (2004) y Slimen et al. (2017).
Stintzing y Carle (2004) y Slimen et al. (2017).

Figura 2
Estructura química de las betalaínas presentes en Beta vulgaris spp. a: betanina, b: isobetanina, c: neobetanina, d: vulgaxantina I y II. Adaptado de Herbach et al. (2006b) y Ninfali y Angelino (2013).
Herbach et al. (2006b) y Ninfali y Angelino (2013).
AGENTES ENCAPSULANTES Y CONDICIONES DE ENCAPSULACIÓN UTILIZADOS PARA ESTABILIZAR BETALAÍNAS

NE NE: No especifica.
