ARTICULO
HONGOS Y LEVADURAS: FÁBRICAS DE LIPASAS
FUNGI AND YEASTS: LIPASE FACTORIES
HONGOS Y LEVADURAS: FÁBRICAS DE LIPASAS
Interciencia, vol. 44, núm. 7, pp. 378-385, 2019
Asociación Interciencia
Recepción: 01 Marzo 2019
Corregido: 12 Julio 2019
Aprobación: 15 Julio 2019
Financiamiento
Fuente: donativos parciales de la Convocatoria de Apoyo a Proyectos de Investigación Científica, Aplicada, Desarrollo Tecnológico e Innovación 2016, 2017, 2018 del Tecnológico Nacional de México, proyectos Nos. 5781.16-P, 6131.17-P y 6525.18-P; los donativos parciales al Laboratorio Nacional SEDEAM del Instituto Tecnológico de Morelia por el apoyo académico de los investigadores y estudiantes en tesis aplicadas a la empresa; asi como la participación del Consejo Nacional de Ciencia y Tecnología (CONACyT) a través del soporte financiero otorgado por la Beca 253782.
Nº de contrato: 5781.16-P, 6131.17-P y 6525.18-P;
Beneficiario: Juan Carlos González-Hernández
Descripción del financiamiento: donativos parciales
Resumen: Las lipasas son enzimas capaces de catalizar reacciones de hidrólisis de triglicéridos; son usadas en numerosos procesos dentro de la industria alimenticia, energética, farmacéutica, etc. Ante la necesidad de cumplir con la demanda comercial e industrial actual de este tipo de enzimas en diversos procesos, se han desarrollado diferentes estrategias de estudio de las mismas y sus aplicaciones. Debido a que la mayoría de las especies bacterianas usadas para la producción de lipasas son patógenas, se han realizado esfuerzos para encontrar sistemas alternativos que sean seguros para los diversos procesos en los que se ven envueltas este tipo de enzimas. Así, las lipasas provenientes de hongos y levaduras han adquirido un alto foco de atención. En este trabajo se pretende mencionar las características generales y de producción de lipasas de diversos microorganismos fúngicos que han sido estudiados últimamente, a fin de determinar dichas alternativas para los procesos biotecnológicos industriales que demandan este tipo de enzimas.
Palabras clave: Hongos, Levaduras, Lipasas .
Abstract: Lipases are enzymes with the capacity of catalyzing triglyceride hydrolysis reactions; they are used in many processes in the food industry, energy production, pharmaceutical catalysis, etc. Given the need to satisfy the current commercial and industrial demand of lipases, different strategies have been developed to study them and their applications. Because most of the bacterial species used for the production of lipases are pathogenic, efforts have been made to find safe alternative systems that could be used the different processes in which lipases are involved. Thus, lipases from fungi and yeasts have won high attention. In this review we intend to cover the general and production characteristics of currently utilized lipases from various fungal microorganisms, in order to determine the existing alternatives for the industrial biotechnological processes that demand this type of enzymes.
Resumo: As lipases são enzimas capazes de catalisar reações de hidrólise de triglicérides; são usadas em numerosos processos dentro da indústria alimentícia, energética, farmacêutica, etc. Diante da necessidade de cumprir com a demanda comercial e industrial atual de este tipo de enzimas em diversos processos, têm sido desenvolvidas diferentes estratégias de estudo de estas e de suas aplicações. Devido à maioria das espécies bacterianas, usadas para a produção de lipase, serem patógenas, têm sido realizados esforços para encontrar sistemas alternativos seguros para os diversos processos em que estão envolvidas este tipo de enzimas. Assim, as lipases provenientes de fungos e leveduras têm adquirido alto foco de atenção. Em este trabalho pretende-se mencionar as características gerais e de produção de lipases, provenientes de diversos microrganismos fúngicos, que foram estudados atualmente, com a finalidade de determinar estas alternativas para os processos biotecnológicos industriais que demandam este tipo de enzimas.
Introducción
Las lipasas son hidrolasas de serina definidas como triacilglicerol acilhidrolasas (E.C. 3.1.1.3), capaces de hidrolizar ésteres carboxílicos de acilglicerol de cadena larga, con cadenas mayores a 10 átomos de carbono, lo que las distingue de las estereasas (Casas-Godoy et al., 2012). La variedad de reacciones que catalizan las ha hecho candidatas ideales para diversas aplicaciones industriales. Después de las proteasas y las amilasas, las lipasas son consideradas como el tercer grupo en volumen de ventas, con un valor de billones de dólares anuales (Kempka et al., 2008). A pesar de que las lipasas son producidas por la mayoría de los organismos vivos, cobra relevancia el uso de microorganismos para su síntesis por las ventajas que presentan sus enzimas: catalizan una gran variedad de reacciones, tienen altos rendimientos, relativa facilidad de manipulación genética, son estructuralmente estables en solventes orgánicos, son independientes de cofactores, catalizan reacciones utilizando una amplia variedad de sustratos y tienen una alta enantioselectividad (Tan et al., 2015). En esta revisión se mencionarán los avances que se han tenido en los últimos años, así como las tendencias en el estudio de las lipasas fúngicas, las que se posicionan por encima del uso de lipasas bacterianas por ser reconocidas como seguras. En primera instancia se describirán las características generales de las lipasas y se mencionará la importancia de las mismas en diversas áreas industriales. Posteriormente, se mencionarán las lipasas conocidas y estudiadas de origen fúngico, a fin de conocer sus propiedades y características generales. Finalmente, se discutirán las últimas tendencias del estudio y aprovechamiento de las lipasas de origen fúngico.
Lipasas: Panorama General
La característica diferencial de las lipasas con respecto a otras enzimas que también pueden hidrolizar ésteres, como las esterasas, es la necesidad de una interfase orgánico-acuosa para dicha función catalítica (Hasan et al., 2009). Las lipasas catalizan una amplia variedad de reacciones, como la hidrólisis parcial o total de triacilglicéridos y reacciones de síntesis que se clasifican en dos grandes grupos: reacciones de esterificación y reacciones de transesterificación. Las lipasas tienen diferentes tipos de selectividad: a) quimioselectividad, b) regioselectividad y c) enantioselectividad (Colla et al., 2010).
Las lipasas tienen un plegamiento α/β característico de las enzimas hidrolíticas (Jaeger et al., 1999). La triada catalítica se encuentra altamente conservada, conformada por tres aminoácidos: serina, aspartato o glutamato e histidina (Brady et al., 1990). La serina forma parte del motivo consenso GX1SX2G. Otra característica importante en la estructura de la lipasa es la presencia de una brecha oxianiónica, encargada de estabilizar el intermediario de la reacción mediante puentes de hidrógeno (Pleiss et al., 2000). Actualmente la base de datos LED (Lipase Engineering Database;http://www.led.uni-stuttgart.de; Fischer y Pleiss, 2003) clasifica a las lipasas en base a la conformación de su oxianión en tres grandes grupos: GGGX, GX y Y; además, se agrupan en 15 superfamilias y 32 familias homólogas.
Importancia de las lipasas
Las lipasas realizan diferentes funciones fisiológicas. En eucariotas, son componentes clave del metabolismo de lípidos y lipoproteínas, por lo que son producidas en el sistema digestivo (Reis et al., 2009). Los campos de aplicación de las lipasas han sido en la industria oleoquímica, manufactura de detergentes y en la industria alimenticia, principalmente. Son usadas como aditivos alimentarios en la modificación del sabor, síntesis de ésteres con actividad antioxidante, hidrólisis de grasas para la fabricación de detergentes, tratamiento de aguas residuales para la degradación y remoción de sustratos grasos, eliminación de lípidos y aceites en la industria cosmética y farmacéutica (Burkert et al., 2004). Su propiedad de enantioselectividad ha permitido aumentar su demanda para métodos eficientes para la síntesis industrial de enantiómeros puros de antiinflamatorios como el ibuprofeno (Sharma et al., 2001). Siendo usados como biosensores, permiten la liberación de glicerol que puede ser medido para diagnosticar algunos padecimientos de pacientes con problemas cardiovasculares y para determinar los niveles de triglicéridos a partir de la hidrólisis de los mismos (Verma et al., 2012). Las lipasas han sido utilizadas como primer paso en la descomposición de lípidos de desperdicios de comida, para la producción de biometano (Meng et al., 2015). Además, se ha propuesto su uso como biocatalizadores en la producción de biodiesel, cuya síntesis catalítica actual por transesterificación genera altos niveles de agua alcalinizada (Aguieiras et al., 2015).
Lipasas de origen fúngico
Los microorganismos con una alta capacidad para producir lipasas pueden ser encontrados en diferentes hábitats, principalmente en desechos o residuos de aceites vegetales empleados en la elaboración de frituras, industrias de productos lácteos, suelos contaminados con aceites y alimentos deteriorados. La producción de lipasas depende de factores ambientales, como temperatura o pH, así como de la composición del medio de fermentación: fuente de carbono mixta (compuesta por un carbohidrato y un lípido), nitrógeno y concentración de sales inorgánicas, pudiendo estos factores alterar la reactividad de la enzima. Además, la síntesis de lipasas se ve favorecida en condiciones aerobias (Alarcón, 2008).
Lipasas de levaduras
Lipasas de Candida rugosa: C. rugosa es una levadura no esporogénica, unicelular y no patógena, reconocida como GRAS. Se han detectado más de siete genes que codifican para lipasas en C. rugosa, denominadas LIP1 a LIP7 (Ferrer et al., 2009). Cada gen de las lipasas de esta levadura codifica para una cadena de aminoácidos de 534 residuos, con masas moleculares de ~60kDa. LIP2 tiene una identidad de secuencia con LIP1 del 79,4%, y de 82,2% con LIP3. Las estructuras de las lipasas LIP1 y LIP3 son muy similares entre sí, con el sitio activo en las posiciones Ser209, His449 y Glu341 (Ferrer et al., 2001). En el caso específico de la enzima LIP2 purificada, el sitio activo está conformado por la triada Ser209, Glu341 e His449 (Mancheño et al., 2003). Las proteínas tienen hasta tres puntos de glicosilación, temperatura óptima entre 30 y 40°C y, pH óptimo cercano a la neutralidad (Brocca et al., 1998; Akoh et al., 2004).
Lipasas de Candida antarctica. C. antarctica sintetiza dos lipasas, denominadas CALA y CALB, de masas moleculares 45 y 33KDa, respectivamente. CALA tiene una tríada catalítica compuesta por Ser184, Asp334 e His366 (Ericsson et al., 2008); esta lipasa es capaz de catalizar la hidrólisis en la posición sn2 (Solymar et al., 2002; Ericsson et al., 2008). CALB, por su parte, tiene una tríada catalítica de Ser105, Asp187 e His224, en conformación abierta con entrada restringida al sitio activo (Uppenberg et al., 1994).
Lipasas de Yarrowia lipolytica. Y. lipolytica es una levadura no-convencional ascomiceta que posee 16 genes parálogos codificantes para lipasas, pero solo tres isoenzimas han sido caracterizadas: Lip2p, Lip7p y Lip8p. La expresión de los genes que codifican para lipasas en Y. lipolytica depende del ácido graso usado como fuente de carbono (Fickers et al., 2011). La lipasa Lip2p es una proteína madura de 301 aminoácidos, ligada a la pared celular que contiene dos puntos diferentes glucosilados de manosa (Jolivet et al., 2007); su sitio catalítico se caracteriza por una serina en la posición Ser162 de la secuencia GHSLG, y completan la triada catalítica los residuos Asp230 e His289. El pH óptimo de Lip2p se encuentra entre 6 y 7.5, mientras su temperatura óptima está entre 37 y 40°C. Las lipasas Lip7p y Lip8p se encuentran principalmente asociadas a pared celular y tienen un motivo del tipo GHSLG, con la serina catalítica en la posición Ser220 (Fickers et al., 2011).
Lipasas de hongos filamentosos
La primera estructura obtenida de una lipasa fúngica fue la de Rhizomucor miehei (antes Mucor miehei), expresada en Aspergillus oryzae, un polipéptido sencillo de 269 residuos de aminoácidos, con un sitio catalítico conformado por Ser144, His257 y Asp203, y la presencia de tres puentes disulfuro (Brady et al., 1990). A continuación se mencionan algunas características importantes de las lipasas y los organismos implicados en su síntesis de los géneros Aspergillus y Penicillium.
Lipasas de Aspergillus y Penicillium. Los hongos filamentosos pertenecientes al género Aspergillus han sido reportados como los mejores productores de lipasas. Yadav et al. (1998) hicieron un screening de 40 cepas fúngicas para la producción extracelular de lipasas usando como sustrato aceite de oliva. Las 11 mejores productoras del género Aspergillus fueron A. alliaceus, A. candidus, A. cameus, A. fischeri, A. niger, A. ochraceus, A. parasiticus, A. sundarbanii, A. terreus y A. versicolor; por otro lado, las 9 mejores de Penicillium fueron P. aurantiogriseum, P. brevicompactum, P. camembert, P. chrysogenum, P. corymbiferum, P. crustosum, P. egyptiacum, P. expansum y P. spiculisporum.Coca et al. (2001) reportaron como buenos productores de lipasas a Aspergillus niger, con una actividad de 0,26 U/ml (pH 6 y 40°C) y A. fumigatus, con actividad lipásica de 0,21 U/ml (pH 7 y 80°C). Se ha reportado, además, que la lipasa de A. carneus tiene una alta tolerancia y estabilidad de pH y temperatura, regioespecificidad 1, 3, estabilidad en medios acuosos y no acuosos, y habilidad de esterificación y transesterificación, con una actividad lipásica de 12,7 U/ml (Kaushik et al., 2006). Una alta actividad lipásica (40 U/g) se ha reportado por el hongo P. verrucosum, cuya enzima tiene temperatura óptima fue de 27,5°C y pH 7, cuando se usó salvado seco como inductor (Kempka et al., 2008).
Discusión: Tendencias Actuales
El continuo desarrollo de nuevos productos y las nacientes necesidades han provocado un amplio estudio de las lipasas provenientes de diferentes organismos. Se pueden mencionar varios ejes en los que se ha enfocado el estudio de las lipasas últimamente: 1) el aprovechamiento de diversos residuos agroindustriales para la inducción de la síntesis de lipasas por hongos y levaduras; 2) la búsqueda de nuevos organismos que sinteticen este tipo de enzimas; 3) la modificación y optimización de los genes implicados en la síntesis de lipasas, así como su expresión heteróloga en organismos competentes, que pueda traer una mayor producción que el organismo natural y que, además, la enzima presente características específicas y mejoradas; y 4) implicación de las lipasas ya conocidas en la obtención de compuestos específicos a través de reacciones de transesterificación e interesterificación.
Sustratos inductores para la síntesis de lipasas
Las lipasas son sintetizadas en presencia de inductores lipídicos; estas moléculas están presentes en los residuos agroindustriales, cuyos efectos contaminantes se prevé reducir (Treichel et al., 2010). El agente inductor usado en la síntesis de lipasas ha sido por excelencia el aceite de oliva. La máxima actividad lipásica detectada usando este agente inductor se ha alcanzado usando A. niger y A. fumigatus (Coca et al., 1999). El hongo Y. lipolytica ha sido usado para la producción de lipasas inducidas por desechos agroindustriales, tales como salvado de cebada, nuez triturada y aceite de girasol, (Domínguez et al., 2003) y, recientemente, semilla y cáscara de mango (Pereira et al., 2019). Kempka et al. (2008) reportaron como mejor sustrato a la harina de soya entre diversos sustratos, incluyendo melaza de caña de azúcar, levadura hidrolizada, licor de maíz fermentado, extracto de levadura, aceite de soya, aceite de ricino, aceite de maíz, aceite de oliva y peptona. Otros sustratos reportados para la producción de lipasas son bagazo de caña de azúcar, salvado de trigo y salvado de arroz, además de aceites residuales de mostaza, maní y coco, aguas residuales, licor de maíz, banana, melón, sandía, cáscara de lenteja, aceite de sésamo, peptona, tributirina, ácido cítrico, glucosa, etc. (Treichel et al., 2010; Bhosale et al., 2012).Ilmi et al. (2017) propusieron el uso del aceite obtenido por presión mecánica de la planta tropical Jatropha curcas L, logrando la inducción de lipasas en A. niger 6516 y R. miehei CBS 260,62. Oliveira et al. (2017), por su parte, utilizaron varios residuos agroindustriales: torta de aceite de andiroba, de cupuasu, aceite de canola, de macauba y de semilla de palma, harina de soja, torta de aceite de café verde y de sésamo. El aceite de palma también se ha utilizado para optimizar la producción de la lipasa halófila de F. solani NFCCL 4084, alcanzando un incremento de 3,2 veces su actividad, siendo de 7,8 U/ml (Geoffry y Achur, 2018). Xiaoyan et al. (2017) propusieron el uso de aceite de cocina residual para evaluar la coproducción de eritrol y lipasas utilizando a Y. lipolytica M53, obteniendo la mayor actividad lipásica de 12,7 U/ml.
Además de la búsqueda del aprovechamiento de residuos agroindustriales para la producción sustentable de lipasas, otros estudios se han centrado en reconocer otros hongos y levaduras productores de lipasas. Para ser usada en la producción de biodiesel, se aisló una levadura de lodos provenientes de petróleo, Cryptococcus diffluens D44, cuya lipasa es alcalina y termoestable, con pH y temperatura óptimos de 9 y 45°C, respectivamente (Yılmaz y Sayar, 2015). Alhelli et al., (2016) obtuvieron una lipasa alcalina extracelular de Penicillium candidum (PCA 1/TT031) en medio sólido. Una cepa de Aspergillus westerdijkiae, aislada de aceite de cocina residual, ha sido usada para la producción de lipasas: la enzima obtenida tiene una actividad de 52 U/g de micelio, con una temperatura óptima de 40°C y pH óptimo entre 7 y 8 (Castro et al., 2017). La lipasa del hongo termófilo Malbranchea cinnamomea ha sido expresada en P. pastoris con el fin de determinar sus propiedades; la actividad lipásica obtenida fue de 4304 U/ml, a pH de 7,5 y temperatura de 40°C (Duan et al., 2019). La síntesis de lipasas a partir de Penicillium spp. sección Gracilenta CBMAI 1583 fue inducida con aceite de olvida, y estas mostraron una actividad de 1,62 U/ml, a un pH de 4 y 70°C, siendo estable en presencia de cationes metálicos y de solventes orgánicos como el hexano, trimetilpentano, acetona, entre otros (Turati et al., 2019).
Ha adquirido relevancia el uso de microorganismos que son capaces de sintetizar enzimas con propiedades únicas, ya que les puede conferir su uso en procesos más diversos. En este sentido, Vyas y Chhabra (2016) aislaron una levadura oleoginosa identificada como Cystobasidium oligophagum (JRC1) de desperdicio celulósico; además de su actividad lipásica (2,88 U/mg), la levadura demostró tener actividad endoglucanasa, exoglucanasa y β–glucosidasa. En otro estudio, Sahay y Chouhan (2018) reportaron dos lipasas con actividades a baja temperatura y con actividad metaloenzimática, provenientes de los hongos Penicillium canesense y Pseudogymnoascus roseus.
Expresión heteróloga de lipasas.
La expresión heteróloga ha sido una herramienta muy utilizada que ha permitido vencer algunos de los obstáculos que representa la síntesis natural de las lipasas, como lo son la no reproducibilidad, los bajos rendimientos de producción y la dificultad de purificación de las mismas (Borrelli y Trono, 2015). Pichia pastoris ha sido el sistema más usado para la expresión heteróloga de diversas proteínas comercialmente relevantes de organismos eucariotes. La principal característica de esta levadura es que puede utilizar el metanol como única fuente de carbono y energía, basado en la regulación de la enzima alcohol oxidasa (AOX), bajo acción del promotor PAOX1 (Alarcón, 2008). Las lipasas LIP1 (Brocca et al., 1998), LIP2 (Ferrer et al., 2009) y LIP3 (Chang et al., 2006) de C. rugosa, y las lipasas de C. antarctica (Kwon et al., 2011), han sido expresadas bajo regulación de este promotor. Por otro lado, la lipasa de F. solani ha sido expresada en P. pastoris, manifestando una alta actividad de 100 U/mL (Jalouli et al., 2016). A su vez, una lipasa termoalcalina proveniente de Talaromyces thermophilus fue expresada en el mismo sistema heterólogo, detectándose una enzima de 39kDa, con un pico de máxima actividad de pH 9,5 y temperatura de 60°C (Zhang et al., 2015). En ocasiones se ha hecho uso de organismos reconocidos como productores de lipasas para expresar enzimas de este tipo. Tal es el caso de la lipasa de Rhizopus oryzae (ROL), que fue expresada en Y. lipolytica bajo acción del promotor inducible PXPR2; la enzima recombinante tuvo una actividad de 7,6 U/ml y pH óptimo de 7,5 pero la característica sobresaliente fue su alta termoestabilidad a 55°C (Yuzbashev et al., 2012). Recientemente, la lipasa Lipy8p de Y. lipolytica fue clonada y expresada en células de insecto Sf9, mediante un sistema de expresión de baculovirus; la enzima mostró una actividad específica de 1102,9 U/mg en ácido oleico, a pH 7,5 y 17°C (Li et al., 2019b). El mismo sistema ha sido utilizado para la expresión de la lipasa regioselectiva sn-1(3) de Cordyceps militaris (Park et al., 2018).
Otras estrategias sobresalientes se han seguido para aprovechar al máximo las características y propiedades de las lipasas. Ejemplo de ello ha sido el expresar heterólogamente la lipasa ligada a la superficie celular del sistema de expresión, importante en el desarrollo de biosensores, vacunas y anticuerpos; por ejemplo, Yamada et al. (2016) expresaron la lipasa BTL2 de Geobacillus thermocatenulatus en la superficie de la levadura P. pastoris. Algunos otros estudios se han enfocado en la modificación molecular de la estructura de las lipasas para mejorar sus propiedades. En el estudio realizado por Skjold-Jørgensen et al. (2016) se obtuvo una lipasa mutante de Thermomyces lanuginosus con la capacidad de controlar la cubierta sobre el sitio activo. Zheng et al. (2016) modificaron la lipasa proveniente de la misma especie de hongo por mutación de sitio, obteniendo dos mutantes con alta capacidad de la resolución del ácido 2-carboxietil-3-ciano-5-metilhexanoico etil éster. Zhou et al. (2017) introdujeron la presencia de un tag de poliamina a la lipasa B de C. antarctica (CALB), con el fin de facilitar su expresión en E. coli y dirigirlo en un solo paso para su inmovilización. La lipasa acídica de A. niger fue expresada heterólogamente en P. pastoris con la fusión de tres modificadores, ayudando a alcanzar una actividad de 40 U/ml a un pH óptimo de 2.5 (Zhang et al., 2019). Por otro lado, se han creado mutantes de la lipasa Lip2 de Y. lipolytica con una mayor canditdad de puentes disulfuro (específicamente 4, 5 y 6), lo que ha permitido mejorar la termoestabilidad de la enzima (Li et al. 2019a).
Uso de lipasas fúngicas para la producción de compuestos de interés comercial
Una de las características más relevante de las lipasas es la de su capacidad para catalizar reacciones de interesterificación y transesterificación, principalmente en presencia de solventes orgánicos y baja actividad de agua. Esta propiedad ha sido explotada a nivel industrial para la producción de diversos compuestos en diferentes áreas. En estudios recientes se ha propuesto el uso de las lipasas para la síntesis de otros compuestos que pueden resultar ser interesantes a nivel industrial. Un recuento de los avances de ejemplos representativos en el último par de años, se muestra en la Tabla I. Son varias las conclusiones que se pueden obtener a partir de dicha información: 1) Las lipasas que se utilizan con fines de síntesis de productos o compuestos de interés en la actualidad, corresponden a aquellas que son más conocidas, provenientes de microorganismos de los géneros Aspergillus, Candida, Penicillium, Rhizomucor, Rizophus, Thermomyces y Yarrowia. Sería interesante ver en próximos años el uso de lipasas aisladas recientemente o provenientes de otros hongos y levaduras que puedan tener la capacidad de catalizar la obtención de otro tipo de compuestos, siendo pocos autores los que lo proponen de esta manera. 2) Muchos de los compuestos reportados últimamente, obtenidos a partir de reacciones que implican el uso de las lipasas fúngicas, corresponden a ésteres de cadena corta que son usados normalmente en la industria alimenticia, ya que proporcionan ciertos aromas y/o sabores. Asimismo, se ha hecho una búsqueda de lipasas que son específicas y capaces de actuar sobre ácidos grasos poliinsaturados del tipo DHA y EPA, vitales para la obtención de productos más nutritivos, debido a los grandes beneficios que estos conllevan en la dieta diaria. En otros casos, se ha hecho uso de la facultad de algunas lipasas para la resolución de mezclas racémicas, de vital importancia en la industria farmacéutica. Además, el uso de las lipasas para la obtención de biodiesel ha continuado a través de la optimización de los procesos y reacciones implicadas, a fin de mejorar rendimientos. 3) La mayoría de los estudios realizados últimamente respecto a las lipasas utilizan algún sistema de inmovilización de las mismas. Los sistemas utilizados y los métodos de inmovilización reportados son muy variados, pero en la mayoría de los casos se logra mejorar los rendimientos de conversión y la eficiencia de las enzimas. Mayor información de los avances de la inmovilización de lipasas se puede revisar en Pereira et al. (2017).
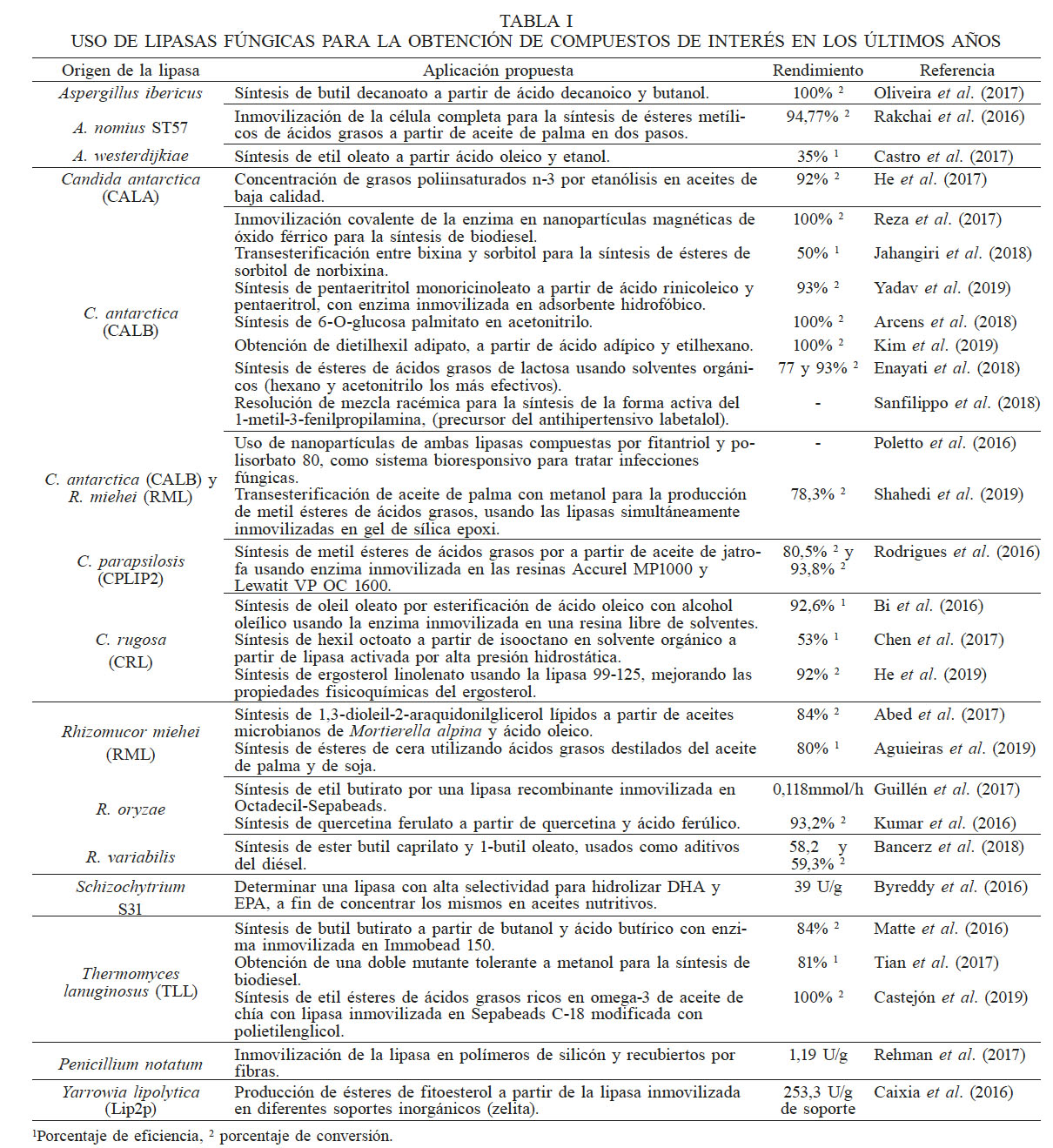
1 1Porcentaje de eficiencia, 2 porcentaje de conversión.
Conclusiones
Las interesantes características y variadas propiedades que presentan las lipasas de origen fúngico les han conferido una amplia importancia industrial y comercial, siendo uno de los grupos de enzimas más utilizados actualmente. Las lipasas no solo son herramientas biotecnológicas prometedoras, sino también son ya una realidad. Este hecho se manifiesta en la gran cantidad de estudios reportados en los diferentes ámbitos mencionados en este escrito. Nuevas alternativas de uso de las lipasas irán surgiendo poco a poco y probablemente desplazarán a las usadas comercialmente en la actualidad.
Agradecimientos
Los autores agradecen los donativos parciales de la Convocatoria de Apoyo a Proyectos de Investigación Científica, Aplicada, Desarrollo Tecnológico e Innovación 2016, 2017, 2018 del Tecnológico Nacional de México, proyectos Nos. 5781.16-P, 6131.17-P y 6525.18-P; los donativos parciales al Laboratorio Nacional SEDEAM del Instituto Tecnológico de Morelia por el apoyo académico de los investigadores y estudiantes en tesis aplicadas a la empresa; asi como la participación del Consejo Nacional de Ciencia y Tecnología (CONACyT) a través del soporte financiero otorgado por la Beca 253782.
HONGOS Y LEVADURAS: FÁBRICAS DE LIPASAS
Abed SM, Zou X, Ali AH, Jin Q (2017) Synthesis of 1,3-dioleoyl-2-arachidonoylglycerol-rich structured lipids by lipase-catalyzed acidolysis of microbial oil from Mortierella alpina. Bioresour. Technol. 243: 448-453.
Aguieiras ECG, Cavalcanti-Oliveira ED, Freire DMG (2015) Current status and new developments of biodiesel production using fungal lipases. Fuel 159: 52-67.
Aguieiras ECG, Papadaki A, Mallouchos A, Mandala I, Sousa H, Freire DMG, Koutinas AA (2019) Enzymatic synthesis of bio-based wax esters from palm and soybean fatty acids using crude lipases produced on agricultural residues. Indust. Crops Prod. 119: 11419.
Akoh CC, Lee GC, Shaw JF (2004) Protein engineering and applications of Candida rugosa lipase isoforms. Lipids 39: 513-526.
Alarcón VMR (2008) Producción de la Lipasa LIP2 de Candida rugosa en el Sistema Pichia pastoris: Caracterización y Aplicación en Reacciones de Síntesis. Tesis. Universidad Autónoma de Barcelona, España. 201 pp.
Alhelli AM, Yazid M, Manap A, Mohammed AS, Mirhosseini SH, Suliman E, Shad Z, Mohammed NK, Hussin ASM (2016) Use of response surface methodology for partitioning, one-step purification of alkaline extracellular lipase from Penicillium candidum (PCA 1/TT031). J. Chromatogr. B 1039: 66-73.
Arcens D, Grau E, Grelier S, Cramail H, Peruch F (2018) 6-O-glucose palmitate synthesis with lipase: Investigation of some key parameters. Mol. Catal. 460: 63-68.
Bancerz R, Osinska-Jaroszuk M, Jaszek M, Sulej J, Wiater A, Matuszewska A, Rogalski j (2018) Fungal polysaccharides as a water-adsorbing material in esters production with the use of lipase from Rhizomucor variabilis. Int. J. Biol. Macromol. 118: 957-964.
Bhosale HJ, Kadam TA, Sukalkar SR, Adekar SD (2012) Lipase production from Bacillus sp. using uoybean oil cake as substrate. Int. J. Pharm. Biol. Res. 3: 213-218.
Bi Y, Yu M, Zhou H, Zhou H, Wei P (2016) Biosynthesis of oleyl oleate in solvent-free system by Candida rugosa lipase (CRL) immobilized in macroporous resin with cross-linking of aldehyde-dextran. J. Mol. Catal. B, Enzym 133: 1-5.
Borrelli GM, Trono D (2015) Recombinant lipases and phospholipases and their use as biocatalysts for industrial applications. Int. J. Mol. Sci. 16: 20774-20840.
Brady L, Brzozowski AM, Derewenda ZS, Dodson E, Dodson G, Tolley S, Turkenburg JP, Christiansen L, Huge-Jensen B, Norskov L, Thim L, Menge U (1990) A serine protease triad forms the catalytic centre of a triacylglycerol lipase. Nature 343: 767-770.
Brocca S, Schmidt-Dannert C, Lotti M, Alberghina L, Schmid RD (1998) Design, total synthesis, and functional overexpression of the Candida rugosa lip1 gene coding for a major industrial lipase. Protein Sci. 7: 1415-1422.
Burkert JFM, Maugeri F, Rodrigues M (2004) Optimization of extracellular space lipase production by Geotrichum sp. using factorial design. Bioresour. Technol. 91: 77-84.
Byreddy AR, Rao NM, Barrow CJ, Puri M (2016) Tween 80 influences the production of intracellular lipase by Schizochytrium S31 in a stirred tank reactor. Proc. Biochem. 53: 30-35.
Caixia A, Nan C, Chen G, Biqiang X, Tan T (2016) Immobilization of Yarrowia lipolytica lipase Ylip 2 for the biocatalytic synthesis of phytosterol ester in a water activity controlled reactor. Coll. Surf. B Biointerf. 146: 490-497.
Casas-Godoy L, Duquesne S, Bordes F, Sandoval G, Marty A (2012) Lipases: An overview. En Sandoval G (Ed.) Lipases and Phospholipases: Methods and Protocols. Springer Protocols 861: 3-30.
Castejón N, Moreno-Pérez S, Abreu Silveira E, Fernández Lorente G, Guisán JM, Señoráns FJ (2019) Synthesis of omega-3 ethyl esters from chia oil catalyzed by polyethylene glycol-modified lipases with improved stability. Food Chem. 271: 433-439.
Castro FF, Ponchio AB, Nassur CB, Parra I (2017) Mycelium-bound lipase from a locally isolated strain of Aspergillus westerdijkiae. Biocatal. Agric. Biotechnol. 10: 321-328.
Chang SW, Lee GC, Shaw JF (2006) Efficient production of active recombinant Candida rugosa LIP3 lipase in Pichia pastoris and biochemical characterization of the purified enzyme. J. Agric. Food Chem. 54: 5831-5838.
Chen G, Du H, Jiang B, Miao M, Feng B (2017) Activity of Candida rugosa lipase for synthesis of hexyl octoate under high hydrostatic pressure and the mechanism of this reaction. J. Mol. Catal. B Enzym. 133: S439-S444.
Coca J, Hernández O, Berrio R, Martínez S, Díaz E, Dustet JC (2001) Producción y caracterización de Aspergillus niger y A. fumigatus. Biotecnol. Aplic. 18: 216-220.
Colla LM, Rizzardi J, Pinto MH, Reinehr CO, Bertolin TE, Vieira CJA (2010) Simultaneous production of lipases and biosurfactants by submerged and solid-state bioprocesses. Bioresour. Technol. 101: 8308-8314.
Domínguez A, Costas M, Longo MA, Sanromán A (2003) A novel application of solid state culture: Production of lipases by Yarrowia lipolytica. Biotechnol. Lett. 25: 1225-1229.
Duan X, Xiang M, Wang L, Yan Q, Yang S, Jiang Z (2019) Biochemical characterization of a novel lipase from Malbranchea cinnamomea suitable for production of lipolyzed milkfat flavor and biodegradation of phthalate esters. Food Chem. 297: 124925.
Enayati M, Gong Y, Goddard JM, Abbaspourrad A (2018) Synthesis and characterization of lactose fatty acid ester biosurfactants using free and immobilized lipases in organic solvents. Food Chem. 266: 508-513.
Ericsson DJ, Kasrayan A, Johansson P, Bergfors T, Sandström AG, Bäckvall J, Mowbray SL (2008) X-ray structure of Candida antarctica lipase a shows a novel lid structure and a likely mode of interfacial activation. J. Mol. Biol. 376: 109-119.
Ferrer P, Alarcón M, Ramón R, Dolors BM, Valero F (2009) Recombinant Candida rugosa LIP2 expression in Pichia pastoris under the control of the AOX1 promoter. Biochem. Eng. J. 46: 271-277.
Ferrer P, Montesinos JL, Valero F, Solà C (2001) Production of native and recombinant lipases by Candida rugosa. Appl. Biochem. Biotechnol. 95: 221-255.
Fickers P, Marty A, Nicaud JM (2011) The lipases from Yarrowia lipolytica: Genetics, production, regulation, biochemical characterization and biotechnological applications. Biotechnol. Adv. 29: 632-644.
Fischer M, Pleiss J (2003) The Lipase Engineering Database: a navigation and analysis tool for protein families. Nucl. Ac. Res. 31: 319-321.
Geoffry K, Achur RN (2018) Optimization of novel halophilic lipase production by Fusarium solani strain NFCCL 4084 using palm oil mill effluent. J. Genet. Eng. Biotechnol. 16: 327-334.
Guillén M, Benaiges MD, Valero F (2017) Improved ethyl butyrate synthesis catalyzed by an immobilized recombinant Rhizopus oryzae lipase: A comprehensive statistical study by production, reaction rate and yield analysis. J. Mol. Catal. B Enzym. 133: S371-S376.
Hasan F, Shah AA, Hameed A (2009) Methods for detection and characterization of lipases: A comprehensive review. Biotechnol. Adv. 27: 782-798.
He WS, Li L, Zhao J, Xu H, Rui J, Cui D, Li H, Zhang H, Liu X (2018) Candida sp. 99-125 lipase-catalyzed synthesis of ergosterol linolenate and its characterization. Food Chem. 280: 286-293.
He Y, Li J, Kodali S, Chen B, Guo Z (2017) Rationale behind the near-ideal catalysis of Candida antarctica lipase A ( CAL-A ) for highly concentrating x-3 polyunsaturated fatty acids into monoacylglycerols. Food Chem. 219: 230-239.
Ilmi M, Hidayat C, Hastuti P, Heeres HJ, Maarel MJEC Van Der (2017) Utilisation of Jatropha press cake as substrate in biomass and lipase production from Aspergillus niger 65I6 and Rhizomucor miehei CBS. Biocatal. Agric. Biotechnol. 9: 103-107.
Jaeger KE, Reetz MT (1998) Microbial lipases form versatile tools for biotechnology. Trends Biotechnol. 16: 396-403.
Jahangiri A, Møller AH, Danielsen M, Madsen B, Joernsgaard B, Vaerbak S, Adlercreutz P, Dalsgaard TK (2018) Hydrophilization of bixin by lipase-catalyzed transesterification with sorbitol. Food Chem. 268: 203-209.
Jalouli R, Parsiegla G, Carrière F, Gargouri Y, Bezzine S (2016) Efficient heterologous expression of Fusarium solani lipase, FSL2, in Pichia pastoris, functional characterization of the recombinant enzyme and molecular modeling. Int. J. Biol. Macromol. 94: 61-71.
Jolivet P, Bordes F, Fudalej F, Cancino M, Vignaud C, Dossat V, Burghoffer C, Marty A, Chardot T, Nicaud JM (2007) Analysis of Yarrowia lipolytica extracellular lipase Lip2p glycosylation. FEMS Yeast Res. 7: 1317-1327.
Kaushik R, Saran S, Isar J, Saxena RK (2006) Statistical optimization of medium components and growth conditions by response surface methodology to enhance lipase production by Aspergillus carneus. J. Mol. Catal. B Enzym. 40: 121-126.
Kempka AP, Lipke NL, Da Luz FPT, Menoncin S, Treichel H, Freire DMG, Di Luccio M, de Oliveira D (2008) Response surface method to optimize the production and characterization of lipase from Penicillium verrucosum in solid-state fermentation. Bioproc. Biosyst. Eng. 31: 119-125.
Kim H, Kim T, Choi N, Kim BH, Oh SW, Kim IH (2019) Synthesis of diethylhexyl adipate by Candida antarctica lipase-catalyzed esterification. Proc. Biochem. 78: 58-62.
Kumar V, Jahan F, Mahajan R V, Saxena RK (2016) Efficient regioselective acylation of quercetin using Rhizopus oryzae lipase and its potential as antioxidant. Bioresour. Technol. 218: 1246-1248.
Kwon MA, Kim HS, Hahm DH, Song JK (2011) Synthesis activity-based zymography for detection of lipases and esterases. Biotechnol. Lett. 33: 741-746.
Li L, Zhang S, Wu W, Guan W, Deng Z, Qiao H (2019a) Enhancing thermostability of Yarrowia lipolytica lipase 2 through engineering multiple disulfide bonds and mitigating reduced lipase production associated with disulfide bonds. Enz. Microb. Technol. 126: 41-49.
Li T, Zhang W, Hao J, Sun M, Lin SX (2019b) Cold-active extracellular lipase: Expression in Sf9 insect cells, purification, and catalysis. Biotechnol. Rep. 21: e00295.
Mancheño JM, Pernas MA, Martínez MJ, Ochoa B, Rúa ML, Hermoso J (2003) Structural insights into the lipase/esterase behavior in the Candida rugosa lipases family: Crystal structure of the lipase 2 isoenzyme at 1.97 Å resolution. J. Mol. Biol. 332: 1059-1069.
Matte CR, Bordinhão C, Poppe JK, Rodrigues RC, Hertz PF, Ayub MAZ (2016) Synthesis of butyl butyrate in batch and continuous enzymatic reactors using Thermomyces lanuginosus lipase immobilized in Immobead 150. J. Mol. Catal. B Enzym. 127: 67-75.
Meng Y, Li S, Yuan H, Zou D, Liu Y, Zhu B, Li X (2015) Effect of lipase addition on hydrolysis and biomethane production of Chinese food waste. Bioresour. Technol. 179: 452-459.
Oliveira F, Souza CE, Peclat VROL, Salgado JM, Ribeiro BD, Coelho MAZ, Venancio A, Belo I (2017) Optimization of lipase production by Aspergillus ibericus from oil cakes and its application in esterification reactions. Food Bioprod. Proc. 102: 268-277.
Park JH, Park KM, Chang Y, Park JY, Han J, Chang PS (2017) Cloning and protein expression of the sn-1(3) regioselective lipase from Cordyceps militaris. Enz. Microb. Technol. 119: 30-36.
Pereira A da S, Fontes-Sant’Ana GC, Amaral PFF (2019) Mango agro-industrial wastes for lipase production from Yarrowia lipolytica and the potential of the fermented solid as a biocatalyst. Food Bioprod. Proc. 115: 68-77.
Pereira E, Andrade E, Fernandez-lafuente R, Maria D, Freire G (2017) Support engineering: relation between development of new supports for immobilization of lipases and their applications. Biotechnol. Res. Innov. 1: 26-34.
Pleiss J, Fischer M, Peiker M, Thiele C, Schmid RD (2000) Lipase engineering database: Understanding and exploiting sequence-structure-function relationships. J. Mol. Catal. B Enzym. 10: 491-508.
Poletto FS, Lima FS, Lundberg D, Nylander T, Loh W (2016) Tailoring the internal structure of liquid crystalline nanoparticles responsive to fungal lipases : A potential platform for sustained drug release. Coll. Surf. B Biointerf. 147: 210-216.
Rakchai N, H-kittikun A, Zimmermann W (2016) The production of immobilized whole-cell lipase from Aspergillus nomius ST57 and the enhancement of the synthesis of fatty acid methyl esters using a two-step reaction. J. Mol. Catal. B Enzym. 133: S128-S136.
Rehman S, Wang P, Bhatti HN, Bilal M, Asgher M (2017) Improved catalytic properties of Penicillium notatum lipase immobilized in nanoscale silicone polymeric films. Int. J. Biol. Macromol. 97: 279-286.
Reis P, Holmberg K, Watzke H, Leser ME, Miller R (2009) Lipases at interfaces: A review. Adv. Coll. Interf. Sci. 147: 237-250.
Reza M, Mohammadi J, Peyda M (2017) Covalent immobilization of Candida antarctica lipase on core-shell magnetic nanoparticles for production of biodiesel from waste cooking oil. Renew. Energy 101: 593-602.
Rodrigues J, Perrier V, Lecomte J, Dubreucq E, Ferreira-Dias S (2016) Biodiesel production from crude jatropha oil catalyzed by immobilized lipase/acyltransferase from Candida parapsilosis in aqueous medium. Bioresour. Technol. 218: 1224-1229.
Sahay S, Chouhan D (2018) Study on the potential of cold-active lipases from psychrotrophic fungi for detergent formulation. J. Genet. Eng. Biotechnol. 16: 319-325.
Sanfilippo C, Paternò AA, Patti A (2017) Resolution of racemic amines via lipase-catalyzed benzoylation: Chemoenzymatic synthesis of the pharmacologically active isomers of labetalol. Mol. Catal. 449: 79-84.
Shahedi M, Yousefi M, Habibi Z, Mohammadi M, As’habi MA (2019) Co-immobilization of Rhizomucor miehei lipase and Candida antarctica lipase B and optimization of biocatalytic biodiesel production from palm oil using response surface methodology. Renew. Energy 141: 847-857.
Sharma R, Chisti Y, Banerjee UC, Chand U (2001) Production, purification, characterization, and applications of lipases. Biotechnol. Adv. 19: 627-662.
Skjold-Jørgensen J, Vind J, Moroz O V, Blagova E, Bhatia VK, Svendsen A, Wilson KS, Bjerrum MJ (2016) Controlled lid-opening in Thermomyces lanuginosus lipase- an engineered switch for studying lipase function. BBA-Prot. Proteom. 1865: 20-27.
Solymar M, Fulop F, Kanerva LT (2002) Candida antarctica lipase A -a powerful catalyst for the resolution of heteroaromatic b-amino esters. Tetrahedron: Asymm. 13: 2383-2388.
Tan CH, Show PL, Ooi CW, Ng EP, Lan JCW, Ling TC (2015) Novel lipase purification methods -a review of the latest developments. Biotechnol. J. 10: 3144.
Tian K, Tai K, Jian B, Chua W, Li Z (2017) Directed evolution of Thermomyces lanuginosus lipase to enhance methanol tolerance for efficient production of biodiesel from waste grease. Bioresour. Technol. 245: 1491-1497.
Treichel H, de Oliveira D, Mazutti MA, Di Luccio M, Oliveira JV (2010) A review on microbial lipases production. Food Bioproc. Technol. 3: 182-196.
Turati DFM, Almeida AF, Terrone CC, Nascimento JMF, Terrasan CRF, Fernandez-Lorente G, Benevides CP, Guisan JM, Carmona EC (2019) Thermotolerant lipase from Penicillium sp. section Gracilenta CBMAI 1583: Effect of carbon sources on enzyme production, biochemical properties of crude and purified enzyme and substrate specificity. Biocatal. Agric. Biotechnol. 17: 15-24.
Uppenberg J, Hansen MT, Patkar S, Jones T (1994) The sequence, crystal structure determination and refinement of two crystal forms of lipase B from Candida antarctica. Structure 2: 293-308.
Verma N, Thakur S, Bhatt AK (2012) Microbial lipases: Industrial applications and properties (A review). Int. Res. J. Biol. Sci. 1: 88-92.
Vyas S, Chhabra M (2016) Isolation, identification and characterization of Cystobasidium oligophagum JRC1: A cellulase and lipase producing oleaginous yeast. Bioresour. Technol. 223: 250-258.
Xiaoyan L, Xinjun Y, Jinshun L, Jiaxing X, Jun X, Zhen W, Tong Z, Yuanfang D (2017) A cost-effective process for the coproduction of erythritol and lipase with Yarrowia lipolytica M53 from waste cooking oil. Food Bioprod. Proc. 103: 86-94.
Yadav MG, Vadgama RN, Kavadia MR, Odaneth AA, Lali AM (2019) Production of Pentaerythritol Monoricinoleate (PEMR) by immobilized Candida antarctica lipase B. Biotechnol. Rep. 23: e00353.
Yadav RP, Saxena RK, Gupta R, Davidson S (1998) Lipase production by Aspergillus and Penicillium species. Folia Microbiol. 43: 373-378.
Yamada R, Kimoto Y, Ogino H (2016) Combinatorial library strategy for strong overexpression of the lipase from Geobacillus thermocatenulatus on the cell surface of yeast Pichia pastoris. Biochem. Eng. J. 113: 7-11.
Yılmaz DE, Sayar NA (2015) Organic solvent stable lipase from Cryptococcus diffluens D44 isolated from petroleum sludge. J. Mol. Catal. B. Enzym. 122: 72-79.
Yuzbashev TV, Yuzbasheva EY, Vibornaya TV, Sobolevskaya TI, Laptev IA, Gavrikov AV, Sineoky SP (2012) Production of recombinant Rhizopus oryzae lipase by the yeast Yarrowia lipolytica results in increased enzymatic thermostability. Prot. Expres. Purif. 82: 83-89.
Zhang X, Li X, Xia L (2015) Expression of a thermo-alkaline lipase gene from Talaromyces thermophilus in recombinant Pichia pastoris. Biochem. Eng. J. 103: 263-269.
Zhang XF, Ai YH, Xu Y, Yu XW (2019) High-level expression of Aspergillus niger lipase in Pichia pastoris: Characterization and gastric digestion in vitro. Food Chem. 274: 305-313.
Zheng R, Ruan L, Ma H, Tang X, Zheng Y (2016) Enhanced activity of Thermomyces lanuginosus lipase by site-saturation mutagenesis for efficient biosynthesis of chiral intermediate of pregabalin. Biochem. Eng. J. 113: 12-18.
Zhou X, Han Y, Lv Z, Tian X, Li H, Xie P, Zheng L (2017) Simultaneously achieve soluble expression and biomimetic immobilization of Candida antarctica lipase B by introducing polyamine tags. J. Biotechnol. 249: 1-9.
Notas de autor
jcgonzal@itmorelia.edu.mx